Dr. Matthias Herrmann, Berlin
Wurde lange Zeit davon ausgegangen, dass in Deutschland rund 80 000 Menschen mit MS leben, wird die Zahl der Erkrankten heute auf circa 280 000 geschätzt [3]. Bei schubförmiger MS tragen dabei zwei Prozesse maßgeblich zur Behinderungsprogression bei: die schubassoziierte Verschlechterung (relapse-associated worsening [RAW]) und die schubunabhängige Progression (progress independent of relapse activity [PIRA]). PIRA kann schon in frühen Krankheitsphasen maßgeblich zur klinischen Verschlechterung beitragen und trotz verlaufsmodifizierender Therapien voranschreiten. Bei Patienten mit einem klinisch isolierten Syndrom (CIS) oder früher MS ist PIRA nach Daten einer italienischen Kohortenstudie mit rund 60 % sogar der stärkere Treiber der Behinderungsprogression nach fünf Jahren als die RAW mit einem Beitrag von etwa 40 % [4].
Axonalen Schaden von Beginn an begrenzen
Der axonale Schaden tritt bei schubförmiger MS bereits in der frühen Krankheitsphase ein und korreliert mit der Entzündungsaktivität. Die verlaufsmodifizierenden Therapien sollten deshalb frühzeitig eingesetzt werden, um Patienten vor Schüben und Behinderungsprogression zu schützen. Bei Patienten mit einem wahrscheinlich hoch aktiven Verlauf ist der sofortige Einsatz eines Arzneimittels der Wirksamkeitskategorie 2 (Cladribin, Fingolimod, Ozanimod, Ponesimod) oder 3 (Alemtuzumab, Natalizumab, Ocrelizumab, Ofatumumab, Rituximab [Off-Label]) durch die S2k-Leitlinie zur Diagnose und Therapie der MS abgedeckt [3]. Verglichen mit dem Eskalationsansatz – beginnend mit einem Arzneimittel der Kategorie 1 (Dimethylfumarat/Diroximelfumarat, Glatirameroide, Interferon beta, Teriflunomid) – kann der frühe Einsatz der hoch aktiven Therapien die Schubrate und die Wahrscheinlichkeit der Behinderungsprogression (Abb. 1; [2]) langfristig deutlich reduzieren.
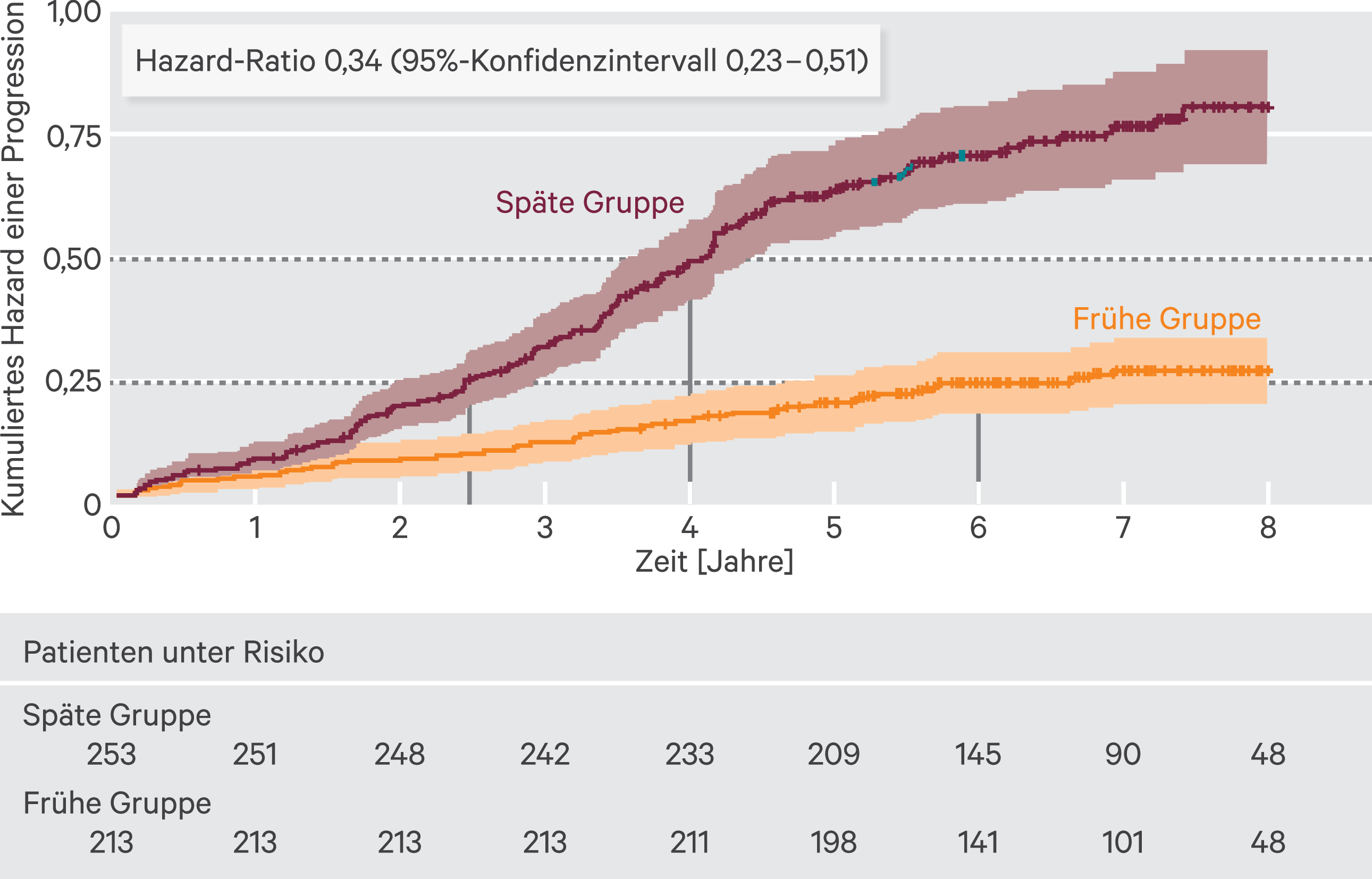
Abb. 1. Kumulative Hazard einer bestätigten Behinderungsprogression bei Patienten mit frühem vs. spätem Beginn einer hoch aktiven MS-Therapie, gemessen ab Beginn der ersten krankheitsmodifizierenden Therapie. Schattierte Bereiche geben das 95%-Konfidenzintervall an (modifiziert nach [2])
Frühe Therapie mit Ofatumumab reduziert die Krankheitsaktivität
Für Ofatumumab (Kesimpta®) belegen Daten der offenen Langzeit-Extensionsstudie ALITHIOS den Nutzen der frühzeitigen Behandlung mit dem Kategorie-3-Arzneimittel [1]. Vor Aufnahme in die Extensionsstudie hatten die 1367 eingeschlossenen Patienten mit schubförmiger MS im Rahmen der Phase-III-Studien ASCLEPIOS I/II Ofatumumab oder Teriflunomid erhalten. Verglichen mit dem späteren Wechsel von Teriflunomid auf Ofatumumab zeigten die schon früh mit Ofatumumab behandelten Patienten während der Kernstudien und der Extensionsstudie in der Magnetresonanztomographie (MRT) und klinisch eine geringere Krankheitsaktivität. Am stärksten profitierten therapienaive oder nur wenig vorbehandelte Patienten sowie jene im Alter von ≤ 40 Jahren.
Aufgrund der subkutanen Gabe eignet sich Ofatumumab gut für Patienten mit dem Wunsch nach Selbstständigkeit. Als B-Zell-depletierendes Arzneimittel reduziert der monoklonale Antikörper die Immunglobulin-G-Spiegel im Serum. Die verbleibenden B-Zellen reichen aber aus, um bei Impfungen eine ausreichende Immunantwort auszubilden. Bestätigte Fälle einer progressiven multifokalen Leukenzephalopathie (PML) wurden unter Ofatumumab bislang nicht beobachtet.
Fazit
Zeichnet sich bei Patienten mit schubförmiger MS ein hoch aktiver Verlauf ab, sollte schon initial ein Arzneimittel der Wirksamkeitskategorie 2 oder 3 zum Einsatz kommen. Der frühzeitige Einsatz von Ofatumumab kann die klinische und subklinische Krankheitsprogression langfristig reduzieren.
Quelle
Prof. Dr. Christoph Kleinschnitz, Essen, Prof. Dr. Ralf Gold, Bochum, Fachpressegespräch „Frühstart in die Therapie der aktiven schubförmigen Multiplen Sklerose“, veranstaltet von Novartis, Berlin, 8. November 2023.
Literatur
1. Cohen JA, et al. Efficacy of early ofatumumab versus late-switch from teriflunomide: subgroup analysis of the ALITHIOS open-label extension study by prior disease-modifying therapy exposure and age. 38. ECTRIMS, Poster P1210, Amsterdam, 26. bis 28. Oktober 2022.
2. He A, et al. Timing of high efficacy therapy for multiple sclerosis: a retrospective observational cohort study. Lancet Neurol 2020;19:307–16.
3. Hemmer B, et al. Diagnose und Therapie der Multiplen Sklerose, Neuromyelitis-optica-Spektrum-Erkrankungen und MOG-IgG-assoziierten Erkrankungen, S2k-Leitlinie, 2023. In: Deutsche Gesellschaft für Neurologie (Hrsg.), Leitlinien für Diagnostik und Therapie in der Neurologie. https://dgn.org/leitlinien (Zugriff am 23.11.2023).
4. Portaccio E, et al. Progression is independent of relapse activity in early multiple sclerosis: a real-life cohort study. Brain 2022;145:2796–805.
Psychopharmakotherapie 2024; 31(01):23-33
