Christian Schmidt-Kraepelin und Mathias Riesbeck, Düsseldorf
Antipsychotische Monotherapie
Antipsychotika stellen weiterhin den zentralen Baustein in der Behandlung von Erkrankungen aus dem Formenkreis der Schizophrenien (Diagnose-Kategorie F.2x des ICD-10) dar. Ihre Effektivität ist sowohl in der Akut- als auch der Langzeitbehandlung in umfangreichen Studien nachgewiesen und wird von evidenzbasierten Leitlinien mit dem höchsten Evidenz- und Empfehlungsgrad empfohlen ([6] Behandlungsempfehlung Nr. 32). Da die zugrunde liegenden Studien alle auf monotherapeutischer Behandlung (Gabe eines Antipsychotikums) beruhen, beinhaltet die Empfehlung ebenfalls eine monotherapeutische Strategie als primäre Behandlungsstrategie (Verabreichung eines Antipsychotikums außer Clozapin aufgrund der damit verbundenen möglichen schwerwiegenden Nebenwirkungen). Zudem bestehe bei der Kombination von Antipsychotika die Gefahr pharmakodynamischer und pharmakokinetischer Interaktionen, was zusammen mit der meist höheren Gesamt-Äquivalenzdosis das Risiko von unerwünschten Nebenwirkungen erhöhe. Weiterhin sprächen höhere Therapiekosten sowie Nachteile in der Steuerung und praktischen Handhabbarkeit für Behandler und Patient mit negativen Auswirkungen auf die Compliance gegen eine Kombinationsbehandlung. Bei ungenügendem Ansprechen auf die Behandlung oder nicht tolerablen Nebenwirkungen wird deshalb ein weiterer Behandlungsversuch mit einem anderen Präparat empfohlen. Bei weiterer Non-Response und gesicherter Behandlungsresistenz (bei Beachtung einer hinreichenden Dosierung und Dauer, vorhandener Adhärenz, Drogenabstinenz und ggf. Diagnosesicherung) sollte eine weitere Monotherapie mit Clozapin erfolgen. Erst bei weiterem Nicht-Ansprechen wird eine Kombinationsbehandlung mit zwei Antipsychotika empfohlen. Das entsprechende Vorgehen sollte dabei dokumentiert, Nebenwirkungen und Interaktion engmaschig monitoriert und im Falle eines weiteren fehlenden Ansprechens wiedereingestellt werden ([6] Empfehlung Nr. 46).
In der klinischen Praxis wird die Kombinationsbehandlung oder antipsychotische Polypharmazie (APP) häufig angewendet. Eine Übersichtsarbeit aus verschiedenen Ländern berichtet Prävalenzen von 30 bis 50 % [8]. Ähnliche oder sogar höhere Werte sind auch in Deutschland zu finden [23].
Die Gründe, die in bestimmten Fällen für den Einsatz einer APP sprechen, sind vielfältig. Besteht z. B. eine ausgeprägte Symptomatik in unterschiedlichen psychopathologischen Domänen (Positiv-, Negativsymptomatik, Agitiertheit, depressive Symptomatik), könnte das breitere Wirksamkeitsspektrum kombinierter Antipsychotika sinnvoll sein [9]. Weitere Vorteile stellen die Nutzung unterschiedlicher Applikationsformen (z. B. orale und intramuskuläre Depotgabe), eine verbesserte Wirksamkeit aufgrund unterschiedlicher Rezeptorbindungsprofile der verschiedenen Präparate [15] sowie die Verminderung von Nebenwirkungen [7] dar. Zudem zeigen Untersuchungen, dass eine Therapieresistenz (je nach zu Grunde liegenden Definitionskriterien) mit 30 bis über 50 % sehr häufig anzutreffen ist [6].
Mögliche Vorteile einer Kombinationstherapie
Die empirische Befundlage zum Vergleich antipsychotischer Monotherapie mit Kombinationsbehandlung stellt sich wie folgt dar. In einer Metaanalyse [5] ergaben sich Hinweise für eine höhere Ansprechrate unter antipsychotischer Kombinationsbehandlung im Vergleich zur Monotherapie. Weiterhin zeigte sich in der dritten Projekt-Phase der CATIE-Studie eine geringere Rate von Therapieabbrüchen unter Kombinationsbehandlung verglichen mit Monotherapie [25]. Matsui et al. [14] fanden in einer Metaanalyse ebenfalls geringere Abbruchraten bei fortgesetzter APP im Vergleich zu einer Umstellung auf Monotherapie, wobei keine Unterschiede bezüglich Effektivität (Symptomatik und Rückfall) oder Nebenwirkungen (Gewichtszunahme) zu verzeichnen waren. Eine weitere Metaanalyse [9] fand ebenfalls Vorteile der APP im Vergleich zu Monotherapie hinsichtlich der Symptomverbesserung mit einer Effektstärke von 0,53 („moderat“). Bei Berücksichtigung nur methodisch hochwertiger oder doppelblinder Studie reduzierte sich dieser Effekt auf ca. 0,35 und erreichte nicht mehr das statistische Signifikanzniveau. Weiterhin fanden Tiihonen et al. [26] bei der Analyse von Medizinregister-Daten von über 60 000 Patienten in Finnland einen signifikanten Vorteil für APP gegenüber Monotherapie hinsichtlich der psychiatrischen Rehospitalisierungsrate und stationärer Aufnahme. Dabei war die Kombination aus Clozapin und Aripiprazol mit dem geringsten Risiko einer psychiatrischen Rehospitalisierung assoziiert und der Monotherapie mit Clozapin überlegen.
Neben dieser empirischen Evidenz für eine (z. T. überlegene) Effektivität der APP ist zu berücksichtigen, dass die weitaus meisten (klinischen) Antipsychotika-Studien an sehr selektierten Patienten durchgeführt werden (z. B. hinsichtlich Einwilligung- und Kooperationsfähigkeit, Selbst- und Fremdgefährdung, Substanzabusus), die deutlich und in einem nicht unerheblichen Umfang von der Klientel in der Versorgungspraxis abweichen können. Stahl [24] spricht in diesem Zusammenhang von der Kluft zwischen evidenzbasierter Praxis und praxisbezogener Evidenz. Verbunden mit dem hohen Anteil therapieresistenter oder gar refraktärer Patienten, einer polygenetischen Bedingtheit und damit ätiopathologischen Heterogenität schizophrener Erkrankungen ist ein breites medikamentöses Wirkungsprofil, wie es die APP potenziell bietet, eine zumindest theoretisch begründete rationale Option. Gründer und Benkert [10] vergleichen dies mit dem Schrotkugel-Prinzip („Magic shotguns“) und dem Potenzial, eine Vielzahl von Zielparametern gleichzeitig zu beeinflussen.
Rationale antipsychotische Kombinationstherapie
Eine „rationale“ im Gegensatz zu einer „nichtrationalen“ antipsychotischen Polypharmazie sollte sowohl evidenz- als auch theoriegeleitet sein und Antipsychotika nach pharmakodynamischen und -kinetischen Gesichtspunkten sinnvoll kombinieren [18]. Für eine solche rationale Therapie wird im Folgenden der Begriff „antipsychotische Kombinationstherapie“ (AKT) verwendet. Zu berücksichtigen wären dabei insbesondere komplementäre neuronale Rezeptorbindungsprofile, Metabolisierungspfade und Nebenwirkungsprofile.
Empfehlungen zur rationalen antipsychotischen Kombinationstherapie wurden bisher vor allem bezüglich Clozapin als Kombinationspartner gegeben. Das Standardwerk zur psychiatrischen Pharmakotherapie in Deutschland, Benkert und Hippius [2], und die nationale Behandlungsleitlinie Schizophrenie [6] nennen Amisulprid, Aripiprazol, Olanzapin, Quetiapin oder Ziprasidon als mögliche Kombinationspartner von Clozapin zur möglichen Behandlung eines refraktären Behandlungsverlaufs. In einem Cochrane-Review [1] konnten (leichte) Vorteile für eine Kombination mit Aripiprazol hinsichtlich der Verträglichkeit sowie mit Amisulprid hinsichtlich der Wirksamkeit festgestellt werden, die Autoren konstatieren jedoch eine weiterhin sehr limitierte Datengrundlage für weitergehende Schlussfolgerungen. Kürzlich erschienene Arbeiten liefern Hinweise auf positive Effekte bei einer Kombination mit Paliperidon in der Wirksamkeit und Verträglichkeit [3] sowie mit Cariprazin [4, 28], was jedoch von Weise et al. [27] nicht bestätigt werden konnte. Insgesamt scheint es jedoch in der Kombinationsbehandlung mit Clozapin auch häufig zu einer nicht leitliniengerechten Behandlung zu kommen [19], wobei die Autoren auch auf eine besondere Krankheitsschwere dieser Patienten hinweisen.
Kombinationspartner Amisulprid und Olanzapin
Nach Messer und Schmauss [15] bilden die Kombinationen von Clozapin oder Olanzapin jeweils mit Amisulprid, Risperidon oder Aripiprazol aus pharmakodynamischer Sicht theoretisch sinnvolle Kombinationspartner. Der Einsatz von Clozapin ist aufgrund des Nebenwirkungsprofils und damit verbundener Kontrolluntersuchungen begrenzt, weshalb Olanzapin einen aussichtsreichen alternativen Kombinationspartner im Sinne eines breiten Rezeptorbindungsprofils darstellt. Auch bewies Olanzapin in der Metaanalyse als Einzelsubstanz eine sehr hohe klinische Wirksamkeit [13]. Weiterhin weist es eine ähnliche chemische trizyklische Struktur und ein vergleichbares Rezeptorbindungsprofil wie Clozapin auf.
Da Amisulprid in der Kombinationsbehandlung mit Clozapin günstige therapeutische Ergebnisse zeigte [17], ist auch in der Kombination von Amisulprid mit Olanzapin ein Behandlungsvorteil zu erwarten. So könnte aufgrund der Rezeptorbindungsprofile die selektive Blockade von dopaminergen D2/D3-Rezeptoren durch Amisulprid die sehr breite Wirkung von Olanzapin auf D1-, D2-, D3-, 5-HT2-, M1-, Alpha-1- und H1-Rezeptoren ergänzen. Bei moderater Blockade von D2-Rezeptoren durch Olanzapin verbunden mit hoher Blockade von D2/D3 durch Amisulprid ergibt sich ein Potenzial für einen komplementären positiven Wirkeffekt [16].
Außerdem bestehen Unterschiede der Substanzen in Bezug auf Nebenwirkungen. Olanzapin führt häufig zu einer Zunahme von Gewicht, Blutglucose- und Lipidspiegel. Bei Amisulprid dagegen stehen extrapyramidal-motorische Wirkungen und Prolactin-assoziierte Wirkungen im Vordergrund [13]. Das ergänzende Rezeptorbindungsprofil beider Substanzen könnte zu einer Effektivitätssteigerung führen und eine geringere Einzeldosierung ermöglichen und damit dosisabhängige unerwünschte Nebenwirkungen reduzieren. In retrospektiven Studien konnte gezeigt werden, dass diese Kombinationsbehandlung eine gute Effektivität und kein erhöhtes Risiko hinsichtlich Verträglichkeit und Sicherheit aufwies [12, 29]. Pharmakokinetische Interaktionen sind aufgrund der unterschiedlichen Wege der Metabolisierung beider Substanzen nicht zu erwarten: Amisulprid wird durch unveränderte Urinexkretion eliminiert, Olanzapin dagegen durch Cytochrom P450 hepatisch metabolisiert.
Zur empirischen Überprüfung dieser aus theoretischen Überlegungen abgeleiteten (möglichen) besseren Wirksamkeit der Kombinationsbehandlung von Amisulprid mit Olanzapin wurde zwischen 2012 und 2018 eine multizentrische, doppelblinde randomisierte klinische Studie an 16 psychiatrischen Kliniken in Deutschland unter Förderung des Bundesministeriums für Bildung und Forschung durchgeführt (Förderkennzeichen 01KG1102; [21, 22].
Design der COMBINE-Studie
In einem dreiarmigen Design wurden nach randomisierter Zuweisung Patienten mit akuter Schizophrenie oder einer schizoaffektiven Erkrankung entweder mit einer Kombination aus Amisulprid plus Olanzapin (AMI + OLA), oder der Monotherapie mit Amisulprid (AMI) bzw. Olanzapin (OLA) in oraler, identischer Kapselform (verblindetes Double-Dummy-Design mit zusätzlicher Placebo-Gabe bei Monotherapie) über einen Zeitraum von 16 Wochen behandelt. Die jeweilige Behandlungsdosis konnte je nach klinischer Einschätzung 200 bis 800 mg/Tag Amisulprid, 5 bis 20 mg/Tag Olanzapin oder aber die jeweilige additive Dosis bei Kombinationstherapie umfassen. Vorab wurden vier zu verabreichende Dosisstufen-Einheiten definiert (Amisulprid in jeweils 200/400/600/800 mg; Olanzapin: 5/10/15/20 mg; Kombination: die jeweilige additive Dosisstufen-Menge, d. h. 200 Ami +5 Ola, 400 Ami +10 Ola etc.), sodass eine individuelle Dosisanpassung bei gewährleisteter Verblindung möglich war. Nach Einschluss und Randomisierung wurde die Vor-Studienmedikation schrittweise vollständig abdosiert und die Studienmedikation parallel schrittweise aufdosiert. Im Abstand von zwei Wochen fanden Studien-Visiten statt (mit der Möglichkeit von Zwischenkontakten bei Bedarf, vor allem in der Eindosierungsphase).
Die Patienten mussten zwischen 18 und 65 Jahren alt sein, eine akute psychotische Symptomatik aufweisen (erfasst über das standardisierte Erhebungsinstrument PANSS [Positive and negative syndrome scale] [11]) sowie ausreichend deutsche Sprachkenntnisse haben, um ihre informierte Einwilligung zu geben. Ausschlusskriterien waren (u. a.) eine erste Erkrankungsepisode, akute Suizidalität, Schwangerschaft, Non-Response auf eine mögliche Clozapin-Vorbehandlung oder keine freiwillige Behandlung. Eine vorliegende Substanzabhängigkeit oder Missbrauch waren dagegen kein Ausschlusskriterium. Vor Beginn der Studie wurden die jeweiligen zustimmenden Ethikvoten eingeholt.
Im Rahmen der alle zwei Wochen stattfindenden Visiten wurde eine Vielzahl relevanter Parameter in der Regel mit standardisierten Instrumenten erhoben: psychotische (PANSS) und andere psychische Symptome, Nebenwirkungen (insbesondere extrapyramidale Symptome), unerwünschte und schwerwiegende unerwünschte Ereignisse ([S]UE) sowie eine Vielzahl körperlicher und Laborparameter (z. B. Gewicht, EKG, Blutbild, Fettstoffwechsel, Diabetesparameter).
Als primäre Zielgröße wurde vorab die Symptomreduktion schizophrener Symptome (Positiv-, Negativ- und allgemeine-Symptome, zusammengefasst im PANSS-Gesamtwert) nach acht Wochen (Visite 4) festgelegt, wofür vorab eine Power-/Fallzahl-Kalkulation durchgeführt wurde. Veränderungen in spezifischen Symptomen, auftretende Nebenwirkungen bzw. SUE, Laborwertveränderungen und die vorzeitige Abbruchrate waren sekundäre Ergebnisparameter. An statistischen Methoden kamen t-Test, Varianz- und Kovarianz-Analysen sowie sogenannte „gemischte Modelle“ (mixed models repeated measurement analysis) zur Anwendung. Wie in nahezu allen Antipsychotika-Studien brach eine nicht unerhebliche Anzahl der Patienten die Studie vorzeitig ab (ca. 38 % nach acht Wochen; ca. 60 % insgesamt vor Erreichen der 16 Wochen; jeweils kein signifikanter Unterschied zwischen den Behandlungsgruppen). Zur Vermeidung dadurch entstehender möglicher Verzerrungen wurden die hierdurch entstandenen fehlenden Werte mittels verschiedener statistischer Methoden (Imputationsverfahren) geschätzt und in die Auswertung miteinbezogen.
Ergebnisse der COMBINE-Studie
An den 16 beteiligten Kliniken wurden zwischen 2012 und 2018 insgesamt über 13 000 Patienten gesichtet, von denen 328 in die Studie eingeschlossen und randomisiert werden konnten. Davon konnten nach den vorab festgelegten Kriterien schließlich 321 in die finale Auswertung einbezogen werden (110 Amisulprid + Olanzapin [AMI + OLA]; 109 Amisulprid + Placebo [AMI]; 102 Olanzapin + Placebo [OLA]). Das Durchschnittsalter lag bei 40,2 Jahren (Standardabweichung [SD] = 11,7), der Anteil der Männer betrug 71 %. Der weitaus größte Teil (84 %) hatte die Diagnose Schizophrenie (15 % schizoaffektive Erkrankung) und nahezu alle Patienten (98 %) befanden sich in stationärer Behandlung.
In Bezug auf das primäre Zielkriterium (Rückgang der psychotischen Symptomatik entsprechend dem PANSS-Gesamtwert von Studienbeginn bis V4/nach acht Wochen) zeigte sich, dass Patienten, die eine Kombination aus Amisulprid und Olanzapin erhielten, eine im Mittel signifikant stärkere Symptomverbesserung (–29,6; SD 14,5) aufwiesen als solche, die eine Monotherapie mit Olanzapin erhielten (–24,1; SD 3,4; p = 0,0249; adjustiert p = 0,049 nach Bonferroni-Holm; Effektstärke Cohen’s d = 0,396). Auch gegenüber der Monotherapie mit Amisulprid (mittlerer Symptomrückgang = –25,2 ± 15,9; Cohen’s d = 0,29) zeigte sich ein Vorteil für die Kombinationsbehandlung, der nach Alpha-Adjustierung jedoch nicht signifikant wurde (p = 0,095; Abb. 1).
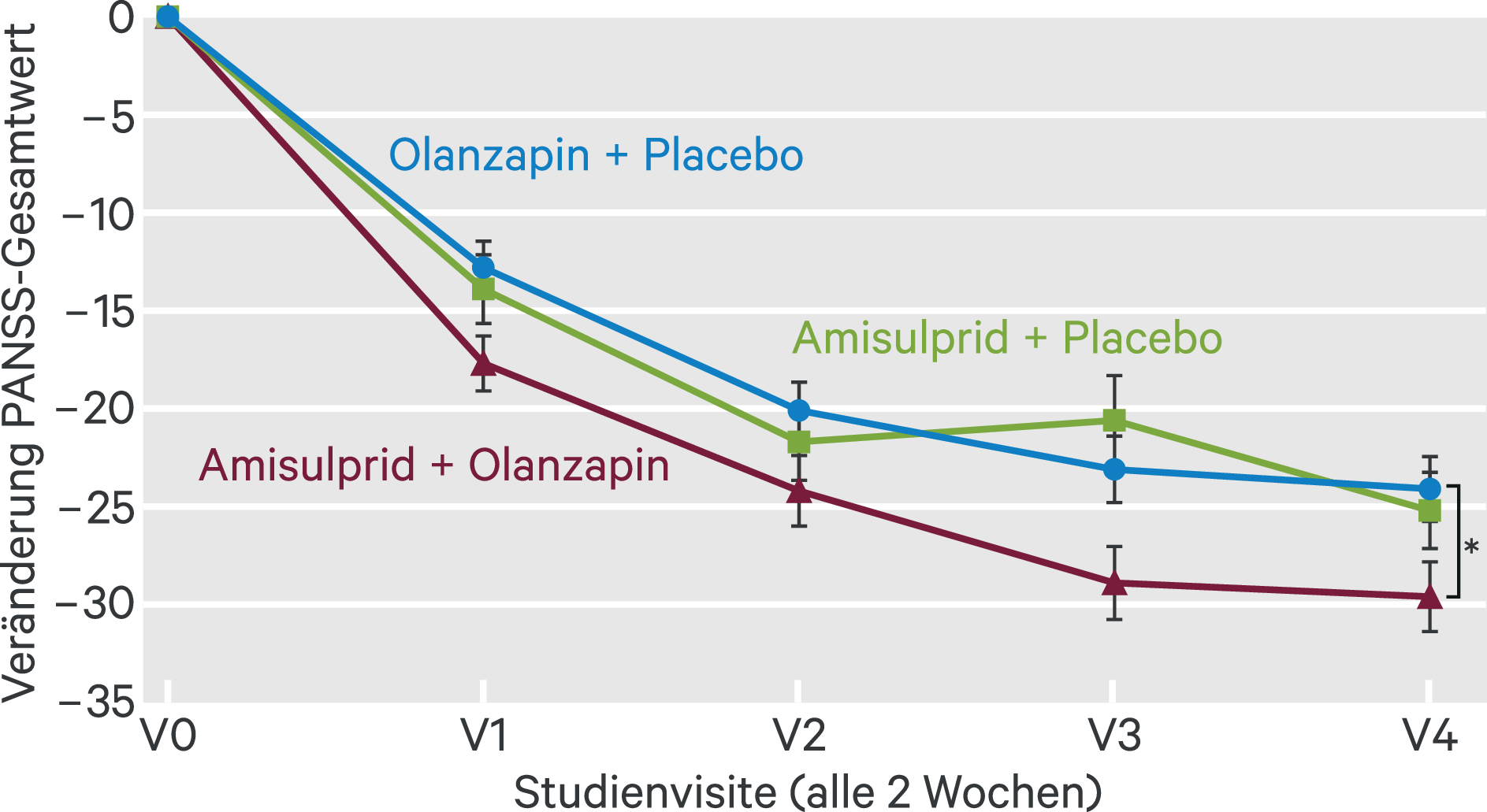
Abb. 1. Rückgang der schizophrenen Symptomatik in den drei Therapiegruppen, erfasst durch den PANSS-Gesamtwert ab Studienbeginn. Punktwerte repräsentieren die Veränderung der Mittelwerte (inkl. 95%-Konfidenzintervall [KI]). Der primäre Endpunkt war die Veränderung zwischen Studieneinschluss und V4 nach acht Wochen: Differenz zwischen Kombinationstherapie und Olanzapin-Monotherapie p = 0,049; Cohen’s d = 0,396; zwischen Kombinationstherapie und Amisulprid-Monotherapie p = 0,095; Cohen’s d = 0,29 (jeweils t-Test mit Alpha-Adjustierung nach Bonferroni-Holm). (Mod. nach [22])
Wie eingangs erwähnt, war eine nicht unerhebliche Drop-out-Rate (ca. 38 % nach acht Wochen; ca. 60 % insgesamt vor Erreichen der 16 Wochen; jeweils kein signifikanter Unterschied zwischen den Behandlungsgruppen) zu verzeichnen. Zur Absicherung gegenüber sich dadurch ergebenden möglichen Verzerrungseffekten wurden verschiedene statistische Verfahren (Bayes-Methoden, Imputationsverfahren, jeweils mit und ohne Adjustierung nach Eingangswerten) durchgeführt, die den Unterschied zwischen Kombinations- und Monotherapie ebenfalls bestätigten und auf Basis der Imputationsverfahren (mit konstant hohen Fallzahlen) sogar noch verdeutlichten (AMI + OLA vs. OLA + PBO p = 0,026, Cohen’s d = 0,35; AMI + OLA vs. AMI + PBO p = 0,037, Cohen’s d = 0,35).
Die sekundären Endpunkte zeigten, dass die globale Erkrankungsschwere, erfasst über den klinischen Gesamteindruck (CGI), bei Patienten unter Kombinationstherapie sich nach acht Wochen signifikant stärker reduzierte als bei Patienten unter der Behandlung mit Amisulprid-Monotherapie (p = 0,046). Darüber hinaus zeigte sich nach acht Wochen eine signifikant stärkere Reduktion von Negativsymptomen gemäß PANSS-Skala bei Patienten mit Kombinationstherapie als bei solchen mit Olanzapin-Monotherapie (p = 0,043; Abb. 2). Es muss jedoch erwähnt werden, dass all diese Unterschiede (einschließlich der Gesamt-Symptomatik, die dem primären Endpunkt zugrunde lag) zum Ende der Studienbehandlung nach 16 Wochen nicht mehr statistisch signifikant unterschiedlich waren.
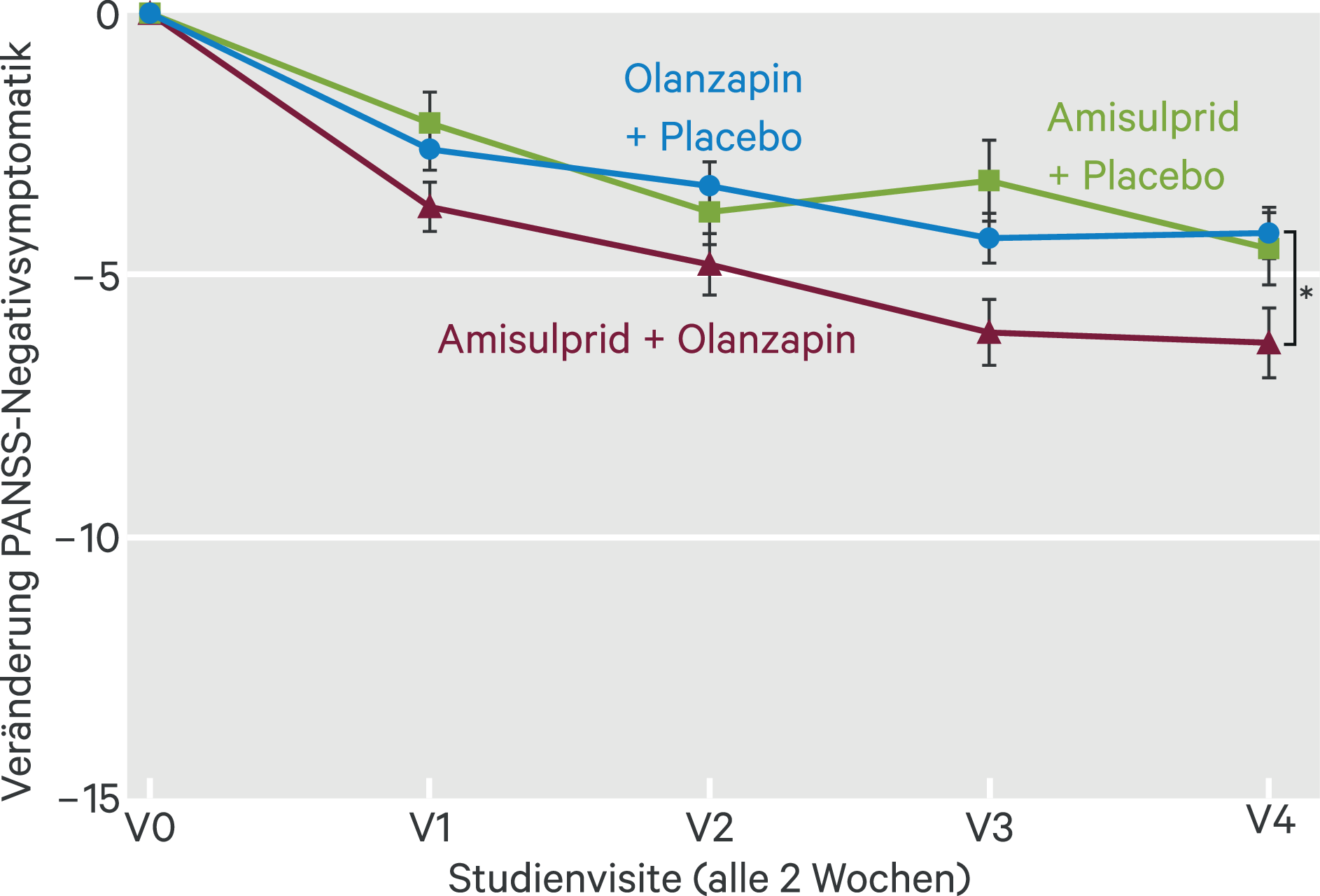
Abb. 2. Rückgang der Negativsymptomatik in den drei Therapiegruppen, erfasst durch die PANSS-Negativskala ab Studienbeginn. Punktwerte repräsentieren die Veränderung der Mittelwerte (inkl. 95%-Konfidenzintervall). Differenz zwischen Kombinationstherapie und Olanzapin-Monotherapie p = 0,043; Cohen’s d = 0,458 (mod. nach [22])
In Bezug auf unerwünschte Nebenwirkungen, war die Kombinationstherapie AMI + OLA sowie die Monotherapie mit Olanzapin im Vergleich zur Monotherapie mit Amisulprid mit einer im Mittel größeren Zunahme des Bauchumfangs nach acht Wochen verbunden (4,4 cm [SD 6,1] bzw. 4,0 cm [SD 6,1] vs. –0,5 cm [SD 5,8]; beide p = 0,001). Auch zeigte sich nach acht Wochen eine größere Gewichtszunahme unter der Kombinationstherapie AMI + OLA als bei der Monotherapie mit Amisulprid (4,4 kg [SD 6,3] vs. 1,4 kg [SD 4,2]; p = 0,027). Weiterhin zeigten sich nach acht Wochen auch im Body-Mass-Index sowohl unter der Kombinationstherapie AMI + OLA als auch unter Monotherapie mit Olanzapin höhere Werte als unter Monotherapie mit Amisulprid (AMI + PBO: 25,5 [SD 4,0]; AMI + OLA: 28,3 [SD 5,5], p = 0,01; OLA+PBO: 28,2 [SD 5,6], p = 0,014). Dagegen zeigten sich keine Unterschiede im Auftreten von Diabetes mellitus, einem metabolischen Syndrom oder einer QTc-Zeit-Verlängerung im EKG. In einem Fragebogen zu sexuellen Funktionen (Derogatis Interview for sexual functioning [DISF]) ergaben sich nach acht Wochen unter Kombinationstherapie signifikant mehr Beeinträchtigungen im Vergleich zur Amisulprid-Monotherapie. Dagegen waren bei der Dokumentation von unerwünschten oder schweren unerwünschten Ereignissen im gesamten Verlauf keine Gruppenunterschiede vorhanden.
Diskussion
Die möglichen Ursachen der höheren Effektivität einer Kombinationstherapie sind kritisch zu diskutieren. So wurde in einer Metaanalyse festgestellt, dass eine hochdosierte Kombinationsbehandlung die Überlegenheit gegenüber Antipsychotika-Monotherapie begünstigt [5]. Eine Erklärung hierfür besteht in einer höheren Dopaminblockade, die auch unter einer Hochdosis-Monotherapie erreicht werden kann. Es bleibt also die Frage offen, ob es sich bei einer derartigen „Überlegenheit“ um einen Effekt einer Kombinationstherapie im eigentlichen Sinne handelt oder ob sie durch eine höhere Gesamt-Dosis zu erklären ist. Bei der Entwicklung des Studiendesigns der COMBINE-Studie wurden verschiedene Varianten in Betracht gezogen, um diese Frage zu klären: So könnte man die Dosis der einzelnen Antipsychotika in der Kombinationsgruppe reduzieren oder eine hochdosierte Monotherapiegruppe zum Vergleich einsetzen, was sich als nicht realisierbar herausstellte. Eine Metaanalyse zur Hochdosistherapie von Antipsychotika konnte jedoch bisher keine Vorteile gegenüber dem herkömmlichen Dosierungsbereich nachweisen [20]. Auch eine Analyse der COMBINE-Daten ergab keinen Zusammenhang zwischen der verabreichten (additiven) Gesamtdosis und dem Therapieerfolg.
Aufgrund der Limitierung klinischer Studien hinsichtlich Durchführbarkeit und Fallzahlplanung bleibt die Beantwortung solcher Fragen in Zukunft eine Herausforderung. Kompromisse, die sich an der täglichen klinischen Praxis orientieren, erscheinen daher unvermeidlich. So strebten wir einen verallgemeinerbaren und klinisch nützlichen Vergleich an und beschlossen, dass die antipsychotische Dosis vom behandelnden Arzt auf der Grundlage der klinischen Wirksamkeit und Sicherheit in allen drei Behandlungsarmen innerhalb eines wirksamen Dosisbereichs individualisiert wird. Dies führte interessanterweise dazu, dass die behandelnden Ärzte den Patienten in der Gruppe der Kombinationstherapie signifikant geringere Dosierungen der jeweiligen Einzelsubstanzen verordneten, was möglicherweise auf ein besseres Ansprechen auf die Therapie in dieser Gruppe zurückzuführen war. Hervorzuheben ist zudem, dass die COMBINE-Studie auch ein höheres Ansprechen auf die Kombinationsbehandlung in Bezug auf Negativsymptome zeigte, was in dieser Form für eine Erhöhung der gesamten antipsychotischen Äquivalenzdosierung eher nicht zu erwarten wäre.
Fazit
Antipsychotische Polypharmazie ist in der klinischen Praxis sehr häufig anzutreffen, obwohl evidenzbasierte Leitlinien Monotherapie mit einem Antipsychotikum eindeutig priorisieren. Dennoch gibt es auch Gründe, die in bestimmten Situationen für eine Kombination von Antipsychotika sprechen können. Die empirische Evidenz für eine rationale Entscheidung hinsichtlich spezifischer Kombination war jedoch bisher kaum vorhanden. Angesichts einer großen Anzahl an therapieresistenten oder gar refraktären Behandlungsverläufen besteht jedoch Bedarf an weiteren Optionen empirisch überprüfter Kombinationstherapie. Für die Kombination von Amisulprid und Olanzapin sehen wir diese durch die Ergebnisse der COMBINE-Studie als gegeben an. Auch wenn unter den Monotherapien die Wirkvorteile der Kombinationsbehandlung nach 16 Wochen wieder ausgeglichen wurden, resultiert insgesamt aus diesen Studienergebnissen, dass Amisulprid und Olanzapin in manchen klinischen Situationen anstelle von anderen Kombinationstherapien ohne vorliegende Evidenz – unter Berücksichtigung potenziell höherer Raten von unerwünschten Wirkungen – verordnet werden könnte. Besonders in Akutsituationen, bei Patienten mit Therapieresistenz, in denen das Ansprechen der Symptomatik beschleunigt werden soll und der Einsatz von Clozapin keine Option darstellt, könnte die Kombinationstherapie aus Amisulprid und Olanzapin sinnvoll sein.
Antipsychotische Kombinationstherapie bleibt ein hochrelevantes Thema für die Versorgung von Patientinnen und Patienten mit schizophrenen Störungen. Die unterschiedlichen, in der klinischen Praxis vorgenommenen Behandlungskombinationen fordern weiterhin eine kritische Bewertung und empirische Fundierung.
Interessenkonflikterklärung
Bei CSK und MR besteht kein Interessenkonflikt.
Literatur
1. Barber S, Olotu U, Corsi M, et al. Clozapine combined with different antipsychotic drugs for treatment-resistant schizophrenia. Cochrane Database Syst Rev 2017;3(3):CD006324.
2. Benkert O, Hippius H. Kompendium der psychiatrischen Pharmakotherapie Berlin, Heidelberg: Springer, 2021.
3. Bioque M, Paradella E, García-Rizo C, et al. Clozapine and paliperidone palmitate antipsychotic combination in treatment-resistant schizophrenia and other psychotic disorders: A retrospective 6-month mirror-image study. Eur Psychiatry 2020;63:e71. doi: 10.1192/j.eurpsy.2020.72.
4. Bogren M, Soltesz M, Hjorth S. Remission of persistent negative symptoms and psychosocial consequences by combined clozapine and cariprazine treatment in a patient with long-standing treatment resistant schizoaffective disorder. Front Psychiatry 2022;13:887547; doi: 10.3389/fpsyt.2022.887547.
5. Correll CU, Rummel-Kluge C, Corves C, et al. Antipsychotic combinations vs monotherapy in schizophrenia: a meta-analysis of randomized controlled trials. Schizophrenia Bull 2009;35:443–57.
6. DGPPN. S3-Leitlinie Schizophrenie. Langfassung Version 1.0, zuletzt geändert am 15. März 2019, verfügbar unter: https://register.awmf.org/assets/guidelines/038-009l_S3_Schizophrenie_2019-03.pdf (Zugriff am 15.08.2022).
7. Fleischhacker WW, Heikkinen ME, Olie JP, et al. Effects of adjunctive treatment with aripiprazole on body weight and clinical efficacy in schizophrenia patients treated with clozapine: a randomized, double-blind, placebo-controlled trial. Int J Neuropsychopharmacol 2010;13:1115–25.
8. Gallego JA, Bonetti J, Zhang JP, et al. Prevalence and correlates of antipsychotic polypharmacy: A systematic review and meta-regression of global and regional trends from the 1970s to 2009. Schizophr Res 2012;138:18–28.
9. Galling B, Roldan A, Hagi K, et al. Antipsychotic augmentation vs. monotherapy in schizophrenia: systematic review, meta-analysis and meta-regression analysis. World Psychiatry 2017;16:77–89.
10. Gründer G, Benkert, O. Handbuch der Psychopharmakotherapie. Berlin, Heidelberg: Springer, 2012.
11. Kay SR, Fiszbein A, Opfer LA. The positive and negative syndrome scale (PANSS) for schizophrenia. Schizophr Bull 1987;13:261–76.
12. Lerner V, Bergman J, Borokhov A, Loewenthal U, et al. Augmentation with amisulpride for schizophrenic patients nonresponsive to antipsychotic monotherapy. Clin Neuropharmacol 2005;28:66–71.
13. Leucht S, Arbter D, Engel RR, Kissling W, et.al. How effective are second-generation antipsychotic drugs? A meta-analysis of placebo-controlled trials. Mol Psychiatry 2009;14:429–47.
14. Matsui K, Tokumasu T, Takekita Y, et al. Switching to antipsychotic monotherapy vs. staying on antipsychotic polypharmacy in schizophrenia: A systematic review and meta-analysis. Schizophr Res 2019;209:50–7.
15. Messer T, Schmauss M. Polypharmazie in der Behandlung psychischer Erkrankungen. Wien: Springer, 2016.
16. Molina JD, Toledo-Romero F, Lopez-Rodriguez E, Amorin-Diaz M, et al. Augmentation treatment with amisulpride in schizophrenic patients partially responsive to olanzapine, Pharmacopsychiatry 2011;44:142–7.
17. Pani L, Villagran JM, Kontaxakis VP, Alptekin K. Practical issues with amisulpride in the management of patients with schizophrenia, Clin Drug Investig 2008;28:465–77.
18. Preskorn, SH, Lacey RL. Polypharmacy: when is it rational? J Psychiatr Pract 2007;13:97–105.
19. Rentrop M, Huhn M, Schwerthöffer D. Clozapin in der Behandlung schizophrener Psychosen: Patientencharakteristika und antipsychotische Kombinationstherapien bei einem Behandlungsjahrgang eines psychiatrischen Versorgungskrankenhauses. Fortschr Neurol Psychiatr 2021;89:622–9.
20. Samara MT, Leucht C, Leeflang MM, Anghelescu IG, et al. Early improvement as a predictor of later response to antipsychotics in schizophrenia: A diagnostic test review. Am J Psychiatry 2015;172:617–29.
21. Schmidt-Kraepelin C, Feyerabend S, Engelke C, Riesbeck M, et al. A randomized double-blind controlled trial to assess the benefits of amisulpride and olanzapine combination treatment versus each monotherapy in acutely ill schizophrenia patients (COMBINE): methods and design. Eur Arch Psychiatry Clin Neurosci 2020;270:83–94.
22. Schmidt-Kraepelin C, Feyerabend S, Engelke C, Riesbeck M, COMBINE Study Group 2022. Amisulpride and olanzapine combination treatment versus each monotherapy in acutely ill patients with schizophrenia in Germany – COMBINE: a double-blind randomised controlled trial. Lancet Psychiatry 2022;9:291–306.
23. Schmidt-Kraepelin C, Meisenzahl-Lechner E, Kujovic M, Cordes J, et al. Antipsychotische Polypharmazie in der Behandlung von Patientinnen und Patienten mit Schizophrenie am Beispiel von neun psychiatrischen Fachkliniken des Landschaftsverbandes Rheinland. Psychiatr Prax 2021;48:250–7.
24. Stahl SM. Antipsychotic polypharmacy: never say never, but never say always. Acta Psychiatr Scand 2012;125:349–51.
25. Stroup TS, Lieberman JA, McEvoy JP, Davis SM, et al.; CATIE Investigators. Results of phase 3 of the CATIE schizophrenia trial. Schizophr Res 2009;107: 1–12.
26. Tiihonen J, Mittendorfer-Rutz E, Majak M, et al. Real-world effectiveness of antipsychotic treatments in a nationwide cohort of 29823 patients with schizophrenia. JAMA Psychiatry 2017;74:686–93.
27. Weise J, Schomerus G, Speerforck S. Add-on cariprazine in patients with long-term clozapine treatment and treatment resistant schizophrenia: two cases of psychotic deterioration and pisa syndrome. Clin Psychopharmacol Neurosci 2022;20:398–401.
28. Werner FM, Covenas R. The novel antipsychotic drug cariprazine and cognition enhancing drugs: indication for their use as the add-on therapy in schizophrenia Curr Pharm Des 2021;27:4033–8.
29. Zink M, Henn FA, Thome J. Combination of amisulpride and olanzapine in treatment-resistant schizophrenic psychoses, Eur Psychiatry 2004;19:56–8.
Dr. Christian Schmidt-Kraepelin, Kaiserswerther Diakonie, Florence Nightingale Krankenhaus, Alte Landstraße 179, 40489 Düsseldorf, LVR-Klinikum Düsseldorf, Kliniken der Heinrich-Heine-Universität Düsseldorf, Bergische Landstraße 2, 40629 Düsseldorf, E-Mail: Christian.Schmidt-Kraepelin@hhu.de
Mathias Riesbeck, LVR-Klinikum Düsseldorf, Kliniken der Heinrich-Heine-Universität Düsseldorf, Bergische Landstraße 2, 40629 Düsseldorf, E-Mail: mathias.riesbeck@lvr.de
Polypharmacy or monotherapy in schizophrenia? Antipsychotic monotherapy or combination treatment in schizophrenia: results of the German COMBINE study
Evidence-based treatment guidelines recommend antipsychotic monotherapy as first-line, however antipsychotic polypharmacy (APP) is frequent in routine clinical practice. Based on theoretical considerations there a some "good reasons" for APP, and also some studies show advantages. Overall, however, the evidence base, especially with regard to specific combinations, is scarce. In the present review article, results on the evidence of antipsychotic combination therapy are summarized narratively and the results of the COMBINE study, which tested the combination therapy of amisulpride and olanzapine in patients with acute symptoms of schizophrenia, are presented. This study including 321 patients, showed significant advantages in primary outcome (symptom reduction after 8 weeks) for combination compared to olanzapine monotherapy. Statistical methods dealing with missing values due to drop-out confirm these results and even show also advantages over amisulpride monotherapy. However, these and other advantages do not prevail after 16 weeks. In addition, combination treatment was afflicted with some more pronounced side effects, especially weight gain, however not different from olanzapine monotherapy. Given advantages in efficacy of amisulpride and olanzapine combination, it should be a rational treatment option in some patients or clinical situations, however risks for side effects have to be considered.
Keywords: Antipsychotic combination treatment, polypharmacy, schizophrenia.
Psychopharmakotherapie 2023; 30(01):5-10
