Henrik Uebel-von Sandersleben, Göttingen
Die Aufmerksamkeitsdefizit-/Hyperaktivitätsstörung (ADHS) ist mit einer weltweiten Prävalenz von 7,2 % eine der häufigsten psychischen Störungen bei Kindern und Jugendlichen [40]. In Deutschland wird die Prävalenz bei Kindern unter 18 Jahren auf 6,1 % geschätzt [2]. Bei etwa 40 bis 50 % der Betroffenen persistiert die Erkrankung bis ins Erwachsenenalter [39]. ADHS ist gekennzeichnet durch die Kernsymptome Hyperaktivität, Unaufmerksamkeit und Impulsivität, die zu funktionellen Beeinträchtigungen in verschiedenen Lebensbereichen, beispielsweise im schulischen, familiären oder beruflichen Alltag, führen [1]. Diese Beeinträchtigungen sind über die gesamte Lebensspanne mit einem hohen Leidensdruck und verschiedenen negativen Konsequenzen assoziiert. So leiden Kinder und Jugendliche mit ADHS häufig unter einem verminderten Selbstwertgefühl [20], haben weniger Freundschaften und erfahren Ablehnung durch Gleichaltrige [3]. Zudem haben ADHS-Patienten ein erhöhtes Verletzungs- und Unfallrisiko [5]. ADHS ist auch mit einem erhöhten Risiko für kriminelles/delinquentes Verhalten assoziiert [33]. Bei 66 % der Betroffenen bestehen komorbide psychiatrische Erkrankungen, die sowohl die Diagnose als auch die Therapie erschweren können [34].
Die Behandlung der ADHS sollte leitliniengemäß im Rahmen eines umfassenden multimodalen Gesamtkonzepts erfolgen, das psychosoziale und pharmakologische Therapien kombiniert und auf die individuellen Bedürfnisse des Patienten zugeschnitten ist [10]. Für die medikamentöse Behandlung der ADHS stehen die Psychostimulanzien Methylphenidat, Amfetamin und Lisdexamfetamin sowie die Nicht-Stimulanzien Atomoxetin und Guanfacin zur Verfügung [10]. Methylphenidat ist in der Regel das Mittel der ersten Wahl und gilt als Goldstandard bei der Pharmakotherapie der ADHS. Dementsprechend ist Methylphenidat in Deutschland der mit Abstand am häufigsten verschriebene Wirkstoff für die Behandlung der ADHS [2]. Die Wirksamkeit und Sicherheit von Methylphenidat in der Behandlung der ADHS wurde in zahlreichen randomisierten kontrollierten Studien und Metaanalysen belegt [9, 12]. Die Ansprechrate auf Methylphenidat beträgt etwa 70 bis 80 % [18].
Ursprünglich waren nur schnellfreisetzende (immediate-release) Methylphenidat-Formulierungen verfügbar. Aufgrund der kurzen Halbwertszeit von Methylphenidat beträgt die Wirkdauer dieser Präparate im Durchschnitt vier Stunden [43]. Daher müssen diese Präparate in der Regel zweimal täglich (manchmal auch öfter) eingenommen werden, was mit verschiedenen Problemen assoziiert sein kann, wie Stigmatisierung (bei Einnahme in der Schule) oder mangelnder Adhärenz. Zudem können Schwankungen im Plasmaspiegel zu einer verminderten Wirksamkeit oder einem erhöhten Risiko für unerwünschte Ereignisse führen [43]. Dies führte zur Entwicklung von Methylphenidat-Retardpräparaten, die aufgrund ihrer längeren Wirkdauer in der Regel nur einmal täglich eingenommen werden müssen.
Methylphenidat-Retardpräparate
In Deutschland sind aktuell mehrere langwirksame, retardierte Methylphenidat-Formulierungen verfügbar: Medikinet® retard/adult, Ritalin® LA/Adult, Concerta® und Equasym® Retard. Mittlerweile sind auch Generika von Ritalin® LA, Concerta® und Equasym® Retard erhältlich. Medikinet® retard ist für Kinder, Jugendliche und Erwachsene zugelassen, Medikinet® adult nur für Erwachsene. Ritalin® LA und Ritalin® Adult sind für Kinder und Jugendliche bzw. Erwachsene zugelassen. Equasym® Retard und Concerta® sind beide für Kinder und Jugendliche zugelassen. Bei Concerta® ist eine Fortführung der Therapie ins Erwachsenenalter möglich, eine Therapieinitiierung bei Erwachsenen ist jedoch nicht angezeigt [21, 25, 26, 28, 29, 38]. Alle Präparate bestehen aus einem Gemisch von sofort freigesetztem und verzögert freigesetztem Methylphenidat, wodurch sowohl ein schneller Wirkungseintritt als auch eine lange Wirkdauer gewährleistet wird. Die einzelnen Präparate basieren jedoch auf unterschiedlichen galenischen Technologien und unterscheiden sich im Verhältnis von sofort und verzögert freigesetztem Methylphenidat [4].
Sowohl bei Medikinet® retard als auch bei Ritalin® LA handelt es sich um Hartgelatinekapseln, die mit 50 % schnell und 50 % verzögert freisetzenden Pellets gefüllt sind. Bei Medikinet® retard wird der Retardierungseffekt durch eine magensaftresistente Beschichtung der Pellets erreicht, die sich erst ab einem pH-Wert von > 5,5 auflöst und somit den Wirkstoff zeitlich verzögert im Dünndarm freisetzt [16]. Ritalin® LA basiert auf der SODAS®(Spheroidal oral drug absorption system)-Technologie. Die verzögert freisetzenden Pellets besitzen eine Polymer-Beschichtung, die eine kontrollierte Diffusion des Wirkstoffs aus den Pellets ermöglicht [8]. Bei Equasym® Retard handelt es sich um Hartgelatinekapseln, die mit 30 % schnell und 70 % verzögert freisetzenden Pellets gefüllt sind. Der Retardierungseffekt wird durch eine Polymer-Beschichtung der Pellets erzeugt, durch die der Wirkstoff verzögert freigesetzt wird (Diffucaps®-Technologie) [41]. Concerta®-Tabletten basieren auf der OROS®(Osmotic release oral system)-Technologie. Die Tabletten sind mit 22 % schnell freisetzendem Methylphenidat ummantelt; die restlichen 78 % der Dosis werden durch osmotischen Druck schrittweise aus dem Inneren der Tablette freigesetzt [8].
Die unterschiedlichen galenischen Technologien und Anteile von sofort und verzögert freigesetztem Methylphenidat führen zu deutlichen Unterschieden in der Pharmakokinetik und Bioverfügbarkeit der Produkte, das heißt, jedes Präparat erzeugt ein spezifisches Freisetzungsprofil. Da die Plasmaspiegel im Tagesverlauf mit der klinischen Wirksamkeit korrelieren, erzeugt jedes Präparat auch ein spezifisches Wirksamkeitsprofil. Darüber hinaus gibt es Unterschiede zwischen den Formulierungen bezüglich der Einnahmeintervalle und -bedingungen (Einnahme mit oder ohne Nahrung, Möglichkeit zum Öffnen der Kapseln). Unterschiede bei den sonstigen Bestandteilen können zu unterschiedlicher Verträglichkeit der Präparate führen. Die wichtigsten Merkmale der Präparate sind in Tabelle 1 zusammengefasst. Der behandelnde Arzt sollte mit den spezifischen Eigenschaften der verfügbaren Methylphenidat-Retardpräparate vertraut sein und bei der Wahl der Medikation die individuellen Bedürfnisse und Präferenzen des Patienten berücksichtigen. Im Folgenden werden die Unterschiede zwischen den Präparaten im Detail dargestellt.
Tab. 1. Methylphenidat-Retardpräparate in Deutschland [6, 19, 21, 25, 26, 28, 29, 38]
|
Medikinet® retard/adult |
Ritalin® LA/Adult* |
Concerta®* |
Equasym® Retard* |
|
|
Stärken |
5/10/20/30/40/50/60 mg |
10/20/30/40 mg |
18/27/36/54 mg |
10/20/30/40/50 mg |
|
Galenische Technologie |
Hartkapseln mit schnell freisetzenden und magensaftresistenten verzögert freisetzenden Pellets |
SODAS® (Spheroidal oral drug absorption system) |
OROS® (Osmotic release oral system) |
Diffucaps® |
|
Methylphenidat-Freisetzung sofort : verzögert [%] |
50 : 50 |
50 : 50 |
22 : 78 |
30 : 70 |
|
Wirkdauer |
Kinder: Bis zu 8 Std. Erwachsene: Bis zu 16 Std. |
Bis zu 8 Std. |
Bis zu 12 Std. |
Bis zu 8 Std. |
|
Einnahmehäufigkeit und -zeitpunkt |
Kinder: 1-mal täglich morgens Erwachsene: 2-mal täglich morgens und mittags |
1-mal täglich morgens |
1-mal täglich morgens |
1-mal täglich morgens |
|
Einnahme mit oder ohne Nahrung |
Kinder: mit oder nach dem Frühstück Erwachsene: mit oder nach einer Mahlzeit |
Mit oder ohne Nahrung |
Mit oder ohne Nahrung |
Vor dem Frühstück |
|
Verabreichung |
Kapsel kann geöffnet und der Kapselinhalt auf eine kleine Menge (Esslöffel) Apfelmus oder Joghurt gestreut werden |
Kapsel kann geöffnet und die Kügelchen über breiige Speisen (z. B. Apfelmus) verteilt werden |
Tablette muss als Ganzes geschluckt werden und darf nicht gekaut, geteilt oder zerkleinert werden |
Kapsel kann geöffnet und der Kapselinhalt auf eine kleine Menge (Esslöffel) Apfelmus oder Brei gestreut werden |
* Für Ritalin® LA/Adult, Concerta® und Equasym® Retard sind Generika verfügbar.
Bioverfügbarkeit und Freisetzungsprofile
Das Wirksamkeitsprofil im Tagesverlauf wird vorrangig von der Bioverfügbarkeit bzw. dem Freisetzungsprofil der Formulierung bestimmt. In mehreren klinischen Studien wurden die Bioverfügbarkeit und pharmakokinetischen Profile verschiedener Methylphenidat-Retardpräparate verglichen. Die Bioverfügbarkeit, das heißt das Ausmaß und die Geschwindigkeit der Absorption eines Wirkstoffs, wird anhand der Plasmakonzentrations-Zeit-Kurven nach oraler Gabe bestimmt. Bioäquivalenz zwischen zwei Präparaten ist gegeben, wenn keine bedeutenden Unterschiede hinsichtlich der Fläche unter der Kurve (AUC) und der Maximalkonzentration (Cmax) bestehen. Gemäß europäischen Guidelines gelten zwei Präparate als bioäquivalent, wenn das 90%-Konfidenzintervall für den Quotienten aus Test- und Referenzpräparat für AUC und Cmax komplett innerhalb von 80 % bis 125 % liegt [7]. Es wird davon ausgegangen, dass bei bioäquivalenten Arzneimitteln auch eine therapeutische Äquivalenz vorliegt, das heißt die Präparate eine vergleichbare klinische Wirksamkeit haben.
Medikinet® retard vs. Ritalin® LA
Die Bioverfügbarkeit einer 40-mg-Einzeldosis von Medikinet® retard und Ritalin® LA wurde in einer Cross-over-Studie mit 28 gesunden männlichen Probanden sowohl im nüchternen als auch im nicht-nüchternen Zustand bestimmt [19]. Die Fläche unter der Plasmakonzentrations-Zeit-Kurve bis unendlich (AUC0–∞) und Cmax wurden für die Bewertung der Bioäquivalenz herangezogen. Die Zeit bis zum Erreichen der maximalen Konzentration (tmax) wurde ebenfalls bestimmt.
Einnahme nach einem Frühstück
Bei Einnahme nach einem Frühstück erzeugten sowohl Medikinet® retard als auch Ritalin® LA ein bimodales Plasmakonzentrations-Zeit-Profil mit zwei tmax-Peaks (Abb. 1). Medikinet® retard zeigte jedoch eine höhere Bioverfügbarkeit als Ritalin® LA. Die mittlere AUC0–∞ betrug 141,5 ± 38,30 ng × h/ml für Medikinet® retard, während der entsprechende Wert für Ritalin® LA 126,8 ± 34,50 ng × h/ml betrug. Die mittlere Cmax war ebenfalls höher bei Medikinet® retard (19,6 ± 5,95 ng/ml vs. 13,3 ± 4,04 ng/ml). Die Bioäquivalenzkriterien für Cmax wurden nicht erfüllt.
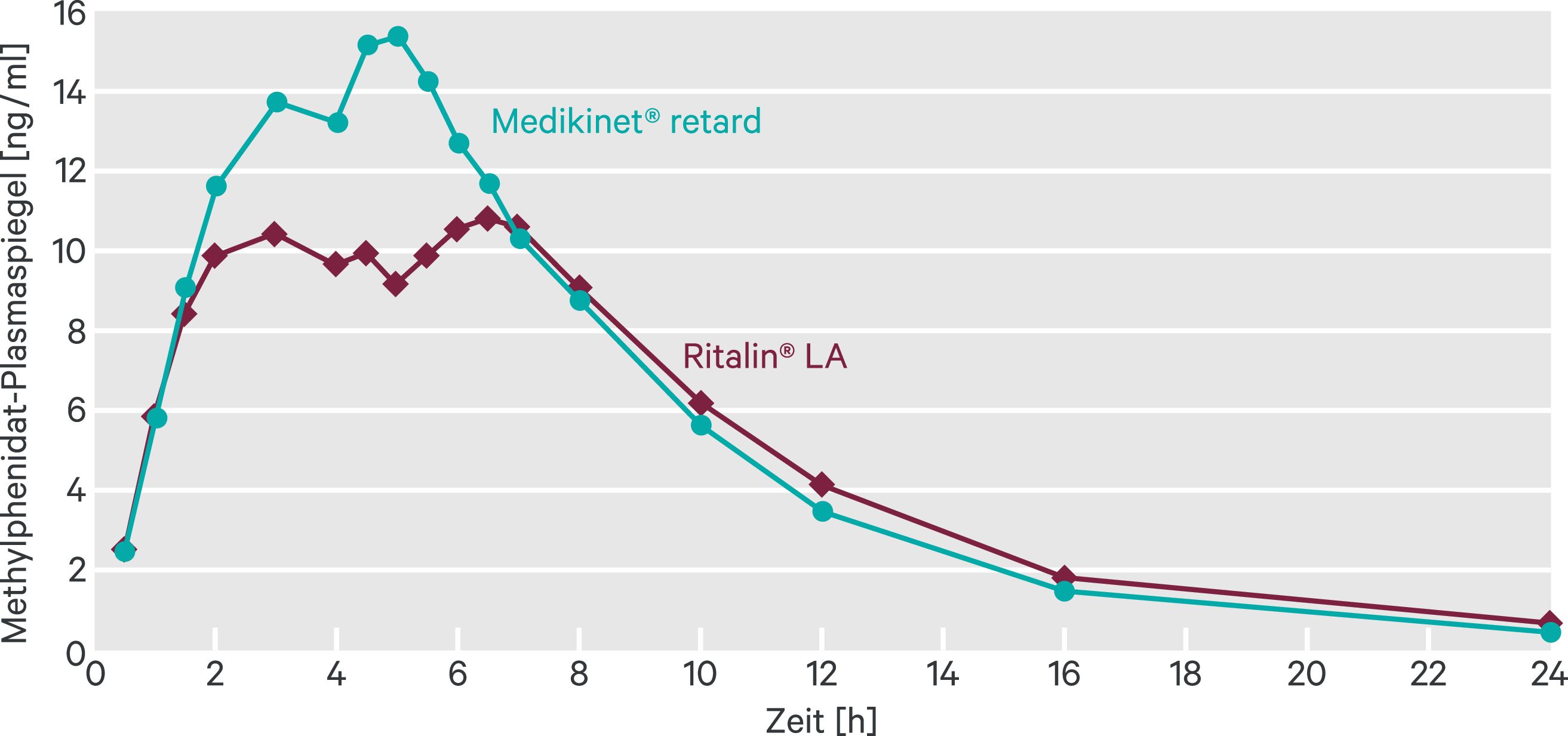
Abb. 1. Mittlere Methylphenidat-Plasmakonzentrationen nach Gabe einer 40-mg-Einzeldosis von Medikinet® retard oder Ritalin® LA im nicht-nüchternen Zustand (adaptiert nach [19])
Einnahme auf nüchternen Magen
Bei Einnahme auf nüchternen Magen erzeugte Ritalin® LA ein bimodales Plasmakonzentrations-Zeit-Profil mit zwei tmax-Peaks, während Medikinet® retard ein Absorptionsprofil mit einem einzigen tmax-Peak aufwies (Abb. 2). Trotz der stark abweichenden Kurvenverläufe erwiesen sich die beiden Präparate als bioäquivalent, da die Werte für AUC0–∞ und Cmax die vorgegebenen Bioäquivalenzkriterien erfüllten. Über den gesamten gemessenen Zeitraum ist die Bioverfügbarkeit bei beiden Präparaten also vergleichbar. Betrachtet man jedoch nur den Zeitraum bis zu vier Stunden nach der Einnahme, lassen sich deutliche Unterschiede erkennen. In diesem Zeitraum zeigt Medikinet® retard eine deutlich höhere mittlere AUC0–4 als Ritalin® LA (44,9 ± 14,77 ng × h/ml vs. 27,6 ± 8,89 ng × h/ml). Auch die mittlere Cmax(0–4) ist bei Medikinet® retard höher (16,5 ± 4,62 ng/ml vs. 10,0 ± 3,51 ng/ml). Im Gegensatz dazu ist die AUC im Zeitraum von vier bis zehn Stunden nach Einnahme (AUC4–10) bei Ritalin® LA deutlich höher als bei Medikinet® retard (57,1 ± 14,36 ng × h/ml vs. 49,3 ± 18,47 ng × h/ml).
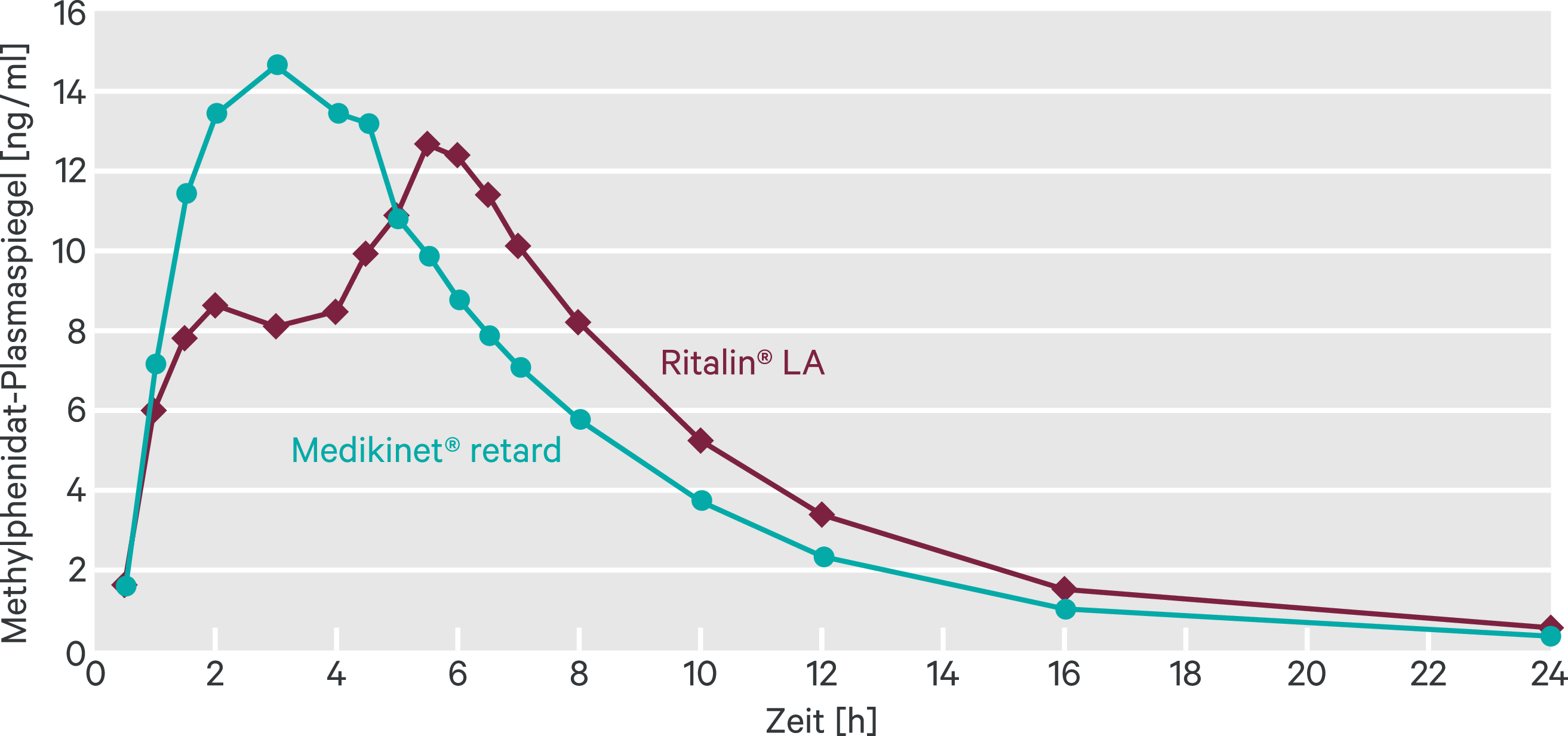
Abb. 2. Mittlere Methylphenidat-Plasmakonzentrationen nach Gabe einer 40-mg-Einzeldosis von Medikinet® retard oder Ritalin® LA im nüchternen Zustand (adaptiert nach [19])
In einer weiteren Cross-over-Studie wurde die Bioäquivalenz von Medikinet® retard 20 mg und Ritalin® LA 20 mg bei 24 Jungen (im Alter von 8 bis 14 Jahren) mit ADHS untersucht [14]. Beide Formulierungen wurden nach einem standardisierten Frühstück verabreicht. Die Methylphenidat-Konzentrationen im Serum wurden über einen Zeitraum von acht Stunden gemessen. Nach Gabe von Medikinet® retard wurden kontinuierlich höhere mittlere Serumkonzentrationen als nach Gabe von Ritalin® LA beobachtet (Abb. 3). Die mittlere Cmax nach Verabreichung von Medikinet® retard betrug 22,6 ± 9,3 ng/ml, während die entsprechende Cmax für Ritalin® LA nur 18,3 ± 8,7 ng/ml betrug. Medikinet® retard zeigte im Vergleich zu Ritalin® LA ebenfalls eine höhere AUC für den Zeitraum von 0 bis 8 Stunden (AUC(0–8)) (111,4 ± 45,8 ng × ml/h vs. 93,1 ± 57,2 ng × ml/h). Die beiden Präparate waren nicht bioäquivalent. Diese Ergebnisse zeigen eindeutig, dass die Bioverfügbarkeit von Medikinet® retard 20 mg höher ist als die von Ritalin® LA 20 mg.
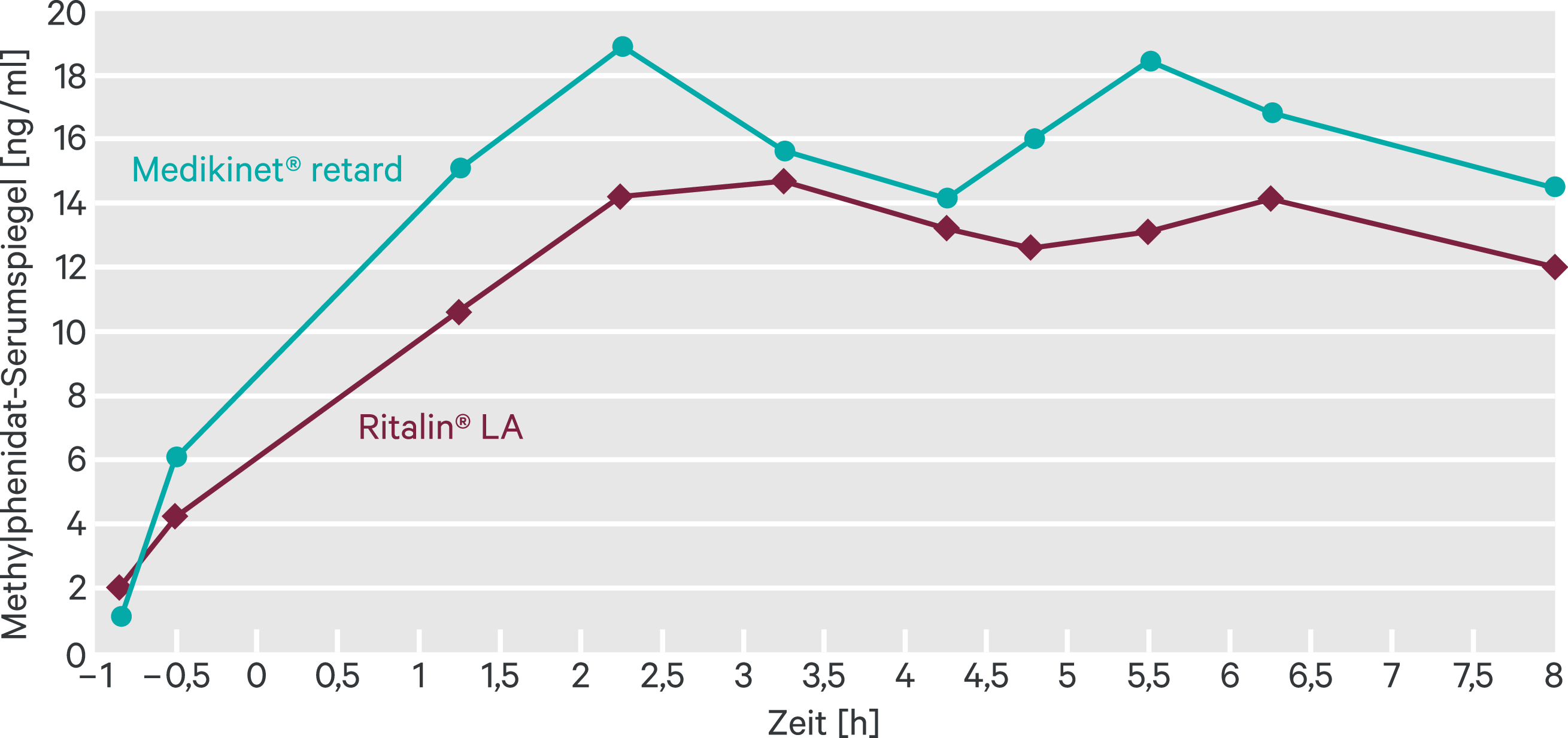
Abb. 3. Mittlere Methylphenidat-Serumkonzentrationen nach Gabe einer Einzeldosis von Medikinet® retard 20 mg und Ritalin® LA 20 mg im nicht-nüchternen Zustand (adaptiert nach [14])
Medikinet® retard vs. Equasym® Retard
Die Bioverfügbarkeit einer Einzeldosis von Medikinet® retard 20 mg und Equasym® Retard 20 mg wurde in einer Cross-over-Studie bei gesunden Erwachsenen verglichen [37]. Beide Formulierungen wurden mit einem leichten Frühstück verabreicht. Die wichtigsten pharmakokinetischen Parameter waren AUC0–t und Cmax. Beide Formulierungen zeigten ein ähnliches Absorptions- und Eliminationsmuster, wobei der erste Peak bei Equasym® Retard weniger stark ausgeprägt war (Abb. 4). Insgesamt wurden bei Medikinet® retard höhere Plasmaspiegel erreicht.
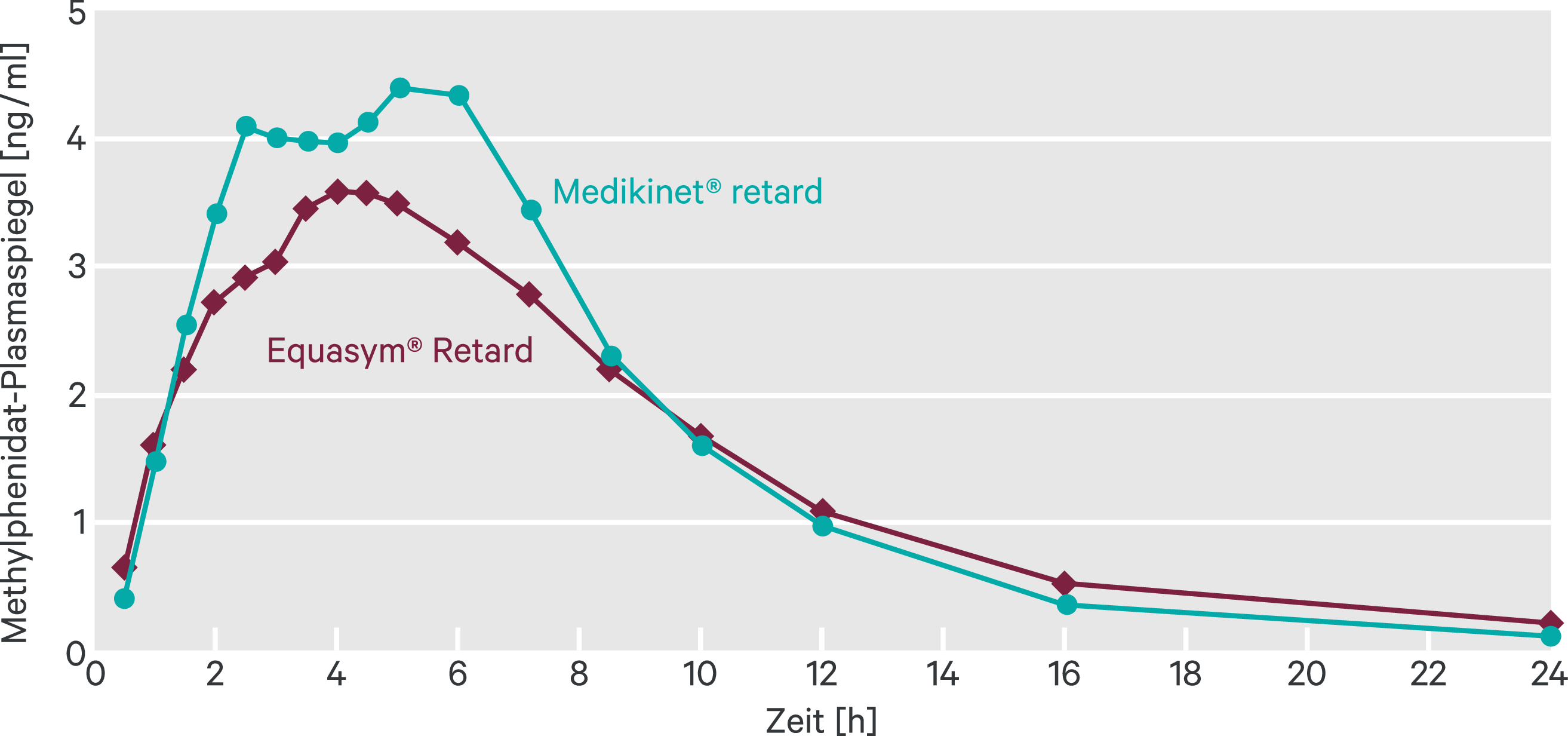
Abb. 4. Mittlere Methylphenidat-Plasmakonzentrationen nach Gabe einer 20-mg-Einzeldosis von Medikinet® retard oder Equasym® Retard im nicht-nüchternen Zustand (adaptiert nach [37])
Die beiden Formulierungen waren nicht bioäquivalent; die Bioäquivalenzkriterien wurden für AUC0–t, nicht aber für Cmax erfüllt. Insbesondere konnte keine Bioäquivalenz innerhalb der ersten vier Stunden nachgewiesen werden, da sowohl AUC0–4 als auch Cmax(0–4) bei Medikinet® retard deutlich höher waren als bei Equasym® Retard. Für Cmax(4–t) wurde ebenfalls keine Bioäquivalenz nachgewiesen.
Concerta® vs. Ritalin® LA
Die relative Bioverfügbarkeit von Ritalin® LA 20 mg und Concerta® 18 mg wurde in einer Cross-over-Studie bei 19 Erwachsenen im nüchternen Zustand untersucht [24]. Ritalin® LA erzeugte ein biphasisches Freisetzungsprofil mit zwei Cmax-Peaks, während die Plasmakonzentration bei Concerta® zunächst eine niedrige Plateauphase durchlief und nach etwa sechs Stunden auf ein Maximum stieg (Abb. 5). Die beiden Formulierungen erzeugten eine vergleichbare Gesamtexposition (AUC0–∞), Ritalin® LA zeigte jedoch eine schnellere Absorption mit höheren Spitzenplasmakonzentrationen. So erreichte Ritalin® LA innerhalb der ersten vier Stunden nach Einnahme etwa doppelt so hohe Werte für Cmax (7,0 µg/l vs. 3,4 µg/l; p < 0,001) und AUC0–4 (18,5 μg × h/l vs. 9,3 μg × h/l; p < 0,001) als Concerta®. Auch der zweite Cmax-Peak war bei Ritalin® LA deutlich höher als bei Concerta®. Daher sind die beiden Präparate nicht bioäquivalent.
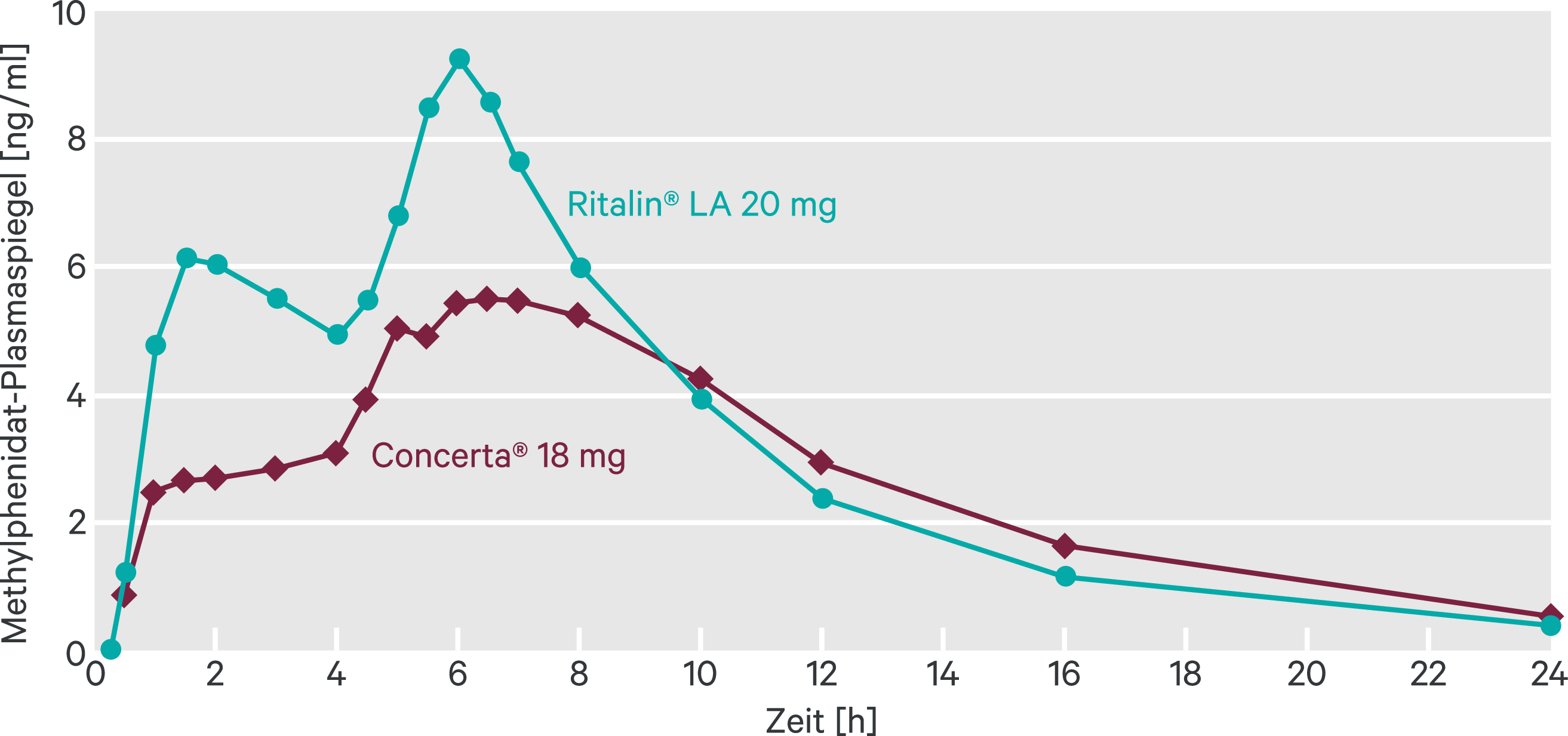
Abb. 5. Mittlere Methylphenidat-Plasmakonzentrationennach Gabe von Ritalin® LA20 mg und Concerta® 18 mg im nüchternenZustand (adaptiert nach [24])
Concerta® vs. Equasym® Retard
Die Bioverfügbarkeit von Concerta® und Equasym® Retard wurde in zwei Cross-over-Studien bei Erwachsenen untersucht [17]. Beide Präparate wurden als Einzeldosis im nüchternen Zustand gegeben. Die erste Studie untersuchte die Bioäquivalenz von 20 mg Equasym® Retard und 18 mg Concerta®. Die zweite Studie untersuchte die Bioäquivalenz von 40 mg Equasym® Retard, 36 mg Concerta®, 60 mg Equasym® Retard und 54 mg Concerta®. Beide Formulierungen zeigten unabhängig von der Dosierung ein biphasisches Freisetzungsprofil mit zwei Cmax-Peaks (Cmax-1 und Cmax-2) (Abb. 6). Die Formulierungen zeigten eine vergleichbare Gesamtexposition (AUC0–last und AUC0–∞). Allerdings gab es Unterschiede im zeitlichen Verlauf der Exposition und der Plasmaspiegel. Equasym® Retard erzeugte im Vergleich zu Concerta® eine höhere Exposition innerhalb der ersten sechs Stunden (AUC0–4 und AUC0–6), ein höheres Cmax-1 und höhere Plasmaspiegel eineinhalb, drei und vier Stunden nach Einnahme. Concerta® wiederum zeigte acht, zehn und zwölf Stunden nach Einnahme höhere Plasmaspiegel als Equasym® Retard. Eine Analyse der dosisnormalisierten pharmakokinetischen Parameter ergab ähnliche Resultate. Insgesamt belegen die Ergebnisse, dass die beiden Formulierungen nicht bioäquivalent sind.
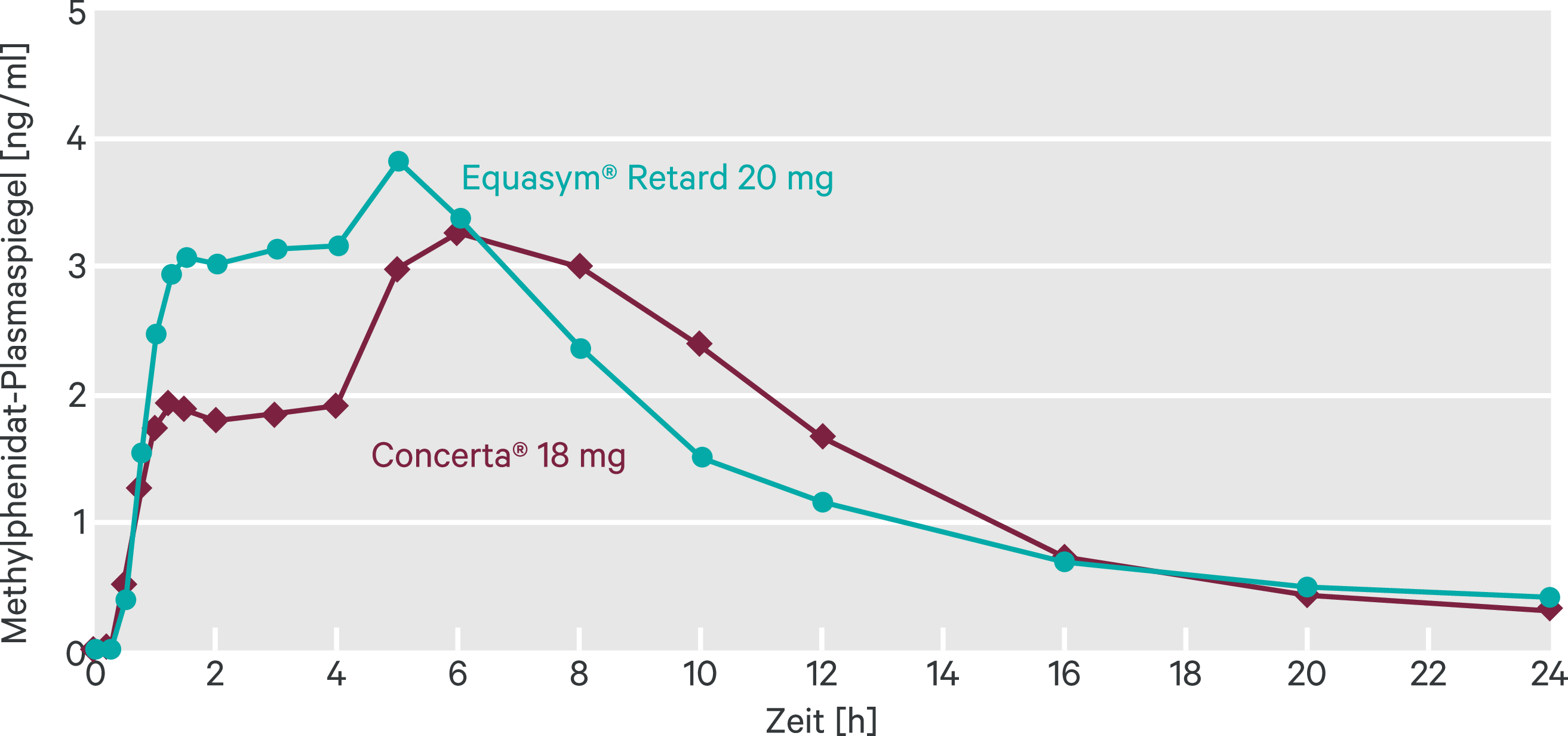
Abb. 6. Mittlere Methylphenidat-Plasmakonzentrationen nach Gabe von Equasym® Retard 20 mg und Concerta® 18 mg im nicht-nüchternen Zustand (adaptiert nach [17]). Die Gabe von 40 mg Equasym® Retard und 36 mg Concerta® bzw. 60 mg Equasym® Retard und 54 mg Concerta® lieferte ähnliche Ergebnisse.
Dosierungsintervall
Bei Kindern werden alle Präparate gemäß den entsprechenden Fachinformationen einmal täglich morgens verabreicht [21, 26, 29, 38]. Bei Medikinet® retard/adult und Ritalin® Adult unterscheiden sich jedoch die empfohlenen Dosierungsintervalle für erwachsene Patienten. Ritalin® Adult sollte laut Fachinformation nur einmal täglich in der Regel morgens eingenommen werden [28]. Im Gegensatz dazu sollte bei Medikinet® retard/adult die Gesamtdosis (Tagesdosis) bei Erwachsenen auf zwei Einnahmen morgens und mittags verteilt werden [25, 26]. Dies hat den Vorteil, dass die Wirkdauer individuell auf bis zu 16 Stunden verlängert werden kann.
Einnahme mit oder ohne Nahrung
Aufgrund der unterschiedlichen galenischen Eigenschaften der Präparate gibt es Unterschiede beim Einfluss von Nahrungsmitteln auf die Bioverfügbarkeit, weshalb sich die Präparate auch hinsichtlich der Empfehlungen zur Einnahme mit oder ohne Nahrung unterscheiden (Tab. 1).
Die pharmakokinetischen Profile von Ritalin® LA und Concerta® sind nach Einnahme im nüchternen oder nicht-nüchternen Zustand vergleichbar, sodass diese Präparate mit oder ohne Nahrung eingenommen werden können [19, 21, 27, 29].
Medikinet® retard sollte mit oder nach dem Frühstück (bzw. bei Erwachsenen mit oder nach einer Mahlzeit morgens und mittags) eingenommen werden, um den Retardierungseffekt zu gewährleisten [26]. Die Hartgelatinekapseln enthalten 50 % schnell freisetzende und 50 % verzögert freisetzende Pellets. Die verzögerte Freisetzung wird durch eine magensaftresistente Beschichtung der Pellets erreicht, die sich erst ab einem pH-Wert von > 5,5 auflöst und somit den Wirkstoff zeitlich verzögert im Dünndarm freisetzt [16]. Durch Nahrung wird der Eintritt der Pellets in den Dünndarm verzögert. Die Einnahme im nüchternen Zustand führt zu einer geringeren Gesamtexposition und einer Abschwächung des Retardierungseffekts [19].
Equasym® Retard sollte laut Fachinformation vor dem Frühstück eingenommen werden. Die Einnahme zusammen mit einer fettreichen Mahlzeit erhöht die Gesamtexposition (AUC) um etwa 17 % und die Cmax um etwa 30 % und verzögert die Resorption (tmax) um ungefähr eine Stunde [38].
Es ist zu beachten, dass Medikinet® retard/adult mit bzw. nach dem Frühstück verabreicht wird, Equasym® Retard hingegen vor dem Frühstück.
Erleichterte Einnahme durch Öffnen der Kapseln
Schwierigkeiten beim Schlucken von festen oralen Darreichungsformen sind ein häufiges Problem bei pädiatrischen, aber auch erwachsenen Patienten und können mit einer verminderten Therapieadhärenz einhergehen. Eine Umfrage unter 304 Eltern ergab, dass mehr als 50 % der Kinder und Jugendlichen nicht in der Lage sind, eine Tablette in Standardgröße oder eine kleine Kapsel zu schlucken [32]. Zudem haben etwa 37 % der erwachsenen Patienten Schwierigkeiten beim Schlucken von Kapseln oder Tabletten [36].
Concerta®-Tabletten müssen als Ganzes geschluckt werden und dürfen nicht gekaut, geteilt oder zerkleinert werden. Daher sollte Concerta® normalerweise nicht verabreicht werden bei Patienten mit Dysphagie oder bei Patienten, die deutliche Schwierigkeiten beim Schlucken von Tabletten haben [21]. Bei Medikinet® retard, Ritalin® LA und Equasym® Retard hingegen besteht die Möglichkeit, die Hartgelatinekapseln zu öffnen und den Kapselinhalt auf eine kleine Menge weicher Nahrung zu verteilen [26, 29, 38]. Die Bioverfügbarkeit dieser Produkte wird dadurch nicht beeinflusst [13, 23, 31]. Um die Wirksamkeit und Dosiergenauigkeit zu gewährleisten, muss der gesamte Kapselinhalt unverzüglich, ohne zu kauen, geschluckt werden [26, 29, 38].
Bei Ritalin® LA kann jegliche breiige Speise verwendet werden (z. B. Apfelmus), bei Equasym® Retard kann Apfelmus oder Brei verwendet werden. Es ist zu beachten, dass bei Medikinet® retard Apfelmus oder Joghurt verwendet werden sollte. Dies wird durch die galenischen Eigenschaften des Produkts bedingt. Da die verzögert freisetzenden (magensaftresistenten) Pellets sich ab einem pH-Wert von > 5,5 auflösen, könnte bei einer Einnahme der Pellets mit Nahrungsmitteln mit höherem pH-Wert das Freisetzungsprofil negativ beeinflusst werden.
Austausch in der Apotheke und damit verbundene Risiken für den Patienten
Bei der Verschreibung von Methylphenidat-Retardpräparaten ist zu beachten, dass es aufgrund von Rabattverträgen in der Apotheke zu einem Austausch gegen wirkstoffgleiche Generika kommen kann, wodurch der Therapieerfolg gefährdet werden könnte.
Bei einer chronischen Erkrankung wie ADHS ist eine hohe Adhärenz bei der medikamentösen Behandlung für den Therapieerfolg von hoher Bedeutung [10]. Mangelnde Adhärenz ist ein häufiges Problem bei ADHS-Patienten und ist mit einer verminderten Wirksamkeit der Therapie assoziiert [10, 15, 22, 35]. Ein Wechsel von einem Präparat auf ein anderes kann bei Patienten zu Verunsicherungen führen, wenn sich die Präparate beispielsweise in Größe, Form oder Farbe unterscheiden, und somit die Therapieadhärenz gefährden. Ebenso könnten die Patienten Abweichungen vom gewohnten Wirksamkeitsprofil oder neue ungewohnte Nebenwirkungen bemerken. So wurde beispielsweise in einigen Studien an ADHS-Patienten gezeigt, dass einige Concerta®-Generika im Vergleich zum Originalpräparat mit einer verminderten Wirksamkeit und Verträglichkeit assoziiert sind [11, 30, 42]. Dies kann ebenfalls die Therapieadhärenz beeinträchtigen und somit die Wirksamkeit und Arzneimitteltherapiesicherheit gefährden. Vor allem ein Austausch eines verschriebenen Arzneimittels gegen das Generikum eines anderen Präparats – was bei Präparaten mit gleichem Verhältnis von schnell zu verzögert freigesetztem Methylphenidat möglich ist, also bei Medikinet® retard und Ritalin® LA (beide 50 : 50) – könnte aufgrund der fehlenden Bioäquivalenz der Präparate problematisch sein.
In der klinischen Praxis kann der behandelnde Arzt durch Ankreuzen des „Aut-idem“-Felds auf dem Rezept eine automatische Substitution in der Apotheke ausschließen und damit die Therapiehoheit absichern.
Fazit für die Praxis
Die medikamentöse Behandlung der ADHS sollte auf die individuellen Bedürfnisse und Präferenzen des Patienten abgestimmt sein. Daher sollte der behandelnde Arzt mit den spezifischen Eigenschaften der verfügbaren Methylphenidat-Retardpräparate genau vertraut sein.
Aufgrund der unterschiedlichen Galenik und Zusammensetzung aus schnell und verzögert freisetzendem Methylphenidat haben die Präparate unterschiedliche Bioverfügbarkeiten und erzeugen spezifische Freisetzungsprofile. In mehreren pharmakokinetischen Vergleichsstudien wurde gezeigt, dass zwischen verschiedenen Präparaten keine Bioäquivalenz besteht. Zudem gibt es teilweise Unterschiede hinsichtlich der Einnahmeintervalle und -bedingungen (Einnahme mit oder ohne Nahrung, Möglichkeit zum Öffnen der Kapseln).
Bei der Wahl des Präparats sollten die individuellen Bedürfnisse des Patienten hinsichtlich der Anforderungen im Tagesverlauf berücksichtigt werden. Aufgrund der unterschiedlichen Freisetzungsprofile unterscheiden sich die Wirksamkeitsprofile im Tagesverlauf. Die unterschiedlichen Freisetzungsmuster könnten auch zu unterschiedlichen Nebenwirkungsspektren führen. Auch die Zusammensetzung der Präparate (Hilfsstoffe) könnte einen Einfluss auf das jeweilige Nebenwirkungsspektrum haben. Andere Aspekte wie Schluckbeschwerden oder Präferenzen hinsichtlich der Einnahme mit oder ohne Frühstück sollten bei der Wahl des Präparats auch berücksichtigt werden. Im Falle einer Umstellung auf ein anderes Präparat muss möglicherweise die Dosis angepasst werden, da es sonst zu einer Über- oder Unterdosierung kommen kann. Das Ansprechen auf Methylphenidat ist, von Patient zu Patient, sehr unterschiedlich und erfordert eine individuelle Dosisfindungsphase.
Bei der Verschreibung von langwirksamen Methylphenidat-haltigen Arzneimitteln sollte generell beachtet werden, dass in der Apotheke ein automatischer Austausch gegen ein Generikum bzw. ein vermeintliches Generikum (siehe Beispiel der 50 : 50 freisetzenden Präparate) erfolgen kann, wodurch die Therapieadhärenz und somit der Therapieerfolg der Patienten beeinträchtigt werden könnten, ohne dass es dem behandelnden Arzt bewusst ist. Um aus ärztlicher Sicht weiterhin die Therapiehoheit innezuhaben, kann dies durch Ankreuzen des „Aut-idem“-Felds auf dem Rezept verhindert und die Therapieadhärenz der Patienten gestärkt werden.
Danksagung
Für redaktionelle Unterstützung bedanke ich mich bei Dr. Michaela Ruhmann, MEDICE Arzneimittel Pütter GmbH & Co. KG.
Interessenkonflikterklärung
Dr. Henrik Uebel-von Sandersleben hat Honorare für Vortragstätigkeiten von MEDICE Arzneimittel Pütter GmbH Co. KG und für das ADHS Digital Science & Advisory Board von eyelevel GmbH erhalten.
Literatur
1. American Psychiatric Association (Hrsg.). Diagnostic and Statistical Manual of Mental Disorders. 5th edition. Washington, DC: American Psychiatric Association, 2013.
2. Bachmann CJ, Philipsen A, Hoffmann F. ADHD in Germany: trends in diagnosis and pharmacotherapy. Dtsch Arztebl Int 2017;114:141–8.
3. Bagwell CL, Molina BS, Pelham WE, Jr., Hoza B. Attention-deficit hyperactivity disorder and problems in peer relations: predictions from childhood to adolescence. J Am Acad Child Adolesc Psychiatry 2001;40:1285–92.
4. Banaschewski T, Coghill D, Santosh P, Zuddas A, et al. Long-acting medications for the hyperkinetic disorders. A systematic review and European treatment guideline. Eur Child Adolesc Psychiatry 2006;15:476–95.
5. Brunkhorst-Kanaan N, Libutzki B, Reif A, Larsson H, et al. ADHD and accidents over the life span – A systematic review. Neurosci Biobehav Rev 2021;125:582–91.
6. Coghill D, Banaschewski T, Zuddas A, Pelaz A, et al. Long-acting methylphenidate formulations in the treatment of attention-deficit/hyperactivity disorder: a systematic review of head-to-head studies. BMC Psychiatry 2013;13:237.
7. Committee for Medicinal Products for Human Use (CHMP). Guideline on the Investigation of Bioequivalence (CPMP/EWP/QWP/1401/98 Rev. 1/ Corr **). London, European Medicines Agency (EMA). http://www.ema.europa.eu/docs/en_GB/document_library/Scientific_guideline/2010/01/WC500070039.pdf (Zugriff am 31.05.2022).
8. Connor DF, Steingard RJ. New formulations of stimulants for attention-deficit hyperactivity disorder: therapeutic potential. CNS Drugs 2004;18:1011–30.
9. Cortese S, Adamo N, Del Giovane C, Mohr-Jensen C, et al. Comparative efficacy and tolerability of medications for attention-deficit hyperactivity disorder in children, adolescents, and adults: a systematic review and network meta-analysis. Lancet Psychiatry 2018;5:727–38.
10. DGKJP, DGPPN, DGSPJ. Langfassung der interdisziplinären evidenz- und konsensbasierten (S3) Leitlinie „Aufmerksamkeitsdefizit-/Hyperaktivitätsstörung (ADHS) im Kindes-, Jugend- und Erwachsenenalter“. Registernummer 028–045. https://www.awmf.org/leitlinien/detail/ll/028-045.html (Zugriff am 31.05.2022).
11. Fallu A, Dabouz F, Furtado M, Anand L, et al. A randomized, double-blind, cross-over, phase IV trial of oros-methylphenidate (CONCERTA®) and generic novo-methylphenidate ER-C (NOVO-generic). Ther Adv Psychopharmacol 2016;6:237–51.
12. Faraone SV, Spencer T, Aleardi M, Pagano C, et al. Meta-analysis of the efficacy of methylphenidate for treating adult attention-deficit/hyperactivity disorder. J Clin Psychopharmacol 2004;24:24–9.
13. Fischer R, Schutz H, Grossmann M, Leis HJ, et al. Bioequivalence of a methylphenidate hydrochloride extended-release preparation: comparison of an intact capsule and an opened capsule sprinkled on applesauce. Int J Clin Pharmacol Ther 2006;44:135–41.
14. Fleischhaker C, Hennighausen K, Schneider-Momm K, Schulz E. A single-center, single-blind, randomized, oral dose cross-over study in prepuberal boys with ADHD to investigate efficacy and bioequivalence of 20 mg Ritalin LA compared to 20 mg Medikinet retard after treatment with o.d. doses over 7 days each. Poster #14255. American Academy of Child & Adolescent Psychiatry (AACAP) 57th Annual Meeting, New York, October 26–31, 2010.
15. Gajria K, Lu M, Sikirica V, Greven P, et al. Adherence, persistence, and medication discontinuation in patients with attention-deficit/hyperactivity disorder – a systematic literature review. Neuropsychiatr Dis Treat 2014;10:1543–69.
16. Garcia-Garcia P, Lopez-Munoz F, Molina JD, Fischer R, et al. Methylphenidate extended-release capsules: a new formulation for attention-deficit hyperactivity disorder. Front Drug Des Discovery 2009;4:228–46.
17. Gonzalez MA, Pentikis HS, Anderl N, Benedict MF, et al. Methylphenidate bioavailability from two extended-release formulations. Int J Clin Pharmacol Ther 2002;40:175–84.
18. Greenhill LL, Swanson JM, Vitiello B, Davies M, et al. Impairment and deportment responses to different methylphenidate doses in children with ADHD: the MTA titration trial. J Am Acad Child Adolesc Psychiatry 2001;40:180–7.
19. Haessler F, Tracik F, Dietrich H, Stammer H, Klatt J. A pharmacokinetic study of two modified-release methylphenidate formulations under different food conditions in healthy volunteers. Int J Clin Pharmacol Ther 2008;46:466–76.
20. Harpin V, Mazzone L, Raynaud JP, Kahle J, et al. Long-term outcomes of ADHD: a systematic review of self-esteem and social function. J Atten Disord 2016;20:295–305.
21. JANSSEN-CILAG. Fachinformation Concerta® 18/27/36/54 mg Retardtabletten. Stand: August 2020.
22. Kooij JJ, Rosler M, Philipsen A, Wachter S, et al. Predictors and impact of non-adherence in adults with attention-deficit/hyperactivity disorder receiving OROS methylphenidate: results from a randomized, placebo-controlled trial. BMC Psychiatry 2013;13:36.
23. Lee L, Kepple J, Wang Y, Freestone S, et al. Bioavailability of modified-release methylphenidate: influence of high-fat breakfast when administered intact and when capsule content sprinkled on applesauce. Biopharm Drug Dispos 2003;24:233–43.
24. Markowitz JS, Straughn AB, Patrick KS, DeVane CL, et al. Pharmacokinetics of methylphenidate after oral administration of two modified-release formulations in healthy adults. Clin Pharmacokinet 2003;42:393–401.
25. MEDICE. Fachinformation Medikinet adult 5/10/20/30/40/50/60 mg. Stand: August 2021.
26. MEDICE. Fachinformation Medikinet retard 5/10/20/30/40/50/60 mg. Stand: November 2021.
27. Modi NB, Wang B, Hu WT, Gupta SK. Effect of food on the pharmacokinetics of osmotic controlled-release methylphenidate HCl in healthy subjects. Biopharm Drug Dispos 2000;21:23–31.
28. Novartis Pharma. Fachinformation Ritalin® Adult 10/20/30/40 mg. Stand: September 2020.
29. Novartis Pharma. Fachinformation Ritalin® LA 10/20/30/40 mg. Stand: September 2020.
30. Park-Wyllie L, van Stralen J, Castillon G, Sherman SE, et al. Differences in adverse event reporting rates of therapeutic failure between two once-daily extended-release methylphenidate medications in Canada: analysis of spontaneous adverse event reporting databases. Clin Ther 2017;39:2006–23.
31. Pentikis HS, Simmons RD, Benedict MF, Hatch SJ. Methylphenidate bioavailability in adults when an extended-release multiparticulate formulation is administered sprinkled on food or as an intact capsule. J Am Acad Child Adolesc Psychiatry 2002;41:443–9.
32. Polaha J, Dalton WT, 3rd, Lancaster BM. Parental report of medication acceptance among youth: implications for everyday practice. South Med J 2008;101:1106–12.
33. Pratt TC, Cullen FT, Blevins KR, Daigle L, et al. The relationship of attention deficit hyperactivity disorder to crime and delinquency: a meta-analysis. Int J Police Sci Manag 2016;4:344–60.
34. Reale L, Bartoli B, Cartabia M, Zanetti M, et al. Comorbidity prevalence and treatment outcome in children and adolescents with ADHD. Eur Child Adolesc Psychiatry 2017;26:1443–57.
35. Safren SA, Duran P, Yovel I, Perlman CA, et al. Medication adherence in psychopharmacologically treated adults with ADHD. J Atten Disord 2007;10:257–60.
36. Schiele JT, Quinzler R, Klimm HD, Pruszydlo MG, et al. Difficulties swallowing solid oral dosage forms in a general practice population: prevalence, causes, and relationship to dosage forms. Eur J Clin Pharmacol 2013;69:937–48.
37. Schutz H, Fischer R, Grossmann M, Mazur D, et al. Lack of bioequivalence between two methylphenidate extended modified release formulations in healthy volunteers. Int J Clin Pharmacol Ther 2009;47:761–9.
38. Shire Pharmaceuticals Ireland Limited. Fachinformation Equasym® Retard 10/20/30/40/50 mg Hartkapseln mit veränderter Wirkstofffreisetzung. Stand: September 2021.
39. Sibley MH, Mitchell JT, Becker SP. Method of adult diagnosis influences estimated persistence of childhood ADHD: a systematic review of longitudinal studies. Lancet Psychiatry 2016;3:1157–65.
40. Thomas R, Sanders S, Doust J, Beller E, et al. Prevalence of attention-deficit/hyperactivity disorder: a systematic review and meta-analysis. Pediatrics 2015;135:e994–1001.
41. Trofimiuk M, Wasilewska K, Winnicka K. How to modify drug release in paediatric dosage forms? Novel technologies and modern approaches with regard to children’s population. Int J Mol Sci 2019;20:3200.
42. van Stralen JP. The clinical impact of switching attention deficit hyperactivity disorder patients from OROS®-MPH to Novo-MPH ER-C®: a paediatric practice review. Paediatr Child Health 2013;18:70–3.
43. Wolraich ML, Doffing MA. Pharmacokinetic considerations in the treatment of attention-deficit hyperactivity disorder with methylphenidate. CNS Drugs 2004;18:243–50.
Dr. Henrik Uebel-von Sandersleben, Universitätsmedizin Göttingen, Klinik für Kinder- und Jugendpsychiatrie und Psychotherapie, Von-Siebold-Str. 5, 37075 Göttingen, E-Mail: huebel@gwdg.de
Individualized ADHD therapy with extended-release methylphenidate preparations
Methylphenidate is the gold standard (first-line therapy) in the pharmacological treatment of attention-deficit/hyperactivity disorder (ADHD). Several long-acting extended-release methylphenidate preparations are available on the German market: Medikinet® retard/adult, Ritalin® LA/Adult, Equasym® Retard and Concerta®, as well as several generics. Due to the different galenics and composition of immediate- and extended-release methylphenidate, the preparations have different bioavailabilities and produce specific release profiles. Therefore, bioequivalence between different preparations could not be shown in comparative pharmacokinetic studies. In addition, there are some differences with regard to the intake intervals and conditions (intake with or without food, possibility of opening the capsules). The treating physician should be thoroughly familiar with the specific characteristics of the available extended-release methylphenidate preparations and consider the individual needs and preferences of the patient when choosing the medication. This review article provides an overview of the specific properties of each preparation.
Key words: ADHD, methylphenidate, bioequivalence, substitution
Psychopharmakotherapie 2022; 29(04):138-145
