Axel Steiger, Kaiserslautern
Daridorexant (Handelsname Quviviq) ist ein neuartiges Schlafmittel, dessen Zulassung die Europäische Kommission nach entsprechender Empfehlung der European Medicines Agency (EMA) vom 24. Februar 2022 [19] am 29. April 2022 beschloss [17]. Bei Daridorexant handelt es sich um den ersten in der Europäischen Union (EU) zugelassenen dualen Orexin-Rezeptorantagonisten (DORA). Die präzise Indikation ist die Behandlung von Erwachsenen mit Schlafstörungen (Insomnie), deren Symptome seit mindestens drei Monaten anhalten und eine beträchtliche Auswirkung auf das Tagesgeschehen haben [18]. Vor der Europäischen Kommission hatte die US-amerikanische Zulassungsbehörde FDA Daridorexant am 7. Januar 2022 zugelassen [14]. Die von der FDA genannte Indikation ist weiter gefasst als in der EU: erwachsene Patienten mit Insomnie, charakterisiert durch Ein- und/oder Durchschlafstörungen [21]. Seit 2. Mai 2022 ist die Substanz in den USA erhältlich [25]. Dort sind schon seit 2014 bzw. 2019 zwei DORAs verfügbar, Suvorexant [13] und Lemborexant [16]. Der Hersteller plant, Daridorexant in den ersten EU-Ländern vor Jahresende auf den Markt zu bringen [26].
DORAs hemmen im Gehirn die Bindung der beiden Neuropeptide Orexin (auch Hypocretin genannt) A und B. Diese fördern den Wachzustand über die beiden Rezeptoren OX1R und OX2R [27]. Der Wirkungsmechanismus von DORAs unterscheidet sich damit deutlich von dem klassischer Schlafmittel, wie der Liganden des GABA-A-Rezeptors (Benzodiazepin-Hypnotika und Non-Benzodiazepin-Hypnotika oder Z-Substanzen). Orexin A und B werden in einer kleinen Gruppe von Neuronen des Hypothalamus gebildet [11, 37]. Die Aktivität dieser Neuronen ist während des Wachzustands am höchsten und ruht während des Schlafs [1]. Sie projizieren zu verschiedenen Populationen von Neuronen, die jeweils spezifische, den Wachzustand fördernde Neurotransmitter enthalten, nämlich Histamin, Noradrenalin, Serotonin, Dopamin und Acetylcholin (Übersicht: [35]). Durch Aktivierung dieser Populationen stabilisieren Orexine den Wachzustand [38]. Beim Krankheitsbild der Narkolepsie, das mit Schlafattacken am Tage einhergeht, liegt ein Orexin-Mangel vor [41]. DORAs hemmen gezielt über die Orexin-Rezeptoren diese den Wachzustand fördernden Neuronenverbände und wirken so schlafanstoßend [15]. Im Unterschied dazu bewirken Benzodiazepin- und Non-Benzodiazepin-Hypnotika eine weniger spezifische, weitreichendere Hemmung der Gehirnaktivität [35]. Diese Substanzen haben auch eine Reihe unerwünschter Wirkungen wie morgendlicher Überhang, Koordinationsstörungen, Stürze, Störungen von Gedächtnis und Koordination sowie die Risiken von Toleranzentwicklung und Abhängigkeit [7, 28, 49].
Die bisher eingeführten DORAs sind nicht frei von einer sedierenden Restaktivität am Morgen nach der Einnahme am Vortag [30]. Daridorexant (Abb. 1) wurde in einem Forschungsprogramm entwickelt, das einen wirksamen, dualen, hirngängigen Orexin-Rezeptorantagonisten zum Ziel hatte, dessen Wirkung bei optimaler Dosierung rasch eintritt, während der Nacht ausreichend lang anhält, aber wiederum kurz genug ist, um frei von morgendlichem Überhang zu sein [6]. Daridorexant wirkt an beiden Orexin-Rezeptoren antagonistisch und zeigt in vitro keine relevante Aktivität an über 130 anderen zentralen und peripheren Bindungsstellen, einschließlich von GABA-A-Rezeptoren [46].
Abb. 1. Strukturformel von Daridorexant
Nichtklinische Befunde zur Wirkung auf den Schlaf
Bei Ratten wurde die Wirkung verschiedener zu Beginn der nächtlichen Wachphase oral verabreichter Dosierungen von Daridorexant und Placebo auf den mit Elektroenzephalographie (EEG) registrierten Schlaf untersucht. Dosisabhängig wurde die Wachzeit vermindert, während REM(Rapid eye movement)- und Non-REM-Schlaf in physiologischen Proportionen anstiegen. Dies zeigt, dass unter der Substanz die normale Schlafarchitektur erhalten bleibt. Im Gegensatz dazu bewirkte Zolpidem im gleichen Experiment dosisabhängig eine Veränderung der Schlafarchitektur, indem Non-REM-Schlaf zunahm und neben dem Wachzustand auch der REM-Schlaf abnahm. Unter Daridorexant schliefen die Versuchstiere schneller ein [6]. Ähnliche Ergebnisse fanden sich bei Beagle-Hunden, deren Schlaf unter Daridorexant und Placebo mit Telemetrie untersucht wurde [6]. Der in diesen Untersuchungen gezeigte proportionale Anstieg von Non-REM- und REM-Schlaf ist eine Besonderheit der DORAs und grenzt diese von Benzodiazepin- und Non-Benzodiazepin-Hypnotika ab, die die Schlafarchitektur verändern, indem sie das Non-REM-Stadium 2 vermehren und REM-Schlaf vermindern [2, 5, 9, 24].
Untersuchungen an Ratten zeigten, dass die Schlafförderung durch Daridorexant von der Tageszeit, dem Schlafdruck und den Orexin-Spiegeln abhängt. Ratten sind in der Nacht aktiv und dann während 60 bis 70 % der Dunkelheit wach. Sie schlafen vor allem am Tag, wenn es hell ist. Besonders viel Schlaf findet sich unter Versuchsbedingungen in den ersten Stunden nach Anschalten einer Beleuchtung. Nach Gabe von Daridorexant zu Beginn der Lichtphase, dem Zeitraum, in dem der natürliche Schlaf dieser Tiere auftritt, blieb die Schlafdauer unverändert. Hingegen nahm die Schlafdauer zu, nachdem die Substanz zu Beginn der Dunkelphase verabreicht wurde, in der die Ratten normalerweise aktiv sind [35]. Eine getrennte Untersuchung von sechsstündigen Abschnitten des 24-Stunden-Tages zeigte, dass die höchsten Dosierungen von Doridorexant auch in der zweiten Hälfte der Dunkelphase die Schlafdauer verlängerten. Hingegen stellte sich eine solche Wirkung weder in der ersten noch in der zweiten Hälfte der Lichtphase ein [35]. Das Ausbleiben der Wirkung während der ersten sechs Stunden der Lichtphase wird durch die hohe Menge an natürlichem Schlaf in diesem Zeitraum erklärt. Die Wirkung von Daridoxant beruht offenbar auf einer Verminderung des Wachzustands und nicht auf einem Einfluss auf den Schlaf per se. Es wird angenommen, dass dem fehlenden Effekt der Substanz in der zweiten Hälfte der Lichtphase ihre eingeschränkte Wirksamkeit bei niedrigem Schlafdruck zugrunde liegt. Zugleich ist in diesem Zeitraum die Orexin-Konzentration im Liquor niedrig [24], entsprechend einer verminderten Aktivität der Orexin-Neurone während der vorangehenden Schlafperiode.
Die Latenz bis zum Auftreten von andauerndem Non-REM- und REM-Schlaf war nach Gabe von Daridorexant zu Beginn der Licht- wie auch der Dunkelperiode verkürzt [35]. Es wird diskutiert, dass in der Lichtperiode die experimentelle Prozedur bei der Verabreichung der Substanz die Orexin-Rezeptoren aktiviert, und dass diese Aktivierung wiederum durch die Substanz gehemmt wird, was zu schnellerem Einschlafen der Ratten führt [35]. Aufgrund dieser Befunde wird postuliert, dass ein Überhang am Morgen infolge von Restkonzentrationen von Daridorexant unwahrscheinlich ist [35]. Diese Sichtweise wird durch eine Studie an Rhesusaffen unterstützt, die am Abend einen anderen DORA (Codename DORA-22), Eszopiclon oder Diazepam erhielten. Obwohl am folgenden Morgen noch restliche Konzentrationen von DORA-22 im Plasma gemessen wurden, traten weder Schläfrigkeit noch Störungen von Gedächtnis und Aufmerksamkeit auf. Hingegen fand sich nach Gabe von Diazepam am Vortag residualer Schlaf am folgenden Morgen; sowohl nach Diazepam wie auch nach Eszopiclon traten kognitive Störungen am folgenden Tag auf [24].
Studien an Nagern und Hunden zeigten, dass die schlaffördernde Wirkung von Daridorexant, ähnlich wie natürlicher Schlaf, sofort und ohne eine Beeinträchtigung der Motorik überwunden werden kann. Eine Untersuchung an Ratten während der Lichtperiode ergab, dass schlaffördernde Dosen von Daridorexant, im Gegensatz zu solchen von Zolpidem, weder die Kraft der Muskulatur noch die Feinmotorik beeinträchtigen [35]. Weiter wurde gezeigt, dass die schlaffördernde Wirkung sofort reversibel ist. Hunden, die drei Stunden nach Verabreichung von Daridorexant schliefen, wurde Futter präsentiert. Daraufhin wachten sie sofort auf, bewegten sich und fraßen normal. Danach schliefen sie weiter. Es wurde auch geprüft, ob in dieser Situation eine Kataplexie-ähnliche Muskelschwäche auftritt. Kataplexien sind neben Schlafattacken ein weiteres Symptom der Narkolepsie, nämlich ein affektiver Tonusverlust, der bei einem Teil der Patienten mit dieser Erkrankung durch Emotionen wie Freude oder Wut ausgelöst wird. In Tiermodellen der Narkolepsie kann das Anbieten von Futter bei Hunden einen solchen Tonusverlust auslösen [44]. Eine Kataplexie-ähnliche Muskelschwäche wurde während des geschilderten Experiments durch Video-Aufnahmen und Elektromyographie nicht festgestellt [6].
Ähnlich zeigten Untersuchungen mit den DORAs Almorexant [8] und DORA-22 [8, 43, 44] an Mäusen, Hunden und Affen ein natürliches Aufwachen nach deutlichen Stimuli, das nicht mit Muskelschwäche oder kognitiven und psychomotorischen Störungen einherging. Im Gegensatz dazu war das Wecken von Affen, die Eszopiclon und Diazepam erhalten hatten, erschwert. Nach dem Aufwachen traten bei diesen Versuchstieren psychomotorische Störungen auf [44]. Aufgrund dieser Befunde wird diskutiert, dass Daridorexant selektiv die über Orexin vermittelte Weckreaktion hemmt, aber nicht andere Neurotransmitter, die zu einer Weckreaktion beitragen [34]. Im Gegensatz dazu stoßen Benzodiazepin- und Non-Benzodiazepin-Hypnotika Schlaf durch eine umfangreiche Hemmung des ZNS an. Daher ist unter diesen Substanzen die Schwelle für Weckungen erhöht [35].
Nichtklinische Befunde zur Wirkung auf Gedächtnis, Kognition und Fahrtauglichkeit
Eine Reihe von Experimenten zeigte, dass die Schlafförderung durch DORAs nicht mit Störungen von Kognition und Gedächtnis einhergeht. Ratten, die hohe Dosen von Almorexant oder einem anderen DORA, ACT-462 206, erhielten, zeigten keine Beeinträchtigung einer Reihe von Gedächtnisfunktionen [12, 31]. Bei Rhesusaffen wurden die Effekte von DORA-22, Eszopiclon, Zolpidem und Diazepam auf den Schlaf und auf zwei Paradigmen zur Untersuchung das Arbeitsgedächtnisses und der Aufmerksamkeit untersucht. Auch unter hohen Dosierungen beeinträchtigte DORA-22 Gedächtnis und Aufmerksamkeit nicht, während schlaffördernde und auch den Schlaf nicht beeinflussende niedrigere Dosierungen der Z-Substanzen und von Diazepam solche Störungen bewirkten. Aus diesen Ergebnissen wurde geschlossen, dass bei DORAs der Abstand zwischen Schlafförderung und unerwünschten kognitiven Wirkungen wesentlich größer als bei herkömmlichen Hypnotika ist [48]. Ähnliche Ergebnisse zeigte eine Studie an jungen gesunden männlichen und weiblichen Versuchspersonen, die in einer dunklen und Stimulus-armen Umgebung Placebo oder Einzeldosen von Almorexant oder Zolpidem erhielten. Beide Arzneimittel führten zu Schläfrigkeit. Die Versuchspersonen hatten die Aufgabe, wach zu bleiben. Komplexere Aufgaben für das verbale Gedächtnis und exekutive Funktionen waren unter Placebo und Almorexant nicht, aber unter Zolpidem deutlich gestört [33].
Die unterschiedlichen kognitiven Wirkungen von DORAs einerseits und Benzodiazepin- sowie Non-Benzodiazepin-Hypnotika anderseits werden mit den jeweiligen neuroanatomischen und funktionellen Grundlagen und Mechanismen erklärt. Orexin-Rezeptoren sind zwar im Gehirn weit verteilt, Orexin-Neurone finden sich jedoch nur in einem kleinen Gebiet, dessen Projektionen zu Hirnregionen, außer denen, die an der Schlaf-Wach-Regulation beteiligt sind, relativ diffus sind [36, 37]. Hingegen ist GABA der wichtigste inhibitorische Neurotransmitter im ZNS. Das GABAerge System ist nicht nur an der Kontrolle des Schlaf-Wach-Verhaltens, sondern auch an der Regulation zahlreicher weiterer physiologischer Funktionen beteiligt. GABA-A-Rezeptoren und GABAerge Bahnen finden sich auch in Gehirnregionen, die Aufmerksamkeit und Gedächtnis regulieren, nämlich Amygdala, Hippocampus und Kortex [22].
Der Effekt von Daridorexant auf die Fahrtauglichkeit gesunder Personen im Alter zwischen 50 und 79 Jahren wurde mithilfe eines Fahrsimulators am Morgen geprüft. Dies erfolgte neun Stunden nach einmaliger Einnahme und nach viermaliger Verabreichung von zwei Dosierungen, 50 mg und 100 mg, der doppelten der empfohlenen Dosis. Es fand sich eine signifikante Störung des Fahrverhaltens in der ersten Testung nach beiden Dosen im Vergleich zu Placebo. Nach vier Nächten fand sich kein signifikanter Effekt. Die Autoren stellen fest, dass Daridorexant simuliertes Fahren bei Personen ohne Insomnie nach initialer, aber nicht nach wiederholter Einnahme störte. Sie raten, dass die Betroffenen vor dem Autofahren gewarnt werden sollen, bis sie wissen, wie Daridorexant auf sie wirkt [32]. In der Produktinformation der FDA zu Daridorexant findet sich in Zusammenhang mit dieser Studie die Feststellung, dass sich zwar nach vier Nächten kein signifikanter Effekt der Behandlung auf die Fahrtauglichkeit fand, dass diese jedoch bei einzelnen Personen gestört war. Bei Einnahme des Arzneimittels solle daher vor einer möglichen Beeinträchtigung der Fahrtüchtigkeit am folgenden Morgen infolge individueller Unterschiede in der Empfindlichkeit gewarnt werden [21]. Die entsprechenden Warnhinweise aus der Produktinformation der EMA werden weiter unten berichtet.
Nichtklinische Befunde zu Rebound, Toleranzentwicklung und den Risiken von Missbrauch und Abhängigkeit
Die längerfristige Behandlung mit herkömmlichen Hypnotika geht oft mit einem allmählichen Wirkungsverlust, der Entwicklung von Toleranz einher. Weiter kann es beim Absetzen dieser Substanzen zu einer Rebound-Insomnie kommen. Um dies zu vermeiden, ist ein schrittweises Ausschleichen dieser Medikamente erforderlich [28]. Tierexperimente deuten darauf hin, dass bei der Behandlung mit Daridorexant kein Risiko für Toleranzentwicklung und Rebound-Insomnie besteht. Die schlaffördernde Wirkung von Almorexant blieb bei Verabreichung über 42 Tage ohne Toleranzentwicklung bestehen. Abruptes Absetzen der Substanz nach 42 Tagen führte nicht zu einem Rebound von Wachzustand [35]. Hingegen trat bei täglicher Gabe von Zolpidem über fünf Tage schon am zweiten Tag des Experiments Toleranz auf [35].
Für Benzodiazepin- und Non-Benzodiazepin-Hypnotika bestehen Risiken von Missbrauch und Abhängigkeit [39]. Auch für Suvorexant wurde ein Missbrauchspotenzial berichtet [40]. Bisher ergaben präklinische Studien keinen Hinweis auf solche Risiken für Daridorexant. Im Einzelnen fand sich kein Hinweis, dass Daridorexant in klinisch wirksamen Konzentrationen an für Missbrauch relevante ZNS-Strukturen bindet. Weiter wurde bei Ratten kein Hinweis auf Verstärkungseffekte gefunden, da experimentell keine intravenöse Selbstverabreichung hervorgerufen wurde. Schließlich traten nach dem Absetzen von chronisch verabreichtem Daridorexant bei Ratten keine Zeichen von Entzug und damit kein Hinweis auf körperliche Abhängigkeit auf [35].
Das Missbrauchspotenzial von Daridorexant wurde bei gesunden Versuchspersonen untersucht, die Freizeitkonsumenten von Sedativa sind. Diese verglichen auf einer visuellen Analogskala die Beliebtheit einer klinisch empfohlenen Dosis (50 mg) und erhöhter Dosierungen (100 mg und 150 mg) von Daridorexant mit erhöhten Dosen von Suvorexant (150 mg) und Zolpidem (30 mg) und mit Placebo. Die Beliebtheit von 50 mg Daridorexant war signifikant geringer als die von Suvorexant und Zolpidem. Ab 100 mg Daridorexant war das Ergebnis ähnlich zu dem für die beiden anderen Substanzen [47].
Pharmakokinetik
Nach Einnahme von 25 bis 50 mg Daridorexant werden bei gesunden Personen dosisabhängige messbare Plasmaspiegel erzielt. Das pharmakokinetische Profil ist nach Einzel- und Mehrfachdosierungen ähnlich; zu Akkumulation kommt es nicht. Die höchsten Plasmakonzentrationen werden ein bis zwei Stunden nach der Einnahme erreicht. Die Substanz wird innerhalb von ungefähr acht Stunden ausgeschieden. Es gibt keinen signifikanten Einfluss von Alter, Geschlecht, ethnischer Zugehörigkeit, Größe und einer leichten bis schweren, nicht dialysepflichtigen Nierenfunktionsstörung auf die Pharmakokinetik der Substanz [21].
Die empfohlene Dosis für Erwachsene beträgt 50 mg einmal pro Nacht, die innerhalb von 30 Minuten vor dem Zubettgehen eingenommen werden sollen. Je nach klinischer Einschätzung können einige Patienten mit 25 mg einmal pro Nacht behandelt werden [18]. Die FDA empfiehlt nach Einnahme einen Abstand von mindestens sieben Stunden bis zum geplanten Wecken [21]. Wenn die Einnahme unmittelbar nach einer großen Mahlzeit erfolgt, kann sich die Wirkung auf das Einschlafen reduzieren [18]. Die Behandlungsdauer sollte so kurz wie möglich sein. Die Zweckmäßigkeit einer Weiterbehandlung sollte innerhalb von drei Monaten und anschließend in regelmäßigen Abständen beurteilt werden [18]. In der Produktinformation der EMA wird festgestellt, dass klinische Daten für eine Behandlung von bis zu zwölf Monaten vorliegen [18]. Bisher wurden keine Daten über eine drei Monate überschreitende Behandlung mit Daridorexant publiziert.
Klinische Studien zur Wirksamkeit
Bisher wurden vier Studien zur klinischen Wirksamkeit und Sicherheit von Daridorexant bei Insomnie veröffentlicht.
Dauvilliers et al. [10] schlossen 359 erwachsene Patienten mit einem Alter bis zu 64 Jahren in eine Phase-II-Studie ein. Diese erhielten randomisiert oral über 30 Tage Placebo, 5, 10, 25 oder 50 mg Daridorexant oder 10 mg Zolpidem. Es fanden sich im Vergleich zu den Ausgangswerten vor Behandlung an den Tagen 1 und 2 dosisabhängig signifikante Verringerungen der Wachzeit nach Schlafbeginn und der Latenz bis zu andauerndem Schlaf. Diese Effekte blieben bis zu den Tagen 28 und 29 erhalten.
Die gleichen vier Dosierungen von Daridorexant wie in der zuvor genannten Studie und Placebo wurden in einer weiteren Phase-II-Studie randomisiert 58 Patienten beiderlei Geschlechts im Alter von 65 bis 85 Jahren während fünf Abschnitten verabreicht, die jeweils aus zwei Nächten mit Behandlung und einer anschließenden fünf bis zwölf Tage dauernden Auswaschphase bestanden. Im Bereich von 10 bis 50 mg der Prüfsubtanz wurden mithilfe von Polysomnographie dosisabhängig Verminderungen der Wachzeit nach Schlafbeginn und der Latenz bis zu andauerndem Schlaf gefunden [50].
Phase-III-Studien
Während die Wirksamkeit von DORAs bei Insomnie schon für die in den USA und anderen Ländern außerhalb Europas zugelassenen Arzneimittel Suvorexant und Lemborexant gezeigt wurde, wurde bisher ihre Wirkung auf Beeinträchtigungen am Tage nicht untersucht, obwohl Insomnie auch mit negativen Auswirkungen auf die Funktionsfähigkeit und das Befinden tagsüber einhergeht. Dieser Aspekt wurde, neben der Wirkung auf den Schlaf, erstmals in zwei multizentrischen, an 156 Prüfzentren in 17 Ländern durchgeführten doppelblinden Phase-III-Studien berücksichtigt, in die Patienten mit mäßiger bis schwerer Insomnie eingeschlossen wurden. Ein zusätzliches Einschlusskriterium war subjektiv gestörter Schlaf in mindestens drei Nächten pro Woche über mindestens drei Monate. Diese beiden Studien liegen den Zulassungen von Daridorexant durch die FDA und die Europäische Kommission zugrunde. Die Patienten erhielten randomisiert zwei Dosierungen von Daridorexant oder Placebo [30]. Bei Studie 1 (n = 930) wurden 25 mg und 50 mg, bei Studie 2 (n = 924) 10 mg und 25 mg der Prüfsubstanz mit Placebo verglichen. Daridorexant oder Placebo wurden während drei Monaten jeden Abend per os eingenommen. Polysomnographien (PSG) wurden während zwei konsekutiven Nächten während einer Placebo-Phase vor dem Beginn der aktiven Behandlung („Run-in-Phase“) sowie am Ende des ersten und des dritten Monats der Behandlung abgeleitet. Die Funktionsfähigkeit am Tage wurde täglich mit einem neu entwickelten Fragebogen erhoben, dem Insomnia Daytime Symptoms and Impacts Questionnaire (IDSIQ). Die Items dieser Skala umfassen drei Bereiche, die bei Insomnie häufig betroffen sind, nämlich Schläfrigkeit, Stimmung und Aufmerksamkeit/Kognition. Primäre Endpunkte waren die mit PSG gemessenen Veränderungen der Wachzeit nach Schlafbeginn und der Latenz bis zu andauerndem Schlaf zwischen dem Ausgangswert und am Ende des ersten und des dritten Monats. Sekundäre Endpunkte waren Veränderungen der subjektiv berichteten totalen Schlafzeit und eines Werts für Schläfrigkeit des IDSIQ-Fragebogens.
In der Studie 1 fanden sich unter 25 mg und unter 50 mg der Prüfsubstanz im Vergleich zu Placebo signifikant verminderte Werte der Wachzeit nach Schlafbeginn und der Latenz bis zum fortwährenden Schlaf sowie ein Ansteigen der totalen Schlafzeit (Abb. 2). Die mit IDSIQ erfragte Schläfrigkeit am Tag war unter 50 mg, aber nicht unter 25 mg Daridorexant nach einem und nach drei Monaten verringert. In Studie 2 fand sich unter 25 mg der Substanz am Ende des ersten und des dritten Monats eine Verringerung der mit PSG bestimmten Wachzeit nach Schlafbeginn und eine Zunahme der subjektiven totalen Schlafzeit, aber keine Veränderung der Latenz bis zu andauerndem Schlaf und der mit IDSIQ erhobenen Schläfrigkeit. Unter 10 mg der Prüfsubstanz wurden keine signifikanten Effekte gefunden. Die Ergebnisse waren konsistent für Studienteilnehmer, die jünger und älter als 65 Jahre waren, und für beide Geschlechter. Die mit visueller Analogskala erfasste Funktionsfähigkeit und Aufmerksamkeit tagsüber waren unter aktiver Medikation im Vergleich zu Placebo erhöht. Die Proportion zwischen den Schlafstadien blieb in allen Behandlungsarmen in Verlauf der Studie erhalten.
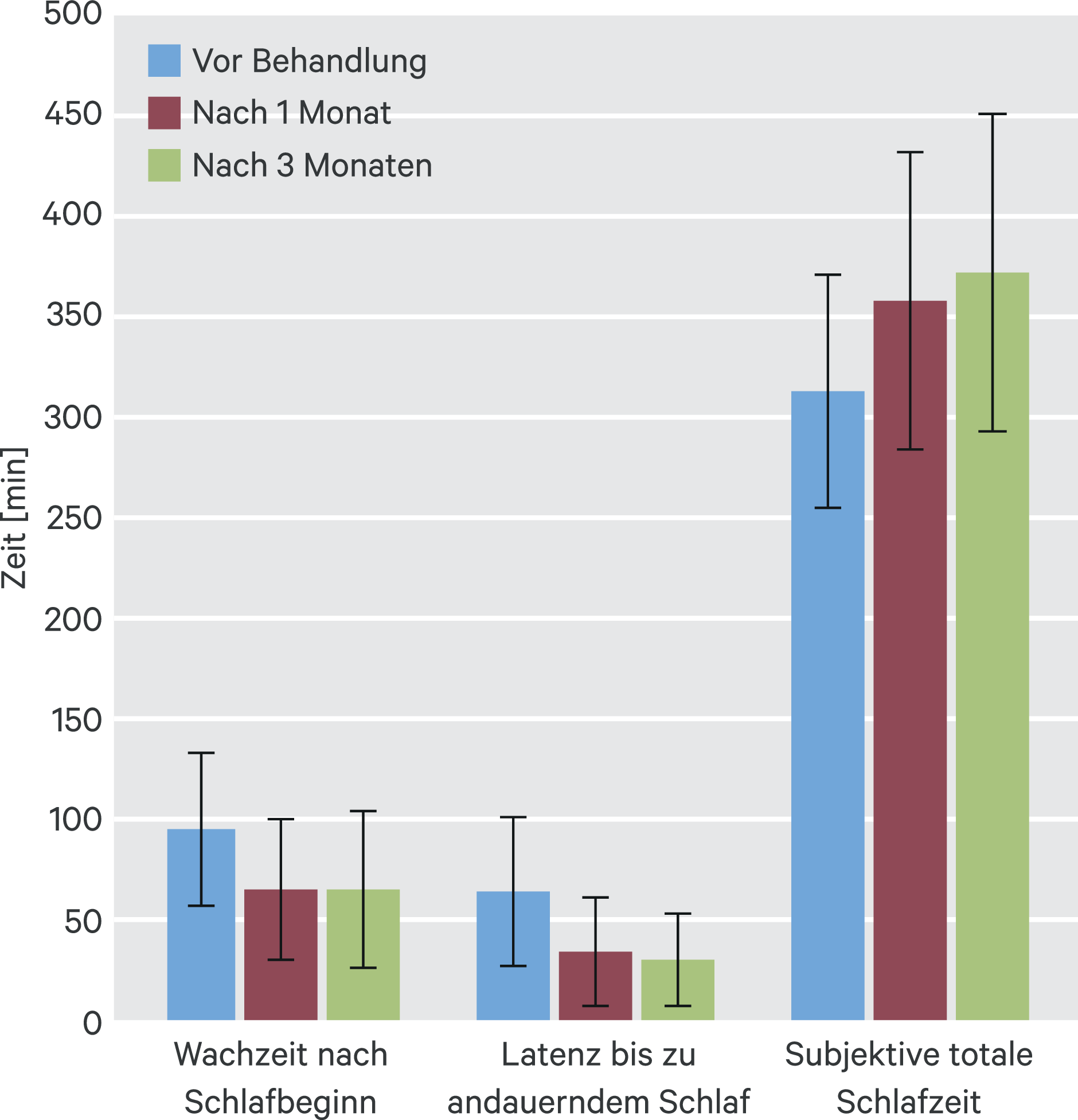
Abb. 2. Wirkung von 50 mg Daridorexant auf objektive und subjektive Schlafparameter in der Phase-III-Studie 1 [30] (Werte entnommen aus [21]). Alle Veränderungen nach 1 bzw. 3 Monaten waren statistisch signifikant (p < 0,0001) größer als unter Placebo (nicht dargestellt).
Aus den Ergebnissen der beiden Studien wurde geschlossen, dass 25 mg und 50 mg Daridorexant bei Insomnie den Schlaf verbessern, und dass die Dosis von 50 mg am stärksten schlafverbessernd wirkt und auch die Funktionsfähigkeit am Tage erhöht, während 10 mg der Substanz nicht wirksam sind.
Dem dreimonatigen Zeitraum mit aktiver Medikation folgte eine einwöchige Placebo-Phase („Run-out“). In deren erster Nacht wurden keine Entzugsphänomene beobachtet. Die mit PSG gemessenen Werte für Wachzeit nach Schlafbeginn und Latenz bis zu permanentem Schlaf waren numerisch niedriger, der Wert für die subjektiv berichtete totale Schlafzeit war höher als die entsprechenden Ausgangswerte vor aktiver Medikation. Dies deutet darauf hin, dass keine Rebound-Insomnie auftrat. Allerdings wurde kein statistischer Vergleich durchgeführt [28a].
Nach der Run-out-Phase konnten sich die Teilnehmer der beiden Studien einer neunmonatigen doppelblinden, Placebo-kontrollierten Verlängerung der Studie unterziehen. 600 Patienten nahmen an dieser mit Studie 3 bezeichneten Fortsetzung über mindestens sechs Monate teil, darunter 373, die mindestens zwölf Monate lang teilnahmen. Zu dieser Studie liegt noch keine Publikation vor. Ein anhaltender schlaffördernder Effekt von Suvorexant wurde in einer klinischen Studie über zwölf Monate dokumentiert [29].
Sicherheit und Verträglichkeit
Die Inzidenz von behandlungsbedingten unerwünschten Wirkungen lag für die vier Dosierungen von Daridorexant in der Phase-II-Studie an Patienten im Alter bis zu 65 Jahren zwischen 35 und 38 %, für Placebo bei 30 % und für Zolpidem bei 40 %. Klinisch relevante ernste unerwünschte Wirkungen traten nicht auf [10]. In der Phase-II-Studie an älteren Patienten war das Auftreten behandlungsbedingter unerwünschter Wirkungen unter Daridorexant und Placebo ähnlich häufig. Am häufigsten (≤ 7 % in allen Gruppen) wurden Müdigkeit, Nasopharyngitis, Gangstörungen und Kopfschmerzen berichtet [50].
Die Häufigkeit unerwünschter Wirkungen war in beiden Phase-III-Studien ähnlich hoch, konsistent in den Gruppen der Studienteilnehmer im Alter bis zu und über 65 Jahren und unabhängig von der Dosierung. Die Häufigkeit von Ereignissen, die zum Abbruch der Studie führte, lag unter aktiver Gabe der Prüfsubstanz bei bis zu 2 %, unter Placebo in Studie 1 bei 3 % und in Studie 2 bei 2 %. Schwere unerwünschte Ereignisse traten in beiden Studien unter aktiver Medikation bei 1 %, unter Placebo in Studie 1 bei 2 % und in Studie 1 bei 1 % der Studienteilnehmer auf. Unter den klinisch wirksamen Dosierungen waren Nasopharyngitis (bei bis zu 7 % der Studienteilnehmer) und Kopfschmerzen (bei bis zu 6 %) die häufigsten unerwünschten Ereignisse. Müdigkeit trat bei bis zu 4 %, Somnolenz bei bis zu 3 %, Schwindel und Nausea bei bis zu 2 %, Stürze, Infektionen der oberen Atemwege, exzessive Tagesschläfrigkeit und Schlafparalyse bei bis zu 1 % der mit diesen Dosierungen behandelten Patienten auf. Andere komplexe Schlaf-assoziierte Verhaltensstörungen wie Schlafwandeln, Sprechen und Essen im Schlaf wurden nicht berichtet. Auch Kataplexien ereigneten sich im Verlauf der beiden Studien nicht. Halluzinationen manifestierten sich bei je einem Patienten mit anamnestisch bekannter paranoider Schizophrenie unter 25 mg der Prüfsubstanz in beiden Studien. In Studie 2 traten bei je einem Patienten mit vorbestehender Depression unter 10 mg und unter 25 mg Daridorexant Suizidgedanken auf. Ein Todesfall durch Herzversagen ereignete sich unter 25 mg Daridorexant in Studie 1 bei einem 78-jährigen Patienten mit vorbestehenden Risikofaktoren. Der Untersucher stellte keinen Zusammenhang zwischen dem Ereignis und der Prüfsubstanz fest [30].
Die Wirkung einer an fünf Tagen am Abend verabreichten Dosis von 50 mg Daridorexant auf Parameter der nächtlichen Atmung und des Schlafs bei 28 Patienten mit leicht und mäßig ausgeprägtem obstruktivem Schlafapnoe-Syndrom wurde in einer randomisierten, doppelblinden, Placebo-kontrollierten Studie mit Cross-over-Design geprüft. Es fanden sich eine Verbesserung des Schlafs und keine Störung der nächtlichen Atmung nach einmaliger und nach wiederholter Gabe der Prüfsubstanz. Die Autoren kamen zu dem Schluss, dass die Anwendung von Daridorexant bei leichtem bis mäßigem obstruktivem Schlafapnoe-Syndrom sicher ist [3, 4].
Angaben in der Fachinformation
Die Produktinformation der EMA [18] enthält die folgenden Warnhinweise:
- Die Substanz kann, auch bei Einnahme entsprechend der Verschreibung, die Wachheit am Tage infolge einer Hemmung des ZNS beeinträchtigen. Bei manchen Patienten kann dieser Effekt noch über mehrere Tage nach Absetzen fortwirken. Patienten sollen auf eine mögliche Schläfrigkeit am Tag nach der Einnahme hingewiesen werden.
- Wegen der allgemeinen Sturzgefahr bei älteren Personen sollte Daridorexant in dieser Population mit Vorsicht angewendet werden, obwohl in klinischen Studien keine Zunahme der Sturzhäufigkeit unter der Substanz im Vergleich zu Placebo beobachtet wurde.
- Bei Patienten über 75 Jahre sollte die Substanz mit Vorsicht angewendet werden, da die für diese Population verfügbaren Daten zur Wirksamkeit und Sicherheit begrenzt sind.
- Unter anderem in Zusammenhang mit den oben berichteten Studienergebnissen im Fahrsimulator findet sich der Hinweis, dass Daridorexant vermindernd auf die Wachheit wirkt. Deshalb sollten Patienten insbesondere in den ersten Tagen der Behandlung vor potenziell risikoreichen Tätigkeiten, dem Führen von Fahrzeugen oder dem Bedienen schwerer Maschinen auf mögliche Gefahren aufmerksam gemacht werden, es sei denn, sie fühlen sich völlig wach. Weiter wird empfohlen, etwa neun Stunden zwischen der Einnahme des Arzneimittels und dem Führen von Fahrzeugen oder dem Bedienen von Maschinen zu warten [18].
- Bei kombinierter Einnahme von Daridorexant und anderen Arzneimitteln mit dämpfender Wirkung auf das ZNS ist aufgrund von potenziell additiven Wirkungen Vorsicht geboten. Es sollte eine Dosisanpassung von Daridorexant oder den gleichzeitig angewendeten ZNS-dämpfenden Arzneimitteln in Betracht gezogen werden.
- Vor dem möglichen Auftreten von Schlaflähmung und hypnagogen/hypnopompen Halluzinationen wird gewarnt.
- Symptome, die einer leichten Kataplexie ähneln, wurden unter Orexin-Antagonisten berichtet [18, 21]. Zu diesen wird eine Schwäche in den Beinen über Sekunden bis zu einigen Minuten gezählt, die nachts und tagsüber, auch unabhängig von emotionalen Stimuli berichtet [21]. Dieser Hinweis dürfte sich auf Beobachtungen unter Suvorexant beziehen [23].
- Bei Patienten mit Depression, die mit Hypnotika behandelt werden, wurde eine Verschlechterung der Depression und Suizidgedanken und Suizidversuche berichtet. Wie andere Hypnotika auch, sollte Daridorexant bei Patienten mit Anzeichen einer Depression mit Vorsicht angewendet werden [18].
- In klinischen Studien der Phase III wurden vereinzelt Suizidgedanken bei Teilnehmern mit vorbestehenden psychiatrischen Störungen und/oder belastenden Lebensumständen in allen Behandlungsarmen, einschließlich Placebo, berichtet. Bei Patienten mit Depression kann eine Suizidneigung vorhanden sein. Vorsichtsmaßnahmen können erforderlich sein.
- Bei Patienten mit psychiatrischen Begleiterkrankungen sollte Daridorexant mit Vorsicht angewendet werden, da die für diese Population verfügbaren Daten zur Wirksamkeit und Sicherheit begrenzt sind.
- Daridorexant sollte bei Patienten mit schwerer obstruktiver Schlafapnoe und schwerer chronisch-obstruktiver Lungenerkrankung mit Vorsicht verordnet werden.
- In klinischen Studien gab es bei Teilnehmern mit Insomnie keine Anzeichen für einen Missbrauch oder Entzugserscheinungen, die auf eine körperliche Abhängigkeit nach dem Absetzen der Behandlung hinwiesen.
- Da Personen mit anamnestischem Missbrauch von Alkohol oder Abhängigkeit von Alkohol oder anderen Substanzen ein erhöhtes Risiko für den Missbrauch von Daridorexant haben können, sollten diese Patienten sorgfältig überwacht werden.
- Eine Anwendung bei Patienten mit schwerer Leberfunktionsstörung wird nicht empfohlen [18].
Nur in der Produktinformation der FDA [21] findet sich der folgende Warnhinweis: Komplexe Schlaf-assoziierte Verhaltensstörungen wurden unter Hypnotika einschließlich von Orexin-Antagonisten wie Daridorexant berichtet. Diese Störung kann nach der ersten oder nach irgendeiner folgenden Einnahme eines Hypnotikums wie Daridorexant auftreten und sollte zum sofortigen Absetzen des Medikaments führen. Ein Warnhinweis der FDA aus dem Jahr 2019 bezieht sich auf das unter Z-Substanzen im Vergleich zu anderen Hypnotika erhöhte Risiko für das Auftreten dieser Störung [20].
Bei Narkolepsie ist eine Behandlung mit Daridorexant kontraindiziert [18, 31]. Auch die gleichzeitige Einnahme starker CYP3A4-Inhibitoren ist eine Gegenanzeige [18].
Diskussion
Die nichtklinischen und klinischen Daten zeigen, dass mit Daridorexant ein neuartiges Hypnotikum entwickelt wurde, das gegenüber den vorhandenen Arzneimitteln zur Behandlung chronischer Insomnien deutliche Vorteile aufweist. Die Substanz fördert das Ein- und Durchschlafen ohne Veränderung der natürlichen Schlafarchitektur [35]. Ein Überhang am Morgen scheint in der Regel einer abendlichen Einnahme nicht zu folgen [30, 35]. Versuchstiere konnten ohne Überhang und frei von Störungen der Motorik aus dem durch die Substanz induzierten Schlaf geweckt werden [35]. Allerdings wird vor einer möglichen Beeinträchtigung der Fahrtüchtigkeit und Risiken beim Bedienen schwerer Maschinen, insbesondere in den ersten Tagen der Medikation, gewarnt [18].
Tierexperimentelle Daten deuten darauf hin, dass das Risiko für Störungen von Kognition und Gedächtnis und für die Entwicklung von Toleranz und Abhängigkeit gering ist [35]. Auch bei Patienten mit Insomnie ergab sich bisher kein Hinweis auf die Entwicklung einer Abhängigkeit. Jedoch wurde nach supratherapeutischen Dosen bei Freizeitkonsumenten von Sedativa eine erhöhte Beliebtheit von Daridorexant festgestellt [47]. Die EMA mahnt zu sorgfältiger Überwachung von Patienten mit Substanzmissbrauch und Abhängigkeit in der Anamnese [18]. Es wäre interessant, die Wirkung von Daridorexant auf das Gedächtnis auch bei gesunden Probanden und Patienten mit Insomnie zu untersuchen.
Die beiden zulassungsrelevanten Phase-III-Studien zeigten, dass die schlaffördernde Wirkung bei Patienten mit Insomnie mindestens drei Monate lang erhalten bleibt [30]. Damit erscheint die Substanz für eine länger dauernde Verordnung geeignet zu sein. Daridorexant erwies sich als sicher und gut verträglich [10, 30, 50]. Entsprechend der Auswahl der Studienteilnehmer wurde Daridorexant in der EU zugelassen für die Behandlung von Erwachsenen mit Insomnie, deren Symptome seit mindestens drei Monaten anhalten und eine beträchtliche Auswirkung auf das Tagesgeschehen haben [18]. Die Autoren der beiden zulassungsrelevanten Studien nennen einige Einschränkungen in der Auswahl der Teilnehmer und den Methoden. Infolge der strengen Kriterien könnten die Teilnehmer nicht repräsentativ für die Gesamtheit der Patienten mit Insomnie sein. Die ethnische Diversität auf der Welt könnte durch die Teilnehmer nur teilweise repräsentiert werden. Patienten mit Komorbidität wurden nicht eingeschlossen. Obwohl subjektive Beeinträchtigung der Tagesaktivität ein Einschlusskriterium war, waren keine hohen Werte der IDSIQ-Skala bei Aufnahme in die Studie erforderlich. Da diese Skala ein neu entwickeltes Instrument ist, gibt es damit nur begrenzt Erfahrung [30]. Phase-IV-Studien sind abzuwarten, um noch genauer abzugrenzen, welche Patienten in welchem Umfang von Daridorexant profitieren.
Der Wirkungsmechanismus von DORAs beruht auf einer Hemmung der die Wachheit fördernden Aktivität des Neuropeptids Orexin [15]. Ein Orexin-Mangel liegt dem Krankheitsbild der Narkolepsie zugrunde, die mit Einschlafattacken und zum Teil auch mit Kataplexien einhergeht [41]. Bisher gibt es jedoch keine Hinweise, dass Daridorexant solche Symptome auslösen könnte. Dies lässt sich dadurch erklären, dass das Medikament keinen völligen Orexin-Mangel wie bei Patienten mit Narkolepsie hervorruft [35]. Daridorexant teilt nach dem gegenwärtigen Stand der Forschung nicht bzw. nur in geringem Umfang die unerwünschten Wirkungen und Risiken, die unter Benzodiazepin- und Non-Benzodiazepin-Hypnotika auftreten können wie Veränderung der natürlichen Schlafarchitektur, Störungen von Kognition und Gedächtnis, Entwicklung von Toleranz und Abhängigkeit [7, 28, 49]. Daridorexant ist auch den in den USA und in anderen außereuropäischen Ländern schon eingeführten DORAs überlegen, weil es sich als erste Substanz auch günstig auf Folgen der Insomnie am Tage auswirkt [30]. EMA und FDA haben jedoch eine Reihe von Warnhinweisen für Daridorexant mitgeteilt [18, 21].
Interessenkonflikterklärung
Interessenkonflikte bestehen nicht.
Literatur
1. Azeez IA, Del Gallo F, Cristino L, Bentivoglio M. Daily fluctuation of orexin neuron activity and wiring: the challenge of “chronoconnectivity”. Front Pharmacol 2018;9:1061.
2. Bettica P, Squassante L, Groeger JA, Gennery B, et al. Differential effects of a dual orexin receptor antagonist (SB-649868) and zolpidem on sleep initiation and consolidation, SWS, REM sleep, and EEG power spectra in a model of situational insomnia. Neuropsychopharmacology 2012;37:1224–33.
3. Boof ML, Dingemanse J, Lederer K, Fietze I, et al. Effect of the new dual orexin receptor antagonist daridorexant on nighttime respiratory function and sleep in patients with mild and moderate obstructive sleep apnea. Sleep 2021;44:zsaa275.
4. Boof ML, Ufer M, Fietze I, Pépin JL, et al. Assessment of the effect of the dual orexin receptor antagonist daridorexant on various indices of disease severity in patients with mild to moderate obstructive sleep apnea. Sleep Med 2022;92:4–11.
5. Borbély AA, Mattmann P, Loepfe M, Strauch I, et al. Effect of benzodiazepine hypnotics on all-night sleep EEG spectra. Hum Neurobiol 1985;4:189–94.
6. Boss C, Gatfield J, Brotschi C, Heidmann B, et al. The quest for the best dual orexin receptor antagonist (daridorexant) for the treatment of insomnia disorders. ChemMedChem 2020;15:2286–305.
7. Brandt J, Leong C. Benzodiazepines and Z-drugs: an updated review of major adverse outcomes reported on in epidemiologic research. Drugs R D 2017;17:493–507.
8. Brisbare-Roch C, Dingemanse J, Koberstein R, Hoever P, et al. Promotion of sleep by targeting the orexin system in rats, dogs and humans. Nat Med 2007;13:150–5.
9. Brunner DP, Dijk DJ, Münch M, Borbély AA. Effect of zolpidem on sleep and sleep EEG spectra in healthy young men. Psychopharmacology (Berl) 1991;104:1–5.
10. Dauvilliers Y, Zammit G, Fietze I, Mayleben D, et al. Daridorexant, a new dual orexin receptor antagonist to treat insomnia disorder. Ann Neurol 2020;87:347–56.
11. De Lecea L, Kilduff TS, Peyron C, Gao X, et al. The hypocretins: hypothalamus-specific peptides with neuroexcitatory activity. Proc Natl Acad Sci USA 1998;95:322–7.
12. Dietrich H, Jenck F. Intact learning and memory in rats following treatment with the dual orexin receptor antagonist almorexant. Psychopharmacology (Berl) 2010;212:145–54.
13. Drugs.com. Belsomra approval history. https://www.drugs.com/history/belsomra.html (Zugriff am 16.04.2022).
14. Drugs com. FDA Approves Quviviq (daridorexant) for the treatment of adults with insomnia. https://www.drugs.com/newdrugs/fda-approves-quviviq-daridorexant-adults-insomnia-5766.html (Zugriff am 16.04.2022).
15. Equihua AC, De La Herrán-Arita AK, Drucker-Colin R. Orexin receptor antagonists as therapeutic agents for insomnia. Front Pharmacol 2013;4:163.
16. Esai. US FDA approves Esai’s Davygo (lemborexant) for treatment of insomnia in adult patients. https://www.eisai.com/news/2019/news201993.html (Zugriff am 16.04.2022).
17. Europäische Kommission. Durchführungsbeschluss der Kommission vom 29.4.2022 über die Erteilung der Zulassung für das Humanarzneimittel „QUVIVIQ – Daridorexant“ gemäß der Verordnung (EG) Nr. 726/2004 des Europäischen Parlaments und des Rates.
18. European Medicines Agency. https://www.ema.europa.eu/documents/product-information/quviviq-epar-product-information_de.pdf. Anhang I, Zusammenfassung der Merkmale des Arzneimittels (Zugriff am 22.05.2022).
19. European Medicines Agency. Quiviq, daridorexant. https://www.ema.europa.eu/en/medicines/human/summaries-opinion/quviviq (Zugriff am 17.04.2022).
20. FDA U.S. Food and Drug Administration. Drug Safety Communications. 04–30–2009 https://www.fda.gov/media/123819/download (Zugriff am 17.04.2022).
21. FDA U.S. Food and Drug Administration. Medication Guide QuivicTM (daridorexant). https://www.accessdata.fda.gov/drugsatfda_docs/label/2022/214985s000lbl.pdf (Zugriff am 17.04.2022).
22. Fritschy JM, Mohler H. GABAA-receptor heterogeneity in the adult rat brain: differential regional and cellular distribution of seven major subunits. J Comp Neurol 1995;359:154–94.
23. Gauld AR. Suvorexant (Belsomra) for insomnia. Am Fam Physician 2016;93:1016–20.
24. Gotter AL, Garson SL, Stevens J, Munden RL, et al. Differential sleep-promoting effects of dual orexin receptor antagonists and GABAA receptor modulators. BMC Neurosci 2014;15:109.
25. Idorsia. Media Release. 02.05.2022, Idorsia’s new treatment QUIVIQ (daridorexant) is now available in the US for adults living with insomnia. https://www.idorsia.com/media/news-details?newsId=2742218 (Zugriff am 25.05.2022).
26. Idorsia. Media Release, 03.05.2022, Europe’s first dual orexin receptor antagonist – QUVIVIQ (daridorexant) – granted approval to improve both nighttime symptoms and daytime functioning in adults with chronic insomnia disorder. https://www.idorsia.com/media/news-details?newsId=2743349 (Zugriff am 25.05.2022).
27. Janto K, Prichard JR, Pusalavidyasagar S. An update on dual orexin receptor antagonists and their potential role in insomnia therapeutics. J Clin Sleep Med 2018;14:1399–408.
28. Kripke DF. Chronic hypnotic use: deadly risks, doubtful benefit. Sleep Med Rev 2000;4:5–20.
28a. Leger D, Fietze I, Pain S, Seboek D, et al. Absence of withdrawal symptoms and rebound insomnia upon discontinuation of daridorexant in patients with insomnia. Sleep 2021;44(Suppl 2):A139.
29. Michelson D, Snyder E, Paradis E, Chengan-Liu M, et al. Safety and efficacy of suvorexant during 1-year treatment of insomnia with subsequent abrupt treatment discontinuation: a phase 3 randomised, double-blind, placebo-controlled trial. Lancet Neurol 2014;13:461–71.
30. Mignot E, Mayleben D, Fietze I, Leger D, et al. Safety and efficacy of daridorexant in patients with insomnia disorder: results from two multicentre, randomised, double-blind, placebo-controlled, phase 3 trials. Lancet Neurol 2022;21:125–39.
31. Morairty SR, Wilk AJ, Lincoln WU, Neylan TC, et al. The hypocretin/orexin antagonist almorexant promotes sleep without impairment of performance in rats. Front Neurosci 2014;8:3.
32. Muehlan C, Brooks S, Vaillant C, Meinel M, et al. Driving performance after bedtime administration of daridorexant, assessed in a sensitive simulator. Clin Pharmacol Ther 2022;111:1334–42.
33. Neylan TC, Richards A, Metzler TJ, Ruoff LM, et al. Acute cognitive effects of the hypocretin receptor antagonist almorexant relative to zolpidem and placebo: a randomized clinical trial. Sleep 2020;43:zsaa080.
34. Parks GS, Warrier DR, Dittrich L, Schwartz MD, et al. The dual hypocretin receptor antagonist almorexant is permissive for activation of wake-promoting systems. Neuropsychopharmacology 2016;41:1144–55.
35. Roch C, Bergamini G, Steiner MA, Clozel M. Nonclinical pharmacology of daridorexant: a new dual orexin receptor antagonist for the treatment of insomnia. Psychopharmacology (Berl) 2021;238:2693–708.
36. Peyron C, Kilduff TS. Mapping the hypocretin/orexin neuronal system: an unexpectedly productive journey. J Neurosci 2017;37:2268–72.
37. Sakurai T, Amemiya A, Ishii M, Matsuzaki I, et al. Orexins and orexin receptors: a family of hypothalamic neuropeptides and G protein-coupled receptors that regulate feeding behavior. Cell 1998;92:573–85.
38. Scammell TE, Arrigoni E, Lipton JO. Neural circuitry of wakefulness and sleep. Neuron 2017;93:747–65.
39. Schifano F, Chiappini S, Corkery JM, Guirguis A. An insight into Z-drug abuse and dependence: an examination of reports to the European Medicines Agency database of suspected adverse drug reactions. Int J Neuropsychopharmacol 2019;22:270–7.
40. Schoedel KA, Sun H, Sellers EM, Faulknor J, et al. Assessment of the abuse potential of the orexin receptor antagonist, suvorexant, compared with zolpidem in a randomized crossover study. J Clin Psychopharmacol 2016;36:314–23.
41. Siegel JM, Moore R, Thannickal T, Nienhuis R. A brief history of hypocretin/orexin and narcolepsy. Neuropsychopharmacology 2001;25(Suppl):S14–20.
42. Stewart SH, Westra HA. Benzodiazepine side-effects: from the bench to the clinic. Curr Pharm Des 2002;8:1–3.
43. Tannenbaum PL, Stevens J, Binns J, Savitz AT, et al. Orexin receptor antagonist-induced sleep does not impair the ability to wake in response to emotionally salient acoustic stimuli in dogs. Front Behav Neurosci 2014;8:182.
44. Tannenbaum PL, Tye SJ, Stevens J, Gotter AL, et al. Inhibition of orexin signaling promotes sleep yet preserves salient arousability in monkeys. Sleep 2016;39:603–12.
45. Tisdale RK, Yamanaka A, Kilduff TS. Animal models of narcolepsy and the hypocretin/orexin system: past, present, and future. Sleep 2021;44:zsaa278.
46. Treiber A, de Kanter R, Roch C, Gatfield J, et al. The use of physiology-based pharmacokinetic and pharmacodynamic modeling in the discovery of the dual orexin receptor antagonist ACT-541468. J Pharmacol Exp Ther 2017;362:489–503.
47. Ufer M, Kelsh D, Schoedel KA, Dingemanse J. Abuse potential assessment of the new dual orexin receptor antagonist daridorexant in recreational sedative drug users as compared to suvorexant and zolpidem. Sleep 2022;45:zsab224.
48. Uslaner JM, Tye SJ, Eddins DM, Wang X, et al. Orexin receptor antagonists differ from standard sleep drugs by promoting sleep at doses that do not disrupt cognition. Sci Transl Med 2013;5:179ra44.
49. Uzun S, Kozumplik O, Jakovljević M, Sedić B. Side effects of treatment with benzodiazepines. Psychiatr Danub 2010;22:90–3.
50. Zammit G, Dauvilliers Y, Pain S, Sebök Kinter D, et al. Daridorexant, a new dual orexin receptor antagonist, in elderly subjects with insomnia disorder. Neurology 2020;94:e2222–32.
Prof. Dr. Axel Steiger, Kaiserslautern, E-Mail: profsteiger@gmail.com
Daridorexant, a new dual orexin receptor antagonist for the treatment of insomnia
Daridorexant is the first dual orexin antagonist (DORA) approved in the European Union for the treatment of chronic insomnia. The mechanism of action is inhibition of the wakefulness-promoting activity of the neuropeptide orexin via its two receptors in the brain. In this way, DORAs act more specifically on sleep-wake regulation than benzodiazepine and nonbenzodiazepine hypnotics. Nonclinical studies showed that daridorexant was sleep-promoting without altering sleep architecture. Experimental animals were immediately arousable from substance-induced sleep and did not show any hangover or disturbances in motor function upon awakening. Further, there was no evidence of disturbances in cognition and memory or risk of developing tolerance and dependence after administration of the substance. However, recreational users of sedatives were found to have increased drug-liking of supratherapeutic doses of the substance. The clinical efficacy of daridorexant was demonstrated in clinical studies in patients with insomnia. In addition to consistently promoting sleep onset and sleep maintenance without a hangover the following morning after evening doses of 25 mg and 50 mg, patients found an improvement in daytime well-being and functioning after 50 mg. No rebound insomnia occurred after discontinuation. The substance proved to be safe and well tolerated.
Key words: Daridorexant, dual orexin antagonist, hypnotic, insomnia
Psychopharmakotherapie 2022; 29(04):130-137
