Lennart Höfs und Björn Falkenburger, Dresden
Die Parkinson-Krankheit zählt zu den am weitesten verbreiteten neurodegenerativen Erkrankungen des Alters und äußert sich durch motorische und nichtmotorische Symptome [10]. Sie ist vor allem für das Auftreten von Rigor, Tremor und Bradykinese bekannt. Ursächlich ist ein Verlust dopaminerger Neurone in der Substantia nigra, der zum Dopamin-Mangel in den nigrostriatalen Projektionen führt [2]. Zu den nichtmotorischen Symptomen zählen REM(Rapid Eye Movement)-Schlaf-Störungen und Störungen des autonomen Nervensystems wie Obstipation oder orthostatische Hypotonie. Außerdem treten psychiatrische Beschwerden auf wie Depression, Angststörung und im fortgeschrittenen Verlauf auch kognitive Einschränkungen. Die medikamentöse Therapie erfolgt derzeit rein symptomatisch und zielt im Wesentlichen auf eine Erhöhung des Dopamin-Spiegels oder die Kompensation des Dopamin-Mangels durch Dopaminagonisten ab. Zum Einsatz kommen insbesondere die Dopamin-Vorstufe Levodopa und Dopamin-Rezeptoragonisten.
Apomorphin ist ein sehr alter Arzneistoff. Die Synthese wurde erstmals im Jahr 1869 beschrieben und die Gabe bei Patienten mit neurologischen Erkrankungen erfolgte 1884 [24, 38]. Effekte auf Tremor und Rigor bei der Parkinson-Krankheit wurden bereits 1951 beschrieben – noch bevor bekannt war, dass Parkinson-Symptome durch einen Dopamin-Mangel verursacht werden [33]. Aufgrund der mangelnden oralen Bioverfügbarkeit und Verträglichkeit wurde Apomorphin in den letzten Jahrzehnten nur subkutan verwendet – in Form eines Pens oder einer Pumpe. Im Mai 2020 wurde eine neue sublinguale Applikationsform für den amerikanischen Markt zugelassen [12a]. Im Folgenden werden wir die Wirkungen von sublingualem Apomorphin darstellen und die neue Möglichkeit in bestehende Therapiekonzepte einordnen.
Das Fundament der modernen Parkinson-Therapie wurde in den späten 60er-Jahren mit der Entdeckung von Levodopa gelegt [7, 39]. Schwer erkrankten Patienten war es vom einen auf den anderen Tag wieder möglich, Willkürbewegungen auszuführen und sich selbstständig zu bewegen. Die Entdeckung stellte einen Durchbruch für das Verständnis und für die Behandlung der Erkrankung dar. In den Folgejahren wurden allerdings auch die Schwächen der Therapie deutlich: Nach einer symptomarmen „Honeymoon-Periode“ treten Wirkschwankungen (Fluktuationen) auf, in denen die Beweglichkeit zwischen „zu wenig“ (OFF), annähernd normal (ON) und zu „zu viel“ oszilliert. Letzteres ist geprägt von störenden Überbeweglichkeiten (Dyskinesien). Im Krankheitsverlauf wird die Zeit im ON immer kürzer. Nichtmotorische Symptome können ebenfalls fluktuieren [21, 34].
Nach einer Krankheitsdauer von vier bis sechs Jahren sind 40 % der Patienten von Wirkschwankungen betroffen, nach neun Jahren sind es über 90 % [1]. Die Ursachen der Fluktuationen sind vielfältig:
- Konkurrenz mit Nahrungseiweiß um die Aufnahme aus dem Darm und intestinale Fehlbesiedelungen beeinflussen die Absorption von Levodopa [5, 31]. Darüber hinaus wird die Aufnahme von Arzneistoffen aus dem Darm durch die abnehmende Magen-Darm-Motilität im Rahmen der Parkinson-Krankheit gestört.
- Durch die Degeneration dopaminerger Axonterminale reduziert sich die Speicherkapazität für Levodopa und Dopamin. Levodopa wird dann in serotonergen Axonterminalen in Dopamin umgewandelt und ohne Kontrolle durch präsynaptische Dopamin-D2-Rezeptoren freigesetzt [12].
- Der chronische Mangel an Dopamin im Striatum führt zu postsynaptischen Adaptationsvorgängen. So verändern die striatalen Projektionsneurone ihre elektrische Erregbarkeit, ihre Dendritenmorphologie und die Dichte dendritischer Dornen, um die fehlenden dopaminergen Afferenzen auszugleichen [13, 17, 35, 36].
Aufgrund dieser Adaptationsvorgänge sind Dyskinesien in der Regel stärker auf derjenigen Körperseite ausgeprägt, die als erste von der Parkinson-Symptomatik betroffen war. Dies ist die Körperseite, für die das Striatum mit dem ausgeprägteren dopaminergen Defizit zuständig ist [12].
Aktuelle therapeutische Strategien bei Wirkschwankungen
Die Konkurrenz mit Nahrungseiweiß kann durch die Einnahme von Levodopa in ausreichendem zeitlichem Abstand zur Nahrung reduziert werden; Levodopa-abbauende Bakterien können potenziell eradiziert werden [14, 20]. Beide Probleme können grundsätzlich auch durch einen Wechsel auf Dopaminagonisten vermieden und Resorptionsstörungen durch den transdermalen Applikationsweg (Rotigotin) umgangen werden. Die präsynaptischen Veränderungen können aktuell nicht therapeutisch adressiert werden. Nach unserem aktuellen Verständnis ihrer Entstehung können sie jedoch durch eine frühe und adäquat dosierte dopaminerge Medikation verzögert werden. Hierzu liegen allerdings insgesamt widersprüchliche Daten vor [23, 26, 30].
Die wichtigste therapeutische Strategie zur Reduktion der Wirkschwankungen ist daher, einen möglichst konstanten Spiegel an dopaminerger Stimulation zu erreichen. Dazu wird die Tagesdosis von Levodopa auf mehrere Einnahmezeitpunkte verteilt. Der Einsatz retardierter Levodopa-Präparate am Tag ist aufgrund der Konkurrenz an Aminosäure-Transportern im Darm nicht sinnvoll, kann jedoch den nächtlichen Wirkspiegel verbessern. Die Verwendung von löslichem Levodopa kann vor allem morgens die Zeit bis zum Beginn der Arzneimittelwirkung verkürzen. Die Wirkdauer von Levodopa kann zudem durch Inhibitoren der metabolisierenden Enzyme (DOPA-Decarboxylase, Catechol-O-Methyltransferase [COMT] und Monoaminoxidase-B [MAO-B]) verlängert werden. Retardierte orale Dopaminagonisten zeigen ein deutlich gleichmäßigeres Wirkprofil als Levodopa-Präparate, müssen aber häufig trotzdem zweimal täglich verordnet werden. Transdermales Rotigotin bietet den zusätzlichen Vorteil, dass es unabhängig von der Magen-Darm-Motilität aufgenommen wird. Wenn diese Strategien nicht ausreichend sind, kommen eine Pumpentherapie und die tiefe Hirnstimulation in Betracht [27].
Geschichte und Pharmakologie des Apomorphins
Apomorphin wurde erstmals 1869 als ein Morphin-Derivat synthetisiert [24]. Es verfügt weder über narkotisierende noch analgetische Wirkungen. Ende des 19. Jahrhunderts wurde Apomorphin als Sedativum in psychiatrischen Einrichtungen eingesetzt. Außerdem kam es als Emetikum zur Anwendung [8]. Eine Ähnlichkeit der chemischen Struktur mit Dopamin wurde im Jahr 1965 beschrieben und beruht auf der polyzyklischen Aminstruktur [11, 19]. Außerdem wurden hypo- sowie hyperkinetische Zustände in Ratten durch Apomorphin-Derivate ausgelöst, bei denen eine Hydroxylgruppe verändert oder diese durch eine Methoxygruppe substituiert wurde [11]. Klinische Relevanz in der Parkinson-Therapie erlangte der Wirkstoff erst 1979, als Apomorphin in Kombination mit dem neuen, nicht Liquor-gängigen Dopamin-Rezeptorantagonisten Domperidon verabreicht wurde [6]. Durch Domperidon konnte die stark emetische Wirkkomponente gelindert werden.
Aufgrund seiner lipophilen Eigenschaften kann Apomorphin leicht die Blut-Hirn-Schranke passieren. Apomorphin hat eine hohe Affinität für den D4-Rezeptor, eine moderate Affinität für D2-, D3-, D5-Rezeptoren und eine geringe Affinität für D1-Rezeptoren. Apomorphin aktiviert also sowohl D1-Rezeptoren als auch D2-Rezeptoren. Außerdem bindet es an adrenerge (α1D, α2B, α2C) sowie serotonerge Rezeptoren (5-HT1A, 5-HT2A, 5-HT2B, 5-HT2C). Die Wirkung bei Parkinson-Patienten beruht wahrscheinlich auf der Stimulation postsynaptischer D2-Rezeptoren im Striatum [19].
Die häufigsten Nebenwirkungen umfassen Übelkeit, Schwindel, Schläfrigkeit, Somnolenz, Halluzinationen, Schweißausbrüche, orthostatische Dysfunktion und QT-Zeit-Verlängerungen [22]. Daher ist insbesondere bei Apomorphin-naiven Patienten die klinische Überwachung inklusive regelmäßiger EKG(Elektrokardiogramm)-Kontrollen zu empfehlen.
Bisherige Applikationswege
Vor allem aus den folgenden zwei Gründen eignet sich Apomorphin nicht zur oralen Einnahme: Es wirkt stark emetisch und es unterliegt einem ausgeprägten First-Pass-Effekt. Die orale Bioverfügbarkeit liegt bei 1,7 %. Es ist nicht möglich, eine therapeutische Wirkstoffkonzentration durch Dosissteigerung zu erreichen, da dies zur Akkumulation nephrotoxischer Metaboliten führen würde. Die Serumhalbwertszeit liegt bei 30 bis 60 Minuten [25]. Für den Erhalt eines stabilen Wirkspiegels ist dies zu kurz. Daher wird Apomorphin in Europa bislang ausschließlich in Form einer subkutanen Injektion verwendet.
Ein Apomorphin- oder Levodopa-Test kann zur Unterscheidung zwischen idiopathischen und atypischen Parkinson-Syndromen verwendet werden. Hierbei wird die Reversibilität der Symptomatik durch die wahlweise Gabe von Apomorphin subkutan oder Levodopa oral getestet. In dieser Verwendung bietet Apomorphin einen klaren Vorteil gegenüber Levodopa, da es parenteral und nahrungsunabhängig resorbiert wird und das klinische Ansprechen im Falle eines idiopathischen Parkinson-Syndroms zügig und zuverlässig eintritt. Nachteilig ist die stärker ausgeprägte Übelkeit [32].
Seit fast 20 Jahren besteht eine Zulassung für einen subkutanen Apomorphin-Bolus im Sinne einer „Rescue-Therapie“ während einer OFF-Phase. Dafür werden verschiedene Apomorphin-Pens verwendet. Diese Therapie hat sich als sehr effektiv erwiesen und ermöglicht bei 90 % der Patienten ein schnelles Ansprechen innerhalb von 15 bis 30 Minuten [9]. Die kurze Halbwertszeit ist für diese Anwendung von Vorteil, da der Rescue-Bolus nicht akkumuliert. Mit dieser Therapie können kurzzeitige OFF-Episoden überbrückt werden und sie kann sowohl für vorhersehbare als auch für nicht vorhersehbare OFF-Zustände eingesetzt werden. Dies kann zur Glättung des Wirkprofils beitragen.
Bei einer subkutanen Dauerinfusion, bekannt als „Apomorphin-Pumpe“, wird der Wirkstoff kontinuierlich abgegeben. Schwankungen in der Beweglichkeit wird so wirksam vorgebeugt. Die Zeit im OFF kann um mehr als 50 % reduziert werden. Außerdem nehmen Dyskinesien im ON ab [4]. Nachteile sind die Invasivität, der pflegerische Aufwand, die mögliche Bildung subkutaner Noduli und das Risiko einer Pannikulitis (lokalen Entzündung des Unterhautfettgewebes) [37]. Dennoch kann ein relevanter Anteil an Patienten über Jahre erfolgreich mit dieser Therapie behandelt werden.
Intravenöses Apomorphin ist mit einem hohen Risiko für thromboembolische Ereignisse verbunden und wird daher praktisch nicht genutzt. Die intranasale Apomorphin-Gabe verursacht Schleimhaut-Irritationen und Vestibulitis. Eine rektale Gabe hat sich aufgrund des umständlichen Applikationsweges nicht durchgesetzt [18].
Sublinguales Apomorphin
Die sublinguale Applikation stellt in der Theorie eine nicht invasive und leicht zu dosierende Alternative dar. Insbesondere die einfache Handhabung ist ein Vorteil im Vergleich zu anderen Arzneiformen/Formulierungen. Daher wurde ein 22 × 22 mm großer, zweischichtiger Filmstreifen entwickelt, der für drei Minuten unter die Zunge gelegt wird. Die obere Schicht besteht aus Cellulose-Ether und enthält einen Stabilisator sowie Apomorphin-HCl. Die darunterliegende Schicht enthält einen Penetrationsbeschleuniger, Geschmacksstoffe und einen Puffer. So soll die Säureproduktion abgemildert werden, die während der Absorption entsteht [3]. Sublinguales Apomorphin ist in den Dosierungen 10 mg, 15 mg, 20 mg, 25 mg und 30 mg verfügbar [12a].
Klinische Phase-II-Studien
In eine Phase-II-Studie zur Testung der Wirksamkeit, Dosierung und Sicherheit des neuen Arzneimittels wurden 19 Patienten eingeschlossen. Die Studienteilnehmer erfüllten die Kriterien der Parkinson‘s Disease Society Brain Bank, hatten in den vergangenen vier Wochen eine stabile Dosis Levodopa, zeigten eine vorhersehbare OFF-Episode nach dem Aufwachen und eine tägliche OFF-Zeit von mehr als zwei Stunden. Die Einschlusskriterien sind vergleichbar mit anderen Studien, in denen Wirkschwankungen im Vordergrund standen. Die Studienteilnehmer wurden aufgefordert, nach 22 Uhr des Vorabends kein Levodopa mehr einzunehmen und die Morgenmedikation auszusetzen. Nachdem eine morgendliche OFF-Phase klinisch bestätigt wurde, erhielten die Patienten 10 mg Apomorphin sublingual. Die klinische Beurteilung fand nach der MDS-UPDRS (Movement Disorder Society-Unified Parkinson‘s Disease Rating Scale) Teil III in regelmäßigen Intervallen über drei Stunden nach Einnahme statt. Stellte sich innerhalb von drei Stunden kein ON-Status ein, wurde die Dosis in 5-mg-Schritten bis auf maximal 30 mg erhöht. Die Gabe erfolgte bis zu zweimal täglich. 15 von 19 (78,8 %) Patienten sprachen vollständig auf die Behandlung an. Zwei Patienten verschluckten den Filmstreifen. Bei zwei weiteren Teilnehmern zeigte auch die Maximaldosis (30 mg) keine ausreichende Wirksamkeit. Diejenigen, die vom sublingualen Apomorphin-Streifen profitierten, sprachen innerhalb von 30 Minuten an, sechs Patienten bereits nach 15 Minuten. Von einer ausreichenden Wirkung profitierten 13 von 15 Patienten (mindestens 30 Minuten) und 9 von 15 Patienten (90 Minuten). Drei Patienten benötigten 10 mg für ein vollständiges Ansprechen, fünf Teilnehmer15 mg, vier 20 mg, zwei 25 mg und ein Patient 30 mg [15].
Die Aussagekraft der Studie ist durch einige Faktoren limitiert. So waren weder Patienten noch Ärzte verblindet. Dadurch könnte die Wirkung überschätzt und auch die Nebenwirkungen verstärkt oder vermindert wahrgenommen worden sein. Darüber hinaus war die Studienpopulation (19 Teilnehmer) vergleichsweise gering. Aufgrund der inkrementellen Dosisfindung waren jeweils Anteile der vorherigen Gabe noch im Blutkreislauf vorhanden. Die für ein Ansprechen notwendige Dosis könnte dadurch unterschätzt worden sein. In der Folgestudie wurde daher das Dosierungsprotokoll verbessert.
Klinische Phase-III-Studien
Basierend auf der ersten Studie folgte ab 2019 eine randomisierte, doppelblinde kontrollierte Studie. Diese wurde an 32 Zentren in den USA und Kanada durchgeführt. Die Einschlusskriterien entsprachen in den kritischen Punkten jenen der Phase-II-Studie. Um die individuell erforderliche Apomorphin-Dosis zu bestimmen, wurde Apomorphin zunächst im OFF-Zustand und ohne Verblindung über mehrere Tage auftitriert. Als ON wurde ein vergleichbares Ansprechen wie nach der Einnahme von Levodopa gewertet.
Nachdem die individuelle Dosis bestimmt worden war, folgte die doppelblinde Randomisierung der 109 Patienten. Die Gruppen waren annähernd gleich groß und in der Krankheitslast vergleichbar. Die Teilnehmer legten bei Bedarf bis zu fünfmal täglich einen Streifen unter die Zunge, der entweder Apomorphin oder Placebo enthielt. Zu Beginn der Studie sowie nach vier, acht und zwölf Wochen erfolgte eine Beurteilung in der Klinik nach der MDS-UDPRS. Diese fand unmittelbar vor sowie alle 15 bis 90 Minuten nach der Einnahme statt. Nach zwölf Wochen zeigte sich im Vergleich zu Placebo eine signifikante Besserung der motorischen Symptomatik 30 Minuten nach sublingualer Apomorphin-Einnahme. 46 der 55 Teilnehmer (84 %) des Placebo-Arms beendeten die Studie, aber nur 34 der 54 Patienten (63 %) des Apomorphin-Arms. Neun Patienten (17 %) des Apomorphin-Arms brachen die Behandlung aufgrund von oropharyngealen Ereignissen wie Lippenulzeration, Gingivaödemen sowie Schwellungen an Lippen, Schleimhaut oder Rachen ab. Glücklicherweise wurde über keine irreversiblen Folgen berichtet [28].
Vor allem die Absorptions-assoziierten Schleimhautläsionen sehen wir als Limitation des Präparats. So hat fast jeder fünfte Studienteilnehmer im Apomorphin-Arm die Therapie abgebrochen. Diese Zahl erscheint hoch – insbesondere vor dem Hintergrund, dass es sich um eine chronische Erkrankung handelt, die oft eine jahrelange Medikation erfordert. Der Apomorphin-Streifen wurde über einen Zeitraum von zwölf Wochen getestet. Es stellt sich daher die Frage, ob Patienten mit initialer Toleranz auch langfristig frei von Nebenwirkungen bleiben. Falls nicht, steigt der Anteil von Patienten, für die sublinguales Apomorphin nicht geeignet ist. Dies muss noch untersucht werden.
Die Autoren fanden keinen Hinweis auf eine Verschlechterung der Dyskinesien, orthostatischen Hypotonie, Impulskontrollstörungen, Halluzinationen oder ungewollten Schlafepisoden während einer sublingualen Apomorphin-Therapie. Über eine Zunahme dieser Symptome wurde hingegen unter einer subkutanen Dauerinfusion berichtet, für die vermutlich die langandauernde Stimulation verantwortlich ist [28].
Erweiterte Dosisfindung
In einer Folgestudie untersuchten Olanow et al., inwiefern sich die Dosisfindung optimieren ließe. Dafür verwendeten sie das Titrierungsprotokoll der Phase-III-Studie mit einer wichtigen Abwandlung. Nachdem bei einem Patienten ein mit Levodopa vergleichbares ON festgestellt wurde, wurde die Dosis um weitere 5 bis 10 mg erhöht (Abb. 1). Es zeigte sich, dass alle 35 Patienten von einer Dosiserhöhung in Form einer verbesserten Motorik nach der MDS-UPDRS profitierten. Limitierend war das Auftreten von Nebenwirkungen wie Somnolenz und Übelkeit. 16 der 35 Patienten haben eine höhere als die initial gewählte Dosis toleriert. Interessanterweise waren Antiemetika nicht zugelassen. Darüber hinaus gab es Patienten, die erst bei einer Dosierung von 40 mg (n = 2) bzw. 50 mg (n = 1) auf sublinguales Apomorphin ansprachen [29]. In den vorherigen Studien wurden keine Patienten mit einem Bedarf von mehr als 30 bzw. 35 mg eingeschlossen [15, 28]. Möglicherweise wurde die Maximaldosis in den vorherigen Studien zu gering gewählt. Somit ist die Frage nach der zu empfehlenden Maximaldosis nicht ohne weitere Analysen zu beantworten.
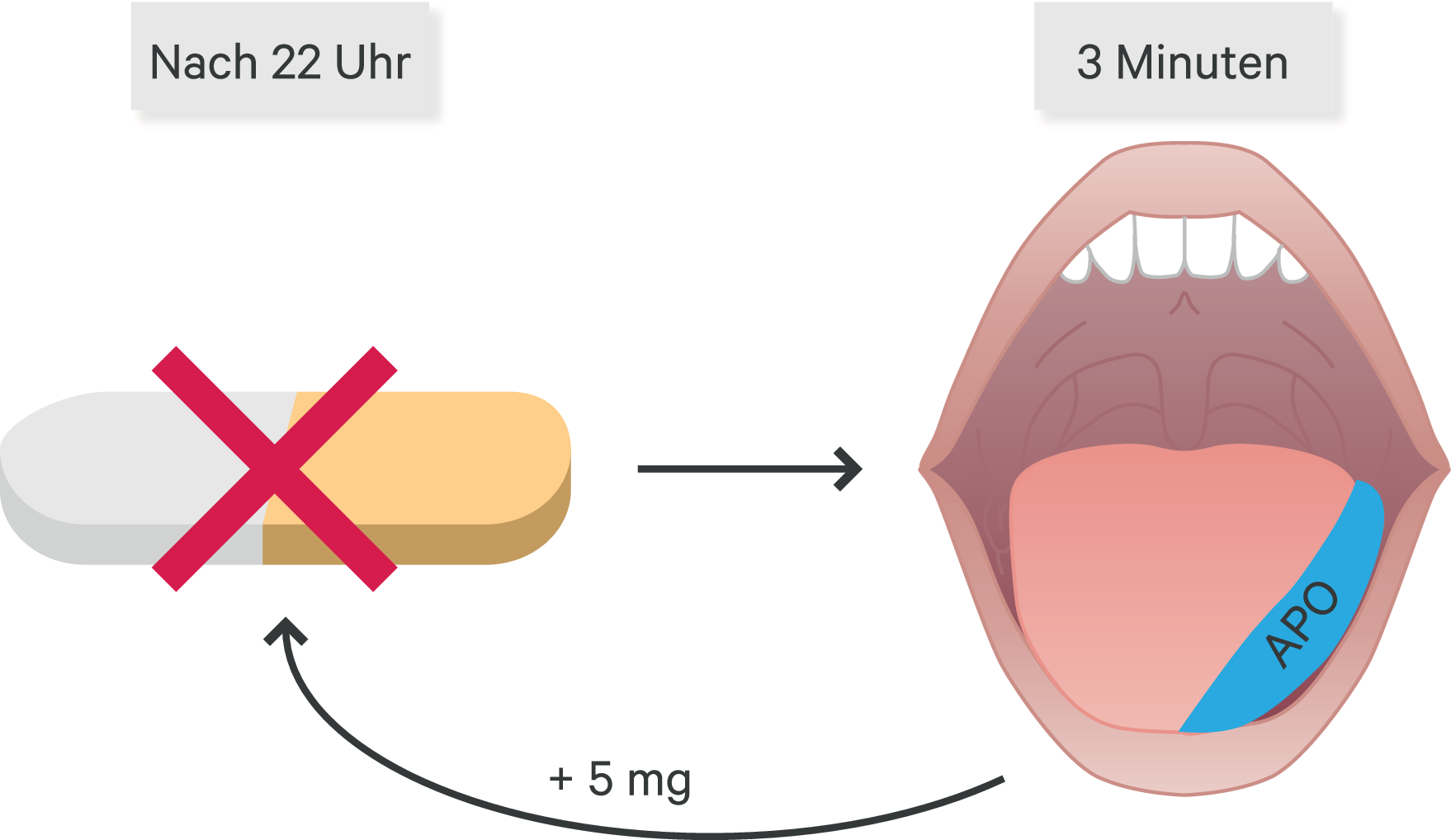
Abb. 1. Schema für das Auftitrieren Die Patienten nehmen am Vorabend und am darauffolgenden Morgen ihre Parkinson-Medikation nicht ein, sodass zu Beginn der Testung ein OFF-Zustand besteht. Begonnen wird mit dem Streifen in der kleinstmöglichen Dosisierung (10 mg). Innerhalb von 45 Minuten sollte sich ein vollständiges ON ohne intolerable Nebenwirkungen einstellen. Setzt kein ON ein, wird das Protokoll an den Folgetagen wiederholt und die Dosierung in 5-mg-Schritten gesteigert. Der höchstdosierte Streifen enthält 30 mg.
Vergleich mit etablierten Therapien
Um zu klären, wie der sublinguale Apomorphin-Streifen gegenüber etablierten Therapien abschneidet, haben Hui et al. sublinguales Apomorphin mit oralem Levodopa/Carbidopa verglichen. 109 Patienten der Phase-III-Studie erhielten dafür an einem weiteren Tag Levodopa/Carbidopa. Um den motorischen Status zu ermitteln, zogen die Autoren die MDS-UPDRS heran. Bereits nach 15 Minuten zeigte die Apomorphin-Gruppe eine verbesserte motorische Antwort. Das Wirkmaximum des Apomorphin-Streifens trat nach 45 Minuten ein, bei Levodopa/Carbidopa dagegen nach 90 Minuten (Abb. 2). Sublinguales Apomorphin war schneller, aber dafür kürzer wirksam als Levodopa/Carbidopa. Der maximale Effekt auf den MDS-UPDRS-Score scheint etwas geringer, jedoch ist der Unterschied nicht statistisch signifikant [16]. Erwähnenswert ist ebenfalls, dass Ergebnisse klinischer Studien zum Vergleich von subkutanem und sublingualem Apomorphin noch ausstehen (NCT03391882).
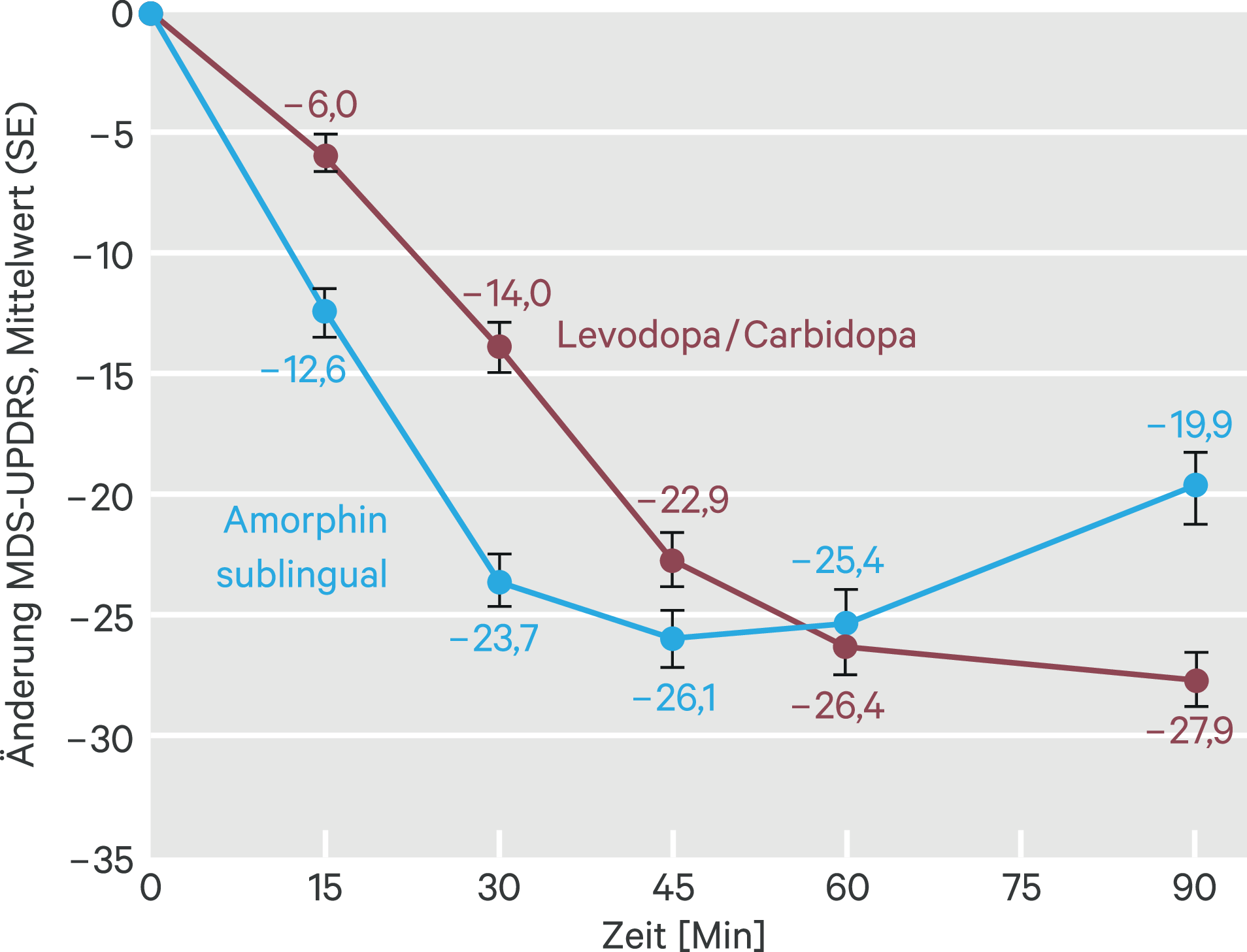
Abb. 2. Motorisches Ansprechen nach der MDS-UPDRS Teil III auf sublinguales Apomorphin (n = 109) verglichen mit oralem Levodopa/Carbidopa (n = 108). Der Status wurde einmal vor (x0, y0) sowie alle 15 bis maximal 90 Minuten nach der Applikation erhoben (angepasst nach Hui et al. [16]) SE: Standardfehler
Fazit
Über 90 % der Parkinson-Patienten leiden im Laufe ihrer Erkrankung an motorischen Fluktuationen und Dyskinesien [1]. Dabei kommt es einerseits zu Hyper- und Dyskinesien, andererseits zum Wiederauftreten motorischer Symptome wie Rigor, Tremor, Bradykinese und Gangunsicherheit zu unvorhersehbaren Zeitpunkten. Eine optimale Einstellung der langwirksamen Medikation steht an erster Stelle bei der Therapie von motorischen Fluktuationen und kann in vielen Fällen die Zeiten im OFF reduzieren. Zur kurzfristigen Verbesserung der Beweglichkeit sind bereits jetzt lösliche Levodopa-Präparate verbreitet und verträglich. Darüber hinaus eignet sich das kurzwirksame Apomorphin gut, um OFF-Phasen rasch zu verkürzen. Aufgrund der parenteralen Applikation wird die Wirkung weder von einer gestörten Magen-Darm-Motilität noch von der Nahrung beeinflusst. Das neue sublinguale Präparat wird für drei Minuten unter die Zunge gelegt und setzt dort Apomorphin frei. Eine OFF-Episode kann damit bei 79 % der Patienten innerhalb von 30 Minuten beendet werden und die Wirkung hält bis zu 90 Minuten an. Die sublinguale Einnahme ist allerdings bei jedem Dritten mit Nebenwirkungen im Oropharynx verbunden. Somit ist die neuartige Darreichungsform nicht uneingeschränkt für alle Patienten geeignet. Insgesamt sehen wir in der neuen Darreichungsform eine wertvolle Ergänzung des therapeutischen Repertoires, auch wenn sie aktuell noch nicht in Europa zugelassen ist.
Interessenkonflikterklärung
Die Klinik und Poliklinik für Neurologie am Universitätsklinikum Dresden war Studienzentrum der von Sunovion Pharmaceuticals Inc. finanzierten Studie „An Open-Label, Randomized, Crossover Trial utilizing a Single-Blinded Rater to evaluate APL-130 277 compared to s. c. Apomorphine in Levodopa Responsive Subjects with Parkinson’s Disease Complicated by Motor Fluctuations“ (EudraCT No: 2016–003456–70). Es bestehen keine Interessenkonflikte.
Literatur
1. Ahlskog JE, Muenter MD. Frequency of levodopa-related dyskinesias and motor fluctuations as estimated from the cumulative literature. Mov Disord 2001;16:448–58.
2. Bernheimer H, Birkmayer W, Hornykiewicz O, Jellinger K, et al. Brain dopamine and the syndromes of Parkinson and Huntington clinical, morphological and neurochemical correlations. J Neurol Sci 1973;20:415–55.
3. Bilbault T, Simon T, Walker R, Grundy LS, et al. Buccal mucosal irritation studies of sublingual apomorphine film (APL-130277) in Syrian golden hamsters. Ther Deliv 2016;7:611–8.
4. Ceballos-Baumann A. Kontinuierliche Therapie mit der Apomorphinpumpe. Aktuelle Neurologie 2011;38(Suppl 01):S17–26.
5. Contin M, Martinelli P. Pharmacokinetics of levodopa. J Neurol 2010;257(Suppl 2):253–61.
6. Corsini G, Zompo MD, Gessa G, Mangoni A. Therapeutic efficacy of apomorphine combined with an extracerebral inhibitor of dopamine receptors in Parkinson’s disease. Lancet 1979;313:954–6.
7. Cotzias GC, Van Woert MH, Schiffer LM. Aromatic amino acids and modification of Parkinsonism. N Engl J Med 1967;276:374–9.
8. Deleu D, Hanssens Y, Northway MG. Subcutaneous apomorphine: An evidence-based review of its use in Parkinson’s disease. Drugs Aging 2004;21:687–709.
9. Dewey RB, Hutton JT, LeWitt PA, Factor SA. A randomized, double-blind, Placebo-controlled trial of subcutaneously injected apomorphine for parkinsonian off-state events. Arch Neurol 2001;58:1385–92.
10. Dorsey ER, Sherer T, Okun MS, Bloem BR. The emerging evidence of the Parkinson pandemic. J Parkinsons Dis 2018;8(Suppl 1):S3–8.
11. Ernst AM. Relation between the action of dopamine and apomorphine and their O-methylated derivatives upon the CNS. Psychopharmacologia 1965;7:391–9.
12. Espay AJ, Morgante F, Merola A, Fasano A, et al. Levodopa-induced dyskinesia in Parkinson’s disease: current and evolving concepts. Ann Neurol 2018;84:797–811.
12a. FDA. Drug Approval Package: Kynmobi. https://www.accessdata.fda.gov/drugsatfda_docs/nda/2020/210875Orig1s000TOC.cfm (Zugriff am 28.02.2022).
13. Fieblinger T, Graves SM, Sebel LE, Alcacer C, et al. Cell type-specific plasticity of striatal projection neurons in parkinsonism and L-DOPA-induced dyskinesia. Nat Commun 2014;5:5315.
14. Hashim H, Azmin S, Razlan H, Yahya NW, et al. Eradication of Helicobacter pylori infection improves levodopa action, clinical symptoms and quality of life in patients with Parkinson’s disease. PLoS One 2014;9:e112330.
15. Hauser RA, Olanow CW, Dzyngel B, Bilbault T, et al. Sublingual apomorphine (APL-130277) for the acute conversion of OFF to ON in Parkinson’s disease. Mov Disord 2016;31:1366–72.
16. Hui JS, Fox SH, Neeson W, Bhargava P, et al. Open-label titration of apomorphine sublingual film in patients with Parkinson’s disease and “OFF” episodes. Parkinsonism Relat Disord 2020;79:110–6.
17. Ingham CA, Hood SH, Arbuthnott GW. Spine density on neostriatal neurones changes with 6-hydroxydopamine lesions and with age. Brain Res 1989;503:334–8.
18. Koller W, Stacy M. Other formulations and future considerations for apomorphine for subcutaneous injection therapy. Neurology 2004;62(Suppl 4):S22–6.
19. LeWitt PA. Subcutaneously administered apomorphine. Neurology 2004;62(Suppl 4):S8–11.
20. Liu H, Su W, Li S, Du W, et al. Eradication of Helicobacter pylori infection might improve clinical status of patients with Parkinson’s disease, especially on bradykinesia. Clin Neurol Neurosurg 2017;160:101–4.
21. Marsden CD, Parkes JD. “On-Off” effects in patients with Parkinson’s disease on chronic levodopa therapy. Lancet 1976;307:292–6.
22. Martinez-Martin P, Reddy P, Antonini A, Henriksen T, et al. Chronic subcutaneous infusion therapy with apomorphine in advanced Parkinson’s disease compared to conventional therapy: a real life study of non motor effect. J Parkinsons Dis 2011;1:197–203.
23. Matarazzo M, Perez-Soriano A, Stoessl AJ. Dyskinesias and levodopa therapy: why wait? J Neural Transm 2018;125:1119–30.
24. Matthiessen A, Wright CRA. Researches into the chemical constitution of the opium bases. Part 1: on the action of hydrochloric acid on morphia. Proc R Soc L B Biol Sci 1869;17:455–60.
25. Neef C, Van Laar T. Pharmacokinetic-pharmacodynamic relationships of apomorphine in patients with Parkinson’s disease. Clin Pharmacokinet 1999;37:257–71.
26. Obeso JA, Rodriguez-Oroz M, Marin C, Alonso F, et al. The origin of motor fluctuations in Parkinson’s disease. Neurology 2004;62(Suppl 1):S17–30.
27. Obeso JA, Stamelou M, Goetz CG, Poewe W, et al. Past, present, and future of Parkinson’s disease: A special essay on the 200th anniversary of the Shaking Palsy. Mov Disord 2017;32:1264–310.
28. Olanow CW, Factor SA, Espay AJ, Hauser RA, et al. Apomorphine sublingual film for off episodes in Parkinson’s disease: a randomised, double-blind, placebo-controlled phase 3 study. Lancet Neurol 2020;19:135–44.
29. Olanow CW, Stocchi F, Peckham EL, De Pandis MF, et al. Dose optimization of apomorphine sublingual film for treating “OFF” episodes in Parkinson’s disease. Park Relat Disord 2021;93:27–30.
30. Picconi B, Hernández LF, Obeso JA, Calabresi P. Motor complications in Parkinson’s disease: Striatal molecular and electrophysiological mechanisms of dyskinesias. Mov Disord 2018;33:867–76.
31. Rekdal VM, Bess EN, Bisanz JE, Turnbaugh PJ, et al. Discovery and inhibition of an interspecies gut bacterial pathway for levodopa metabolism. Science 2019;364:eaau6323.
32. S3-Leitlinie Idiopathisches Parkinson-Syndrom. Stand: 1. Januar 2016 (Zugriff am 10.01.2022).
33. Schwab RS, Amador LV, Lettvin JY. Apomorphine in Parkinson’s disease. Trans Am Neurol Assoc 1951;56:251–3.
34. Storch A, Schneider CB, Wolz M, Stürwald Y, et al. Nonmotor fluctuations in Parkinson’s disease: severity and correlation with motor complications. Neurology 2013;80:800–9.
35. Suarez LM, Alberquilla S, García-Montes JR, Moratalla R. Differential synaptic remodeling by dopamine in direct and indirect striatal projection neurons in pitx3–/– mice, a genetic model of Parkinson’s disease. J Neurosci 2018;38:3619–30.
36. Tanimura A, Du Y, Kondapalli J, Wokosin DL, et al. Cholinergic interneurons amplify thalamostriatal excitation of striatal indirect pathway neurons in Parkinson’s disease models. Neuron 2019;101:444–58.e6.
37. Timpka J, Nitu B, Datieva V, Odin P, et al. Device-aided treatment strategies in advanced Parkinson’s disease. Int Rev Neurobiol 2017;132:453–74.
38. Weill E. De l’apomorphine dans certains troubles nerveux. Lyon Med 1884;48:411–9.
39. Yahr MD, Duvoisin RC, Schear MJ, Barrett RE, et al. Treatment of Parkinsonism with levodopa. Arch Neurol 1969;21:343–54.
Prof. Dr. med. Björn Falkenburger, Lennart Höfs, Klinik und Poliklinik für Neurologie, Universitätsklinikum Carl Gustav Carus an der Technischen Universität Dresden, Fetscherstraße 74, 01307 Dresden, E-Mail: bfalken@ukdd.de
Sublingual apomorphine: old friend in new clothes
Apomorphine is one of the oldest drugs used to treat the motor symptoms of Parkinson’s disease. Due to the low bioavailability and poor tolerability of oral administration, apomorphine has been injected subcutaneously.
In May 2020, a new sublingual application form was approved for the American market. In this overview we will present the effects of sublingual apomorphine, compare it with existing drugs and classify it in current therapy concepts.
Key words: Parkinson’s disease, motor fluctuations, dyskinesias, apomorphine sublingual
Psychopharmakotherapie 2022; 29(02):43-48
