Sara Bienentreu, Zülpich, Christoph U. Correll, Berlin, Beat Nick, Solothurn, Roland Vauth, Basel, und Dietmar Winkler, Wien
Sprechende Medizin, die das Arzt-Patienten-Gespräch als heilwirksamen Faktor nutzt, ist ein Hauptbestandteil einer psychiatrischen Behandlung. Dies gilt auch bei Patienten mit Schizophrenie. Gute Kommunikation ist ein wichtiger Faktor für den Therapieerfolg [44]. Die Qualität der Arzt-Patienten-Beziehung und der Kommunikation zwischen beiden sind wichtige Prädikatoren für die Adhärenz [65]. Allerdings gelingt die Kommunikation nicht immer gut: Beispielsweise sind in extremen Fällen Patienten überzeugt, gar nicht krank zu sein und keine Behandlung zu benötigen. In einer solchen Situation kann eine strukturierte Kommunikationsstrategie helfen, den Patienten trotzdem behandeln zu können [3]. Strukturierte Kommunikationstechniken können also bei der Behandlung einer Schizophrenie der Schlüssel zum Erfolg sein. Dies wird auch an weniger extremen Beispielen deutlich, wie etwa der kürzlich veröffentlichten Studie PRELAPSE, in der ein Teil der Behandler ein Kommunikationstraining erhielt. Unter anderem dank dieses Trainings konnten Patienten gut für die Studie rekrutiert werden und 91 % der Patienten im Interventionsarm konnten dafür gewonnen werden, mindestens eine Injektion mit einem Depot-Antipsychotikum auszuprobieren [36]. Infolgedessen kam es zu einer Reduktion der Krankenhausaufenthalte: 44 % weniger Patienten der Interventionsgruppe hatten einen Krankenhausaufenthalt innerhalb von zwei Jahren [37]. Es kann also für Behandler von Patienten mit Schizophrenie nützlich sein, sich strukturierte Kommunikationstechniken nochmals in Erinnerung zu rufen und die Evidenz für ihren Nutzen zu betrachten.
In letzter Zeit hat in der Arzt-Patienten-Beziehung eine Veränderung stattgefunden: Während es früher an der Tagesordnung war, dass der behandelnde Arzt dem Patienten Vorgaben machte, deren Einhaltung als Compliance bezeichnet wurde, wird nun vermehrt eine Beziehung auf Augenhöhe angestrebt, in welcher Entscheidungen bezüglich der Behandlung gemeinsam getroffen werden. Die Therapietreue des Patienten wird in einem solchen Szenario als Adhärenz bezeichnet [11, 12, 23, 53]. Um solche partnerschaftlichen Beziehungen zu ermöglichen, kommen nun auch vermehrt patientenzentrierte Kommunikationstechniken zum Einsatz.
Als hilfreiche, patientenzentrierte Kommunikationstechniken stehen unter anderem Motivational Interviewing (MI) und Shared-Decision-Making (SDM) zur Verfügung. Darüber hinaus sind Patienten, die über ihre Erkrankung und deren Behandlung Bescheid wissen, stärker zur Adhärenz motiviert [8]. Um Patienten mit Schizophrenie das nötige Wissen zu vermitteln, wurde die Psychoedukation entwickelt. Für diese drei Methoden wird hier ein Überblick über die zugrunde liegende Theorie, das praktische Vorgehen, den Einsatz bei Schizophrenie und die verfügbare Evidenz für die Indikation Schizophrenie gegeben.
Methode
Hier werden in einem fokussiert selektiven, narrativen Review die Psychoedukation, Motivational Interviewing (MI) und Shared-Decision-Making (SDM) und ihre Rolle in der Behandlung der Schizophrenie vorgestellt.
Psychoedukation
Methodik
Definition und Hintergrund
Psychoedukation kann zusammengefasst definiert werden als „psychotherapeutisch gestützte Fortbildung“, um die Patienten und ihre Angehörigen über die Krankheit zu informieren [7, 8]. Sie soll Erkrankte in die Lage versetzen, aktiv an ihrer Gesundung mitzuwirken (Empowerment). Um dies zu gewährleisten, soll Fachwissen über die Erkrankung für Laien verständlich vermittelt werden. Das Krankheitsverständnis soll gefördert und der Umgang mit der Krankheit verbessert werden.
Die Grundüberlegung hinter einer psychoedukativen Intervention ist, dass ein größeres Krankheitsverständnis zu mehr Krankheitseinsicht führen sollte und sich dadurch Therapieadhärenz und Coping verbessern [7, 8]. Patienten und auch Angehörige stehen häufig intuitiv einer medikamentösen Behandlung kritisch gegenüber oder lehnen diese sogar kategorisch ab. Wenn sie jedoch die Sinnhaftigkeit und Wirkungsmechanismen einer medikamentösen Behandlung verstanden haben, sind sie oft bereit, diese für sich anzunehmen. Dabei soll die Psychoedukation dazu dienen, die Symptomkontrolle durch die Medikation mit den internen Steuerungskräften des Patienten in Verbindung zu bringen und so zu verbesserten Behandlungsergebnissen (Outcomes) führen [7, 8]. Die Präsentation der Informationen soll übersichtlich und klar strukturiert sein, da viele Patienten unter neurokognitiven Problemen leiden.
Allerdings reicht eine alleinige „Belehrung“ über die Krankheitsursachen und das Rückfallrisiko ohne medikamentöse Behandlung nicht aus, um höhere Krankheitseinsicht zu erreichen. Entscheidend ist vielmehr, dass es gelingt, die vermittelten Sachinformationen mit den persönlichen Erfahrungen der Patienten zu verknüpfen [40]. Das Einbeziehen der Angehörigen ist dabei für den Erfolg der Intervention sehr wichtig [42].
Neuere Ansätze in der Psychoedukation legen einen zusätzlichen Fokus auf die Lebensqualität der Patienten [58] oder basieren auf Achtsamkeit [16, 17]. Unter Achtsamkeit wird eine Haltung verstanden, in der sich die Aufmerksamkeit auf die Gegenwart richtet und die wahrgenommenen Phänomene nicht gewertet werden. Durch diese Technik können die Patienten lernen, ihre Krankheit besser zu akzeptieren, weniger Disstress zu erleiden und bei Anzeichen eines Rückfalls überlegt zu reagieren und Hilfe zu suchen [16].
Ziele
Ziele einer Psychoedukation sind nach Bäuml und Pitschel-Walz [7, 8]:
- Informierten, selbstverantwortlichen Umgang mit der Erkrankung ermöglichen
- „Expertenrolle“ der Patienten vertiefen, umfangreiches Krankheitskonzept entwickeln
- „Co-Therapeuten“-Funktion der Angehörigen stärken
- Professionelle Therapieverfahren mit Selbsthilfestrategien verbinden
- Krankheitseinsicht und Adhärenz verbessern
- Rezidivprophylaxe fördern, Sensibilität für Wiederauftreten von Symptomen schaffen
- Gesundung unterstützen
- Verständnis und Akzeptanz für Medikation schaffen, Einschätzung von Wirkung und Nebenwirkung ermöglichen
- Coping, konstruktive Haltung gegenüber psychotischem Erleben und Einordnung der Krankheit ins Leben fördern [46]
- Problemlöse- und Kommunikationsfertigkeiten innerhalb der Familie verbessern [8, 34]
- Stress reduzieren, der durch negative oder übermäßig emotionale Kommunikation (high-expressed emotions) innerhalb der Familie ausgelöst werden kann [9, 42]
- Soziales Netzwerk ausbauen (durch Gruppentherapie, Gruppen-Familienintervention) [42]
Praktische Durchführung
Wichtige Punkte zur Praxis [7, 8]:
Mit den Patienten wird ein Krankheitskonzept der Schizophrenie auf Basis des Vulnerabilitäts-Stress-Bewältigungs-Modells erarbeitet. Dabei werden die Mechanismen der Krankheit und der Therapie an die Sichtweise der Patienten und Angehörigen angepasst und sehr anschaulich dargestellt. Beiträge der Patienten sollen genutzt werden, um die Anschaulichkeit zu fördern. Es sollen außerdem Hoffnung und Zuversicht vermittelt werden, um die Patienten emotional zu unterstützen. Über die Vor- und Nachteile verfügbarer Behandlungsmethoden soll offen berichtet werden. Die Betonung liegt auf dem Selbsthilfepotenzial des Patienten. Auch die Angehörigen sollen mit einbezogen werden, da sie positiven Einfluss auf den Krankheitsverlauf nehmen können. Dazu finden Angehörigengruppen statt, üblicherweise abends und getrennt von den Gruppensitzungen der Patienten (bifokaler Ansatz). Angehörige können in ihren Sitzungen nicht nur Informationen über die Erkrankung erhalten, sondern auch Kommunikationskompetenzen trainieren, um negative Kommunikationsspiralen zu verhindern, und systematisches Problemlösen einüben.
Die Gruppenleiter sollten den Teilnehmern stets unbedingte Wertschätzung entgegenbringen und empathisch auf sie eingehen. Die Informationen über die Erkrankung sollen immer mit emotionaler Entlastung kombiniert werden, denn sonst könnten sie als Zumutung und Kränkung erfahren werden oder ein übermäßiges Gefühl der Hilflosigkeit und des Ausgeliefertseins auslösen. Zu Beginn und Ende der Sitzung sollen sich die Patienten kurz zu ihrer Befindlichkeit äußern, damit aktuelle Krisen erkannt werden können – denn diese können auch durch das vermittelte Wissen oder dessen Umsetzung ausgelöst werden. Während psychoedukativer Interventionen können insbesondere depressive Symptome und Suizidalität steigen, wenn biologische Faktoren, wie etwa der genetische Einfluss, von den Patienten als deterministisch erlebt werden [40]. Diese möglichen Prozesse sollten immer mit bedacht werden, damit bei einem Verdacht auf Suizidalität schnell und adäquat reagiert werden kann.
Zentrale Themen
Die Inhalte umfassen zwei Hauptbereiche, nämlich Information und emotionale Entlastung (Abb. 1) [7, 8].
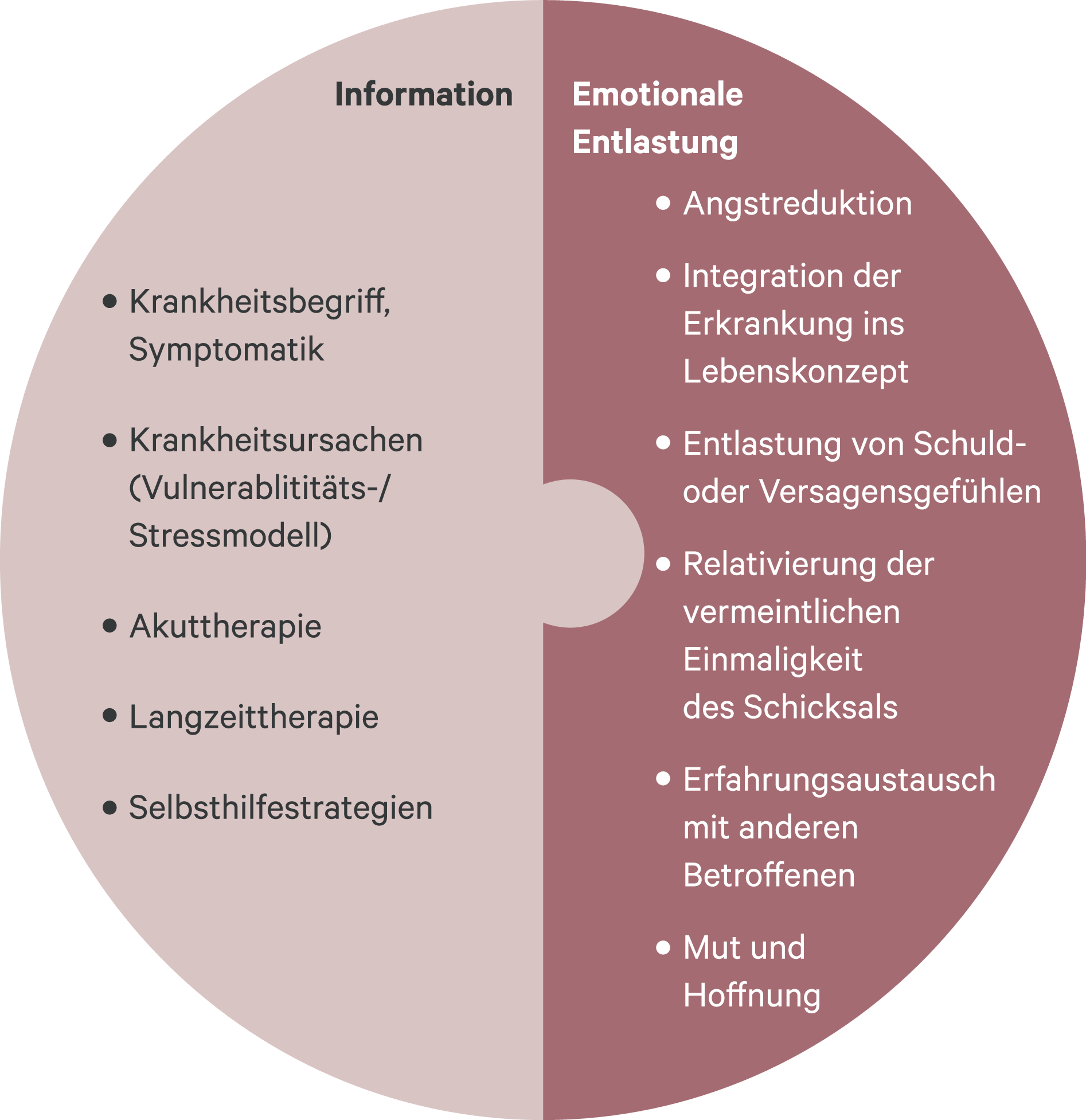
Abb. 1. Inhalte der Psychoedukation
Einsatz bei Schizophrenie
In der S3-Leitlinie der DGPPN [20] heißt es:
„Menschen mit Schizophrenie soll zur Verbesserung des Behandlungsergebnisses und Krankheitsverlaufs eine strukturierte Psychoedukation im Rahmen eines Gesamtbehandlungsplans ausreichend lange und möglichst in Gruppen angeboten werden. Angehörige und andere Vertrauenspersonen sollen in die psychoedukative Intervention einbezogen werden.“
Empfehlungsgrad A (Bezug auf [66]).
Ein Überblick über verschiedene Therapiemanuale für Schizophrenie findet sich bei Bäuml und Pitschel-Walz [8]. Es sind Manuale für Schizophrenie oder für die Doppeldiagnose Schizophrenie und Sucht verfügbar.
Evidenz bei Schizophrenie
Ein Cochrane-Review zu Psychoedukation bei Schizophrenie von 2011 [66] analysierte Daten von 5142 Patienten, die meisten davon stationär, aus 44 Studien mit insgesamt moderatem Verzerrungsrisiko. Unter Psychoedukation war die Inzidenz von Nonadhärenz geringer als in Vergleichsgruppen (n = 1400; Risk-Ratio [RR] 0,52; Konfidenzintervall [KI] 0,40–0,67; Number needed to treat [NNT] 11; KI 9–16; kurze Nachbeobachtung). Dieses Ergebnis konnte auch für mittlere und lange Nachbeobachtungszeiträume bestätigt werden. Unter Psychoedukation kam es deutlich seltener zu Rückfällen (n = 1214; RR 0,70; KI 0,61–0,81; NNT 9; KI 7–14) und Rehospitalisierungen (n = 206; RR 0,71; KI 0,56–0,89; NNT 5; KI 4–13).
Ein anderer Cochrane-Review zu kurzer Psychoedukation (bis zu zehn Sitzungen) aus dem Jahr 2015 [67] umfasste 20 randomisierte kontrollierte Studien (RCT) mit 2337 Patienten mit Schizophrenie oder schizoaffektiver Störung. Patienten, die Psychoedukation erhielten, zeigten verringerte Nonadhärenz bei kurzfristigem (n = 448; 3 RCTs; RR 0,63; KI 0,41–0,96; moderate Qualität der Evidenz) und mittelfristigem Follow-up (n = 118; 1 RCT; RR 0,17; KI 0,05–0,54; geringe Qualität der Evidenz). Rückfallraten waren mittelfristig signifikant gesenkt (n = 406; RR 0,70; KI 0,52–0,93; moderate Qualität der Evidenz), jedoch nicht langfristig. Daten aus einzelnen RCTs wiesen darauf hin, dass eine kurze Psychoedukation außerdem den Globalzustand langfristig verbessern, den mentalen Zustand kurz- und mittelfristig verbessern und zu weniger Angst und Depression führen kann. Außerdem war die soziale Funktion unter kurzer Psychoedukation verbessert. Die Lebensqualität und die Mortalität waren zwischen Psychoedukations- und Kontrollgruppen nicht verschieden.
McDonagh und Kollegen [41] zitieren einen systematischen Review von hoher Qualität, der zehn Studien mit insgesamt 1125 Patienten umfasst. Demzufolge verbesserte Psychoedukation gegenüber Standardbehandlung die Outcomes für Kernsymptome der Schizophrenie, Funktionalität und Rückfälle. Ein Review von drei Studien kommt zu dem Ergebnis, dass Psychoedukation einen positiven Effekt auf die globale Funktion der Patienten (gemessen an der Global Assessment of Functioning Scale oder Global Assessment Scale) nach einem Jahr hat (Mittelwertsdifferenz –5,23; 95%-KI –8,76 bis –1,71; geringe Qualität der Evidenz). Psychoedukation wirkte sich nach einem systematischen Review von sechs Studien positiv auf die Rückfallraten zu neun und 18 Monaten aus (RR 0,80; 95%-KI 0,70–0,92; moderate Qualität der Evidenz).
Psychoedukation in Form einer Familienintervention gehört zu den erfolgreichsten Interventionen, mit einer Reduktion der Rückfälle und Hospitalisierungen innerhalb zwei Jahren Beobachtungszeit um 20 bis 50 % [42].
Um wirksam zu sein, müssen Familieninterventionen mindestens sechs Monate dauern und Problemlösefähigkeiten, Coping, Kommunikationsfähigkeiten und eine Ausweitung der sozialen Netzwerke (durch andere betroffene Familien) zum Inhalt haben.
Besonders effektiv sind sie, wenn sie möglichst früh im Krankheitsverlauf stattfinden [42].
Fazit zur Psychoedukation
Die verfügbare Evidenz stützt den Einsatz von Psychoedukation bei Schizophrenie, und eine Psychoedukation sollte allen Patienten mit Schizophrenie angeboten werden [20].
Motivational Interviewing
Methodik
Ursprünglich wurde Motivational Interviewing (MI) zum Einsatz bei Suchterkrankungen entwickelt [52]. Diese Gesprächstechnik kann aber bei allen chronischen Erkrankungen eingesetzt werden, um Therapieadhärenz zu fördern [68]. Beim MI geht man von einer sehr häufig bestehenden, natürlichen Ambivalenz beim Patienten gegenüber der Behandlungsbereitschaft aus. Seine Motivation zu Verhaltensänderungen in Richtung vermehrter Behandlungsbereitschaft und zuverlässiger Einnahme der Medikation wird im partnerschaftlichen, patientenzentrierten Dialog aktiviert und unterstützt. Dabei werden die vorhandenen Ambivalenzen bearbeitet und aufgelöst, sodass es dem Patienten leichter fällt, sich zur Verhaltensänderung zu motivieren [52].
Zunächst werden dem Patienten durch eine Verhaltensanalyse dysfunktionale Verhaltensweisen (z. B. Substanzmissbrauch, unregelmäßige Medikamenteneinnahme) und ihre Konsequenzen bewusst gemacht [52]. Dabei sollen alle Argumente vom Patienten kommen. Der Therapeut unterstützt diesen Prozess durch offene Fragen und Reflexion. Für diesen Prozess der Evokation ist Geduld nötig.
Die Äußerungen des Patienten können dabei Änderungssequenzen („change talk“) oder Widerstandssequenzen („sustain talk“) zugeordnet werden. „Change talk“ bedeutet, dass der Patient zu einer Veränderung seines Verhaltens motiviert ist. „Sustain talk“ hingegen bedeutet, dass der Patient sein derzeitiges Verhalten nicht ändern möchte. Ziel des Therapeuten ist es, den Patienten anzuleiten, etwaige Widersprüche, sogenannte kognitive Dissonanzen, zwischen seinem momentanen Verhalten (z. B. Medikations-Nonadhärenz, Substanzmissbrauch) und wichtigen Zielen (z. B. Vermeidung von Rückfällen, Krankenhausaufenthalten) zu erkennen. Der Patient muss dabei diese Widersprüche selbst wahrnehmen und sich stets frei für oder gegen ein Verhalten entscheiden können. Die Erfahrung dieser Widersprüche soll den Patienten dazu motivieren, sein Verhalten anzupassen, um seine Ziele erfolgreicher erreichen zu können. Der Therapeut erarbeitet dann mit dem Patienten konkrete Verhaltensänderungen und bestärkt ihn in seiner Selbstverpflichtung, damit diese auch umgesetzt werden.
Ablauf
MI besteht aus vier sich überlappenden Prozessen: Beziehungsaufbau, Fokussierung, Evokation, und Planung (Abb. 2) [44]. Dabei kann sich das Gespräch jederzeit auf allen Stufen vor- oder zurückbewegen, eine feste Reihenfolge gibt es nicht.
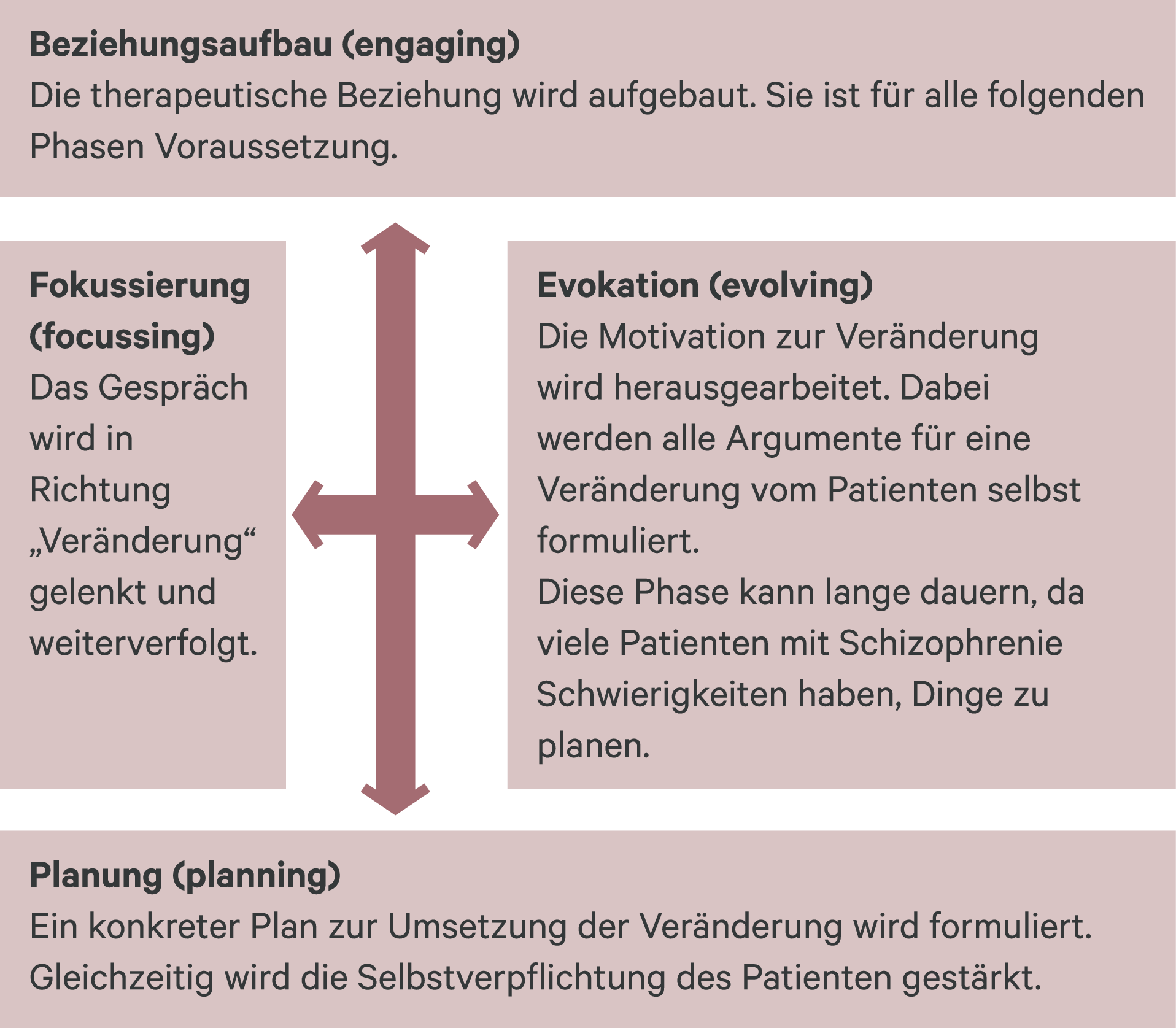
Abb. 2. Prozesse des Motivational Interviewing
Haltung des Therapeuten
Nach [52] ist für die Haltung des Therapeuten bei MI wesentlich:
- Kooperation: Der Dialog mit dem Patienten ist partnerschaftlich und nicht bevormundend. Beide Parteien sind auf gleicher Augenhöhe.
- Patientenzentrierung: Die Sichtweisen, Werte und Ziele des Patienten stehen im Mittelpunkt. Seine Motivation soll aktiviert und gestärkt werden. Belehrungen sind fehl am Platz.
- Autonomie: Der Patient entscheidet und handelt selbstbestimmt. Eine Änderung seines Verhaltens kann nicht erzwungen oder angeordnet werden.
- Anteilnahme: Der Behandler soll ein selbstloses Interesse daran haben, dass es dem Patienten gut geht. Er sollte dem Patienten nicht gleichgültig gegenüberstehen oder eigene Vorstellungen (z. B. Nutzenmaximierung) vom Ziel der Therapie haben.
- Gesprächstechniken: Der Behandler leitet das Gespräch mit offenen Fragen, Affirmationen, und Reflexion (direkte Wiederholung dessen, was gesagt wurde, oder Verbindung von sustain talk und change talk, Zusammenfassungen).
Einsatz bei Schizophrenie
Ambivalenz kommt bei Patienten mit Schizophrenie häufig vor [52]. Durch verflachten Affekt kommt es zudem häufig zu einem generellen Mangel an Motivation [52]. Der Einsatz von MI bietet sich an, um die Ambivalenzen aufzulösen und die Motivation zu steigern.
Da MI zunächst für Suchterkrankungen entwickelt wurde, kommt es derzeit meist bei der Doppeldiagnose Schizophrenie und Substanzgebrauchsstörung zum Einsatz.
In der S3-Leitlinie der DGPPN wird MI nur erwähnt im Zusammenhang mit beruflicher Rehabilitation, und zwar als Add-on zu unterstützter Integration in den allgemeinen Arbeitsmarkt („supported employment“) [20].
Evidenz bei Schizophrenie
Reimer und Kollegen [52] kommen in ihrem Review anhand der derzeit verfügbaren Studien zu dem Schluss, dass MI wichtige Parameter des Krankheitsverlaufs wie die Medikamentenadhärenz, die Häufigkeit und Schwere psychotischer Exazerbationen, die Hospitalisierungsdauer, das Funktionsniveau, die Krankheitseinsicht sowie die kognitive Rehabilitation positiv beeinflussen kann. Allerdings sind die Studien wenig einheitlich und weisen nicht durchweg positive Resultate auf. Dazu kommt eine Reihe forschungsmethodischer Mängel, etwa, dass häufig nur wenige Patienten rekrutiert wurden, die Beobachtungsdauer stark unterschiedlich war und oft Patienten mit Doppeldiagnose mit unterschiedlichen Formen von komorbidem Substanzkonsum eingeschlossen wurden, was die Qualität der Evidenz beeinträchtigt.
Eine Metaanalyse zu Motivational Interviewing bei chronischen Erkrankungen (Epilepsie, chronische Nierenerkrankung, Diabetes mellitus, HIV/AIDS, Bluthochdruck, Schizophrenie, Osteoporose und psychotische Störung) kommt basierend auf 16 RCTs auf eine Effektstärke von 0,12 (95%-KI 0,05–0,20) für MI in Bezug auf die Medikamentenadhärenz [68].
Ein Review aus dem Jahr 2015 zum Einfluss vom MI auf die Medikamentenadhärenz bei Schizophrenie [64] umfasste sechs relevante Studien. Davon wurde nur in einer ein direkter Zusammenhang zwischen MI und Medikamentenadhärenz gefunden, die übrigen Studien unterstützten einen solchen Zusammenhang nicht. Allerdings wurden Hinweise auf Zusammenhänge zwischen MI und Verbesserungen bei anderen Outcomes gefunden, wie etwa psychotische Symptomatik oder Rehospitalisierungen.
Fazit zu MI
Zwar wurden im mehreren Studien positive Effekte für MI gefunden, jedoch ist insgesamt die Studienlage zu MI bei Schizophrenie noch heterogen und mehr Evidenz ist für eine uneingeschränkte Empfehlung nötig. MI kann zur Unterstützung anderer Therapieverfahren und Kommunikationstechniken eingesetzt werden.
Shared-Decision-Making
Methodik
Beim Shared-Decision-Making (SDM) arbeiten Patient und Arzt zusammen, um gemeinsam Entscheidungen zur Behandlung gesundheitlicher Probleme zu finden [1].
Zugrunde liegende Theorie
Sowohl der Arzt wie auch der Patient verfügen über Informationen, die für eine Behandlungsentscheidung relevant sind: Der Arzt verfügt über Fachwissen hinsichtlich der Diagnose, des Krankheitsverlaufs, Einflussgrößen, Behandlungsoptionen und deren Wirksamkeit und Sicherheit; der Patient trägt mit seinen persönlichen Werten, Behandlungszielen, Behandlungsvorerfahrung und seinen Präferenzen bezüglich Behandlung und Medikation, Unterkunft, Rehabilitierung, Bildung, Arbeit und Selbstpflege dazu bei [1].
Im Entscheidungsmodell des SDM betrachten Arzt und Patient die verfügbare Information zu Chancen und Risiken verschiedener Behandlungsoptionen, was auch Abwarten und Beobachten miteinschließt, und diskutieren diese. Dann wird der Patient ermuntert, eine informierte Entscheidung zu treffen und dafür möglichst viel Verantwortung zu übernehmen. Beim SDM ist der Arzt ein Berater des Patienten, der Information zu Verfügung stellt, verschiedene Behandlungsoptionen diskutiert, bei der Klärung von Werten und Zielen hilft, und die Autonomie des Patienten unterstützt [1].
SDM soll zur Verbesserung der Arzt-Patienten-Beziehung, Therapieadhärenz, Zufriedenheit mit der Therapie und biomedizinischen Outcomes führen. Vor allem bei chronischen Erkrankungen hat der Patient notwendigerweise die Verantwortung für seine tägliche Behandlung, da etwa Medikation eingenommen werden muss. SDM kann auch als ethischer Imperativ angesehen werden [21].
Präferenzen von Patienten bezüglich Entscheidungen
Fast alle Patienten wünschen sich, so gut wie möglich über ihre Erkrankung informiert zu werden [1]. Dabei scheint allerdings der Wert der Information aus Patientenperspektive nicht allein darin zu liegen, dass sie bei Behandlungsentscheidungen eine Rolle spielt: vielmehr könnte es die verringerte Unsicherheit und psychologische Bestärkung sein, die Information in Anbetracht der Belastung durch eine Diagnose geben kann [15]. Das Gefühl, dass ein vertrauenswürdiger und sachkundiger Arzt die Dinge in die Hand nimmt, scheint vielen Patienten zu helfen und ihre Ängste zu reduzieren.
Die Präferenzen hinsichtlich der Beteiligung an medizinischen Entscheidungen hingegen schwanken stark zwischen verschiedenen Patienten und auch Krankheitsbildern: Es gibt Patienten, die allein eine Entscheidung treffen möchten und den Arzt nur als Informationsvermittler ansehen; andere wollen als gleichberechtigte Partner im Dialog mit dem Arzt zu einem Konsens kommen; andere wiederum geben gern die Verantwortung für eine Entscheidung komplett an den Arzt ab [1, 19]. Insbesondere in akuten Krankheitsphasen berichten viele Patienten, dass sie sich nicht dazu in der Lage fühlen, sich an Entscheidungen zu beteiligen [33].
Für Patienten sind oft Funktion und Lebensqualität wichtiger als die Abwesenheit von Symptomen [48, 57], weshalb davon ausgegangen wird, dass beim SDM diese Parameter stark in den Fokus rücken.
Oft wird übersehen, dass außer Patient und Arzt noch weitere Personen (Angehörige, Freunde) an Entscheidungen beteiligt sein können [15].
Kontroverse zum Shared-Decision-Making
Mögliche Nachteile, die eine Entscheidungsbeteiligung des Patienten haben könnte [1]:
- Zu viele Entscheidungsmöglichkeiten können Patienten überfordern
- Eine bestimmte Entscheidung kann das Gefühl erzeugen, weitere Möglichkeiten verpasst zu haben
- Patienten könnten ihre Entscheidungen bereuen oder Entscheidungsmöglichkeiten ablehnen, um spätere Reue zu vermeiden
- Es könnte schwierig für Patienten sein, verschiedene Outcomes zu bewerten, weil sie nicht einschätzen können, wie stark der Krankheitsverlauf eventuell ihre Entwicklungsmöglichkeiten einschränken kann
- Die Kontrolle über Entscheidungen kann zu einer gesteigerten Erwartungshaltung führen, die unter Umständen später enttäuscht wird
Die Zielsetzung bei der Implementierung eines SDM-Ansatzes ist zunächst unklar: Sollen alle Patienten mehr Entscheidungen selbst treffen, oder soll für jeden Patienten ermöglicht werden, dass er die für ihn bevorzugte Rolle beim Entscheiden einnimmt (also unter Umständen auch eine völlig passive Rolle) [1]?
Der Patient kann auch schlechte Entscheidungen treffen, dies soll akzeptiert werden. Allerdings wird bei fehlender Krankheitseinsicht vom Patienten oft gar keine Interaktion mit dem Arzt gewünscht [1].
Speziell bei psychiatrischen Erkrankungen kommt erschwerend hinzu, dass Entscheidungen oft nicht zu einem vorher festgelegten Zeitpunkt getroffen werden, sondern ständig während der Behandlung [33].
Die Kommunikationsfähigkeiten des Patienten sind wichtig, um sich an Entscheidungen beteiligen zu können. Allerdings sind bei manchen Patienten mit depressiven Symptomen, starker Negativsymptomatik oder kognitiven Defiziten die kommunikativen Fähigkeiten deutlich eingeschränkt [33].
Vorgehensweise
Die Standard-Vorgehensweise umfasst neun Schritte (Abb. 3) [40].

Abb. 3. Vorgehen bei Shared-Decision-Making
Interventionen zur Förderung von SDM
Zur Förderung von SDM stehen als Ansätze zur Verfügung [1]:
- Kommunikationstraining für Ärzte
- Kommunikationstraining für Patienten
- Entscheidungshilfen (z. B. Broschüren mit Information)
- Apps (z. B. Stimmungstagebuch, Tracker für Medikamenteneinnahme)
Kommunikationstraining für Ärzte dient der Verbesserung der verbalen und nonverbalen Fähigkeiten, mit dem Ziel die therapeutische Allianz zu verbessern, Patienten vermehrt zu Nachfragen aufzufordern, und diese adäquat zu beantworten. Die Vor- und Nachteile einer Entscheidung können oft so dargestellt werden, dass sie nicht stigmatisierend wirken und der Patient ermutigt wird, sich gemeinsam mit dem Arzt mit der Entscheidung auseinanderzusetzen. Für jedes Argument, das gegen eine bestimmte Handlungsoption spricht, sollte über Kommunikationsstrategien nachgedacht werden, die diese Option weniger bedrohlich erscheinen lassen [1].
Kommunikationstraining für Patienten soll Hemmungen abbauen, damit der Patient mehr Fragen stellt, seine Meinung einbringt, und Bedenken äußert. Einfache Strategien, beispielsweise das Erstellen einer Liste mit Fragen vor dem Gespräch, können sehr effektiv sein [1].
Entscheidungshilfen sind Material, das strukturiert verdeutlicht, welche Entscheidungen getroffen werden müssen und welche häufigen Fragen dazu auftauchen können. Entscheidungshilfen können beispielsweise Broschüren oder Internetseiten sein. In der somatischen Medizin sind die positiven Effekte von Entscheidungshilfen gut belegt [59].
Ein neuer Ansatz sind Gesundheits-Apps. Diese könnten beispielsweise genutzt werden, um Behandlungsinformationen zu vermitteln und individuelle Risiken zu berechnen [61] oder bei der Dokumentation der Medikamenteneinnahme [2] und des Auftretens von Symptomen und Nebenwirkungen helfen (Stimmungstagebücher) [49] und so Grundlage für ein Arzt-Patienten-Gespräch und weitere Entscheidungen sein.
Einsatz bei Schizophrenie
In der S3-Leitlinie der DGPPN heißt es [20]:
„Ziel ist die aktive Teilnahme am therapeutischen Entscheidungsprozess des über Wirkungen und Nebenwirkungen aufgeklärten Patienten als gleichberechtigten Partner (partizipative Entscheidungsfindung/Shared-Decision-Making). […] Überlegungen zum Einsatz eines bestimmten Präparats oder einer psychotherapeutischen, sowie psychosozialen Therapieform und die damit verbundene Risiko-Nutzen-Evaluation müssen den Betroffenen so erklärt werden, dass eine partizipative Entscheidungsfindung möglich wird. […] Shared-Decision-Making soll dabei nicht nur krankheitsbezogene Endpunkte (wie Remission, Rezidivprophylaxe) verbessern, sondern die therapeutischen Entscheidungen des Shared-Decision-Makings sollen als patientenrelevanter Endpunkt an sich betrachtet werden. […] In jedem Fall ist es hilfreich, die Angehörigen und andere Vertrauenspersonen unter Einverständnis des Betroffenen in Therapieentscheidungen mit einzubeziehen. […] Die partizipative Entscheidungsfindung muss dabei mehr in der Regelversorgung verankert werden. […] Die Grenzen der partizipativen Entscheidungsfindung liegen in Situationen, in denen Patienten aufgrund der Schwere der Erkrankung in ihrer Einwilligungsfähigkeit eingeschränkt sind oder sich durch den Prozess überfordert fühlen […]; bei Menschen mit einer Schizophrenie sind dies beispielsweise Notfallsituationen (z. B. Erregungszustände, katatone Zustände), Episoden mit schwerem Wahn oder Halluzinationen oder Episoden mit schweren formalen Denkstörungen. In solchen Fällen kann nach Stabilisierung des akuten Zustandsbildes die partizipative Entscheidungsfindung jedoch für den weiteren Behandlungsverlauf eingeleitet werden.
[…]
Empfehlung: Zu Beginn einer Pharmakotherapie soll eine Aufklärung des Patienten über die akuten und langfristigen Wirkungen sowie Nebenwirkungen (Risiko-Nutzen-Evaluation) der Medikamente erfolgen und der Patient soll aktiv in den therapeutischen Entscheidungsprozess (partizipative Entscheidungsfindung/Shared-Decision-Making […]) einbezogen werden. Vor- und Nachteile der Behandlung und mögliche Alternativen sollen in einer verständlichen Sprache mit Erläuterung der Fachbegriffe erfolgen. Empfehlungsgrad: KKP [klinischer Konsenspunkt]“
Shared-Decision-Making ist jedoch in der Schizophrenie-Therapie kaum implementiert, die Patienten fühlen sich meist nicht in die Entscheidungen einbezogen [33]. Insbesondere die Wahl eines Antipsychotikums und seiner Formulierung wird meist von den Ärzten allein getroffen [51].
Die häufigsten Hindernisse, die den Einsatz von Shared-Decision-Making verhindern, sind [33]:
- Der vermutete höhere Zeitaufwand
- Die Ansicht, dass SDM bereits praktiziert werde
- Die Meinung, dass SDM von den Patienten gar nicht gewünscht sei
- Die Ansicht, SDM sei ungeeignet für akut psychotische Patienten und Patienten ohne Krankheitseinsicht
- Die Annahme, zu wenig Nachdruck bei der Diskussion der Pharmakotherapie könnte Patienten dazu verleiten, kein Medikament einzunehmen
Evidenz bei Schizophrenie
Generelle Forschungsergebnisse zu SDM
Der größte Teil der Evidenz zu SDM stammt aus der somatischen Medizin [33]. Dabei sind drei grundsätzliche Erkenntnisse [1]:
- Patienten wollen über ihren Gesundheitszustand und ihre Behandlung gut informiert werden
- Patienten wünschen sich einen Arzt, zu dem sie eine vertrauensvolle Beziehung aufbauen können
- Patienten haben unterschiedliche Präferenzen bezüglich ihrer Rolle in der Entscheidungsfindung (das Spektrum reicht von alleiniger Entscheidung des Patienten bis zur völligen Passivität des Patienten)
Patienten, die eine aktivere Rolle bevorzugen, sind tendenziell jünger, gebildeter, und gesünder [10]. Patienten mit schwerwiegenden und chronischen Erkrankungen hingegen tendieren dazu, eine passive Rolle vorzuziehen.
Verschiedene Studien haben gezeigt, dass patientenzentrierte Kommunikation (unterschiedlicher Definition) mit verringertem Disstress und verbesserter Funktionalität assoziiert ist [39, 43, 54]. Dabei sind die spezifischen Verhaltensweisen des Arztes, die mit solchen Outcomes assoziiert sind:
- Mehr Fragen stellen, um die Probleme, Erwartungen und Ansichten des Patienten zu verstehen
- Den Patienten ermutigen, mehr Fragen zu stellen
- Informationen klar und deutlich vermitteln
- Unterstützung und Empathie zeigen
- Den Patienten an Entscheidungen beteiligen
Obwohl retrospektive Studien zu dem Ergebnis kommen, dass Patienten, die ihre bevorzugte Rolle bei der Entscheidungsfindung einnehmen können, zufriedener sind [38], haben die wenigen Studien, die versucht haben, prospektiv die Patientenrolle zu beeinflussen, hinsichtlich Zufriedenheit, Adhärenz, und Krankheitsverläufen gemischte Ergebnisse erbracht [4–6]. Sogar unter standardisierten Bedingungen mit dem immer gleichen Behandler unterscheidet sich die Wahrnehmung des Patienten, wie viel Einfluss er hat, deutlich. Experimente, die die Kontrolle des Patienten steigern sollen, führen nicht dazu, dass der Patient auch einen subjektiven Eindruck von mehr Kontrolle hat [5, 24]. Obwohl also der Eindruck des Patienten, Einfluss nehmen zu können, mit positiven Outcomes assoziiert ist, scheint dieser Eindruck eher vom Patienten selbst als vom Arzt-Patienten-Gespräch abzuhängen und schwer beeinflussbar zu sein.
Dementsprechend sind Interventionen für Ärzte auch weniger erfolgreich als Interventionen für Patienten [1]. Die Nutzung von Entscheidungshilfen führt bei Patienten zu besserem Wissensstand, höherer Akzeptanz von Behandlungsverfahren, und besserer Zufriedenheit [33]. Fühlt sich der Patient in Entscheidungen einbezogen, so führt dies tendenziell zu besserem Verständnis, höherer Zufriedenheit, und mehr Vertrauen [56].
Shared-Decision-Making bei Schizophrenie
Auch Patienten mit schweren psychiatrischen Erkrankungen wie Schizophrenie sind grundsätzlich in der Lage, Entscheidungen bezüglich ihrer Behandlung zu treffen [13, 25], selbst bei akuter Erkrankung und nach unfreiwilliger Einweisung [28]. Allerdings ist SDM bei akuten Psychosen ohne Krankheitseinsicht schwer einzusetzen – hier sollten besser speziell an diese Situation angepasste Gesprächsverfahren angewandt werden [3]. Bei der Planung einer Langzeitbehandlung, insbesondere mit Depot-Antipsychotika, kann und soll der Patient hingegen stärker einbezogen werden. Der Einsatz von SDM ist also von der individuellen Psychopathologie und dem Krankheitsstadium des Patienten abhängig.
In der Psychiatrie sind die Kommunikationsfähigkeiten des Arztes mit erhöhter Patientenzufriedenheit, Adhärenz, und besseren Outcomes assoziiert [18]. Bei Patienten mit Schizophrenie sind deren Bewertungen der Arzt-Patienten-Beziehung mit Adhärenz und erhöhter Funktionalität vergesellschaftet [22].
Eine randomisierte kontrollierte Pilotstudie mit 61 stationär behandelten Patienten mit Schizophrenie untersuchte die Effekte eines SDM-Trainings für die Patienten [31]. Die Patienten waren anschließend motivierter, sich an Entscheidungen zu beteiligen und Verantwortung für ihre Behandlung zu tragen. Die behandelnden Psychiater nahmen diese Patienten als schwieriger zu behandeln wahr, wohl weil Behandlungsentscheidungen öfter hinterfragt wurden. Die Patienten gaben an, nach dem SDM-Training adhärenter gegenüber ihrer Medikation zu sein, die behandelnden Psychiater bestätigten dies jedoch nicht.
In einer randomisierten kontrollierten Studie mit 107 stationären Patienten mit Schizophrenie wurde ein SDM-Programm mit Standardbehandlung verglichen [30]. Patienten in der Interventionsgruppe wussten besser über ihre Erkrankung Bescheid (p = 0,01) und fühlten sich stärker in medizinische Entscheidungen eingebunden (p = 0,03). Mehr Patienten in der Interventionsgruppe nahmen später an einer Psychoedukation teil (p = 0,003). Allerdings wurden keine Unterschiede zwischen den Gruppen in Bezug auf Adhärenz und Rehospitalisierungen gefunden [27].
Eine andere RCT mit 264 stationär behandelten Patienten mit Schizophrenie an vier deutschen Behandlungszentren verglich ein SDM-Training für die Patienten in fünf Sitzungen mit unspezifischen Gruppensitzungen [32]. Das SDM-Training umfasste Aspekte der Motivation (Aussichten der Beteiligung an Entscheidungen, Patientenrechte) und des Verhaltens (z. B. Rollenspiele, Fragen stellen, Feedback geben). Der primäre Endpunkt war die Therapieadhärenz sechs und zwölf Monate nach der Entlassung. Hier wurden keine Unterschiede zwischen den Gruppen festgestellt. Allerdings beteiligten sich die Patienten der SDM-Gruppe stärker, wollten mehr Verantwortung für medizinische Entscheidungen übernehmen und änderten ihr Verhalten gegenüber ihren Behandlern.
Stein et al. prüften den Einsatz einer digitalen Entscheidungshilfe, die bei 1122 ambulant behandelten Patienten unter psychotroper Medikation vor einem Arztbesuch eingesetzt wurde [60]. Sie sollte den Patienten zu einer stärkeren Beteiligung bei der Behandlungsentscheidung verhelfen. Primärer Endpunkt war die Adhärenz zur Medikation. Es wurde in den 180 Tagen nach dem Arztbesuch jedoch kein Einfluss auf die Adhärenz gefunden.
Ein anderes internetbasiertes Informations- und Entscheidungshilfe-Tool wurde an 250 Patienten mit psychotischen Erkrankungen getestet [63]. Nur 73 Patienten schlossen die Studie ab, und es wurde kein Einfluss des Tools auf die vom Patienten wahrgenommene Beteiligung an Behandlungsentscheidungen gefunden.
Vermutlich sind komplexe Interventionen nötig, um eine spürbare Verbesserung der Arzt-Patienten-Interaktion zu erreichen [33]. SDM könnte in solche komplexeren Interventionen eingebunden werden.
So prüften Pickett und Kollegen das Programm BRIDGES (Building recovery of individual dreams and goals), einen achtwöchigen Kurs für Patienten mit psychiatrischen Erkrankungen, der von ehemaligen Patienten geleitet wird und die Fähigkeit stärken soll, aktiv an der eigenen Behandlung mitzuwirken [50]. Dabei werden Elemente der Psychoedukation mit einer Anleitung zur „Selbstfürsprache“ („self-advocacy“) verbunden, die beim Arzt-Patienten-Gespräch helfen soll, die bevorzugten Behandlungsmethoden zu diskutieren. 428 Patienten mit psychiatrischen Erkrankungen, davon 15,4 % mit Schizophrenie, wurden auf eine Behandlung mit BRIDGES oder eine Warteliste randomisiert. Patienten fühlten sich nach BRIDGES stärker befähigt, die eigene Behandlung mit zu gestalten, und berichteten ein größeres Selbstvertrauen und besseres Durchsetzungsvermögen für ihre Belange. Leider wurden weitere interessante Parameter, wie die Nutzung von Behandlungsmöglichkeiten oder die Adhärenz, nicht erfasst.
Ein anderes umfassendes Programm ist „SDM-PLUS“ [29], welches für die Patienten Training und Infomaterial und für das Personal Training in Techniken des SDM, Motivational Interviewing, und Verhandlungstechniken aus dem Harvard-Modell umfasst. Mit „SDM-PLUS“ behandelte Patienten fühlten sich stärker in Behandlungsentscheidungen bezüglich ihrer Medikation einbezogen (p = 0,002) und wiesen während ihres Klinikaufenthalts eine stärkere therapeutische Allianz, Behandlungszufriedenheit und eigenberichtete Medikamentenadhärenz auf [28]. Allerdings waren nach sechs und zwölf Monaten keine signifikanten Unterschiede bei Adhärenz und Rehospitalisierungen im Vergleich zur Kontrollgruppe festzustellen. Außerdem lehnten auffallend viele Patienten eine Teilnahme an der Studie ab.
Fazit zu SDM
Insgesamt liegt nur wenig Evidenz vor, dass SDM bei Patienten mit Schizophrenie zu besseren Outcomes führt. Jedoch sind aus anderen Bereichen der Medizin positive Effekte von SDM bekannt [56, 59], die sich eventuell übertragen lassen. Auch sprechen ethische Gründe für eine Entscheidungsbeteiligung des Patienten, weshalb die S3-Leitlinie Schizophrenie eine Implementierung von SDM fordert [20].
Diskussion
Psychoedukation für Patienten mit Schizophrenie kann Nonadhärenz reduzieren, Rückfälle verhindern und Hospitalisierungen vermeiden [41, 42, 66, 67]. Ihr Einsatz wird in der S3-Leitlinie empfohlen [20] und es sind zahlreiche Therapiemanuale verfügbar.
Für den Einsatz von MI und SDM bei Schizophrenie ist deutlich weniger Evidenz vorhanden, Studien dazu erbrachten gemischte Ergebnisse [28, 30, 32, 52, 64, 68]. Der Einsatz von SDM wird trotzdem in der S3-Leitlinie empfohlen [20], da aus ethischen Gründen der Patient in Therapieentscheidungen einbezogen werden soll [21].
Vermutlich dürfte eine Kombination von patientenzentrierten Kommunikationstechniken wie MI und SDM mit Psychoedukation und Familieninterventionen den größten Effekt haben. SDM und MI können andere Formen der Therapie unterstützen und sind relativ leicht zu implementieren. Durch Psychoedukation kann der Patient in die Lage versetzt werden, seine Erkrankung besser zu verstehen und informierte Entscheidungen zu treffen, was als Basis für die Anwendung von SDM und MI genutzt werden kann. Nicht immer ist eine Informationsvermittlung erfolgreich: Beispielsweise gaben bei einer Umfrage 75 % der befragten Psychiater an, ihre Patienten über die Option einer Depotbehandlung informiert zu haben – von den befragten Patienten jedoch beschrieben 67 %, sie hätten keine Information über Depots von ihren Psychiatern erhalten [35]. Hier kann eine strukturierte Vorgehensweise helfen, wie sie die manualisierte Psychoedukation bietet.
Psychiatrische Patienten erwarten unter anderem von einem „idealen Arzt“, dass er auf ihre Bedürfnisse eingeht und ein kooperatives Arzt-Patienten-Verhältnis auf Augenhöhe ermöglicht [62]. Die Zufriedenheit psychiatrischer Patienten mit einer stationären Behandlung hängt stark von den kommunikativen Fähigkeiten des Behandlungsteams ab [45]. Dies sollte ein Anreiz für Behandler sein, ihre kommunikativen Fähigkeiten zu stärken.
Ob sich Patienten mit Schizophrenie motivieren können, stellt einen wichtigen Aspekt der „subjektiven Recovery“ (Genesung) dar [65]. Zudem ist die Motivation ein wichtiger Mittler, der bei Patienten mit verbesserter sozialer Wahrnehmung und Urteilsbildung dazu führt, dass auch die soziale Funktionalität sich verbessert [47, 55]. Studien weisen darauf hin, dass Patienten weniger stark zur Erreichung von Therapiezielen motiviert sind als ihre Therapeuten [26]. Daher ist es für Behandler wichtig, ihre Patienten zu Veränderungen motivieren und Hindernisse hierzu wie komorbid bestehende Depressionen, Selbststigmatisierung [14] und Negativsymptomatik vermindern zu können. Hierbei werden neben Gesprächsführungstechniken und der therapeutischen Beziehung auch pharmakologische Interventionen eingesetzt. MI kann hier als auf Motivation abzielende Kommunikationstechnik ein Baustein sein.
Zu den weiteren subjektiven Merkmalen einer Genesung gehören Selbstwirksamkeit, Eigenverantwortung und Empowerment [65]. Grundvoraussetzung dafür ist ein patientenzentrierter Therapieansatz, der dem Patienten Informiertheit und Entscheidungskompetenzen zuspricht. Dies unterstreicht die Wichtigkeit, dem Patienten durch Psychoedukation solche Kompetenzen zu vermitteln und ihn durch patientenzentrierte Kommunikation zu ermutigen, eigene Entscheidungen zu treffen und individuelle Therapieziele zu verfolgen.
Zu den Limitationen der in diesem Artikel diskutierten Verfahren gehört, dass sie bei sehr schwer erkrankten Patienten deutlich schwerer anzuwenden sein können. Insbesondere bei Patienten mit fehlender Krankheitseinsicht und solchen, die unfreiwillig behandelt werden, kann der Einsatz mitunter nicht zielführend sein – hier müssen speziell angepasste Gesprächsverfahren zum Einsatz kommen, bei denen aber ebenfalls MI als Basis dient [3]. Patienten, die wegen akuter Agitiertheit nicht gruppenfähig sind, können in eine Psychoedukationsgruppe eventuell nicht mit einbezogen werden und nicht von den Sichtweisen und Erfahrungen von Mitbetroffenen profitieren. Ebenso muss eine Gruppenteilnahme von Patienten, welche im Rahmen ihrer Krankheitsverarbeitung bilanzieren oder Suizidgedanken haben, kritisch erwogen werden, da die Konfrontation mit der eigenen Erkrankung und deren Auswirkungen zu einer akuten Verschlechterung führen kann. Für eine erfolgreiche Anwendung der MI-Technik ist ebenfalls eine Voraussetzung, dass der Patient nicht zu stark kognitiv beeinträchtigt ist. SDM bringt eine Reihe möglicher Nachteile mit sich, die bereits oben im Abschnitt „Kontroverse zum Shared-Decision-Making“ diskutiert wurden, und wobei es auch darum geht, die Entscheidung nicht an die „Krankheit“ zu delegieren.
Fazit
Spezielle Kommunikationstechniken können einen wertvollen Beitrag bei der Behandlung von Patienten mit Schizophrenie leisten. Für Behandler kann es deshalb nützlich sein, sich solche Techniken immer wieder in Erinnerung zu rufen, sich mit ihnen zu beschäftigen und sie zielführend anzuwenden. Die Evidenz für den Einsatz dieser Techniken ist noch beschränkt, jedoch im Wachsen begriffen, was zu begrüßen ist.
Interessenkonflikterklärung
Dr. Bienentreu erhielt Honorare für Vortrags- und Beratertätigkeiten der Firmen Janssen-Cilag, Lilly, Lundbeck, Servier, AstraZeneca, Pfizer, Wyeth und Otsuka. Dr. Correll erhielt Honorare für Vortrags- und Beratertätigkeiten der Firmen Acadia, Alkermes, Allergan, Angelini, Axsome, Gedeon Richter, Gerson Lehrman Group, Indivior, IntraCellular Therapies, Janssen/J&J, Karuna, LB Pharma, Lundbeck, MedAvante-ProPhase, MedInCell, Medscape, Merck, Mitsubishi Tanabe Pharma, Mylan, Neurocrine, Noven, Otsuka, Pfizer, Recordati, Rovi, Servier, Sumitomo Dainippon, Sunovion, Supernus, Takeda, and Teva. Er hat als Experte ausgesagt für Janssen and Otsuka. Er war im Data Safety Monitoring Board für Lundbeck, Rovi, Supernus, and Teva. Er hat Forschungsgelder von Janssen and Takeda erhalten. Er hält Anteile an LB Pharma. Dr. Nick war Berater von Lundbeck und Recordati. Dr. Vauth gibt an, dass keine Interessenkonflikte vorliegen. Dr. Winkler gibt Vortrags- und Autorenhonorare bzw. Beratungstätigkeit für Angelini Pharma, Lundbeck Austria und den MedMedia Verlag an.
Danksagung
Die Autoren danken Philipp Bauknecht (Dr. Carl GmbH) für die Unterstützung bei der Literatursuche und der Ausformulierung dieses Artikels, der von der Lundbeck GmbH und Otsuka Pharma GmbH ermöglicht wurde, und Wolfgang Janetzky (Lundbeck GmbH) für die Koordinierung bei der Erstellung des Artikels.
Literatur
1. Adams JR, Drake RE. Shared decision-making and evidence-based practice. Community Ment Health J 2006;42:87–105.
2. Alipour A, Gabrielson S, Patel PB. Ingestible sensors and medication adherence: focus on use in serious mental illness. Pharmacy (Basel) 2020;8:103.
3. Amador X. I Am Not Sick, I Don’t Need Help! How To Help Someone With Mental Illness Accept Treatment. 10th Anniversary Edition. Vida Press, 2011.
4. Auerbach SM, Martelli MF, Mercuri LG. Anxiety, information, interpersonal impacts, and adjustment to a stressful health care situation. J Pers Soc Psychol 1983;44:1284–96.
5. Auerbach SM, Penberthy AR, Kiesler DJ. Opportunity for control, interpersonal impacts, and adjustment to a long-term invasive health care procedure. J Behav Med 2004;27:11–29.
6. Auerbach SM. Should patients have control over their own health care?: empirical evidence and research issues. Ann Behav Med 2000;22:246–59.
7. Bäuml J, Behrendt B, Henningsen P, Pitschel-Walz G (editors). Handbuch der Psychoedukation fuer Psychiatrie, Psychotherapie und Psychosomatische Medizin. Stuttgart: Schattauer, 2016.
8. Bäuml J, Pitschel-Walz G. Psychoedukation. Psychiatrie und Psychoterapie up2date 2011;5:161–76.
9. Bebbington P, Kuipers L. The clinical utility of expressed emotion in schizophrenia. Acta Psychiatr Scand Suppl 1994;382:46–53.
10. Benbassat J, Pilpel D, Tidhar M. Patients’ preferences for participation in clinical decision making: a review of published surveys. Behav Med 1998;24:81–8.
11. Bienentreu S. Motivation zur Depotmedikation bei Patienten mit Schizophrenie. Psychopharmakotherapie 2014;21:112–7.
12. Bullinger M, Kuhn J, Leopold K, Janetzky W, et al. [Quality of life as a target criterion in schizophrenia therapy]. Fortschr Neurol Psychiatr 2019;87:348–56.
13. Carpenter WT, Gold JM, Lahti AC, Queern CA, et al. Decisional capacity for informed consent in schizophrenia research. Arch Gen Psychiatry 2000;57:533–8.
14. Cavelti M, Beck E-M, Kvrgic S, Kossowsky J, et al. The role of subjective illness beliefs and attitude toward recovery within the relationship of insight and depressive symptoms among people with schizophrenia spectrum disorders. J Clin Psychol 2012;68:462–76.
15. Charles C, Gafni A, Whelan T. Shared decision-making in the medical encounter: what does it mean? (or it takes at least two to tango). Soc Sci Med 1997;44:681–92.
16. Chien WT, Bressington D, Yip A, Karatzias T. An international multi-site, randomized controlled trial of a mindfulness-based psychoeducation group programme for people with schizophrenia. Psychol Med 2017;47:2081–96.
17. Chien WT, Cheng HY, McMaster TW, Yip ALK, et al. Effectiveness of a mindfulness-based psychoeducation group programme for early-stage schizophrenia: An 18-month randomised controlled trial. Schizophr Res 2019;212:140–9.
18. Cruz M, Pincus HA. Research on the influence that communication in psychiatric encounters has on treatment. Psychiatr Serv 2002;53:1253–65.
19. De las Cuevas C, Peñate W, de Rivera L. Psychiatric patients’ preferences and experiences in clinical decision-making: examining concordance and correlates of patients’ preferences. Patient Educ Couns 2014;96:222–8.
20. DGPPN e. V. (Hrsg.) für die Leitliniengruppe. S3-Leitlinie Schizophrenie. Langfassung, 2019, Version 1.0, zuletzt geändert am 15. März 2019 (Zugriff am 06.11.2020).
21. Drake RE, Deegan PE. Shared decision making is an ethical imperative. Psychiatr Serv 2009;60:1007.
22. Frank AF, Gunderson JG. The role of the therapeutic alliance in the treatment of schizophrenia. Relationship to course and outcome. Arch Gen Psychiatry 1990;47:228–36.
23. Gardner CL. Adherence: a concept analysis. Int J Nurs Knowl 2015;26:96–101.
24. Greenfield S, Kaplan SH, Ware JE, Yano EM, et al. Patients’ participation in medical care: effects on blood sugar control and quality of life in diabetes. J Gen Intern Med 1988;3:448–57.
25. Grisso T, Appelbaum PS. The MacArthur treatment competence study. III: Abilities of patients to consent to psychiatric and medical treatments. Law Hum Behav 1995;19:149–74.
26. Gründer G, Bauknecht P, Klingberg S, Leopold K, et al. Treatment goals for patients with schizophrenia – a narrative review of physician and patient perspectives. Pharmacopsychiatry published online December 8, 2020; doi: 10.1055/a-1298-4546.
27. Hamann J, Cohen R, Leucht S, Busch R, et al. Shared decision making and long-term outcome in schizophrenia treatment. J Clin Psychiatry 2007;68:992–7.
28. Hamann J, Holzhüter F, Blakaj S, Becher S, et al. Implementing shared decision-making on acute psychiatric wards: a cluster-randomized trial with inpatients suffering from schizophrenia (SDM-PLUS). Epidemiol Psychiatr Sci 2020;29:e137.
29. Hamann J, Holzhüter F, Stecher L, Heres S. Shared decision making PLUS – a cluster-randomized trial with inpatients suffering from schizophrenia (SDM-PLUS). BMC Psychiatry 2017;17:78.
30. Hamann J, Langer B, Winkler V, Busch R, et al. Shared decision making for in-patients with schizophrenia. Acta Psychiatr Scand 2006;114:265–73.
31. Hamann J, Mendel R, Meier A, Asani F, et al. “How to speak to your psychiatrist”: shared decision-making training for inpatients with schizophrenia. Psychiatr Serv 2011;62:1218–21.
32. Hamann J, Parchmann A, Sassenberg N, Bronner K, et al. Training patients with schizophrenia to share decisions with their psychiatrists: a randomized-controlled trial. Soc Psychiatry Psychiatr Epidemiol 2017;52:175–82.
33. Heres S, Hamann J. [Shared decision-making in acute psychiatric medicine: Contraindication or a challenge?]. Nervenarzt 2017;88:995–1002.
34. Hesse K, Klingberg S. [Psychosis: cognitive behavioral treatment strategies]. Psychother Psychosom Med Psychol 2018;68:481–94.
35. Jaeger M, Rossler W. Attitudes towards long-acting depot antipsychotics: a survey of patients, relatives and psychiatrists. Psychiatry Res 2010;175:58–62.
36. Kane JM, Schooler NR, Marcy P, Achtyes ED, et al. Patients with early-phase schizophrenia will accept treatment with sustained-release medication (long-acting injectable antipsychotics): Results from the recruitment phase of the PRELAPSE trial. J Clin Psychiatry 2019;80:18m12546; doi: 10.4088/JCP.18m12546.
37. Kane JM, Schooler NR, Marcy P, Correll CU, et al. Effect of long-acting injectable antipsychotics vs usual care on time to first hospitalization in early-phase schizophrenia: A randomized clinical trial. JAMA Psychiatry 2020;77:1–8.
38. Keating NL, Guadagnoli E, Landrum MB, Borbas C, et al. Treatment decision making in early-stage breast cancer: should surgeons match patients’ desired level of involvement? J Clin Oncol 2002;20:1473–9.
39. Kiesler DJ, Auerbach SM. Integrating measurement of control and affiliation in studies of physician-patient interaction: the interpersonal circumplex. Soc Sci Med 2003;57:1707–22.
40. Lencer R, Korn D. [Adherence to psychopharmacological treatment: Psychotherapeutic strategies to enhance adherence]. Nervenarzt 2015;86:637–46; quiz 647.
41. McDonagh MS, Dana T, Selph S, Devine EB, et al. Treatments for schizophrenia in adults: A systematic review. Rockville (MD): Agency for Healthcare Research and Quality (US), 2017.
42. McFarlane WR. Family interventions for schizophrenia and the psychoses: A review. Fam Proces. 2016;55:460–82.
43. Mead N, Bower P. Patient-centredness: a conceptual framework and review of the empirical literature. Soc Sci Med 2000;51:1087–110.
44. Miller WR, Rollnick S. Motivierende Gesprächsführung: Motivational Interviewing. 3. Auflage des Standardwerks in Deutsch. 4th ed. Freiburg im Breisgau: Lambertus, 2015.
45. Möller-Leimkühler AM, Dunkel R. [Patient satisfaction with psychiatric services. Findings of a key date survey]. Nervenarzt 2003;74:40–7.
46. Morin L, Franck N. Rehabilitation interventions to promote recovery from schizophrenia: A systematic review. Front Psychiatry 2017;8:100.
47. Najas-Garcia A, Gómez-Benito J, Huedo-Medina TB. The relationship of motivation and neurocognition with functionality in schizophrenia: A meta-analytic review. Community Ment Health J 2018;54:1019–49.
48. Noble LM, Douglas BC. What users and relatives want from mental health services. Curr Opin Psychiatry 2004;17:289–96.
49. Palmier-Claus JE, Ainsworth J, Machin M, Barrowclough C, et al. The feasibility and validity of ambulatory self-report of psychotic symptoms using a smartphone software application. BMC Psychiatry 2012;12:172.
50. Pickett SA, Diehl SM, Steigman PJ, Prater JD, et al. Consumer empowerment and self-advocacy outcomes in a randomized study of peer-led education. Community Ment Health J 2012;48:420–30.
51. Potkin S, Bera R, Zubek D, Lau G. Patient and prescriber perspectives on long-acting injectable (LAI) antipsychotics and analysis of in-office discussion regarding LAI treatment for schizophrenia. BMC Psychiatry 2013;13:261.
52. Reimer J, Kuhn J, Wietfeld R, Janetzky W, et al. [Motivational interviewing: A possibility for doctor-patient communication in schizophrenia?]. Nervenarzt 2019;90:1144–53.
53. Roll SC, Knecht G, Kuhn J, Spittler S. Antipsychotika-Depotbehandlung im Wandel der Zeit. Nervenheilkunde 2016;35:41–9.
54. Ruben BD. What patients remember: A content analysis of critical incidents in health care. Health Commun 1993;5:99–112.
55. Schmidt SJ, Mueller DR, Roder V. Social cognition as a mediator variable between neurocognition and functional outcome in schizophrenia: empirical review and new results by structural equation modeling. Schizophr Bull 2011;37(Suppl 2):S41–54.
56. Shay LA, Lafata JE. Where is the evidence? A systematic review of shared decision making and patient outcomes. Med Decis Making 2015;35:114–31.
57. Shumway M, Saunders T, Shern D, Pines E, et al. Preferences for schizophrenia treatment outcomes among public policy makers, consumers, families, and providers. Psychiatr Serv 2003;54:1124–8.
58. Sibitz I, Gössler R, Katschnig H, Amering M. [“Knowing – enjoying – better living”. A seminar for persons with psychosis to improve their quality of life and reduce their vulnerability]. Psychiatr Prax 2006;33:170–6.
59. Stacey D, Légaré F, Lewis K, Barry MJ, et al. Decision aids for people facing health treatment or screening decisions. Cochrane Database Syst Rev 2017;4:CD001431.
60. Stein BD, Kogan JN, Mihalyo MJ, Schuster J, et al. Use of a computerized medication shared decision making tool in community mental health settings: impact on psychotropic medication adherence. Community Ment Health J 2013;49:185–92.
61. Stephan LS, Almeida ED, Guimarães RB, Ley AG, et al. Oral anticoagulation in atrial fibrillation: Development and evaluation of a mobile health application to support shared decision-making. Arq Bras Cardiol 2018;110:7–15.
62. Theisel S, Schielein T, Spiessl H. [The “ideal” doctor from the view of psychiatric patients]. Psychiatr Prax 2010;37:279–84.
63. van der Krieke L, Emerencia AC, Boonstra N, Wunderink L, et al. A web-based tool to support shared decision making for people with a psychotic disorder: randomized controlled trial and process evaluation. J Med Internet Res 2013;15:e216.
64. Vanderwaal FM. Impact of motivational interviewing on medication adherence in schizophrenia. Issues Ment Health Nurs 2015;36:900–4.
65. Wietfeld R, Pechler S, Janetzky W, Leopold K. Therapieerfolg bei Schizophrenie – ist ein Perspektivenwechsel notwendig? Psychopharmakotherapie 2019;26:185–91.
66. Xia J, Merinder LB, Belgamwar MR. Psychoeducation for schizophrenia. Cochrane Database Syst Rev 2011;(6):CD002831.
67. Zhao S, Sampson S, Xia J, Jayaram MB. Psychoeducation (brief) for people with serious mental illness. Cochrane Database Syst Rev 2015;(4):CD010823.
68. Zomahoun HTV, Guénette L, Grégoire J-P, Lauzier S, et al. Effectiveness of motivational interviewing interventions on medication adherence in adults with chronic diseases: a systematic review and meta-analysis. Int J Epidemiol 2017;46:589–602.
Dr. Sara Bienentreu, Fachklinik für Psychiatrie und Psychotherapie, Marienborn gGmbH, Luxemburger Straße 1, 53909 Zülpich (Hoven), E-Mail: s.bienentreu@marienborn-zuelpich.de
Prof. Dr. Christoph U. Correll, Charité Universitätsmedizin, Klinik für Psychiatrie, Psychosomatik und Psychotherapie des Kindes- und Jugendalters, Augustenburger Platz 1 (Mittelallee 5A), 13353 Berlin, und The Zucker Hillside Hospital, Department of Psychiatry, Northwell Health, 75–59263rd St, Glen Oaks, NY 11004, USA, und Hofstra Northwell School of Medicine, Department of Psychiatry and Molecular Medicine, 500 Hofstra Blvd, Hempstead, NY 11549, USA
Dr. Beat Nick, Solothurner Spitäler AG, Psychiatrische Dienste, Weissensteinstrasse 102, 4503 Solothurn, Schweiz
Prof. Dr. Roland Vauth, Zentrum für Verhaltensmedizin Basel, Rheinsprung 1 (2.OG), 4051 Basel, Schweiz
Prof. Dr. Dietmar Winkler, Michaelerstraße 23/18/2, 1180 Wien, Österreich
Techniques of doctor-patient communication in schizophrenia: psychoeducation, motivational interviewing, shared decision making
In the treatment of schizophrenia, communication between the practitioner and the patient is an important factor for therapeutic success. The use of structured communication techniques can be helpful in this regard. This review article briefly introduces psychoeducation, motivational interviewing (MI), and shared decision making (SDM) and reviews the evidence for their use in the treatment of schizophrenia.
Psychoeducation informs the patient about his/her illness and should enable him/her to optimally combine self-help strategies and offered treatments. Controlled studies and meta-analyses show that the use of psychoeducation can improve adherence and prevent relapses and hospitalization.
Motivational interviewing is a conversational technique that aims to increase the patient's willingness to change and motivate them to adopt behaviours that prevent relapse and promote recovery. Several studies have found positive effects of MI in schizophrenia, but results are heterogeneous and more evidence is needed for unqualified recommendation. MI can be used to support other therapeutic procedures and communication techniques.
Shared decision-making means that treatment decisions are discussed and made jointly by patients and practitioners. Evidence for improved outcomes after the use of SDM is limited and primarily given in the context of more complex interventions, but the use of SDM is mandatory for ethical reasons.
Overall, structured communication techniques are useful tools that can help in the treatment of schizophrenia.
Key words: Doctor-patient communication, schizophrenia, psychoeducation, motivational interviewing, shared decision making
Psychopharmakotherapie 2021; 28(02):52-62
