Ralf Ihl, Krefeld, und Walter E. Müller, Worms
Demenzen zählen zu den bedeutendsten Krankheiten im Alter. Mit 65 Jahren leidet einer von Hundert, mit 80 jeder Fünfte und mit 90 jeder Dritte bis Zweite an einer Demenz. Als häufigste Ursache von Demenzen mit etwa 60 bis 70 % wird die Alzheimer-Krankheit angesehen. Die Symptome anderer Demenzformen zeigen große Überlappungsbereiche mit den Krankheitszeichen der Alzheimer-Krankheit, deren Kardinalsymptome Gedächtnis- und Orientierungsstörungen sind. Zu Beginn der Erkrankung stehen sie allerdings nur bei etwa 50 % der Erkrankten im Vordergrund. Die häufigsten Symptome finden sich in Tabelle 1, eine differenzierte Auflistung nach Demenzursachen in Tabelle 2.
Tab. 1. Symptome der Demenz
|
Symptom |
Beispiel |
|
Verstärkte Vergesslichkeit |
Schlüssel oder andere Gegenstände werden häufiger als früher verlegt, Fragen wiederholen sich, die Haustür wird nicht verschlossen, der Herd wird angelassen |
|
Orientierungsstörungen |
Tag, Monat und Jahr können nicht mehr benannt werden, Monate und Jahreszeiten können nicht mehr zugeordnet werden, die Lage früher bekannter Orte wird nicht mehr gewusst, die Zuordnung von Namen zu Personen geht verloren |
|
Sprachstörungen |
Schwierigkeiten, die richtigen Worte zu finden, zu verstehen, was gemeint ist und sich selbst verständlich zu machen. Umschreibungen häufen sich. |
|
Gefühlsstörungen |
Eine leichte Euphorie, Depressivität und auch Aggressivität können auftreten. Oft werden diese Gefühle als „Böswilligkeit“ oder „wahre Gefühle“ verkannt. |
|
Wahnvorstellungen |
Kranke können sich bestohlen fühlen, wenn sie vergessen, wohin sie ihre Gegenstände gelegt haben. |
|
Erhaltene Fassade |
Die vorhandenen Fähigkeiten werden genutzt, um die Beschwerden zu überspielen: die äußere Fassade ist sehr lange intakt |
|
Weitere Symptome: Motorische Unruhe, Umherlaufen, Halluzinationen, Unsicherheit, Interesselosigkeit, fehlende Organisation von Körperpflege und Kleidung, Blasen- und Darmentleerungsstörungen, Persönlichkeitsveränderungen |
|
Tab. 2. Vergleich diagnostischer Kriterien (verändert nach [8])
|
Alzheimer-Demenz (AD) |
Vaskuläre Demenz (VD) |
Lewy-Körperchen-Demenz (LBD) |
Frontotemporale Degeneration (FD) |
Creutzfeldt-Jakob-Krankheit (CJD) |
|
|
Spezielle Symptome neben dem demenziellen Syndrom |
Nur 50 % zeigen zu Beginn eine Gedächtnisstörung, erhaltene Fassade |
Frühe Gangstörung, Blasenstörung ohne urologische Ursache, Stürze, fokale neurologische Zeichen |
Fluktuierende Vigilanz, paranoide und halluzinatorische Symptome, Parkinson-ähnliche Rigidität, Übersensibilität gegenüber Neuroleptika, REM-Schlafstörungen |
Euphorie, emotionale Verflachung, Disinhibierung, Vergröberung des Sozialverhaltens, visuelle und räumliche Funktionen anfangs gut erhalten |
Visuelle und zerebelläre Störungen, pyramidale und extrapyramidale Symptome, Myoklonus, akinetischer Mutismus |
|
Verlauf |
Langsame Progression |
Schrittweise Progression, partielle Kompensation nach einem Schritt möglich |
Wie AD |
Wie AD nur im Vergleich schneller |
Schnelle Progression, häufig weniger als 1 Jahr Dauer |
|
EEG |
Vom Schweregrad abhängige Verlangsamung, verringerte Alpha-Aktivität assoziiert mit schnellerer Progression, keine Veränderung auch möglich |
Öfter fokale Veränderungen |
Prominente verlangsamte posteriore Aktivität, EEG mit periodischem Fluktuieren im Prä-Alpha/Theta-Bereich Polysomnographische Bestätigung von REM-Schlaf ohne Atonie-Veränderungen im PET |
Keine charakteristischen Veränderungen |
Periodische scharfe Wellen (triphasische Wellen oft präsent), nicht bei der neuen Variante |
|
Biomarker |
Erhöhtes Tau und Phospho-Tau; erniedrigtes aβ im Liquor |
Keine |
Auffällig geringe Aufnahme von 123Iod-MIBG in der myokardialen Szintigraphie |
Keine |
Erhöhtes Protein 14-3-3 im Liquor |
|
Strukturelle Bildgebung CT/MRT |
Atrophie (medial temporal am Anfang, später temporo-parietal, frontal und am Ende generalisiert; hippokampale vom Schweregrad abhängige Atrophie) |
Multiple Infarkte Einzelne Infarkte an strategisch wichtiger Stelle Extensive Läsionen der weißen Substanz |
Medio-temporale Strukturen im CT/MRI-Scan meist ausgespart |
Frontale und/oder temporale Atrophie, oft asymmetrisch |
Unspezifisch |
|
Funktioneller Glucose-Hypo-metabolismus im PET |
Anfangs temporo-parietal und posteriorer Cingulus, später frontal, zuletzt generalisiert |
In ischämischen Gebieten |
Generalisiert niedrige Aufnahme im SPECT/PET Perfusions/Metabolismus-Scan mit reduzierter okzipitaler Aktivität, anfangs mit dem Zeichen der cingulären Insel im FDG-PET |
Frontaler und temporaler Kortex, oft asymmetrisch |
Variabel |
|
Amyloid-PET positiv in % |
Bis 100 |
7–64 |
29–84 |
3–43 |
Unzureichende Datenlage |
|
Neuropathologie |
Plaques, fibrilläre Tangles, kongophile Angiopathie |
Ischämische Läsionen |
Lewy-Körperchen |
Astrozytose, Atrophie der Lamina I–III im frontalen Kortex, Neuropil-Mikrovaskularisierung Veränderungen in Tau und TDP43 |
Spongiforme Enzephalopathie |
EEG: Elektroenzephalogramm; FDG: Fluorodesoxyglucose; MIBG: Metaiodobenzylguanidin; MRT: Magnetresonanztomographie; PET: Positronen-Emissionstomographie; SPECT: Single photon emission computed tomography (Einzelphotonen-Emissionscomputertomographie)
Diagnostik der Demenz
Die Alzheimer-Krankheit beginnt schleichend und führt langsam voranschreitend zum Tode, sofern nicht wie bei den meisten Erkrankten andere Erkrankungen wie Infektionen den Tod früher herbeiführen. Erkrankte merken die Krankheit selbst zuerst. Da allerdings Vergessen zum normalen Leben des Menschen gehört, ist die Krankheit nicht leicht zu erkennen. Ein zusätzliches Warnsignal kommt auf, wenn Nahestehende den Eindruck einer Verschlechterung des Gedächtnisses oder anderer Fähigkeiten teilen.
Die Diagnostik wird häufig durch den Versuch der Kranken erschwert, ihre Symptome zu überspielen. Hier wird von einer „erhaltenen Fassade“ gesprochen. Differenzialdiagnostisch sind auch Depressionen abzugrenzen, die häufig mit kognitiven Störungen einhergehen und damit als Pseudodemenz imponieren. Für den Übergangsbereich von Gesundheit zu Demenz gibt es mehr als zehn Begrifflichkeiten, zum Beispiel „mild cognitive impairment“; sie helfen aber nur sehr begrenzt weiter, da sie meist mit nur wenig überprüfbaren Kriterien beschrieben sind.
Auch die Definitionen der Demenz unterliegen einem raschen Wandlungsprozess, was eine Vergleichbarkeit von Studien über die Jahre hinweg erheblich erschwert bis verunmöglicht und damit ein entscheidendes Hemmnis des wissenschaftlichen Vorankommens mit sich bringt. Interessanterweise wurden einfache methodische Herangehensweisen in den letzten Jahrzehnten weitgehend vermieden, obwohl sie immer wieder einmal vorgeschlagen wurden (z. B. Gruppierung über definierte Laborwerte oder über Ergebnisse apparativer Untersuchungen wie bestimmte Symptomkonstellationen in psychometrischen Tests oder EEG-Veränderungen). Wenn denn Verfahren eingesetzt wurden, spielte deren wissenschaftlich überprüfte Genauigkeit meist keine Rolle. Ein Beispiel ist der Mini-Mental-Status-Test, der sich vielfach als wenig sensitiv und spezifisch und damit als für die meisten Aufgaben untauglich erwiesen hat. Obwohl inzwischen bessere Tests bekannt sind, wird er auch heute noch im niedergelassenen wie stationären Alltag sowie zum Beispiel von Krankenkassen genutzt und ist selbst in der aktuellen S3-Leitlinie Demenz noch aufgeführt. Die Krankheitsschweregrade können hingegen valide mit der Global Deterioration Scale (GDS) gemessen werden [20]. Neuere Diagnosekriterien wie „Subjective Cognitive Decline“ (SCD, [10]) oder die Unterscheidung in minore and majore neurokognitive Störung durch die DSM-5 [1] haben hierzu einen engen Bezug (Abb. 1).
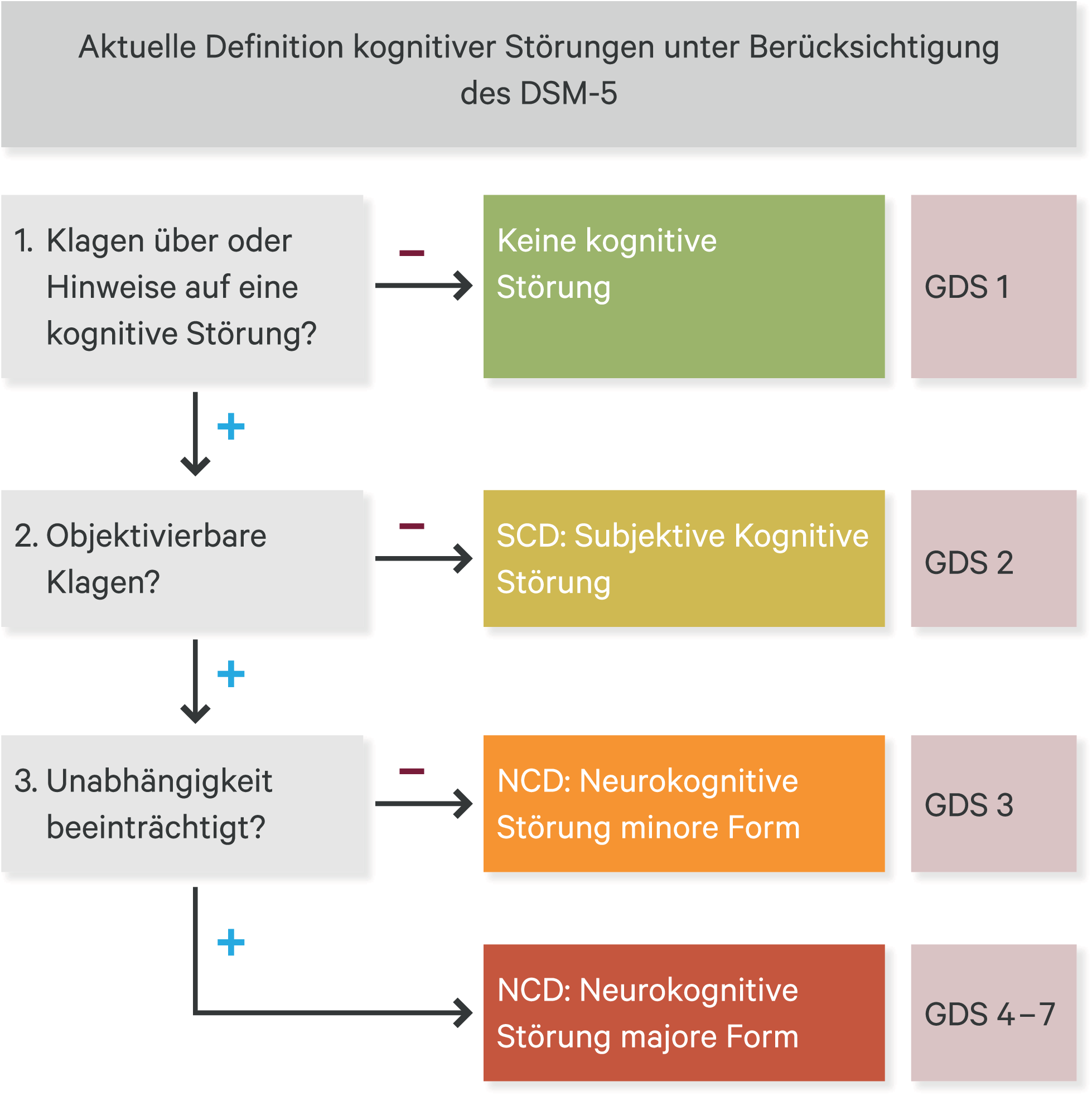
Abb. 1. Beschreibung des diagnostischen Vorgehens bei kognitiven Störungen nach den DSM-5-Kriterien. Aus historischer Sicht besteht ein Bezug zu den GDS-Stadien nach Reisberg [20]; GDS: Global Deterioration Scale
Im ersten Schritt der Diagnostik wird meist geprüft, ob ein demenzielles Syndrom vorliegt. Im zweiten Schritt erfolgt dann eine weitere Differenzierung. Valide Kriterien wie das Protein 14-3-3 als Marker der Creutzfeldt-Jakob-Krankheit sind für den zweiten Schritt allerdings rar. Für andere Demenzen fehlt es an validen Markern. Eine detaillierte Analyse der Bedeutung von Markern findet sich in der WFSBP-Leitlinie zur Diagnose der Demenz [15].
Für die dringend notwendige weitere Forschung Klassifizierungskriterien mithilfe von Markern zu finden, ist ein vielversprechender Ansatz, da über homogenere Gruppen validere Aussagen für die Praxis zu erwarten sind. Für eine aktuelle Beurteilung therapeutischer Möglichkeiten bei der Demenz wird hier auf die herkömmliche Einteilung zurückgegriffen. Die für die Einteilung bekannten Diagnosekriterien sind in Tabelle 2 dargestellt.
Medikamentöse Therapie der Demenz
Zur medikamentösen Therapie der Demenz hat die World Federation of Societies of Biological Psychiatry (WFSBP) unter Berücksichtigung der bis dahin vorliegenden randomisiert-kontrollierten Studien (RCT) hinreichender Qualität eine Leitlinie erstellt [8, 9]. Sie hat in wesentlichen Zügen auch heute noch Gültigkeit. Die Behandlung umfasst dabei die Bereiche Kognition und neuropsychiatrische Störungen. Die zusammenfassende Feststellung der Leitlinie sagt aus: Keine Substanz kann bisher eine degenerative Demenz heilen oder stoppen.
Diverse methodische Probleme tragen zu diesem Ergebnis bei:
- Das diagnostische Vorgehen führt zu heterogenen Gruppen.
- Ein „Goldstandard“ zur Diagnostik fehlt.
- Heterogene Gruppen verschleiern den Blick auf
- mögliche Krankheitsursachen und
- Therapieeffekte bei Untergruppen.
- Die Menge der Daten beinhaltet das Risiko, Ergebnisse zu übersehen.
Zwischenzeitlich wurden aber auch wesentliche zusätzliche Informationen gefunden, beispielsweise hat sich unser Wissen
- über reversible Demenzen,
- zur Risikosenkung,
- zu Kombinationstherapieeffekten und
- zu Nebenwirkungen vermehrt.
Unglücklicherweise ist die neuere Literatur bei fehlenden RCTs im Wesentlichen durch Metaanalysen und Übersichtsarbeiten charakterisiert. Solche Publikationen sollten einem rigorosen methodischen Prozess folgen. Ob so vorgegangen wurde, lässt sich anhand der Publikationen meist nicht prüfen. Soweit valide neue Daten erhoben werden konnten, wurden sie im folgenden Text berücksichtigt. Der Annahme, dass Übersichtsarbeiten oder Metaanalysen größere behandlungsrelevante Effekte entdecken könnten, als sie in den Originalarbeiten beschrieben sind, fehlt meist eine Begründung.
Die eingeschränkte Nutzung methodischer Möglichkeiten führte bisher nur zu wenigen Substanzen, die einen Einfluss auf Symptome der Demenz haben können. Die Erkenntnisse zu den Bereichen Kognition und neuropsychiatrische Störungen (NPS) sind nachfolgend geordnet nach den zugelassenen Antidementiva sowie den Möglichkeiten einer Kombinationstherapie für die Alzheimer-Krankheit aufgelistet. Soweit Erkenntnisse zu anderen Demenzen vorliegen, sind sie entsprechend zugeordnet. Die meisten Daten stammen weiter aus vom Hersteller initiierten Studien. Fakten und ihre Interpretation sind daher auf zu vermeidende euphorische Überinterpretationen zu prüfen [7]. Ein Ausschluss von Einschätzungen erfolgt auch, wenn unbegründet diskriminierende Qualitätskriterien für eine Studie ohne wissenschaftliche Basis einbezogen wurden (z. B. das Herkunftsland einer Studie) oder testpsychologische Erkenntnisse ausgeklammert wurden (z. B. die fehlende Vergleichbarkeit von Studien nicht zu benennen, wenn die Alzheimer-Disease-Assessment-Scale in von Studie zu Studie variierenden, nicht validierten Versionen genutzt wurde).
Pharmakologie der Antidementiva
Als Antidementiva stehen heute die drei Acetylcholinesterase-Hemmstoffe Donepezil, Galantamin und Rivastigmin, der NMDA-Rezeptorantagonist Memantin und der die mitochondriale Funktion verbessernde Ginkgo-Extrakt (EGb761) zur Verfügung. Sie wirken nicht nur über sehr unterschiedliche Targets, sondern beeinflussen damit auch sehr unterschiedliche Bereiche der pathophysiologischen Veränderungen im Gehirn dementer Patienten. Dies erklärt, dass die Wirksamkeit am individuellen Patienten sehr unterschiedlich und ein Wechsel auf eine andere Klasse bei schlechtem Ansprechen sinnvoll sein kann.
Acetylcholinesterasehemmstoffe (AChE-Hemmer)
Im Rahmen der breiten neurodegenerativen Veränderungen im Gehirn von AD-Patienten kommt es zu einem sehr deutlichen Verlust von cholinergen Neuronen, die ausgehend vom Nucleus basalis Meynert in verschiedene Hirnareale projizieren, die für Gedächtnisfunktionen relevant sind. AChE-Hemmer werden mit dem Ziel eingesetzt, durch Hemmung des synaptischen Acetylcholin-Abbaus die cholinerge Neurotransmission der noch vorhandenen cholinergen Neuronen zu verstärken. Diese Maßnahme ist aber leider nicht so effektiv, wie man ursprünglich erhofft hatte, da die Relevanz dieses cholinergen Defizits für die kognitive Beeinträchtigung der AD-Patienten begrenzt ist und es auch im Rahmen des Alterungsprozesses oder bei vaskulärer Demenz zu cholinerger Unterfunktion kommen kann.
Alle drei Substanzen (Abb. 2) hemmen reversibel das Enzym Acetylcholinesterase, das an der cholinergen Synapse den Neurotransmitter Acetylcholin durch Hydrolyse zu Cholin und Acetat inaktiviert. Acetylcholin verweilt dann länger an der Synapse und seine Wirkung ist intensiviert. Rivastigmin bindet an die gleiche Stelle des Enzyms wie Acetylcholin und wird dabei ebenfalls hydrolysiert, allerdings dauert dieser Prozess sehr viel länger als bei Acetylcholin, sodass das Enzym über Stunden funktionell blockiert ist. Donepezil und Galantamin blockieren die Enzymfunktion über eine Bindung an anderen Positionen. Ihre Metabolisierung erfolgt über das Cytochrom-P450-System mit damit verbundenen Interaktionen [2]. Galantamin hat noch einen Nikotinrezeptoren-modulierenden Effekt und Rivastigmin hemmt noch die eher extrasynaptische Butyrylcholinesterase; allerdings gibt es keine Daten, dass sich diese Zusatzeffekte auf die klinische Effektivität auswirken. Das gilt auch für die unterschiedliche Veränderung der AChE-Aktivität nach Langzeitbehandlung, die bei Rivastigmin eher vermindert und bei den beiden anderen eher erhöht ist (Tab. 3).
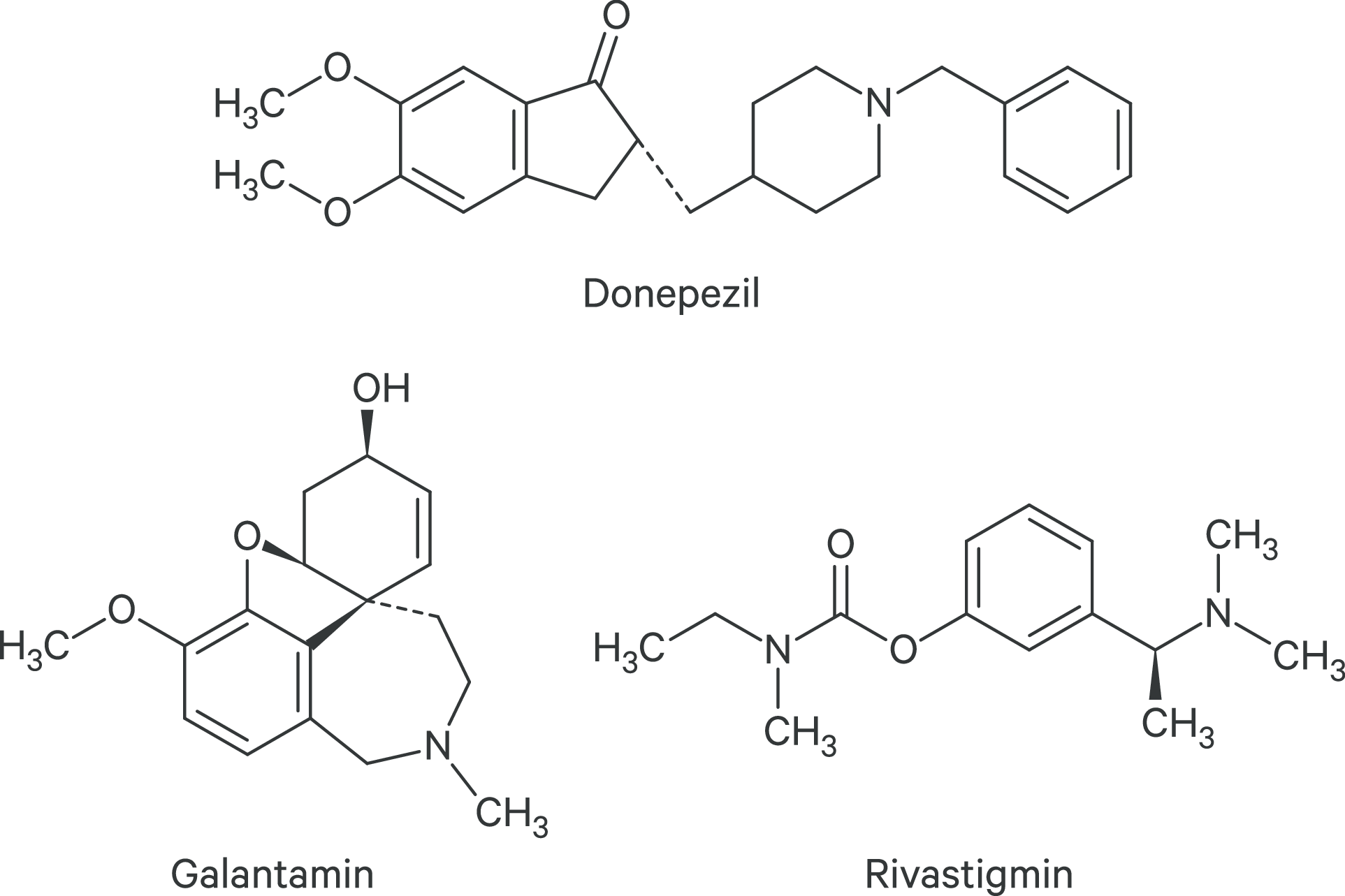
Abb. 2. Chemische Struktur der drei als Antidementiva eingesetzten Acetylcholinesterasehemmstoffe
Tab. 3. Pharmakologische Charakteristika der als Antidementiva eingesetzten Acetylcholinesterasehemmstoffe
|
Donepezil |
Galantamin |
Rivastigmin |
|
|
Pharmakodynamische Eigenschaften |
|||
|
Enzymhemmung |
|||
|
Ja |
Ja |
Ja |
|
Nein |
Nein |
Ja |
|
Modulation von Nikotinrezeptoren |
Nein |
Ja |
Nein |
|
AChE-Aktivität nach Langzeitbehandlung (6–12 Monate) |
Erhöht |
Erhöht |
Vermindert |
|
Pharmakokinetische Eigenschaften |
|||
|
tmax [h] |
3–4 |
2–4 |
2 |
|
t1/2 [h] |
73 |
6 |
5 |
|
Metabolisierung |
Hepatisch (P450) |
Hepatisch (P450) |
ACh-Esterase |
Allen drei ist aber die funktionelle Einschränkung des synaptischen Acetylcholin-Abbaus gemeinsam. Allen drei gemeinsam ist damit aber auch, dass sie zwar auf das Target bezogen sehr spezifisch sind, funktionell aber eine sehr breite, nicht spezifische Wirkung haben, da cholinerge Synapsen in allen Bereichen des Nervensystems eine Rolle spielen, vom ZNS über die Ganglien des vegetativen Nervensystems, über den postganglionären Parasympathikus zu der Endplatte des motorischen Teils des peripheren Nervensystems. Allen gemeinsam ist damit auch die große Breite von unerwünschten Wirkungen, wie im klinischen Teil beschrieben. Die Substanzen sind hier eher ähnlich. Die etwas häufigeren unerwünschten Arzneimittelwirkungen bei oralem Rivastigmin sind durch die kurze Halbwertszeit und die damit verbundene relative hohe orale Dosis bedingt (hoher initialer Plasmapeak). Durch Glättung des Plasmaspiegelverlaufs ist dieses Problem bei der transdermalen Arzneiform etwas besser.
Memantin
Memantin ist ein Antagonist am glutamatergen NMDA-Rezeptor und interagiert mit einer Bindungsstelle im Calciumkanal. Die Bindungsstärke ist so ausbalanciert, dass neurotoxische Glutamatkonzentrationen eher geblockt werden, dafür aber die synaptische (neurotransmittorische) Wirkung von Glutamat auf kognitive Mechanismen her unbeeinflusst bleibt. Daneben weist Memantin auch neuroprotektive Effekte auf, die über eine Verbesserung der mitochondrialen Funktion und damit auch der gestörten Neuroplastizität bei Demenz erklärt werden können.
Memantin wird nach oraler Gabe rasch resorbiert (tmax 3–8 h) und mit einer Halbwertszeit von 54 bis 74 Stunden überwiegend unverändert renal ausgeschieden [2].
Ginkgo-biloba-Extrakt (EGb761)
Neueren Konzepten zufolge spielen mitochondriale Funktionsbeeinträchtigungen bei Entstehung und Verlauf von Alzheimer-Demenz eine wichtige Rolle (mitochondriale Kaskaden-Hypothese, [18]). Über die Radikalfänger-Eigenschaften der Polyphenolfraktion und die direkt Mitochondrien-protektiven Eigenschaften von Bilobalid und den Ginkgoliden erhöht EGb761 die Bereitstellung von ATP, reduziert die Bildung von freien Radikalen und verbessert die Funktion der Nervenzellen und der gestörten neuronalen Plastizität. Damit greift EGb761 in einen wichtigen Teil des Krankheitsprozesses bei Alzheimer-Demenz außerhalb der gestörten Neurotransmission ein, allerdings sind auch hier die therapeutischen Effekte wie bei den anderen Antidementiva begrenzt.
Klinische Aspekte der Antidementiva
Die ersten für die Beurteilung der Wirksamkeit ausschlaggebenden Studien sind im Detail in den WFSBP-Leitlinien dargestellt [8]. Die Studiendaten sind dort für jede Studie, die die Einschlusskriterien erfüllte, in der Anlage aufgeführt. Die für die fünf zugelassenen Antidementiva resultierenden Aussagen waren:
- Über den Verlauf der Krankheit
- kann ein moderater Effekt
- bei manchen Patienten
- für eine begrenzte Zeit gesehen werden.
Die Aussage wurde später mehrfach bestätigt (u. a. [11]). Nachfolgende Daten werden nur für zugelassene Substanzen dargestellt und lediglich Cochrane-Analysen zur Übersicht einbezogen.
Mehrere Hundert Substanzen wurden bisher untersucht, erreichten die Zulassungsreife jedoch nicht, da RCTs ihre Wirksamkeit nicht bestätigen konnten.
Für den Bereich der Kognition sind die oben pharmakologisch beschriebenen fünf Substanzen zugelassen: Donepezil, Galantamin, Ginkgo-biloba-Extrakt, Memantin und Rivastigmin. Seit mehr als 20 Jahren gibt es hier keine Neuerung. Die Gründe hierfür werden derzeit breit diskutiert. Neben den methodischen werden auch begrenzte Ursachenkenntnisse als Limitierung fehlenden Fortschritts angeschuldigt. Optimierte Methodik gepaart mit einem Fortschritt bei ätiologischen Erkenntnissen könnte diesen Zustand ändern.
Risikosenkung und Prävention
Ein Charakteristikum der Demenz ist ein Mangel von Acetylcholin. Er gilt als Voraussetzung für die Wirkung von Cholinesterasehemmern. Für die Annahme, ein Erhöhen des Acetylcholin-Angebots bei ausgeglichenem Stoffwechsel könne präventiv wirken, gibt es keine Hinweise. Für Ginkgo-biloba-Extrakt (Radikalfängereigenschaften) und Memantin (NMDA-Rezeptor-Modulation) liegt eine prüfbare Hypothese zur präventiven Wirksamkeit vor, allerdings ist die Studienlage für eine Beurteilung nicht hinreichend.
Wirkungsbeurteilung
Symptomatisch mögliche Beeinflussungen einer Demenz in den Bereichen Kognition, neuropsychiatrische Störungen (NPS), Alltagsaktivitäten (ADL) sowie im klinischen Gesamteindruck (CGI) sind nachfolgend für die fünf zugelassenen Antidementiva beschrieben. Aussagen zur Wirksamkeit bei diversen Demenzformen über die Alzheimer-Krankheit oder vaskuläre Demenz hinaus reichen nach Ansicht der Cochrane-Arbeitsgruppe nicht für einen Hinweis auf Wirksamkeit aus [16]. Soweit nachfolgend hierzu Aussagen erwähnt werden, empfiehlt es sich, diese Einschränkung bei der Beurteilung der Wirksamkeit zu berücksichtigen.
Donepezil
In den ersten neun RCTs zu Donepezil konnte eine Wirksamkeit im kognitiven Bereich sowohl für die wahrscheinliche Alzheimer-Krankheit als auch für die vaskuläre Demenz belegt werden. Für NPS und Aktivitäten des täglichen Lebens (ADL) war die Studienlage uneinheitlich. Der klinische Gesamteindruck (CGI) zeigte sich für Donepezil gegenüber Placebo signifikant besser [8].
In der aktuellen Cochrane-Analyse zu Donepezil [6] konnte kein neuer methodisch nachvollziehbarer RCT zur Wirksamkeit gefunden werden. Die beobachteten Nebenwirkungen (s. dort) bewegten sich im zu erwartenden bekannten Rahmen.
Zu anderen Demenzformen sind für Donepezil neuere RCTs zu finden. Die für die Alzheimer-Demenz geltende Aussage eines moderaten Effekts für einzelne Patienten über eine begrenzte Zeit soll demnach auch für die Parkinson-Demenz und die Demenz mit Lewy-Körperchen gelten.
Galantamin
In den ersten sechs RCTs zu Galantamin konnte eine Wirksamkeit im kognitiven Bereich sowohl für die wahrscheinliche Alzheimer-Krankheit als auch für die vaskuläre Demenz belegt werden. Die Studien erfassten eine einheitliche Schweregradgruppe in einem gleichen Alter. Die Aussagen zu Galantamin können daher nur für die Schweregrade GDS 3 bis 5 und für eine Dauer von sechs Monaten eine Wirksamkeit belegen. Für NPS war die Studienlage uneinheitlich, für ADL negativ. Der klinische Gesamteindruck (CGI) zeigte sich für Galantamin gegenüber Placebo signifikant besser. In der Einschätzung der Cochrane-Arbeitsgruppe [5] wurde eine Wirksamkeit bei der Behandlung der vaskulären Demenz gesehen.
Ginkgo-Extrakt
Fünf methodisch qualifizierte RCTs untersuchten den Ginkgo-biloba-Extrakt (EGb761). Im Bereich Kognition konnte in fünf Studien ein signifikant besserer Testwert unter Verum im Vergleich zu Placebo erzielt werden. NPS wurden in zwei RCTs gemessen und ein signifikant besseres Ergebnis unter Verum als unter Placebo erzielt. Für ADL zeigten vier von fünf RCTs eine Überlegenheit. Zum CGI lagen keine Daten vor. Alle Studien schlossen auch Patienten mit vaskulärer Demenz ein, die auch separat analysiert wurden. Das Ergebnis entsprach dem von Patienten mit Alzheimer-Krankheit. In einer dreiarmigen Vergleichsstudie von Donepezil, Ginkgo-biloba-Extrakt und einer Kombination aus beiden, fanden sich keine signifikanten Unterschiede in der Wirksamkeit. Eine differenzierte Analyse findet sich in der WFSBP-Leitlinie.
Memantin
In den ersten neun RCTs fand sich ein Verhältnis von fünf signifikanten zu vier nicht signifikanten Ergebnissen im Bereich der Kognition. Im NPS- und im ADL-Bereich überwog die Anzahl nicht signifikanter Ergebnisse in fünf Studien gegenüber zwei Studien mit signifikanten Ergebnissen. Für den CGI zeigte sich ein Verhältnis von 4 zu 1. Bei Betrachtung des Schweregrads, konnte bei schwerer Erkrankung allerdings eine Überlegenheit von Memantin im kognitiven und NPS-Bereich belegt werden.
Im aktuellen Cochrane-Review [17] wird Memantin bei moderater bis schwerer Demenz eine geringe Wirksamkeit bescheinigt. Soweit stimmt das Ergebnis mit dem der WFSBP-Leitlinie überein. Die analysierte Studienlage bezieht allerdings eine Reihe von RCTs nicht ein.
Auch bei vaskulärer Demenz fand sich unter Memantin ein signifikant besseres Ergebnis als unter Placebo. Für LBD und Parkinson-assoziierte Demenz (PDD) konnten Stubendorff et al. [21] nach 36 Monaten Beobachtungsphase unter Memantin nach vorangehender 6-monatiger RCT eine längere Überlebenszeit feststellen als in der Placebo-Gruppe. Hier greift jedoch die in der Einleitung angeführte methodische Einschränkung.
Rivastigmin
In den ersten vier RCTs erzielte Rivastigmin im kognitiven Bereich signifikant bessere Werte als Placebo. Für eine Wirksamkeit bei NPS liegen keine Hinweise vor. Für ADL wie für den CGI-Bereich fanden sich Hinweise unter methodischen Einschränkungen. Die Ergebnisse wurden bei Patienten mit GDS 5, einem mittleren Alter von 71 bis 75 Jahren über sechs Monate erzielt und können daher auch nur für vergleichbare Gruppen eine Aussage machen. Cochrane-Analysen zur Wirksamkeit bei der Alzheimer-Krankheit und der vaskulären Demenz liegen vor und sehen für beide Erkrankungen Hinweise auf eine Wirksamkeit, berücksichtigen aber leider die benannten limitierenden Studienbedingungen nicht [4, 5].
Kombinationstherapien
Da bei den fünf zugelassenen Substanzen drei unterschiedliche pathophysiologische Behandlungswege genutzt werden, ist zu prüfen, inwieweit eine Kombination zu einem besseren Ergebnis führt. Der Effekt einer Kombination aller drei Zugangswege wurde bisher nicht untersucht. Zu den meisten Zweierkombinationsmöglichkeiten liegen keine Studien vor oder, wenn doch, methodisch begrenzt, beispielsweise indem kein Vergleich zu einer Monotherapie oder Placebo eingeschlossen wurde. Für die Kombination Memantin mit Rivastigmin konnte keine Überlegenheit der Kombination gegenüber einer Monotherapie gezeigt werden. Für eine Aussage zur Wirksamkeit von Kombinationstherapien ist neben den grundlegenden qualitativen Kriterien für RCTs ein Vergleich mit den jeweiligen Monotherapien oder zumindest Placebo zu fordern. Bei Berücksichtigung dieser methodischen Limitierungen können nur sehr eingeschränkte Aussagen zu Kombinationstherapien gemacht werden.
Schlussfolgerungen zur Wirksamkeit in Abhängigkeit von Schweregrad, Diagnose, Altersgruppe oder anderen differenzierenden Variablen sind nicht möglich. Lediglich für die Kombinationen von Donepezil mit Ginkgo-Extrakt oder mit Memantin gibt es Hinweise auf einen möglichen moderaten positiven Effekt. Bei depressiven Patienten ergaben sich Hinweise auf einen positiven Effekt bei einer Kombination von Memantin mit Escitalopram [12, 13]. Ebenfalls Hinweise auf eine kognitive Besserung fanden sich bei Patienten mit Vitamin-D-Mangel und vaskulärer Demenz bei Behandlung über sechs Monate [14].
Nebenwirkungen
Bei nur moderaten Effekten bei einzelnen Patienten als Behandlungserfolg spielt die Abwägung von Risiken und Nutzen eine besondere Rolle. Das Gebot, möglichst geringe Risiken zuzulassen, hat hier ein besonderes Gewicht (Tab. 4).
Tab. 4. Nebenwirkungen von Antidementiva
|
Generischer Name (alphabetische Reihenfolge) |
Kontraindikation |
Übelkeit und gastrointestinale Beschwerden |
Schlaf |
Verhalten |
Neurologie |
Andere |
|
Donepezil |
Hypersensitivität gegenüber Piperidin-Derivaten |
Diarrhö, Übelkeit, Erbrechen, Appetitverlust, gastrointestinale Beschwerden |
Müdigkeit, Schlaflosigkeit |
Halluzinationen, Agitation, aggressives Verhalten |
Kopfschmerz, Muskelkrämpfe, Synkope, Schwindel, Kopfschmerz |
Erkältung, Unfälle, Hautaus-schlag, Inkontinenz der Blase, Dyspnoe |
|
Galantamin |
Schwere Leber- und Nierenstörungen |
Übelkeit, Erbrechen, verringerter Appetit, Gewichtszunahme, Bauchschmerzen, Dyspepsie, gastrointestinale Beschwerden |
Schlaflosigkeit, Somnolenz |
Asthenie, Konfusion, Depression, Fatigue, Unwohlsein |
Schwindel, Synkope, Tremor, Kopfschmerz |
Rhinitis, urogenitale Infektionen, Fieber, Stürze, Verletzungen, Dyspnoe |
|
Ginkgo-biloba-Extrakt (EGb761) |
Keine |
Keine |
Keine |
Keine |
Keine |
Keine |
|
Memantin |
Schwere Leber- und Nierenstörungen |
Verstopfung |
Müdigkeit |
Irritabilität |
Schwindel, Kopfschmerz |
Erhöhter Blutdruck |
|
Rivastigmin |
Schwere Leberstörung, Hypersensitivität bei Carbamat-Derivaten |
Übelkeit, Erbrechen, Diarrhö, Appetitverlust, Bauchschmerzen, Dyspepsie, Gewichtsverlust |
Somnolenz, Müdigkeit |
Agitation, Konfusion, Asthenie |
Schwindel, Kopfschmerz, Tremor, Synkope |
Vermehrtes Schwitzen, Dyspnoe |
Nebenwirkungen mit einer Wahrscheinlichkeit von >10 % sind in fetter Schrift hervorgehoben. Eine umfassende Darstellung findet sich in den Fachinformationen.
Beginn und Beendigung der Therapie
Angaben zur üblichen Dosierung der besprochenen Antidementiva zu Therapiebeginn und im Verlauf sind in Tabelle 5 zusammengefasst.
Tab. 5. Dosierung von Antidementiva
|
Generischer Name |
Therapiebeginn |
Standarddosis [mg/d] |
|
Donepezil |
5 mg die ersten 4 Wochen |
10 |
|
Galantamin |
8 mg die ersten 4 Wochen |
24 |
|
Ginkgo-biloba-Extrakt |
240 mg |
240 |
|
Memantin |
5 mg (wöchentlich +5 mg) |
20 |
|
Rivastigmin |
3 mg (2 × 1,5 mg) für 2 Wochen 4,6-mg-Pflaster |
9,2 12 |
Alle Entscheidungen zu Beginn, Änderung und Beendigung der Therapie sind grundsätzlich individuell und mit den primären Bezugspersonen abzustimmen [19]. Da eine präventive Wirkung für keine der Substanzen belegt werden konnte, ist es sinnvoll, die Therapie direkt nach der Diagnosesicherung zu beginnen. Studien zu Auswirkungen unterschiedlicher Beginnzeitpunkte liegen nicht vor. Aussagen zum Beginn lassen sich daher am ehesten durch „Extrapolieren“ von Studienergebnissen und die Beurteilung von Nebenwirkungen gewinnen. Durchgängig nebenwirkungsarm ist der Ginkgo-biloba-Extrakt (Tab. 4), der damit risikoarm zu Beginn eingesetzt werden kann. Etwa ein Drittel der Patienten verträgt Cholinesterasehemmer meist aufgrund gastrointestinaler Nebenwirkungen nicht. Auch hier ist in frühen Stadien Ginkgo-biloba-Extrakt eine Alternative. Schreitet die Erkrankung fort, ist auch für Memantin Wirksamkeit belegt. Es kommt damit ab mittelschwerer Demenz in Betracht (Reisberg-Stadium 5 und höher).
Es empfiehlt sich, das Ende der Therapie mit der primären Versorgungsperson abzustimmen. Solange die subjektive Wahrnehmung der primären Versorgungsperson einen positiven Nutzen erkennen lässt, sollte die Therapie beibehalten werden bzw. bei Fehlen abgesetzt. Unterstützend können valide testpsychologische Kontrolluntersuchungen herangezogen werden, beispielsweise mit DemTect (Demenz-Detektionstest) oder TFDD (Test zur Früherkennung von Demenzen mit Depressionsabgrenzung). Hinweise darauf, dass nach Absetzen und Wiederansetzen das Niveau von vorher nicht mehr erreicht werden kann, sollten mit abgewogen werden [22]. Auch hier sind die Effekte allerdings als gering einzuschätzen.
Zusammenfassung
Vor einer medikamentösen Therapie der Demenz stehen die Abklärung und gegebenenfalls Behandlung anderer Krankheiten, die Stabilisierung metabolischer Prozesse wie eines Vitamin-B12-Mangels und das Berücksichtigen von Nebenwirkungen, beispielsweise von Cortison. Ist die Diagnose einer Demenz gestellt, gilt es, für die Medikationsauswahl den Schweregrad zu bestimmen (Abb. 3).

Abb. 3. Therapeutische Aspekte von Antidementiva
In den letzten zehn Jahren hat sich die Therapie der Demenzen nur in Nuancen verändert. Die Studiendaten belegen die Wirksamkeit von fünf Medikamenten (Donepezil, Galantamin, Ginkgo-biloba-Extrakt, Memantin und Rivastigmin) für die Alzheimer-Krankheit. Soweit Studien zu vaskulären Demenzformen durchgeführt wurden, entsprachen die Ergebnisse meist denen zur Alzheimer-Demenz. Sie lassen bei einzelnen Patienten einen moderaten Effekt über eine begrenzte Zeit erwarten, bei Memantin erst bei Vorliegen eines zumindest mittleren Schweregrads. Das gilt in meist vernachlässigbar unterschiedlichem Umfang für kognitive Symptome, neuropsychiatrische Störungen, Aktivitäten des Alltags und den klinischen Gesamteindruck. Diesen Belegen stehen differenzierte Belege zu vereinzelt sogar vital gefährdenden Nebenwirkungen gegenüber. Die Schaden-Nutzen-Abwägung steht daher mit hohem Gewicht an erster Stelle. Ein Therapieende sollte erst nach Einholen einer Beurteilung durch die primäre Pflegeperson und unter Einbezug testpsychologischer Daten von beispielsweise DemTect oder TFDD erfolgen. Die Datenlage zu anderen Demenzformen lässt eine hinreichend begründete Aussage derzeit nicht zu.
Interessenkonflikterklärung
RI: Publikationshonorare u. a. von Via Salus GmbH und Qualworld, Forschungsbeihilfe von der EU (Projekt Certification-D) und Pflegeselbsthilfekontaktbüro
WEM: Vortrags-und Beratungstätigkeit für Dr. W. Schwabe, Karlsruhe
Literatur
1. American Psychiatric Association. Diagnostic and Statistical Manual of Mental Disorders. 5th edition. Washington DC, 2013.
2. Benkert O, Hippius H (Hrsg.). Kompendium der Psychiatrischen Pharmakotherapie. 12. Auflage. Heidelberg: Springer, 2019.
3. Birks J, Craig D. Galantamine for vascular cognitive impairment. Cochrane Database Syst Rev 200;(4):CD004746.
4. Birks JS, Grimley Evans J. Rivastigmine for Alzheimer’s disease. Cochrane Database Syst Rev 2015;(4):CD001191.
5. Birks J, McGuinness B, Craig D. Rivastigmine for vascular cognitive impairment. Cochrane Database Syst Rev 2013;(5):CD004744.
6. Birks JS, Harvey RJ. Donepezil for dementia due to Alzheimer’s disease. Cochrane Database Syst Rev 2018;6(6):CD001190.
7. Gilstad JR, Finucane TE. Results, rhetoric, and randomized trials: the case of donepezil. J Am Geriatr Soc 2008;56:1556–62.
8. Ihl R, Frölich L, Winblad B, Schneider L, et al.; WFSBP Task Force on Treatment Guidelines for Alzheimer’s Disease and other Dementias. World Federation of Societies of Biological Psychiatry (WFSBP) guidelines for the biological treatment of Alzheimer’s disease and other dementias. World J Biol Psychiatry 2011;12:2–32.
9. Ihl R, Bunevicius R, Frölich L, Winblad B, et al.; WFSBP Task Force on Mental Disorders in Primary Care; WFSBP Task Force on Dementia. World Federation of Societies of Biological Psychiatry guidelines for the pharmacological treatment of dementias in primary care. Int J Psychiatry Clin Pract 2015;19:2–7.
10. Jessen F, Amariglio RE, van Boxtel M, Breteler M, et al.; Subjective Cognitive Decline Initiative (SCD-I) Working Group. A conceptual framework for research on subjective cognitive decline in preclinical Alzheimer’s disease. Alzheimers Dement 2014;10:844–52.
11. Kobayashi H, Ohnishi T, Nakagawa R, Yoshizawa K. The comparative efficacy and safety of cholinesterase inhibitors in patients with mild-to-moderate Alzheimer’s disease: a Bayesian network meta-analysis. Int J Geriatr Psychiatry 2016;31:892–904.
12. Krause-Sorio B, Siddarth P, Kilpatrick L, et al. Combined treatment with escitalopram and memantin increases gray matter volume and cortical thickness compared to escitalopram and placebo in a pilot study of geriatric depression. J Affect Disord 2020;274:464–70.
13. Lavretsky H, Laird KT, Krause-Sorio B, et al. A randomized double-blind placebo-controlled trial of combined escitalopram and memantin for older adults with major depression and subjective memory complaints. Am J Geriatr Psychiatry 2020;28:178–90.
14. Lemire P, Brangier A, Beaudenon M, Duval GT, et al. Cognitive changes under memantin according to vitamin D status in Alzheimer patients: An exposed/unexposed cohort pilot study. J Steroid Biochem Mol Biol 2018;175:151–6.
15. Lewczuk P, Riederer P, O’Bryant SE, Verbeek MM, et al.; Members of the WFSBP Task Force Working on this Topic: Peter Riederer, Carla Gallo, Dimitrios Kapogiannis, Andrea Lopez Mato, Florence Thibaut. Cerebrospinal fluid and blood biomarkers for neurodegenerative dementias: An update of the Consensus of the Task Force on Biological Markers in Psychiatry of the World Federation of Societies of Biological Psychiatry. World J Biol Psychiatry 2017;27:1–85.
16. Li Y, Hai S, Zhou Y, Dong BR. Cholinesterase inhibitors for rarer dementias associated with neurological conditions. Cochrane Database Syst Rev 2015;(3):CD009444.
17. McShane R, Westby MJ, Roberts E, et al. Memantin for dementia. Cochrane Database Syst Rev 2019;3(3):CD003154.
18. Müller WE, Eckert A, Eckert GP, et al. Therapeutic efficacy of the Ginkgo special extract EGb761® within the framework of the mitochondrial cascade hypothesis of Alzheimer’s disease. World J Biol Psychiatry 2019;20:173–89.
19. Parsons C. Withdrawal of antidementia drugs in older people: Who, when and how? Drugs Aging 2016;33:545–56.
20. Reisberg B, Ferris SH, de Leon MJ, Crook T. Global deterioration scale (GDS). Psychopharmacol Bull 1988;24:661–3.
21. Stubendorff K, Larsson V, Ballard C, Minthon L, et al. Treatment effect of memantin on survival in dementia with Lewy bodies and Parkinson’s disease with dementia: a prospective study. BMJ Open 2014;4:e005158. Published 2014 Jul 3; doi:10.1136/bmjopen-2014-005158.
22. Tariot PN. Cessation of donepezil is associated with clinical decline in patients with moderate-to-severe Alzheimer’s disease compared to continuation of donepezil or addition or substitution of Memantin. Evid Based Med 2013;18:62–3.
Prof. Dr. med. Ralf Ihl, Demenz Forschungszentrum Alexianer Krefeld GmbH, Dießemer Bruch 81, 47805 Krefeld, E-Mail: r.ihl@alexianer.de
Prof. Dr. Walter E. Müller, Höhenstraße 49A, 67550 Worms
Psychopharmakotherapie 2020; 27(05):247-254
