Sebastian Wurthmann, Michael Nsaka, Armin Scheffler und Dagny Holle, Essen
Calcitonin Gene-related Peptide (CGRP) ist ein Neuropeptid, welches eine wesentliche Rolle in der Pathophysiologie der Migräne spielt. Die ersten Grundlagen-Studien zu seiner Bedeutung in der Migräne stammen aus den 1980er-Jahren. Diese Erkenntnisse mündeten in klinische Studien, die die Wirksamkeit und Verträglichkeit von CGRP-Antagonisten in der Migränetherapie untersuchten. Dabei traten jedoch bei einigen Patienten deutliche Leberwert-Erhöhungen auf, sodass dieser Therapieweg zunächst verlassen wurde. Seit einiger Zeit stehen nun Antikörper gegen CGRP bzw. den Rezeptor des CGRP zur Verfügung (Tab. 1). Leberwerterhöhungen sowie schwerwiegendere andere Nebenwirkungen sind bislang weder in den klinischen Studien noch in der Anwendung in der Praxis aufgetreten. Die Einführung der CGRP-Antikörper stellt einen wichtigen Meilenstein in der Prophylaxe der Migräne dar, da nun zum ersten Mal ein spezifischer Therapieansatz zur Verfügung steht. Die bislang eingesetzten First-Line-Therapien (Metoprolol, Propranolol, Flunarizin, Topiramat, Valproinsäure, Amitriptylin, Botulinumtoxin A) sind allesamt Medikamente, die verschiedenste Wirkungsmechanismen aufweisen und als „Nebenwirkung“ auch noch zu einer Migräne-Reduktion führen können. Diese Medikamente sind mit verschiedenen Nebenwirkungen verbunden, beispielsweise Müdigkeit, Gewichtszunahme oder kognitiven Störungen, was häufig die Compliance der Medikamenteneinnahme erheblich vermindert. Die schlechte Compliance wird häufig noch dadurch verstärkt, dass bei Einnahme der „alten“ Migräneprophylaktika die Wirksamkeit erst nach vier bis acht Wochen einsetzt, die Nebenwirkungen häufig aber schon ab dem ersten Tage wahrzunehmen sind. Für die CGRP-(Rezeptor-)mAB konnte nun ein deutlich früherer Wirkeintritt, teilweise schon in der ersten Therapiewoche, nachgewiesen werden.
Tab. 1. Übersicht über die aktuell zur Migränetherapie zur Verfügung stehenden monoklonalen Antikörper
|
Wirkstoff |
Handelsname |
Target |
Dosierung |
Dosierintervall |
Jahrestherapiekosten* |
|
Erenumab |
Aimovig® |
Rezeptor |
70 mg oder 140 mg s. c. |
Alle 4 Wochen |
6188,74 EUR |
|
Fremanezumab |
Ajovy® |
Ligand |
225 mg s. c. |
Monatlich |
5379,20 EUR |
|
625 mg s. c. |
Alle 3 Monate |
||||
|
Galcanezumab |
Emgality® |
Ligand |
Starterdosis: 240 mg s. c. Dann 120 mg |
Monatlich |
1. Jahr: 6188,74 EUR ab 2. Jahr: 5712,68 EUR |
|
Eptinezumab** |
Vyepti™ |
Ligand |
100 mg i. v. |
Alle 3 Monate |
* Lauer-Taxe, VK, Stand 15.08.2020; ** Zulassung in USA
Erenumab
Erenumab (Aimovig®) ist der erste in Deutschland zugelassene monoklonale Antikörper gegen den CGRP-Rezeptor, der zur Migräneprophylaxe zur Verfügung stand. Erenumab wirkt im Gegensatz zu den anderen monoklonalen Antikörpern, die zur Migräneprophylaxe zugelassen sind, direkt am CGRP-Rezeptor, während die anderen am CGRP-Liganden wirken.
Die subkutane (s. c.) Gabe von Erenumab erfolgt in einem Dosisintervall von vier Wochen. Es stehen zwei unterschiedliche Dosierungen mit 70 mg und 140 mg zur Verfügung. Positive Studienergebnisse liegen sowohl für die episodische als auch die chronische Migräne vor.
Die Wirksamkeit von Erenumab bei der episodischen Migräne wurde in zwei Phase-III-Studien untersucht. In der STRIVE-Studie wurde bei 955 Patienten 70 mg oder 140 mg Erenumab s. c. oder ein Placebo einmal monatlich über einen Zeitraum von sechs Monaten angewandt [17]. In der ARISE-Studie wurden 577 Patienten mit episodischer Migräne mit 70 mg Erenumab s. c. einmal im Monat über drei Monate behandelt [10]. In der Verum-Gruppe ließ sich jeweils eine signifikante Reduktion der Migränetage pro Monat feststellen (Tab. 2). Die 50%-Responderrate, die ein Maß für das Ansprechen im Sinne einer Reduktion der monatlichen Migränetage um 50 % darstellt, war dementsprechend jeweils deutlich höher als in der Placebo-Gruppe (Tab. 2).
Tab. 2. Ergebnisse mit Erenumab zur Prophylaxe der episodischen und chronischen Migräne
|
Studie |
Endpunkt |
70 mg Erenumab |
140 mg Erenumab |
Placebo |
|
STRIVE (episodische Migräne) [17] |
Reduktion der Migränetage (initial 8,3 Tage/Monat) |
–3,2 Tage/Monat |
–3,7 Tage/Monat |
–1,6 Tage/Monat |
|
50%-Responderrate |
43,4 % |
50,0 % |
26,6 % |
|
|
ARISE (episodische Migräne) [10] |
Reduktion der Migränetage (initial 8,2 Tage/Monat) |
–2,9 Tage/Monat |
–1,8 Tage/Monat |
|
|
50%-Responderrate |
39,7 % |
29,5 % |
||
|
Tepper et al. (chronische Migräne) [34] |
Reduktion der Migränetage |
–6,6 Tage/Monat |
–6,6 Tage/Monat |
–4,2 Tage/Monat |
|
50%-Responderrate |
40 % |
41 % |
23 % |
Erenumab wurde auch bei Patienten mit chronischer Migräne evaluiert, wobei die Dosierung von 70 mg im Vergleich zu 140 mg und mit Placebo untersucht wurde [34]. In die Studie wurden 667 Patienten eingeschlossen. Nach 12 Wochen ließ sich in beiden Dosierungen eine signifikante Reduktion der Migränetage um 6,6 Tage und eine 50%-Responderrate von circa 40 % feststellen (Tab. 2).
Die Reduktion der Einnahmetage von Akutmedikamenten ist ein wichtiger Faktor, um Komplikationen, wie Kopfschmerzen durch Medikamentenübergebrauch, zu minimieren. Erenumab konnte sowohl bei Patienten mit episodischer, als auch bei chronischer Migräne eine Abnahme der Einnahmetage der Akuttherapie bewirken [10, 17, 23]. Ferner konnte eine Wirksamkeit bei Migränepatienten nachgewiesen werden, die zuvor mit zwei bis vier anderen etablierten Migräneprophylaktika (z. B. Amitriptylin) behandelt worden waren, und bei denen sich unter diesen Substanzen keine Besserung der Migräne zeigte. Demnach lag nach 12 Wochen Therapie eine 50%-Responderrate bei 30 % der mit Erenumab behandelten Patienten und bei 14 % der Placebo-Gruppe vor [23].
Die Wirksamkeit von Erenumab setzt im Vergleich zu konventionellen, Migräne-unspezifischen Prophylaktika in indirekten Vergleichen deutlich früher ein, bereits nach einer Woche lassen sich Effekte auf die Migränefrequenz feststellen [25]. Es wird empfohlen, eine Behandlung mit Erenumab über mindestens drei Monate erfolgen zu lassen und bei Wirksamkeit nach etwa sechs bis neun Monaten zu überprüfen, ob sie noch notwendig ist [9].
Das Nebenwirkungsprofil von Erenumab ist mit dem von Placebo vergleichbar: Atemwegsinfekte, lokaler Injektionsschmerz und Obstipationen sind die am häufigsten beklagten Nebenwirkungen [1, 10]. In seltenen Fällen kann es zu einer schweren Obstipation kommen.
Fremanezumab
Fremanezumab ist ein mAB, der gegen den CGRP-Liganden gerichtet und zur Prophylaxe der episodischen und chronischen Migräne zugelassen ist.
Die Gabe von Fremanezumab erfolgt subkutan. Es stehen zwei unterschiedliche Dosierungen mit 225 mg und 675 mg zur Verfügung. Die Besonderheit an dieser Substanz ist, dass sie monatlich (225 mg) oder einmal im Quartal (675 mg) appliziert werden kann.
Im Rahmen der HALO-Studie zeigte sich mit beiden Dosierungsregimes nach einer Behandlungsdauer von 12 Wochen eine Reduktion der monatlichen Migränetage um rund vier Tage (Tab. 3) [12]. Die 50%-Responderraten waren bei der monatlichen Gabe etwas höher als bei der einmaligen Gabe im Quartal (Tab. 3).
Tab. 3. Ergebnisse mit Fremanezumab zur Prophylaxe der episodischen und chronischen Migräne
|
Studie |
Endpunkt |
Fremanezumab |
Fremanezumab |
Placebo |
|
HALO (episodische Migräne) [12] |
Reduktion der Migränetage |
–4 Tage/Monat |
–3,9 Tage/Monat |
–2,6 Tage/Monat |
|
50%-Responderrate |
47,7 % |
44,4 % |
27,9 % |
|
|
HALO-C (chronische Migräne) [27] |
Reduktion der Migränetage |
–5,3 Tage/Monat |
–5,2 Tage/Monat |
–3,6 Tage/Monat |
|
50%-Responderrate |
41 % |
38 % |
18 % |
* In HALO-C mit einmaliger Loading-Dosis von 675 mg
In der HALO-C-Studie wurden Patienten mit chronischer Migräne über 12 Wochen behandelt [27]. Hierbei erfolgte entweder eine monatliche Gabe von 225 mg Fremanezumab mit einer einmaligen Loading-Dosis von 675 mg oder eine Therapie mit 675 mg einmal im Quartal. Auch bei diesem Patientenkollektiv zeigte sich eine deutliche Reduktion der Migränetage im Monat mit beiden Fremanezumab-Dosierungsregimes (Tab. 3). Die 50%-Responderraten betrugen etwa 40 % bei dem Wirkstoff vs. 18 % bei Placebo (Tab. 3).
Auch durch die Therapie mit Fremanezumab zeigte sich also eine deutliche Besserung der monatlichen Migränetage. Ferner nahm die Anzahl der Einnahmetage der Akutmedikamente im Monat mit etwa drei Tagen in beiden Dosierungsregimes ab [12]. Eine Wirksamkeit der Therapie mit Fremanezumab (monatlich oder quartalsweise verabreicht) bei episodischer sowie chronischer Migräne konnte auch nachgewiesen werden, wenn in den vergangenen zehn Jahren zwei bis vier etablierte Migräneprophylaxen in diesem Kollektiv unwirksam waren. Die Wirksamkeit von Fremanezumab auf die Migränefrequenz setzt vergleichbar frühzeitig (siehe z. B. Erenumab) schon innerhalb der ersten Wochen ein [5] und unterscheidet sich hierdurch erheblich von den bislang gängigen „klassischen“ zur Migräneprophylaxe eingesetzten Substanzen. Die Verträglichkeit und die Sicherheit von Fremanezumab sind gut und Nebenwirkungen waren zumeist eher mild ausgeprägt, wie Rötung oder Schmerzen an der Injektionsstelle oder Nasopharyngitiden [28].
Galcanezumab
Galcanezumab (Emgality®) ist ein humanisierter monoklonaler Antikörper gegen CGRP. Während der Versuch, Galcanezumab in der Behandlung der Osteoarthritis einzusetzen [4], nicht erfolgreich war [18], zeigte sich in den Phase-II-Studien ein positiver Effekt in der prophylaktischen Behandlung der episodischen Migräne [11, 31]. Behandlungsabhängige Nebenwirkungen waren vorwiegend leicht (lokaler Schmerz an der Einstichstelle, Infektionen der oberen Atemwege insbesondere Nasopharyngitis und Rückenschmerzen).
In der Phase-III-Studie EVOLVE-1 wurden 858 Patienten mit episodischer Migräne über einen Zeitraum von sechs Monaten in drei Gruppen (monatlich 120 mg mit einer initialen Loading-Dose von 240 mg, monatlich 240 mg sowie Placebo) untersucht. In der ersten Gruppe (die derzeit zugelassene und empfohlene Dosierung) zeigte sich eine signifikante Reduktion der monatlichen Migränetage (MMT) (Tab. 4; Differenz zur Placebo-Gruppe: –1,9 Prozentpunkte; 95%-Konfidenzintervall [KI] –2,5 bis –1,4; p < 0,001). Im Vergleich zur monatlichen Gabe von 240 mg ergaben sich keine wesentlichen Unterschiede. Die 50%-Responderrate der MMT betrug 62,3 % (Placebo: 38,6 %). Als Nebenwirkungen wurden erneut vorwiegend lokale Reaktionen bzw. Schmerzen an der Einstichstelle, eine Nasopharyngitis sowie Harnwegsinfekte beschrieben. In der höheren Dosierung von 240 mg pro Monat kam es vermehrt zu Juckreiz im Vergleich zu Placebo [32].
Tab. 4. Ergebnisse mit Galcanezumab zur Prophylaxe der episodischen und chronischen Migräne
|
Studie |
Endpunkt |
Galcanezumab |
Galcanezumab |
Placebo |
|
EVOLVE-1 (episodische Migräne) [32] |
Reduktion der Migränetage |
–4,7 Tage/Monat |
–4,6 Tage/Monat |
–2,8 Tage/Monat |
|
50%-Responderrate |
62.3 % |
60,9 % |
38,6 % |
|
|
EVOLVE-2 (episodische Migräne) [22] |
Reduktion der Migränetage |
–4,3 |
–4,2** |
–2,3 |
|
50%-Responderrate |
59,3 % |
56,5 %** |
36,0 % |
|
|
REGAIN (chronische Migräne) [15] |
Reduktion der Migränetage |
–4,8 |
–4,2** |
–2,7 |
|
50%-Responderrate |
27,6 % |
27,5 %** |
15,4 %** |
* Initiale Loading-Dose 240 mg
** Werte dem EPAR entnommen [12a]
In der EVOLVE-2-Studie wurden 915 Patienten mit einer episodischen Migräne in dieselben drei Gruppen eingeteilt und ebenfalls über sechs Monate beobachtet. Erneut zeigte sich ein ähnlich gutes Ansprechen in der 120-mg-Gruppe mit einer signifikanten Reduktion der MMT im Vergleich zum Placebo-Arm (Tab. 4; Differenz: –2,0 Prozentpunkte; 95%-KI –2,6 bis –1,5; p < 0,001). Wieder zeigten sich keine deutlichen Unterschiede im Vergleich zur höheren monatlichen Dosis von 240 mg. Die 50%-Responderrate war vergleichbar zur EVOLVE-1-Studie (Tab. 4). Kumulativ konnte eine 50%-Responderrate von 56,5 % nach sechs Monaten berechnet werden, wobei die Rate nach jedem behandelten Monat zunahm [15]. Die aufgetretenen Nebenwirkungen waren mit der EVOLVE-1-Studie vergleichbar [30], eine Analyse (einschließlich der REGAIN-Studie [s. u.]) ergab keinen Hinweis auf ein erhöhtes kardiovaskuläres Risiko [22]. Eine Subgruppenanalyse ergab eine Wirksamkeit sowohl für die hochfrequente (8 bis 14 MMT) als auch für weniger frequente (4 bis 7 MMT) Migräne [29]. Ein früher Wirkeintritt innerhalb der ersten Woche [16], theoretisch bereits ab Tag 1 nach der Injektion [8], war möglich. In der Nachbeobachtung beider EVOLVE-Studien zeigte sich nach Beendigung der Behandlung (vier Monate nach Beendigung, also zehn Monate nach Beginn der Behandlung) eine stetige Abnahme der Wirkung [33].
In der REGAIN-Studie wurde die Wirksamkeit von Galcanezumab in der Behandlung der chronischen Migräne an 1113 Patienten in einem Beobachtungszeitraum von drei Monaten untersucht. Unter monatlich 120 mg Galacanezumab (Loading-Dose 240 mg) kam es nach dreimonatiger Behandlung im Mittel zu einer signifikanten Reduktion der MMT im Vergleich zur Placebo-Gruppe (Tab. 4; Differenz: –2,1 Prozentpunkte; 95%-KI –2,9 bis –1,3; p < 0,001). Die 50%-Responderrate bezogen auf die monatlichen Migränetage betrug im Mittel 27,6 %, im dritten Behandlungsmonat kumulativ 30,2 % [15]. Die Gruppe, die monatlich 240 mg erhielt, zeigte keine wesentlichen Unterschiede bezüglich der Wirksamkeit im Vergleich zur niedrigen Dosis (Tab. 4). Als Nebenwirkungen wurden das Auftreten einer Nasopharyngitis und weitere Infekte der oberen Atemwege sowie lokale Reaktion an der Injektionsstelle wie Schmerz, Juckreiz und Rötung beschrieben (mit einer Tendenz eines häufigeren Auftretens in der Gruppe mit 240 mg monatlich). Eine geringe Identifikation von Medikamenten-Antikörpern hatte (zumindest in dem 3-monatigen Untersuchungszeitraum) zu keinem Wirkverlust geführt. Die Ergebnisse einer 9-monatigen Open-Label-Phase stehen noch aus [7].
Daher liegen Daten zur längeren Behandlung mit Galcanezumab bislang kaum vor. Eine Open-Label-Studie mit 270 Patienten, die über 12 Monate entweder mit 120 mg oder mit 240 mg Galcanezumab behandelt wurden, konnte den positiven Effekt und die Verträglichkeit des Medikaments bestätigen. Es zeigten sich eine etwas deutlichere Reduktion der MMT im Vergleich zu den Zulassungsstudien und etwas bessere Ergebnisse in der 240-mg-Gruppe im Vergleich zu der Gruppe, die mit 120 mg monatlich behandelt wurde (MMT-Reduktion im Mittel nach 12 Monaten: 120 mg: –5,6 [SD: 0,34], 240 mg: –6,5 [SD: 0,33]; 50%-Responderrate 120 mg: 65,6 %, 240 mg: 73,7 %). Hier müssen jedoch die studienbedingt fehlende Kontrollgruppe, die fehlende Unterscheidung in chronische und episodische Migräne und das kleinere Patientenkollektiv berücksichtigt werden [6]. Die Behandlung ging jedoch mit einer hohen Patientenzufriedenheit einher [14]. Auch in der längeren Behandlung von einem Jahr scheint das Medikament weiterhin gut vertragen zu werden [3].
Über die bereits abgeschlossene dreimonatige Phase-III-Studie (CONQUER) an Patienten mit therapieresistenter episodischer Migräne liegen bislang noch keine endgültigen Daten vor. Allerdings zeigen erste Auswertungen die Wirksamkeit auch bei diesem Patientenkollektiv [21]. Eine Studie an Kindern zwischen 6 und 17 Jahren mit episodischer Migräne (REBUILD) soll Mitte des Jahres 2023 beendet sein.
Eptinezumab
Eptinezumab (Vyepti™), ein monoklonaler Antikörper, der Calcitonin Gene-related Peptide (CGRP) angreift, gilt als eine Erfolg versprechende Migräneprophylaxe. Die Zulassung von Eptinezumab in Europa ist noch ausstehend. Es bleibt weiter abzuwarten, wie sich Eptinezumab in der heutigen Wettbewerbssituation der CGRP-mABs darstellt. Auf molekularer Ebene hat Eptinezumab gegenüber den anderen CGRP-mABs den Vorteil, dass es mit einer tmax von 4,8 Stunden am schnellsten wirkt [26].
Eptinezumab ist der erste und einzige monoklonale Antikörper, der intravenös verabreicht werden darf. Hiermit bietet Eptinezumab einen Vorteil für Patienten, die sich regelmäßige ärztliche Gespräche wünschen. Die empfohlene Dosis beträgt 100 mg im dreimonatigen Intervall. Einige Patienten können möglicherweise von einer Dosis von 300 mg profitieren [31]. Gemäß Fachinformation soll Eptinezumab über 30 Minuten in 100 ml isotoner Natriumchloridlösung 0,9 % verdünnt werden (Lundbeck Seattle BioPharmaceuticals, Inc. 11804 North Creek Parkway South Bothell, WA 98011 USA, Initial U.S. Approval: 2020). Die Wirksamkeit und Sicherheit von Eptinezumab wurde in zwei klinischen Studien der Phase III (PROMISE-1 bei episodischer Migräne und PROMISE-2 bei chronischer Migräne) nachgewiesen [2, 19].
In der PROMISE-1-Studie, einer multizentrischen Doppelblindstudie (n = 665), konnte bei Patienten, die an episodischer Migräne leiden, eine Reduktion der Migränetage (MMD) um 3,9 bei einer Dosis von 100 mg und um 4,3 bei 300 mg gezeigt werden (p = 0,0182; Placebo –3,2; p = 0,0001). Die 50%-Responderraten lagen bei 49,8 % (100 mg) vs. 56,3 % (300 mg) vs. 37,4 % für Placebo [31, 32]. Die am häufigsten berichteten unerwünschten Arzneimittelwirkungen waren Nasopharyngitis (100 mg, 9,9 %; 300 mg, 10,3 %; Placebo, 7,2 %) und Fatigue (100 mg, 3,6 %; 300 mg, 3,6 %; Placebo < 1 %) [2].
Die PROMISE-2-Studie befasste sich mit an chronischer Migräne und Medikamentenübergebrauchskopfschmerzen (MOH) leidenden Patienten [19]. Es lässt sich anhand der randomisierten kontrollierten Studie (n = 1072) von Richard B. Lipton et al. belegen, dass mit Eptinezumab eine Reduktion der Kopfschmerztage bzw. Migräne- und MOH-Tage gegenüber Placebo erzielt werden kann. Die 50%-Responderraten lagen bei 57,6 % (100 mg) vs. 61,4 % (300 mg) vs. 39,3 % (Placebo). Ebenfalls ist festzustellen, dass bereits am ersten Tag nach Therapieinitiierung ein Nachweis für einen therapeutischen Effekt vorlag, welcher über 24 Wochen anhielt [19].
Anwendung der CGRP-(Rezeptor-)mAB im Alltag
Bislang ist die Anwendung der CGRP-(Rezeptor-)mAB in Deutschland überwiegend auf therapierefraktäre Patienten beschränkt, da die gesetzlichen Krankenkassen aktuell die Therapiekosten (Tab. 1) nur für diejenigen Patienten übernehmen, die auf sämtliche First-Line-Therapien nicht respondiert haben, diese nicht vertragen haben oder bei denen hierfür Kontraindikationen bestehen. Konkret bedeutet dies, dass Patienten vor Beginn einer Therapie mit mABs Amitriptylin, Betablocker (Metoprolol, Propranolol), Flunarizin, Topiramat und Botulinumtoxin A [für chronische Migräne]) ausprobiert haben müssen. Das gilt nicht mehr für Valproinsäure: Diese darf nach aktuellem Beschluss des Gemeinsamen Bundesausschusses erst dann off Label zur Migräneprophylaxe verordnet werden, wenn alle anderen dafür zugelassenen Arzneimittel einschließlich der CGRP-(Rezeptor-)mAB nicht erfolgreich waren oder kontraindiziert sind [15a].
Die Therapie mit CGRP-(Rezeptor-)mAB ist ab 18 Jahren zugelassen, Daten für Patienten über 65 Jahre liegen nur eingeschränkt vor. Grundsätzlich besteht die Möglichkeit die Therapie auch mit höheren Dosen, z.B. mit Erenumab (140 mg) oder der 675-mg-Dosis Fremanezumab bei dreimonatlicher Gabe zu beginnen. Die Autoren dieser Arbeit empfehlen jedoch aufgrund des ohnehin raschen Wirkungseintritts mit der jeweiligen niedrigeren Dosis zu beginnen und erst nach 12 Wochen eine Wirksamkeitsbeurteilung und ggf. Aufdosierung vorzunehmen. Die Therapie sollte nicht während der Schwangerschaft oder Stillzeit eingesetzt werden. Ferner sollte bei Frauen im gebärfähigen Alter von einer dreimonatigen Behandlung ohne adäquate Kontrazeption abgesehen werden [9].
Klare Kontraindikationen für den Einsatz von mAB liegen aktuell nicht vor, zumal in den randomisierten Studien Patienten mit Autoimmunerkrankungen oder schweren kardiovaskulären Erkrankungen von der Studienteilnahme ausgeschlossen wurden. Allerdings sollte bei Patienten mit zusätzlichen Autoimmunerkrankungen – z. B. der Haut oder des Gastrointestinaltrakts – oder mit ausgeprägtem kardiovaskulären Risikoprofil der Einsatz in einem spezialisierten Zentrum evaluiert werden, da CGRP in diesen klinischen Konstellationen möglicherweise einen protektiven Effekt haben könnte.
Aktuell liegen keine Head-to-Head-Studien zwischen den mAB vor. Auch die Nebenwirkungen der drei mAB sind vergleichbar, sodass in der Anwendung aktuell keiner der drei mAB favorisiert werden kann. Die ersten Real-World-Daten aus Deutschland bestätigen das Wirksamkeitsprofil der Zulassungsstudien [24].
Bislang wurden noch keine unerwünschten Arzneimittelwirkungen (UAW) im zentral-nervösen System bei der Therapie mit CGRP-(Rezeptor-)mAB beobachtet. Jedoch wurde kürzlich erstmalig eine Kasuistik mit schwerer Wundheilungsstörung in Assoziation zu einer CGRP-Rezeptor-Antikörper-Therapie als systemische Nebenwirkung beschrieben [35].
Die deutschen Therapieleitlinien empfehlen, die mAB zunächst für drei Monate einzusetzen und dann das Therapieansprechen zu prüfen [20] (Abb. 1). Eine Wirksamkeit kann dann attestiert werden, wenn die Migränefrequenz reduziert ist. Daneben kann diese auch mit signifikanter Besserung in Lebensqualitäts-Fragebögen nachgewiesen werden. Bei guter Wirksamkeit sollte die Therapie zunächst für sechs bis neun Monate fortgesetzt werden. Danach wird eine Therapiepause empfohlen, um zu evaluieren, inwieweit weiterhin eine Wirksamkeit besteht. Bei mangelnder Wirksamkeit nach drei Monaten kann erwogen werden, einen alternativen mAB einzusetzen, beispielsweise Wechsel von einem CGRP-mAB auf einen CGRP-Rezeptor-mAB, wobei für dieses Vorgehen bislang jegliche wissenschaftliche Evidenz fehlt. Es lässt sich lediglich vermuten, dass es einen zumindest individuellen Unterschied in der Wirksamkeit zwischen den einzelnen mABs geben könnte. Wie lange eine Therapiepause zwischen den einzelnen mABs erfolgen sollte, ist bislang noch nicht einheitlich festgelegt. Einige Experten stellen direkt zum nächsten Therapieintervall um, andere warten bis zu sechs Monate vor dem Wiederbeginn einer alternativen mAB-Therapie.
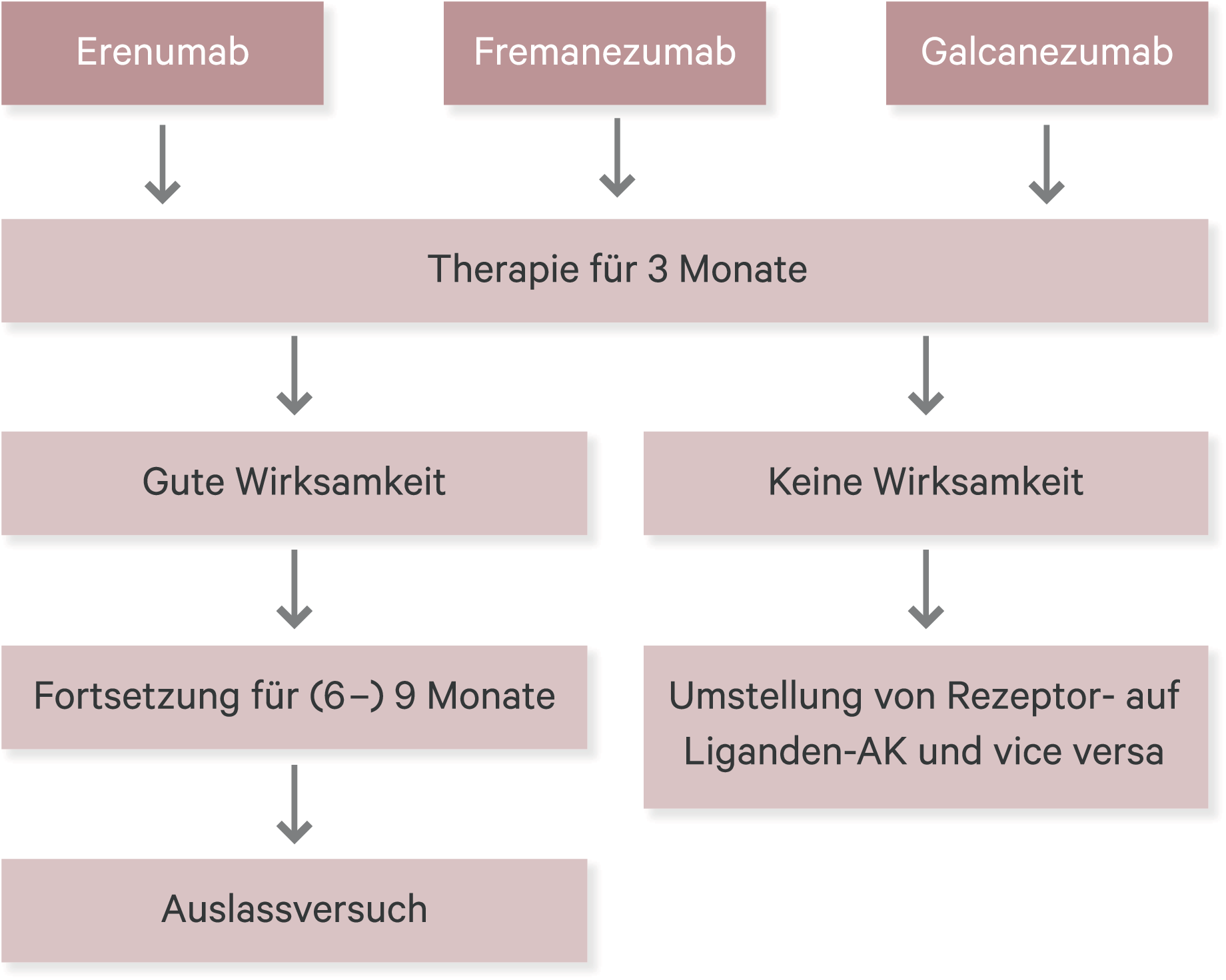
Abb. 1. Therapiealgorithmus für die Anwendung der CGRP-(Rezeptor-)mAB in der Praxis entsprechend der aktuellen Therapieleitlinien der Deutschen Gesellschaft für Neurologie [20]; AK: Antikörper
Fazit
Mit Erenumab, Fremanezumab und Galcanezumab steht eine sehr vielversprechende, neue, nebenwirkungsarme spezifische Migräneprophylaxe zur Verfügung, die für viele Patienten mit beeinträchtigender Migräne eine neue Hoffnung darstellt. Möglicherweise wird Eptinezumab das Therapiespektrum zukünftig noch erweitern.
Interessenkonflikterklärung
SW gibt an, Honorare für die Beratung oder Teilnahme an Advisory Boards der Firmen Lilly und Novartis erhalten zu haben.
AS gibt an, an der Universitätsmedizin Essen, Klinik für Neurologie, beschäftigt zu sein. Im August 2019 hat er Honorare für die Beratung oder Teilnahme an Advisory Boards der Firma Novartis erhalten. Außerdem sind die Kongressgebühren, Übernachtungs- und Reisekosten zum Jahreskongress der Deutschen Gesellschaft für Neurologie 2019 in Stuttgart von der Firma Teva übernommen worden. Er ist Mitglied der Deutschen Migräne- und Kopfschmerzgesellschaft (DMKG).
MN gibt an, dass keine Interessenkonflikte bestehen.
Literatur
1. Ashina M, Goadsby PJ, Reuter U, Silberstein S, et al. Long-term safety and tolerability of erenumab: Three-plus year results from a five-year open-label extension study in episodic migraine. Cephalalgia 2019;39:1455–64.
2. Ashina M, Saper J, Cady R, Schaeffler BA, et al. Eptinezumab in episodic migraine: A randomized, double-blind, placebo-controlled study (PROMISE-1). Cephalalgia 2020;40:241–54.
3. Bangs ME, Kudrow D, Wang S, Oakes TM, et al. Safety and tolerability of monthly galcanezumab injections in patients with migraine: integrated results from migraine clinical studies. BMC Neurol 2020;20:25.
4. Benschop RJ, Collins EC, Darling RJ, Allan BW, et al. Development of a novel antibody to calcitonin gene-related peptide for the treatment of osteoarthritis-related pain. Osteoarthritis Cartilage 2014;22:578–85.
5. Bigal ME, Dodick DW, Krymchantowski AV, VanderPluym JH, et al. TEV-48125 for the preventive treatment of chronic migraine. Neurology 2016;87:41–8.
6. Camporeale A, Kudrow D, Sides R, Wang S, et al. A phase 3, long-term, open-label safety study of galcanezumab in patients with migraine. BMC Neurol 2018;18:188.
7. Detke HC, Goadsby PJ, Wang S, Friedman DI, et al. Galcanezumab in chronic migraine: The randomized, double-blind, placebo-controlled REGAIN study. Neurology 2018;91:e2211–21.
8. Detke HC, Millen BA, Zhang Q, Samaan K, et al. Rapid onset of effect of galcanezumab for the prevention of episodic migraine: Analysis of the EVOLVE studies. Headache 2020;60:348–59.
9. Diener H, May A. Prophylaxe der Migräne mit monoklonalen Antikörpern gegen CGRP oder den CGRP-Rezeptor, Ergänzung der S1-Leitlinie Therapie der Migräneattacke und Prophylaxe der Migräne, 2019. In: Deutsche Gesellschaft für Neurologie (Hrsg.). Leitlinien für Diagnostik und Therapie in der Neurologie. Online: www.dgn.org/leitlinien (Zugriff am 12.08.2020).
10. Dodick DW, Ashina M, Brandes JL, Kudrow D, et al. ARISE: A phase 3 randomized trial of erenumab for episodic migraine. Cephalalgia 2018;38:1026–37.
11. Dodick DW, Goadsby PJ, Spierings ELH, Scherer JC, et al. Safety and efficacy of LY2951742, a monoclonal antibody to calcitonin gene-related peptide, for the prevention of migraine: a phase 2, randomised, double-blind, placebo-controlled study. Lancet Neurol 2014;13:885–92.
12. Dodick DW, Silberstein SD, Bigal ME, Yeung PP, et al. Effect of fremanezumab compared with placebo for prevention of episodic migraine: A randomized clinical trial. JAMA 2018;319:1999–2008.
12a. European Medicines Agency EMA. Emgality (galcanezumab). www.ema.europa.eu/documents/overview/emgality-epar-medicine-overview_en.pdf (Zugriff am 31.8.20).
13. Ferrari MD, Diener HC, Ning X, Galic M, et al. Fremanezumab versus placebo for migraine prevention in patients with documented failure to up to four migraine preventive medication classes (FOCUS): a randomised, double-blind, placebo-controlled, phase 3b trial. Lancet 2019;394:1030–40.
14. Ford JH, Foster SA, Stauffer VL, Ruff DD, et al. Patient satisfaction, health care resource utilization, and acute headache medication use with galcanezumab: results from a 12-month open-label study in patients with migraine. Patient Prefer Adherence 2018;12:2413–24.
15. Förderreuther S, Zhang Q, Stauffer VL, Aurora SK, et al. Preventive effects of galcanezumab in adult patients with episodic or chronic migraine are persistent: data from the phase 3, randomized, double-blind, placebo-controlled EVOLVE-1, EVOLVE-2, and REGAIN studies. J Headache Pain 2018;19:121.
15a. Gemeinsamer Bundesausschuss. Arzneimittel-Richtlinie/Anlage VI: Off-Label-Use, Aktualisierung Teil A Ziffer V, Valproinsäure bei der Migräneprophylaxe im Erwachsenenalter. www.g-ba.de/beschluesse/4212/ (Zugriff am 27.08.20).
16. Goadsby PJ, Dodick DW, Martinez JM, Ferguson MB, et al. Onset of efficacy and duration of response of galcanezumab for the prevention of episodic migraine: a post-hoc analysis. J Neurol Neurosurg Psychiatry 2019;90:939–44.
17. Goadsby PJ, Reuter U, Hallström Y, Broessner G, et al. A controlled trial of erenumab for episodic migraine. N Engl J Med 2017;377:2123–32.
18. Jin Y, Smith C, Monteith D, Brown R, Camporeale A, McNearney TA, et al. CGRP blockade by galcanezumab was not associated with reductions in signs and symptoms of knee osteoarthritis in a randomized clinical trial. Osteoarthritis Cartilage 2018;26:1609–18.
19. Lipton RB, Goadsby PJ, Smith J, Schaeffler BA, et al. Efficacy and safety of eptinezumab in patients with chronic migraine: PROMISE-2. Neurology 2020;94:e1365–77.
20. LL 030057 CGRP_Addendum Migraene-Leitlinie 2019 [Internet]. DGN – Deutsche Gesellschaft für Neurologie. Available from: https://dgn.org/leitlinien/ll-030-057-cgrp-addendum-migraene-leitlinie-2019/ (Zugriff am 08.08.2020).
21. Muelleners W, Kim B, Lainez M, Lanteri-Minet. A phase 3 placebo-controlled study of galcanezumab in patients with treatment-resistant migraine: Results from the 3-month double-blind treatment phase of the CONQUER study. J Neurol Sci 2019;405(Suppl):Poster WCN19–2248; doi: 10.1016/j.jns.2019.10.1817.
22. Oakes TM, Kovacs R, Rosen N, Doty E, et al. Evaluation of cardiovascular outcomes in adult patients with episodic or chronic migraine treated with galcanezumab: Data from three phase 3, randomized, double‐blind, placebo‐controlled EVOLVE‐1, EVOLVE‐2, and REGAIN studies. Headache 2020;60:110–23.
23. Reuter U, Goadsby PJ, Lanteri-Minet M, Wen S, et al. Efficacy and tolerability of erenumab in patients with episodic migraine in whom two-to-four previous preventive treatments were unsuccessful: a randomised, double-blind, placebo-controlled, phase 3b study. Lancet 2018;392:2280–7.
24. Scheffler A, Messel O, Wurthmann S, Nsaka M, et al. Erenumab in highly therapy-refractory migraine patients: First German real-world evidence. J Headache Pain 2020;21:84.
25. Schwedt T, Reuter U, Tepper S, Ashina M, et al. Early onset of efficacy with erenumab in patients with episodic and chronic migraine. J Headache Pain 2018;19:92.
26. Scuteri D, Adornetto A, Rombolà L, Naturale MD, et al. New trends in migraine pharmacology: Targeting calcitonin gene-related peptide (CGRP) with monoclonal antibodies. Front Pharmacol 2019;10:363.
27. Silberstein SD, Dodick DW, Bigal ME, Yeung PP, et al. Fremanezumab for the preventive treatment of chronic migraine. N Engl J Med 2017;377:2113–22.
28. Silberstein SD, McAllister P, Ning X, Faulhaber N, et al. Safety and tolerability of fremanezumab for the prevention of migraine: A pooled analysis of phases 2b and 3 clinical trials. Headache 2019;59:880–90.
29. Silberstein SD, Stauffer VL, Day KA, Lipsius S, et al. Galcanezumab in episodic migraine: subgroup analyses of efficacy by high versus low frequency of migraine headaches in phase 3 studies (EVOLVE-1 & EVOLVE-2). J Headache Pain 2019;20:75.
30. Skljarevski V, Matharu M, Millen BA, Ossipov MH, et al. Efficacy and safety of galcanezumab for the prevention of episodic migraine: Results of the EVOLVE-2 phase 3 randomized controlled clinical trial. Cephalalgia 2018;38:1442–54.
31. Skljarevski V, Oakes TM, Zhang Q, Ferguson MB, et al. Effect of different doses of galcanezumab vs placebo for episodic migraine prevention: A randomized clinical trial. JAMA Neurol 2018;75:187.
32. Stauffer VL, Dodick DW, Zhang Q, Carter JN, et al. Evaluation of galcanezumab for the prevention of episodic migraine: The EVOLVE-1 randomized clinical trial. JAMA Neurol 2018;75:1080–8.
33. Stauffer VL, Wang S, Voulgaropoulos M, Skljarevski V, et al. Effect of galcanezumab following treatment cessation in patients with migraine: Results from 2 randomized phase 3 trials. Headache 2019;59:834–47.
34. Tepper S, Ashina M, Reuter U, Brandes JL, et al. Safety and efficacy of erenumab for preventive treatment of chronic migraine: a randomised, double-blind, placebo-controlled phase 2 trial. Lancet Neurol 2017;16:425–34.
35. Wurthmann S, Nägel S, Hadaschik E, et al. Impaired wound healing in a migraine patient as a possible side effect of calcitonin gene-related peptide receptor antibody treatment: A case report. Cephalalgia 2020; Epub 2020 Jun 14. doi:10.1177/0333102420933571.
Prof. Dr. med. Dagny Holle, Dr. med. Sebastian Wurthmann, Michael Nsaka, Dr. med. Armin Scheffler, Klinik für Neurologie, Westdeutsches Kopfschmerzzentrum Essen, Universitätsklinikum Essen, Hufelandstraße 55, 45147 Essen, E-Mail: Dagny.holle-lee@uk-essen.de
CGRP (receptor) antibodies in migraine prophylaxis
With the CGRP (receptor) monoclonal antibodies (mAB), a specific prophylactic drug-based migraine therapy is available for the first time. Currently, three different mABs can be used in Germany (erenumab, fremanezumab, galcanezumab), which have shown their efficacy in large clinical studies. In terms of the side effect profile and efficacy, no significant differences have been demonstrated to date, although head-to-head studies between the mABs have not been carried out. All mABs show a significantly better tolerability profile than the first-line therapies available to date (beta-blockers, flunarizine, topiramate, amitriptyline, botulinum toxin A [for chronic migraine]). All available mABs are applied subcutaneously. Another mAB is currently being tested in clinical trials (eptinezumab), which is administered intravenously and may show a faster response to therapy. Currently, the statutory health insurance companies are covering the therapy costs for those migraine patients who have not responded to the previous first-line prophylactics.
Key words: CGRP antibodies, migraine, prophylaxis, therapy
Psychopharmakotherapie 2020; 27(05):224-230
