Michael Soyka, Bernau/München, und Susanne Rösner, Zürich
Schädlicher Gebrauch oder Alkoholabhängigkeit (nach ICD-10-Kriterien) oder Alkoholkonsumstörungen (nach DSM-5) sind sehr häufige psychische Störungen. Das ICD-10, und auch das bald anstehende ICD-11, definiert schädlichen Gebrauch anhand sozialer oder körperlicher Folgeschäden. Beim Vorliegen einer Abhängigkeit müssen nach ICD-10 drei von sieben Symptomen vorliegen:
- Gesteigerte Toleranz
- Entzugssymptome
- Alkoholkonsum wird in größeren Mengen oder länger konsumiert
- Anhaltender Wunsch oder erfolgloser Versuch, den Substanzgebrauch zu verringern oder zu kontrollieren.
- Viel Zeit für Aktivitäten, um Alkohol zu beschaffen
- Wichtige soziale, berufliche oder private Freizeitaktivitäten werden aufgrund des Alkoholkonsums aufgegeben oder eingeschränkt
- Fortschreitender Alkoholkonsum trotz Folgeschäden
Dagegen definiert das DSM-5 Substanzkonsumstörungen anhand eines dimensionalen Konzepts. Alkoholkonsumstörungen werden hier anhand von elf Kriterien definiert (Tab. 1). Treffen zwei oder drei zu, so liegt eine leichte, bei vier oder fünf eine mittelgradige, bei sechs oder mehr eine schwere Alkoholkonsumstörung vor. Von den einzelnen Symptomen sind die ersten vier einer beeinträchtigten Kontrolle (Kontrollverlust) zuzuordnen. Die Kriterien 5 bis 7 reflektieren soziale Folgeschäden und Beeinträchtigungen. Die Kriterien 8 bis 9 zeigen einen riskanten Konsum an und die Kriterien 10 und 11 (Toleranz und Entzug) sind pharmakologisch definiert.
Tab. 1. DSM-5-Kriterien für Alkoholkonsumstörungen
|
Ein problematisches Alkoholkonsummuster führt in klinisch bedeutsamer Weise zu Beeinträchtigung oder Leiden, wobei mindestens zwei der folgenden Kriterien innerhalb eines Zeitraums von 12 Monaten vorliegen. |
|
1. Alkohol wird in größeren Mengen oder länger als beabsichtigt konsumiert. |
|
2. Anhaltender Wunsch oder erfolglose Versuche, den Substanzkonsum zu verringern oder zu kontrollieren |
|
3. Hoher Zeitaufwand, um Alkohol zu beschaffen oder zu konsumieren oder sich von dessen Wirkung zu erholen |
|
4. Starkes Craving oder Alkoholverlangen |
|
5. Wiederholter Alkoholkonsum, der zu einem Versagen bei der Erfüllung wichtiger Verpflichtungen bei der Arbeit, in der Schule oder zu Hause führt |
|
6. Fortgesetzter Alkoholkonsum trotz ständiger oder wiederholter sozialer oder zwischenmenschlicher Probleme |
|
7. Wichtige soziale, berufliche oder Freizeitaktivitäten werden aufgrund des Substanzkonsums aufgegeben oder eingeschränkt |
|
8. Wiederholter Alkoholkonsum in Situationen, in denen der Konsum zu einer körperlichen Gefährdung führt |
|
9. Fortgesetzter Substanzkonsum trotz Kenntnis eines anhaltenden oder wiederkehrenden körperlichen oder psychischen Problems, das wahrscheinlich durch Alkohol verursacht oder verstärkt wurde |
|
10. Toleranzentwicklung, definiert durch: • Verlangen nach ausgeprägter Dosissteigerung • Deutlich verminderte Wirkung bei fortgesetztem Konsum |
|
11. Entzugssymptome, die sich durch eines der folgenden Kriterien äußern: • Charakteristisches Entzugssyndrom • Alkohol wird konsumiert, um Entzugssymptome zu lindern oder zu vermeiden |
Sowohl ICD-10 als auch DSM-5 vermeiden dabei genauere Angaben, ab welchem Grad des Alkoholkonsums (g/Tag) ein Alkoholkonsum als pathologisch angesehen werden muss (Übersicht in [24]).
Aus den genannten beschriebenen Klassifikationen ergibt sich zwanglos, dass Alkoholismus oder Alkoholkonsumstörung eine sehr heterogene Diagnose ist; entsprechend überrascht es auch nicht, dass in klinischen und Therapiestudien sehr unterschiedliche Patientengruppen eingeschlossen werden.
Für erhöhten (riskanten) Alkoholkonsum, Missbrauch und Abhängigkeit liegen verschiedene Prävalenzschätzungen vor (Übersicht in [13, 16]). Für Erwachsene fand sich demnach eine Rate für Alkoholmissbrauch von 1,8 % (Männer 3,1 %, Frauen 0,4 %), 3 % der Bevölkerung sind alkoholabhängig (Männer 4,4 %, Frauen 1,6 %), entsprechend Daten des Robert-Koch-Instituts. Einige andere Daten mögen die Bedeutung der Alkoholkonsumstörung in der Bevölkerung verdeutlichen:
So werden jährlich in Deutschland mehr als 2000 Kinder mit einem fetalen Alkoholsyndrom geboren. Es gibt über 200 Alkoholfolgekrankheiten (Abb. 1).
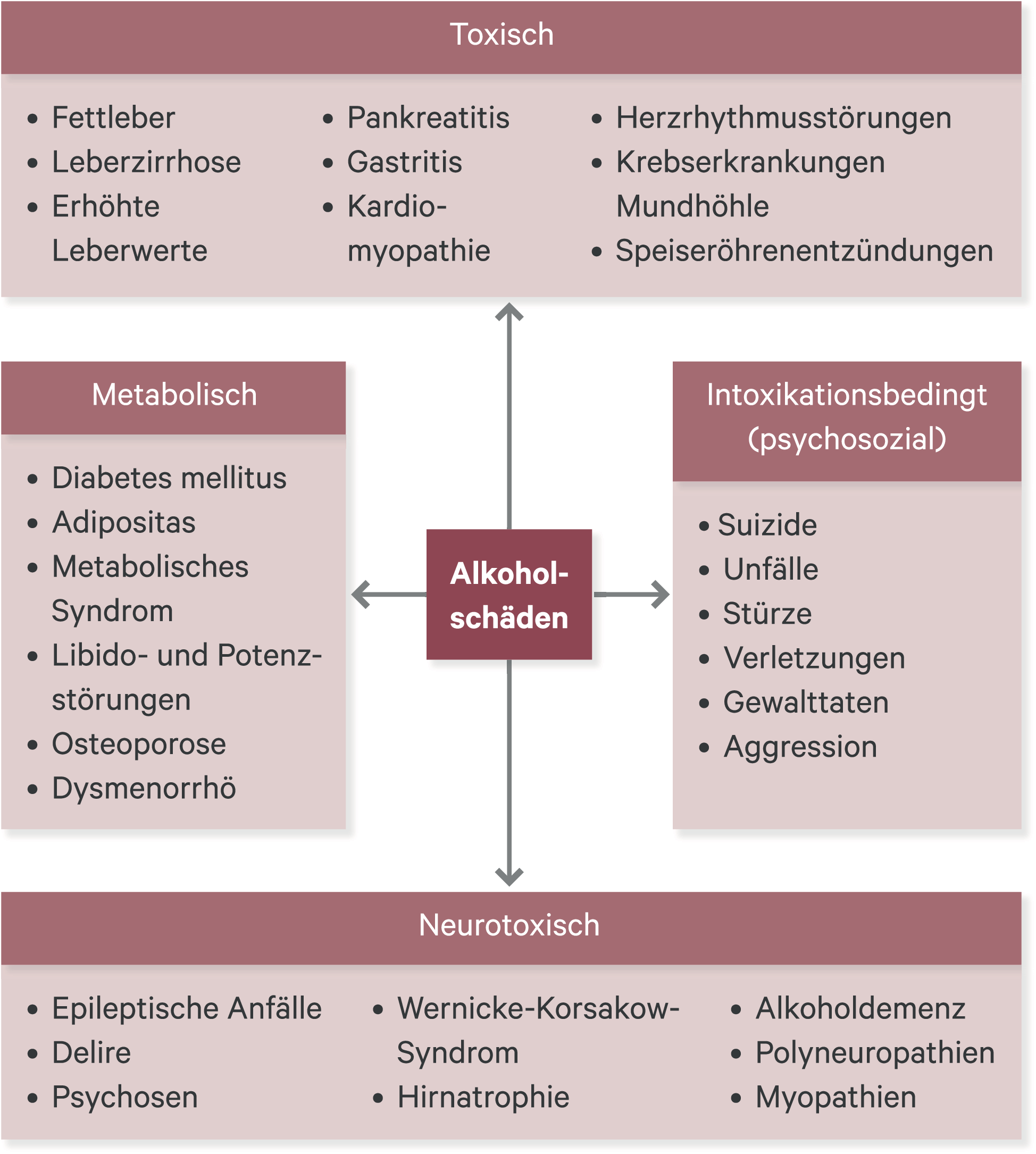
Abb. 1. Toxische Wirkungen von Alkohol
Zu den häufigsten Folgeerkrankungen bei Alkoholismus gehören [16]:
- Fettleber, Leberzirrhose
- Pankreatitis
- Suizid und Unfälle
- Gastritis, gastrointestinale Blutungen
- Adipositas, Diabetes, Hypertonie
- Kardiomyopathie, Herzerkrankungen
- Neuropsychiatrische Erkrankungen:
- Wernicke-Korsakow-Syndrom
- Epileptische Anfälle
- Hirnblutungen
- Hirnatrophien
Für die Diagnose und Behandlung alkoholbezogener Störungen liegt eine gültige S3-Leitlinie vor [16], die sich aktuell in Revision befindet, wobei wahrscheinlich keine grundlegenden Änderungen notwendig sind. Die klinische und wissenschaftliche Literatur zur Therapie der Alkoholabhängigkeit ist ausgesprochen umfangreich. Ambulante und stationäre Entwöhnungstherapien haben sich im Prinzip als erfolgreich erwiesen, wobei Abstinenzraten von über 40 % in den meisten Katamnesen nicht erreicht werden. Wirksame Therapieelemente sind beispielsweise verhaltenstherapeutische und kognitiv/verhaltenstherapeutische Interventionen, Psychoedukation, Rückfallprophylaxe, soziales Kompetenztraining, Paar- und Familientherapie, Verfahren zur Stressbewältigung und Entspannung, zum Teil auch psychodynamische Ansätze (Übersicht in [13]).
Erst in den letzten Jahren sind auch vermehrt pharmakotherapeutische Behandlungsstrategien entwickelt worden und einige wenige Medikamente sind zur Behandlung der Alkoholabhängigkeit zugelassen. Es gibt definierte methodische Standards, wobei die statistischen Ergebnisse stark von den postulierten Outcome-Kriterien abhängen [22].
Neurobiologische Grundlagen
Die zahlreichen neurobiologischen Befunde zur Wirkung von Alkohol (Ethanol), einem chemisch einfachen Molekül, im Gehirn sind sehr komplex (siehe auch [6, 23, 25]) und können hier nur stichwortartig angesprochen werden. Die relevanten Hirnstrukturen sind bekannt: Dabei handelt es sich um mesolimbische Strukturen, die für Belohnungserwartungen entscheidend sind (Nucleus accumbens und ventrales Tegmentum), Amygdala und Hippocampus (Gedächtnis- und Lernsystem), den orbito-frontalen Kortex (Motivation und Antrieb) und den präfrontalen Kortex (kognitive Kontrolle).
Dopaminerge Neuronen, die in der Substantia nigra und dem ventralen tegmentalen Areal entspringen, projizieren in das ventrale und dorsale Striatum sowie in limbische und präfrontale Areale. Es handelt sich hier um natürliche Belohnungsbahnen, über die die psychotropen Substanzen einschließlich Alkohol ihre Wirkung entfalten. Alle Substanzen mit Missbrauchspotenzial führen direkt oder indirekt zu einer Ausschüttung von Dopamin und verstärken damit die Motivation, Alkohol zu konsumieren. Auch das Stresssystem ist von Bedeutung; Alkoholkonsum führt über dessen Beeinflussung zu einer Reduktion von Stress und Angst. Gesichert ist auch eine erhebliche Bedeutung genetischer Faktoren für die Entwicklung der Alkoholabhängigkeit. Das glutamaterge und das GABAerge System sind vor allem für Toleranzentwicklung und die Entzugssymptomatik von Bedeutung. Alkohol verstärkt die Wirkung GABAerger Neurone. Insgesamt zeigt das Gehirn erhebliche neuroplastische, adaptive Anpassungen an die Wirkung von Alkohol, was sich klinisch zum Beispiel in Toleranzentwicklung, Entzugssymptomen und Belohnungserwartung äußert.
Alkohol selbst führt indirekt über eine Beeinflussung GABAerger Interneurone und das Opioidendorphinsystem zu einer vermehrten Dopaminausschüttung. Außerdem wirkt Alkohol inhibitorisch auf verschiedene glutamaterge Rezeptoren, insbesondere NMDA-Rezeptoren, sowie spannungsabhängige Calciumkanäle und nikotinische Acetylcholinrezeptoren. Zudem werden auch eine Reihe anderer Neurotransmitter beeinflusst (siehe Darstellung der einzelnen Substanzen).
Zugelassen zur Behandlung der Alkoholabhängigkeit sind in Deutschland Acamprosat sowie die beiden Opioidantagonisten Naltrexon und Nalmefen. Disulfiram wird nicht mehr vertrieben, wird aber aus didaktischen Gründen mitbesprochen und ist auch beispielsweise in der Schweiz noch erhältlich. Alle Substanzen werden klinisch nur sehr selten eingesetzt, wie aktuelle Verschreibungszahlen belegen. Abschließend sollen einige, möglicherweise zukünftig interessante Substanzen angesprochen werden.
„Entwöhnungsmittel“
Disulfiram
Disulfiram wird in Deutschland nicht mehr vertrieben, ist aber beispielsweise noch in der Schweiz zugelassen. Disulfiram (Antabus) war jahrzehntelang das einzige Medikament zur Rückfallprophylaxe der Alkoholabhängigkeit. Disulfiram selbst beeinflusst nicht die neurochemischen Effekte von Alkohol, sondern inhibiert das Enzym Acetaldehyd-Dehydrogenase und damit den Abbau von Acetaldehyd, dem ersten Stoffwechselprodukt von Ethanol. Acetaldehyd wird sonst rasch metabolisiert. Die Akkumulation von Acetaldehyd führt zur sogenannten Disulfiram-Alkohol-Reaktion (meist 60 bis 80 Minuten nach Alkoholkonsum), einer durch Blockade des Acetaldehydabbaus künstlich herbeigeführten Vergiftung, die klinisch mit Übelkeit, Erbrechen, Schweißausbrüchen, Blutdrucksteigerung, Kreislaufschwäche, Herzrasen, in schweren Fällen kardiovaskulären Reaktionen oder Kollaps einhergeht (Übersicht in [21]). Die klinische Wirkung von Disulfiram basiert also auf aversiven Erwartungen und der Antizipation der geschilderten Effekte.
Disulfiram hat eine Bioverfügbarkeit von 80 bis 90 % und eine Halbwertszeit von sechs bis neun Stunden. Die übliche Dosis beträgt 400 mg am Tag. Die Durchführung eines EKGs, Kontrolle der Leberwerte usw. sind sinnvoll. Mindestens drei Tage Abstinenz ist vor Behandlungsbeginn notwendig. Der früher übliche Trinkversuch mit Alkohol, um die Wirkung von Disulfiram aus Patientensicht abschätzen zu können, ist nicht mehr obligat.
Kontraindikationen für die Gabe von Disulfiram sind schwere psychiatrische Störungen, Leberfunktionsstörungen, Epilepsie, Polyneuropathie, Schwangerschaft, Herz- und Nierenerkrankungen, Diabetes mellitus (relative Kontraindikation).
Typische Nebenwirkungen sind Benommenheit, Antriebsmangel, allergische Hautreaktionen, Kopfschmerzen, Durchfall, Verstopfung, Libidoverlust, Blutdruckabfall, gelegentlich Hepatitis. Vorsicht bei kardialer Vorschädigung.
Evidenz
Die größte zur Frage der Wirkung von Disulfiram durchgeführte randomisierte klinische Studie konnte keinen Wirknachweis zeigen [5]. Einige Metaanalysen zeigten positive Effekte am ehesten in offenen nicht randomisierten Therapiestudien. Offensichtlich werden die Behandlungsergebnisse bei Supervision der Einnahme von Disulfiram besser. Die Therapie mit Disulfiram hat immer noch einige Befürworter (siehe dazu [21]). Die wissenschaftliche Evidenz ist aber insgesamt begrenzt.
Acamprosat
Acamprosat ist seit Jahrzehnten für die Behandlung der Alkoholabhängigkeit zugelassen, in Deutschland seit 1995. Strukturchemisch handelt es sich bei der Substanz um ein Analogon der Aminosäure Homotaurin. Der Wirkungsmechanismus ist trotz jahrzehntelanger Forschung einigermaßen mysteriös. Acamprosat hat keine GABAergen Eigenschaften, wirkt auch nicht sedierend und hat keine anderen psychotropen Effekte. Zahlreiche Befunde aus der Grundlagenforschung deuten auf eine antagonisierende Wirkung an exzitatorischen glutamatergen Neuronen (insbesondere am NMDA-Rezeptor) hin. Auch eine Wirkung über Glycinrezeptoren wurde diskutiert. Mannheimer Forscher haben postuliert, dass die Wirkung der Substanz ausschließlich über das Calciumatom des Acamprosat-Moleküls zu erklären ist, was allerdings umstritten ist.
Acamprosat wird relativ schlecht aus dem Gastrointestinaltrakt resorbiert (weniger als 10 % der Dosis, geringe orale Bioverfügbarkeit). Deswegen sind klinisch hohe Dosen notwendig: Die Substanz überwindet die Blut-Hirn-Schranke, sie wird nicht an Plasmaproteine gebunden, unterliegt keiner Biotransformation und wird renal ausgeschieden. Die Plasmahalbwertszeit beträgt etwa 13 Stunden. Bei einem Körpergewicht von über 60 kg werden drei Dosen von zwei Tabletten à 333 mg (entsprechend 1998 mg/Tag) empfohlen.
Klinisch häufige Nebenwirkungen sind Durchfall (Diarrhö), Blähungen, Übelkeit, Erbrechen, Juckreiz und Hautausschlag. Wechselwirkungen mit Alkohol bestehen nicht. Aus den Metaanalysen ist bekannt, dass nur Durchfall oder weicher Stuhl bei Acamprosat häufiger ist als bei Placebo.
Evidenz
Es gibt zahlreiche randomisierte Doppelblinduntersuchungen zu Acamprosat, die in mehreren Metaanalysen ausgewertet wurden [4, 10, 14]. Die beiden Metaanalysen haben über 7000 Patienten eingeschlossen. Der Cochrane-Review zu Acamprosat (siehe [16]) zeigte eine signifikante, aber moderate Reduktion des Konsumrisikos für Alkohol auf 81 %. Auch die anderen Metaanalysen haben eine Wirkung vor allem auf die Abstinenzrate, zum Teil auch auf die Trinkmengen oder die Anzahl der Trinktage ergeben. Die europäischen Studien haben insgesamt bessere Wirknachweise gezeigt als die amerikanischen Untersuchungen. Insgesamt hat sich Acamprosat als sehr gut verträgliches Medikament zur Abstinenzsicherung bei Alkoholabhängigkeit erwiesen.
Es gibt wenige Vergleichsuntersuchungen zu Acamprosat versus Naltrexon. In der deutschen Studie zu dieser Frage [11] zeigte Naltrexon bessere Ergebnisse als Acamprosat, wobei die Kombination von beiden Substanzen überlegen war. In der großen amerikanischen Combine-Studie [3] konnte kein Wirknachweis von Acamprosat gezeigt werden.
Opioidantagonisten
Naltrexon
Naltrexon ist in Deutschland sowohl zur Behandlung der Opiatabhängigkeit nach erfolgter Opioidentgiftung als auch zur Behandlung der Alkoholabhängigkeit zugelassen. Typischerweise werden 50 mg/Tag oral werden verwendet. In den USA ist auch eine Depotform von Naltrexon zur monatlichen intramuskulären Gabe für die Behandlung der Alkoholabhängigkeit verfügbar.
Naltrexon ist ein nichtselektiver Opioidantagonist, der den My-, Kappa- und Delta-Opioid-Rezeptor blockiert. Durch die Blockade des Opioidendorphinsystems im mesolimbischen Bereich wird indirekt auch die alkoholindizierte Ausschüttung von Dopamin im Nucleus accumbens blockiert, sodass Naltrexon die „positiven“ Effekte von Alkohol vermindern kann. Zahlreiche auch verhaltenspharmakologische, experimentelle Untersuchungen konnten zeigen, dass die wesentlichen Effekte von Alkohol, nämlich Alkoholverlangen (Craving), Stimulation, Sedierung, aber auch negative Stimmungen nach Alkoholkonsum nach Naltrexon vermindert werden können (Metaanalyse siehe [20]). Kurz gesagt, Naltrexon blockiert die hedonistischen Effekte von Alkohol, die durch die Dopamin-Ausschüttung vermittelt werden.
Naltrexon hat eine Bioverfügbarkeit von 5 bis 40 % bei Einnahme von 50 mg. Es weist einen hohen First-Pass-Metabolismus und einen aktiven Metaboliten (6-β-Naltrexol) auf. Die Ausscheidung erfolgt überwiegend renal. Die Halbwertszeit beträgt etwa 72 bis 108 Stunden. Der Opioidrezeptor ist für etwa 24 Stunden blockiert.
Häufige Nebenwirkungen von Naltrexon sind Schlafstörungen und Angstzustände, gesteigerte Erregbarkeit, vor allem aber gastrointestinale Beschwerden, Übelkeit und Erbrechen. Vorsicht ist bei Patienten mit reduzierter Leber- und Nierenfunktion geboten. Kontraindiziert ist die Gabe bei bestehender Opiatabhängigkeit, da es hier zur Auslösung eines Opiatentzugssyndroms kommen kann. Abhängigkeit- oder Toleranzentwicklung gibt es bei Naltrexon nicht.
Evidenz
Naltrexon wurde seit Anfang der 90er-Jahre intensiv beforscht. Mittlerweile liegen zahlreiche randomisierte Placebo-kontrollierte Therapiestudien vor (Metaanalyse siehe [4, 10]). Naltrexon hat sich insgesamt als wirksame Substanz in der Reduktion der Trinkmenge oder der Verminderung schwerer Alkoholrückfälle erwiesen und hat weniger Einfluss auf die Abstinenzrate. So zeigte auch der Cochrane-Review (siehe [16]) eine signifikante Reduktion des Risikos für einen Alkoholrückfall (5 oder mehr Standarddrinks) auf 83 % des Risikos der Kontrollgruppe.
Nalmefen
Nalmefen ist zugelassen zur Reduktion des Alkoholkonsums bei erwachsenen Patienten mit Alkoholabhängigkeit, deren Alkoholkonsum sich auf einem hohen Risikoniveau befindet und bei denen keine körperlichen Entzugserscheinungen vorliegen und keine sofortige Entgiftung erforderlich ist. Die Substanz wurde 2013 von der Europäischen Kommission zugelassen; in den USA ist sie nicht verfügbar.
Nalmefen hat eine ähnliche Struktur wie Naltrexon und ist ein Antagonist am My-Opioid-Rezeptor, aber ein Modulator am Kappa-Opioid-Rezeptor-Subtyp. Wie Naltrexon blockiert Nalmefen indirekt die Ausschüttung von Dopamin durch My-Opioid-Rezeptorblockade. Die funktionelle Wirkung am Kappa-Opioid-Rezeptor wird noch nicht ausreichend verstanden.
Nach oraler Gabe wird die maximale Plasmakonzentration nach 1 bis max. 1,5 Stunden erreicht. Die Bioverfügbarkeit beträgt 41 %. Nalmefen wird verstoffwechselt – Hauptmetabolit ist Nalmefen-3-O-Glucuronid – und dann renal ausgeschieden. Die Halbwertszeit beträgt 13 Stunden. Die Rezeptorbindung klingt nur langsam ab. Nach Nalmefen-Einnahme sind nach 50 Stunden noch mehr als die Hälfte der Opioid-Rezeptoren blockiert.
Die Nebenwirkungen entsprechen im Prinzip denen von Naltrexon: Sehr häufige Nebenwirkungen sind: Schlaflosigkeit, Schwindel, Kopfschmerzen, Übelkeit. Weitere Nebenwirkungen sind: verminderter Appetit, Verwirrtheit, Ruhelosigkeit, verminderte Libido, Libidoverlust, Somnolenz, Tremor, Aufmerksamkeitsstörungen, Parästhesien, Hypästhesien, Tachykardien, Palpitationen, Erbrechen, trockener Mund, Muskelspasmen, Ermüdung, Unwohlsein, Gewichtsabnahme. Auch hier ist Vorsicht bei Opiatabhängigkeit oder Behandlung mit Opioid-Analgetika geboten (Entzugssyndrom).
Evidenz
Die klinischen Studien zu Nalmefen unterscheiden sich von den meisten Untersuchungen zu Acamprosat und Naltrexon dahingehend, dass die Substanz von vorneherein mit dem Ziel Trinkmengenreduktion, nicht Abstinenzerhalt, eingesetzt wurde. Die vorliegenden Doppelblindstudien folgten damals einem „as needed“-Ansatz. Das heißt, es erfolgte keine feste Dosierung, sondern der Patient konnte entscheiden, ob und wann er das Medikament einnimmt, insbesondere vor Hochrisikosituationen. Mittlerweile wurden eine Reihe von Placebo-kontrollierten Doppelblinduntersuchungen durchgeführt [7, 15, 19] wobei eine Tablette Nalmefen 18 mg pro Tag „as needed“ vs. Placebo untersucht wurde. Die Patienten waren überwiegend mittelschwere Fälle von Alkoholkonsumstörungen. Die Untersuchungen zeigten insgesamt eine gewisse, wenn auch nur mäßiggradige Reduktion der Trinkmenge. Der Einsatz von Nalmefen folgt also einer „harm reduction“-Strategie. Die Datenlage zu Nalmefen wurde zum Teil kontrovers beurteilt, auch in Metaanalysen [z. B. 18]. Kritisch diskutiert wurde vor allem die relativ hohe Dropout-Rate in einigen Studien, die höher war als die von Placebo. Auch die Reduktion der Trinkmenge von im Mittel etwa 10 g Alkohol pro Tag wurde hinsichtlich ihrer klinischen Relevanz diskutiert. Zuletzt wurden aber wieder positive Ergebnisse einer japanischen Studie publiziert, die zeigte, dass Nalmefen zu einer Reduktion von „heavy drinking“ führt.
Vergleichsuntersuchungen von Naltrexon mit Nalmefen liegen nicht vor.
Nicht zugelassene Substanzen
Baclofen
Baclofen ist ein selektierter GABA-B-Rezeptor-Agonist, der klinisch zur Behandlung bei schwerer chronischer Spastizität bei multipler Sklerose und anderen neurologischen Erkrankungen eingesetzt wird. In Frankreich, nicht aber in Deutschland, ist die Substanz für die Behandlung der Alkoholabhängigkeit zugelassen.
Baclofen wird nach oraler Einnahme komplett aufgenommen. Die Plasmahalbwertszeit beträgt drei bis vier Stunden. Baclofen wird überwiegend unverändert über die Nieren ausgeschieden, es gibt keinen aktiven Metaboliten.
Typische Nebenwirkungen sind: Müdigkeit, Schlafstörungen, Übelkeit, Benommenheit. Bei Überdosierung kann es zu Übelkeit, Erbrechen, Schwindel, Atemschwäche, Hypertonie, Bradykardie und Hypothermie kommen.
Evidenz
Bekannt wurde Baclofen durch die Selbstbehandlung eines mittlerweile verstorbenen französischen Arztes, Olivier Ameisen [2], der die Substanz in sehr hohen Dosen bis 270 mg einnahm.
In der Folge wurde eine Reihe von anderen randomisierten Therapiestudien mit verschiedenen Dosierungen durchgeführt. Zuletzt wurden zwei größere Untersuchungen in Frankreich durchgeführt. Eine deutsche Untersuchung mit Baclofen bis 270 mg zeigte im Gegensatz zu einigen anderen Untersuchungen einen positiven Effekt auf die Abstinenzrate ohne klaren Dosiseffekt. Sicherheitsbedenken wegen toxischer Nebenwirkungen und Vergiftungen gibt es insbesondere in Frankreich.
Trotz schmaler Datenbasis gibt es mehrere Metaanalysen. Ein Cochrane-Review [17] über zwölf randomisierte klinische Studien zeigte zuletzt eher negative Ergebnisse und legte auch nahe, dass Baclofen zu einer Steigerung depressiver Symptome führen kann. Offene Fragen betreffen die Wirksamkeit, aber auch die notwendige Dosis von Baclofen. Die Substanz ist klinisch interessant und Gegenstand der Forschung.
Gabapentin
Gabapentin ist klinisch zur Behandlung von epileptischen Anfällen (einfache und komplex-partielle Anfälle mit und ohne sekundäre Generalisierung) zugelassen, außerdem zur Behandlung neuropathischer Schmerzen. Off Label wird es zum Teil auch zur Behandlung der Spastik bei multipler Sklerose und zur Behandlung des Restless-Legs-Syndroms eingesetzt.
Der Wirkungsmechanismus von Gabapentin ist nicht völlig klar, die Substanz führt nicht zu einer direkten Aktivierung von GABA-Rezeptoren. Eine Hemmung der glutamatergen Erregung als zentraler Calciumkanalblocker wird diskutiert.
Gabapentin hat eine Bioverfügbarkeit von rund 60 % und eine Halbwertszeit von fünf bis sieben Stunden. Es wird über den Urin ausgeschieden.
Nebenwirkungen sind: ausgeprägte Mundtrockenheit, Müdigkeit, Schläfrigkeit, Schwindel, Kopfschmerzen, Übelkeit, Erbrechen, Gewichtszunahme, Schlaflosigkeit, Nervosität, Ataxie, Augenzittern, Parästhesie, gesteigerter wie auch verminderter Appetit und Anorexie. Seltener können auch psychische Symptome (Angst, Depression, Halluzinationen) auftreten. Die Wirkung von Gabapentin kann beispielsweise durch Alkohol oder Opioide verstärkt werden. Bei Reizleitungsstörung des Herzens ist Gabapentin kontraindiziert.
Evidenz
Eine kürzlich veröffentlichte Metaanalyse [12] über sieben randomisierte kontrollierte Studien fand einen mittelgradigen Effekt von Gabapentin auf die Anzahl von Tagen mit schwerem Alkoholkonsum. Alle anderen Kriterien waren unter Gabe von Gabapentin nicht signifikant besser als unter Placebo. Fraglich ist ein Missbrauchspotenzial. Eine andere Metaanalyse zeigte eine gewisse Wirkung auf Entzugssymptome und Alkoholverlangen (Craving).
Die American Psychiatric Association empfiehlt Gabapentin, sowie Topiramat für alkoholkranke Patienten, die unter zugelassenen Medikamenten wie Acamprosat und Naltrexon nicht respondieren oder diese nicht vertragen.
Topiramat
Topiramat wird zur Epilepsiebehandlung in Dosen von 25 bis 200 mg sowie zur Migränetherapie eingesetzt. Auch zur Cluster-Kopfschmerz-Prophylaxe wird die Substanz verwendet. Topiramat blockiert die Glycinbindungsstelle am exzitatorischen glutamatergen AMPA-Rezeptor und verstärkt durch Bindung an GABA-Rezeptoren deren hemmenden Effekt. Außerdem inaktiviert Topiramat spannungsabhängige Calciumkanäle.
Topiramat wird rasch oral gut resorbiert, hat eine Halbwertszeit von 20 bis 30 Stunden und wird überwiegend über die Niere ausgeschieden. Bei Niereninsuffizienz muss die Dosis angepasst werden.
Topiramat hat teratogene Effekte! An Nebenwirkungen können Schläfrigkeit, Schwindel, vermindertes Sehvermögen, klingendes Geräusch im Ohr, Verlust von Geschmackssinn auftreten. Häufig sind vor allem Parästhesien. Auch Konzentrationsstörungen, Kopfschmerzen, erhöhte Reizbarkeit, Schlafstörungen, Albträume können auftreten.
Gesichert ist eine verminderte Dopamin-Freisetzung im kortikalen mesolimbischen System durch Topiramat, sodass die Substanz auch in einigen doppelblinden, randomisierten, Placebo-kontrollierten Studien bei Alkoholkonsumstörungen untersucht wurde. Meist wurden Dosen von 200 bis 300 mg eingesetzt. Die Ergebnisse sind etwas widersprüchlich, aber insgesamt positiv. In den meisten Studien konnte ein reduzierter Alkoholkonsum gezeigt werden, wobei pharmakogenetische Untersuchungen eine Relevanz von Polymorphismen in der Kainat-GluK1-Rezeptoruntereinheit (GRIK1) nahe legen.
Vareniclin
Vareniclin ist zur Behandlung der Nikotinabhängigkeit (Raucherentwöhnung) zugelassen. Die Substanz ist ein partieller α4β2-Agonist und (mit geringerer Affinität) ein voller α7-Nicotinacetylcholin-Rezeptoragonist.
Zu den Nebenwirkungen gehören Übelkeit, Kopfschmerzen, Erbrechen, Blähungen, Schlafstörungen, Somnolenz, Vertigo, Geschmacksstörungen, selten Depressionen und Aggressivität sowie Suizidalität.
Die Substanz wurde auch bei Alkoholabhängigkeit eingesetzt. Vor Kurzem wurde eine Metaanalyse über neun Placebo-kontrollierte Doppelblindstudien (n = 585) berichtet, die zeigte, dass Vareniclin im Vergleich mit Placebo zwar nicht die Zahl der Heavy-Drinking-Days, aber den Alkoholkonsum insgesamt vermindern konnte. Die Substanz gehört zu den aktuell intensiv beforschten Arzneistoffen.
Andere Substanzen
Zu den interessanten experimentellen Ansätzen gehören der NMDA-Rezeptorantagonist Ketamin sowie zuletzt auch Oxytocin. Einige klinische Ansätze gibt es auch für Prazosin. Nichts davon kann aktuell empfohlen werden.
Kontrovers ist die Gabe der in Österreich für Alkoholabhängigkeit zugelassenen Gamma-Hydroxy-Buttersäure (GHB) zu beurteilen, einer GABAergen, stark psychotrop wirkenden Substanz mit hohem Missbrauchspotenzial, die als „rape-drug“ (Missbrauch bewusstloser junger Frauen) traurige Berühmtheit erlangt hat. In Bezug auf Alkoholabhängigkeit gibt es einige positive Befunde. Da GHB aber stark toxisch ist und auch die Effekte von Alkohol potenzieren kann, muss der Einsatz in diesem Indikationsbereich sehr kritisch gesehen werden.
Wenig bekannt ist über klassische psychotrope Substanzen. Konventionelle Psychopharmaka haben nach allen vorliegenden Befunden keine Effekte auf die Trinkmenge, jedenfalls nicht bei nicht-komorbiden Alkoholkranken. Antidepressiva [1] können bei komorbiden Patienten mit affektiven Störungen und Alkohol eingesetzt werden, beeinflussen hier aber nur affektive Symptome. Es fällt schwer, in diesem Indikationsbereich ein Antidepressivum besonders hervorzuheben, wie die schöne Übersicht von Hillemacher et al. [9] gezeigt hat.
Leitlinienempfehlungen
Es gibt eine auslaufende S3-Leitlinie [16] für Diagnostik und Behandlung von Alkoholabhängigkeit, die aktuell zur Revision ansteht. Bedeutsame Änderungen sind nicht zu erwarten. In den Leitlinien wird die Evidenz wohl für Acamprosat, wie für Naltrexon, als sehr gut angesehen (Level of Evidence 1a, Empfehlungsgrad B); Nalmefen wurde seinerzeit noch nicht ausreichend berücksichtigt.
Pharmakogenetik
Bislang haben die pharmakogenetischen Ansätze bei Alkoholabhängigkeit nur theoretisches Interesse gefunden. Für die Klinik haben sie bislang keine Bedeutung. Am ehesten haben noch Polymorphismen des My-Opioid-Rezeptors für die Wirkung von Naltrexon eine gewisse Bedeutung, wobei neuere Untersuchungen hier keinen klaren Zusammenhang gezeigt haben [8].
Diskussion und Ausblick
Bislang sind nur wenige Medikamente als „Entwöhnungsmittel“ zur Rückfallprophylaxe oder Trinkmengenreduktion bei Alkoholabhängigkeit zugelassen – beide Therapieziele werden auch in der S3-Leitlinie als legitim angesehen, wobei man mit Abstinenz immer auf der sicheren Seite ist. Nur Nalmefen wird ausdrücklich als Arzneimittel vermarktet, das zur Trinkmengenreduktion vorgesehen ist. Für Acamprosat ist die Evidenzbasierung bezüglich Abstinenz besser. Naltrexon führt eher zu einer Trinkmengenreduktion bzw. zu einer geringeren Anzahl von schweren Alkoholrückfällen. Klinisch werden alle diese Substanzen viel zu wenig eingesetzt, was möglicherweise daran liegt, dass der Wirkungsmechanismus von Acamprosat schwierig zu erklären ist, während der für Naltrexon relativ evident ist (Blockade positiv verstärkender, „motivierender“ Effekte). Die Wirksamkeit, ausgedrückt in der Effektstärke, ist bei Acamprosat und Naltrexon durchaus vergleichbar der von Antidepressiva bei affektiven Erkrankungen. Die Substanzen, die alternativ nahe am klinischen Einsatz sind – Gabapentin, Topiramat, eventuell Prazosin –, entstammen alle anderen Indikationsbereichen und sind nicht primär zur Behandlung der Alkoholabhängigkeit entwickelt worden. Da konventionelle Psychopharmaka, speziell Antidepressiva und Antipsychotika, zur Therapie der Alkoholabhängigkeit bei nicht komorbiden Patienten nutzlos sind, ist zu hoffen, dass zumindest einige der in präklinischer Entwicklung befindlichen Substanzen ihren Weg in die Klinik finden werden. Zuvor geht es darum, zumindest die Substanzen, die verfügbar sind, beherzter zu nutzen, was allerdings auch ein größeres Interesse von Ärzten an der Behandlung Alkoholkranker voraussetzt.
Interessenkonflikterklärung
MS: In den letzten fünf Jahren als Consultant oder im Rahmen von Fortbildungen tätig für: Amomed, Camurus, Indivior, Lundbeck.
Literatur
1. Agabio R, Trogu E, Pani PP. Antidepressants for the treatment of people with co-occurring depression and alcohol dependence. Cochrane Database Syst Rev 2018;4:CD008581.
2. Ameisen O. Complete and prolonged suppression of symptoms and consequences of alcohol-dependence using high-dose baclofen: a self-case report of a physician. Alcohol Alcohol 2005;40:147–50.
3. Anton RF, O’Mallex SS, Ciraulo DA, Cisler RA, et al.; Combine Study Research Group. Combined pharmacotherapies and behavioral interventions for alcohol dependence: the COMBINE study: randomized controlled trial. JAMA 2006;295:2003–17.
4. Donoghue K, Elzerbi C, Saunders R, Whittington C, et al. The efficacy of acamprosate and naltrexone in the treatment of alcohol dependence, Europe versus the rest of the world: a meta-analysis. Addiction 2015;110:920–30.
5. Fuller RK, Branchey L, Brightwell DR, Derman RM, et al. Disulfiram treatment of alcoholism. A veterans administration cooperative study. JAMA 1986;256:1449–55.
6. Goh ET, Morgan MY. Review article: pharmacotherapy for alcohol dependence – the why, the what and the wherefore. Aliment Pharmacol 2017;45:865–82.
7. Gual A, He Y, Torup L, et al. A randomized, double-blind, placebo-controlled, efficacy study of nalmefene, as-needed use, in patients with alcohol dependence. Eur Neuropsychopharmacol 2013;23:1432–42.
8. Hartwell EE, Feinn R, Morris PE, Gelermter J, et al. Systematic review and meta-analysis of the moderating effect of rs1799971 in OPRM1, the mu-opioid receptor gene, on response to naltrexone treatment of alcohol use disorder. Addiction 2020; doi:10.1111/add.14975.
9. Hillemacher T, Frieling H. Pharmacotherapeutic options for co-morbid depression and alcohol dependence. Expert Opin Pharmacother 2019;20:547–69.
10. Jonas DE, Amick HR, Feltner C, Bobashev G, et al. Pharmacotherapy for adults with alcohol use disorders in outpatient settings: a systematic review and meta-analysis. JAMA 2014;311:1889–900.
11. Kiefer F, Jahn H, Tarnaske T, Helweig H, et al. Comparing and combining naltrexone and acamprosate in relapse prevention of alcoholism: a double-blind, placebo-controlled study, Arch Gen Psychiatry 2003;60:92–9.
12. Kranzler HR, Feinn R, Morris P, Hartwell EE. A meta-analysis of the efficacy of gabapentin for treating alcohol use disorder. Addiction 2019;114:1547–55.
13. Kranzler HR, Soyka M. Diagnosis and pharmacotherapy of alcohol use disorder. A review. JAMA 2018;320:815–26.
14. Maisel NC, Blodgett JC, Wilbourne PL, Humphreys K, et al. Meta-analysis of naltrexone and acamprosate for treating alcohol use disorders: when are these medications most helpful? Addiction 2013;108:275–93.
15. Mann K, Bladström A, Torup L, Gual A, et al. Extending the treatment options in alcohol dependence: a randomized controlled study of as-needed nalmefene. Biol Psychiatry 2013;73:706–13.
16. Mann K, Hoch E, Batra A (Hrsg.) S3-Leitlinie Screening, Diagnose und Behandlung alkoholbezogener Störungen. Heidelberg Berlin: Springer, 2016.
17. Minozzi S, Saulle R, Rösner S. Baclofen for alcohol use disorder. Cochrane Database Syst Rev 2018;11:CD012557.
18. Palpacuer C, Duprez R, Huneau A, Locher C, et al. Pharmacologically controlled drinking in the treatment of alcohol dependence or alcohol use disorders: a systematic review with direct and network meta-analyses on nalmefene, naltrexone, acamprosate, baclofen and topiramate. Addiction 2018;113:220–37.
19. Palpacuer C, Laviolle B, Boussageon R, et al. Risks and benefits of nalmefene in the treatment of adult alcohol dependence: a systematic literature review and meta-analysis of published and unpublished double-blind randomized controlled trials. Plos Med 2015;12:e1001924.
20. Ray LA, Green RJ, Roche DJO, Magill M, et al. Naltrexone effects on subjective responses to alcohol in the human laboratory: A systematic review and meta-analysis. Addict Biol 2019;24:1138–52.
21. Rösner S, Grosshans M, Mutschler JH. Disulfiram: Aktuelle Befunde und Wirkmechanismen. Suchtmedizin 2014;16:47–52.
22. Rösner S, Soyka M. Outcome assessment in trials of pharmacological treatments for alcohol use disorders. CNS Drugs 2019;33:649–57.
23. Shen WW. Anticraving therapy for alcohol use disorder: A clinical review. Neuropsychopharmacol Rep 2018;38:105–16.
24. Soyka M. Diagnostische Kriterien für Suchterkrankungen. In: Soyka M, Batra A, Heinz A, Moggi F, et al. (Hrsg.). Suchtmedizin. München: Elsevier, 2019: 3–12.
25. Witkiewitz K, Litten RZ, Leggio L. Advances in the science and treatment of alcohol use disorder. Sci Adv 2019;5:eaax4043.
Prof. Dr. Michael Soyka, Medical Park Chiemseeblick, Rasthausstraße 25, 83233 Bernau/Felden, und Psychiatrische Universitätsklinik LMU München, Nußbaumstraße 7, 80336 München, E-Mail: michael.soyka@med.uni-muenchen.de
Dr. Susanne Rösner, Forel Klinik, Zwingliplatz 1, 8001 Zürich, Schweiz
Psychopharmakotherapie 2020; 27(04):199-205
