Idalia Nowak, Georg Juckel und Martin Brüne, Bochum
Korrekturhinweis
Der Satz „Lamotrigin induziert den Abbau von Quetiapin, andererseits kann sein Abbau durch Valproinsäure beschleunigt werden.“ (S. 131) ist in Bezug auf die Interaktion Lamotrigin/Valproinsäure leider falsch. Richtig ist: Der Abbau von Lamotrigin wird durch eine gleichzeitige Behandlung mit Valproinsäure verlangsamt, sodass es zu erhöhten (bis zu 3-fach) Lamotrigin-Spiegeln kommen kann, da Valproinsäure die Glucuronidierung von Lamotrigin hemmt und dessen Halbwertszeit daher mehr als verdoppelt wird (von ca. 33 h auf ca. 70 h; vgl. Fachinformation).
Wir bitten um Entschuldigung für das Versehen.
Emotional-instabile Persönlichkeitsstörungen vom Borderline-Typ (oder kurz: Borderline-Persönlichkeitsstörung; BPS) sind klinisch gekennzeichnet durch massive Verlassensängste, instabile Beziehungsmuster mit Spaltung bzw. abrupten Wechseln zwischen Idealisierung und Entwertung, Störungen der Identität mit oft erheblichen Selbstwertdefiziten, impulsive, teils hoch-riskante bzw. selbstschädigende Verhaltensweisen oder wiederholte Selbstverletzungen sowie Suizidalität, ausgeprägte Stimmungsschwankungen, ein Gefühl chronischer Leere (oft schwer unterscheidbar von Depressivität), unkontrollierbare Wut und aggressives Verhalten sowie belastungs- oder stressabhängige psychotische oder dissoziative Symptome. Gemäß dem Diagnostic and Statistical Manual for Mental Disorders (DSM), das nun in seiner fünften Revision vorliegt, müssen fünf dieser neun Kriterien gleichzeitig für die Diagnose einer BPS vorliegen [3]. Die in Europa gebräuchlichere 10. Auflage der International Classification of Diseases (ICD), von der World Health Organisation (WHO) herausgegeben, ist in Bezug auf die diagnostischen Kriterien der BPS weit weniger präzise. Die in Kürze erscheinende 11. Auflage (ICD-11) nähert sich jedoch diesbezüglich deutlich den Kriterien der Amerikanischen Gesellschaft an [16]. Die Heterogenität des Störungsbilds spiegelt sich dennoch dadurch wider, dass mathematisch mehr als 100 Symptomkonstellationen möglich sind und sich zwei Patienten nur in einem Symptom überlappen können, ein Umstand, dem therapeutisch bisher recht wenig Rechnung getragen wird (aufgrund besserer Lesbarkeit verzichten wir in diesem Beitrag auf die feminine Form „Patientinnen“).
BPS sind in der Allgemeinbevölkerung mit einer Prävalenz von etwa 2 bis 6 % außerordentlich häufig [23], wobei subklinische Phänotypen nicht berücksichtigt sind. In ambulant-psychiatrischen Kollektiven finden sich BPS in bis zu 10 %, in stationären Stichproben sogar in bis zu 20 %. Meist tritt maladaptives Verhalten bereits in der Kindheit oder Jugend in Erscheinung, die Diagnosestellung verzögert sich jedoch aus vielfältigen Gründen oft um Jahre [57, 62]. Zu den Risikofaktoren für die Entwicklung einer BPS zählen vor allem aversive Kindheitserfahrungen, etwa emotionale Vernachlässigung, invalidierende Erziehungsstile der Eltern und auch sexuelle Traumatisierung [41, 42, 65, 67]. Wenngleich eine hereditäre Komponente der Störung als belegt gelten darf [20], sind „Risikogene“ für die BPS bislang nicht identifiziert worden [1]. Neurobiologisch werden Dysfunktionen, zum Teil auch strukturelle Abweichungen, vor allem in neuronalen Netzwerken vermutet, die an der Emotionsverarbeitung und -regulation beteiligt sind. Dazu zählen in erster Linie die Mandelkerne (Amygdalae), die vordere Inselregion, der anteriore zinguläre Kortex sowie der mediale und laterale orbitofrontale und der dorsomediale und dorsolaterale präfrontale Kortex (Übersicht bei [26, 51]). Neurochemisch gibt es Hinweise auf Dysfunktionen in verschiedenen Neurotransmittersystemen. New et al. [37] postulieren beispielsweise einen Zusammenhang zwischen Amygdalahyperaktivität und einer defizitären Serotonin-vermittelten kortikalen Top-down-Regulation. Darüber hinaus scheint die Verfügbarkeit von Neuropeptiden wie Oxytocin, das eine wichtige Rolle für sozial-kognitive Funktionen hat, bei Patienten mit BPS verändert zu sein (Übersicht bei [14]). Des Weiteren wurde bei BPS unter sozialen Stressbedingungen eine reduzierte Cortisol-Ausschüttung beobachtet [35] und Beeinträchtigungen im Hinblick auf affiliatives Verhalten legen eine Fehlfunktion des endogenen Opioid-Systems nahe [58].
Behandlungsrealität bei BPS
Sämtliche internationale Leitlinien wie etwa die der American Psychiatric Association (APA), des National Institute of Health and Excellence (NICE) sowie des australischen National Health and Medical Research Council (NHMRC) sehen psychotherapeutische Verfahren als Methode der Wahl bei Patienten mit Persönlichkeitsstörungen, einschließlich BPS [4, 36, 43]. Mit einer deutschen Leitlinie auf S3-Niveau ist voraussichtlich 2019 zu rechnen. Zu den etablierten Verfahren für die BPS zählen die dialektisch behaviorale Therapie (DBT), die mentalisierungsbasierte Therapie (MBT), die übertragungsfokussierte Therapie (ÜFT) und die Schematherapie [12].
Trotz mangelnder Evidenz ist es jedoch klinische Realität, dass viele Patienten mit BPS oft auch psychopharmakologisch behandelt werden, nicht selten sogar „polypragmatisch“ mit mehreren Substanzen [8]. Einer US-amerikanischen Studie zufolge nahmen über 70 % der Patienten mit einer BPS Psychopharmaka ein; 50 % nahmen mindestens zwei Medikamente ein, 36 % drei Substanzen, mehr als 20 % vier Präparate und mehr als 11 % nahmen mindestens fünf verschiedene Psychopharmaka ein [66]. In einer Studie aus Spanien fanden sich noch höhere Prozentsätze psychopharmakologischer Behandlungen: 94 % der Patienten mit BPS erhielten Psychopharmaka, durchschnittlich nahmen die Patienten 2,7 Präparate ein [43]. Diese Zahlen bestätigten sich auch in einer neueren Studie, in der psychopharmakotherapeutische Interventionen bei Patienten mit BPS in den vergangenen 15 Jahren untersucht wurden. Diese Untersuchung ergab, dass in diesem Zeitraum 88,4 % der Betroffenen medikamentös mit Psychopharmaka behandelt wurden und 53,8 % mehr als drei Psychopharmaka einnahmen [32]. Zwar bestand ein Zusammenhang zwischen Polypharmazie und dem Vorhandensein komorbider Störungen wie Depressionen, zugleich zeigte sich aber, dass 80 % der Patienten ohne Komorbiditäten ebenfalls medikamentös behandelt wurden, wobei 42 % mehrere Medikamente erhielten [32]. Teilweise noch höhere Verordnungszahlen von Psychopharmaka und Polypharmazie bei Patienten mit BPS wurden in anderen Ländern beobachtet wie etwa in Spanien und Italien [13, 40]. Im Hinblick auf die Substanzgruppen werden vor allem Antidepressiva, Antipsychotika, Stimmungsstabilisierer und Sedativa verordnet, wobei die Verschreibungspraktiken erheblich variieren und von verschiedenen Faktoren, beispielsweise der Symptomausprägung, dem Komorbiditätsprofil und auch persönlichen Vorlieben und Erfahrungen der behandelnden Ärzte abhängen [13, 40, 43, 45]. Hinsichtlich der Verordnung von Benzodiazepinen gibt es erhebliche regionale Unterschiede [13, 40]. Zudem zeichnet sich ab, dass die Verschreibung von trizyklischen Antidepressiva und Benzodiazepinen rückläufig ist, jedoch atypische Antipsychotika zunehmend häufiger verordnet werden [32].
Insgesamt zeigt die Datenlage, dass Polypharmazie bei Personen mit einer BPS weit verbreitet ist und die Empfehlungen auch in den Ländern, in denen Leitlinien erarbeitet worden sind, im klinischen Alltag nur bedingt umgesetzt werden.
Die Gründe für diese Verordnungspraktiken sind sicher vielfältig. Neben einem Mangel an psychotherapeutischen Behandlungsplätzen und der Zurückhaltung von Psychotherapeuten unterschiedlicher „Schulenzugehörigkeit“, Patienten mit BPS in Behandlung zu nehmen, stellen sicher die das Cluster B (nach DSM-Klassifikation) kennzeichnenden „dramatisierenden“ Verhaltensweisen, in erster Linie Erregungszustände, selbstschädigendes oder aggressives Verhalten, dissoziative Zustände und „Pseudohalluzinationen“, häufige Indikationen für psychopharmakologische Interventionen dar. Diese führen oft zur Inanspruchnahme psychiatrischer oder somatischer Notfallambulanzen, was in der Regel dazu führt, auch aus Gründen des Zeitmanagements, dass der medikamentösen Therapie gegenüber einer psychotherapeutischen Intervention der Vorzug gegeben wird. Hinzu kommt, dass viele Notfallkontakte von Patienten mit BPS durch Intoxikationen mit psychotropen Substanzen kompliziert sind, was ebenfalls eine akute pharmakologische Behandlung erfordern kann. Aber auch im weiteren Behandlungsverlauf stellt sich die Frage nach einer adäquaten Therapie zur Linderung der vielfältigen Symptome, unter denen Patienten mit einer BPS leiden.
Dieser Artikel hat daher zum Ziel, eine Übersicht zur aktuellen Studienlage hinsichtlich psychopharmakologischer Behandlungsmöglichkeiten der BPS zu geben. Dabei werden zunächst die wichtigsten Substanzgruppen bewertet und im Anschluss zwei Behandlungsalgorithmen vorgeschlagen, die die medikamentöse Therapie der häufigsten komorbiden Störungen der BPS und ein symptomorientiertes Vorgehen der klinisch bedeutsamsten Störungen des Erlebens und Verhaltens der BPS skizzieren. Hier ist zu beachten, dass viele der genannten Strategien „off Label“ sind, nur teilweise einem Evidenzgrad 2 entsprechen, weil Placebo-kontrollierte, doppelt-verblindete Studien fehlen, sodass im vorliegenden Artikel auch die klinische Erfahrung der Autoren einfließt, die von der anderer Arbeitsgruppen natürlich abweichen kann.
Behandlung mit Antidepressiva
Antidepressiva sind die bei Persönlichkeitsstörungen am häufigsten verordneten Psychopharmaka. Auffällig ist in diesem Zusammenhang, dass nur bei weniger als der Hälfte der Patienten, die Antidepressiva erhielten, klinisch eine depressive Störung diagnostiziert wurde. Anders ausgedrückt, bei der Mehrzahl der Patienten bestand gar keine Indikation zur Verordnung von Antidepressiva [17]. Bedenklich ist zudem, dass, wie andere Studien zeigen, bei Patienten mit Persönlichkeitsstörung und komorbider Depression das klinische Outcome schlechter ist, wenn sie Antidepressiva einnehmen als ohne thymoleptische Medikation [22, 38]. Dies liegt möglicherweise daran, dass Antidepressiva ohnehin nur bei mindestens mittelschweren Depressionen eingesetzt werden sollten, nicht aber bei leichten depressiven Verstimmungen. Umstritten ist weiterhin der Einsatz von Antidepressiva bei Trauerreaktionen, die nicht selten mit Depressionen und bei der BPS mit Verlustängsten verwechselt werden [55].
Im Hinblick auf die BPS zeigte eine Metaanalyse von 21 randomisierten Studien, dass eine antidepressive Medikation lediglich – und dies nur in geringem Ausmaß – starke Affekte wie Angst und Wut lindern [27] und auch nur geringfügig impulsive Aggressivität oder Affektlabilität dämpfen kann [48]. Dabei ist zu beachten, dass insbesondere trizyklische Antidepressiva aufgrund ihrer anticholinergen Eigenschaften kognitive Defizite verstärken und sogar Aggressivität und Suizidalität verschlimmern können [48].
Eine Alternative dazu könnten Monoaminoxidasehemmer (MAOH) sein, die sich als effektiv bei der Behandlung von Impulsivität und Depressivität erwiesen haben; aufgrund der geringen therapeutischen Breite werden aber irreversible MAOH bei Patienten mit BPS nicht gerne verordnet, und zu den reversiblen MAOH gibt es bisher keine fundierten Studien bei der BPS [48].
Unsere klinische Einschätzung ist, dass Antidepressiva bei der BPS zurückhaltend und nur bei klinisch relevanter depressiver Symptomatik mit einem Schweregrad einer mindestens mittelgradigen depressiven Episode eingesetzt werden sollten, zumal sedierende Antidepressiva (etwa Mirtazapin) häufig zu Gewichtszunahme führen, sodass insbesondere bei jungen Frauen der Einsatz nicht gerechtfertigt ist und auch nicht toleriert wird. Bei schweren Antriebsstörungen kann Bupropion hilfreich sein, vor allem dann, wenn auch Aufmerksamkeit und Konzentration beeinträchtigt sind.
Behandlung mit Antipsychotika
Antipsychotika der ersten Generation wie Haloperidol wirken vor allem über den Dopamin-D2-Rezeptor-Antagonismus und sind in der Behandlung schwerster akuter psychomotorischer Erregungszustände oft unverzichtbar. Unter höheren Dosen muss mit einer Verlängerung der QTc-Zeit und Herzrhythmusstörungen sowie extrapyramidal motorischen Symptomen (EPMS) gerechnet werden. Im Hinblick auf die BPS berichten Shafti und Shahveisi [53], dass Patienten, die aufgrund von Angst, Anspannung oder psychosenahen Symptomen Haloperidol erhielten, häufiger unter Tremor, Parkinsonismus und Akathisie litten als Patienten, die mit Olanzapin behandelt wurden. Generell werden bei Patienten mit BPS daher häufiger Antipsychotika der zweiten Generation eingesetzt. Am häufigsten scheint Quetiapin bei der BPS im Indikationsbereich Schlafstörungen, Impulsivität und emotionale Dysregulation verordnet zu werden [7, 13], wobei jenseits von 300 mg Tagesdosis vermehrt unerwünschte Wirkungen wie Mundtrockenheit, Appetitstörungen und Sedierung auftreten [9]. Wegen seines dämpfenden Effekts wird auch Olanzapin in der Behandlung von Aggressions- und Angstzuständen eingesetzt [5]. Auch Clozapin scheint einen Effekt auf Impulsivität, Aggressivität und Erregungszustände zu haben [25]. Aripiprazol zeigte sich wirksam im Hinblick auf eine Verbesserung von Affektregulation, Impulskontrolle sowie dissoziative und paranoide Symptome bei insgesamt guter Toleranz von Nebenwirkungen, wie Kopfschmerzen, Übelkeit oder Schlafstörungen [6, 39]. Risperidon scheint vor allem im Hinblick auf Aggressivität wirksam zu sein [15, 49]. Für Ziprasidon hingegen fand sich bei der Untersuchung von Patienten mit BPS keine positive Wirkung im Hinblick auf depressive und ängstliche Verstimmungen, Impulsivität und psychosenahe Symptome [44].
Insgesamt ergeben metaanalytische Studien, dass Antipsychotika einen signifikanten Effekt auf kognitiv-perzeptive Symptome (paranoide Ideen, Dissoziation und Pseudohalluzinationen), Aggressivität sowie das globale Funktionsniveau bei Patienten mit BPS hatten [27]. Auch ein Cochrane-Review deutet darauf hin, dass Antipsychotika der zweiten Generation unter strenger Indikationsstellung bei der BPS hilfreich sein können, wenngleich die vorhandenen Studien einen geringen Evidenzgrad aufweisen [30, 61].
Generell haben Antipsychotika der zweiten Generation Vorteile gegenüber älteren Substanzen in Bezug auf das Risiko für die Entwicklung extrapyramidal-motorischer Symptome. Jedoch kommt es vor allem unter Ziprasidon, Clozapin, Olanzapin und Quetiapin gehäuft zu einer Gewichtszunahme, Müdigkeit und Benommenheit, und die Gefahr der Entwicklung eines metabolischen Syndroms ist erheblich. In diesem Zusammenhang ist aus unserer Sicht zu bedenken, dass viele junge Frauen mit BPS ohnehin schon häufig unter Minderwertigkeitsgefühlen leiden, die durch eine unerwünschte Gewichtszunahme verstärkt werden können. Zudem muss bedacht werden, dass komorbide Essstörungen in dieser Patientenpopulation nicht selten sind. Clozapin werden zwar antisuizidale und antiaggressive Wirkungen zugeschrieben [2], es besteht aber bekanntermaßen die Gefahr gefährlicher Blutbildveränderungen bis hin zur Agranulozytose sowie schwerwiegender kardiotoxischer Effekte, die ein engmaschiges Monitoring dieser Behandlung erfordern [18].
Unsere klinische Erfahrung ist, dass stationär zugewiesene Patienten mit BPS oft (zu) hohe Dosen sedierender Antipsychotika einnehmen. Dies wirkt sich nicht selten auch deshalb negativ auf die Therapie aus, weil pharmakogene Negativsymptomatik wie Anhedonie, Affektverflachung und Abulie den Zugang zum eigenen emotionalen Erleben geradezu behindern, sodass zuerst eine langsame und vorsichtige Dosisreduktion erforderlich ist, bevor psychotherapeutische Interventionen greifen können. Daher halten wir einen zurückhaltenden Umgang mit diesen Substanzen in der symptomatischen Behandlung der BPS für erforderlich.
Behandlung mit stimmungsstabilisierenden Substanzen
Die antikonvulsiv wirksame Substanz Valproinsäure, aber auch biochemisch andere Antikonvulsiva wie Lamotrigin werden in der pharmakologischen Behandlung der BPS vielfach zur Reduktion von Impulsivität und Aggressivität sowie zur Stimmungsstabilisierung eingesetzt [13, 25, 29, 56, 63]. Auch Topiramat scheint bei Patienten mit BPS zu einer Verringerung von Aggressivität und Wut zu führen [31, 64]. Auch die bereits mehrfach genannte Metaanalyse [27] resümiert, dass stimmungsstabilisierende Antikonvulsiva bei Patienten mit BPS vor allem impulsives Verhalten, Angsterleben und das globale Funktionsniveau positiv beeinflussen können.
Insgesamt werden diese Substanzen meistens besser vertragen als viele Antipsychotika. Dennoch ist auch hier die Indikation streng zu stellen, weil Valproinsäure etwa bei Frauen im gebärfähigen Alter nicht empfohlen wird und in der Schwangerschaft streng kontraindiziert ist (aufgrund des Risikos von Neuralrohrdefekten), Lamotrigin mit dem Risiko eines Stevens-Johnson-Syndroms einhergeht und zur Verhinderung eines Lyell-Syndroms sehr behutsam eindosiert werden muss, und Topiramat zu einer unerwünschten Gewichtsreduktion führen kann. Vor allem in Bezug auf Lamotrigin sind zudem Interaktionen mit anderen Substanzen zu beachten. Lamotrigin induziert den Abbau von Quetiapin, andererseits kann sein Abbau durch Valproinsäure beschleunigt werden. Außerdem sind Interaktionen mit oralen Kontrazeptiva möglich. In Kombination mit Sertralin besteht die Gefahr, dass durch die Hemmung eines Schlüsselenzyms, das für die Glukuronidierung von Lamotrigin verantwortlich ist, über alternative Abbauwege ein toxisches Zwischenprodukt entsteht [28].
Interessanterweise gibt es kaum Untersuchungen zur Wirksamkeit von Lithium bei der BPS. Indikationen für eine Verordnung von Lithiumsalzen könnten Stimmungsstabilisierung, Augmentation einer Antidepressivabehandlung bei komorbider Depression und vor allem die Reduktion von Suizidalität sein. Wegen der geringen therapeutischen Breite von Lithium und der manchmal schwierigen Therapieadhärenz und Compliance von Patienten mit BPS ist diese Option bislang nicht systematisch in Betracht gezogen worden [47].
Behandlung mit Benzodiazepinen
Der Einsatz von Benzodiazepinen bei der BPS hat allenfalls im Rahmen akuter Erregungszustände und suizidalen Krisen eine Berechtigung, wenn psychotherapeutische Strategien nicht ausreichen. Manche Autoren raten sogar generell von einer Behandlung mit Benzodiazepinen bei akuter Suizidalität aufgrund der Gefahr einer Enthemmung ab [21]. Auch ein oft ohnehin schon vermindertes Gefühl von Selbstwirksamkeit kann durch die Gabe von Benzodiazepinen verstärkt werden. Wichtig ist weiterhin, dass die Gabe von Benzodiazepinen bei dissoziativen Zuständen kaum hilfreich ist und möglicherweise zu deren Aufrechterhaltung wegen der Verstärkung von Derealisation und Depersonalisation beiträgt [52]. Eine längere Verordnung von Benzodiazepinen ist wegen der bekannten Abhängigkeitsentwicklungen in der Regel nicht indiziert.
Behandlung mit anderen Substanzen
Die Behandlung dissoziativer Zustände („flashbacks“) und Albträumen stellt eine besondere therapeutische Herausforderung dar. Antipsychotika und Antidepressiva sind hier kaum hilfreich. Ein Therapieversuch mit Clonidin, einem zentralen Alpha-2-Rezeptoragonisten, kann im Hinblick auf vegetative Übererregbarkeit, innere Unruhezustände, dissoziative Symptome und Selbstverletzung bei komorbider posttraumatischer Belastungsstörung (PTBS) indiziert sein [46]. Auch die biochemisch verwandte Substanz Doxazosin, ein zentraler alpha-1-adrenerger Antagonist, kann bei Angst, Flashbacks und vor allem Albträumen möglicherweise durch eine De-Fragmentierung des REM-Schlafs hilfreich sein [50].
Naltrexon ist ein kompetitiver µ-Opioidrezeptorantagonist, der zur Entwöhnungsbehandlung bei Opiatabhängigkeit sowie zur Reduktion des Rückfallrisikos bei Alkoholabhängigkeit verordnet werden kann. Es gibt jedoch auch Hinweise darauf, dass der Arzneistoff dissoziative Symptome und selbstverletzendes Verhalten bei Patienten mit BPS lindert [33]. In der experimentellen Erprobung ist auch das Neuropeptid Oxytocin bzw. agonistisch wirkende Substanzen, die möglicherweise zu einer Stress- und Angstreduktion beitragen können. Problematisch ist bei Oxytocin die kurze Halbwertszeit, die wiederholte Gaben erfordert, unter Umständen auch die experimentelle Beobachtung, dass Oxytocin zu keiner Verbesserung affiliativen und prosozialen Verhaltens bei BPS führt [14]. Nahrungsergänzungsstoffe wie Omega-3-Fettsäuren haben möglicherweise positive Effekte auf die Reduktion von Impulsivität und Aggressivität bei Patienten mit BPS [11].
Die beiden Schaubilder illustrieren zusammenfassend die pharmakologischen Behandlungsstrategien bei dem Vorliegen komorbider Störungen (Abb. 1) und symptom- bzw. syndromorientierte Behandlungsoptionen bei der BPS (Abb. 2). An dieser Stelle sei noch einmal darauf hingewiesen, dass kontrollierte randomisierte Studien weitgehend fehlen, der Evidenzgrad der meisten Empfehlungen daher gering ist und manche der skizzierten Behandlungsmöglichkeiten „off Label“ sind und auf unkontrollierte Studien und Anwendungsbeobachtungen beruhen.
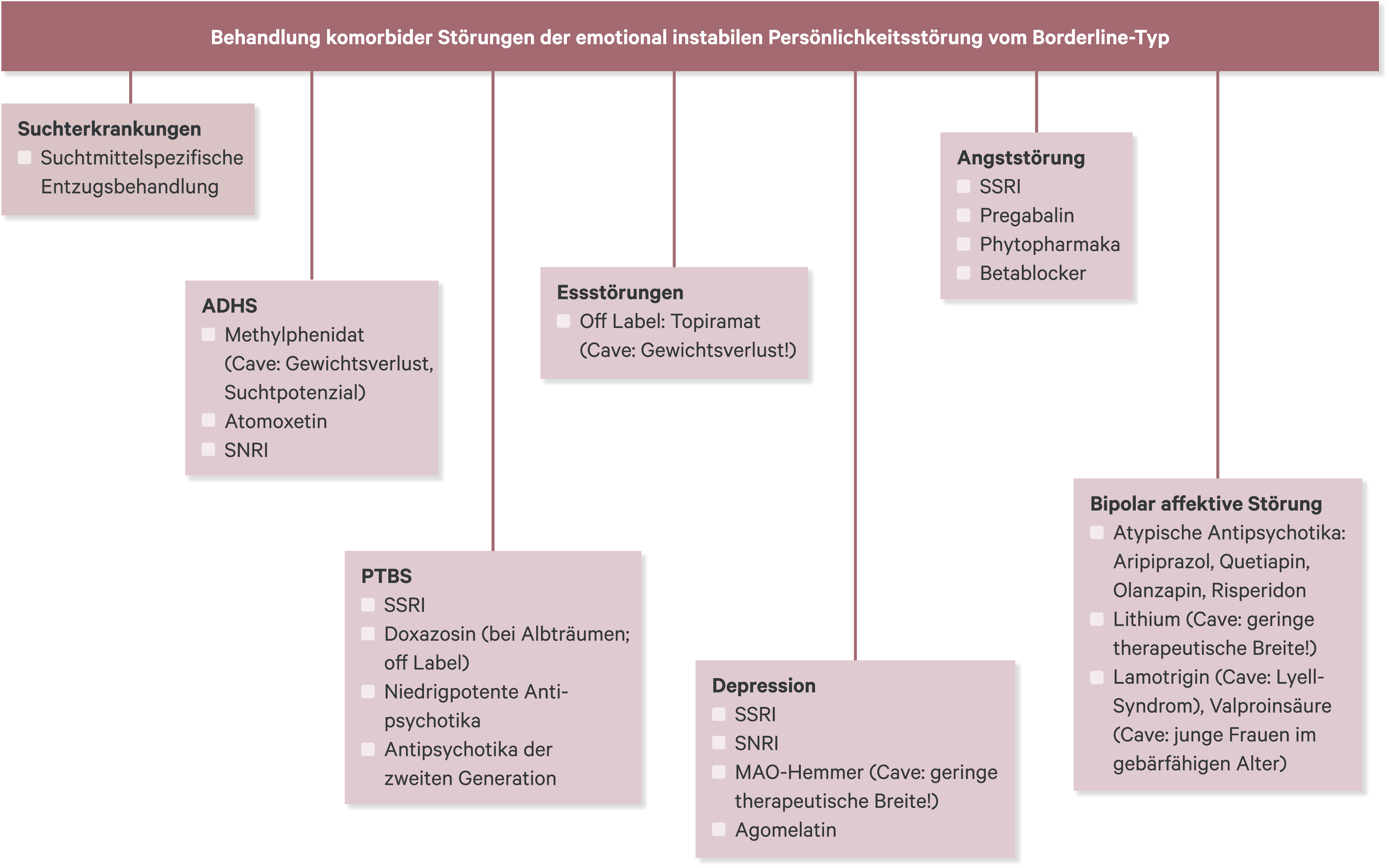
Abb. 1. Behandlung komorbider Störungen der emotional instabilen Persönlichkeitsstörung vom Borderline-Typ. SSRI: selektive Serotonin-Wiederaufnahmehemmer; SNRI: selektive Noradrenalin-Wiederaufnahmehemmer (z. B. Bupropion); MAO: Monoaminoxidase

Abb. 2. Behandlungsoptionen spezifischer Symptome der emotional instabilen Persönlichkeitsstörung vom Borderline-Typ
Diskussion
Die BPS ist eine schwere psychische Störung, deren Behandlung oft langwierig und kompliziert ist. Die Therapie des Störungsbildes ist primäre Domäne psychotherapeutischer Verfahren, von denen sich DBT, MBT, ÜFT und Schematherapie als etabliert und wirksam erwiesen haben. Die BPS ist oft vergesellschaftet mit komorbiden psychischen Erkrankungen, vor allem Depressionen, PTBS, bipolaren affektiven Störungen, Aufmerksamkeitsdefizit-/Hyperaktivitätsstörungen (ADHS), Abhängigkeitserkrankungen und anderen Persönlichkeitsstörungen. Die Behandlung der Komorbidität rechtfertigt bei entsprechender Indikationsstellung die Behandlung mit Psychopharmaka, wobei stets auch das Risikoprofil der BPS, etwa im Hinblick auf die um den Faktor sechs bis sieben erhöhte Rate kardiovaskulärer Ereignisse, berücksichtigt werden muss [34].
In Bezug auf die medikamentöse Behandlung der BPS kritisieren Ingenhoven et al. [27] und Hancock-Johnson et al. [24] in ihren Metaanalysen die geringe Anzahl Placebo-kontrollierter randomisierter Studien, geringe Stichprobengrößen mit vorrangig weiblichen Probanden sowie oft zu kurze Beobachtungszeiträume und das Fehlen von Follow-up-Untersuchungen. Wie bei pharmakologischen Studien üblich, fordern die Autoren die Einhaltung wissenschaftlicher Standards, etwa die präzise Definition von Ein- und Ausschlusskriterien, des Behandlungssettings (ambulant vs. stationär), des Studiendesigns (Randomisierungstyp, Beobachtungsintervalle), der Verblindung, der Reliabilität und Validität von Ergebnisvariablen, der Abbruchrate, der Intent-to-treat-Analyse, der Baseline-Werte der untersuchten Parameter sowie Messung von Effektstärken.
Lieb et al. [30] weisen in ihrem Cochrane-Review darauf hin, dass es in Bezug auf mehrere Kernsymptome der BPS, etwa chronisches Leeregefühl, Verlustängste und Identitätsstörungen keine brauchbaren medikamentösen Behandlungsoptionen gibt. In diesem Zusammenhang ist auch herauszustellen, dass sich Depressivität bei der BPS oft anders äußert als bei klassischen depressiven Episoden bzw. bei der „Major Depression“ [55]. Starcevic und Janca [60] halten daher zusammenfassend fest, dass Medikamente bei der BPS symptomorientiert, in Krisen oder bei Exazerbation spezifischer Beschwerden möglichst nur über einen kurzen Zeitraum verordnet werden sollten. Die Notwendigkeit einer Fortführung pharmakotherapeutischer Interventionen sollte häufig reevaluiert und Polypharmazie verhindert werden.
Der therapeutische Umgang mit Patienten mit BPS stellt Therapeuten und therapeutische Teams oft vor große Herausforderungen. Die Reinszenierung verstrickter Beziehungsmuster, Projektion und projektive Identifikation sowie Spaltungsmechanismen, aber auch negative Gegenübertragung, können die Gesamtbehandlung erheblich beeinflussen, einschließlich der Entscheidungsfindung im Hinblick auf eine adäquate medikamentöse Behandlung. Verständlicherweise erwarten viele Patienten eine möglichst rasche Linderung ihrer Beschwerden und reagieren mit Frustration oder Enttäuschung, wenn sich dieses Anliegen nicht unmittelbar realisieren lässt. Hohe Erwartungshaltungen an die Wirksamkeit einer medikamentösen Behandlung, gepaart mit geringer Selbstwirksamkeitserwartung, kann Drucksituationen erzeugen, denen sich Ärzte und Therapeuten, teils auch aus Zeitmangel, nicht gerne aussetzen, sodass der Griff zum Rezeptblock oft die einfachste Lösung zu sein scheint. So kann es eigentlich nicht verwundern, dass gerade Patienten mit BPS häufiger Medikamente verordnet bekommen als Patienten mit anderen Persönlichkeitsstörungen. Umgekehrt konnte gezeigt werden, dass sie in Zentren, die auf die Behandlung der BPS spezialisiert sind, weniger Medikamente erhielten als Patienten, die in allgemeinpsychiatrischen Abteilungen behandelt wurden. Dies weist darauf hin, dass die Schulung des therapeutischen Teams im Umgang mit Anspannungszuständen und manipulativem Verhalten wichtig ist, diesen Herausforderungen professionell begegnen zu können [10, 19, 59]. Sollte die Indikation einer medikamentösen Behandlung komorbider Störungen oder spezieller Symptome gestellt werden, befürwortet Silk [54], erst nach Etablierung einer tragfähigen therapeutischen Beziehung eine Behandlung mit Medikamenten zu beginnen bzw. eine bereits bestehende zu verändern. Ziel muss sein, in einem offenen und vertrauensvollen Dialog mit dem Patienten über die Möglichkeiten und Grenzen sowie die Risiken einer medikamentösen Behandlung zu sprechen, auch, um unrealistischen Erwartungen zu begegnen. Die Evaluation einer pharmakotherapeutischen Behandlung sollte unter Förderung von Selbstwirksamkeitserwartungen und Ermutigung zur Anwendung von „Skills“ erfolgen, um das Gefühl einer Abhängigkeit von Medikamenten zu vermeiden. Ist die Rollenverteilung dergestalt, dass ärztliche und psychotherapeutische Behandlung nicht in einer Hand liegen, empfiehlt sich eine enge Absprache aller an der Behandlung Beteiligten, um Effekte der Medikation objektivieren und potenziell manipulatives Verhalten des Patienten auffangen zu können. In jedem Fall sollte darauf geachtet werden, dass die Wirksamkeit von Psychotherapie und einer Pharmakotherapie nicht gegeneinander ausgespielt wird, etwa dergestalt, dass Schwierigkeiten im psychotherapeutischen Prozess nicht vorschnell durch die (gut gemeinte) ergänzende Verordnung von Medikamenten zu beheben versucht wird.
Zusammenfassend bleibt festzuhalten, dass pharmakologische Behandlungsansätze bei der BPS individuell in Ergänzung zur Psychotherapie erwogen werden können, nicht aber Therapie der ersten Wahl sind, außer bei Vorliegen klinisch relevanter komorbider Störungen. Entscheidend bleibt die Beziehungsgestaltung zwischen Behandlungsteam und Patient, die eine empathische Grundhaltung erfordert und belastbar genug ist, interpersonelle Schwierigkeiten und Spannungen gemeinsam zu bewältigen.
Interessenkonflikterklärung
Die Autoren erklären, dass keine Interessenkonflikte vorliegen.
Literatur
1. Amad A, Ramoz N, Thomas P, Jardri R, et al. Genetics of borderline personality disorder: systematic review and proposal of an integrative model. Neurosci Biobehav Rev 2014;40:6–19.
2. Amamou B, Salah WB, Mhalla A, Benzarti N, et al. Use of clozapine for borderline personality disorder: a case report. Clin Psychopharmacol Neurosci 2016;14:226–8.
3. American Psychiatric Association (APA). Diagnostic and statistical manual of mental disorders. 5. Auflage. Washington DC, 2013.
4. American Psychiatric Association. American Psychiatric Association Practice Guidelines. Practice guideline for the treatment of patients with borderline personality disorder. Am J Psychiatry 2001;158(Suppl):1–52.
5. Belli H, Ural C, Akbudak M. Borderline personality disorder: bipolarity, mood stabilizers and atypical antipsychotics in treatment. J Clin Med Res 2012;4:301–8.
6. Bellino S, Paradiso E, Bogetto F. Efficacy and tolerability of aripiprazole augmentation in sertraline-resistant patients with borderline personality disorder. Psychiatry Res 2008;161:206–12.
7. Bellino S, Paradiso E, Bogetto F. Efficacy and tolerability of quetiapine in the treatment of borderline personality disorder: a pilot study. J Clin Psychiatry 2006;67:1042–6.
8. Bender DS, Dolan RT, Skodol AE, Sanislow CA, et al. Treatment utilization by patients with personality disorders. Am J Psychiatry 2001;158:295–302.
9. Black DW, Zanarini MC, Romine A, Shaw M, et al. Comparison of low and moderate dosages of extended-release quetiapine in borderline personality disorder: a randomized, double-blind, placebo-controlled trial. Am J Psychiatry 2014;171:1174–82.
10. Bland AR, Tudor G, McNeil Whitehouse D. Nursing care of inpatients with borderline personality disorder. Perspect Psychiatr Care 2007;43:204–12.
11. Bozzatello P, Brignolo E, De Grandi E, Bellino S. Supplementation with omega-3 fatty acids in psychiatric disorders: a review of literature data. J Clin Med 2016;5. pii: E67. doi: 10.3390/jcm5080067.
12. Bradley R, Conklin CZ, Westen D. Borderline personality disorder. In: O‘Donohue W, Fowler K, Lilienfeld S (editors). Sage handbook of personality disorders. Thousand Oaks, California: Sage, 2007: 167–202.
13. Bridler R, Häberle A, Müller ST, Cattapan K, et al. Psychopharmacological treatment of 2195 in-patients with borderline personality disorder: a comparison with other psychiatric disorders. Eur Neuropsychopharmacol 2015;25:763–72.
14. Brüne M. On the role of oxytocin in borderline personality disorder. Br J Clin Psychol 2016;55:287–304.
15. Carrasco JL, Palomares N, Marsá MD. Effectiveness and tolerability of long-acting intramuscular risperidone as adjuvant treatment in refractory borderline personality disorder. Psychopharmacology 2012;224:347–48.
16. Clark LA, Cuthbert B, Lewis-Fernández R, Narrow WE, et al. Three approaches to understanding and classifying mental disorder: ICD-11, DSM-5, and the National Institute of Mental Health’s Research Domain Criteria (RDoC). Psychol Sci Public Interest 2017;18:72–145.
17. Crawford MJ, Kakad S, Rendel C, Mansour NA, et al. Medication prescribed to people with personality disorder: the influence of patient factors and treatment setting. Acta Psychiatr Scand 2011;124:396–402.
18. De Berardis D, Rapini G, Olivieri L, Di Nicola D, et al. Safety of antipsychotics for the treatment of schizophrenia: a focus on the adverse effects of clozapine. Ther Adv Drug Saf 2018;9:237–56.
19. Dickens GL, Hallett N, Lamont E. Interventions to improve mental health nurses’ skills, attitudes, and knowledge related to people with a diagnosis of borderline personality disorder: systematic review. Int J Nurs Stud 2016;56:114–27.
20. Distel MA, Trull TJ, Derom CA, Thiery EW, et al. Heritability of borderline personality disorder features is similar across three countries. Psychol Med 2008;38:1219–29.
21. Gardner DL, Cowdry RW. Alprazolam-induced dyscontrol in borderline personality disorder. Am J Psychiatry 1985;142:98–100.
22. Gorwood P, Rouillon F, Even C, Falissard B, et al. Treatment response in major depression: effects of personality dysfunction and prior depression. Br J Psychiatry 2010;196:139–42.
23. Grant BF, Chou SP, Goldstein RB, Huang B, et al. Prevalence, correlates, disability, and comorbidity of DSM-IV borderline personality disorder: results from the Wave 2 National Epidemiologic Survey on Alcohol and Related Conditions. J Clin Psychiatry 2008;69:533–45.
24. Hancock-Johnson E, Griffiths C, Picchioni M. A focused systematic review of pharmacological treatment for borderline personality disorder. CNS Drugs 2017;31:345–56.
25. Haw C, Stubbs J. Medication for borderline personality disorder: a survey at a secure hospital. Int J Psychiatry Clin Pract 2011;15:280–5.
26. Herpertz SC, Dietrich TM, Wenning B, Krings T, et al. Evidence of abnormal amygdala functioning in borderline personality disorder: a functional MRI study. Biol Psychiatry 2001;50:292–8.
27. Ingenhoven T, Lafay P, Rinne T, Passchier J, et al. Effectiveness of pharmacotherapy for severe personality disorders: meta-analyses of randomized controlled trials. J Clin Psychiatry 2010;71:14–25.
28. Kaufman KR, Gerner R. Lamotrigine toxicity secondary to sertraline. Seizure 1998;7:163–5.
29. Leiberich P, Nickel MK, Tritt K, Pedrosa Gil F. Lamotrigine treatment of aggression in female borderline patients, Part II: an 18-month follow-up. J Psychopharmacol 2008;22:805–8.
30. Lieb K, Völlm B, Rücker G, Timmer A, et al. Pharmacotherapy for borderline personality disorder: Cochrane systematic review of randomised trials. Br J Psychiatry 2010;196:4–12.
31. Loew TH, Nickel MK, Muehlbacher M, Kaplan P, et al. Topiramate treatment for women with borderline personality disorder: a double-blind, placebo-controlled study. J Clin Psychopharmacol 2006;26:61–6.
32. Martín-Blanco A, Ancochea A, Soler J, Elices M, et al. Changes over the last 15 years in the psychopharmacological management of persons with borderline personality disorder. Acta Psychiatr Scand 2017;136:323–31.
33. Moghaddas A, Dianatkhah M, Ghaffari S, Ghaeli P. The potential role of naltrexone in borderline personality disorder. Iran J Psychiatry 2017;12:142–6.
34. Moran P, Stewart R, Brugha T, Bebbington P, et al. Personality disorder and cardiovascular disease: results from a national household survey. J Clin Psychiatry 2007;68:69–74.
35. Nater UM, Bohus M, Abbruzzese E, Ditzen B, et al. Increased psychological and attenuated cortisol and alpha-amylase responses to acute psychosocial stress in female patients with borderline personality disorder. Psychoneuroendocrinology 2010;35:1565–72.
36. National Institute for Clinical Excellence. Borderline personality disorder-treatment and management. London: National Institute for Clinical Excellence, 2008.
37. New AS, Goodman M, Triebwasser J, Siever LJ. Recent advances in the biological study of personality disorders. Psychiatr Clin North Am 2008;31:441–61.
38. Newton-Howes G, Tyrer P, Johnson T. Personality disorder and the outcome of depression: meta-analysis of published studies. Br J Psychiatry 2006;188:13–20.
39. Nickel MK, Muehlbacher M, Nickel C, Kettler C, et al. Aripiprazole in the treatment of patients with borderline personality disorder: a double-blind, placebo-controlled study. Am J Psychiatry 2006;163:833–8.
40. Paolini E, Mezzetti FA, Pierri F, Moretti P. Pharmacological treatment of borderline personality disorder: a retrospective observational study at inpatient unit in Italy. Int J Psychiatry Clin Pract 2017;21:75–9.
41. Paris J, Zweig-Frank H, Guzder J. Psychological risk factors for borderline personality disorder in female patients. Compr Psychiatry 1994;35:301–5.
42. Paris J. Childhood trauma as an etiological factor in the personality disorders. J Pers Disord 1997;11:34–49.
43. Pascual JC, Martín-Blanco A, Soler J, Ferrer A, et al. A naturalistic study of changes in pharmacological prescription for borderline personality disorder in clinical practice: from APA to NICE guidelines. Int Clin Psychopharmacol 2010;25:349–55.
44. Pascual JC, Soler J, Puigdemont D, Pérez-Egea R, et al. Ziprasidone in the treatment of borderline personality disorder: a double-blind, placebo-controlled, randomized study. J Clin Psychiatry 2008;69:603–8.
45. Paton C, Crawford MJ, Bhatti SF, Patel MX, et al. The use of psychotropic medication in patients with emotionally unstable personality disorder under the care of UK mental health services. J Clin Psychiatry 2015;76:e512–8.
46. Philipsen A, Richter H, Schmahl C, Peters J, et al. Clonidine in acute aversive inner tension and self-injurious behavior in female patients with borderline personality disorder. J Clin Psychiatry 2004;65:1414–9.
47. Rifkin A, Quitkin F, Carrillo C, Blumberg AG, et al. Lithium carbonate in emotionally unstable character disorder. Arch Gen Psychiatry 1972;27:519–23.
48. Ripoll LH. Clinical psychopharmacology of borderline personality disorder: an update on the available evidence in light of the Diagnostic and Statistical Manual of Mental Disorders – 5. Curr Opin Psychiatry 2012;25:52–8.
49. Rocca P, Marchiaro L, Cocuzza E, Bogetto F. Treatment of borderline personality disorder with risperidone. J Clin Psychiatry 2002;63:241–4.
50. Roepke S, Danker-Hopfe H, Repantis D, Behnia B, et al. Doxazosin, an α-1-adrenergic-receptor antagonist, for nightmares in patients with posttraumatic stress disorder and/or borderline personality disorder: a chart review. Pharmacopsychiatry 2017;50:26–31.
51. Ruocco AC, Amirthavasagam S, Zakzanis KK. Amygdala and hippocampal volume reductions as candidate endophenotypes for borderline personality disorder: a meta-analysis of magnetic resonance imaging studies. Psychiatry Res 2012;201:245–52.
52. Sadock BJ, Sadock VA. Kaplan and Sadock’s comprehensive book of psychiatry. Seventh edition. Philadelphia, PA: Lippincott, Williams and Wilkins, 2000.
53. Shafti SS, Shahveisi B. Olanzapine versus haloperidol in the management of borderline personality disorder: a randomized double-blind trial. J Clin Psychopharmacol 2010;30:44–7.
54. Silk KR. The process of managing medications in patients with borderline personality disorder. J Psychiatr Pract 2011;17:311–9.
55. Silk KR. The quality of depression in borderline personality disorder and the diagnostic process. J Pers Disord 2010;24:25–37.
56. Simeon D, Baker B, Chaplin W, Braun A, et al. An open-label trial of divalproex extended-release in the treatment of borderline personality disorder. CNS Spectr 2007;12:439–43.
57. Skodol AE, Siever LJ, Livesley WJ, Gunderson JG, et al. The borderline diagnosis II: biology, genetics, and clinical course. Biol Psychiatry 2002;51:951–63.
58. Stanley B, Sher L, Wilson S, Ekman R, et al. Non-suicidal self-injurious behavior, endogenous opioids and monoamine neurotransmitters. J Affect Disord 2010;124:134–40.
59. Stapleton A, Wright N. The experiences of people with borderline personality disorder admitted to acute psychiatric inpatient wards: a meta-synthesis. J Ment Health 2017;7:1–15.
60. Starcevic V, Janca A. Pharmacotherapy of borderline personality disorder: replacing confusion with prudent pragmatism. Curr Opin Psychiatry 2018;31:69–73.
61. Stoffers J, Völlm BA, Rücker G, Timmer A, et al. Pharmacological interventions for borderline personality disorder. Cochrane Database Syst Rev 2010;16(6):CD005653.
62. Stone MH. Long-term outcome in personality disorders. Br J Psychiatry 1993;162:299–313.
63. Tritt K, Nickel C, Lahmann C, Leiberich PK, et al. Lamotrigine treatment of aggression in female borderline-patients: a randomized, double-blind, placebo-controlled study. J Psychopharmacol 2005;19:287–91.
64. Varghese BS, Rajeev A, Norrish M, Khusaiby SB. Topiramate for anger control: a systematic review. Indian J Pharmacol 2010;42:135–41.
65. White CN, Gunderson JG, Zanarini MC, Hudson JI. Family studies of borderline personality disorder: a review. Harv Rev Psychiatry 2003;11:8–19.
66. Zanarini MC, Frankenburg FR, Hennen J, Silk KR. Mental health service utilization by borderline personality disorder patients and Axis II comparison subjects followed prospectively for 6 years. J Clin Psychiatry 2004;65:28–36.
67. Zanarini MC. Childhood experiences associated with the development of borderline personality disorder. Psychiatr Clin North Am 2000;23:89–101.
Prof. Dr. med. Martin Brüne, Dr. Idalia Nowak, Prof. Dr. Georg Juckel, LWL Universitätsklinikum Bochum, Klinik für Psychiatrie, Psychotherapie und Präventivmedizin, Ruhr-Universität Bochum, Alexandrinenstraße 1, 44791 Bochum, E-Mail: martin.bruene@rub.de
Pharmacotherapeutic strategies for emotionally unstable personality disorder, Borderline type
Borderline personality disorder (BPD) is characterised by poor emotion regulation abilities with rapid mood swings, affective instability, aggression, impulsivity, fears of abandonment and dissociative symptoms. BPD is often associated with interpersonal problems and with other psychiatric disorders. Even though there is no specific recommendation for drug treatment of BPD, and international guidelines suggest that psychotherapy is first choice for BPD, many patients with the condition receive several, if not more, psychotropic drugs.
The present article provides an overview of the current state of affairs regarding psychopharmacological treatment of BPD. First, it deals with the most important substance groups (antidepressants, antipsychotics, mood stabilizer, benzodiazepines), and subsequently suggests two treatment algorithms focusing on the most frequent comorbid conditions including substance dependence, unipolar and bipolar affective disorder, anxiety disorders, posttraumatic stress disorder, and attention-deficit/hyperactivity disorder (ADHD). The other algorithm proposes a symptom-based approach for the most relevant signs and symptoms associated with BPD, whereby many of the suggested strategies are “off label”.
Together, psychotropic medication for people with BPD is justified in the presence of clinically relevant comorbid psychiatric disorders. Evidence for a symptom-based approach is scarce, however, and warrants further evaluation.
Key words: borderline personality disorder; comorbidity; pharmacotherapy.
Psychopharmakotherapie 2019; 26(03):128-135
