Gerd Laux, Soyen/Waldkraiburg/München, und Walter E. Müller, Worms/Frankfurt a. M.
Schlafphysiologie
Der normale Schlaf zeigt in der Polysomnographie ein typisches Profil mit fünf ausgeprägten Stadien, die während einer durchschnittlichen Schlafdauer von acht Stunden in zyklischer Form auftreten (Abb. 7–1). Beim Einschlafen werden zuerst die vier Stadien des orthodoxen Schlafs durchlaufen. Stadium I bedeutet dabei den Übergang vom Wachsein zum Schlafen und umfasst etwa 4 bis 5 % der Schlafdauer. Das tiefere Schlafstadium II nimmt etwa 50 % der gesamten Schlafzeit ein; es ist im EEG durch das Auftreten sogenannter Spindelwellen und auffallend hoher Wellen, sogenannter K-Komplexe, gekennzeichnet. Die Tiefschlafstadien III und IV werden als „Slow-Wave“-Schlaf bezeichnet, da sie im EEG durch langsame Delta-Wellen mit hoher Amplitude imponieren. Dieser Delta-Schlaf tritt zum größten Teil während der ersten Hälfte der Schlafperiode auf. Nach dem Stadium IV durchläuft der Schläfer die Stadien in umgekehrter Reihenfolge. Dazwischen treten periodisch etwa alle 90 bis 100 Minuten sogenannte REM-Phasen auf. Dieser REM-Schlaf ist durch schnelle Augenbewegungen (REM = Rapid eye movements) und eine allgemeine Muskelerschlaffung charakterisiert. Zusätzlich sind Gehirnstoffwechsel, Gehirndurchblutung und Körpertemperatur gegenüber den anderen Schlafstadien auffällig gesteigert. REM-Phasen umfassen etwa 20 bis 25 % der Schlafdauer. Während dieser Zeit treten die meisten Träume auf. Auf REM-Schlaf-Entzug, also auf Traumentzug, reagiert der Mensch unter anderem mit Angstzuständen und Konzentrationsstörungen. REM-Schlaf und orthodoxer Schlaf sind für einen erholsamen Schlaf und das „Gefühl des Ausgeschlafenseins“ wichtig.
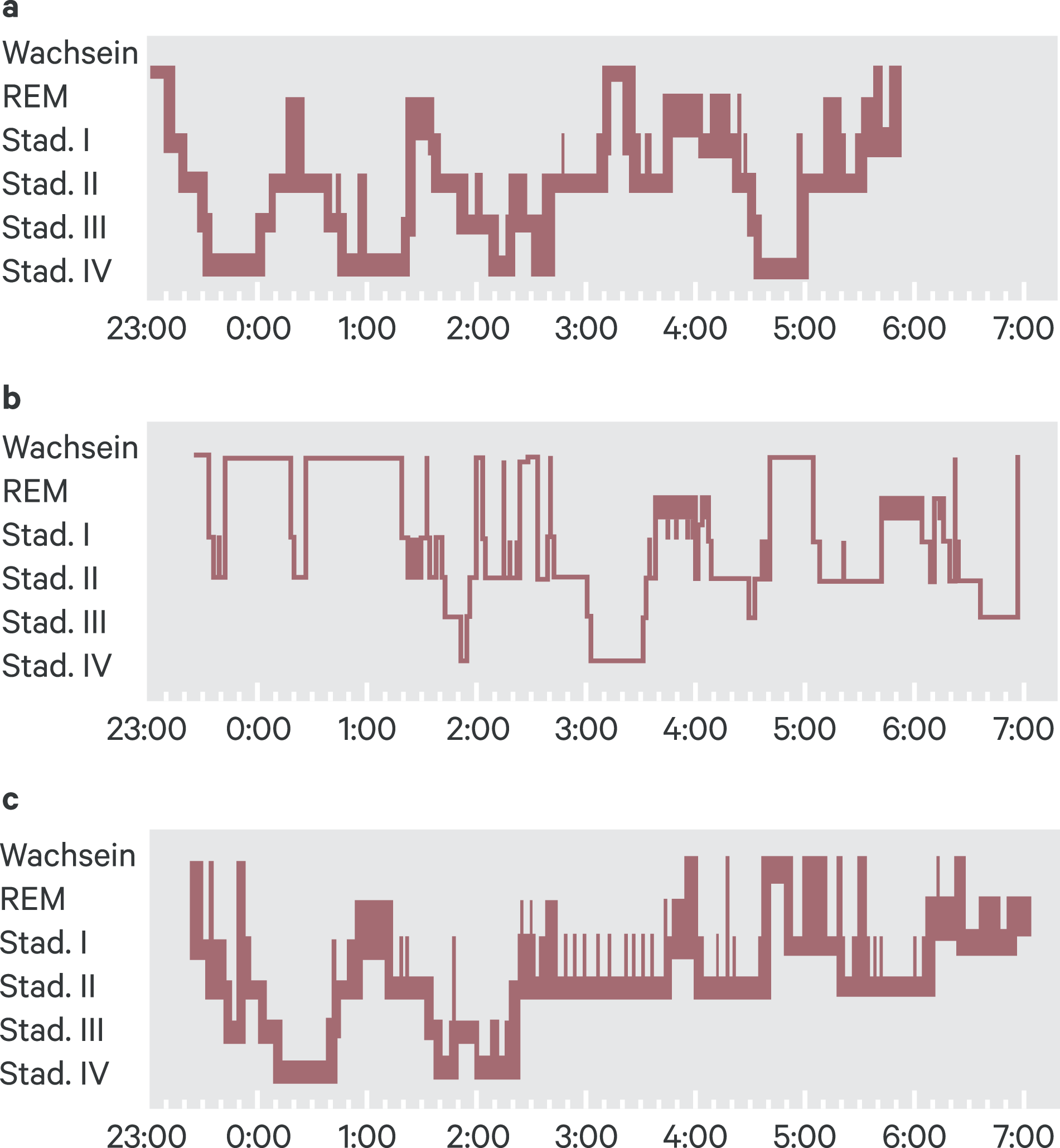
Abb. 7–1. Polysomnographische Aufzeichnung des Schlaf-Wach-Rhythmus (a) Typisches Schlafprofil beim Gesunden. (b) Schlaf eines Schlafgestörten ohne Medikation. Typisch ist dabei die Zerstückelung des physiologischen Profils mit häufigen, längeren Aufwachphasen und verkürztem Delta- und REM-Schlaf. (c) Schlafprofil unter Benzodiazepin-Medikation mit weitgehender Annäherung an das physiologische Profil. Allerdings ist deutlich die Verminderung der REM- Phasen und des Tiefschlafs zu erkennen. Auch alle anderen Hypnotika greifen auf verschiedenartige Weise in dieses Schlafmuster ein und verändern es mehr oder weniger in Richtung eines unphysiologischen Schlafablaufs [3].
Mit zunehmendem Lebensalter ändert sich das Schlafprofil. So nimmt die Schlaftiefe ab, die Anzahl der orthodoxen Phasen und die Häufigkeit des Erwachens gegen Morgen nehmen zu. Wie Abbildung 7–1c zeigt, verändern auch Schlafmittel das Schlafprofil mehr oder weniger stark. Das ideale Hypnotikum, das keinerlei Einfluss auf den natürlichen Schlaf ausübt, ist immer noch ein Wunsch, dem die heute verfügbaren Schlafmittel mehr oder weniger nicht entsprechen.
Schlafmittel der ersten Generation
Sieht man von einigen seit dem Altertum verwendeten natürlichen Substanzen wie Opium, Belladonna-Alkaloiden und Alkohol ab, begann die Ära der Schlafmittel mit der Verwendung verschiedener Alkohol-, Aldehyd- und Harnstoffderivate, aus denen letztlich auch die Barbiturate hervorgegangen sind. Gemeinsam war allen diesen Substanzen eine Dosis-abhängige Depression des ZNS, von Sedierung über Schlafinduktion bis zur Narkose und letztlich bis hin zu Atemdepression und Exitus. Die einzige Substanz, die aus dieser Generation noch zur Verfügung steht, ist Chloralhydrat (Trichloraldehydhydrat). Chloralhydrat soll sowohl eine Verstärkung GABAerger Effekte im ZNS als auch eine Hemmung des NMDA-induzierten Calciumionen-Einstroms in die Zelle bewirken. Die Substanz hat im Schlaflabor günstige Ergebnisse gezeigt. So bleibt der REM-Schlaf unverändert, das Tiefschlafstadium wird etwas vermehrt. Die Wirkung tritt rasch ein und hält nur kurz an. Chloralhydrat spielt jedoch selbst als Reservesubstanz (ohne relevante Muskelrelaxation) beispielsweise bei Sturz-gefährdeten Patienten heute kaum noch eine Rolle, zumal es schnell an Wirksamkeit verliert und eine beträchtliche Toxizität aufweist.
Erst mit den in den 60er-Jahren eher zufällig als Anxiolytika [16] entwickelten Benzodiazepinen standen nach ihrer Entwicklung als Hypnotika zum ersten Mal Schlafmittel mit deutlich geringerer Toxizität zur Verfügung, die praktisch keine narkotische bis atemdepressive Wirkung aufwiesen. Zur medikamentösen Behandlung von Insomnien stehen zwar verschiedene Substanzen zur Verfügung (Tab. 7–1). Die klassischen Benzodiazepine und andere an der Benzodiazepin-Bindungsstelle des GABA-A-Rezeptorkomplexes (Abb. 7–2) angreifende Substanzen (Z-Substanzen) spielen jedoch mit Abstand die wichtigste Rolle [5, 8, 10, 11, 15].
Tab. 7–1. Die wichtigsten heute zur Behandlung von Insomnien zur Verfügung stehenden Substanzgruppen mit Vor- und Nachteilen
|
Wirkstoffgruppe, Wirkstoff |
Vorteile |
Nachteile |
|
Benzodiazepine |
Gute hypnotische Potenz Jahrelange Erfahrung bezüglich des Wirkungs- und Nebenwirkungsprofils Geringe Toxizität |
Abhängigkeitspotenzial Rebound-Phänomene Amnesie Muskelrelaxation, Sturzrisiko Atemsuppression Paradoxe Reaktionen Tiefschlafunterdrückung |
|
Z-Substanzen (Zolpidem, Zopiclon) |
Gute hypnotische Potenz Kurze Wirkungsdauer, kaum Hangover Geringe Rebound-Problematik Geringe Toxizität |
Benzodiazepin-ähnliches Nebenwirkungsprofil |
|
Antidepressiva (Mirtazapin, Doxepin, Trimipramin) |
Kein Abhängigkeitspotenzial Geringe Absetzprobleme Keine Tiefschlafunterdrückung Antidepressive Wirkung |
Vergleichsweise höhere Toxizität Anticholinerge und kardiale Nebenwirkungen Lange Wirkungsdauer REM-Schlaf-Unterdrückung (nur Trimipramin) Wenige Anwendungsstudien |
|
Neuroleptika (Melperon, Pipamperon, Quetiapin) |
Kein Abhängigkeitspotenzial Keine REM-Schlafunterdrückung Geringe Kardiotoxizität Zum Teil antipsychotische Wirkung |
Anticholinerge, extrapyramidal-motorische, hämatologische, blutdrucksenkende Nebenwirkungen Zum Teil lange Wirkungsdauer Wenige Anwendungsstudien |
|
Chloralhydrat |
Unbeeinflusstes Schlafprofil Schneller Wirkungseintritt |
Geringe hypnotische Potenz Geringe therapeutische Breite Rascher Wirkungsverlust |
|
Antihistaminika |
Verhältnismäßig geringe Toxizität Nicht verschreibungspflichtig |
Geringe hypnotische Potenz Schneller Wirkungsverlust Anticholinerge Nebenwirkungen |
|
Clomethiazol |
Gute hypnotische Potenz Schneller Wirkungseintritt Kurze Wirkungsdauer |
Abhängigkeitspotenzial Atemdepression Hypersekretion |
|
Melatonin |
Nebenwirkungsarm Keine Beeinflussung des Schlafprofils |
Keine akute hypnotische Wirkung, sondern regulierender Einfluss auf den Schlaf-Wach-Rhythmus nach längerer Einnahme (ca. 3 Wochen) Klinische Erfahrungen bisher kaum vorhanden |
|
Phytotherapeutika |
Kein Abhängigkeitspotenzial Nahezu fehlende Toxizität Nicht verschreibungspflichtig |
Minimale hypnotische Potenz |
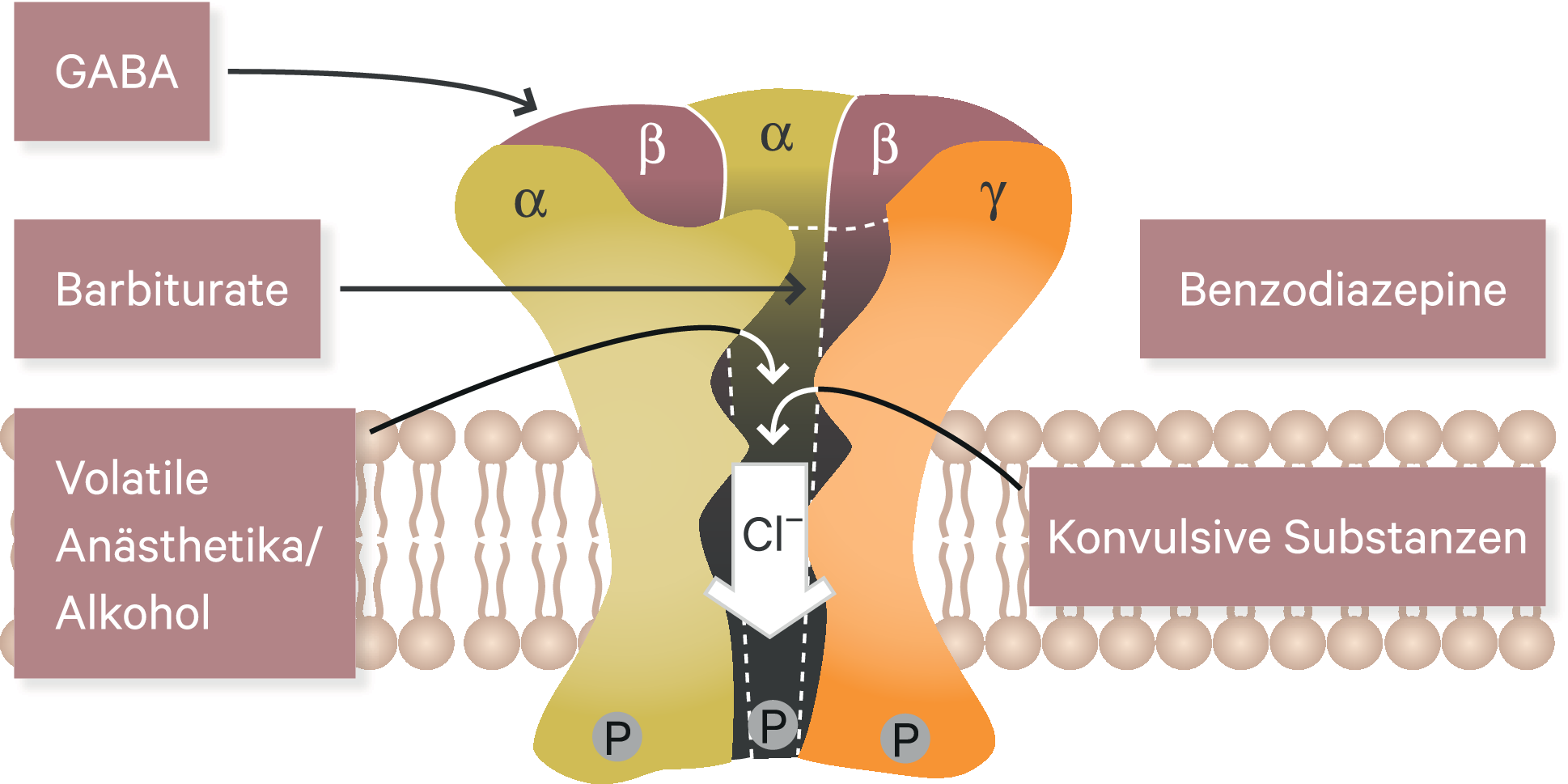
Abb. 7–2. Der durch Gamma-Aminobuttersäure (GABA) gesteuerte GABA-A-Rezeptor besteht aus verschiedenen Untereinheiten (alpha, beta, gamma), die zusammengesetzt einen Chloridionen-Kanal ergeben. Wird die GABA-Bindungsstelle durch GABA aktiviert, kommt es zu einem vermehrten Chloridionen-Einstrom in die Zelle mit einer Hyperpolarisation als Folge, damit wird das Membranpotenzial negativer [16]. Benzodiazepine verstärken nur die GABA-Antwort, während zum Beispiel Barbiturate über eine andere Bindungsstelle direkt den Chloridionen-Kanal aktivieren können. Die Untereinheiten können zusätzlich in verschiedenen Variationen vorkommen. GABA-A-Rezeptoren mit bestimmten Untereinheiten (besonders vom Typ alpha1) scheinen für hypnotische Effekte besonders wichtig zu sein. Benzodiazepine binden eher nicht unterschiedlich an diese Variationen, während die Z-Substanzen etwas besser an für die hypnotische Wirkung relevante Untereinheiten (besonders Typ alpha1) binden, sodass sie im therapeutischen Bereich eine gewisse selektive hypnotische Wirkung aufweisen mit geringeren unerwünschten Wirkungen wie eine Muskelrelaxation.
Benzodiazepine und Non-Benzodiazepine (Z-Substanzen)
Der Wirkungsmechanismus der Benzodiazepine ist eng mit der Funktion des postsynaptischen GABA-A-Rezeptors (Abb. 7–2) assoziiert. Gamma-Aminobuttersäure (GABA) ist der wichtigste inhibitorische Neurotransmitter des zentralen Nervensystems (ZNS). GABAerge Neuronen sind im ZNS weit verbreitet, sie sind sehr komplex mit anderen Neuronen verschaltet und reduzieren in der Regel deren Erregbarkeit. Diese GABAerge Hemmung – ein ubiquitärer Prozess im gesamten ZNS – verhindert überschießende Erregungen bestimmter Neuronen oder Neuronenverbände und ist damit für die Ausbalancierung aller zentralen Funktionen unerlässlich [16]. Die GABAerge Hemmung spielt auch eine wichtige Rolle in der Schlafregulation. Hierbei sind aber noch viele andere Neurotransmitter an der Verarbeitung verschiedener Signale (beispielsweise visueller oder akustischer Signale, innere Uhr) beteiligt, die letztlich den Wach- oder Schlafzustand auslösen (Abb. 7–3) [15].
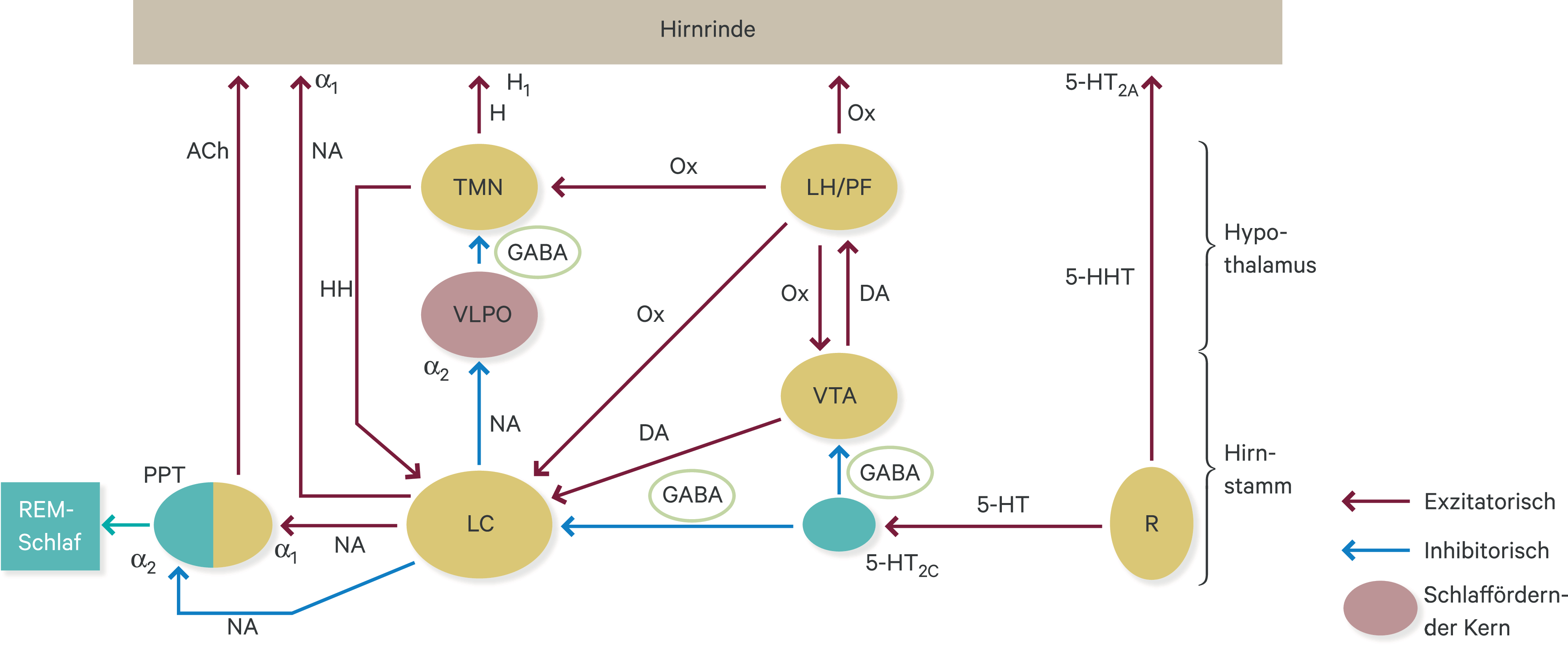
Abb. 7–3. Schlafregulation durch Neurotransmitter (mod. nach [15]) Die Regulation des Schlaf-Wach-Zustands wird durch ein komplexes neuronales Netzwerk vermittelt, in dem viele Neurotransmitter involviert sind. Dies erklärt, dass pharmakologisch sehr unterschiedliche Substanzen schlaffördernde bzw. hypnotische Effekte haben können. Orexin-haltige Neuronen spielen hier eine wichtige Rolle, da ihr Verlust mit den typischen Störungen des Wachzustands (Schlafattacken) bei Narkolepsie-Patienten in Verbindung gebracht wird [1]. TMN: tuberomammillärer Kern; LH/PF: lateraler hypothalamischer/perifornikaler Bereich; LC: Locus coeruleus; VTA: ventrale tegmentale Region; PPT: pedunkulopontiner tegmentaler Kern; : Raphe-Kern; VLPO: ventrolateraler präoptischer Kern; Ach: Acetylcholin; NA: Noradrenalin; H: Histamin; Ox: Orexin; GABA: Gamma-Aminobuttersäure; DA: Dopamin; 5-HT: 5-Hydroxytryptamin; α1: exzitatorischer α1-Adrenozeptor; α2: inhibitorischer α2-Adrenozeptor; H1: exzitatorischer H1-Histaminrezeptor; 5-HT2A und 5-HT2C: exzitatorische 5-HT-Rezeptoren
Benzodiazepine greifen nicht direkt am GABA-A-Rezeptor an, sondern sie binden an eine spezifische Bindungsstelle, den Benzodiazepin-Rezeptor, die allosterisch an den GABA-A-Rezeptor gekoppelt ist (Abb. 7–2). Als Folge kommt es nur zu einer indirekten Verstärkung der GABAergen Hemmung, während Barbiturate die GABAerge Hemmung direkt verstärken. Benzodiazepine werden deshalb auch vereinfacht als „Bremskraftverstärker“ im ZNS bezeichnet.
Alle pharmakologischen Eigenschaften der Benzodiazepine und die davon ableitbaren therapeutischen Effekte und unerwünschten Wirkungen können über eine Verstärkung GABAerger Hemmprozesse durch Aktivierung des Benzodiazepin-Rezeptors erklärt werden. Benzodiazepine wirken
- antikonvulsiv (zentral ausgelöste Krampfzustände, Epilepsie)
- zentral muskelrelaxierend (Spastik, Muskelverspannungen, Tetanus)
- sedativ/hypnotisch (Schlafstörungen, Prämedikation in der Anästhesie)
- amnestisch (verschiedene Anwendungen in der Anästhesie)
- anxiolytisch, erregungs- und aggressionsdämpfend (Spannungs-, Erregungs-, und Angstzustände unterschiedlicher Genese, Stressabschirmung)
Aufgrund der Bindung an die spezifische Bindungsstelle können alle Benzodiazepin-Wirkungen im Bedarfsfall sehr schnell und spezifisch durch den Rezeptorantagonisten Flumazenil (Anexate®) aufgehoben werden.
Trotz dieses sehr spezifischen Angriffspunkts ist die Wirkung der Benzodiazepine auf das ZNS wegen der breiten Bedeutung der GABAergen Hemmung eher unspezifisch. Im therapeutischen Bereich weisen Benzodiazepine dennoch eine deutliche Selektivität auf, weil in Abhängigkeit von Dosis und der damit erreichten Besetzung der Benzodiazepin-Bindungsstelle sowie der begrenzten maximalen Verstärkung der GABA-Wirkung durch den indirekten Wirkungsmechanismus nur bestimmte ZNS-Funktionen ausreichend ansprechen.
Die heute im Handel erhältlichen Benzodiazepine unterscheiden sich in ihren agonistischen Eigenschaften am Benzodiazepin-Rezeptor nicht wesentlich. Sehr deutliche Unterschiede sieht man aber in ihrer Affinität zum Benzodiazepin-Rezeptor und der damit verbundenen hypnotischen Einzeldosis (Tab. 7–2).
Tab. 7–2. Pharmakodynamische und pharmakokinetische Eigenschaften von synthetischen Hypnotika
|
Substanz (INN) |
Handelsname (Beispiele) |
Mittlere Tagesdosis [mg] |
t1/2 [h] |
tmax [h] |
IC50 [nmol/l] |
Hinweise |
|
Benzodiazepine |
||||||
|
Brotizolam |
Lendormin |
0,125–0,25 |
3–8 |
0,8–1,0 |
2 |
|
|
Flunitrazepam |
Rohypnol |
0,5–2,0 |
16–35 |
0,75–2,0 |
4 |
Betäubungsmittel |
|
Flurazepam |
Dalmadorm |
15–30 |
50–100 |
1–3 |
8,1 |
Aktive Metaboliten Desalkylflurazepam, Hydroxyethylflurazepam |
|
Lormetazepam |
Noctamid |
0,5–2,0 |
8–14 |
2,0 |
4 |
|
|
Nitrazepam |
Mogadan |
2,5–10,0 |
25–30 |
0,5–2,0 |
10 |
|
|
Temazepam |
Remestan |
10–40 |
5–13 |
1,0 |
20 |
|
|
Triazolam |
Halcion |
0,125–0,25 |
2–5 |
0,7–2,4 |
2 |
|
|
Z-Substanzen |
||||||
|
Zolpidem |
Stilnox |
5,0–10,0 |
1,5–2,5 |
2,0 |
50 |
|
|
Zopiclon |
Ximovan |
3,75–7,5 |
2–6 |
1,5–2,0 |
30 |
|
|
Antidepressiva |
||||||
|
Mirtazapin |
Remergil |
15–45 |
20–40 |
2 |
||
|
Trimipramin |
Stangyl |
25–100 |
24 |
3 |
||
|
Trazodon |
Trazodon-neuraxpharm |
25–150 |
5–8 |
1,1 |
||
|
Doxepin |
Aponal |
25–100 |
8–25 |
2,9 |
||
|
Neuroleptika |
||||||
|
Melperon |
Melperon-neuraxpharm |
25–100 |
4–8 |
1–1,5 |
||
|
Pipamperon |
Pipamperon-neuraxpharm |
40–60 |
4–17 |
2 |
||
|
Promethazin |
Atosil |
25–200 |
8–15 |
1,5–3 |
||
|
Quetiapin |
Seroquel |
12,5–100 |
6–12 |
6 |
Off Label |
|
|
H1-Antihistaminika |
||||||
|
Doxylamin |
Hoggar night |
25–50 |
10–11 |
2,4 |
||
|
Diphenhydramin |
Betadorm |
50 |
2,4–9,3 |
1 |
||
|
Sonstige |
||||||
|
Chloralhydrat |
Chloraldurat |
250–500 |
0,5–1 |
4 min, Metabolit 7–10 h |
Aktiver Metabolit Trichlorethanol |
|
|
Clomethiazol |
Distraneurin |
384–768 |
2–5 |
1,5 |
||
|
Melatonin |
Circadin |
2 |
3,5–4 |
3 |
Zulassung Alter > 55 Jahre |
|
t1/2: Terminale Eliminationshalbwertszeit; tmax: Zeit bis zum Erreichen maximaler Blutspiegel nach Einnahme der festen oralen Arzneiform; IC50: halbmaximale Hemmkonstante für die Bindung an den Benzodiazepin-Rezeptor in vitro; je niedriger die Konzentration, desto höher die Affinität zum Rezeptor.
Die enge Assoziation des Wirkungsmechanismus aller Benzodiazepine mit dem gesamten pharmakologischen Wirkungsspektrum hat den Nachteil, dass man bei den heutigen zur Verfügung stehenden Substanzen immer auch mit sedierenden Effekten rechnen muss, wenn durch eine zu lange Verweildauer im Organismus mit relevanten Plasmaspiegeln am nächsten Tag zu rechnen ist. Diese können sich in Tagesmüdigkeit und in einer Verminderung der kognitiven Leistungsfähigkeit wie Konzentrationsstörungen und Merkfähigkeitsdefizite äußern, was bei ihrer Anwendung als Schlafmittel besonders störend empfunden wird.
Gewisse qualitative Unterschiede bestehen zwischen den klassischen Benzodiazepinen und den Z-Substanzen Zolpidem und Zopiclon. Diese Unterschiede gehen auf die Struktur des GABA-A-Rezeptorkomplexes zurück. Der Liganden-gesteuerte Chlorid-Kanal besteht aus verschiedenen Untereinheiten (alpha, beta, gamma), von denen wiederum jede in verschiedenen Varianten vorkommen kann. Während die Bindungsstärke der Benzodiazepine an alle Varianten eher gleich ist, binden die Z-Substanzen stärker an Alpha1-Untereinheiten als an die anderen Komponenten, was man mit einer selektiveren hypnotischen Wirkung in Verbindung bringt. In experimentellen Untersuchungen zeigten sich sedierende Eigenschaften bei niedrigeren Dosierungen als für eine antikonvulsive, muskelrelaxierende oder anxiolytische Wirkung notwendig ist. Tatsächlich sind unerwünschte Arzneimittelwirkungen bei den Z-Substanzen wie Muskelrelaxation, Aufmerksamkeitsstörungen und Abhängigkeitsentwicklung etwas geringer ausgeprägt als bei den Benzodiazepinen, allerdings wird dieser Vorteil bei höheren Dosen wesentlich geringer. Damit sind die Z-Substanzen nicht problemfreie Hypnotika, haben jedoch gegenüber den Benzodiazepinen einen Verträglichkeitsvorteil bei gleich guter hypnotischer Wirksamkeit [2]. Zopiclon und Zolpidem beeinflussen den REM-Schlaf nicht signifikant; sie verlängern aber die orthodoxen Schlafstadien.
Deutliche Unterschiede gibt es bei den pharmakokinetischen Eigenschaften der einzelnen Benzodiazepin-Derivate und der Z-Substanzen. Dies hat auch praktische Auswirkungen auf die bei Hypnotika übliche Anwendung als Einmalgabe (Abb. 7–4). Bei der Einnahme am Abend sollen maximale Wirkspiegel des Benzodiazepins (tmax) möglichst rasch erreicht werden, um bald eine schlaffördernde Wirkung zu erhalten. Ausreichende Wirkspiegel sollten über einige Stunden bestehen bleiben, allerdings am Morgen abgeklungen sein, um möglichst keine unerwünschten Wirkungen über den Tag zu haben. Auch bei mehrtägiger abendlicher Einnahme sollte es nicht zur Kumulation der Plasmaspiegel kommen, weil sich hierdurch das Risiko für unerwünschte Arzneimittelwirkungen am Tag erhöht.
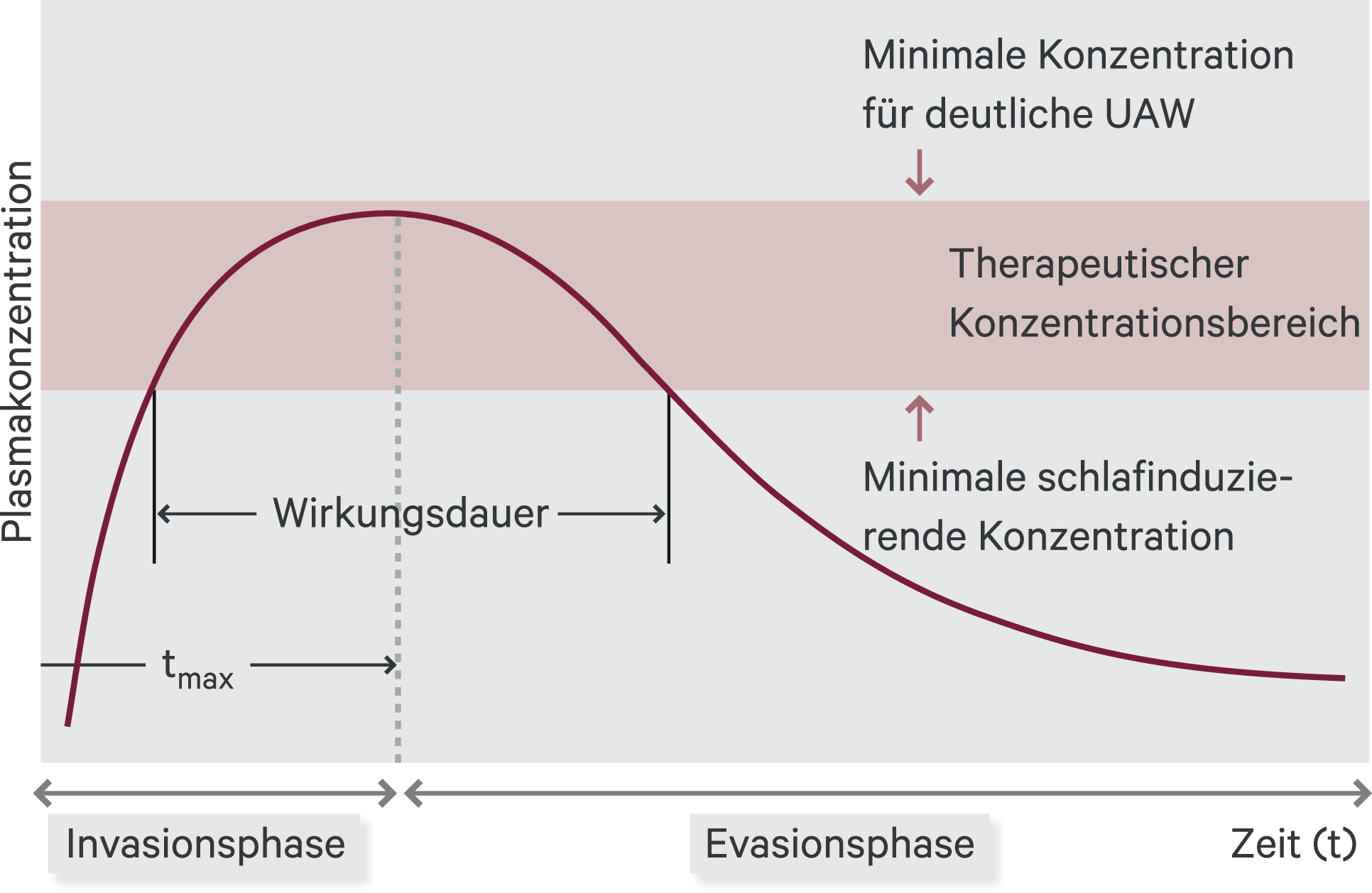
Abb. 7–4. Optimaler Plasmaspiegelverlauf eines Hypnotikums [7]. Ein gutes Schlafmittel sollte nach oraler Einnahme sehr schnell zu relevanten Plasmaspiegeln führen. Darauf basiert die Empfehlung, das Schlafmittel vor dem Zu-Bett-Gehen einzunehmen. Bis in die Morgenstunden sollten sich die Plasmaspiegel im therapeutischen Bereich bewegen. Beim Aufstehen sollte allerdings das Schlafmittel weitgehend eliminiert sein, um relevante Effekte wie Tagesmüdigkeit zu vermeiden.
Ist die Dosis des Hypnotikums zu hoch, erhöht sich das Risiko von unerwünschten Wirkungen ebenfalls. Dazu gehören vor allem verstärkte muskelrelaxierende Effekte mit erhöhtem Sturzrisiko. Hiermit ist auch bei Z-Substanzen zu rechnen, insbesondere wenn bei älteren Patienten die Dosis nicht angepasst wird.
Andere Schlafmittel
Neben den dominierenden Benzodiazepinen und Z-Substanzen gibt es noch verschiedene synthetische und pflanzliche Schlafmittel sowie weitere Medikamente, die unter bestimmten Bedingungen als Schlafmittel eingesetzt werden (Tab. 7–1 und Tab. 7–2). Nachfolgend sollen die wichtigeren Gruppen kurz vorgestellt werden [9].
H1-Antihistaminika
Histaminerge Neuronen spielen in der Tag-Wach-Regulation eine wichtige Rolle (Abb. 7–3). H1-Antihistaminika der ersten Generation können in ausreichendem Maß die Blut-Hirn-Schranke überwinden und die histaminerge Neurotransmission im ZNS hemmen. Diphenhydramin und Doxylamin stehen seit vielen Jahren als freiverkäufliche Schlafmittel zur Verfügung. Sie verändern sowohl den REM-Schlaf als auch den orthodoxen Schlaf.
Nachteilig ist die schnelle Toleranzentwicklung gegenüber der hypnotischen Wirkung mit einer Dosissteigerung als Folge und die Toxizität, besonders durch die sehr ausgeprägten anticholinergen Eigenschaften.
Antidepressiva und Antipsychotika
Als akut wirkende Hypnotika können besonders bei Patienten, die keine Benzodiazepine einnehmen sollten, bestimmte sedierende Antidepressiva (Trizyklika, Mirtazapin) und einige sedierende Antipsychotika wie Melperon, Pipamperon und Promethazin eingesetzt werden [7]. Die schlaffördernde Wirkung geht bei diesen Substanzen nicht auf den antidepressiven bzw. antipsychotischen Wirkungsmechanismus zurück, sondern auf die deutlichen H1-antagonistischen Eigenschaften, gegebenenfalls kombiniert mit 5-HT2-antagonistischen Wirkungen bei einigen dieser Substanzen. Mirtazapin gehört zu den wenigen Substanzen, die den REM-Schlaf nicht unterdrücken. Amitriptylin, Trimipramin und Trazodon vermindern die REM-Phasen [6]. Antipsychotika sollen die Schlafphasen nur wenig beeinflussen und den REM-Schlaf nicht unterdrücken, allerdings gibt es dazu nur sehr wenige Daten.
Clomethiazol
Clomethiazol ist zur Behandlung schwerer Schlafstörungen im höheren Lebensalter zugelassen, wenn andere Maßnahmen nicht wirken oder nicht anwendbar sind. Clomethiazol verstärkt die elektrophysiologische Reaktion auf die inhibitorischen Neurotransmitter GABA und Glycin, beeinflusst aber nicht die inhibitorischen Reaktionen auf Acetylcholin und Adenosin. Daten zur Wirkung auf das Schlafprofil sind nicht verfügbar.
Melatonin
Das Neurohormon Melatonin spielt in der Tag-Nacht-Regulation eine wichtige Rolle. Aufgrund des Wirkungsmechanismus ist keine akute hypnotische Wirkung vorhanden, sondern es wirkt nach längerer Einnahme (etwa drei Wochen) regulierend auf den Schlaf-Wach-Rhythmus. Melatonin soll die Einschlafzeit verkürzen und keine Veränderungen von Schlafarchitektur und REM-Schlaf induzieren. Die Daten zum Einsatz von Melatonin bei Insomnien sind allerdings eher enttäuschend.
Agomelatin (Valdoxan®), ein Antidepressivum mit 5-HT2C-antagonistischen und Melatonin-agonistischen Eigenschaften scheint sich dagegen bei Insomnien nicht nur im Rahmen depressiver Störungen zu bewähren.
L-Tryptophan
Die Aminosäure L-Tryptophan ist eine Vorstufe (Präkursor) des Neurotransmitters Serotonin. Der Einsatz des Nahrungsergänzungsmittels L-Tryptophan als Hypnotikum geht von der Vermutung aus, dass durch eine Steigerung der Serotonin-Konzentration im Gehirn Schlafmechanismen verbessert werden können. Die hypnotischen klinischen Effekte sind allerdings gering, ausreichende Daten zur Wirkung fehlen.
Orexin-Rezeptorantagonisten
Orexin-haltige Neuronen regulieren Essverhalten, Kognition sowie Stimmung und spielen darüber hinaus in der Schlaf-Wach-Regulation eine wichtige Rolle (Abb. 7–3). Defizite im Orexin-System scheinen mit den Schlafattacken von Narkolepsie-Patienten zusammenzuhängen. Aufgrund der spezifischen Rolle dieser nur wenige Neuronen umfassenden Strukturen war die Entwicklung von Orexin-Rezeptorantagonisten als Schlafmittel mit direktem und selektivem Angriffspunkt in Strukturen der Schlaf-Wach-Regulation mit großen Hoffnungen verbunden [1]. Mit Suvorexant wurde 2014 in den USA der erste Orexin-Rezeptorantagonist als Schlafmittel zugelassen. Tagesmüdigkeit scheint jedoch ein großes Problem bei der Einnahme dieser Substanz zu sein. Darüber hinaus kann es zu Narkolepsie-ähnlichen Symptomen und etwas häufigeren Suizid-Gedanken kommen. Dies hat zur Zulassung einer nur niedrigen Dosierung mit nicht überzeugender hypnotischer Wirkung geführt. Insgesamt hat dieser innovative Ansatz in der Praxis enttäuscht.
Pflanzliche Schlafmittel
Von der großen Anzahl von pflanzlichen Schlafmitteln auf der Basis von Extrakten aus zum Beispiel Baldrian, Hopfen und Melisse gibt es nur für wenige hochdosierte Baldrianextrakt-Präparate Hinweise auf eine schlafverbessernde Wirkung, die über die beträchtliche Placebo-Wirkung bei dieser Indikation hinausgeht. Die Datenlage ist allerdings kontrovers. Beim offizinellen Baldrian aus der europäischen Baldrianwurzel sind die wirksamkeitsbestimmenden Inhaltsstoffe bisher noch nicht exakt bekannt. Baldrianextrakt soll GABAerg wirken und Adenosin-Rezeptoren im Gehirn aktivieren. Adenosin soll ein wichtiger endogener Schlaffaktor sein, der sich tagsüber im Gehirn anreichert und nachts abgebaut wird.
Die schlafbahnende Wirkung von Baldrian ist eher nicht akut, sondern benötigt in der Regel eine Einnahme über mehrere Tage. Über diese verzögert eintretende Wirkung sollten die Patienten informiert werden, da sie bei der Einnahme eines Schlafmittels üblicherweise erste Effekte bereits in der ersten Nacht nach Einnahme erwarten.
Phytotherapeutika scheinen die Schlafphasen nicht zu beeinflussen und damit weder Schlaflatenz, Schlafdauer noch Schlafeffizienz signifikant zu verbessern. Es ist ihnen keine hypnotische, sondern allenfalls eine „schlafinduzierende“ Wirkung zuzuschreiben.
Indikationen für Hypnotika
Schlafstörungen gehören zu den häufigsten Symptomen, über die Patienten klagen. Nach Feldstudien leiden etwa 15 % der Bevölkerung unter Schlafstörungen, nach Erhebungen in Arztpraxen sind es 20 bis 40 %. Frauen und ältere Menschen überwiegen deutlich. 2 bis 4 % der deutschen Bevölkerung nehmen regelmäßig Schlafmittel ein. Bei den über 65-Jährigen sind es sogar über 10 %.
Besonders bei neurologisch-psychiatrischen Erkrankungen treten Störungen des physiologischen Schlafs auf. So klagen bei stationärer Aufnahme in psychiatrische Kliniken rund 70 % der Patienten über Schlafstörungen, und auch in nervenärztlichen Praxen scheint die Inzidenz etwa doppelt so hoch zu sein wie in einer Durchschnittsklientel.
Schlafstörungen können nach der Internationalen Klassifikation der Krankheiten (ICD), der Internationalen Klassifikation der Schlafstörungen (ICSD) oder nach der 5. Auflage des Diagnostic and Statistical Manual of Mental Disorders (DSM-5) klassifiziert werden:
- Hypo-/Insomnien (Ein- und Durchschlafstörungen; die mit Abstand häufigsten Schlafstörungen)
- Hypersomnien (Störungen mit exzessiver Schläfrigkeit)
- Störungen des Schlaf-Wach-Rhythmus (z. B. bedingt durch Schichtwechsel oder Flugreisen)
- Parasomnien (Dysfunktionen in Verbindung mit dem Schlaf; z. B. Enuresis nocturna oder Schlafwandeln)
Hauptform ist die nicht-organische, psychophysiologische Insomnie (ICD-10 F51.0). Zahlreiche psychiatrische Erkrankungen gehen mit Schlafstörungen einher (Depressionen, Angststörungen, Demenzen, Psychosen, Abhängigkeitsstörungen), hier kann eine Indikation zur kurzfristigen Komedikation mit Hypnotika bestehen. Auch verschiedene körperliche Erkrankungen sind von einer Insomnie begleitet.
Die häufigste Form, die nicht-organische Insomnie, wird als ein Zustand definiert, der durch folgende Kriterien gekennzeichnet ist:
- Klagen über Ein-/Durchschlafstörungen
- Schlafstörungen mindestens dreimal pro Woche während mindestens eines Monats
- Deutlicher Leidensdruck oder Störung der beruflich-sozialen Funktionsfähigkeit
Die Ursachen von Schlafstörungen sind äußerst vielfältig; sie reichen von situativen Faktoren über psychiatrische und neurologische bis zu internistischen Erkrankungen. Auch Drogen und bestimmte Medikamente können Schlafstörungen verursachen. Den prozentual größten Anteil an diesen Ursachen haben diejenigen, die auf situative und Stressfaktoren zurückzuführen sind. Zusammenfassend gilt, dass bei Jüngeren eher psychosoziale Stressoren, bei Älteren eher körperliche Erkrankungen die Ursache von Schlafstörungen sind.
Die vor der Einführung stehende ICD-11 orientiert sich an DSM-5, welches im Kapitel Schlaf-Wach-Störungen zehn Störungen bzw. Störungsgruppen, nämlich vor allem Insomnie, Hypersomnie, Narkolepsie, atmungsbezogene Schlafstörungen, zirkadiane Schlaf-Wach-Rhythmus-Störungen, REM-Schlaf-Verhaltensstörung, Restless-Legs-Syndrom und Substanz-/Arzneimittel-induzierte Schlafstörung unterscheidet.
Als wesentliches Merkmal einer Insomnie wird hier die Unzufriedenheit mit der Schlafmenge oder Schlafqualität mit Beschwerden einer Ein- oder Durchschlafstörung charakterisiert. Die Schlafstörung kann im Verlauf verschiedener psychischer Störungen oder medizinischer Krankheitsfaktoren oder als unabhängige Störung auftreten.
Behandlungsablauf
Liegt eine schlafstörungsrelevante körperliche Grunderkrankung vor, muss primär diese behandelt werden. Vor der Verordnung von Hypnotika sind zunächst organisch-symptomatische Ursachen und psychiatrische Grunderkrankungen auszuschließen (sekundäre Insomnie). Obligat ist eine Aufklärung und Beratung über die physiologische Schlafdauer, insbesondere bei älteren Menschen (Schlafhygiene). Zu den Schlafhilfen gehört die Beseitigung schlafstörender Faktoren (so weit möglich). Beachtet werden sollten unter anderem eine adäquate Temperatur des Schlafzimmers sowie das Vorhandensein eines orthopädisch-physiologischen Anforderungen entsprechenden Bettes. Zur Schlafhygiene gehört die Empfehlung, „den Tag ausklingen zu lassen“, also die physiologische Umschaltung von Spannung auf Entspannung zu ermöglichen. Besonders bei alten Menschen sollte für ausreichende körperliche Aktivität und eine Begrenzung des Schlafs am Tage gesorgt werden, um eine „natürliche Erschöpfung“ am Abend zu erreichen.
Häufig werden Schlafstörungen durch Lebensstil und Lebensumstände ausgelöst oder begünstigt. Analyse und Änderung dieser Störfaktoren ist hier die oft schwierige erste therapeutische Maßnahme.
Bewährt haben sich auch Entspannungsverfahren wie progressive Muskelrelaxation (PMR) oder autogenes Training sowie verhaltenstherapeutische Maßnahmen (z. B. Gedankenstopp-Training, Stimuluskontrolle).
Der „Glaube an ein Medikament“ (Placebo-Effekt) spielt gerade bei Schlafmitteln eine besondere Rolle; die Akuteffekte von Benzodiazepinen, Z-Substanzen und von sedierenden Antidepressiva oder Neuroleptika (bei Depressionen oder Psychosen) sind aber in Studien belegt.
Für die erfolgreiche Behandlung einer Schlafstörung ist neben der Klärung der Ätiologie eine möglichst genaue Beschreibung der jeweiligen Störung erforderlich. Hierzu gehören eine Schilderung der Symptomatik (Form und Dauer der Schlafstörung), des Befindens am Tag, des Schlafverhaltens (Gewohnheiten, Umgebungseinflüsse) sowie der Vorbehandlung und der Untersuchungsbefund. Der daraus resultierende ursachenorientierte Gesamtbehandlungsplan muss nicht grundsätzlich durch eine Schlaf-Polygraphie abgesichert sein. Gerade bei unklaren und vor allem bei chronischen Störungen kann das Schlaflabor jedoch eine zusätzliche Hilfe bei Diagnosestellung und Therapie sein.
Wegen unterschiedlicher therapeutischer Konsequenzen seien das Schlafapnoe-Syndrom, der periodische nächtliche Myoklonus sowie das Restless-Legs-Syndrom hier nur erwähnt. Schlafinduzierte Apnoen (obstruktiv, zentral) imponieren vor allem durch Schnarchen mit längeren Atempausen sowie Tagesschläfrigkeit und machen etwa 3 % der Schlafstörungen aus.
Auswahl der Hypnotika
Beim Vorliegen von leichten Schlafstörungen kann ein Behandlungsversuch mit Phytotherapeutika unternommen werden. Zur Wirksamkeit dieser Präparate liegen nur wenige kontrollierte Studien vor, am besten ist bislang die Wirksamkeit für Extrakte aus europäischer Baldrianwurzel belegt. Allerdings ist zu beachten, dass Insomnien hohe Placebo-Ansprechraten aufweisen. Vorteile der pflanzlichen Präparate sind die sehr gute Verträglichkeit sowie das Fehlen eines Abhängigkeitspotenzials. Extrakte aus Hopfen, Melisse und Lavendel können nach den derzeit vorliegenden Daten allenfalls in der Kombination mit Extrakten aus Baldrianwurzel empfohlen werden. Zur Behandlung von Durchschlafstörungen besitzt keines der genannten Phytotherapeutika eine ausreichende Wirkung. Gewarnt werden muss vor Mischpräparaten, die pflanzliche Wirkstoffe zusammen mit anderen Komponenten (beispielsweise Alkohol!) enthalten.
Aufgrund ihrer gesicherten Wirksamkeit sind Benzodiazepin-Hypnotika häufig verordnete Präparate. Üblicherweise werden beispielsweise Temazepam (20 mg) oder Lormetazepam (1 mg) verordnet. Benzodiazepine unterscheiden sich in ihrer Wirkungsstärke – sehr stark wirksam sind beispielsweise Flunitrazepam und Triazolam – und in ihren pharmakokinetischen Eigenschaften. Die Verweildauer im Organismus weist zwischen einzelnen Präparaten teilweise erhebliche Unterschiede auf (siehe Tab. 7–2). Dies ist für die Dauer der Wirkung (Ein- oder Durchschlafstörung, Überhang am nächsten Morgen, Tagesresteffekt) sowie für das Risiko einer Kumulation des Arzneimittels von Bedeutung. So sind Benzodiazepine mit kurzer Halbwertszeit insbesondere bei Einschlafstörungen einsetzbar. Dem Vorteil, dass am nächsten Tag kein Überhang („Hangover“) zu beobachten ist, steht der Nachteil der eventuell verstärkten Entzugsinsomnie gegenüber. Substanzen mit langer Halbwertszeit – hierbei sind eventuell aktive Metaboliten zu berücksichtigen – sollten wegen der Kumulationsgefahr und des Hangover zurückhaltend eingesetzt werden. Sie sind allerdings indiziert, wenn gravierende Durchschlafstörungen und/oder morgendliches Früherwachen bestehen oder eine Sedierung auch tagsüber gewünscht wird.
Als Grundregeln bei der Einnahme von Benzodiazepinen sollten beachtet werden:
- Gezielte Indikation
- Zeitlich begrenzte Einnahme
- Langsames Absetzen
- Einleitung anderer Behandlungsmaßnahmen (z. B. Entspannungsverfahren, Verhaltensregeln) falls erforderlich
- Bei älteren Patienten genügt in der Regel die Hälfte der Dosis
Als Alternative zu den Benzodiazepinen haben sich die sogenannten Z-Substanzen Zopiclon und Zolpidem etabliert. Sie besitzen einen schnellen Wirkungseintritt und haben eine kurze Halbwertszeit. In verschiedenen Studien konnten Zolpidem und Zopiclon eine den Benzodiazepinen vergleichbare Wirkung bei Schlafstörungen erzielen, wobei sich bei den Nebenwirkungen Hinweise auf gewisse Vorteile (keine Muskelrelaxation, geringere Rebound- und Überhangeffekte) gegenüber den Benzodiazepinen zeigten. Die Abhängigkeitsgefahr scheint etwas geringer zu sein. Wie alle Hypnotika sollten auch diese Substanzen nur kurzzeitig (vier Wochen) kontinuierlich eingenommen werden.
Schlafstörungen vor allem im Rahmen depressiver Erkrankungen können gut mit dämpfenden Antidepressiva (z. B. Mirtazapin, Trimipramin) bei abendlichem Dosisschwerpunkt oder abendlicher Einmalgabe behandelt werden.
Insbesondere die niederpotenten Neuroleptika wie Melperon, Pipamperon oder Promethazin wirken ausgeprägt sedierend. Wegen der im Vergleich zu Benzodiazepinen gravierenden Nebenwirkungen, vor allem anticholinerger und extrapyramidal-motorischer Art, erfordert die Therapie von Schlafstörungen mit Neuroleptika eine sorgfältige Indikationsstellung.
Das Antipsychotikum der zweiten Generation Quetiapin wird neuerdings (off Label) niedrig dosiert (25 bis 100 mg zur Nacht) auch zur Schlafförderung eingesetzt. Infrage kommen vor allem Patienten, bei denen Suchtgefahr besteht – wegen der Suchtfreiheit der Neuroleptika –, daneben auch Patienten mit psychomotorischen Erregungszuständen und Schlafstörungen im Rahmen von Psychosen und bei akuter Suizidalität.
Bei älteren Patienten (> 55 Jahre) kann ein Therapieversuch mit Melatonin (2 mg zur Nacht) über drei Wochen erfolgen. Die Wirkung soll nach zwei bis vier Tagen einsetzen, der zirkadiane Rhythmus über drei Wochen stabilisiert werden.
Chloralhydrat liegt als Einschlaf- und Durchschlafmittel (verzögerte Wirkstofffreisetzung) vor. Es beeinträchtigt das Schlafprofil kaum, weist aber rasche Toleranzentwicklung (Wirkungsverlust) auf. Bei Patienten mit schweren Nieren-, Leber- oder Herzfunktionsstörungen ist Vorsicht geboten; als Nebenwirkung kann eine Reizung der Magenschleimhaut auftreten.
Hauptindikation von Clomethiazol sind Alkoholentzugssymptome. Wegen der großen Gefahr von Missbrauch und Abhängigkeit sollte diese Substanz nicht als Hypnotikum verwendet werden. Die einzige Ausnahme stellen Schlafstörungen bei Alterspatienten dar, wenn andere Hypnotika paradoxe Reaktionen hervorrufen.
Antihistaminika gehören zu den am meisten verwendeten nichtpflanzlichen Hypnotika, da sie ohne Rezept erhältlich sind. Zu beachten sind jedoch anticholinerge Nebenwirkungen, Beeinträchtigungen des Reaktionsvermögens und Toleranzbildung mit daraus resultierender Dosissteigerung. Trotz der relativ großen therapeutischen Breite kommen Vergiftungen (Suizidversuche!) vor. So können zum Beispiel 7 g Diphenhydramin, bei Kindern schon 500 mg Diphenhydramin, letal sein.
Die Vor- und Nachteile der einzelnen Hypnotika sind in Tabelle 7–1 zusammengefasst.
Differenzialindikationen
Bei Alterspatienten kann aufgrund des Melatonin-Mangels ein Therapieversuch mit Melatonin (2 mg zur Nacht) gemacht werden. Für Benzodiazepine gilt es, die erhöhte Kumulationsgefahr und das Sturzrisiko zu beachten (Dosisanpassung!) Bei dementen Patienten sind (zusätzlich) paradoxe Reaktionen möglich [13, 14].
Während einer Schwangerschaft sollten Benzodiazepine im ersten Trimenon vermieden, vor der Entbindung ausgeschlichen werden. Chloralhydrat, Diphenhydramin und Doxylamin sind in Schwangerschaft und Stillzeit kontraindiziert. Zolpidem und Zopiclon sind in der Stillzeit kontraindiziert.
Therapiedauer
In der Regel sollten Hypnotika nicht länger als drei bis vier Wochen kontinuierlich verordnet werden. Primär sollte eine diskontinuierliche Therapie im Sinne einer Bedarfsmedikation erfolgen. Wirksamkeitsbelege für einen Therapiezeitraum länger als vier Wochen liegen bislang nicht vor. Untersuchungsergebnisse aus dem Schlaflabor belegen Wirkungsverluste bereits nach Tagen oder Wochen. Bei chronischer Einnahme zeigt sich häufig ein Schlafmuster, das ziemlich genau der Ausgangssituation entspricht. Toleranzbildung mit Dosissteigerung führt zu zunehmender Beeinträchtigung der kognitiven Leistungsfähigkeit (Konzentration, Gedächtnis).
Absetzsyndrome
Schon nach kurzer Einnahmedauer kann – vor allem bei Substanzen mit kurzer Halbwertszeit – das abrupte Absetzen zu einer ausgeprägten Insomnie führen, die das Ausmaß der ursprünglichen Schlafstörung übersteigt („Rebound-Insomnie“). Dies verleitet häufig zur Wiedereinnahme und kann in einen Circulus vitiosus einmünden. Gleichzeitig kommt es häufig zur Steigerung des REM-Schlafes („REM-Rebound“), was mit vermehrter Traumtätigkeit und verminderter Schlafqualität einhergeht.
Benzodiazepine und Z-Substanzen müssen immer langsam ausschleichend abgesetzt werden.
Missbrauch von Benzodiazepin-Hypnotika kommt relativ häufig ohne Dosissteigerung in Form einer Niedrigdosis-Abhängigkeit vor. Hier ist ebenfalls ein langsames Ausschleichen durch kontinuierliche Dosisreduktion über einen längeren Zeitraum unerlässlich.
Bei Patienten mit bereits vorbehandelten chronifizierten Insomnien ist eine weitere Therapie mit klassischen Hypnotika kontraindiziert. Hier empfiehlt sich ein schrittweises Absetzen der Benzodiazepine und gleichzeitige Verordnung eines sedierenden Antidepressivums wie Mirtazapin, Doxepin, Amitriptylin oder Trimipramin. Wenn die Hypnotika ganz abgesetzt sind (Reduktion um etwa 50 % innerhalb von vier Wochen), wird auch ein Ausschleichen des Antidepressivums versucht.
Nebenwirkungen und Gegenanzeigen
Grundsätzlich gilt für alle Pharmaka mit sedierenden und hypnotischen Eigenschaften, dass sie das Reaktionsvermögen negativ beeinträchtigen können. Langzeiteinnahme von Hypnotika kann zu Antriebsverminderung, emotioneller Abstumpfung mit Gleichgültigkeit im Sinne einer (leichten) chronischen Intoxikation (Kumulation vor allem bei Alterspatienten) führen. Die zu späte abendliche Einnahme eines Hypnotikums mit längerer Halbwertszeit kann eine deutliche Tagesrestwirkung (Hangover) mit entsprechender Vigilanzbeeinträchtigung bewirken.
Benzodiazepine. Alle Nebenwirkungen und Gegenanzeigen, die für Benzodiazepine mit Tranquilizer-Indikation gelten, kommen auch für Benzodiazepin-Hypnotika zum Tragen: Sedierung, Tagesmüdigkeit, Schläfrigkeit, Beeinträchtigung der Aufmerksamkeit und des Reaktionsvermögens, Muskelschwäche, Mattigkeit, Ataxie, Verwirrtheit, Depression, Demaskierung einer Depression und Schwindelgefühl [16].
„Z“-Substanzen. Als Nebenwirkungen können unter Zopiclon gelegentlich Mundtrockenheit, bitterer bis metallischer Mundgeschmack, Benommenheit, Überhang-(Tagesrest-)Effekte, Schwindelgefühl, Amnesien und Kopfschmerzen auftreten. Gegenanzeigen sind Myasthenia gravis, schwere Leber- oder Ateminsuffizienz und schweres Schlafapnoe-Syndrom.
Unter Zolpidem wurden als Nebenwirkungen gelegentlich bzw. häufig Schwindel, Kopfschmerzen, Diarrhö, Übelkeit und Amnesien beobachtet. In letzter Zeit wurde vermehrt über Missbrauch und Abhängigkeit berichtet (Dosissteigerung mit Halluzinationen und Schlafwandeln). Gegenanzeigen sind schwere Leber- oder Ateminsuffizienz, Schlafapnoe-Syndrom und Myasthenia gravis.
Bei relativ später Einnahme wurden auch unter Zolpidem und Zopiclon negative Tagesrestwirkungen in Fahrtauglichkeitstests beschrieben.
Die Anwendung von Benzodiazepin-Rezeptoragonisten kann, wie bei Benzodiazepinen, zur Entwicklung von physischer und psychischer Abhängigkeit sowie Missbrauch führen. Ausprägung und Häufigkeit scheinen aber geringer als unter Benzodiazepinen zu sein. Beim Absetzen, insbesondere bei plötzlichem Therapieabbruch, können Absetzsymptome und Rebound-Phänomene auftreten. Patienten mit Suchtanamnese, insbesondere unter Benzodiazepinen, sollten Z-Substanzen nicht oder nur unter besonderer Kontrolle erhalten. Die Dauer einer Behandlung sollte, einschließlich einer schrittweisen Absetzphase, vier Wochen nicht übersteigen.
Chloralhydrat. Chloralhydrat hat eine sehr geringe therapeutische Breite. Die therapeutische (0,25–1 g) und die toxische Dosis (bereits ab 5 g/Tag) liegen nicht weit auseinander. Nebenwirkungen sind Übelkeit und Erbrechen, bedingt durch die Reizung der Magenschleimhaut. Durch Verwendung dünndarmlöslicher Kapseln kann dieser Effekt verringert werden. Der typische unangenehme Mundgeruch wird durch die Abatmung der Aldehyde über die Lunge verursacht. Für Chloralhydrat konnte keine negative Beeinträchtigung der psychomotorischen Leistungsfähigkeit nachgewiesen werden.
Gegenanzeigen sind schwere Herz-, Leber- und Nierenerkrankungen.
Antihistaminika. Nebenwirkungen sind zum Beispiel Mundtrockenheit, Miktionsstörungen und Herzklopfen, daneben auch Magen-Darm-Beschwerden und Durchfall. Auch photosensibilisierende Eigenschaften werden berichtet. In höherer Dosierung kann es zu Schwindelgefühl, Sehstörungen und Halluzinationen kommen. Besonders bei alten Menschen ist auf die mögliche Provokation von Verwirrtheitszuständen und deliranten Symptomen zu achten. Gegenanzeigen sind akuter Asthma-Anfall, Prostata-Adenom, Engwinkelglaukom, Epilepsie und Phäochromozytom.
Antidepressiva. Trimipramin und andere trizyklische Substanzen haben unterschiedlich ausgeprägte anticholinerge und/oder kardiotoxische (Chinidin-artige) Nebenwirkungen: Mundtrockenheit, verstopfte Nase, Schwitzen, Schwindel, Hypotonie, orthostatische Dysregulation, Tachykardie, Tremor, Akkommodationsstörungen, Obstipation und passagerer Anstieg der Leberenzymaktivitäten können auftreten, gelegentlich auch Miktionsstörungen. Bei Patienten mit kardialer Vorschädigung oder in Kombination mit anderen Arzneimitteln, die gleichfalls zu EKG-Veränderungen (QT-Zeit!) führen können, sollen sie nicht eingesetzt werden. Bei älteren Patienten besteht vor allem bei zu schneller Dosissteigerung ein erhöhtes Risiko für das Auftreten von deliranten Syndromen, Gedächtnisstörungen und Verwirrtheit. Bei älteren Patienten sollten Trizyklika deshalb nicht zum Einsatz kommen, ihre potenziell delirogenen Eigenschaften machen sie für Patienten mit Demenz gänzlich ungeeignet.
Trazodon und Mirtazapin besitzen dagegen kaum anticholinerge Eigenschaften. Unter Mirtazapin ist Verschlechterung oder neues Auftreten eines Restless-Legs-Syndroms beschrieben.
Alle Antidepressiva weisen kein Abhängigkeitsrisiko auf.
Neuroleptika/Antipsychotika. Trizyklische Substanzen wie Promethazin besitzen ausgeprägte anticholinerge und kardiale Nebenwirkungen. Melperon und Pipamperon dagegen weisen kein klinisch relevantes anticholinerges Wirkungsprofil und keine kardialen Nebeneffekte auf. Risiko beim Einsatz sind Blutdrucksenkung und extrapyramidal-motorische Störungen.
Clomethiazol. Sehr häufig treten starke Speichelsekretion und Zunahme der Bronchialsekretion auf. Weitere Nebenwirkungen sind Kopfschmerzen, Herzklopfen, Missempfindungen wie Taubheit oder Kribbelgefühl, Juckreiz, Hautausschläge, Magenschmerzen, Sodbrennen, Übelkeit, Erbrechen, Durchfall, Brennen in Hals und Nase, Schnupfengefühl und Hustenreiz. Clomethiazol darf nicht angewandt werden bei Schlafapnoe-Syndrom, Asthma bronchiale und allen zentral verursachten Atemstörungen. Clomethiazol hat ein starkes Abhängigkeitspotenzial.
Melatonin. Melatonin hat nur ein geringes Nebenwirkungspotenzial.
Phytotherapeutika. Sie sind bei kurzfristiger Einnahme praktisch nebenwirkungsfrei. Beachtet werden muss allerdings der Alkoholgehalt bei vielen flüssigen pflanzlichen Arzneimittelzubereitungen.
Interaktionen
Generell gilt für alle Hypnotika, dass sie bei Kombination mit anderen zentral dämpfenden Substanzen zu verstärkter Sedierung und ZNS-Dämpfung führen können. Besondere Vorsicht ist bei der gleichzeitigen Einnahme von Alkohol geboten.
Benzodiazepine. Viele Benzodiazepine werden über das Cytochrom-P450-System metabolisiert. Daher sind Wechselwirkungen mit CYP-Hemmern und CYP-Induktoren möglich. Weitere Interaktionen sind mit Muskelrelaxanzien möglich.
Z-Substanzen. Bei Kombination mit Muskelrelaxanzien kann es zu einer verstärkten relaxierenden Wirkung kommen. Zolpidem und Zopiclon sind Substrate des Cytochrom-P450–3A4-Isoenzyms. Bei gemeinsamer Gabe mit Inhibitoren (z. B. Erythromycin, Ketoconazol) oder Induktoren (z. B. Carbamazepin, Johanniskrautextrakt) kann der Plasmaspiegel von Zolpidem und Zopiclon steigen oder sinken.
Chloralhydrat. Vorsicht ist bei Patienten angeraten, die Antikoagulanzien vom Cumarin-Typ (Phenprocoumon) einnehmen. Die gleichzeitige Anwendung von Arzneimitteln, die zur QT-Zeit-Verlängerung im EKG führen können, sollte genauso wie die von Medikamenten, die Hypokaliämien auslösen können, vermieden werden.
Chloralhydrat darf nicht mit Disulfiram kombiniert werden, weil diese Substanz den Abbau zum aktiven Metaboliten Trichlorethanol hemmt.
Antihistaminika. Antihistaminika dürfen nicht gleichzeitig mit MAO-Hemmern gegeben werden. Mit anderen Arzneimitteln, die ebenfalls anticholinerg wirken, kann es zu deutlich verstärkten anticholinergen Effekten kommen.
Vorsicht ist angebracht bei der gleichzeitigen Anwendung von Arzneimitteln, die zur QT-Zeit-Verlängerung im EKG führen, und bei Medikamenten, die Hypokaliämien auslösen können. Bei gleichzeitiger Gabe von Inhibitoren des CYP2D6 wie Fluoxetin oder Paroxetin können Wirkungen und Nebenwirkungen des Antihistaminikums verstärkt werden.
Melatonin. Die Metabolisierung von Melatonin wird überwiegend durch CYP1A2 vermittelt. Potente Inhibitoren dieses Enzyms wie Fluvoxamin oder Ciprofloxacin können die Melatonin-Spiegel deutlich erhöhen. Rauchen kann zu einer Senkung der Melatonin-Spiegel führen.
Phytotherapeutika. Es sind keine nennenswerten Interaktionen zu erwarten.
Kontrolluntersuchungen
Benzodiazepine und Z-Substanzen. Bei Behandlung mit Hypnotika vom Benzodiazepin-Typ und mit Z-Substanzen sind keine routinemäßigen Laborkontrollen erforderlich. Bei schwerer Leber- und Niereninsuffizienz sollten die Präparate nicht angewendet werden.
Chloralhydrat. Unter Chloralhydrat ist ein EKG vor Beginn der Behandlung empfehlenswert. Eine EKG-Kontrolle sollte nur bei längerfristiger Behandlung oder Kombinationstherapie mit anderen Arzneimitteln, die zur Verlängerung der QT-Zeit führen können, nach etwa einem Monat durchgeführt werden.
Antihistaminika. Bei Einnahme von Antihistaminika ist ein EKG sowie die Bestimmung des Blutbilds und der Leber- und Nierenwerte vor Beginn der Behandlung empfehlenswert. Eine EKG-Kontrolle sollte nur bei längerfristiger Behandlung oder Kombinationstherapie mit anderen Arzneimitteln, die zur Verlängerung der QT-Zeit führen können, nach etwa einem Monat durchgeführt werden. Blutbild und Leberwerte sollten in den ersten drei Behandlungsmonaten monatlich, später vierteljährlich, die Nierenwerte nach einem Monat und später vierteljährlich kontrolliert werden.
Antidepressiva. Unter Antidepressiva-Therapie sollten vor Therapiebeginn und nach einem Monat Blutbild, Leber- und Nierenwerte, EKG, EEG, Blutdruck und Puls sowie Blutzuckerkonzentration und HbA1c-Wert kontrolliert werden [4].
Antipsychotika. Unter Antipsychotika-Therapie notwendige Kontrolluntersuchungen umfassen Blutbild und Leberenzyme.
Phytotherapeutika. Es sind keine routinemäßigen Laborkontrollen erforderlich.
Empfehlung der Leitlinien
Die Nutzen-Risiko-Bilanz für Hypnotika ist im Vergleich zu anderen Psychopharmaka als kritisch zu bewerten, Übersichtsbeiträge zeigen eine erhebliche Varianz von Studienergebnissen, bei einigen Substanzen (wie Melatonin) besteht eine Publikationsverzerrung.
Die S3-Leitlinie der Deutschen Gesellschaft für Schlafforschung und Schlafmedizin (DGSM 2016) empfiehlt zur Therapie von Insomnien [12]:
- Kognitiv-verhaltenstherapeutische Strategien (Empfehlungsgrad A)
- Benzodiazepin-Rezeptoragonisten für den Kurzzeitgebrauch von drei bis vier Wochen (Empfehlungsgrad A)
- Kurzzeitbehandlung mit sedierenden Antidepressiva (Trazodon, Trimipramin, Doxepin) unter Beachtung von Kontraindikationen (Empfehlungsgrad A)
- Retardiertes Melatonin kann bei Patienten > 55 Jahre empfohlen werden (Empfehlungsgrad B)
Interessenkonflikterklärung
GL: Honorare für Vorträge und Beratungen oder unbeschränkte Subventionen für Schulungen von Bayer, Janssen-Cilag, Lundbeck, Pfizer und Servier.
WEM: Beratungstätigkeit für Schwabe Arzneimittel
Literatur
1. Chieffi S, Carotenuto M, Monda V, et al. Orexin system: The key for a healthy life. Front Physiol 2017;8:357.
2. Hajak G, Müller WE, Wittchen HU, et al. Abuse and dependence potential for the non-benzodiazepine hypnotics zolpidem and zopiclone: a review of case reports and epidemiological data. Addiction 2003;98:1371–8.
3. Laux G, Dietmaier O. Psychopharmaka. Ratgeber für Patienten und Angehörige. 10., neu bearbeitete Auflage. Berlin: Springer, 2018.
4. Laux G, Müller WE. Weiterbildungs-Curriculum Psychopharmakologie/Pharmakotherapie. Folge 2: Verhaltenspharmakologie und klinische Pharmakotherapie der Antidepressiva. Psychopharmakotherapie 2018;25:21–35.
5. Mayer G, Rodenbeck A, Hajak G. Pharmakotherapie der chronischen Insomnie. Internistische Praxis 2018;59:681–96.
6. Mikoteit T, Holsboer-Trachsler E. Beeinflussung des Schlaf-Wach-Rhythmus durch Antidepressiva. Psychiatrie & Neurologie 2013;4–8.
7. Müller WE, Laux G. Weiterbildungs-Curriculum Psychopharmakologie/Pharmakotherapie. Teil 1: Allgemeine Psychopharmakotherapie, allgemeine Pharmakologie, Antidepressiva – Pharmakologie. Psychopharmakotherapie 2017;24:276–82.
8. Nissen C, Frase L, Hajak G, et al. Hypnotika – Stand der Forschung. Nervenarzt 2014;85:67–76.
9. Pagel JF, Pandi-Perumal SR, Monti JM. Treating insomnia with medications. Sleep Science Practice 2018;2:5.
10. Pollmächer T. Schlafstörungen. In: Möller H-J, Laux G, Kapfhammer H-P (Hrsg.). Psychiatrie, Psychosomatik, Psychotherapie. 5. Auflage. Berlin: Springer, 2017.
11. Riemann D, Baglioni C, Feige B, et al. Insomnien – Stand der Forschung. Nervenarzt 2014;85:43–9.
12. Riemann D, Baum E, Cohrs S, et al. S3-Leitlinie Nicht erholsamer Schlaf/Schlafstörungen: Kapitel „Insomnie bei Erwachsenen“, Update 2016. Somnologie 2017;21:2–44.
13. Schröder J. Pharmakotherapie von Schlafstörungen bei älteren Menschen. Dtsch Med Wochenschr 2013;138:2550–3.
14. Schwarz S, Frölich L, Deuschle M. Pharmakologische Behandlung von Schlafstörungen bei älteren Menschen. Arzneimittel-, Therapie-Kritik 2013;45:377–90.
15. Szabadi E. Drugs for sleep disorders: mechanisms and therapeutic prospects. Br J Clin Pharmacol 2006;61:761–6.
16. Volz HP, Müller WE. Weiterbildungs-Curriculum Psychopharmakologie/Pharmakotherapie. Teil 3: Pharmakologie und klinische Psychopharmakotherapie der Tranquilizer/Anxiolytika. Psychopharmakotherapie 2018;25:69–75.
Prof. Dr. med. Dipl.-Psych. Gerd Laux, Institut für Psychologische Medizin (IPM), Nussbaumstraße 9, 83564 Soyen, E-Mail: ipm@imp-laux.de
Prof. Dr. Walter E. Müller, Höhenstraße 49A, 67550 Worms
Psychopharmakotherapie 2019; 26(02):85-95
