Prof. Dr. Hans-Christoph Diener, Essen
Für die immunmodulatorische Therapie der schubförmigen multiplen Sklerose gibt es inzwischen viele zugelassene Medikamente. Das gilt allerdings kaum für progrediente MS-Formen; zugelassen sind hier der monoklonale Antikörper Ocrelizumab (Ocrevus®; bei früher primär progredienter MS) und das Chemotherapeutikum Mitoxantron (z. B. Ralenova®; zugelassen für hochaktive schubförmige MS, Leitlinienmempfehlung für sekundär progrediente MS).
Ibudilast (Abb. 1) hemmt mehrere zyklische Nucleotid-Phosphodiesterasen, den Makrophagen-Migrations-Inhibitions-Faktor und den Toll-like-Rezeptor IV. Es kann die Blut-Hirn-Schranke überwinden und daher im zentralen Nervensystem wirken. Ibudilast ist in Asien zur Behandlung von Asthma bronchiale und von Schwindel nach Schlaganfall zugelassen.
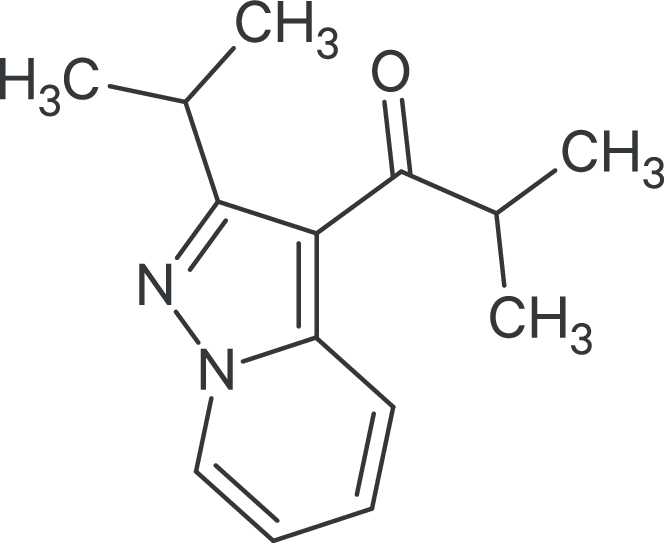
Abb. 1. PDE4-Hemmer Ibudilast
In einer Phase-II-Studie bei Patienten mit schubförmiger MS führte Ibudilast in Dosierungen von 30 bis 60 mg pro Tag zu einer Verlangsamung der Progression der Hirnatrophie, verhinderte aber nicht das neue Auftreten von Entmarkungsherden. Jetzt sollte in einer randomisierten Phase-II-Studie die Substanz bei der progredienten multiplen Sklerose untersucht werden.
Methodik
In die Studie wurden 255 Patienten mit primär oder sekundär progredienter multipler Sklerose aufgenommen. Sie wurden für einen Zeitraum von 96 Wochen mit Ibudilast (n = 129) oder Placebo (n = 126) behandelt. Die Verum-Patienten erhielten initial über zwei Wochen 60 mg/Tag Ibudilast; anschließend wurde die Dosis auf 100 mg/Tag erhöht. Patienten, die unter Nebenwirkungen litten, konnten bis Woche 8 die Dosis auf 60 mg oder 80 mg/Tag reduzieren.
Primärer Endpunkt war das Ausmaß der Hirnatrophie, das mit speziellen MR-Sequenzen zu Beginn und am Ende der Studie gemessen wurde. Außerdem wurde der Behinderungsgrad der Patienten mit der Expanded Disability Status Scale (EDSS) erfasst.
Ergebnisse
53 % der Patienten in der Ibudilast-Gruppe und 52 % in der Placebo-Gruppe hatten eine primär progrediente MS. Die Patienten waren im Mittel 56 Jahre alt und im Median seit zehn Jahren erkrankt. Bei 30 % bestand eine Vorbehandlung mit Glatirameracetat oder Interferon beta, die während der Studie beibehalten wurde. Der EDSS-Score bei Beginn der Studie betrug 6,0.
Das Ausmaß der Progression der Hirnatrophie war unter Ibudilast geringer als unter Placebo. Der Unterschied entsprach etwa 2,5 ml weniger Verlust an Hirngewebe mit Ibudilast, was eine relative Differenz von 48 % ergab. Für die Behinderungsprogression der MS gemessen mit der EDSS-Skala ergab sich ein Hazard-Ratio von 0,74 für Ibudilast, das statistisch jedoch nicht signifikant war.
92 % der Ibudilast- und 88 % der Placebo-Patienten berichteten von Nebenwirkungen. Unter Ibudilast kam es signifikant häufiger zu gastrointestinalen Störungen, Kopfschmerzen, Hautinfektionen, Infektionen der oberen Atemwege und Depressionen.
Kommentar
In dieser Phase-II-Studie bei Patienten mit primär oder sekundär progredienter multipler Sklerose verminderte der PDE4-Inhibitor Ibudilast die Progression der Hirnatrophie im Vergleich zu Placebo in einem Zeitraum von 96 Wochen relativ um 48 %. In den Studien mit Ocrelizumab hatte der Unterschied 17,5 % und mit Siponimod 15 % betragen. Ibudilast hatte allerdings keinen signifikanten Einfluss auf die Progression der klinischen Symptome und das Ausmaß der Behinderung. Zudem war im Vergleich zu Placebo mit mehr unerwünschten Arzneimittelwirkungen assoziiert. Die Frage, ob diese Substanz eine Zukunft in der Behandlung der progredienten MS hat, kann erst entschieden werden, wenn eine große Phase-III-Studie einen Unterschied in der klinischen Progression und im Behinderungsgrad bei Patienten mit progredienter MS zeigt.
Quelle
Fox RJ, et al. Phase 2 trial of ibudilast in progressive multiple sclerosis. N Engl J Med 2018;379:846–55.
Psychopharmakotherapie 2019; 26(02):104-113
