Gerd Laux, Soyen/Waldkraiburg/München
Die Geschichte der Entdeckung und Entwicklung der Psychopharmaka ist die eines Erfolgs: Das Gründerjahrzehnt der 50er-Jahre als der „goldenen Ära“ bescherte in dichter Folge bahnbrechende psychopharmakologische Meilensteine mit revolutionären Konsequenzen für die psychiatrische Therapie. Chlorpromazin (Megaphen), Lithium, Imipramin (Tofranil) Methylphenidat (Ritalin), Chlordiazepoxid (Librium) und der erste Monoaminoxidase-(MAO-)Hemmer wurden meist per Zufall, in Selbstversuchen sowie aus Experimentierfreude bei Fehlen stringenter ethischer, rechtlicher und administrativer Vorgaben klinisch eingeführt – die Psychopharmaka-Hauptgruppen der Neuroleptika, Antidepressiva und Tranquilizer waren geboren [16, 22–24, 27]. Die psychiatrische Pharmakotherapie stellte die Behandlung der Patienten auf eine neue Grundlage, wurde auch ein Instrument zur Erforschung neurobiologischer Mechanismen psychischer Störungen und führte zum Begriff der „biologischen Psychiatrie“, die von etwa 1975 bis etwa 2012 in der deutschen Psychiatrie dominierte. Aber auch Rückschläge waren zu verzeichnen – Beispiele für Marktrückzug zwischen 1986 und 1993 wegen gravierender Nebenwirkungen sind das Antidepressivum Nomifensin (Alival) und das Benzamid-Neuroleptikum Remoxiprid (Roxiam). Clozapin (Leponex) konnte nur durch den persönlichen Einsatz führender Pharmakopsychiater wie Hanns Hippius unter strikten Auflagen im Handel bleiben. Heute gehören Psychopharmaka auch in Deutschland zu den meistverordneten Medikamenten. Die Entwicklung des Verordnungsvolumens ist in Abbildung 1 wiedergegeben. In den letzten zehn Jahren ist es wieder um fast 40 % gestiegen. Deutlich wird eine Verschiebung der Substanzklassen mit einer immensen Zunahme der Antidepressiva-Verordnungen und einem robust-konstanten Rückgang der (Benzodiazepin-)Tranquilizer [26].
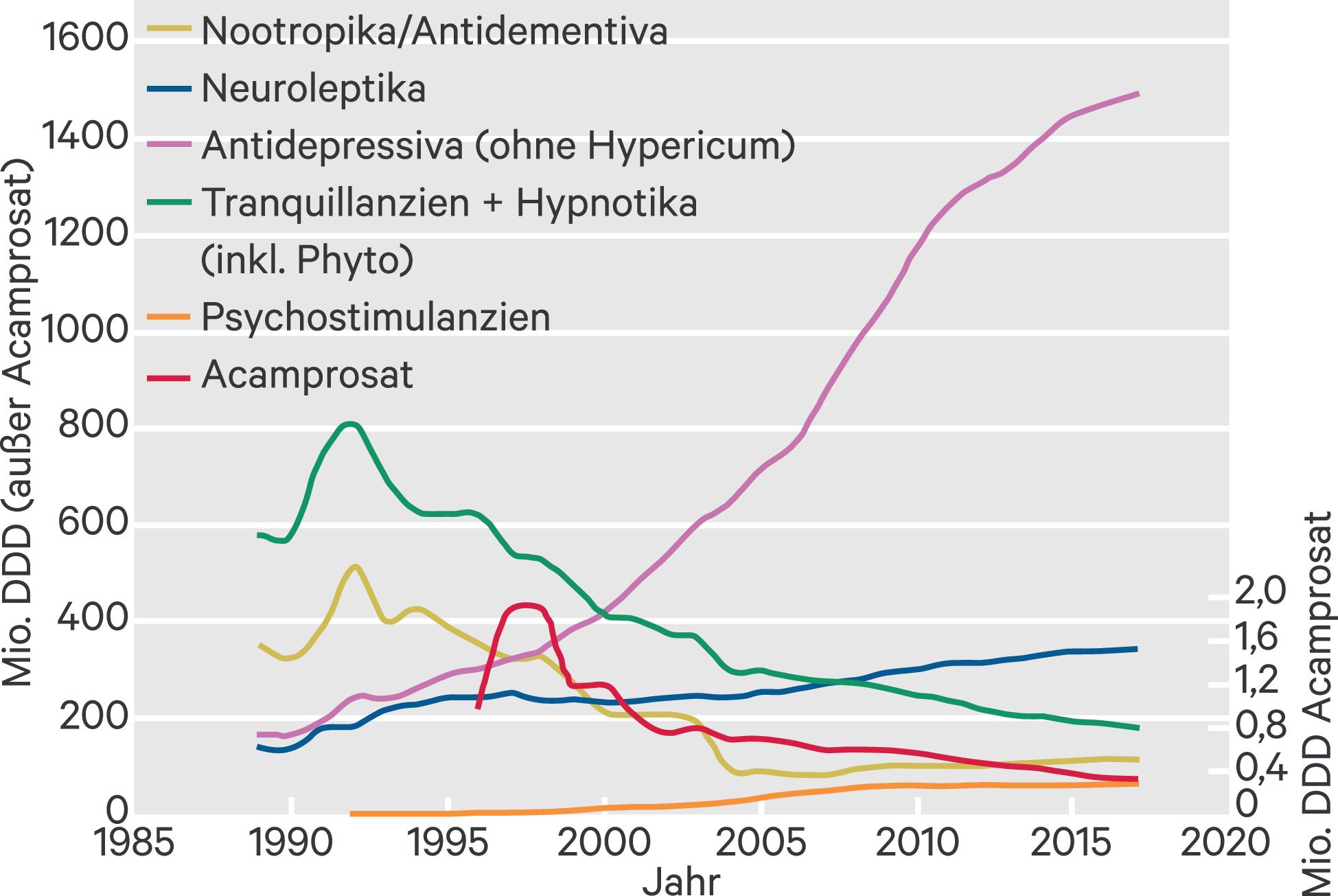
Abb. 1. Entwicklung des Verordnungsvolumens von Psychopharmaka zulasten der GKV in den letzten 25 Jahren [5a]
Der Therapie mit Psychopharmaka wird in deutschen Medien seit geraumer Zeit ein Negativ-Tenor zuteil – überwiegend wird über Nebenwirkungen, Risiken und fragliche Wirksamkeit berichtet. Auch ein Teil der Fachpresse konstatiert, dass die Kosten-Nutzen-Bilanz vielfach negativ sei und Ergebnisse von profitorientierten pharmazeutischen Unternehmen geschönt würden (Publication bias). Objektive, seriöse, Industrie-unabhängige Gremien und Studien kämen zu dem Ergebnis, dass für die meisten neueren Medikamente kein Zusatznutzen bestehe [26]. Die großen methodologischen Probleme beim Vergleich mit Psychotherapie-Studien oder zwischen selektierten RCT-Studienergebnissen und „Real-World-Daten“ sowie die Placebo-Problematik wurden in der Psychopharmakotherapie (PPT) immer wieder aufgezeigt, auch die Diskrepanz zwischen stationärer und ambulanter Versorgung. So konnte eine große Studie zur Versorgung aus sektorenübergreifender Perspektive gravierende Unterschiede in der Verordnung von typischen und atypischen Antipsychotika aufzeigen. Eine indizierte kontinuierliche Arzneimitteltherapie fand überwiegend nicht statt. Die Sektoralisierung des deutschen Versorgungssystems gilt als eine wesentliche Ursache für Ineffektivität auch in der Psychopharmakotherapie [14].
Tatsächlich ist der Wissensstand über Psychopharmaka in der deutschen Bevölkerung niedrig und eine objektive, ausgewogene Information findet derzeit kaum statt.
1994–2018
1994 konstatierten Fritze und Aldenhoff, dass die aktuellen psychopharmakologischen Therapiemöglichkeiten dem Stand der 60er-Jahre entsprächen [6]. Knapp zehn Jahre später hatte sich das Bild deutlich gewandelt: Im Rückblick „10 Jahre PPT“ wurde 2003 konstatiert, dass eine wahrscheinlich zumindest zahlenmäßig auf absehbare Zeit nicht mehr zu erreichende Fülle neuer Psychopharmaka zugelassen und in den deutschen Markt eingeführt worden sei: 1994 Risperidon, 1996 Olanzapin, Mirtazapin, Venlafaxin, Citalopram, 1997 Sertralin, Sertindol, Nefazodon, 1998 Donepezil, Reboxetin, Rivastigmin, 1999 Amisulprid, 2000 Quetiapin und Galantamin, 2002 Ziprasidon [11]. Zwischen 2003 und 2005 wurden dann nochmals eine Reihe von Psychopharmaka zugelassen, seitdem deutlich weniger, seit 2015 nur vier, davon eines (3-Monats-Formulierung von Paliperidonpalmitat) als Weiterentwicklung einer bereits zugelassenen Substanz (Tab. 1). Die innovativen Alkoholentwöhnungsmittel Acamprosat und Nalmefen konnten sich nicht im Markt platzieren. Aktuell etablieren sich partielle Dopaminagonisten (Aripiprazol, Cariprazin, Brexpiprazol) als eine Antipsychotika-Subgruppe, innovativ sind Versuche mit Botulinumtoxin und Ketamin bei Depressionen, vor der Zulassung steht Esketamin.
Tab. 1. Neue Psychopharmaka der letzten 25 Jahre in Deutschland (1994–2018) [aktuelle Informationen unter www.fachinfo.de, www.ema.europa.eu und www.pharmnet-bund.de]
|
Jahr der Zulassung |
INN |
Handelsname® |
Hersteller |
Indikation |
Wirkung |
Besonderheiten/Bemerkungen |
|
1994 |
Risperidon |
Risperdal |
Janssen/Organon |
Zur Behandlung der Schizophrenie, mäßiger bis schwerer manischer Episoden assoziiert mit bipolaren Störungen, zur Kurzzeitbehandlung (bis zu 6 Wochen) von anhaltender Aggression bei Patienten mit mäßiger bis schwerer Alzheimer-Demenz, die auf nichtpharmakologische Methoden nicht ansprechen und wenn ein Risiko für Eigen- und Fremdgefährdung besteht. Zur symptomatischen Kurzzeitbehandlung (bis zu 6 Wochen) von anhaltender Aggression bei Verhaltensstörung bei Kindern im Alter ab 5 Jahren und Jugendlichen mit unterdurchschnittlicher intellektueller Funktion oder mentaler Retardierung, die gemäß den DSM-IV-Kriterien diagnostiziert wurden, bei denen der Schweregrad der aggressiven oder anderen störenden Verhaltensweisen eine pharmakologische Behandlung erfordert. |
Atypisches Neuroleptikum. Selektiver monoaminerger Antagonist mit hoher Affinität für 5-HT2- und D2-Rezeptoren. Bindet ebenfalls an alpha1-adrenerge Rezeptoren und, mit geringerer Affinität, an H1-histaminerge und alpha2-adrenerge Rezeptoren. Keine Affinität zu cholinergen Rezeptoren. Obwohl Risperidon ein starker D2-Antagonist ist, der bekanntermaßen die positiven Symptome der Schizophrenie verbessert, verursacht es eine geringere Dämpfung der motorischen Aktivität und Induktion der Katalepsie als klassische Antipsychotika. |
Seit 2013 auf der Liste der unentbehrlichen Arzneimittel der WHO: http://www.who.int/topics/essential_medicines/en/ |
|
Kava-Kava |
Generalisierte Angst-Störung (GAD) |
Pflanzliches Anxiolytikum |
2002 wegen UAW außer Handel |
|||
|
1995 |
Acamprosat |
Campral |
Merck Serono |
Zur Unterstützung der Aufrechterhaltung der Abstinenz beim alkoholabhängigen Patienten im Rahmen eines therapeutischen Gesamtkonzepts |
Die Wirkung basiert wahrscheinlich auf einer Stimulierung der inhibitorischen GABAergen Neurotransmission sowie auf einem antagonistischen Effekt auf die erregenden Aminosäuren, insbesondere Glutamat |
|
|
1996 |
Venlafaxin |
Trevilor |
Pfizer |
Retardkapseln zur Behandlung von Episoden einer Major Depression Rezidivprophylaxe von Episoden einer Major Depression Behandlung der generalisierten Angststörung Behandlung der sozialen Angststörung Behandlung der Panikstörung, mit oder ohne Agoraphobie |
Antidepressivum, SSNRI Venlafaxin und sein aktiver Hauptmetabolit O-Desmethyl-Venlafaxin (ODV) sind Inhibitoren der neuronalen Serotonin- und Noradrenalin-Wiederaufnahme. Venlafaxin inhibiert außerdem die Dopamin-Wiederaufnahme schwach. Venlafaxin und ODV reduzieren die beta-adrenerge Ansprechbarkeit bei Einzelgabe (Einzeldosis) und bei chronischer Gabe. |
Ursprünglich von Wyeth angeboten, das 2009 von Pfizer übernommen wurde |
|
1996 |
Mirtazapin |
Remergil |
MSD Sharp & Dohme |
Behandlung depressiver Erkrankungen (Episoden einer Major Depression) bei Erwachsenen |
Tetrazyklisches Antidepressivum, das noradrenerg und spezifisch serotonerg wirkt (NaSSA). Zentral wirksamer, präsynaptisch angreifender alpha2-Antagonist, der die zentrale noradrenerge und serotonerge Neurotransmission verstärkt. Die Verstärkung der serotonergen Neurotransmission wird spezifisch durch 5-HT1-Rezeptoren vermittelt. 5-HT2- und 5-HT3-Rezeptoren werden durch Mirtazapin blockiert. |
Ursprünglich von Organon ausgeboten, das 2007 von Schering-Plough übernommen wurde, welches in Deutschland unter Essex-Pharma firmierte. Schering-Plough und Essex Pharma wurden 2007 von MSD Sharp & Dohme übernommen. |
|
1996 |
Citalopram |
Cipramil |
Lundbeck |
Behandlung depressiver Erkrankungen und Panikstörungen mit und ohne Agoraphobie |
Antidepressivum, SSRI Potenter und sehr selektiver Wiederaufnahmehemmer von Serotonin. Kein oder nur ein minimaler Effekt auf die Noradrenalin-, Dopamin- und Gamma-Aminobuttersäure-(GABA-)Aufnahme. |
Ursprünglich von der Chemischen Fabrik Promonta eingeführt, die 1994 ein Joint-Venture mit Lundbeck einging und unter dem Namen Promonta-Lundbeck Arzneimittel GmbH & Co. agierte. Seit Ende des Joint-Ventures im Jahr 2001 heißt das Unternehmen Lundbeck GmbH |
|
1996 |
Olanzapin |
Zyprexa Zyprexa-Velotab (2000) |
Lilly |
Behandlung der Schizophrenie. Bei Patienten, die initial auf die Behandlung angesprochen haben, ist Olanzapin bei fortgesetzter Behandlung zur Aufrechterhaltung der klinischen Besserung wirksam. Behandlung von mäßig schweren bis schweren manischen Episoden. Bei Patienten, deren manische Episode auf eine Behandlung mit Olanzapin angesprochen hat, ist Olanzapin zur Phasenprophylaxe bei Patienten mit bipolarer Störung angezeigt. |
Atypisches Neuroleptikum. Neuroleptischer antimanischer und stimmungsstabilisierender Wirkstoff, der mit einer größeren Anzahl von Rezeptorsystemen reagiert. |
|
|
1997 |
Sertindol |
Serdolect |
Lundbeck |
Behandlung der Schizophrenie. Aufgrund kardiovaskulärer Sicherheitsbedenken sollte Sertindol nur bei Patienten angewendet werden, die zumindest ein anderes Antipsychotikum nicht vertragen haben. Sertindol sollte nicht in Notfallsituationen bei akut gestörten Patienten zur raschen Symptomreduktion verabreicht werden. |
Atypisches Neuroleptikum mit Strukturähnlichkeit zu Risperidon Es wird angenommen, dass dem neuropharmakologischen Profil von Sertindol als Neuroleptikum seine selektive Hemmwirkung auf mesolimbische dopaminerge Neuronen und die ausgewogenen inhibitorischen Effekte auf zentrale D2- und 5-HT2-Rezeptoren sowie auf alpha1-adrenerge Rezeptoren zugrunde liegen. |
Ursprünglich von der Chemischen Fabrik Promonta eingeführt, jetzt Lundbeck GmbH (vgl. Citalopram) |
|
1997 |
Sertralin |
Zoloft |
Pfizer |
Behandlung von Episoden einer Major-Depression. Rezidivprophylaxe von Episoden einer Major Depression Behandlung von
|
Antidepressivum, SSRI Potenter und selektiver Hemmer der neuronalen Wiederaufnahme von Serotonin. Nur sehr schwache Effekte auf die neuronale Noradrenalin- oder Dopamin-Aufnahme |
|
|
1997 |
Nefazodon |
Nefadar |
BMS |
Antidepressivum Wurde 2003 wegen des Risikos von Leberschäden aus dem Handel genommen |
||
|
1998 |
Donepezil |
Aricept |
Eisai |
Leichte bis mittelschwere Alzheimer-Demenz |
Acetylcholinesterasehemmer |
Mitvertrieb durch Pfizer |
|
1998 |
Modafinil |
Vigil |
Teva |
Behandlung von Erwachsenen mit exzessiver Schläfrigkeit, die mit Narkolepsie mit oder ohne Kataplexie einhergeht |
Psychoanaleptikum, zentral wirksames Sympathomimetikum. Modafinil verbessert die Wachheit bei einer Vielzahl von Spezies, den Menschen eingeschlossen. Der exakte Wirkungsmechanismus, durch den Modafinil die Wachheit fördert, ist unbekannt. |
|
|
1998 |
Reboxetin |
Edronax |
Pfizer |
Behandlung akuter depressiver Erkrankungen/Major Depression |
Antidepressivum, selektiver Noradrenalin-Wiederaufnahmehemmer. Reboxetin hat nur einen schwachen Effekt auf die 5-HT-Wiederaufnahme und beeinflusst die Aufnahme von Dopamin nicht. |
Ursprünglich von Pharmacia Upjohn eingeführt, das 1999 mit Monsanto fusionierte und dann nur noch Pharmacia hieß (die landwirtschaftlich-chemische Sparte wurde 2002 unter dem Namen Monsanto eigenständig). Reboxetin wurde von Farmitalia Carlo Erba entwickelt, das wiederum im Jahr 1993 von Pharmacia gekauft worden war. Pharmacia wurde 2003 von Pfizer gekauft. |
|
1998 |
Rivastigmin |
Exelon |
Novartis |
Antidementivum |
Acetyl- und Butyrylcholinesterasehemmer |
|
|
1999 |
Amisulprid |
Solian |
Sanofi |
Behandlung von akuten und chronischen schizophrenen Störungen:
|
Psychopharmakon, Dopaminrezeptor-Antagonist Amisulprid bindet selektiv mit einer hohen Affinität an menschliche D2- und D3-Rezeptor-Subtypen. Keine Affinität zu D1-, D4- und D5-Rezeptoren Im Gegensatz zu klassischen und anderen atypischen Neuroleptika zeigt Amisulprid keine Affinität zu Serotonin-, alpha-adrenergen-, H1- und cholinergen Rezeptoren. Zudem bindet es nicht an Sigma-Rezeptoren. |
Ursprünglich von Synthelabo eingeführt, das 1999 von Sanofi übernommen wurde und als Sanofi-Synthelabo firmierte. Sanofi-Synthelabo übernahm im Jahr 2004 Aventis, das 1999 aus der Fusion von Hoechst und Rhone-Poulenc entstanden war. |
|
1999 |
Zaleplon |
Sonata |
Meda AB |
Insomnie |
Z-Substanz Hypnotikum |
EU-Zulassung 2015 auf Antrag des Herstellers zurückgezogen |
|
2000 |
Galantamin |
Reminyl |
Janssen |
Leichte bis mittelschwere Alzheimer-Demenz |
Acetylcholinesterasehemmer |
|
|
2000 |
Quetiapin |
Seroquel |
AstraZeneca |
Behandlung der Schizophrenie. Behandlung von bipolaren Störungen: Zur Behandlung von mäßigen bis schweren manischen Episoden bei bipolaren Störungen Zur Behandlung von schweren depressiven Episoden bei bipolaren Störungen Zur Rückfallprävention von manischen oder depressiven Episoden bei Patienten mit bipolaren Störungen, die zuvor auf eine Quetiapin-Behandlung angesprochen haben. |
Atypisches Neuroleptikum Quetiapin und der aktive Plasmametabolit N-Desalkylquetiapin interagieren mit einem breiten Spektrum von Neurotransmitterrezeptoren. Sie besitzen Affinität zu zerebralen serotonergen (5-HT2) und dopaminergen (D1 und D2) Rezeptoren. Es wird angenommen, dass diese Kombination eines Rezeptorantagonismus mit höherer Selektivität für 5-HT2- verglichen mit D2-Rezeptoren für die klinischen antipsychotischen Eigenschaften und das gering ausgeprägte extrapyramidale Nebenwirkungsprofil (EPS) von Quetiapin im Vergleich zu typischen Antipsychotika mitverantwortlich ist. |
Quetiapin wurde von der britischen Firma Zeneca entwickelt. Im Jahr 1999 entstand aus Zeneca und der schwedischen Astra die Firma AstraZeneca |
|
2002 |
Memantin |
Ebixa, Axura |
Lundbeck bzw. Merz |
Moderate bis schwere Alzheimer-Demenz |
Nichtkompetitiver NMDA-Antagonist Antidementivum |
|
|
2002 |
Ziprasidon |
Zeldox |
Pfizer |
Behandlung der Schizophrenie bei Erwachsenen. Bei Erwachsenen und bei Kindern und Jugendlichen im Alter von 10 bis 17 Jahren zur Behandlung von manischen oder gemischten Episoden bis zu einem mäßigen Schweregrad bei bipolaren Störungen (die Prävention von Episoden bipolarer Störungen wurde nicht nachgewiesen). |
Atypisches Neuroleptikum Ziprasidon hat eine hohe Affinität zu D2-Rezeptoren und eine noch wesentlich höhere Affinität zu 5-HT2A-Rezeptoren |
|
|
2002 |
Risperidon-Depot |
Risperdal Consta |
Janssen |
Parenterale Depotform zur Erhaltungstherapie der Schizophrenie bei Patienten, die mit oralen Antipsychotika stabilisiert sind. Erste Depotform eines atypischen Neuroleptikums. |
Atypisches Neuroleptikum |
|
|
2003 |
Escitalopram |
Cipralex |
Lundbeck |
Behandlung von Episoden einer Major Depression. Behandlung von Panikstörung mit oder ohne Agoraphobie. Behandlung von sozialer Angststörung (sozialer Phobie). Behandlung von generalisierter Angststörung. Behandlung von Zwangsstörung |
Antidepressivum, SSRI mit hoher Affinität zur primären Bindungsstelle. Es bindet auch an einer allosterischen Bindungsstelle des Serotonintransporters, allerdings mit einer 1000-fach geringeren Affinität. Keine oder nur eine sehr geringe Affinität zu einer Reihe von anderen Rezeptoren, darunter 5-HT1A-, 5-HT2-, D1- und D2-Rezeptoren sowie Alpha1-, Alpha2-, Beta-Adrenorezeptoren, H1-Rezeptoren sowie cholinerge Rezeptoren vom Muskarin-Typ, Benzodiazepin- und Opioidrezeptoren. |
|
|
2004 |
Aripiprazol |
Abilify |
Otsuka |
Behandlung der Schizophrenie bei Erwachsenen und bei Jugendlichen ab 15 Jahren Behandlung von mäßigen bis schweren manischen Episoden der Bipolar-I-Störung und für die Prävention einer neuen manischen Episode bei Erwachsenen, die überwiegend manische Episoden hatten und deren manische Episoden auf die Behandlung mit Aripiprazol ansprachen. Bis zu 12 Wochen dauernde Behandlung von mäßigen bis schweren manischen Episoden der Bipolar-I-Störung bei Jugendlichen ab 13 Jahren |
Antipsychotikum Es wird vermutet, dass die Wirkung bei Schizophrenie und Bipolar-I-Störung über die Kombination einer partiell agonistischen Wirkung auf D2- und 5-HT1A-Rezeptoren und einer antagonistischen Wirkung auf 5-HT2A-Rezeptoren vermittelt wird. |
|
|
2004 |
Duloxetin |
Cymbalta |
Lilly |
Behandlung von depressiven Erkrankungen (Major Depression), Schmerzen bei diabetischer Polyneuropathie und generalisierter Angststörung. |
Antidepressivum, SSNRI Kombinierter Serotonin-(5-HT-) und Noradrenalin-(NA-)Wiederaufnahmehemmer. Geringe Wiederaufnahmehemmung von Dopamin ohne signifikante Affinität für histaminerge, dopaminerge, cholinerge und adrenerge Rezeptoren. |
|
|
2004 |
Atomoxetin |
Strattera |
Lilly |
Behandlung der Aufmerksamkeitsdefizit-/Hyperaktivitätsstörung (ADHS) bei Kindern ab 6 Jahren, bei Jugendlichen und bei Erwachsenen als Teil eines umfassenden Behandlungsprogramms. |
Psychoanaleptikum, zentral wirkendes Sympathomimetikum. Hochselektiver und potenter Hemmstoff des präsynaptischen Noradrenalin-Transporters. Dies ist der postulierte Wirkungsmechanismus. Keine direkte Wirkung auf Serotonin- oder Dopamin-Transporter. Sehr geringe Affinität zu anderen noradrenergen Rezeptoren oder zu anderen Neurotransmitter-Transportern oder Rezeptoren. |
|
|
2006 |
Vareniclin |
Champix |
Pfizer |
Nicotin-Entwöhnungsmittel |
Partieller Agonist am Nikotin-Rezeptor |
|
|
2007 |
Bupropion |
Elontril |
GSK |
Behandlung von Episoden einer depressiven Erkrankung (Episoden einer Major Depression) |
Psychoanaleptikum, Antidepressivum. Hemmt selektiv die neuronale Wiederaufnahme von Katecholaminen (Noradrenalin und Dopamin), hemmt nur minimal die Wiederaufnahme von Indolaminen (Serotonin) und bewirkt keine Hemmung der beiden Monoaminoxidasen. Der Mechanismus der antidepressiven Wirkung von Bupropion ist nicht bekannt. Es wird jedoch vermutet, dass diese Wirkung über noradrenerge und/oder dopaminerge Mechanismen verläuft. |
|
|
2007 |
Paliperidon |
Invega |
Janssen |
Behandlung der Schizophrenie bei Erwachsenen und bei Jugendlichen ab 15 Jahre und Behandlung von schizoaffektiven Störungen bei Erwachsenen. |
Antipsychotikum, aktiver Metabolit des atypischen Neuroleptikums Risperidon. Selektiver Inhibitor monoaminerger Effekte, dessen pharmakologische Eigenschaften sich von denen klassischer Neuroleptika unterscheiden. Paliperidon bindet stark an 5-HT2- und D2-Rezeptoren. Es blockiert darüber hinaus auch alpha1-adrenerge Rezeptoren und, in geringerem Ausmaß, H1-histaminerge sowie alpha2-adrenerge Rezeptoren. Die pharmakologische Wirkung der (+) und (–) Paliperidon-Enantiomere ist qualitativ und quantitativ ähnlich. Paliperidon bindet nicht an cholinerge Rezeptoren. Obwohl es ein starker D2-Antagonist ist, von dem angenommen wird, dass er die positiven Symptome der Schizophrenie mildert, führt es in geringerem Maße zu einer Katalepsie und Verminderung der motorischen Funktionen als klassische Neuroleptika. Der dominierende zentrale Serotonin-Antagonismus könnte die Tendenz von Paliperidon zur Auslösung extrapyramidaler Nebenwirkungen vermindern. |
|
|
2008 |
Rivastigmin transdermal |
Exelon |
Novartis |
Leichte bis mittelschwere Alzheimer-Demenz |
Acetyl- und Butyrylcholinesterasehemmer |
|
|
2008 |
Olanzapinpamoat |
Zypadhera |
Lilly |
Erhaltungstherapie erwachsener Patienten mit Schizophrenie |
Atypisches Antipsychotikum |
|
|
2009 |
Agomelatin |
Valdoxan |
Servier |
Behandlung von Episoden einer Major Depression bei Erwachsenen. |
Psychoanaleptikum, Antidepressivum. Melatonerger (MT1- und MT2-Rezeptoren) Agonist und 5-HT2C-Antagonist. Bindungsstudien zeigen, dass Agomelatin keinen Effekt auf die Monoaminaufnahme hat und keine Affinität zu alpha- und beta-adrenergen, histaminergen, cholinergen, dopaminergen und Benzodiazepin-Rezeptoren aufweist. Agomelatin resynchronisiert zirkadiane Rhythmen in Tiermodellen mit Störung des zirkadianen Rhythmus. Es erhöht die Freisetzung von Noradrenalin und Dopamin speziell im frontalen Kortex und hat keinen Einfluss auf den extrazellulären Serotoninspiegel. |
|
|
2009 |
Lavendelöl |
Lasea |
Schwabe |
Unruhezustände bei ängstlicher Verstimmung |
Pflanzliches Psychopharmakon |
|
|
2010 |
Asenapin |
Sycrest |
Organon |
Behandlung mäßiger bis schwerer manischer Episoden einer Bipolar-I-Störung bei Erwachsenen. |
Antipsychotikum, Psycholeptikum Der Wirkungsmechanismus ist nicht vollständig geklärt. Jedoch wird auf der Grundlage seiner Rezeptor-Pharmakologie vermutet, dass die Wirksamkeit von Asenapin durch eine Kombination antagonistischer Aktivitäten an D2- und 5-HT2A-Rezeptoren vermittelt wird. Aktivitäten an anderen Rezeptoren wie 5-HT1A-, 5-HT1B-, 5-HT2C-, 5-HT6-, 5-HT7-, D3- und alpha2-adrenergen Rezeptoren tragen möglicherweise ebenfalls zu den klinischen Wirkungen bei. |
|
|
2011 |
Paliperidonpalmitat (LAI-Depot) |
Xeplion |
Janssen-Cilag |
Erhaltungstherapie der Schizophrenie bei erwachsenen Patienten, die auf Paliperidon oder Risperidon eingestellt wurden |
Atypisches Antipsychotikum |
|
|
2012 |
Tianeptin |
Tianeurax |
Neuraxpharm Arzneimittel GmbH |
Behandlung von Depressionen bei Erwachsenen |
Trizyklisches Antidepressivum Soll als Serotonin-Wiederaufnahmeverstärker wirken |
In Frankreich und Österreich stand Tianeptin bereits seit den 80er-Jahren als Stablon® zur Verfügung |
|
2013 |
Loxapin |
Adasuve |
Ferrer |
Zur schnellen Kontrolle von leichter bis mittelschwerer Agitiertheit bei erwachsenen Patienten mit Schizophrenie oder bipolarer Störung. Die Patienten sollten unmittelbar nach der Kontrolle von akuten Agitationssymptomen eine reguläre Behandlung erhalten. |
Antipsychotikum zur Inhalation Es wird vermutet, dass die Wirksamkeit von Loxapin über einen hoch affinen Antagonismus von D2- und 5-HT2A-Rezeptoren vermittelt wird. Loxapin bindet an noradrenerge, histaminerge und cholinerge Rezeptoren, und sein pharmakologisches Wirkungsspektrum kann durch seine Wechselwirkung mit diesen Systemen beeinflusst werden. |
Wurde ursprünglich von Trommsdorff angeboten, das zur spanischen Ferrer-Gruppe gehörte. Nach dem Verkauf von Trommsdorff Ende 2017 an Dermapharm werden die Klinikprodukte und Spezialpräparate von der neu gegründeten Ferrer Deutschland GmbH vertrieben |
|
2013 |
Lisdexamfetamin |
Elvanse |
Shire |
Behandlung der Aufmerksamkeitsdefizit-/Hyperaktivitätsstörung (ADHS) im Rahmen einer Gesamtstrategie bei Kindern ab sechs Jahren, die unzureichend auf Methylphenidat angesprochen haben |
Psychostimulans (Prodrug) Wird nach oraler Gabe im Magen-Darm-Trakt schnell resorbiert und zu Dexamfetamin hydrolysiert, das für die Wirksamkeit des Arzneimittels verantwortlich ist. Der Wirkungsmechanismus von Amfetaminen bei ADHS ist nicht vollständig geklärt. Es wird jedoch angenommen, dass eine Blockade der Wiederaufnahme von Noradrenalin und Dopamin in das präsynaptische Neuron und eine vermehrte Freisetzung dieser Monoamine in den extraneuronalen Raum stattfindet. |
|
|
2013 |
Nalmefen |
Selincro |
Lundbeck |
Zur Reduktion des Alkoholkonsums bei erwachsenen Patienten mit Alkoholabhängigkeit, deren Alkoholkonsum sich auf einem hohen Risikoniveau befindet |
Selektiver Opioid-Rezeptorligand mit antagonistischer Aktivität am My- und Delta-Rezeptor und mit partieller agonistischer Aktivität am Kappa-Rezeptor |
|
|
2013 |
Vortioxetin |
Brintellix |
Lundbeck |
Behandlung von Episoden einer Major Depression bei Erwachsenen |
Antidepressivum Wirkt antagonistisch an den Serotoninrezeptoren 5-HT3- und 5-HT7 und agonistisch an 5-HT1A und 5-HT1B. Zusätzlich hemmt Vortioxetin den Serotonin-Transporter (SERT). |
Der Vertrieb wurde zum 15. August 2016 eingestellt, da sich der Hersteller nach der Entscheidung des G-BA außerstande sah, das Präparat in Deutschland kostendeckend anzubieten. Es ist aber nach wie vor zugelassen und verkehrsfähig und kann über internationale Apotheken bezogen werden. |
|
2013 |
Aripiprazol-Depotformulierung |
Abilify Maintena |
Otsuka |
Erhaltungstherapie von Schizophrenie bei erwachsenen Patienten, die stabil mit oral angewendetem Aripiprazol eingestellt wurden |
Atypisches Antipsychotikum Partieller Dopaminagonist |
|
|
2014 |
Lurasidon |
Latuda |
Takeda |
Behandlung der Schizophrenie bei Erwachsenen |
Antipsychotikum Selektiver Inhibitor dopaminerger und monoaminerger Effekte. Bindet stark an D2-, 5-HT2A- und 5-HT7-Rezeptoren. Blockiert auch alpha2C-adrenerge und alpha2A-adrenerge Rezeptoren. Lurasidon besitzt einen partiellen Agonismus am 5-HT1A-Rezeptor. Es bindet nicht an histaminerge oder muskarinerge Rezeptoren. |
Nach G-BA-Beschluss kein Zusatznutzen. Der Hersteller nahm das Präparat am 01.03.2015 vom deutschen Markt. Im ärztlich begründeten Einzelfall können Patienten auch von der GKV die Kostenerstattung nach Antrag gegebenenfalls erhalten, das Präparat ist als EU-Import (z. B. Dänemark) weiterhin erhältlich. |
|
2015 |
Guanfacin |
Intuniv |
Shire |
Behandlung des Aufmerksamkeitsdefizit-/Hyperaktivitäts-Syndroms (ADHS) bei Kindern und Jugendlichen im Alter von 6 bis 17 Jahren, für die Stimulanzien nicht angezeigt oder nicht wirksam sind. Guanfacin muss als Teil eines Gesamtprogramms angewendet werden, das normalerweise psychologische, erzieherische und soziale Maßnahmen beinhaltet. |
Selektiver Alpha2A-Adrenozeptoragonist, der Signalwege im Gehirn modulieren soll, die für ADHS-assoziierte Symptome verantwortlich sind. Guanfacin war in den 80er-Jahren als Antihypertonikum (Estulic, Novartis, Wander) im Handel. Der Wirkungsmechanismus bei ADHS ist nicht vollständig geklärt. Präklinische Forschungen deuten darauf hin, dass Guanfacin die Signalübertragung im präfrontalen Kortex und in den Basalganglien durch eine direkte Modifikation der synaptischen Noradrenalin-Übertragung an den alpha2-adrenergen Rezeptoren verändert |
Seit 2009 in den USA zugelassen |
|
2016 |
Milnacipran |
Milnaneurax |
Neuraxpharm |
Behandlung von Episoden einer Major Depression bei Erwachsenen |
Antidepressivum Dualer Wiederaufnahmehemmer von Serotonin (5-HT) und Noradrenalin (NA). Im Gegensatz zu vielen trizyklischen Antidepressiva hat Milnacipran keine Affinität zu Alpha1-Adrenorezeptoren oder H1-Rezeptoren. |
Seit 1998 in Österreich verfügbar |
|
2016 |
Pitolisant |
Wakix |
Bioprojet |
Behandlung der Narkolepsie mit oder ohne Kataplexie bei Erwachsenen |
Starker, oral wirksamer H3-Rezeptor-Antagonist/inverser Agonist des H3-Rezeptors, der mittels Blockierung der Histamin-Autorezeptoren die Aktivität von histaminergen Neuronen im Gehirn, einem wichtigen Erregungssystem mit weitläufigen Projektionen in das gesamte Gehirn, verstärkt. Darüber hinaus moduliert Pitolisant verschiedene Neurotransmittersysteme und erhöht dadurch die Ausschüttung von Acetylcholin, Noradrenalin und Dopamin im Gehirn |
|
|
2016 |
Paliperidonpalmitat (LAI-Depot 3 Mon) |
Trevicta |
3-Monats Depot-Antipsychotikum Erhaltungstherapie bei erwachsenen Patienten, die klinisch stabil auf Xeplion eingestellt wurden |
Atypisches Antipsychotikum |
Umbenennung von Paliperidon Janssen, das bereits 2014 zugelassen, aber nicht auf den Markt gebracht wurde |
|
|
2017 |
Cariprazin |
Reagila |
Gedeon Richter |
Behandlung von Schizophrenie bei Erwachsenen |
Antipsychotikum, atypisches Neuroleptikum Wirkt möglicherweise über eine Kombination aus einer partialagonistischen Aktivität an den D3-, D2- und 5-HT1A-Rezeptoren und einer antagonistischen Aktivität an den 5-HT2B-, 5-HT2A- und H1-Rezeptoren. Cariprazin weist eine niedrige Affinität zu den 5-HT2C-Rezeptoren und den Alpha1-Adrenozeptoren auf. Es besitzt keine nennenswerte Affinität zu cholinergen Muskarinrezeptoren. Die beiden aktiven Hauptmetaboliten, Desmethylcariprazin und Didesmethylcariprazin, besitzen in vitro ein ähnliches Rezeptorbindungs- und funktionelles Aktivitätsprofil wie die Muttersubstanz. |
5-HT: Serotonin; D: Dopamin; H: Histamin; NaSSA: noradrenerges und spezifisch serotonerges Antidepressivum; SSNRI: selektiver Serotonin- und Noradrenalin-Wiederaufnahmehemmer; SSRI: selektiver Serotonin-Wiederaufnahmehemmer
Viele pharmazeutische Unternehmen, die Psychopharmaka vertrieben haben, sind vom Markt verschwunden – erinnert sei an bekannte Namen wie Tropon, Ciba-Geigy, Promonta, Hoechst, Sandoz, Rhone-Poulenc, Organon, Duphar, Galenus oder Wyeth.
Innovationen oder „Me-too“?
Bschor stellt fest, dass es seit dem Gründerjahrzehnt 1949 bis 1960 keine bahnbrechenden Entwicklungen mehr gegeben habe, die Risiken der Pharmakotherapie seien immer deutlicher geworden, falsche ökonomische Anreize hätten Unternehmen auf Scheininnovationen setzen lassen [2].
Gemäß GKV-Arzneimittelschnellinformationssystem und Arzneiverordnungsreport werden die Begriffe Me-too-Präparat, Analogpräparat, Schritt- und Scheininnovationen synonym gebraucht und definiert als Präparate mit Wirkstoffen, die keinen oder nur marginale Unterschiede zu bereits eingeführten Wirkstoffen aufweisen. 2006 wurden im Gefolge des Arzneimittelbudget-Ablösungsgesetzes die jährliche Arzneimittelvereinbarungen festgelegt, wonach der durch den Vertragsarzt verursachte Arztgruppen-bezogene Verordnungsanteil des Bruttoumsatzes der Me-too-Präparate um fünf Prozentpunkte zu reduzieren sei [5]. Bei Inkrafttreten der Zielvereinbarung umfasste die Liste der Me-too-Präparate unter anderem Escitalopram, Reboxetin, Rivastigmin, Dosulepin, Pregabalin, Zotepin, Risperidon, Quetiapin, Zaleplon, Venlafaxin, Ziprasidon, Olanzapin und Aripiprazol [7, 8]. 2007 wurde die Me-too-Quote in der Verschreibungspraxis der deutschen Psychiater mit 13,8 % angegeben. 2008 diskutierten Möller und Fritze in der PPT die Problematik von Me-too-Listen unter der Überschrift „(irrationale) Rationierung von Psychopharmaka im deutschen Gesundheitssystem“ [20], die Problematik der „Me-too“-Definition und der Zusatznutzenbewertung wurde von Möller in der PPT ausführlich dargelegt [18, 19].
Entwicklungen zu Klassifikation – Einteilung
Mit der Einführung zahlreicher Antidepressiva fand für die Verordnungspraxis das in den 70er-Jahren entwickelte Kielholz-Schema weite Verbreitung. 1995 stellten Rüther et al. das Asolo-Schema zur multidimensionalen Klassifizierung der Antidepressiva vor [3, 25]. Von internationalen psychopharmakologischen Fachgesellschaften wurde vor Kurzem eine neue Nomenklatur für Psychopharmaka vorgeschlagen, die Probleme der bisherigen indikationsbezogenen Terminologie umgehen soll (z. B. werden Antidepressiva nicht nur zur Therapie von Depressionen eingesetzt) und an pharmakologischen Wirkorten/Wirkungsmechanismen orientiert ist [21].
PPT
Sämtliche neu in Deutschland zugelassenen Psychopharmaka wurden in der PPT in pharmakologischen und klinischen Übersichtsarbeiten ausführlich und differenziert vorgestellt. Mit der gewachsenen Zahl zur Verfügung stehender Psychopharmaka stellte sich immer mehr die Frage von Differenzialindikationen, einer differenzierten Psychopharmakotherapie. Dieser Frage hat die PPT diverse Themenschwerpunkte gewidmet. Für Therapiewahlentscheidungen wurde ein Therapiewahlfragebogen in der PPT vorgestellt [17]. Die PPT der letzten Jahre konzentrierte sich angesichts der geringen Zahl „neuer“ Psychopharmaka auf Kombinations- und Add-on-Therapien (z. B. Quetiapin bei therapieresistenter Depression) sowie das Problem des Off-Label-Use: In der PPT wurde 2011 eine diesbezügliche Übersichtspublikation zum Thema zugelassene Indikationen publiziert [10, 30]. Weitere Themen waren Hirndoping – Neuroenhancement [29], das therapeutische Drug-Monitoring mit aktualisierten Konsensus-Leitlinien [9] und die vermehrte Beachtung unerwünschter Arzneimittelwirkungen.
Zunehmende Beachtung fand die Fahrtauglichkeit unter Psychopharmaka, hier wurden erhobene klinische Patientendaten unter Antidepressiva und Antipsychotika publiziert [15]. Die Problematik der frühen Zusatznutzenbewertung von Arzneimitteln (AMNOG-Verfahren) wurde in der PPT 2015 dargestellt [19]. Ein Schwerpunktheft widmete sich 2015 dem Thema „Psychopharmaka in der Schwangerschaft“.
2012 debattierte das British Journal of Psychiatry über die „Identitätskrise der Psychiatrie“ weiter. Immer mehr geriet die Psychopharmakologie gerade in Deutschland „ins Abseits“ [12]. Die neue Berufsrolle des Facharztes für Psychiatrie und Psychotherapie wird nun berufspolitisch hauptsächlich im Feld der Psychotherapie gesehen. Damit droht psychopharmakotherapeutische Kompetenz verloren zu gehen. Mit Heft 6/2017 wurde deshalb in der PPT ein Weiterbildungscurriculum Psychopharmakologie, Pharmakotherapie begonnen, um den Stellenwert der Psychopharmakotherapie zu unterstreichen und den Wissensstand gerade für den Nachwuchs zu verbessern [13].
Pharmakoökonomie
Schon 1994 wies Fritze darauf hin, dass der psychopharmakologische Forschungsstandort Deutschland durch Kostendämpfungsmaßnahmen im Gesundheitssystem gefährdet sei. Angesichts der ökonomischen und wissenschaftlichen Bedingungen verlagere die forschende pharmazeutische Industrie ihre Aktivitäten zunehmend ins Ausland [4]. 1998 wurden mit dem GKV-Solidaritätsstärkungsgesetz wieder Budgets neben den gesetzlich vorgeschriebenen Richtgrößen eingeführt. Daraufhin empfahlen kassenärztliche Vereinigungen die strikte Beachtung von Negativlisten und generell die Verordnung der billigsten Generika. Zur Orientierung wurden fragwürdige Listen neuer Wirkstoffe angeboten, von denen die Mehrzahl als Me-too-Drugs klassifiziert wurden [7, 8]. Aus heutiger Sicht bemerkenswert sind die im Jahr 2000 von einem interdisziplinär besetzten Expertengremium formulierten „Berliner Empfehlungen“ zur Beseitigung des Behandlungsnotstands angesichts der durch Richtgrößenverordnung limitierten Verordnung teurerer atypischer Antipsychotika. 2002 änderte der Bundesausschuss der Ärzte und Krankenkassen die Arzneimittelrichtlinien bezüglich atypischer Neuroleptika und äußerte dazu, dass der generelle Einsatz der mit sehr viel höheren Kosten verbundenen atypischen Neuroleptika bei der Behandlung schizophrener Patienten medizinisch nicht gerechtfertigt sei. Hierzu erfolgte in der PPT 2003 eine Stellungnahme der DGPPN und der AGNP – die wissenschaftlichen Fachgesellschaften gehörten ausdrücklich nicht zu den Anhörungsberechtigten [8]. Fritze kommentierte dies in der PPT zu Recht mit einem „Aushebeln des Anspruchs auf Therapie gemäß des Standes der Wissenschaft durch Zielvereinbarungen“ [5]. 2007 konstatierte Schwerdtfeger, seinerzeit Leiter der Unterabteilung „Arzneimittel, Apotheken“ im Bundesministerium für Gesundheit, dass Arzneimittel, die innerhalb der letzten fünf Jahre in Deutschland auf den Markt gekommen sind und neuartige Wirkstoffe enthalten, am Gesamtmarkt nur einen Anteil von etwa 8,5 % ausmachen – im europäischen Vergleich der mit Abstand niedrigste Wert.
Nota: Die Tagestherapiekosten für ein Antidepressivum oder Antipsychotikum (95 % Generikums-Markt, niedergelassene Kollegen verordnen automatisch per Computerprogramm das billigste Präparat) liegen bei etwa 30 Cent. Kann so eine Therapie bei den Beteiligten eine „Wertschätzung“ erfahren?
Laut aktuellem Arzneiverordnungs-Report haben Generika heute einen Verordnungsanteil von 88 %, patentgeschützte Arzneimittel werden immer seltener verordnet und liegen bei etwa 6 % [26]. Immer wieder wurde auf Risiken bei der Umstellung von Originalpräparaten auf Generika auch im Rahmen psychopharmakologischer Behandlungen hingewiesen [28]. Fallbeispiele aus der täglichen Praxis belegen die Risiken einer Generikasubstitution auch unter dem Aspekt der Compliance, problematisch sind in diesem Zusammenhang die Rabattverträge. Bis heute wichtig ist hierbei der Hinweis, dass der Nachweis der therapeutischen Äquivalenz mittels klinischer Studien mit Patienten nicht erforderlich ist.
Aufgrund ökonomischer Kalkulationen wurden in Deutschland das neue multimodale Antidepressivum Vortioxetin sowie das Antipsychotikum Lurasidon nicht eingeführt – ihnen wurde vonseiten des Gemeinsamen Bundesausschusses (G-BA) kein Zusatznutzen attestiert. Jüngst finden sich etwas andere Töne: Zehn Jahre nach Einführung der Arzneimittelrabatte sparen die Krankenkassen im Sinne der vom Gesetzgeber auferlegten WANZ-Regel (wirtschaftlich, ausreichend, notwendig, zweckmäßig) Milliardensummen. Nun haben Arzneimittel-Lieferengpässe aufgezeigt, dass Marktkonzentrationen und industrielle Rationalisierungsprozesse Vorkehrungen fordern, um Engpässen entgegenzuwirken. Hinzu kommen Qualitäts-Unsicherheiten ausländischer Produktionsstätten (vgl. Valsartan-Skandal). Man liest nun auch, dass das Statement, im internationalen Pharmamarkt werde zu viel Geld verdient, eine kaum beweisbare Pauschalplattitüde sei. Auch der Vorsitzende der pharmakritischen Arzneimittelkommission der Deutschen Ärzteschaft erläutert, dass die Preise, die derzeit für Medikamente erzielt werden, eindeutig zu niedrig sind, um einen gewissen Gewinn abzuwerfen und äußerte die Befürchtung, dass so niedrige Preise gleichermaßen Produzenten, Forschung und Entwicklung demotivieren.
Ausblick
Die teure, komplizierte und sehr aufwendige Forschung im Bereich der Psychopharmaka wurde von vielen pharmazeutischen Unternehmen aufgegeben. Demgegenüber stehen verschiedene „Unmet needs“, unter anderem die Wirklatenz der bislang verfügbaren Antidepressiva. Perspektivisch lassen weitere Substanzen mit den bekannten Wirkungsmechanismen (z. B. dopaminerge bzw. serotonerge Neurotransmission) keinen Fortschritt erwarten. Interessant können neue Ansätze wie der nichtkompetitive NMDA-Rezeptorantagonist Ketamin und das in Kürze verfügbare intranasale Esketamin sowie glutamaterge Mechanismen und metabotrope Glutamatrezeptoren (mGluR) sein [1]. Die Entwicklung völlig neuer Wirkungsansätze (Immunsystem, Antikörper) impliziert angesichts fehlender valider Tiermodelle, aufwendiger Forschungsstrategien bedingt durch die Komplexität des menschlichen Gehirns und langwieriger Studien- und Zulassungsverfahren einen längeren Zyklus, sodass in absehbarer Zeit nicht mit der Einführung innovativer Psychopharmaka zu rechnen sein dürfte.
Danksagung
Ich danke den Chefredakteurinnen der PPT, Dr. Susanne Heinzl (1994–2007) und Dr. Heike Oberpichler-Schwenk (seit 2008), für die langjährige gute Zusammenarbeit und für die Unterstützung bei der Recherche für den vorliegenden Beitrag.
Interessenkonflikterklärung
GL erhielt Honorare für Vorträge und Beratungen oder unbeschränkte Subventionen für Schulungen von Bayer, Janssen-Cilag, Lundbeck, Pfizer und Servier.
Literatur
1. Artigas F. Development in the field of antidepressants, where do we go now? Eur Neuropsychopharmacol 2015;25:657–70.
2. Bschor T. 66 Jahre moderne Psychopharmakotherapie. Das Gründerjahrzehnt und der heutige (Still-)Stand. Nervenheilkunde 2015;34:710–4.
3. Dieterle D, Scherer J, Rüther E. Beurteilung von Antidepressiva mit dem Asolo-Schema. I. Psychopathologische Ergebnisse. Psychopharmakotherapie 1995;2:165–9.
4. Fritze J. Klinische Forschung in der Psychopharmakologie. Psychopharmakotherapie 1994;1:57–9.
5. Fritze J. Aushebeln des Anspruchs auf Therapie gemäß des Standes der Wissenschaft durch Zielvereinbarungen? Psychopharmakotherapie 2006;13:212–3.
5a. Fritze J. Verordnung von Neuro-Psychopharmaka. Anmerkungen zum Arzneiverordnungsreport 2018. Psychopharmakotherapie 2019;26:39–41.
6. Fritze J, Aldenhoff J. Klinische Forschung in der Psychopharmakologie. II. Erreichte Qualität der Psychopharmakotherapie und Bedarf an Innovation: Antipsychotische und nootropische Substanzen. Psychopharmakotherapie 1994;1:117–21.
7. Fritze J, Möller HJ, Saß H, Gastpar M. Der Budgetdruck ist in vollem Gange – und die Folgen? Psychopharmakotherapie 1999;6:72–4.
8. Fritze J, Schmauß M, Holsboer F. Änderung der Arzneimittel-Richtlinien des Bundesausschusses der Ärzte und Krankenkassen bezüglich atypischer Neuroleptika. Stellungnahme der DGPPN und der AGNP. Psychopharmakotherapie 2003;10:72–4.
9. Hefner G, Laux G, Baumann P, et al. Konsensus-Leitlinien für therapeutisches Drug-Monitoring in der Neuropsychopharmakologie; Update 2017. Psychopharmakotherapie 2018;25:92–140.
10. Jandl N, Baumhauer-Gessler H, Kaschka WP, Steinert T. Arzneimittelzulassungen und Off-Label-Use bei Psychopharmaka. Psychopharmakotherapie 2011;18:220–6.
11. Laux G. 10 Jahre PPT – eine Dekade zahlreicher Psychopharmaka-Innovationen. Psychopharmakotherapie 2003;10:131.
12. Laux G. Psychopharmakologie im Abseits. Die neue Berufsrolle des Facharztes für Psychiatrie und Psychotherapie. Psychopharmakotherapie 2012;19: 271–4.
13. Laux G. Vorschlag eines Psychopharmakologie-Pharmakotherapie-Curriculums für die neue Weiterbildungsordnung Fach Psychiatrie und Psychotherapie. Psychopharmakotherapie 2014;21:64–8.
14. Laux G. Verordnung von typischen und atypischen Antipsychotika (FGA, SGA) nach Versorgungs-Sektoren. Psychopharmakotherapie 2016;23:67–72.
15. Laux G, Brunnauer A. Fahrtauglichkeit unter Antidepressiva. Psychopharmakotherapie 2015;22:335–41.
16. Linde OK (Hrsg.). Pharmakopsychiatrie im Wandel der Zeit. Klingenmünster: Tilia-Verlag Mensch und Medizin, 1988.
17. Linden M. Begründungen von Ärzten für die Auswahl eines Arzneimittels. Der Therapiewahlfragebogen. Psychopharmakotherapie 2004;11:76–9.
18. Möller HJ. Die Problematik der „me-too“-Definition im Kontext der Psychopharmakologie. Psychopharmakotherapie 2007;14:227–8.
19. Möller HJ. Zusatznutzen-Bewertung: Probleme für Entwicklung/Inverkehrbringen GKV-verschreibungsfähiger neuer Psychopharmaka. Psychopharmakotherapie 2015;22:59–64.
20. Möller HJ, Fritze J. (Irrationale) Rationierung von Psychopharmaka im deutschen Gesundheitssystem. Zur Problematik von „me-too“-Listen. Psychopharmakotherapie 2008;15:30–5.
21. Möller HJ, Kasper S. Neurosciene based Nomenclature (NbN) für Psychopharmaka – eine wichtige neue Entwicklung. Psychopharmakotherapie 2017;24:2–6.
22. Preskorn SH. CNS drug development. Part I: The early period of CNS drugs. J Psychiatr Pract 2010;16:334–9.
23. Preskorn SH. CNS drug development: Part II: Advances from the 1960s to the 1990s. J Psychiatr Pract 2010;16:413–5.
24. Preskorn SH. CNS drug development. Lessons learned part 3: Psychiatric and central nervous system drugs developed over the last decade – Implications for the field. J Psychiatr Pract 2017;23:352–60.
25. Rüther E, Ahrens B, Dieterle D, Erzigkeit A, et al. Das Asolo-Schema zur therapierelevanten multidimensionalen Klassifizierung der Antidepressiva. Psychopharmakotherapie 1995;2:158–64.
26. Schwabe U, Paffrath E, Ludwig WD, Klauber J (Hrsg.). Arzneiverordnungs-Report 2018. Aktuelle Daten, Kosten, Trends und Kommentare. Berlin: Springer, 2018.
27. Siepmann M, Kirch W. Psychopharmakotherapie im 20. Jahrhundert. Wien Med Wochenschr 2001;151:397–402.
28. Volz HP, Staedt J, Anghelescu IG, Rüther E. Risiken bei der Umstellung von Originalpräparaten auf Generika im Rahmen psychopharmakologischer Behandlungen. Psychopharmakotherapie 2009;16:198–202.
29. Weiergräber M, Broich K. Neuroenhancement – Hirndoping. Psychopharmakotherapie 2019;26: im Druck.
30. Wolter D, Winkler W. Zugelassene Indikationen und Maximaldosierungen in der Psychiatrie. Psychopharmakotherapie 2011;18:164–71.
Prof. Dr. med. Dipl.-Psych. Gerd Laux, Institut für Psychologische Medizin (IPM), Nussbaumstraße 9, 83564 Soyen, Zentrum für Neuropsychiatrie, 84478 Waldkraiburg, E-Mail: ipm@ipm-laux.de
25 years of psychotropics in Germany. Which substances were newly approved and which are still available? An overview
To mark 25 years of PPT, an overview of psychotropic medications in Germany has been compiled. Between 1994 and 2018 a total of 30 substances were approved and put on the market, among them 13 antidepressants and 12 neuroleptic/antipsychotic drugs. Of these 30 substances three are no longer available due to approval expiration related to adverse side effects and also for economic reasons (price regulations by AMNOG/G-BA). Scientific debate argues how many of those drugs are “real innovations” and “me-too compounds”. While in the 1990s the focus was on the development of selective substances (SSRIs, SNRIs, SSNRIs) it has shifted lately to multimodal “dirty drugs”. Newly approved were medications with transdermal or inhalation application or depot delivery of long-acting atypical antipsychotics. At the moment partial dopamine agonists are being expanded and intranasal esketamine will soon be available. No further advances are expected regarding other substances with well-known mechanisms such as dopamine or serotonin neurotransmission. Developing new mechanisms (immune system, antibodies) takes longer because there are no valid animal models and the complexity of the human brain and lengthy approval procedures also require extensive research methods. Therefore, an introduction of new psychotropic substances is not expected in the foreseeable future.
Key words: retrospect, psychotropic history, innovations
Psychopharmakotherapie 2019; 26(01):3-15
