Robert Waltereit, Dresden, und Walter E. Müller, Worms/Frankfurt a.M.
Zu den Stimulanzien zählt man die von der natürlichen Substanz Ephedrin (einem Alkaloid) abgeleiteten Amphetamine und das Methylphenidat, daneben das pharmakologisch, aber nicht strukturell ähnliche Cocain und das auch heute noch nicht klar einordenbare Modafinil. Neben peripheren sympathomimetischen Effekten, die besonders bei Ephedrin ausgeprägt sind, führen die Substanzen zu einer dosisabhängigen spezifischen Aktivierung des ZNS mit Unterdrückung von Müdigkeit und Hungergefühl, Leistungssteigerung, verbesserter Aufmerksamkeit und Konzentrationsfähigkeit, aber auch zu Wohlbefinden, Euphorie und psychotischen Effekten mit dem Risiko der Abhängigkeit (Abb. 4–1). Die letzten Symptome sind von der Geschwindigkeit der zerebralen Verfügbarkeit abhängig und besonders stark bei den sehr lipophilen Amphetaminen, deutlich schwächer bei Methylphenidat und Ephedrin. Die Wirkungen gehen auf eine unterschiedliche Hemmung des neuronalen Rücktransports von Noradrenalin und Dopamin zurück und besonders bei den Amphetaminen auf eine Störung der Speicherfähigkeit der synaptischen Vesikel. Als weitere Substanz wäre das chemisch und auch pharmakologisch etwas abweichende Modafinil zu nennen, das man trotzdem heute zu den Stimulanzien zählt. Da Cocain zwar als Droge mit extrem hohem Abhängigkeitspotenzial auch heute noch sehr verbreitet ist, aber als Arzneisubstanz keine Rolle mehr spielt, soll es nur im Hinblick auf den Wirkungsmechanismus erwähnt werden. Schwerpunkt der Ausführungen sind die Amphetamine und Methylphenidat und ihre wesentliche Rolle in der Therapie von ADHS (Aufmerksamkeitsdefizit-/Hyperaktivitätsstörung; Tab. 4–1). Erwähnt werden daher auch Atomoxetin und Guanfacin als nicht zu den Stimulanzien zählende Wirkstoffe zur Behandlung der ADHS.
Tab. 4–1. Psychostimulanzien, die für die Behandlung der Aufmerksamkeitsdefizit-/Hyperaktivitätsstörung (ADHS) zugelassen sind
|
Substanz |
Handelsname® |
Wirkdauer |
Zulassung für Erwachsene |
|
Methylphenidat (unretardiert) |
Ritalin |
1–4 h |
Nein |
|
Retardiertes Methylphenidat |
Equasym retard |
7–8 h |
Nein |
|
Medikinet retard/ |
6–8 h |
Ja |
|
|
Ritalin LA/Ritalin adult |
6–8 h |
Ja |
|
|
Concerta |
9–12 h |
Weiterverordnung |
|
|
Kinecteen |
9–12 h |
Nein |
|
|
Dexamfetamin |
Attentin |
4–6 h |
Nein |
|
Lisdexamfetamin |
Elvanse |
12–14 h |
Weiterverordnung |

Abb. 4–1. Dosisabhängige zentrale Effekte von Stimulanzien (Amphetamine, Cocain). Die Intensität der zentralen Effekte hängt von der Geschwindigkeit und dem Ausmaß der Penetration ins ZNS ab, deutlich bei Amphetaminen und Cocain, geringer bei Methylphenidat und Ephedrin. Im Fall von Methylphenidat muss man beachten, dass die Effekte auf die Dopaminrückaufnahme eher bei niedrigeren Dosen auftreten als die Effekte auf den Noradrenalintransporter. Bei ADHS ist eine wahrscheinliche dopaminerge Dysfunktion auch mit der Hyperaktivität verbunden, sodass Methylphenidat in diesem Fall durch eine Normalisierung der dopaminergen Neurotransmission paradoxerweise aktivitätsreduzierend wirkt.
Pharmakologie als Grundlage der Anwendung bei ADHS
Amphetamin-Derivate
Es gilt heute als sicher, dass die klinische Wirksamkeit der Stimulanzien auf eine Beeinflussung des Stoffwechsels von Noradrenalin und vor allen Dingen Dopamin zurückgeht, während die serotonerge Neurotransmission unter therapeutischen Bedingungen eher nicht relevant beeinflusst wird (im Gegensatz zu psychotomimetischen Effekten beim Missbrauch hoher Dosen). Der spezifische Effekt auf die noradrenerge und dopaminerge Neurotransmission geht auf eine Hemmung der Transportproteine zurück, die die präsynaptisch freigesetzten Neurotransmitter in die Synapse zurückpumpen (Abb. 4–2).
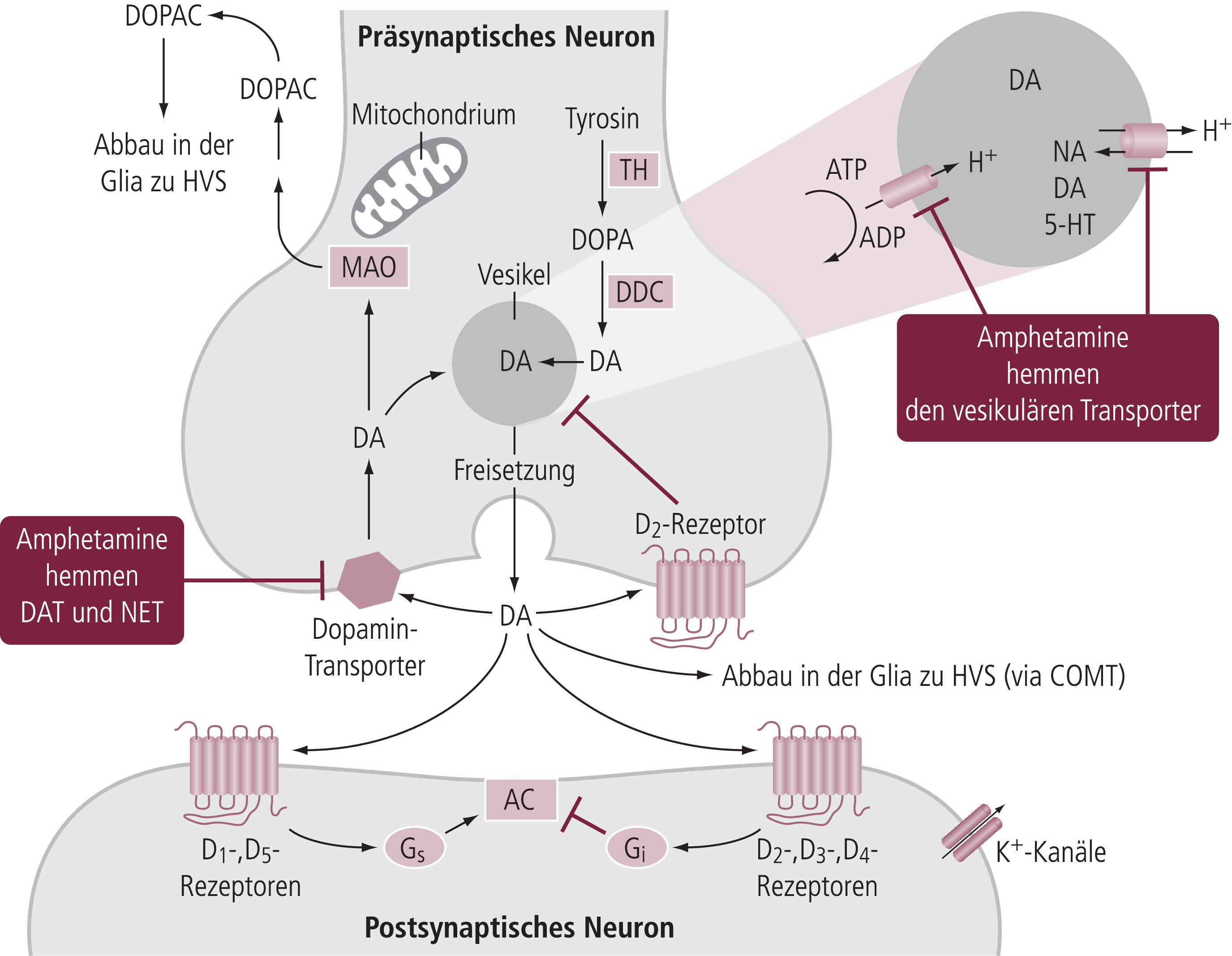
Abb. 4–2. Modell einer dopaminergen Synapse des ZNS. Die Inaktivierung von Dopamin (DA) an der Synapse wird hier im Wesentlichen durch den Rücktransport ins präsynaptische Neuron über den Dopamintransporter (DAT) bewirkt. Der DAT wird durch Methylphenidat stärker als durch Amphetamine gehemmt. Monoaminoxidase (MAO) kann zusätzlich intraneuronal Dopamin abbauen. Amphetamine, nicht aber Methylphenidat können darüber hinaus aus der Präsynapse Dopamin in den synaptischen Spalt unabhängig von einem Nervenimpuls freisetzen, ausgelöst über eine Störung der Speicherfähigkeit der Vesikel durch ihren Hemmeffekt auf den vesikulären Transporter. Dieses Wirkprinzip ist an der noradrenergen Synapse sehr ähnlich, da hier die gleichen vesikulären Transporter vorliegen. Der Noradrenalintransporter (NET) unterscheidet sich dagegen sehr deutlich vom DAT, was die unterschiedliche Hemmung beider Transporter durch Amphetamin und Methylphenidat erklärt. AC: Adenylatcyclase; COMT: Catechol-O-Methyltransferase; DDC: Dopadecarboxylase; DOPAC: Dihydroxyphenylessigsäure; HVS: Homovanillinsäure; 5-HT: Serotonin; NA: Norardenalin; TH: Tyrosinhydroxylase
Während das natürliche Vorbild Ephedrin noch sehr viel stärker den Noradrenalintransporter (NET) als den Dopamintransporter (DAT) hemmt, hemmen die Amphetamine den DAT fast so stark wie den NET, was zusammen mit der extrem schnellen Aufnahme ins Gehirn aufgrund der hohen Lipophilie das wesentlich größere Abhängigkeitspotenzial erklärt. Die beim chronischen Missbrauch häufig auftretenden psychotomimetischen Symptome gelten als klassisches Modell für dopaminerge Psychosen.
Der Effekt auf den DAT ist bei Dexamfetamin deutlicher als bei den anderen Amphetamin-Isomeren, sodass diese Substanz heute in der Therapie bevorzugt wird. Es steht auch Lisdexamfetamin zur Verfügung, ein Prodrug mit protrahierter Wirkung durch den langsamen Abbau der Muttersubstanz im Blut zu Dexamfetamin. Racemisches Amphetamin spielt heute in der Therapie keine Rolle mehr.
Methylphenidat (MPH)
Methylphenidat (MPH) ist nicht nur hydrophiler als Amphetamin und wird deshalb deutlich langsamer ins ZNS aufgenommen, sondern es unterscheidet sich auch pharmakologisch deutlich von den Amphetaminen. Bei MPH steht eine Beeinflussung des Dopamintransporter (DAT) im Vordergrund, den es stärker hemmt als den Noradrenalintransporter (NET). Die Blockade des DAT führt hier in direkter Korrelation zur Plasmakonzentration und zur Okkupation des DAT im Gehirn zu den positiven Effekten auf alle Komponenten der Psychopathologie von ADHS. Diese sehr enge Beziehung zwischen Dosis, Plasmakonzentration und der akuten Okkupation, Bindung des pharmakologischen Targets mit der therapeutischen Wirkung ist in der Psychopharmakotherapie sehr untypisch. Dies schließt allerdings nicht aus, dass auch sekundäre kompensatorische Effekte auftreten, diese scheinen aber für die hervorragende Beziehung zwischen Plasmakonzentration und Wirkung eher von untergeordneter Bedeutung zu sein, während sie bei Atomoxetin (siehe später) wohl eine wesentliche Rolle spielen.
MPH unterscheidet sich aber noch in einem anderen Aspekt von den Amphetaminen: Während diese deutlich die Speicherfähigkeit der synaptischen Vesikel reduzieren können, wobei eine direkte Hemmung des vesikulären Transporters (Abb. 4–2), aber auch noch andere Mechanismen eine Rolle spielen, zeigt MPH diese Effekte deutlich weniger, sodass es weniger die Impuls-unabhängige Transmitterfreisetzung stimuliert. Dies spielt sicher auch eine Rolle für das geringere Abhängigkeitspotenzial von MPH, wohingegen der akute „Kick“ bei Amphetaminen (schnelle ZNS-Aufnahme und massive Erhöhung der synaptischen Dopamin-Konzentration durch vesikuläre Freisetzung und Transporter-Hemmung) größer ist. Bei chronischem Missbrauch kann es über diesen Mechanismus – die Verringerung der vesikulären Speicherfähigkeit – zu einem plötzlichen Wirksamkeitsverlust kommen, da in den Nervenendigungen zu wenig gespeicherter Transmitter vorhanden ist. Diese Art von Toleranz wird als Tachyphylaxie bezeichnet. Auch das massive Erschöpfungssyndrom, das nach einer Periode von Hochdosis-Amphetamin-Missbrauch auftreten kann und lebensbedrohlich ist, geht unter anderem auf diesen Mechanismus (auch in der Peripherie?) zurück.
Methylphenidat hat bei Therapien von ADHS eine dominierende Rolle. Diese wurde in den zurückliegenden zehn Jahren noch durch die Verfügbarkeit von verzögert freisetzenden Präparaten verbessert, die den wesentlichen pharmakokinetischen Nachteil der Substanz, die kurze Halbwertszeit, ausgleichen, sodass die störende, bei einigen Patienten notwendige 2- bis 3-malige Einnahme über den Tag nicht mehr erforderlich ist. Die sehr gute Wirksamkeit von Methylphenidat ist bestens belegt. Mit Effektstärken von 1 oder knapp darüber und NNT-Werten (Number needed to treat) von etwas über 2 nimmt Methylphenidat innerhalb der Psychopharmaka eine herausragende Stellung ein. Darüber hinaus ist seine Wirkung hervorragend steuerbar. Plasmakonzentration und Target-Bindung im zentralen Nervensystem (Dopamintransporter) sind direkt assoziiert. Die Substanz kann problemlos abgesetzt werden und führt beim Neuansetzen in der Regel zu gleichen Effekten; in ihrer Langzeitwirkung ist sie für mindestens ein Jahr belegt. Es gibt kein einziges Psychopharmakon, dessen Wirkung so klar und so zeitlich umrissen mit Plasmakonzentration und Target-Bindung assoziiert ist, wie Methylphenidat. Das Nebenwirkungsprofil von Methylphenidat ist sehr gut bekannt und daher trotz gewisser Probleme beherrschbar. Wie alle Stimulanzien kann auch Methylphenidat eine Abhängigkeit auslösen, obwohl bei ADHS-Patienten dieses Problem praktisch keine Rolle spielt.
Als Alternative stehen Dexamfetamin und sein Prodrug Lisdexamfetamin zur Verfügung. Dexamfetamin wird allerdings in den USA sehr viel häufiger benutzt als in Europa, wo es eher eine untergeordnete Rolle spielt. Es ist seit Kurzem auch als Fertigpräparat in Deutschland verfügbar. Da Dexamfetamin und Methylphenidat pharmakologisch nicht identisch sind, ist ein Therapieversuch mit (Lis-)Dexamfetamin, bei Patienten, die schlecht auf Methylphenidat ansprechen, durchaus sinnvoll.
Andere, auch bei ADHS verwendete Substanzen mit ähnlichem Wirkungsmechanismus
Als Alternative für Stimulanzien oder bei vorliegenden Kontraindikationen (Abhängigkeitspatienten) für die Stimulanzientherapie stehen als zugelassene Medikation Atomoxetin aus der Gruppe der selektiven Noradrenalin-Wiederaufnahmehemmer und der Alpha2-Agonist Guanfacin zur Verfügung. Die letzte Verbindung geht auf Befunde zurück, dass Alpha2-Rezeptoren im präfrontalen Kortex eine wichtige Rolle in der Regulation kognitiver Funktionen haben.
Atomoxetin ist aus der Entwicklung Transporter-selektiver Antidepressiva hervorgegangen und zeichnet sich als spezifischer Noradrenalin-Wiederaufnahmehemmstoff aus, der im Unterschied zu den älteren Verbindungen wie Desipramin aus der Gruppe der trizyklischen Antidepressiva (die auch bei ADHS eingesetzt wurden) keine zusätzlichen und UAW-relevanten Rezeptor-antagonistischen Eigenschaften aufweist [4].
Da Aufmerksamkeit und andere kognitive Effekte sehr stark vom präfrontalen Kortex gesteuert sind, geht man in der Neurobiologie der ADHS davon aus, dass Verbesserungen dopaminerger Mechanismen im präfrontalen Kortex eine wichtige Rolle für den therapeutischen Ansatz beinhalten (siehe später). Hier konnte für Atomoxetin gezeigt werden, dass, obwohl die Substanz den Dopamintransporter nicht hemmt, Atomoxetin im präfrontalen Kortex auch zu einem extrazellulären Anstieg von Dopamin führt, aber nicht in anderen Hirnarealen, während bei Methylphenidat dieser Effekt Areal-unabhängig ist. Die Erklärung ist darin zu sehen, dass der Noradrenalintransporter nicht sehr selektiv ist und auch relativ gut Dopamin transportieren kann. Im präfrontalen Kortex gibt es fast keine Dopamintransporter, sodass aus dopaminergen Neuronen freigesetztes Dopamin über den Noradrenalintransporter an den Synapsen inaktiviert wird und dabei auch in noradrenerge Neurone aufgenommen wird und wiederum mit einem eigentlich noradrenergen Signal freigesetzt werden kann. Diese Vermischung gilt als Erklärung dafür, dass Atomoxetin, obwohl es nicht direkt den Dopamintransporter beeinflusst, trotzdem im relevanten präfrontalen Kortex die dopaminerge Neurotransmission ähnlich wie MPH beeinflusst.
Für die Blockade des Noradrenalintransporters durch Atomoxetin gibt es keine direkte Beziehung zwischen Konzentration am Wirkort und Effekten auf die Psychopathologie. Die Transporterblockade passiert in wenigen Stunden nach Gabe, die therapeutische Wirkung bildet sich aber erst nach Wochen aus. Analog zum verzögerten Eintritt der Wirkung von Antidepressiva müssen wir davon ausgehen, dass eine ganze Reihe von zwischengeschalteten adaptiven Prozessen möglicherweise funktionelle Adaptionen der Regelkreise im ZNS bewirken, die dann mit einer Latenz von mehreren Wochen langsam eine Verbesserung der ADHS-Symptomatik erreichen [4].
Bupropion ist als Antidepressivum und zur Behandlung des Nikotinentzugs zugelassen. Besonders in den USA gilt es als Reservesubstanz (off Label) für die Therapie von ADHS. Es ist ein schwacher Hemmer von DAT mit relativ geringen Effekten an NET.
Cocain und Modafinil
Modafinil ist bei uns zugelassen zur Behandlung von Hypersomnie bei Narkolepsie ähnlich den Amphetaminen. Für beide Substanzen scheint die Vigilanzerhöhung hier Grundlage der therapeutischen Wirksamkeit zu sein. Der Wirkungsmechanismus von Modafinil ist nicht sicher bekannt, aber es ist auch ein schwacher Hemmstoff des DAT.
Cocain spielt heute keine Rolle mehr als Arzneistoff, wo es allerdings immer nur als Lokalanästhetikum eingesetzt wurde. Es ist ein starker Hemmer von NET und DAT, analog zu den Amphetaminen, hemmt aber im Gegensatz zu den anderen Substanzen auch den Serotonintransporter, was möglicherweise die höhere Tendenz zu psychischen bis psychotischen Effekten bei Abhängigen erklärt.
Neurobiologie von ADHS als Ansatzpunkt der therapeutischen Anwendung von Stimulanzien
Unter den neuropsychiatrischen Erkrankungen zeigt ADHS eine der höchsten genetischen Komponenten mit einer Aufklärung der Gesamtvarianz durch genetische Faktoren von 70 bis 80 %. Die genetische Assoziation ist allerdings auf sehr viele Gene verteilt, sodass kausale Zuordnungen zwischen genetischem Risiko und Entstehung bzw. Verlauf oder sogar Therapie der Erkrankung praktisch nicht möglich sind. Sehr viele Risiko-Gene deuten aber in die Richtung der dopaminergen und noradrenergen Neurotransmission und stehen damit in Einklang mit der Neuropharmakologie der Erkrankung, wo dopaminerge bzw. noradrenerge Mechanismen im Vordergrund stehen [3].
In Analogie zu den genetischen Assoziationen gibt es auch viele neurobiologische Befunde, die auf funktionelle Veränderungen der dopaminergen Neurotransmission bei ADHS hindeuten. Signifikante Erhöhungen der Dichte des Dopamintransporters wurden in vielen, aber nicht allen Untersuchungen gefunden. Die vereinfachte Hypothese einer dopaminergen Störung bei ADHS (erniedrigte synaptische Dopaminkonzentration durch eine vermehrte Wiederaufnahme ins Neuron; siehe Abb. 4–3) muss daher mit Vorsicht gesehen werden, da die Störung auch in anderen Bereichen der dopaminergen Neurotransmission liegen kann. Dies scheint dadurch überlagert zu sein, dass bei Gesunden, aber auch bei Patienten die DAT-Dichte mit zunehmendem Alter deutlich reduziert wird, womit die Nachweisbarkeit von möglicherweise vorhandenen Unterschieden sinkt; das geht parallel mit Befunden, dass mit zunehmendem Alter die ADHS-Symptomatik häufig abklingt. In neueren Untersuchungen wurden darüber hinaus Veränderungen in anderen Bereichen der dopaminergen Neurotransmission, zum Beispiel von verschiedenen Dopaminrezeptoren, gesehen. Trotzdem kann ADHS nicht einfach als dopaminerge Erkrankung erklärt werden, da es durchaus auch Assoziationen mit Genen gibt, deren Produkte im Bereich der noradrenergen, aber auch der serotonergen Neurotransmission lokalisiert sind. Die robuste Assoziation von Bindung an den DAT und therapeutischer Wirksamkeit im Zusammenhang mit den neurobiologischen Befunden legt dennoch nahe, dass Methylphenidat ein dopaminerges Defizit akut kompensiert.
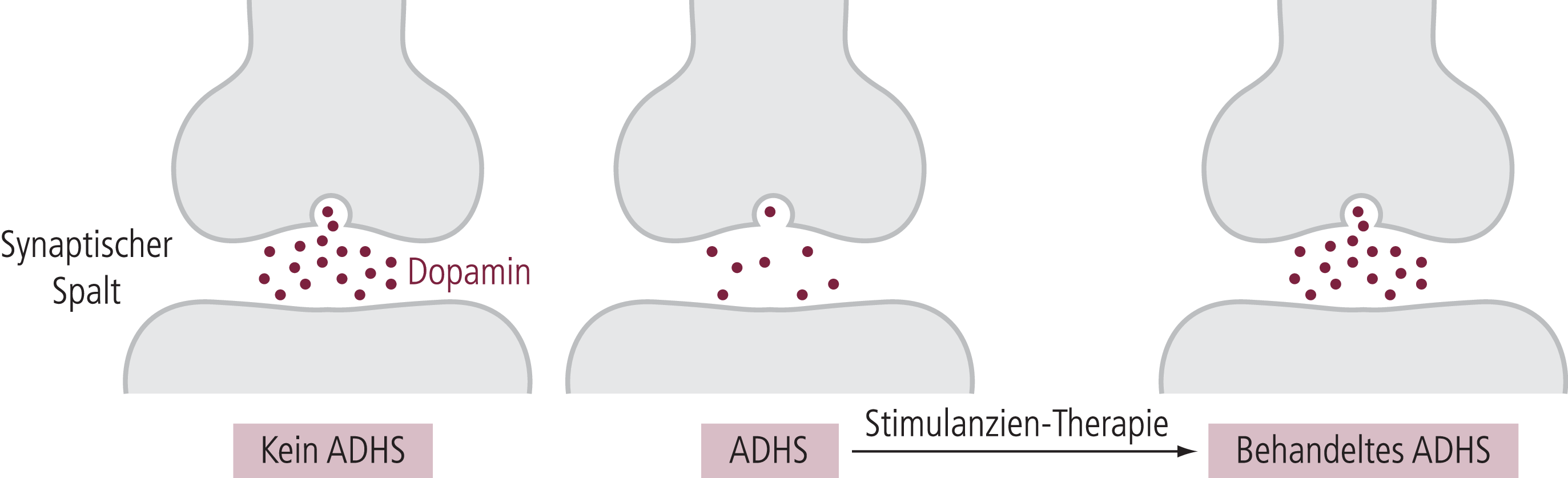
Abb. 4–3. Hypothetisches Modell des durch Methylphenidat normalisierten dopaminergen Defizits bei ADHS
Die Bedeutung der Pharmakokinetik für die therapeutische Wirksamkeit von MPH in der ADHS-Therapie
Wie bereits erwähnt, spielt die Pharmakokinetik bei der Therapie von ADHS mit Methylphenidat eine besondere Rolle, da die Wirkung auf die ADHS-Symptomatik sehr gut mit der Dosis, besser mit den Plasmaspiegeln und noch besser mit dem finalen Wert der DAT-Okkupation im Gehirn korreliert. Bei einer Halbwertszeit von wenigen Stunden bedeutet dies eine Abnahme der Wirkung am späten Vormittag (also noch in der Schule) bei Einnahme am Morgen, was bei vielen Patienten eine zweite Einnahme noch in der Schule erfordert. Dies war mit erheblichen Problemen behaftet (Stigmatisierung, Compliance), kann aber heute durch Retard-Präparate vermieden werden. Diese enthalten in der Regel einen Teil der Substanz schnell freisetzend und den anderen retardiert. Da sich die einzelnen Präparate im Anteil der retardierten Form unterscheiden, kann man durch die individuelle Wahl eines Präparats die Therapie dem individuellen Bedarf des Patienten anpassen (höhere Plasmaspiegel in der Morgenstunde oder in den frühen Nachmittag hinein.
Durch die enge Korrelation zwischen Dosis und Plasmaspiegel sowie die klare Dosis-Wirkungs-Korrelation ergibt sich für Methylphenidat die Möglichkeit des Absetzens und Neuansetzens bei wiederkehrender Wirkung. Es nimmt damit eine Sonderstellung bei der Psychopharmakologie ein. Die besondere Pharmakokinetik von MPH mit langsamer Anflutung im Gehirn selbst noch nach intravenöser Gabe im Vergleich zu Amphetamin und Cocain bewirkt darüber hinaus ein geringeres „High“-Gefühl, was das geringere Abhängigkeitspotenzial erklärt.
Klinische Psychopharmakotherapie von ADHS
Indikationen
Die Indikation für eine Behandlung mit Stimulanzien ist in fast allen Fällen das Vorliegen einer Aufmerksamkeitsdefizit-/Hyperaktivitätsstörung (ADHS). Für das Präparat Ritalin® ist als weitere Indikation die Behandlung der Narkolepsie zugelassen. Im Rahmen individueller Heilversuche werden Stimulanzien gelegentlich in antriebssteigernder Indikation eingesetzt. Ein Einsatz als Appetitzügler ist obsolet. Diese Darstellung fokussiert sich auf die Anwendung von Stimulanzien bei ADHS.
Behandlungsablauf, Medikamentenauswahl, Dosierung
Methylphenidat ist nach Studienlage und klinischen Leitlinien der Goldstandard in der Behandlung der ADHS. Bei der ADHS-Kernsymptomatik, bestehend aus Aufmerksamkeitsstörung, Hyperaktivität und Impulsivität, zeigt Methylphenidat in qualitativ guten Studien hohe Effektstärken von etwa 1,0. Die Effektstärken von Lisdexamfetamin liegen noch höher, in einem sehr hohen Bereich von 1,5. Im Vergleich dazu haben nichtmedikamentöse Therapien, unter Zugrundelegung ähnlich hoher Standards, nur niedrige Effektstärken von etwa 0,3 in Bezug auf die ADHS-Kernsymptomatik. Bei der Therapieplanung muss jedoch berücksichtigt werden, dass der Großteil der ADHS-Patienten unter komorbiden psychischen Störungen leidet. Im Kindes- und Jugendalter können dies eine Störung des Sozialverhaltens, eine Angst- oder eine affektive Störung sein, im Erwachsenenalter auch Persönlichkeitsstörungen oder Suchterkrankungen. Die komorbiden psychischen Störungen werden umgekehrt nicht unbedingt durch eine Therapie mit Stimulanzien beeinflusst und benötigen fast immer einen eigenen, oft nichtmedikamentösen Therapieansatz. Deshalb muss eine Behandlung mit Stimulanzien immer in einen Gesamtbehandlungsplan mit psychosozialen Interventionen eingebunden werden.
Ein Behandlungsversuch mit Stimulanzien setzt voraus, dass die Diagnose einer ADHS korrekt gestellt wurde. Ebenso müssen komorbid vorliegende, andere psychische Störungen zuverlässig erfasst sein. Solange das psychopathologische Bild noch nicht hinreichend verstanden ist, sollte nicht mit einem Behandlungsversuch begonnen werden. Es besteht ansonsten ein hohes Risiko für ein nicht interpretierbares Ergebnis. Die Vorstellung der Findung einer ADHS-Diagnose ex juvantibus, also retrospektiv nach einer Behandlung mit Stimulanzien, ist kein geeignetes Vorgehen.
Es ist notwendig, vor dem Behandlungsversuch mit dem Patienten, den Angehörigen und anderen wichtigen Bezugspersonen zu klären, welche Symptome das individuell gewichtete ADHS-Kernsyndrom darstellen und welche Symptome anderen Störungskomplexen zuzuordnen sind. Bei Kindern und Jugendlichen gehört hierzu auch die Einbeziehung der Schule. Dieses Vorgehen gewährleistet, dass alle Beteiligten verstanden haben, welche Symptome durch die Behandlung besser werden können und welche nicht unbedingt. Nur durch dieses Vorgehen erhält der Behandler die richtigen Rückmeldungen während des Behandlungsversuchs und falsche Erwartungen von Patient und Angehörigen werden reduziert. Dieses Vorgehen ist auch ein wichtiger Grundstein für die spätere Adhärenz des Patienten zur Medikation.
Vor Beginn einer Behandlung mit Stimulanzien werden zunächst die üblichen Kontrolluntersuchungen zum Ausschluss einer somatischen Kontraindikation durchgeführt, die auch bei anderen Psychopharmaka eingesetzt werden. Notwendig sind ein Standardlabor und eine sorgfältige somatische Anamnese, in Hinblick auf kardiale Vorerkrankungen auch die Anamnese der Eltern. Ein EKG zum Ausschluss einer relevanten QTc-Verlängerung ist sinnvoll, notwendig jedoch nur bei entsprechendem Hinweis auf ein kardiovaskuläres Risiko. Körpergröße und Gewicht sollten gemessen werden, Blutdruck und Puls mehrfach zur Abklärung eines arteriellen Hypertonus. Ein EEG ohne klinischen Hinweis auf eine Epilepsie ist nicht indiziert.
Start des Methylphenidat-Behandlungsversuchs
Ziel der ADHS-Therapie ist nicht eine immer wieder impulsartige Anhebung des verfügbaren Dopamins, sondern eine längerfristige Normalisierung des Dopaminspiegels im Gehirn. Deshalb gibt es kaum mehr einen Grund, eine Methylphenidat-Behandlung nicht auf einem retardierten Präparat aufzubauen. „Retardiertes Methylphenidat“ ist in den industriell verfügbaren Zubereitungen dabei immer eine Mischung aus unretardiertem und retardiertem Methylphenidat. Der unretardierte Bestandteil der Präparate gewährleistet einen rasch anflutenden hohen Wirkspiegel, während der retardierte Bestandteil für eine Wirkdauer von bis zu 8 bis 12 Stunden sorgt.
Im Regelfall kann bei Kindern, Jugendlichen und Erwachsenen gleich mit 10 mg retardiertem Methylphenidat morgens begonnen werden. Üblich ist, zunächst ein Präparat mit mittlerer Wirkdauer (6 bis 8 Stunden) einzusetzen. In Einzelfällen, insbesondere wenn Bedenken gegenüber Methylphenidat an sich bestehen, kann alternativ eine Dosis von 5 oder 10 mg unretardiertem Methylphenidat eingesetzt werden. Eine probatorische Gabe von unretardiertem Methylphenidat hat auch den Vorteil, dass der Behandler sich aufgrund des schnelleren Abflutens und der geringeren Beobachtungszeit leichter von der Wirkung des Medikaments einen eigenen Eindruck verschaffen kann. Eine fundierte Beurteilung der ADHS-Kernsymptomatik ist bei einer einmaligen Gabe jedoch nicht zu erwarten. Im Prinzip kann jede Äußerung einer Wirkung zunächst als Ausdruck einer möglicherweise spezifischen Reaktion des Medikaments gewertet werden.
Titration der geeigneten Dosis
Pathophysiologisch liegt dem ADHS-Syndrom in den meisten Fällen ein Mangel an verfügbarem Dopamin in den für die Aufmerksamkeit relevanten Regionen des Gehirns zugrunde. Durch die Behandlung mit Methylphenidat wird vereinfachend formuliert dieser Mangel für die Wirkdauer des Medikaments ausgeglichen, sodass vorübergehend ein physiologischer Zustand im Dopaminhaushalt hergestellt wird (Abb. 4–3). Eine zu geringe Dosis des Medikaments führt zu einer zu geringen Korrektur und somit Beibehaltung des pathologischen Zustands. Eine zu hohe Dosis führt dagegen zu einer pathologisch hohen Anhebung des verfügbaren Dopamins und weist vom klinischen Bild her auf eine Intoxikation mit Stimulanzien hin. Ziel der Titration ist es, die richtige Dosis des Stimulans zu finden. Da der biologische Zusammenhang nicht direkt gemessen werden kann, wie bei der Einstellung des arteriellen Blutdrucks oder des Blutzuckerspiegels, muss die Entscheidung, ob noch zu wenig oder bereits zu viel oder aber die richtige Dosis erreicht ist, von der klinischen Symptomatik abgeleitet werden.
Die Titration sollte in der Regel konsequent bis zur benötigten Dosis fortgeführt werden. Bei der Einstellung des Blutdrucks oder des Blutzuckers ist unmittelbar einsichtig, dass diese bis zur Normalisierung der Werte anzustreben ist. Bei der Einstellung auf Stimulanzien gibt es manchmal das Phänomen, dass nach einer eher willkürlichen Dosis die Einstellung als abgeschlossen betrachtet wird. Die Ursache hierfür liegt oft in einer Besorgnis des Patienten oder der Angehörigen in Hinblick auf die Medikation an sich. Sobald die untere Schwelle des Wirkbereichs erreicht ist, soll dann nach Wunsch von Patient oder Angehörigen keine weitere Aufdosierung mehr erfolgen. Diesem Phänomen könnte aber auch zugrunde liegen, dass kein geeignetes Monitoring über die ADHS-Kernsymptomatik im Verlauf der Titration erfolgt und der Behandler aufgrund fehlender Informationen die Eindosierung zu früh beendet. Der Patient profitiert jedoch nur dann nachhaltig von einer Stimulanzien-Therapie, wenn diese auch fachgerecht und in ausreichender Dosis durchgeführt wird. Sind Patient und Angehörige skeptisch gegenüber einer konsequenten Auftitrierung, so sollte weitere Psychoedukation über das Störungsbild und Aufklärung über die Medikation erfolgen.
Zur Aufdosierung von Methylphenidat sind insbesondere in der Arbeitsgruppe von David Coghill an der Universität von Dundee ausführliche Schemata entwickelt worden, die aufgrund des aufwendigen Protokolls im klinischen Alltag jedoch nicht leicht umzusetzen sind. Wir schlagen hier ein pragmatisches Vorgehen vor. Zu Beginn der Titration wird mit allen Beteiligten, die im Verlauf Beobachtungen zum Verhalten des Patienten an den Behandler rückmelden können, vereinbart, welche Zielsymptome des ADHS-Kernsyndroms im Fokus des Monitorings stehen sollen. Im ambulanten Behandlungssetting können der Patient, die Familie und bei Kindern und Jugendlichen die Schule in die Verhaltensbeobachtung einbezogen werden. Eine Information über das Vorgehen und Rückmeldung durch den Lehrer kann im Einzelfall auch an die Eltern übertragen werden. Im stationären Setting der Kinder- und Jugendpsychiatrie sind tägliche Verhaltensbeobachtungen durch den Pflege- und Erziehungsdienst, die Klinikschule, Kotherapeuten und die Behandler üblich.
Eine Woche jeweils nach Beginn der Titration oder nach letzter Dosissteigerung findet eine Evaluation des klinischen Monitorings statt. Der Behandler fügt alle Informationen, einschließlich der Angaben des Patienten, zusammen und kommt in der Zusammenschau zu vier möglichen Bewertungen und Konsequenzen:
- Das klinische Syndrom ist unverändert zum Status vor dem Behandlungsversuch: Der Kliniker schätzt ein, ob die Höchstdosis noch nicht erreicht ist. Diese liegt bei bis zu 1 mg Methylphenidat pro kg Körpergewicht, wobei eine Obergrenze von 60 mg im Regelfall nicht überschritten wird. Falls die Höchstdosis noch nicht erreicht ist, kann die Titration fortgesetzt und retardiertes Methylphenidat um weitere 10 mg erhöht werden.
- Es ist durch die letzte Erhöhung zu einer klinischer Verbesserung gekommen: Der Kliniker schätzt ein, ob die Höchstdosis noch nicht erreicht ist. Falls dies der Fall ist, kann die Titration fortgesetzt und retardiertes Methylphenidat um weitere 10 mg erhöht werden.
- Eine Verbesserung des klinischen Syndroms ist durch vorherige Schritte bereits erfolgt, es tritt nun keine klinischer Veränderung mehr ein: Die Titrierung ist abgeschlossen.
- Es ist durch die letzte Erhöhung zu einer klinischen Verschlechterung gekommen: Die Erhöhung wird rückgängig gemacht, die Titrierung ist abgeschlossen.
Zu beachten ist, dass die Wirkung von retardiertem Methylphenidat zum geeigneten Zeitpunkt beurteilt werden muss. Da der Patient die Medikation morgens einnimmt und je nach Präparat nach 6 bis 12 Stunden die Wirkung nachlässt, kann diese in der Regel nur vormittags valide eingeschätzt werden. Nachmittags oder abends kommt es dagegen, im Vergleich zu den Stunden zuvor, aufgrund des Abflutens der Medikation im Sinne eines Rebound-Phänomens oft zu einer Verstärkung des ADHS-Kernsyndroms, die für diesen Zeitpunkt sogar als Verschlechterung im Vergleich zu einer Nichtbehandlung wahrgenommen werden kann.
Entscheidung über den Erfolg des Behandlungsversuchs
- Die erste Möglichkeit ist, dass es unter Behandlung mit Methylphenidat insgesamt zu einer klinischen Verschlechterung gekommen ist. Diese Verschlechterung würde sich konkret im ADHS-Kernsyndrom zeigen: Statt einer Verbesserung der Aufmerksamkeitsstörung ist die Aufmerksamkeit schlechter, statt einer Verbesserung von Hyperaktivität ist der Patient psychomotorisch unruhig, angespannt und gereizt, statt einer Verbesserung von Impulsivität ist der Patient unüberlegt und sprunghaft. Dies bedeutet, dass kein relevanter Mangel an verfügbarem Dopamin im Gehirn vorliegt und dass die Behandlung mit Methylphenidat nicht zu einem Ausgleich des Dopaminspiegels geführt hat, sondern zu einer Steigerung über den physiologischen Spiegel. Es liegt somit ein Syndrom vor, das einer latenten Intoxikation mit Stimulanzien entspricht. In Bezug auf ADHS liegt entweder eine Subgruppe einer ADHS vor, die nicht über einen Mangel an Dopamin begründet wird, oder die Diagnose einer ADHS trifft möglicherweise gar nicht zu. Methylphenidat sollte also abgesetzt werden und ein Behandlungsversuch mit Amphetaminen kommt nicht in Betracht. Bei Validität der ADHS-Diagnose sollte eine medikamentöse Alternative mit Nicht-Stimulanzien wie Atomoxetin oder Guanfacin erwogen werden.
- Die zweite Möglichkeit ist, dass unter der Eindosierung von Methylphenidat das ADHS-Kernsyndrom suffizient gebessert wurde. Der Behandlungsversuch war erfolgreich und Methylphenidat sollte weiterverordnet werden.
- Die dritte Möglichkeit ist, dass auch unter Aufdosierung zur höchstmöglichen Dosis das ADHS-Kernsyndrom nicht oder nur unzureichend gebessert ist. Diese Variante spricht zunächst für das Vorliegen einer ADHS, da bei Nichtvorliegen von ADHS ein Aufdosieren von Methylphenidat zu einem relativen Intoxikationssyndrom führen sollte. Die wahrscheinlichste Erklärung für dieses Phänomen ist, dass die Wirkstärke von Methylphenidat nicht ausreicht. Es kommt daher ein Behandlungsversuch mit Amphetaminen in Betracht.
Optionen bei unklaren Ergebnissen der Methylphenidat-Titration
- Auslassversuch im Rahmen des Behandlungsversuchs: Die Medikation wird von einem auf den anderen Tag weggelassen und in den nächsten Tagen verglichen, ob sich durch das Weglassen eine klinische Verschlechterung ergibt. Ein Auslassversuch ist nur dann sinnvoll, wenn Methylphenidat bereits aufdosiert ist.
- Doppelblindversuch: Dieser kann in der Regel nur im stationären Kontext stattfinden. Zu empfehlen ist, dass ähnlich dem Auslassversuch die Auftitration von Methylphenidat abgeschlossen ist, bevor ein Doppelblindversuch sichere Erkenntnis über dessen Wirkung erbringen soll. Über einen Zeitraum von meistens zwei Wochen erhält der Patient in zufälliger Reihenfolge Wirkstoff oder Placebo in gleich gestalteten Kapseln. Notwendig ist, dass ausnahmslos alle Personen, die den Patienten während des Doppelblindversuchs klinisch einschätzen, ihrerseits in Unkenntnis über die Verabreichung von Wirkstoff und Placebo sind. Alle Personen, die den Verlauf einschätzen, notieren vormittags ihre Beobachtungen zu den ADHS-Kernsymptomen bzw. ausgewählten Zielsymptomen, beispielsweise als nicht vorhanden (0), leicht vorhanden (1) oder deutlich ausgeprägt (2). Diese Beurteilung kann auch anhand der Conners-Skalen operationalisiert vorgenommen werden. Wichtig für eine valide Beurteilung ist, dass tatsächlich die Zielsymptome eingeschätzt werden und nicht eine allgemeine Beurteilung des Gesamtbilds vorgenommen wird, da sich hierbei oft ADHS-Symptome und Symptome komorbider Störungen vermischen. Die Einschätzung der Frage, ob der Rater davon ausgeht, dass am betreffenden Tage Verum verabreicht wurde, kann zu verwirrenden Ergebnissen führen, wenn Rater die Hypothese haben sollten, dass Methylphenidat für den Patienten ungeeignet sei.
Behandlungsversuch mit Amphetaminen
Die Indikationen für eine Behandlung mit Amphetaminen liegen sowohl in einer zu geringen Wirkstärke von aufdosiertem Methylphenidat als auch in einer zu geringen Wirkdauer von retardiertem Methylphenidat. Da Lisdexamfetamin in der erhältlichen Zubereitung eine deutlich längere Wirkdauer hat als Dexamfetamin und im Vergleich zu diesem ein geringeres Missbrauchspotenzial bei Suchtkranken aufweist, hat Lisdexamfetamin in der Praxis Dexamfetamin weitgehend abgelöst. Fast keine Bedeutung mehr haben in der Apotheke individuell zubereitete Amphetamin-Präparationen. Wir besprechen hier Lisdexamfetamin.
Anders als Methylphenidat wird die Dosierung von Lisdexamfetamin nicht nach Körpergewicht dosiert, sondern nur nach klinischer Wirkung. 30 mg Lisdexamfetamin ist die normale Startdosis. Nur bei Kindern wird auch mit 20 mg begonnen. Bei der Titrierung von Methylphenidat kann um 20 mg pro Woche gesteigert werden. Die Höchstdosis beträgt 70 mg.
Behandlungsversuche mit Nicht-Stimulanzien
Nicht-Stimulanzien sind als Medikamentengruppe in der ADHS-Therapie „Second-Line“ zu Stimulanzien und kommen dann in Frage, wenn entweder eine Untergruppe der ADHS vorliegt, die pathophysiologisch nicht primär auf Dopamin-Stimulation respondiert, oder aber Nebenwirkungen und Kontraindikationen gegen eine Stimulanzien-Therapie sprechen, zum Beispiel Bluthochdruck oder eine nicht stabilisierte Suchterkrankung. Ein grundsätzlicher Vorteil ist der Umstand, dass Nicht-Stimulanzien ohne Betäubungsmittel-Rezept verordnet werden können. Wesentlicher Nachteil im Vergleich zu Stimulanzien ist die geringere Effektstärke bei den meisten Patienten mit ADHS.
- Atomoxetin hat eine mittlere Effektstärke von etwa 0,6 auf die ADHS-Kernsymptomatik und wirkt über die Erhöhung von Noradrenalin antriebssteigernd. Mit Atomoxetin wird gelegentlich die Vorstellung verbunden, dass sich hierunter mit ADHS komorbide auftretende emotional-instabile Stimmungslagen abmildern. Diese Ansicht muss jedoch ebenso als überholt betrachtet werden wie die früher vermutete Besserung emotional-instabiler Stimmungslagen durch Serotonin-Wiederaufnahmehemmer (SSRI). Wie SSRI wirkt Atomoxetin stattdessen auf den Affekt antidepressiv. Atomoxetin ist auch für Erwachsene zugelassen.
- Guanfacin hat im Vergleich zu Atomoxetin eine etwas bessere Effektstärke von etwa 0,8 auf die ADHS-Kernsymptomatik. Guanfacin ist ein Alpha-Adrenozeptor-Agonist und wirkt zentral blutdrucksenkend. Ein Vorteil von Guanfacin ist, wie von Atomoxetin, die konstante Wirkung. Guanfacin wirkt möglicherweise günstig auf mit ADHS komorbid auftretende Anspannungszustände und Aggressivität. Ein wichtiger Nachteil von Guanfacin ist der Umstand, dass es langsam ausgeschlichen werden muss, da es sonst zu erheblichen Blutdruckschwankungen kommen kann.
UAW, Kontraindikationen, Interaktionen, Absetzsyndrome
Psychostimulanzien werden seit langer Zeit als Medikamente eingesetzt, haben hohe Wirkstärken in Bezug auf die Zielsymptome und werden generell gut vertragen. Die Nebenwirkungsprofile von Methylphenidat und von Amphetaminen sind ähnlich, wobei allerdings entsprechend der stärkeren Wirkung der Amphetamine im Vergleich zu Methylphenidat auch die Nebenwirkungen der Amphetamine prinzipiell stärker ausgeprägt sind. Lisdexafetamin flutet jedoch sanfter an und ab als Methylphenidat-Präparate und wird hierdurch trotz der stärkeren Wirkung oft als verträglicher erlebt.
Das formale Nebenwirkungsspektrum von Methylphenidat ist breit gefächert. Als „sehr häufig“ werden angeben: Schlaflosigkeit, Nervosität, Kopfschmerzen. Als „häufig“ werden angegeben: Nasopharyngitis, Anorexie, Affektlabilität, Aggression, Agitiertheit, Angst, Depression, Reizbarkeit, anormales Verhalten, Schwindel, Dyskinesie, psychomotorische Hyperaktivität, Schläfrigkeit, Arrhythmie, Tachykardie, Palpitationen, Hypertonie, Husten, Rachen- und Kehlkopfschmerzen, Bauchschmerzen, Durchfall, Übelkeit, Magenbeschwerden und Erbrechen, Mundtrockenheit, Alopezie, Pruritus, Hautausschlag, Urtikaria, Arthralgie, Pyrexie, Wachstumsverzögerung unter längerer Anwendung bei Kindern. Hierzu muss jedoch berücksichtigt werden, dass ein Großteil der angegeben Nebenwirkungen unspezifisch ist und in der Praxis keine große Bedeutung hat.
Unter den möglichen Nebenwirkungen und Kontraindikationen sind einige von besonderer Bedeutung für die Beratung der Patienten und Angehörigen und sollen deswegen hier ausführlich besprochen werden: Appetitminderung und Gewichtsverlust, Risiko einer Psychose, „Persönlichkeitsveränderungen“, Reizbarkeit und Stimmungsschwankungen, Bluthochdruck und andere kardiovaskuläre Erkrankungen sowie Interaktionen mit Suchterkrankungen.
Appetitminderung und Gewichtsverlust
Insbesondere bei Kindern kommt es unter Methylphenidat häufig zu einer Appetitminderung, die sich in einer verminderten Gewichtszunahme bis hin zu einem Gewichtsverlust äußern kann. Das Ausmaß dieser Problematik wird aber oft von Eltern überschätzt und ist mit übertriebenen Befürchtungen verbunden. Die morgendliche Einnahme der Medikation sollte stets nach dem Frühstück erfolgen, auch wenn das intuitive Vorgehen der Eltern oft ist, die Wirkung der Medikation möglichst früh herbeizuführen. Beim Mittagessen und bei Zwischenmahlzeiten sollten die Eltern unter Berücksichtigung der Speisenauswahl auf ausreichende Nahrungsaufnahme achten. Nicht selten wird zum Abendessen das nachgeholt, was tagsüber unter der appetitzügelnden Wirkung von Methylphenidat weniger gegessen wurde. Über einen längeren Behandlungszeitraum sind eine verminderte Gewichtszunahme oder ein Gewichtsverlust oft rückläufig.
Induktion einer Psychose
Stimulanzien steigern im intrasynaptischen Spalt verfügbares Dopamin und entsprechen somit geradezu idealtypisch dem Modell der Dopamin-induzierten Psychose. Eine erhebliche Intoxikation mit Stimulanzien kann dementsprechend zu einem schizomanischen Bild führen. Bei Patienten, die eine therapeutische Dosis Stimulanzien einnehmen und sich nicht bereits gegenwärtig in einem Psychose-nahen Zustand befinden, ist eine psychotische Reaktion auf Stimulanzien jedoch sehr selten. Die Sorge vor einer psychotischen Exazerbation ist bei bestimmungsgemäßem Gebrauch in den allermeisten Fällen unbegründet. Auch eine Schizophrenie, bei der nicht gegenwärtig eine positiv-psychotische Episode besteht, stellt keine absolute Kontraindikation gegen eine Stimulanzien-Therapie dar. Besteht der Verdacht, dass der Patient psychotisch auf Stimulanzien reagieren könnte, so kann eine probatorische Gabe von unretardiertem Methylphenidat unter stationären Bedingungen Klarheit bringen.
„Persönlichkeitsveränderungen“, Reizbarkeit und Stimmungsschwankungen
Gelegentlich berichten Angehörige, vor allem Eltern, über den subjektiven Eindruck einer „Persönlichkeitsveränderung“ unter Eindosierung von Stimulanzien. Der Patient sei nicht mehr er selbst, er sei ungewohnt ruhig geworden, es bestehe Sorge, dass die Medikation den Patienten „ruhig gestellt“ habe. Rein pathophysiologisch ist die Sache einfach: Durch die Erhöhung von verfügbarem Dopamin ist es zu einer Verbesserung der Aufmerksamkeit gekommen, Hyperaktivität und Impulsivität haben nachgelassen. Der Patient zeigt jetzt seine Persönlichkeit unter physiologischem Dopamin-Haushalt. Das ADHS-Syndrom kann jedoch auch als Ausdruck von Lebhaftigkeit, Kreativität und Spontanität interpretiert werden und Angehörige sind an den Patienten unter ADHS-Syndrom gewöhnt. Die Herausforderung an den Kliniker besteht nun darin, dem Patienten und den Angehörigen diese Zusammenhänge zu vermitteln. Der Eindruck einer „Persönlichkeitsveränderung“ mildert sich in der Regel im Verlauf ab.
Ebenfalls rein pathophysiologisch gedacht, schwächen sich Reizbarkeit und Stimmungsschwankungen unter Normalisierung des Dopaminspiegels ab. Berichten Patient und Angehörige während des Behandlungsversuchs über zunehmende Reizbarkeit und Stimmungsschwankungen, so ist eine sorgfältige Analyse notwendig. Treten Reizbarkeit und Stimmungsschwankungen eindeutig während der Sättigungsphase und stärker im Behandlungsverlauf auf, so ist die optimale Dosis vermutlich überschritten. Zeigen sich Reizbarkeit und Stimmungsschwankungen jedoch während des Abflutens des Medikaments oder danach, so handelt es sich am ehesten um ein Rebound-Phänomen. Je nach Analyse des klinischen Monitorings kann sich also die Indikation zu einer Dosisreduktion oder Dosissteigerung bzw. Veränderung der Wirkdauer ergeben.
Bluthochdruck und andere kardiovaskuläre Erkrankungen
Stimulanzien führen zu einer Erhöhung des arteriellen Blutdrucks. Im Kindes- und Jugendalter stellt dies in der Regel kein Problem dar, sofern es nicht zu einem manifesten jugendlichen Hypertonus kommt. Werden Stimulanzien nur im Kindes- und Jugendalter verordnet, so besteht unter dieser Bedingung kein erhöhtes Risiko für eine hypertensive Erkrankung im späteren Erwachsenenalter. Dies kann nach jahrzehntelanger Erfahrung mit der Verordnung von Stimulanzien im Kindes- und Jugendalter als gesichert angenommen werden.
Etwas vorsichtiger sollte die Situation bei einer Verordnung von Stimulanzien im Erwachsenenalter betrachtet werden. Da diese Anwendung noch relativ neu ist, fehlen Erkenntnisse über die Langzeitwirkung. Ein unbehandelter Hypertonus stellt im Erwachsenenalter ein Risiko für eine Gefäß- und Nierenschädigung dar, welche zu einem weiteren Fortschreiten des Hypertonus führen kann und deshalb konsequent mit einem Blutdrucksenker behandelt werden soll. In der Umkehrbetrachtung wird durch eine Behandlung mit Stimulanzien der arterielle Blutdruck potenziell erhöht. Bei der Erhöhung des Blutdrucks durch Stimulanzien ist allerdings auch zu beachten, dass diese Erhöhung ähnlich der klinischen Wirkung nur auftritt, solange eine ausreichende Plasmakonzentration vorliegt.
Liegt eine kardiovaskuläre Erkrankung oder Risikokonstellation vor, sollte eine Eindosierung von Stimulanzien im Kindes-, Jugend- und Erwachsenenalter auf jeden Fall in Abstimmung und in weiterer Betreuung durch einen Kardiologen erfolgen.
Interaktionen mit Suchterkrankungen
Kinder und Jugendliche mit ADHS haben ein erhöhtes Risiko, später an einer Suchterkrankung zu leiden. Umgekehrt hat ein relevanter Teil der Suchtkranken eine ADHS. Stimulanzien wiederum unterliegen dem Betäubungsmittelgesetz und werden teilweise von Suchtkranken missbräuchlich verwendet.
Wenn bei Kindern oder Jugendlichen Stimulanzien eindosiert werden sollen, fragen Eltern oft besorgt, ob hierdurch eine Suchterkrankung hervorgerufen werden könnte. Mit erfolgreicher Therapie der ADHS sinkt jedoch das Risiko, dass ein ADHS-Patient eine Suchterkrankung entwickelt, auf das Niveau der Allgemeinbevölkerung. Auch aus diesem Grunde kann man zu einem Behandlungsversuch mit Stimulanzien raten. Bei Patienten, die an einer Suchterkrankung leiden, kommt es auf die konkrete Situation an, ob eine Behandlung mit Stimulanzien möglich ist. Werden gegenwärtig Substanzen missbräuchlich konsumiert, wird eine Behandlung mit Stimulanzen im Regelfall nicht möglich sein und Nicht-Stimulanzien sind bei diagnostizierter ADHS eine Option. Bei nachgewiesener Abstinenz ist eine Behandlung mit Stimulanzien möglich. Da viele Suchtkranke eine unbehandelte ADHS haben und diese wiederum die Suchterkrankung zumindest potenziell mit triggert, sollte hier keine zu restriktive Haltung eingenommen werden.
Therapiedauer, Kontrolluntersuchungen
Eine Behandlung mit Stimulanzien hat grundsätzlich dauerhaften Charakter, da die zugrundeliegende ADHS naturgemäß ebenfalls längerfristig vorliegt und durch die Stimulanzien-Therapie die Psychopathologie nur für die Dauer des Medikamentenspiegels normalisiert wird. „Drug Holidays“ können klinisch sinnvoll sein für die Festigung der Adhärenz, sind aber pharmakologisch eigentlich nicht geboten. Die Leitlinien sehen einen jährlichen Auslassversuch vor, um die Notwendigkeit weiterer Therapie zu prüfen. Der Auslassversuch sollte einen Zeitraum von vier bis sechs Wochen umfassen und Rückmeldungen aus Familie, Schule und Arbeitsplatz beinhalten, um zu einer validen Aussage zu kommen. Bei Eindosierung im Kindesalter sollte die Dosis im Verlauf regelmäßig dem steigenden Gewicht angepasst werden. Spätestens im Jugendalter sollte geprüft werden, ob eine Stimulanzien-Behandlung weiterhin notwendig ist, da bei etwa der Hälfte der ADHS-Betroffenen die Symptomatik in diesem Alter weitgehend remittiert. Bei Persistenz der ADHS sollte berücksichtigt werden, dass aus der Psychopathologie der ADHS nicht selten andere Komorbiditäten entstehen können. Erwachsene haben zudem oft Strategien entwickelt, um Aufmerksamkeitsschwäche, Desorganisiertheit und Impulsivität zu kompensieren. Eine dauerhafte Behandlung mit Stimulanzien im Erwachsenenalter sollte im Vergleich zum Kindes- und Jugendalter einer vorsichtigeren Indikationsstellung unterliegen.
Kontrolluntersuchungen bei Stimulanzien-Therapie beinhalten Wiederholungen des Routinelabors, der Messung von Blutdruck und Puls sowie bei Bedarf des EKGs.
Leitlinien
Eine gemeinsame S3-Leitlinie für Kinder, Jugendliche und Erwachsene mit ADHS wurde von den Fachgesellschaften für Kinder und Jugendliche sowie für Erwachsene entwickelt und ist Ende Juni 2018 veröffentlicht worden (https://www.awmf.org/uploads/tx_szleitlinien/028-045l_S3_ADHS_2018-06.pdfhttps://www.awmf.org/uploads/tx_szleitlinien/028-045l_S3_ADHS_2018-06.pdf). Diese Leitlinie ersetzt die früheren Leitlinien der DGPPN (2003) und der DGKJP (2006). Unter Berücksichtigung der internationalen wissenschaftlichen Entwicklungen stärkt die neue Leitlinie den Stellenwert der Pharmakotherapie, insbesondere der Stimulanzien.
Die britischen NICE(National Institute for Health and Care Excellence)-Leitlinien „Attention deficit hyperactivity disorder: diagnosis and management“ für Kinder, Jugendliche und Erwachsene wurden zuletzt 2016 überarbeitet. Ein Update ist für 2018 angekündigt.
Interessenkonflikterklärung
RW: Keine Interessenkonflikte
WE: Keine Interessenkonflikte
Literatur
1. Bachmann CJ, Philipsen A, Hoffmann F. ADHS in Deutschland: Trends in Diagnose und medikamentöser Therapie. Dtsch Ärztebl Int 2017;114:141–8.
2. Banaschewski T, Becker K, Döpfner M, Holtmann M, et al. Aufmerksamkeitsdefizit-/Hyperaktivitätsstörung. Dtsch Arztebl Int 2017;114:149–59.
3. Müller WE. Neuropharmakologie der Psychostimulanzien. Pharmakon 2015;3:211–7.
4. Müller WE, Laux G. Weiterbildungs-Curriculum Psychopharmakologie/Pharmakotherapie. Teil 1: Allgemeine Psychopharmakotherapie, allgemeine Pharmakologie, Antidepressiva – Pharmakologie. Psychopharmakotherapie 2017;24:276–82.
5. Sonuga-Barke EJ, Brandeis D, Cortese S, Daley D, et al.; European ADHD Guidelines Group. Nonpharmacological interventions for ADHD: systematic review and meta-analyses of randomized controlled trials of dietary and psychological treatments. Am J Psychiatry 2013;170:275–89.
6. Thapar A, Cooper M. Attention deficit hyperactivity disorder. Lancet 2016;387:1240–50.
Priv.-Doz. Dr. med. Robert Waltereit, Klinik und Poliklinik für Kinder- und Jugendpsychiatrie und -psychotherapie, Universitätsklinikum Carl Gustav Carus, Technische Universität Dresden, Fetscherstraße 74, 01307 Dresden
Univ.-Prof. Dr. Walter E. Müller, Höhenstraße 49A, 67550 Worms, E-Mail: w.e.mueller@em.uni-frankfurt.de
Psychopharmakotherapie 2018; 25(04):199-207
