Sven Ulrich, Roland Ricken, Berlin, Peter Schlattmann, Jena, und Mazda Adli, Berlin
Tranylcypromin (TCP) ist der einzige in Deutschland und Österreich zugelassene irreversible und nichtselektive Monoaminoxidase-(MAO)-A/B-Hemmer. Die Wirksamkeit in der Indikation Depression ist entsprechend neuen Studien, Übersichten und klinischen Guidelines anerkannt [23, 41, 42, 44]. Erhöhte Aktivität von MAO wurde als therapeutisch sinnvolle pharmakologische Zielstruktur bestätigt, beispielsweise in neuen Studien zu atypischer Depression [6] und Placebo-Response bei Depression [24]. Wegen der notwendigen Tyramin-armen Diät beschränkt sich die Anwendung jedoch auf Patienten mit therapieresistenter Depression (TRD) [11]. Obwohl TCP schon mehr als 50 Jahre als Antidepressivum verordnet wird [45], existiert in der Fachliteratur bisher keine Metaanalyse kontrollierter Studien. Anliegen dieser Arbeit war deshalb die vollständige Sichtung kontrollierter Studien von TCP bei Depression, die Bewertung des Studiendesigns und die statistische Zusammenfassung der Daten in einer Metaanalyse.
Methode
Kontrollierte Studien zu TCP bei Depression wurden zunächst in drei tabellarischen Zusammenstellungen aus umfassenden Übersichten klinischer TCP-Studien der Jahre 1965, 1995 und 2002 identifiziert [1, 23, 44]. Studien nach 1993 wurden zusätzlich in Medline anhand der Suchwörter „Tranylcypromin“ und „Depression“ gesucht. Berücksichtigung der Studien in den vorherigen Reviews und Übereinstimmung mit grundlegenden Anforderungen (prospektive parallele oder Überkreuzstudie, offen, einfach- oder doppelblind, Placebo oder aktive Kontrolle, nur depressive Patienten, akute Behandlung, keine antidepressive Komedikation, wenigstens zehn Patienten, ausreichende Beschreibung) war zunächst ausreichend für die Berücksichtigung in der Metaanalyse. Für eine weitere Bewertung der Qualität des Studiendesigns diente die „Guideline on clinical investigation of medicinal products in the treatment of depression“ der European Medicines Agency (EMA) als Grundlage [7]. Gemäß den Bewertungskriterien wurden die Studien mit „–“, „±“ oder „+“ (z.B. für adäquate Diagnostik und Dosis) bzw. „Ja“ oder „Nein“ (z.B. für adäquate Krankheitsschwere zu Beginn) kodifiziert. Den Codes wurden entsprechend Kriteriumswerte von 0, 0,5 oder 1 bzw. 0 oder 1 (0 oder 3 für höher gewichtete Kriterien wie Verblindung und Randomisierung) zugeordnet. Für das komplexe und höher gewichtete Kriterium der Erfassung des therapeutischen Effekts wurden vier Einzelkriterien zusammengefasst (Codes Ja/Nein) und mit den Werten 0, 1, 2 oder 3 versehen. Aus den Kriteriumswerten lässt sich ein Gesamtwert pro Studie als Summe berechnen. Dessen Maximalwert ergibt sich zu 18 bzw. 100%. Die Daten der Studien wurden doppelt durch zwei Autoren gesichtet. Die Bewertung der Studienqualität wurde durch das heute sehr verbreitete „Cochrane Collaboration’s tool for assessing risk of bias in randomised trials“ ergänzt, welches versucht, auch die Methodik der Randomisierung und Verblindung sowie mögliche Einflüsse von Datenverlusten oder -verzerrungen einzuschätzen. Dies erfolgt in sieben Kriterien durch Einordnung des Risikos für systematische Fehler als hoch, niedrig oder nicht einschätzbar [17].
Die Effektstärken von TCP im Vergleich mit der Kontrolle wurden als natürlicher Logarithmus des Odds-Verhältnisses (LogOV, engl. Log odds ratio) der Anzahl von Respondern (R) und Nonrespondern (NR) unter Einbeziehung der Therapieabbrecher (Intention-to-treat-Population, ITT) berechnet. Im Falle fehlender Daten zum Grund eines Therapieabbruchs wurden diese als NR eingesetzt. Für Nullzellen erfolgte eine Standard-Kontinuitätskorrektur mit 0,5. Die sich aus mehreren Studien ergebende gemeinsame Effektstärke wurde separat für Studien mit Placebo und aktiver Kontrolle jeweils als gemeinsames LogOV entsprechend einem Fixed-Effekt-Modell in einem Microsoft-Excel-Datenblatt berechnet. Die Verwendung des LogOV ist dabei äquivalent der nicht logarithmischen Berechnung, wird aber in der grafischen Darstellung als gefälliger empfunden, weil symmetrische Konfidenzintervalle resultieren. Die Grenze für Über-/Unterlegenheit liegt in dieser Darstellungsweise bei null [8, 28]. Die Abschätzung formaler Inhomogenität der Studien erfolgte auf Basis der Differenzen von LogOV und gemeinsamem LogOV in einem Chi-Quadrat-Test. Im Falle von Inhomogenität wurden explorative Sensitivitätsanalysen mit Subgruppen von Studien durchgeführt. Diese Subgruppen wurden in einem ersten Schritt entsprechend dem Vorliegen von therapieresistenter Depression und in einem zweiten Schritt anhand der pharmakologischen Zuordnung des Kontrollarzneimittels gebildet. Weitere Sensitivitätsanalysen schlossen dann auch die Qualität der Studien ein. Eine kürzere Version der Metaanalyse wurde bereits in englischer Sprache publiziert [39].
Ergebnisse
Studienqualität
Es wurden 23 kontrollierte Studien von TCP bei Depression gefunden, vier mit Placebo, 17 mit aktiver Kontrolle und zwei als dreiarmige Studien mit Placebo und aktiver Kontrolle, die insgesamt 664 TCP-Patienten einschlossen. Aktive Kontrolle waren überwiegend trizyklische Antidepressiva (TCA) in neun Studien (Imipramin, Amitriptylin, Nortriptylin) und MAO-Inhibitoren in sechs Studien (Phenelzin, Moclobemid, Brofaromin). In je einer Studie wurden 5-Hydroxytryptophan, Nomifensin, Lamotrigin und eine Kombination aus einem selektiven Serotonin-Noradrenalin-Wiederaufnahmehemmer (SSNRI) mit Mirtazapin verwendet. Die vorgefundenen weitergehenden Charakteristika der Patienten bezüglich der Diagnose Depression waren sehr heterogen und ergaben sich entweder zufällig ohne spezielle Vorgaben oder entsprechend Einschlusskriterien gemäß einem speziellen Studienziel. Aus der heutigen Sicht der ICD10 mit rein phänomenologischer Konzeption sind die genannten Subtypen der Depression (z.B. reaktive, atypische, neurotische, endogene Depression) zwar in den Codes F32 (depressive Episode), F33 (rezidivierende depressive Episode) und F31.3/4 (bipolare affektive Störung, gegenwärtig depressive Episode) enthalten, erscheinen aber nur am Rande unter „dazugehörige Begriffe“. Überwiegend wurden weibliche und männliche Patienten rekrutiert bei einem Alter von 18 bis 65 Jahre. Ältere Patienten wurden ausgeschlossen. Die Dosis von TCP lag zumeist in einem Bereich von 20 bis 60 mg/Tag, also eine der heutigen Zulassung entsprechende Dosis, in sechs Studien aber auch darüber (fünf Studien bis 100 mg/Tag, eine Studie bis 150 mg/Tag). Als Komedikation waren mit Ausnahme einer Studie mit Lithium, Valproinsäure und Carbamazepin und einer Studie mit Analgetika nur Hypnotika und Sedativa erlaubt.
In Tabelle 1 sind die therapeutischen und patientenbezogenen Daten der Studien entsprechend dem Jahr der Publikation zeitlich geordnet zusammengefasst. Dementsprechend können sieben Studien als frühe Studien (1960–1964) und 16 Studien als modernere Studien (ab 1980) bezeichnet werden. Nicht unerwartet ist, dass entsprechend der therapeutischen und wissenschaftlichen Entwicklung keine der sieben frühen Studien Patienten mit therapieresistenter Depression einschloss, dagegen fünf der sieben letzten Studien. Wohl aufgrund der damals unvorbereitet aufgetretenen Tyramin-Problematik mit im Einzelfall auch dramatischen Folgen wurden ab 1965 und in den 70er-Jahren keine neuen Studien mit TCP bei Depression durchgeführt.
Tab. 1. Daten kontrollierter Studien zu Tranylcypromin (TCP) bei Depression
|
Studie |
Lit. |
Anzahl Patienten |
Weitere Charakteristika der Patienten bezüglich der Diagnose Depression |
Alter* [Jahre] |
Geschlecht |
Kontrolle |
TCP-Dosis* [mg/Tag] |
Komedikation |
||
|
Gesamt |
TCP |
Kontrolle |
||||||||
|
Freyhan 1960 |
[12] |
122 |
14 |
108 |
n. d. |
57 |
m/w |
Imi |
30–150 |
Keine |
|
Bartholomew 1962 |
[2] |
102 |
51 |
51 |
62% reaktiv, 22% endogen, 16% ID |
25–67 |
m/w |
Plc |
30–60 |
Sedativa |
|
Gottfries 1963 |
[15] |
50 |
25 |
25 |
22% endogen, 78% reaktiv und neurotisch |
n. d. |
n. d. |
Plc |
15–30 |
Sedativa |
|
Khanna 1963 |
[22] |
30 |
15 |
15 |
n. d. |
24–47 |
w |
Plc |
30 |
Keine |
|
Spear 1964 |
[40] |
78 |
37 |
41 |
Endogen, atypisch |
44,5 |
m/w |
Imi |
30 |
Sedativa |
|
Richmond 1964 |
[38] |
60 |
20 |
40 |
75% endogen, 25% reaktiv |
n. d. |
n. d. |
Imi, Ami |
40 |
Barbiturate |
|
Glick 1964 |
[14] |
35 |
9 |
13 |
38% endogen, 38% ID, 12% neurotisch, 12% SD |
48,5 |
m/w |
Plc |
37 |
Sedativa |
|
13 |
Phe |
|||||||||
|
White 1980 |
[48] |
20 |
11 |
9 |
MD, MiD, 40% neurotisch, 30% BD, u.a. |
33 (19–61) |
m/w |
Ami |
30 |
n. d. |
|
Himmelhoch 1982 |
[18] |
59 |
28 |
31 |
MD, v. a. anerg, 29 bipolar, RVS (TRD auf TCA) |
37,4±11,6 |
m/w |
Plc |
40 |
Flurazepam |
|
Razani 1983 |
[37] |
51 |
21 |
30 |
MD, 37% endogen |
41±12,8 |
m/w |
Ami |
40 |
n. d. |
|
White 1984 |
[49] |
183 |
63 |
59 |
MD, 80% nichtendogen, 20% endogen |
37 (18–60) |
m/w |
Plc |
44,4 (30–60) |
Sedativa, Analgetika, Antihistaminika |
|
61 |
Nor |
|||||||||
|
Nolen 1985 |
[31] |
43 |
26 |
17 |
MD, v. a. melancholisch (TRD auf SSRI/TCA) |
20–65 |
m/w |
5HTP |
82 (60–100) |
Lorazepam |
|
Nolen 1988 |
[32] |
34 |
19 |
15 |
MD, v. a. melancholisch (TRD auf SSRI/TCA) |
20–65 |
m/w |
Nom |
78 (40–100) |
Lorazepam |
|
Himmelhoch 1991 |
[19] |
56 |
28 |
28 |
MD, v. a. anerge BD, RVS |
40,2±11,6 |
m/w |
Imi |
36,8±11,9 |
n. d. |
|
Thase 1992 |
[43] |
16 |
12 |
4 |
MD, v. a. anerge BD, RVS (TRD auf Imi ) |
37,7±12,7 |
m/w |
Imi (nach TCP) |
39,2 (20–60) |
n. d. |
|
Heinze 1993 |
[16] |
160 |
79 |
81 |
Depression (ICD-9), endogen unipolar |
47,2±12,3 |
m/w |
Moc |
24,3±5,9 |
Sedativa |
|
Nolen 1993 |
[29] |
39 |
17 |
22 |
MD, 60% melancholisch (TRD auf TCA) |
48,8±10,7 |
m/w |
Bro |
81,2±25,9 |
Lorazepam |
|
O‘Brien 1993 |
[33] |
54 |
26 |
28 |
MD, je ca. 50% endogen und neurotisch |
18–65 |
m/w |
Ami |
22,4±7,8 |
Benzodiazepine |
|
Volz 1994a |
[46] |
93 |
47 |
46 |
MD, inkl. 10% atypisch (TRD auf TCA/SSRI) |
42,4 (18–67) |
m/w |
Bro |
20–30 |
Sedativa |
|
Volz 1994b |
[47] |
46 |
11 |
35 |
Depression (ICD-9, DSM-III), alle nichtendogen |
18–65 |
m/w |
Bro |
20 |
Sedativa |
|
Birkenhäger 2004 |
[4] |
77 |
39 |
38 |
MD, inkl. 8% atypisch (TRD auf TCA/SSRI) |
18–65 |
m/w |
Phe |
60,6 (30–100) |
Lorazepam |
|
McGrath 2006 |
[25] |
109 |
58 |
51 |
MD, inkl. 21% atypisch (TRD auf SSRI/SSNRI/TCA/Augment.) |
46,0±11,1 |
m/w |
Ven + Mir |
36,9 |
n. d. |
|
Nolen 2007 |
[30] |
19 |
8 |
11 |
MD, v. a. BD (TRD auf SSRI/SSNRI/TCA/Bupropion) |
46,2±12,9 |
m/w |
Lam |
20–100 |
Li, VPA, CBZ |
*Mittelwert, Bereich, Mittelwert (Bereich) oder Mittelwert ± Standardabweichung; Ami: Amitriptylin; Bro: Brofaromin; CBZ: Carbamazepin; 5HTP: 5-Hydroxytryptophan; Imi: Imipramin; Lam: Lamotrigin; Li: Lithium; Mir: Mirtazapin; Moc: Moclobemid; Nom: Nomifensin; Nor: Nortriptylin; Phe: Phenelzin; Plc: Placebo; SSRI: selektive Serotonin-Wiederaufnahmehemmer; TCA: trizyklische Antidepressiva; Ven: Venlafaxin; VPA: Valproinsäure; BD: bipolare Depression; ID: Involutionsdepression; MD: Majore Depression; MiD: Minore Depression; RVS: reverse vegetative Symptomatik; SD: schizophrene Depression; TRD: therapieresistente Depression; n.d.: nicht definiert (keine Daten)
Tabelle 2 enthält die Zusammenstellung der Qualitätsbewertung des Studiendesigns entsprechend der EMA-Guideline für Depressionsstudien, wobei aus Platzgründen pro Studie und Kriterium nur die Kodierung der Qualität, aber ohne den entstehenden einzelnen Kriteriumswert zur Berechnung des Gesamtwerts angegeben ist. Die Diagnostik der Depression war zufriedenstellend (Code „±“) in den frühen Studien bis gut (Code „+“) in den moderneren Studien. Ähnlich ist das Bild eines klaren zeitlichen Trends für die notwendige detaillierte Darstellung der psychiatrischen Anamnese. Bis auf eine Studie mit nur 20 bis 30 mg/Tag TCP bei therapieresistenter Depression war die Dosis adäquat, also zumindest „±“.
Tab. 2. Qualität kontrollierter Studien zu Tranylcypromin (TCP) bei Depression gemäß EMA-Richtlinie für Antidepressiva-Studien
|
Allgemein akzeptierte, systematische diagnostische Kriterien |
Detail-lierte psychiatrische Anamnese |
Adäquate Dosis§ |
Ambulante Patienten |
Wenigstens moderat krank |
Strenge Ausschlusskriterien |
Doppelblind |
Randomisiert |
Dauer§§ |
|
|
Codes |
(–, ±, +) |
(Ja, Nein) |
|||||||
|
Werte |
(0; 0,5; 1) |
(0; 1) |
(0; 1) |
(0; 1) |
(0; 3) |
(0; 3) |
(0; 1) |
||
|
Freyhan 1960 |
± |
± |
+ |
Nein |
n. d. |
Nein |
Nein |
Nein |
5–193 |
|
Bartholomew 1962 |
± |
± |
+ |
Ja |
Nein |
Ja |
Ja |
Ja |
6 |
|
Gottfries 1963 |
± |
± |
+ |
Nein |
n. d. |
Nein |
Ja### |
Nein### |
2 |
|
Khanna 1963 |
± |
± |
+ |
Nein |
n. d. |
Nein |
Ja |
Ja |
2 |
|
Spear 1964 |
± |
± |
+ |
Ja |
n. d. |
Ja |
Ja |
Ja |
3 |
|
Richmond 1964 |
± |
± |
+ |
Ja |
n. d. |
Nein |
Nein** |
Ja |
3 |
|
Glick 1964 |
± |
± |
+ |
Ja |
Nein |
Nein |
Ja |
Ja |
4 |
|
White 1980 |
+ (RDC) |
± |
+ |
Nein |
Nein |
Nein |
Nein |
Ja |
4 |
|
Himmelhoch 1982 |
+ (RDC, DSM-III) |
+ |
± |
Ja |
Ja (RDS>7) |
Ja |
Ja |
Ja |
6 |
|
Razani 1983 |
+ (DSM-III) |
+ |
+ |
Ja |
Ja |
Nein |
Ja |
Ja |
4 |
|
White 1984 |
+ (RDC) |
± |
+ |
Ja |
Ja |
Ja |
Ja |
Ja |
4 |
|
Nolen 1985 |
+ (DSM-III) |
+ |
+ |
n. d. |
Ja (HAMD >17) |
n. d. |
Nein |
Ja |
4 |
|
Nolen 1988 |
+ (DSM-III) |
+ |
+ |
n. d. |
Ja (HAMD >17) |
n. d. |
Ja |
n. d.*** |
4 |
|
Himmelhoch 1991 |
+ (RDC, DSM-III) |
+ |
+ |
Ja |
Ja (HAMD >15) |
Ja |
Ja |
Ja |
6 |
|
Thase 1992 |
+ (RDC, DSM-III) |
+ |
± |
Ja |
Ja (HAMD >15) |
Ja |
Ja |
Ja |
6 |
|
Heinze 1993 |
+ (ICD-9) |
+ |
± |
Ja |
Ja (HAMD >20) |
Ja |
Ja |
Ja |
>4 |
|
Nolen 1993 |
+ (DSM-IIIR) |
+ |
+ |
Nein |
Ja (HAMD >17) |
n. d. |
Ja |
Ja |
4 |
|
O‘Brien 1993 |
+ (RDC, ICD-9) |
+ |
± |
Nein |
Ja (HAMD >15) |
Ja |
Ja |
Ja |
6 |
|
Volz 1994a |
+ (DSM-III) |
+ |
– |
Nein |
Ja (HAMD >17) |
Ja |
Ja |
Ja |
6 |
|
Volz 1994b |
+ (DSM-III, ICD-9) |
+ |
± |
Nein |
Ja (HAMD >17) |
Ja |
Ja |
Ja |
4 |
|
Birkenhäger 2004 |
+ (DSM-IV) |
+ |
+ |
Nein |
Ja (HAMD >13) |
Ja |
Ja |
Ja |
5 |
|
McGrath 2006 |
+ (DSM-IV) |
+ |
± |
Ja |
Ja |
Ja |
Nein** |
Ja |
12 |
|
Nolen 2007 |
+ (DSM-IV) |
+ |
+ |
Ja |
Ja (IDS-C >15) |
Ja |
Nein |
Ja |
10 |
|
Qualität Kriterium [%] |
84,8 |
80,4 |
82,6 |
52,2 |
65,2 |
56,5 |
73,9 |
87,0 |
43,5 |
(Fortsetzung folgende Seite)
Tab. 2. (Fortsetzung)
|
Erfassung Symptomänderung Beginn/Ende Therapie mit Ratingskala |
>50% Besserung in Ratingskala als Responsekriterium# |
Akzeptierte Ratingskala zur Bewertung klinische Besserung## |
Globale Bewertung klinische Besserung |
Wash-out relevanter Medikation |
Keine inadäquate Komedikation |
Qualität Studie |
||
|
Codes |
(Ja, Nein) |
|||||||
|
Werte |
(0; 1; 2; 3) |
(0; 1) |
(0; 1) |
(0–18) |
% |
|||
|
Freyhan 1960 |
Nein |
Nein |
Nein |
Ja |
n. d. |
Ja |
5 |
27,8 |
|
Bartholomew 1962 |
Nein |
Nein |
Nein |
Ja |
n. d. |
Ja |
13 |
72,2 |
|
Gottfries 1963 |
Ja |
Nein |
Nein* |
Ja |
n. d. |
Ja |
8 |
44,4 |
|
Khanna 1963 |
Ja |
Nein |
Ja (MMPI) |
Nein |
Ja |
Ja |
11 |
61,1 |
|
Spear 1964 |
Ja |
Nein |
Nein* |
Nein |
n. d. |
Ja |
12 |
66,7 |
|
Richmond 1964 |
Ja |
Nein |
Ja (HAMD) |
Ja |
n. d. |
Ja |
9 |
50,0 |
|
Glick 1964 |
Ja |
Nein |
Ja (LMSRPP) |
Ja |
Nein |
Ja |
12,5 |
69,4 |
|
White 1980 |
Ja |
Ja |
Ja (HAMD) |
Ja (CGI) |
n. d. |
n. d. |
8,5 |
47,2 |
|
Himmelhoch 1982 |
Ja |
Ja |
Ja (NPRL, KDS) |
Ja (GAS) |
Ja |
Ja |
17,5 |
97,2 |
|
Razani 1983 |
Ja |
Nein |
Ja (HAMD) |
Ja (CGI) |
n. d. |
n. d. |
13 |
72,2 |
|
White 1984 |
Ja |
Nein |
Ja (HAMD) |
Ja (GIS) |
Ja |
Ja |
17 |
94,4 |
|
Nolen 1985 |
Ja |
Ja |
Ja (HAMD) |
Nein |
Ja |
Ja |
11 |
61,1 |
|
Nolen 1988 |
Ja |
Ja |
Ja (HAMD) |
Nein |
Ja |
Ja |
14 |
77,8 |
|
Himmelhoch 1991 |
Ja |
Nein |
Ja (HAMD) |
Ja (CGI) |
n. d. |
n. d. |
15 |
83,3 |
|
Thase 1992 |
Ja |
Ja |
Ja (HAMD) |
Ja (CGI) |
n. d. |
n. d. |
15,5 |
86,1 |
|
Heinze 1993 |
Ja |
Nein |
Ja (HAMD) |
Ja (CGI) |
Ja |
Ja |
15,5 |
86,1 |
|
Nolen 1993 |
Ja |
Ja |
Ja (HAMD) |
Ja (CGI) |
Ja |
Ja |
15 |
83,3 |
|
O‘Brien 1993 |
Ja |
Nein |
Ja |
Ja |
Ja |
Ja |
16,5 |
91,7 |
|
Volz 1994a |
Ja |
Ja |
Ja (HAMD) |
Ja |
Ja |
Ja |
16 |
88,9 |
|
Volz 1994b |
Ja |
Ja |
Ja |
Ja |
Ja |
Ja |
15,5 |
86,1 |
|
Birkenhäger 2004 |
Ja |
Ja |
Ja (HAMD) |
Ja (CGI) |
Ja |
Ja |
16 |
88,9 |
|
McGrath 2006 |
Ja |
Ja |
Ja |
Nein |
Nur TCP |
Ja |
12,5 |
69,4 |
|
Nolen 2007 |
Ja |
Ja |
Ja (IDS-C) |
Ja (CGI) |
Ja |
Ja |
15 |
83,3 |
|
Qualität Kriterium [%] |
91,3 |
47,8 |
82,6 |
78,3 |
52,2 |
82,6 |
||
|
73,9 |
||||||||
§ Erforderlich >≈ 20 mg/Tag bzw. >≈ 40 mg/Tag für TRD; §§ erforderlich ≥4 Wochen für Placebo-kontrollierte Studien und ≥6 Wochen für Studien mit aktiver Kontrolle; # andere Responsekriterien können verwendet werden bzw. auch Remission; ## Teilwert =1 zusammen mit Erfassung Beginn/Ende, mehrere Studien verwendeten noch mehr als nur die genannte Skala; ### auch: „To largest extent the patients were unaware of the trial.“ Doppelblind impliziert eine Randomisierung. Obwohl die Autoren die Studie nicht als randomisiert bezeichnen, war sie deshalb aber sicherlich randomisiert. * eigene kleine Ratingskala; ** einfach verblindet, für die Studie McGrath (2006) scheint es aber unwahrscheinlich, dass die Verblindung der Bewerter des Therapieeffekts nicht dadurch aufgehoben wurde, dass nur die TCP-Patienten an die Tyramin-arme Diät gebunden waren; *** Im Kontext der gemeinsamen Durchführung und Publikation mit der Studie Nolen (1985) sehr wahrscheinlich ebenfalls randomisiert. Außerdem ist Randomisierung Voraussetzung doppelblinder Studien. CGI: Clinical Global Impression Scale; DSM: Diagnostic and Statistical Manual of Mental Disorders; GAS: Global Assessment Scale; GIS: Global Improvement Scale; HAMD: Hamilton Depression Rating Scale; ICD: International Classification of Diseases; IDS-C: Inventory of Depression Symptomatology – Clinical Version; KDS: Kupfer Detre System; LMSRPP: Lorr Multidimensional Scale for Rating of Psychiatric Patients; MMPI: Depression Scale of Minnesota Multiphasic Personality Inventory; NPRL: New Physician’s Rating List; QIDS-SR: Quick Inventory of Depressive Symptomatology – Self-Report; RDC: Research Diagnostic Criteria; RDS: Raskin Depression Scale; TRD: therapieresistente Depression
Da so in der EMA-Richtlinie gefordert, wurde das Kriterium „ambulante Patienten“ in die Bewertung aufgenommen. In etwa der Hälfte der Studien war dies gegeben (Kodierung mit „Ja“), wobei dieses Kriterium gerade für TCP, das heute überwiegend stationär eingestellt wird, eher nicht zweckmäßig erscheint. Das Erfordernis einer zumindest moderaten Schwere der Erkrankung ist wiederum weniger bei den frühen Studien und nahezu vollständig bei den moderneren Studien erfüllt. Strenge Ausschlusskriterien sind in 56,6% der Studien gegeben, in zwei von sieben frühen und 11 von 16 der moderneren Studien (nicht signifikant, Fisher-Test). Für die wichtigsten Kriterien der doppelten Verblindung und Randomisierung sind keine oder nur sehr geringe Unterschiede zwischen frühen und moderneren Studie zu erkennen (nicht signifikant, Fisher-Test). Insgesamt ist die Qualität der Studien hier gut (fast 75% doppelblind) bzw. sehr gut (fast 90% randomisiert).
Die erforderliche Studiendauer von ≥4 Wochen für Placebo-kontrollierte Studien und ≥6 Wochen für Studien mit aktiver Kontrolle war nur in 43,5% der Studien gegeben, was der geringste Wert der Erfüllung der EMA-Richtlinie ist.
Für das komplexe und zentrale Kriterium der Erfassung des therapeutischen Effekts ergibt sich selbst unter Einbeziehung der strengen Forderung 50%-Skalenbesserung als Responsekriterium eine gute prozentuale Erfüllung von 73,9%. Wird in Betracht gezogen, dass eine Auswertung der Response basierend auf einer globalen Bewertung des Therapieeffekts beispielsweise mit der Clinical Global Impression Scale (CGI) hohe Akzeptanz hat, wie in der Mehrzahl der anderen Studien verwendet, kann die Studienqualität hier sogar noch höher angesetzt werden. Das erforderliche Auswaschen relevanter Vormedikation wurde zu 52,2% und das wichtige Qualitätskriterium des Ausschlusses relevanter Komedikation (v. a. Antidepressiva) zu 82,6% erfüllt.
Die prozentuale Erfüllung der Studienqualität per Qualitätskriterium beträgt entsprechend der letzten Zeile von Tabelle 2 insgesamt 70,7%±16,1% (Mittelwert±Standardabweichung). Die prozentuale Erfüllung der geforderten Studienqualität per Studie lag entsprechend der letzten Spalte von Tabelle 2 insgesamt bei 73,4%±18,0%. Die Qualität der frühen Studien ist entsprechend der EMA-Richtlinie mit 55,9%±16,1% gegenüber 81,1%±13,0% der moderneren Studien signifikant niedriger (p<0,001, t-Test).
Studienqualität bezüglich Anforderungen TRD
Die EMA-Richtlinie für Depressionsstudien stellt bezüglich therapieresistenter Depression (TRD) weitere Anforderungen. Als Kriterium der therapieresistenten Depression gilt das Fehlschlagen von mindestens zwei suffizienten Behandlungen mit Antidepressiva, ein Therapiefehler ist dabei im Idealfall prospektiv zu zeigen und als Kontrolle soll eine für therapieresistente Depression nicht etablierte Substanz verwendet werden. Allein Placebo-kontrollierte Studien sind für therapieresistente Depression unzureichend. In Tabelle 3 sind neun TCP-Studien bei therapieresistenter Depression bezüglich dieser Kriterien bewertet worden. Zwei Studien erfüllen alle drei Anforderungen [31, 32].
Tab. 3. Qualität kontrollierter Studien zu Tranylcypromin (TCP) gemäß speziellen Anforderungen für Studien über therapieresistente Depression (TRD) der EMA-Richtlinie
|
Kriterium Therapieresistenz |
Ein Therapiefehler prospektiv gezeigt |
Nicht etablierte Behandlung als aktiver Vergleich |
||
|
≥2 suffiziente Therapien mit Antidepressiva |
Anzahl Vortherapien |
|||
|
Himmelhoch 1982 |
± |
>1* oder mehr |
Nein |
Nicht zutreffend (Plc) |
|
Nolen 1985 |
+ |
4–5** |
Ja |
Ja |
|
Nolen 1988 |
+ |
4–5** |
Ja |
Ja |
|
Thase 1992 |
– |
1 |
Ja |
Ja |
|
Nolen 1993 |
+ |
2–3 |
Ja |
Nein |
|
Volz 1994a |
+ |
>2*** |
Nein |
Nein |
|
Birkenhäger 2004 |
± |
1–2# |
Ja |
Nein |
|
McGrath 2006 |
+ |
3## |
Ja |
Nein |
|
Nolen 2007 |
– |
1 |
Nein |
Ja |
* “had failed on trials on previous tricyclic antidepressants” und “had long-standing and chronic refractory depression”, ** zzgl. Schlafentzug, *** “at least two classes of antidepressants”, # 30% zwei Vortherapien (inkl. Li-Augmentation), ## teilweise inkl. kognitiver Verhaltenstherapie und Li-/T3-Augmentation
Studienqualität bezüglich Cochrane-Bewertung von Studienbias
Die Ergebnisse des Cochrane-Tools sind in Abbildung 1 wie gewohnt zusammengefasst. Hinsichtlich der Methode der Randomisierung war überwiegend keine Bewertung möglich, weil bis vor wenigen Jahren die Erwähnung von Details hierzu nicht als übliche Praxis galt. Selbst bei sonst teilweise sehr umfangreichen Beschreibungen der Methodik hielten die Autoren dies offensichtlich für nicht notwendig. Hinsichtlich der Verblindung ist das Ergebnis gemischt. Die Autoren waren sich der Problematik bewusst und mehrere gingen deshalb auch genauer auf die praktische Umsetzung der Verblindung ein. Offene Studien wurden als mit hohem Risiko eines systematischen Fehlers behaftet bewertet.
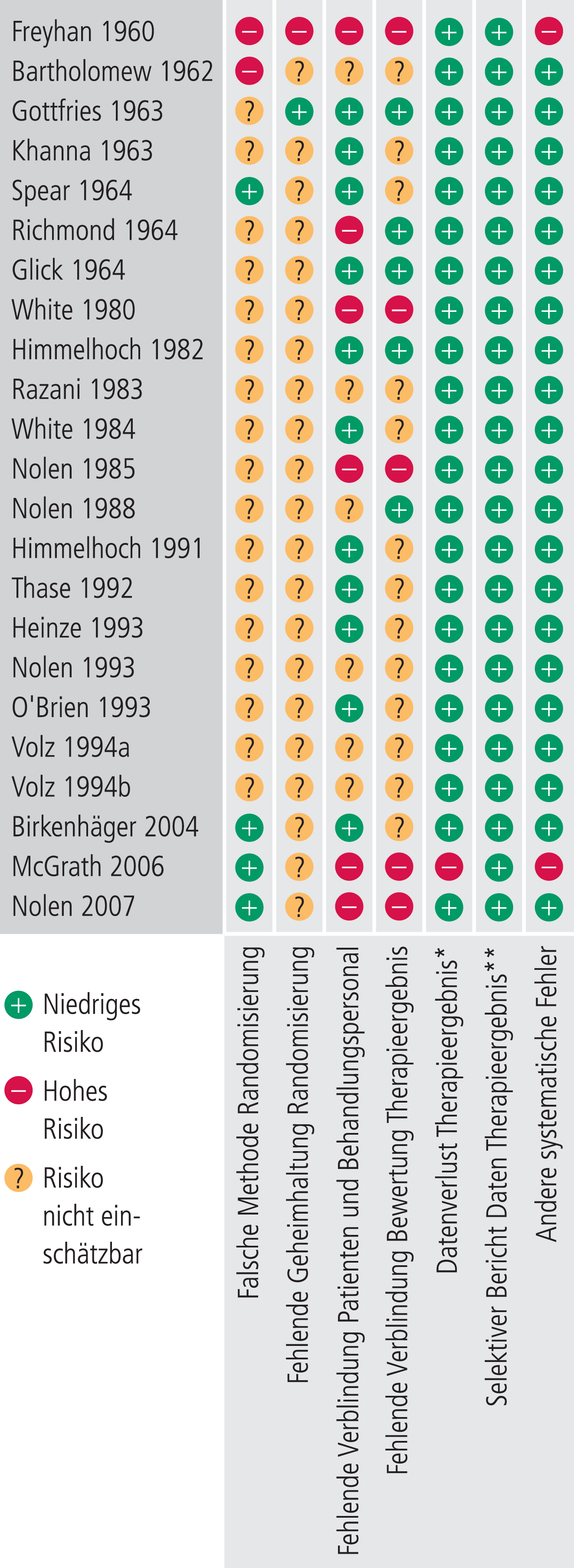
Abb. 1. Zusammenfassung des Risikos von Bias für kontrollierte Studien von TCP bei Depression entsprechend dem Cochrane Collaboration‘s Tool. * Unter Berücksichtigung dass möglicher Datenverlust wegen Therapieabbrechern für die Metaanalyse von begrenzter Bedeutung ist, da diese ohne zusätzliche Information generell als Nonresponder gezählt wurden. **Eine mögliche Selektivität der berichteten Daten ist von geringer Bedeutung für die Metaanalyse, da festgelegt war, ausschließlich die Responder-Rate zu verwenden.
Das Risiko von Datenverlust oder selektiver Darstellung der Daten wurde auch unter dem Aspekt der hier vorgegebenen Verwendung in der Metaanalyse eingeschätzt. Datenverlust durch Therapieabbrecher war deshalb von geringer Relevanz, da diese bei unbekanntem Grund einheitlich als Nonresponder festgelegt wurden. Die Beschränkung der Metaanalyse auf die auf einer kategorialen Variablen beruhenden Responder-Rate verringerte die Bedeutung eines Fehlers durch mögliche selektive Ergebnispräsentation in den Studien. Weiterhin stimmten in Studien mit Auswertung mehrerer Ergebnisvariablen (zumeist zusätzlich Ratingskalen als kontinuierliche Variable) diese zusätzlichen Ergebnisse mit den Daten der Responder-Raten überein. Für das Cochrane-Tool folgt daraus bezüglich Datenqualität eine sehr einheitliche Bewertung der Studien als mit eher geringem Risiko behaftet.
Auch insgesamt folgt ein relativ einheitliches Bild, aus dem sich nur drei Studien abheben. Die erste Studie von 1960 und etwas unerwartet die STAR*D-Studie fallen gegenüber dem Durchschnitt ab [12, 25]. Eine frühe Studie erhielt etwas überraschend die meisten Bewertungen als „geringes Risiko“ [15]. Dass diese Studie in der Bewertung nach EMA-Richtlinie nur das zweitniedrigste Ergebnis hat, ist kein Widerspruch, denn beide Bewertungen bilden unterschiedliche und sich ergänzende Inhalte ab.
Metaanalyse
Die therapeutischen Ergebnisse der einzelnen Studien sind in Tabelle 4 zusammengefasst.
Tab. 4. Ergebnisse kontrollierter Studien zu Tranylcypromin (TCP) bei Depression
|
Studie |
Verwendetes Responsekriterium |
TCP |
Kontrolle |
LogOV |
UG(LogOV) |
OG(LogOV) |
Therapieabbrecher [%] |
||||
|
R (ITT) |
NR (ITT) |
R (ITT) |
NR (ITT) |
TCP |
Kontrolle |
||||||
|
Freyhan 1960 |
Moderate bis starke Besserung gemäß globaler Bewertung |
6 |
8 |
60 |
48 |
–0,52 |
–1,64 |
0,61 |
n. d. |
n. d. |
|
|
Bartholomew 1962 |
Moderate bis starke Besserung gemäß globaler Bewertung |
28 |
23 |
20 |
31 |
0,63 |
–0,15 |
1,42 |
17,6 |
17,6 |
|
|
Gottfries 1963 |
Positiver und unsicherer Effekt gemäß globaler Bewertung |
10 |
15 |
7 |
18 |
0,54 |
–0,65 |
1,72 |
0,0 |
0,0 |
|
|
Khanna 1963 |
n. d. |
n d |
n. d. |
Keine Berechnung möglich |
0,0 |
6,7 |
|||||
|
Spear 1964 |
n. d. |
n. d. |
n. d. |
Keine Berechnung möglich |
8,1 |
12,2 |
|||||
|
Richmond 1964 |
Kombinierte Beurteilung globaler Bewertung/ HAMD |
8 |
12 |
9 |
31 |
0,83 |
–0,33 |
1,99 |
0,0 |
0,0 |
|
|
Glick 1964 |
Moderate bis starke Besserung gemäß globaler Bewertung |
2 |
7 |
1 |
12 |
1,23 |
–1,34 |
3,81 |
55,6 |
53,8 |
|
|
3 |
10 |
-0,05 |
–-2,08 |
1,98 |
53,8 |
||||||
|
White 1980 |
Abnahme HAMD um >14 |
8 |
3 |
7 |
2 |
-0,27 |
–2,33 |
1,78 |
9,1 |
11,1 |
|
|
Himmelhoch 1982 |
Moderate bis starke CGI-Besserung |
20 |
8 |
4 |
27 |
2,83 |
1,49 |
4,16 |
21,4 |
45,2 |
|
|
Razani 1983 |
Moderate bis starke CGI-Besserung |
13 |
8 |
16 |
14 |
0,35 |
–0,78 |
1,49 |
19,0 |
30,0 |
|
|
White 1984 |
Moderate bis starke CGI-Besserung |
25 |
38 |
19 |
40 |
0,32 |
–0,42 |
1,07 |
41,3 |
23,7 |
|
|
25 |
36 |
0,05 |
–0,77 |
0,66 |
34,4 |
||||||
|
Nolen 1985 |
50% HAMD-Besserung |
15 |
11 |
0 |
17 |
3,85 |
0,94 |
6,77 |
0,0 |
5,9 |
|
|
Nolen 1988 |
50% HAMD-Besserung |
10 |
9 |
2 |
13 |
1,98 |
0,24 |
3,72 |
10,5 |
6,7 |
|
|
Himmelhoch 1991 |
Moderate bis starke CGI-Besserung |
21 |
7 |
10 |
18 |
1,69 |
0,53 |
2,84 |
7,1 |
25,0 |
|
|
Thase 1992 |
50% HAMD- und moderat/starke CGI-Besserung, HAMD <10 |
9 |
3 |
1 |
3 |
2,20 |
–0,42 |
4,81 |
0,0 |
50,0 |
|
|
Heinze 1993 |
Moderate bis starke CGI-Besserung |
59 |
20 |
60 |
21 |
0,03 |
–0,68 |
0,74 |
15,2 |
4,9 |
|
|
Nolen 1993 |
50% HAMD-Besserung* |
5 |
12 |
10 |
12 |
–0,69 |
–2,03 |
0,65 |
11,8 |
0,0 |
|
|
O‘Brien 1993 |
HAMD <11 |
15 |
11 |
14 |
14 |
0,31 |
–0,76 |
1,38 |
19,2 |
25,0 |
|
|
Volz 1994a |
50% HAMD-Besserung* |
34 |
13 |
34 |
12 |
–0,08 |
–1,00 |
0,84 |
8,5 |
8,7 |
|
|
Volz 1994b |
50% HAMD-Besserung** |
6 |
5 |
20 |
15 |
–0,10 |
–1,47 |
1,26 |
9,1 |
2,9 |
|
|
Birkenhäger 2004 |
50% HAMD-Besserung |
17 |
22 |
18 |
20 |
–0,15 |
–1,05 |
0,75 |
7,7 |
18,4 |
|
|
McGrath 2006 |
50% QIDS-SR-Besserung*** |
7 |
51 |
12 |
39 |
–0,81 |
–1,83 |
0,21 |
46,6 |
21,6 |
|
|
Nolen 2007 |
50% IDS und/ oder CGI stark/sehr stark gebessert |
5 |
3 |
4 |
7 |
1,07 |
–0,82 |
2,96 |
25,0 |
54,5 |
|
* Bessere Response von TCP vs. Bro bei zwei anderen Responsekriterien; ** etwas schlechtere Response von TCP vs. Bro bei einem weiterem Responsekriterium; *** primärer Endpunkt war Remission (HAMD <8); R/NR: Anzahl Responder/Nonresponder; ITT: Intention-to-treat; LogOV: natürlicher Logarithmus des Odds-Verhältnisses; UG(LogOV), OG(LogOV): Unter- und Obergrenze des 95%-Konfidenzintervalls des LogOV; Abkürzung der Skalen siehe Tab. 2; n.d.: nicht definiert (keine Daten)
Für fünf von sechs Studien mit Placebo-Kontrolle lagen auswertbare Daten über die Zahl von Respondern und Nonrespondern vor. Dem Forestplot in Abbildung 2 ist zu entnehmen, dass TCP in jedem Fall Placebo überlegen war. Aber nur in einer Studie schneidet das 95%-Konfidenzintervall (95%-KI) die Nullachse nicht und ist demzufolge signifikant. Die Metaanalyse ergibt ein gemeinsames LogOV von 0,779 mit 95%-KI=0,324 bis 1,233 bei signifikantem Test auf formale Heterogenität (χ2=10,9; df=4; p<0,05). Die fünf Studien sind also inhomogen, was augenscheinlich auf eine Studie mit sehr starker Effektstärke zurückzuführen ist (Studie 5 in Abb. 2: LogOV =2,826; 95%-KI=1,494–4,158). Wesentlicher Unterschied dieser Studie ist die Behandlung von therapieresistenten Depressionen. Ohne die Studie bei therapieresistenter Depression wird bei nun homogenem Datenset (χ2=0,64; df=3; p>0,05) ein gemeinsames LogOV von 0,509 mit 95%-KI=0,026 bis 0,993 gefunden, welches die Nullachse nicht schneidet und demzufolge mit p<0,05 eine signifikante Differenz mit Überlegenheit von TCP widergibt. Unterstützt wird dieses Ergebnis durch die Ergebnisse der Studie ohne auswertbare Responder und Nonresponder, da diese entsprechend der eigenen Auswertung TCP als im Trend überlegen versus Placebo bewertet [22].
Für die gemeinsame Auswertung aller Vergleichsstudien von TCP mit Antidepressiva ergibt sich ähnlich den Placebo-kontrollierten Studien zunächst kein homogenes Datenset (χ2=29,72; df=17; p<0,05). Die Auswertung in Subgruppen von Studien mit und ohne TRD ist also plausibel. In zehn Studien ohne TRD war TCP nur in einer Studie Imipramin statistisch signifikant überlegen. Für neun Studien schneiden die 95%-KI die Nullachse bei leicht negativem oder leicht positivem LogOV (Abb. 3). Die Berechnung des gemeinsamen LogOV von 0,208 mit 95%-KI=–0,128 bis 0,544 (homogen: χ2=10,31, df=9, p>0,05) bestätigt die einfache grafische Auswertung der einzelnen Studien, das heißt gleiche Wirksamkeit von TCP und anderen Antidepressiva. Die Studie ohne auswertbare Daten zu Respondern und Nonrespondern erbrachte mit übereinstimmender Wirksamkeit von TCP mit Imipramin keine Abweichung von der Metaanalyse [40].
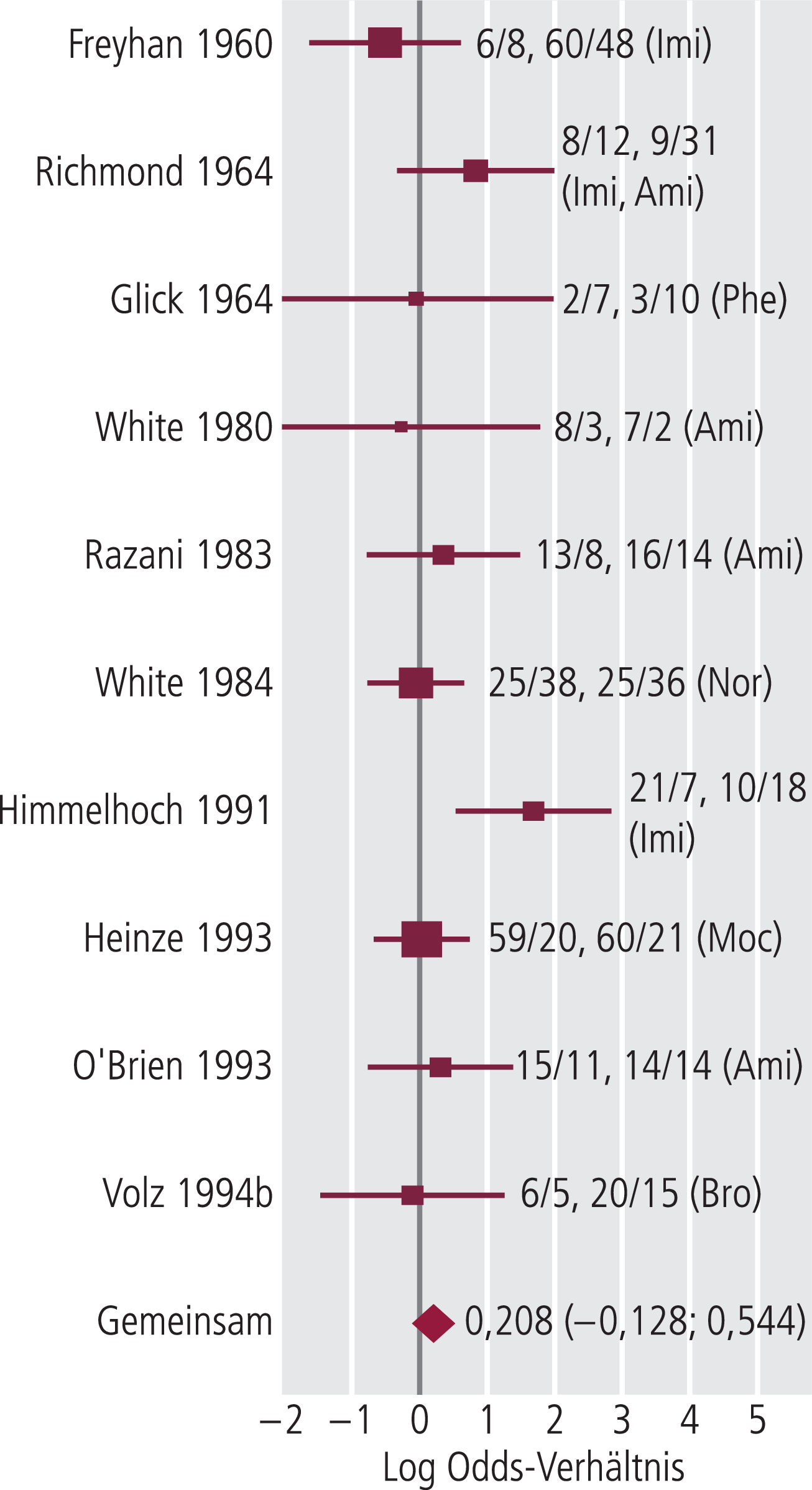
Abb. 3. Forestplot zur Metaanalyse kontrollierter Studien von Tranylcypromin (TCP) bei Depression mit Anzahl Responder/Nonresponder (erstes Paar TCP, zweites Paar aktive Kontrolle) der einzelnen Studien und Wert des gemeinsamen LogOV (95%-Konfidenzintervall); Studien ohne therapieresistente Depression (TRD); Abkürzungen aktive Kontrollen siehe Tab. 1
Die Auswertung der acht Studien zu therapieresistenter Depression mit aktiver Kontrolle resultiert in zwei homogenen Datensets, wenn entsprechend der Anforderung der EMA-Richtlinie für Depressionsstudien die Vergleichssubstanzen dahingehend eingeteilt werden, ob sie für TRD nicht etabliert (5-Hydroxytryptophan, Nomifensin, TCA nach einem MAO-Inhibitor, Lamotrigin) oder etabliert sind (MAO-Hemmer, Kombinationen von SSNRI mit Mirtazapin) [5, 20]. Gegenüber den Pseudoplacebos hat TCP entsprechend dem berechneten gemeinsamen LogOV von 1,976 mit 95%-KI=0,907 bis 3,045 (homogen: χ2=2,51; df=3; p>0,05) eine positive und hoch signifikante Effektstärke (Abb. 4). Verglichen mit anderen MAO-Inhibitoren und der Kombination ist es gleich wirksam: gemeinsames LogOV =–0,366 mit 95%-KI=–0,869 bis 0,137 (homogen: χ2=1,54; df=3; p>0,05) (Abb. 5). Die gemeinsame Auswertung aller acht Studien ergab ein inhomogenes Datenset.
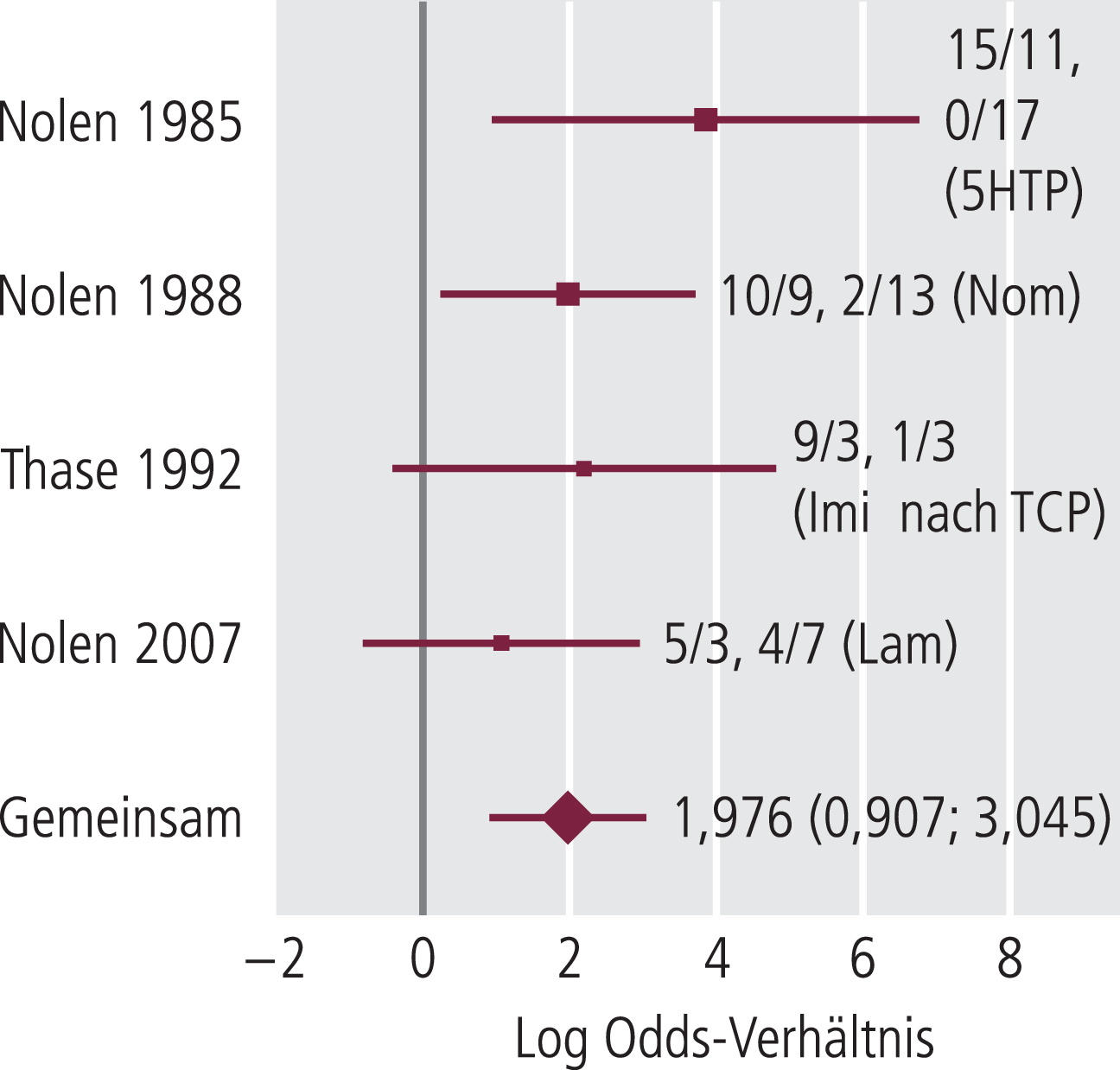
Abb. 4. Forestplot zur Metaanalyse kontrollierter Studien von Tranylcypromin (TCP) bei therapieresistenter Depression (TRD) mit Anzahl Responder/Nonresponder (erstes Paar TCP, zweites Paar aktive Kontrolle – nicht etabliert bei TRD) der einzelnen Studien und Wert des gemeinsamen LogOV (95%-Konfidenzintervall), Abkürzungen aktive Kontrolle siehe Tab. 1.
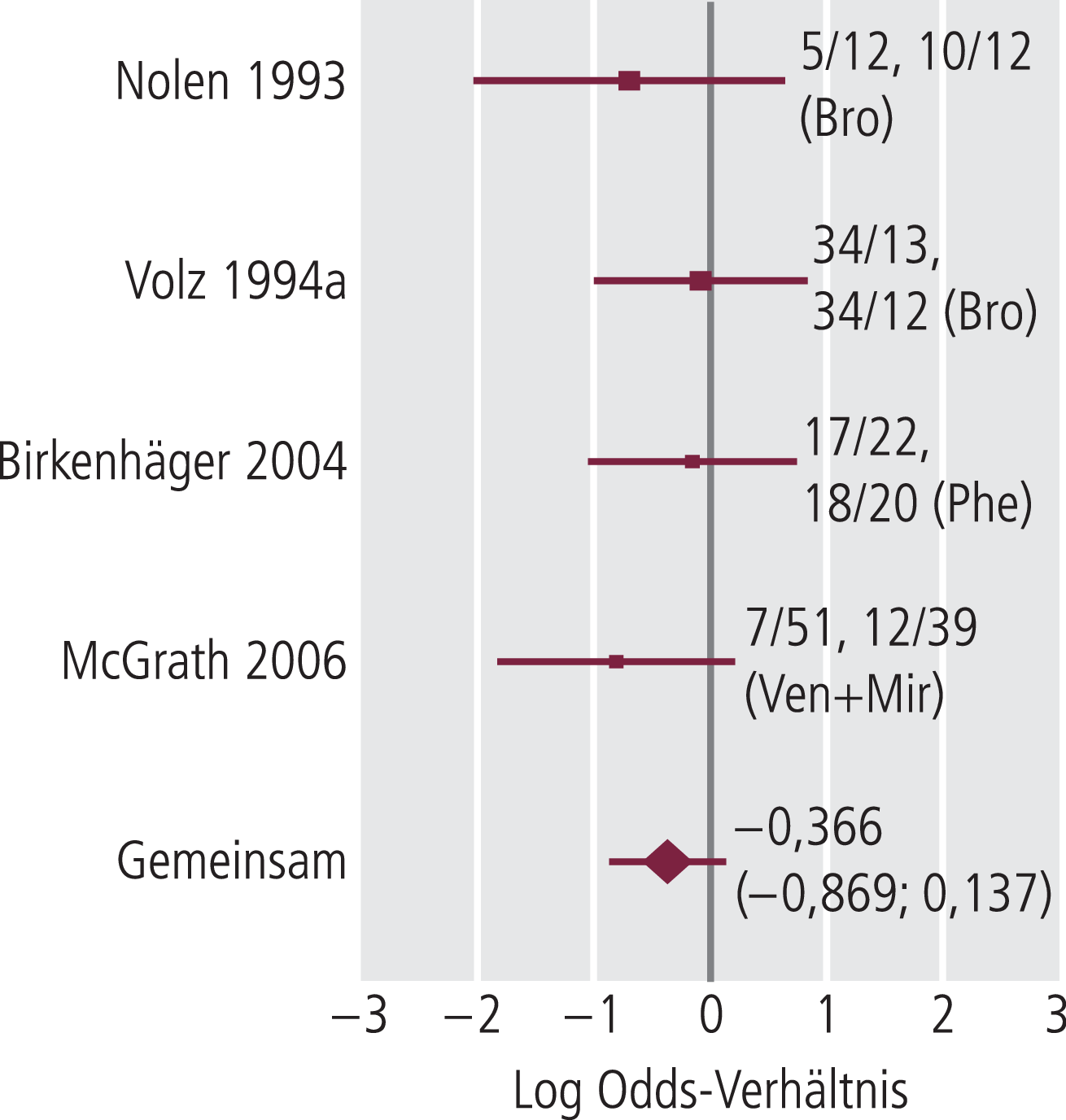
Abb. 5. Forestplot zur Metaanalyse kontrollierter Studien von Tranylcypromin (TCP) bei therapieresistenter Depression (TRD) mit Anzahl Responder/Nonresponder (erstes Paar TCP, zweites Paar aktive Kontrolle – etabliert bei TRD) der einzelnen Studien und Wert des gemeinsamen LogOV (95%-Konfidenzintervall), Abkürzungen aktive Kontrolle siehe Tab. 1.
Sensitivitätsanalysen
In der Metaanalyse der Placebo-kontrollierten Studien ohne therapieresistente Depression (Abb. 2, Nr. 1 bis 4) wird bei Verzicht auf die Studie mit der hier geringsten Qualität nach EMA-Richtlinie [15] die Signifikanz nun knapp verfehlt, es folgt ein gemeinsames LogOV von 0,504 mit 95%-KI=–0,025 bis 1,033 (homogen: χ2=0,63; df=2; p>0,05). Da eine Placebo-kontrollierte Studie mit leichter Überlegenheit von TCP keine Daten für die Metaanalyse enthielt, ist davon auszugehen, dass eine Einbeziehung dieser Studie dann wieder zu einem signifikanten 95%-KI führen würde [22]. Alle Placebo-kontrollierten Studien waren doppelblind.
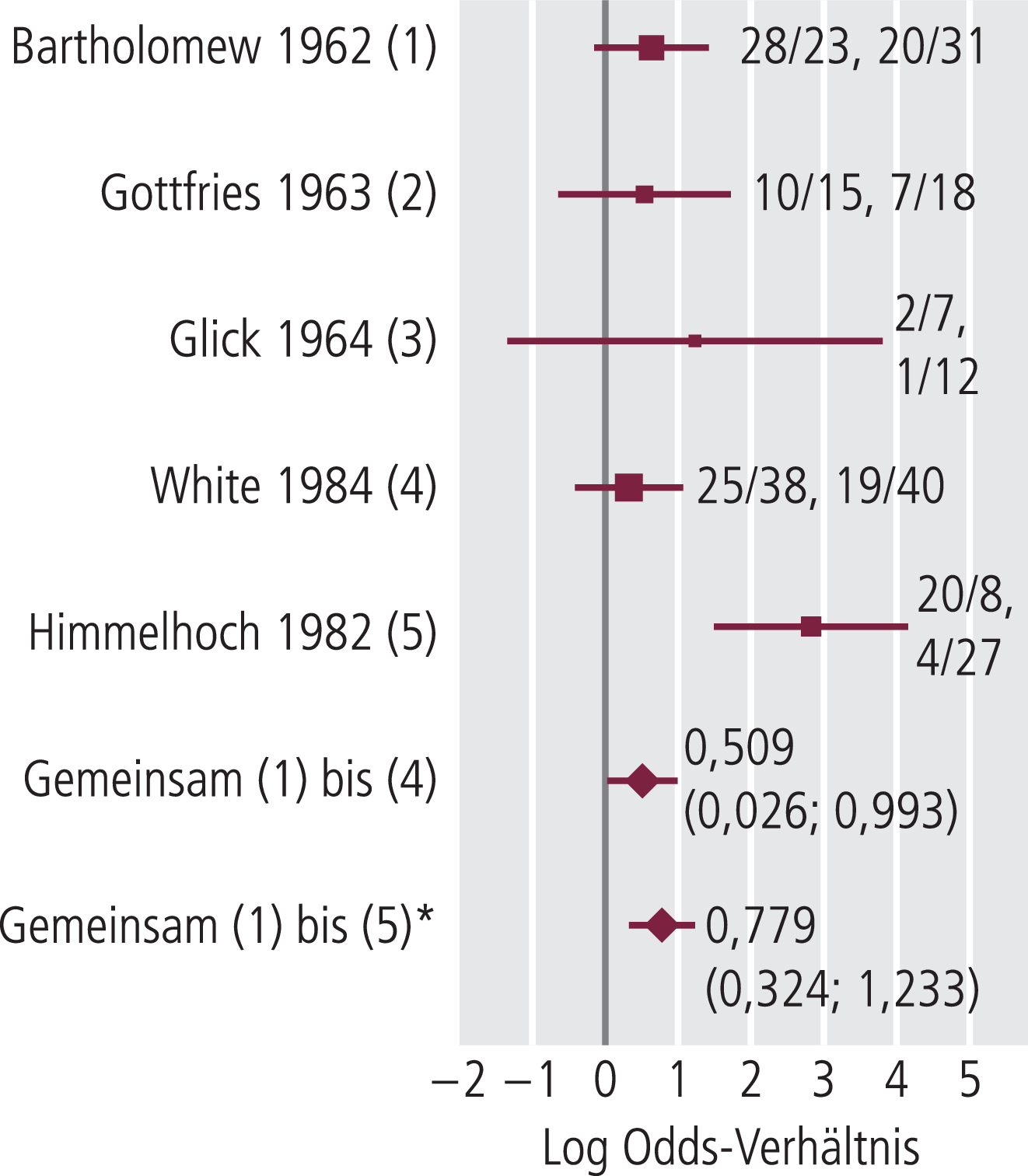
Abb. 2. Forestplot zur Metaanalyse Placebo-kontrollierter Studien von Tranylcypromin (TCP) bei Depression mit Anzahl Responder/Nonresponder (erstes Paar TCP, zweites Paar Placebo) der einzelnen Studien und Werten des gemeinsamen LogOV (95%-Konfidenzintervall); Studie 5 bei therapieresistenter Depression (TRD); *nicht homogen
Wird in der Metaanalyse von TCP vs. Antidepressiva ohne therapieresistente Depression (Abb. 3) die Studie mit dem geringsten Qualitätswert weggelassen [12], ergibt sich mit einem gemeinsamen LogOV von 0,279 und 95%-KI=–0,073 bis 0,631 (homogen: χ2=8,58; df=8; p>0,05) keine Änderung des Ergebnisses. Ein Vergleich von TCP nur mit den TCA dieses Sets von Studien resultiert in einem gemeinsamen LogOV von 0,425 mit 95%-KI=–0,009 bis 0,859 (homogen: χ2=7,28; df=5; p>0,05), zeigt also nun nahezu eine signifikante Überlegenheit von TCP gegenüber TCA. Die Studien des Vergleichs von TCP mit anderen MAO-Hemmern ergeben mit einem gemeinsamen LogOV von –0,002 bei einem 95%-KI=–0,603 bis 0,599 (homogen: χ2=0,03; df=2; p>0,05) gleiche Wirksamkeit. Da die Mehrzahl der Antidepressiva-kontrollierten Studien ohne therapieresistente Depression doppelblind waren (7 von 9, eine Studie einfach verblindet), wurde auf eine separate Auswertung verzichtet.
Eine Beschränkung der Analyse von Studien bei therapieresistenter Depression auf die beiden Studien mit Erfüllung aller drei Anforderungen der EMA-Richtlinie für TRD [31, 32] bestätigt das Ergebnis von Abbildung 4, das heißt gemeinsames LogOV von 2,471 mit 95%-KI=0,977 bis 3,965 (homogen: χ2=1,17; df=1; p>0,05). Nur eine dieser beiden Studien war doppelblind, ergab aber auch allein eine signifikante Überlegenheit von TCP. Der Vergleich von TCP mit anderen MAO-Hemmern bei therapieresistenter Depression (vgl. Abb. 5) ergibt mit einem gemeinsamen LogOV von –0,225 und 95%-KI=–0,803 bis 0,354 (homogen: χ2=0,59; df=2; p>0,05) wie schon zuvor in Studien ohne TRD gleiche Wirksamkeit. Alle drei Studien waren doppelblind.
Diskussion
Zur Methode der Bewertung der Studienqualität entsprechend der EMA-Richtlinie für Antidepressiva-Studien
Die inhaltliche Heterogenität der gefundenen 23 kontrollierten Studien zu TCP bei Depression ist erwartungsgemäß sehr hoch. Wichtige Faktoren für das Therapieergebnis wie Subtypen der Depression, therapieresistente Depression, Dosis von TCP, Schweregrad der Depression, Dauer der Behandlung, Kontrollsubstanz, Komorbidität, Vor- und Kotherapien sowie Verblindung, Randomisierung und Methode der Bewertung des Therapieerfolgs unterscheiden sich nachweislich teilweise stark. Zwischen diesen Faktoren können Abhängigkeiten bestehen. Weitere unbekannte Faktoren sind möglich, die nicht erfasst sind, beispielsweise unterschiedliche Erwartungshaltung von Therapeuten und Patienten auch im Kontext des großen Zeitraumes von 47 Jahren, in dem die Studien publiziert wurden.
Trotzdem ist bei aller Begrenztheit ein Versuch der Bewertung des Studiendesigns nach einheitlichen Kriterien sinnvoll, um einen groben Überblick zu ermöglichen und grundlegende Trends zu erkennen. Das schließt die Kodifizierung der einzelnen Kriterien mit Zuordnung von Einzelwerten und einem Gesamtwert, die die Qualität der Studie abbilden, ein. Selbstverständlich ist die Operationalisierung der einzelnen Kriterien eine Herausforderung und es stellt sich die Frage der inhaltlichen Validität des Gesamtwerts, vor allem hinsichtlich der Zuordnung von gewichteten Einzelwerten für das jeweilige Kriterium. Zur Vereinfachung wurden deshalb überwiegend nur die Werte Null und Eins verwendet, abgesehen von höheren Werten für offensichtlich bedeutsame Kriterien wie Verblindung, Randomisierung und Methode der Beurteilung des Therapieerfolgs. Die Reliabilität des Instruments wurde nicht untersucht. Als Grundlage erscheint die EMA-Richtlinie zur Durchführung kontrollierter Studien bei Depression am besten geeignet. Damit besteht eine hohe Gewähr der inhaltlichen Validität zumindest in Bezug auf die Auswahl der Kriterien. Diese Richtlinie wurde auf der Basis allgemeiner studientheoretischer Überlegungen und mit der langen praktischen Erfahrung von Antidepressiva-Studien, nicht zuletzt auch der hier diskutierten Studien, entwickelt. Andere Richtlinien für Antidepressiva-Studien sind aber schon lange bekannt und stimmen weitgehend überein. Beispielsweise weicht selbst die FDA-Richtlinie von 1977 nur in wenigen Details ab, wie fehlende Beschränkung des Schweregrads der Depression, generell vier Wochen Therapiedauer ausreichend und keine Vorgabe von Responsekriterien [10]. Als Vereinfachung für die vorliegenden Studien zu TCP wurde auf die Einbeziehung eines Kriteriums Interraterreliabilität für Depressionsskalen und antidepressive Kotherapien (z.B. Psychotherapien) verzichtet, da diese ohnehin überwiegend nicht berichtet wurden. Berücksichtigt wurde dabei bezüglich notwendiger Interraterreliabilität (und Ratertraining), dass die TCP-Studien überwiegend monozentrische Studien sind.
Bei der Interpretation des Qualitätswerts einer Studie ist zu bedenken, dass einzelne Kriterien je nach Studienziel eine konservative oder antikonservative Ausrichtung haben können. Wenn beispielsweise die Forderung nach einer Mindestschwere der Erkrankung erhoben wird und bekannt ist, dass die Rekrutierung schwer erkrankter Patienten die Chancen, einen Therapieunterschied zu finden, erhöhen, wird dadurch die Chance auf Erfolg einer Placebo-kontrollierten Studie verbessert. Die Chance einer Antidepressiva-kontrollierten Studie kann dadurch aber verschlechtert werden. Denn die Placebo-kontrollierte Studie soll einen Therapieunterschied bestätigen. Die meisten Antidepressiva-kontrollierten Studien sollen lediglich Nichtunterlegenheit zeigen. Eine Placebo-kontrollierte Studie oder eine (der seltenen) Antidepressiva-kontrollierten Studien mit Überlegenheit als Studienziel sind also konservativ, wenn entgegen der Forderung der EMA-Richtlinie weniger schwer kranke Patienten einbezogen werden. Eine Durchsicht aller Kriterien ergibt, dass die Mehrzahl einen derartigen konservativen Charakter für Überlegenheitsstudien aufweist. Allein das Erfordernis der doppelten Verblindung ist im Grundsatz antikonservativ, weil die positive Erwartungshaltung einen nicht vorhandenen Therapieeffekt vortäuschen kann. Bis auf die doppelte Verblindung und teilweise auch Randomisierung sind die Qualitätskriterien von Antidepressiva-Studien also für Überlegenheitsstudien eher konservativ. Mit anderen Worten, der Forscher ist zwar „selbst schuld“, wenn durch schlechtes Design kein positives Studienergebnis der Überlegenheit gegen Placebo vorliegt, er wird aber zumindest kein falsch positives Ergebnis erzeugen. Die EMA-Richtlinie hilft hier lediglich, die Chance auf ein Studienergebnis mit Überlegenheit des Antidepressivums zu erhöhen, und zielt natürlich auf die Einhaltung ethischer Standards, da eine schlecht durchgeführte Studie unethisch ist. Für die zahlreichen Antidepressiva-kontrollierten Studien mit dem Ziel Nichtunterlegenheit kann umgekehrt schlechte Studienqualität das Studienziel begünstigen.
Schließlich ist zu bemerken, dass die Bewertung so vorgenommen wurde, dass keine Studie von vorn herein einen Gesamtwert von Null nur aufgrund Fehlschlagens in einem Kriterium, als kategoriales Kriterium, erhalten kann. Andere Metaanalysen werden oft nur nach Auswahl doppelblinder und randomisierter Studien durchgeführt. Hier sollte dies wenn notwendig – aufgrund der Besonderheit des großen Zeitraums der Studien mit Einbeziehung von Studien aus den frühen 60er-Jahren – erst in nachfolgenden Schritten der Sensitivitätsanalyse und in der Diskussion erfolgen. Diese Studien waren teilweise durch eine Quasi-Verblindung gekennzeichnet. Beispielsweise war es noch möglich, dass die Patienten (auch) durch fehlende Information über die Durchführung der Studie an sich verblindet waren [15]. Oder primäres Studienziel war nicht die Auffindung von Unterschieden der Wirksamkeit zwischen zwei Antidepressiva, sondern von unterschiedlichen Wirkqualitäten, wodurch eine Erwartungshaltung bezüglich Überlegenheit im Sinne der Metaanalyse nicht gegeben ist.
Studienqualität
Im grundsätzlichen Trend ist die gefundene Studienqualität der kontrollierten Studien von TCP bei Depression gut bis sehr gut. Einschränkend wäre noch die aufgrund fehlender Daten fehlende Bewertung des Studienmonitorings anzuführen, die nach heutigen Maßstäben in der Mehrzahl wahrscheinlich bestenfalls rudimentär vorlag. Nur für die Studien des Vergleichs mit neu eingeführten Antidepressiva der 90er-Jahre (Moclobemid, Brofaromin) lässt sich ein adäquates Monitoring vermuten. Weiterhin ließ sich die Qualität der Randomisierung und Verblindung entsprechend den heutigen Standards des Cochrane-Tools nur für wenige Studien vollständig bewerten. Die Patientenzahl ist mit im Durchschnitt 30 TCP-Patienten pro Studie nur gering (Maximum Placebo-kontrollierte Studien: n=63 [49], Maximum Antidepressiva-kontrollierte Studien: n=79 [16]) und nicht vergleichbar mit heutigen Antidepressiva-Studien des Wirksamkeitsnachweises, wo beispielsweise für Vortioxetin pro Therapiearm 100 bis 150 Patienten rekrutiert wurden.
Die geringere Qualität der frühen Studien kann akzeptiert werden, da hier überwiegend die Ergebnisse der Placebo-kontrollierten Studien bedeutsam sind. Lücken im Studiendesign dieser Studien haben deshalb schlechtestenfalls die gefundene Effektstärke geschmälert. Das trifft insbesondere auf die notwendige Krankheitsschwere zu Studienbeginn und das flexible Dosisdesign für den bestmöglichen Nachweis eines Vorteils gegenüber Placebo zu [21]. Nur zwei Placebo-kontrollierte Studien schlossen explizit Patienten mit geringer Krankheitsschwere aus [18, 49] und nur drei Studien ermöglichten therapeutisch sinnvolle Dosisanpassungen [2, 14, 49]. Die erste Studie von 1960 mit zugleich geringstem Qualitätswert aller TCP-Studien ist, wie gezeigt, für die Metaanalyse verzichtbar [12]. Eine pauschale Entwertung der frühen Studien aufgrund des Studiendesigns ist demzufolge zu verwerfen. Überraschend ist die unter den moderneren Studien verhältnismäßig schlechte Qualität der STAR*D-Studie mit, bezogen auf TCP, dem drittschlechtesten Qualitätswert von 16 TCP-Studien entsprechend der Bewertung nach EMA-Richtlinie [25]. Auch im Cochrane-Tool fällt die STAR*D-Studie ab.
Für TCP mit klinischer Anwendung vorwiegend bei therapieresisenter Depression ist es wichtig, dass zwei Studien alle Kriterien für Antidepressiva-Studien bei TRD erfüllen, davon eine doppelblinde Studie [31, 32]. Die Qualitätswerte dieser beiden Studien sind nur scheinbar niedrig, beispielsweise verglichen mit der STAR*D-Studie, da sie nicht explizit auf ambulante Patienten beschränkt waren. Die Relevanz dieses Kriteriums ist aber für TCP und therapieresistente Depression, wie schon oben diskutiert, gering. Schließlich liegt eine randomisierte und doppelblinde Placebo-kontrollierte Studie von TCP bei therapieresistenter Depression mit hoher allgemeiner Studienqualität vor [18].
Metaanalyse
Die Metaanalyse bestätigt für TCP eine höhere Wirksamkeit als Placebo in der Therapie depressiver Patienten, insbesondere auch bei therapieresistenter Depression (jeweils p<0,05). Zu berücksichtigen ist auch, dass die Metaanalyse von Placebo-kontrollierten Studien aufgrund der Auswertung von ITT-Daten konservativ angelegt ist [13]. Die gefundene Effektstärke als gemeinsames LogOV von 0,509 mit 95%-KI=0,026 bis 0,993 rangiert dabei am oberen Ende des Vergleichs von Antidepressiva mit Placebo, wofür ein gemeinsames LogOV von 0,39 mit 95%-KI=0,24 bis 0,54 beschrieben wurde [3]. TCP ist gleich wirksam wie trizyklische Antidepressiva und andere MAO-Hemmer bei Depression und ebenfalls gleich wirksam wie andere MAO-Hemmer bei therapieresistenter Depression.
Wie für andere wirksame Antidepressiva ist damit in der Gesamtschau der Metaanalyse das Erfordernis einer Überlegenheit gegenüber Placebo und gleicher Wirksamkeit wie aktive Vergleichssubstanzen für TCP gegeben. Zum Vergleich mit SSRI, SSNRI und Mirtazapin fehlen Studien. Das erscheint zunächst nur als theoretischer Mangel, da TCP nicht am Therapiebeginn einer Depression verordnet wird. Der fehlende Vergleich mit diesen heute üblichen Antidepressiva der ersten Wahl stellt aber auch einen praktischen Mangel dar, wenn es um die Auswahl des Antidepressivums bei einem geplanten Switch bei therapieresistenter Depression nach Fehlschlagen mehrerer Antidepressiva geht. Hier liefert die Metaanalyse immerhin indirekte Evidenz, da für TCP eine gute Wirksamkeit bei therapieresistenter Depression auch nach SSRI mit einem gemeinsamen LogOV von 1,976 und mit 95%-KI=0,907 bis 3,045 (p<0,05) bestätigt wurde. Theoretische Überlegungen favorisieren TCP für den Switch, da die Verordnung von TCP einen grundlegenden Wechsel des Wirkungsmechanismus mit MAO als neuen pharmakologischen Ansatzpunkt beinhaltet.
Die S3-Leitlinie Unipolare Depression der DGPPN diskutiert, dass der Wechsel des Antidepressivums die häufigste Vorgehensweise bei therapieresistenter Depression ist und ein Wechsel des Wirkungsmechanismus empfohlen wird [9]. Die Rationale eines Switches auf TCP lässt sich theoretisch auch aus weiteren Studien ableiten, beispielsweise war die Aktivität von MAO-A im ZNS bei therapieresistenter Depression nach SSRI erhöht [26]. Für jeden Patienten mit therapieresistenter Depression ist es deshalb zweckmäßig, eine Therapie mit TCP in Betracht zu ziehen.
Wichtige Studien
Trotz der geringen Teststärke sollen ausgewählte Studien einzeln diskutiert werden. Zwei Studien waren dreiarmig mit gleichzeitiger Placebo- und Antidepressiva-Kontrolle als verbessertes Studiendesign im Sinne sogenannter „blinderer“ Studien [36]. Wenn einzeln statistisch auch nicht signifikant, war TCP mit Responderraten von 22,2% und 39,7% überlegen gegenüber Placebo mit entsprechend 7,7% und 32,2%. Die Responderraten für die aktive Kontrolle waren TCP sehr ähnlich mit entsprechend 23,1% (Phenelzin) und 41,0% (Nortriptylin) [14, 49]. Im Trend zeichnet sich also die Erfüllung dieser Anforderung zur Wirksamkeit schon in den einzelnen Studien mit gleichzeitiger Placebo- und aktiver Kontrolle ab. Die STAR*D-Studie hat mit nur 12,1% die mit Abstand niedrigste Responderrate aller neun Studien in TRD [25]. Die übrigen acht Studien haben eine mittlere Responderrate von 58,1% (29,4–75,0). Als Ursache ist ein Nocebo-Effekt besonders für TCP zu diskutieren, denn es wird mehr als einmal explizit ausgeführt, dass Ärzte und Patienten in dieser offenen Studie „uncomfortable“ mit dem MAO-Hemmer waren. Weiterhin mussten nur die Patienten der TCP-Gruppe und nicht in der Vergleichsgruppe die Tyramin-arme Diät einhalten. Folgerichtig war trotz gleicher Nebenwirkungen (Häufigkeit, Schweregrad, Belastung) die Abbruchrate aufgrund von Nebenwirkungen für TCP mit 41,4% sehr hoch und signifikant höher als für die Kombination (21,6%, p<0,05). Im Cochrane-Tool führte dieses Design zur Einschätzung als hohes Risiko für systematische Fehler in den Kriterien „Verblindung“, „andere systematische Fehler“ und „Datenverlust Therapieergebnis“. Auch die Responderrate der Lithium-Augmentation war in der STAR*D-Studie mit 16,2% unerwartet niedrig [27]. Wichtigstes Ergebnis der STAR*D-Studie für TCP ist deshalb vielleicht die Bestätigung der Notwendigkeit einer guten Behandlungsmotivation. In den beiden niederländischen Studien der 80er-Jahre wurde schon ein ähnliches Konzept der sequenziellen Studien bis hin zu TCP ähnlich dem STAR*D-Projekt verfolgt. Hier lag die Responderrate für TCP zusammen bei 55,6% gegenüber 6,2% für Placebo. Wichtig ist, dass auch die Auswertung des Verlaufs der HAMD signifikante Vorteile für TCP ergab (p<0,05). Da diese beiden Studien aktive Placebos als Kontrollen verwendeten und auch weiterhin wichtigen Qualitätskriterien von Antidepressiva-Studien entsprachen, stellen sie derzeit eine maßgebende wissenschaftliche Evidenz der Wirksamkeit von TCP bei therapieresistenter Depression dar [31, 32].
Hervorzuheben ist schließlich die einzige Placebo-kontrollierte Studie von TCP bei therapieresistenter Depression [18]. Randomisiert und doppelblind wurden insgesamt 59 ambulante Patienten mit überwiegend atypischer Depression sehr ähnlich den später definierten Columbia-Kriterien untersucht [35]. Außerdem hatten 29 Patienten die Depression im Rahmen einer bipolaren Erkrankung und 19 weitere Patienten ein zusätzliches Borderline-Syndrom. Die Patienten waren mindestens moderat krank und in einem chronischen und therapierefraktären Zustand nach erfolglosen Vorbehandlungen mit TCA. Spezielle Maßnahmen wie getrennte psychopathologische Bewertung und Bewertung/Therapie von Nebenwirkungen wurden zur Verhinderung einer Entblindung unternommen. Nach sechs Wochen mit 40 mg/Tag TCP oder Placebo wurde nicht nur eine deutlich höhere Responderrate von 71,4% für TCP gegenüber 12,9% für Placebo gefunden (p<0,001), sondern auch signifikant bessere Verläufe für TCP in verschiedenen Ratingskalen der Depression inklusive Subskalen (NPRL, p<0,01), NPRL-Depression (p<0,02), NPRL-Angst (p<0,05), KDS-Depression (p<0,001). Die Autoren betonen dabei das schnelle Ansprechen mit TCP schon nach einer Woche in einigen Ratings wie NPRL (p<0,005) und NPRL-Depression (p<0,01). 14 Patienten (45,2%) unter Plazebo und sechs (21,4%) unter TCP brachen die Therapie ab (p<0,05). Die somatischen Beschwerden der Patienten nahmen unter TCP ab. Hervorhebenswert ist, dass die Autoren im Gegensatz zu gängigen Empfehlungen die Einstellung auf TCP auch für ambulante Patienten als möglich und sinnvoll einschätzen.
Neben der üblichen Spontanerfassung und tiefergehenden Tests zu Nebenwirkungen (EKG, klinische Chemie, Blutdruck, Körpergewicht, sexuelle Funktionsstörungen) untersuchten nicht wenige Studien im wissenschaftlichen Begleitprogramm weitere wichtige und interessante Faktoren der Therapie mit TCP wie MAO-B-Hemmung in den Thrombozyten, Plasmaspiegel von TCP, Schlafprofile, Kombination mit TCA, Erhaltungstherapie mit TCP und andere, die zum heutigen Verständnis der klinischen Psychopharmakologie von TCP beitragen.
Schlussfolgerung
Erste klinische Erfahrungen mit Tranylcypromin wurden in einer unkontrollierten Studie mit 52 depressiven Patientinnen schon 1959 publiziert [34, 45]. Als Extrakt sehr zahlreicher und sehr unterschiedlicher weiterer Studien und Erfahrungsberichte stellen die hier diskutierten 23 kontrollierten Studien bei Depression einen Versuch der Beschreibung und Bewertung von TCP mit strengeren wissenschaftlichen Methoden dar. Die Metaanalyse liefert erstmals eine systematische Übersicht und statistische Aufbereitung dieses Kernstücks der klinischen Forschung zu TCP. Therapieentscheidungen werden weiter versachlicht. Wenn in der individuellen Behandlungssituation eines Patienten TCP erwogen wird, sprechen diese wissenschaftlichen Daten der Wirksamkeit für einen Versuch mit dem MAO-Hemmer. Der Erwerb eigener praktischer Therapieerfahrungen bleibt dabei aber die entscheidende Komponente.
Interessenkonflikterklärungen
Die Autoren geben folgende potenziellen Interessenkonflikte an:
SU: Mitarbeiter von Aristo Pharma
RR: Vortragshonorar, Reisekostenunterstützung und Forschungsbeihilfe von Aristo Pharma
PS: Honorare für die Beratung oder Teilnahme an einem Expertenbeirat im Rahmen des EU-Projekts CoCA (Comorbid conditions of attention deficit/hyperactivity disorder) und Forschungsbeihilfe von der EU (DISCHARGE-Studie)
MA: Honorare für die Beratung oder Teilnahme an einem Expertenbeirat von Aristo Pharma, Bristol-Myers Squibb, Deutsche Bank, Janssen-Cilag, Lundbeck, Merz; Vortragshonorare von Aristo, Bristol-Myers Squibb, Deutsche Bank, Gilead, Helios Media, HRM Forum, Janssen-Cilag, Johanniterorden, Lundbeck, MSD, Ostdeutscher Sparkassenverband, Pusch Wahlig Legal, Schindler, Servier, ViiV; Reisekostenunterstützung von Alfred Herrhausen Gesellschaft, Lundbeck, Servier; Forschungsbeihilfe von Alfred Herrhausen Gesellschaft, Aristo, Servier; sonstige Unterstützung von Servier
Literatur
1. Atkinson RM, Ditman KS. Tranylcypromine: A review. Clin Pharmacol Ther 1965;6:631–55.
2. Bartholomew AA. An evaluation of tranylcypromine (“Parnate”) in the treatment of depression. Med J Aust 1962;49:655–62.
3. Bauer M, Pfennig A, Severus E, Whybrow PC, et al. World Federation of Societies of Biological Psychiatry (WFSBP) guidelines for biological treatment of unipolar depressive disorders, part 1: update 2013 on the acute and continuation treatment of unipolar depressive disorders. World J Biol Psychiat 2013;14:334–85.
4. Birkenhäger TK, van den Broek WW, Mulder PG, Bruijn JA, et al. Efficacy and tolerability of tranylcypromine versus phenelzine: a double-blind study in antidepressant-refractory depressed inpatients. J Clin Psychiat 2004;65:1505–10.
5. Bschor T, Bauer M, Adli M. Chronic and treatment resistant depression – diagnosis and stepwise therapy. Dtsch Arztebl Int 2014;111:766–76.
6. Chiuccariello L, Houle S, Miler L, Cooke RG, et al. Elevated monoamine oxidase A binding during major depressive episodes is associated with greater severity and reversed neurovegetative symptoms. Neuropsychopharmacol 2014;39:973–80.
7. Committee for Medicinal Products for Human Use (CHMP). Guideline on clinical investigation of medicinal products in the treatment of depression. 2013, www.ema.europa.eu/docs/en_GB/document_library/Scientific_guideline/2013/05/WC500143770.pdf (Zugriff am 20.06.2017).
8. D’Agostino RB, Weintraub M. Meta-analysis: a method for synthesizing research. Clin Pharmacol Ther 1995;58:605–16.
9. DGPPN. S3-Leitlinie/Nationale Versorgungsleitlinie Unipolare Depression, 2015.
10. FDA. Guidelines for the clinical evaluation of psychotropic drugs – antidepressant and antianxiety drugs. Psychopharmacol Bull 1978;14:45–63.
11. Flockhart DA. Dietary restrictions and drug interactions with monoamine oxidase inhibitors: an update. J Clin Psychiat 2012;73(Suppl 1):17–24.
12. Freyhan FA. The modern treatment of depressive disorders. Am J Psychiat 1960;116: 1057–64.
13. Fritze J, Möller HJ. Design of clinical trials of antidepressants: should a placebo control arm be included? CNS Drugs 2001;15:755–64.
14. Glick BS. Double-blind study of tranylcypromine and phenelzine in depression. Dis Nerv Syst 1964;25:617–9.
15. Gottfries CG. Clinical trial with the monoamino oxidase inhibitor tranylcypromine on a psychiatric clientele. Acta Psychiat Scand 1963;39:463–72.
16. Heinze G, Rossel L, Gabelic I, Galeano-Munoz J, et al. Double-blind comparison of moclobemide and tranylcypromine in depression. Pharmacopsychiatry 1993;26:240–5.
17. Higgins JP, Altman DG, Gøtzsche PC, Jüni P, et al. The Cochrane Collaboration’s tool for assessing risk of bias in randomised trials. BMJ 2011;343:d5928.
18. Himmelhoch JM, Fuchs CZ, Symons BJ. A double-blind study of tranylcypromine treatment of major anergic depression. J Nerv Ment Dis 1982;170:628–34.
19. Himmelhoch JM, Thase ME, Mallinger AG, Houck P. Tranylcypromine versus imipramine in anergic bipolar depression. Am J Psychiat 1991;148:910–6.
20. Hoencamp E, Haffmans PM, Dijken WA, Hoogduin CA, et al. Brofaromine versus lithium addition to maprotiline. A double-blind study in maprotiline refractory depressed outpatients. J Affect Disord 1994;30:219–27.
21. Khan A, Schwartz K. Study designs and outcomes in antidepressant clinical trials. Essent Psychopharmacol 2005;6:221–6.
22. Khanna JL, Pratts S, Burdzik EG, Chaddha RL. A study of certain effects of tranylcypromine, a new antidepressant. J New Drugs 1963;3:227–32.
23. Laux G, Becker T, Müller U. 7.4.1 Indikationen. In: Riederer P, Laux G, Pöldinger W (Hrsg.). Neuro-Psychopharmaka. Ein Therapiehandbuch, Band 3 Antidepressiva, Phasenprophylaktika und Stimmungsstabilisierer. Wien, New York: Springer, 2002: 489–507.
24. Leuchter AF, McCracken JT, Hunter AM, Cook IA, et al. Monoamine oxidase A and catechol-O-methyltransferase functional polymorphisms and the placebo response in major depressive disorder. J Clin Psychopharmacol 2009;29:372–7.
25. McGrath PJ, Stewart JW, Fava M, Trivedi MH, et al. Tranylcypromine versus venlafaxine plus mirtazapine following three failed antidepressant medication trials for depression: a STAR*D report. Am J Psychiat 2006;163:1531–41.
26. Meyer JH, Wilson AA, Sagrati S, Miler L, et al. Brain monoamine oxidase A binding in major depressive disorder: relationship to selective serotonin reuptake inhibitor treatment, recovery, and recurrence. Arch Gen Psychiatry 2009;66:1304–12.
27. Möller HJ. Das Problem der Heterogenität zwischen in den USA und nicht in den USA durchgeführten Antidepressivastudien. Psychopharmakotherapie 2014;21:211–8.
28. Neyeloff JL, Fuchs SC, Moreira LB. Meta-analyses and Forest plots using a microsoft excel spreadsheet: step-by-step guide focusing on descriptive data analysis. BMC Res Notes 2012;5:52.
29. Nolen WA, Haffmans PM, Bouvy PF, Duivenvoorden HJ. Monoamine oxidase inhibitors in resistant major depression. A double-blind comparison of brofaromine and tranylcypromine in patients resistant to tricyclic antidepressants. J Affect Disord 1993;28: 189–97.
30. Nolen WA, Kupka RW, Hellemann G, Frye MA, et al. Tranylcypromine vs. lamotrigine in the treatment of refractory bipolar depression: a failed but clinically useful study. Acta Psychiatr Scand 2007;115:360–5.
31. Nolen WA, van de Putte JJ, Dijken WA, Kamp JS. L-5HTP in depression resistant to re-uptake inhibitors. An open comparative study with tranylcypromine. Br J Psychiat 1985;147:16–22.
32. Nolen WA, van de Putte JJ, Dijken WA, Kamp JS, et al. Treatment strategy in depression. II. MAO inhibitors in depression resistant to cyclic antidepressants: two controlled crossover studies with tranylcypromine versus L-5-hydroxytryptophan and nomifensine. Acta Psychiatr Scand 1988;78:676–83.
33. O’Brien S, McKeon P, O’Regan M. The efficacy and tolerability of combined antidepressant treatment in different depressive subgroups. Br J Psychiatry 1993;162:363–8.
34. Petersen MC, McBrayer JW. Treatment of affective depression with trans-dl-phenylcyclopropylamine hydrochloride; a preliminary report. Am J Psychiatry 1959;116:67–8.
35. Quitkin FM. Depression with atypical features: Diagnostic validity, prevalence, and treatment. Prim Care Companion J Clin Psychiatry 2002;4:94–9.
36. Quitkin FM, Rabkin JG, Gerald J, Davis JM, et al. Validity of clinical trials of antidepressants. Am J Psychiatry 2000;157:327–37.
37. Razani J, White KL, White J, Simpson G, et al. The safety and efficacy of combined amitriptyline and tranylcypromine antidepressant treatment. A controlled trial. Arch Gen Psychiatry 1983;40:657–61.
38. Richmond PW, Roberts AH. A comparative trial of imipramine, amitriptyline, isocarboxazid and tranylcypromine in out-patient depressive illness. Br J Psychiatry 1964; 110:846–50.
39. Ricken R, Ulrich S, Schlattmann P, Adli M. Tranylcypromine in mind (Part II): Review of clinical pharmacology and meta-analysis of controlled studies in depression. Eur Neuropsychopharmacol 2017;27:714–31.
40. Spear FG, Hall P, Stirland JD. A comparison of subjective response to imipramine and tranylcypromine. Br J Psychiatry 1964;110:53–5.
41. Stewart JW, Deliyannides DA, McGrath PJ. How treatable is refractory depression? J Affect Disord 2014;167:148–52.
42. Thase ME. The role of monoamine oxidase inhibitors in depression treatment guidelines. J Clin Psychiatry 2012;73(Suppl 1):10–6.
43. Thase ME, Mallinger AG, McKnight D, Himmelhoch JM. Treatment of imipramine-resistant recurrent depression, IV: A double-blind crossover study of tranylcypromine for anergic bipolar depression. Am J Psychiatry 1992;149:195–8.
44. Thase ME, Trivedi MH, Rush AJ. MAOIs in the contemporary treatment of depression. Neuropsychopharmacology 1995;12:185–219.
45. Ulrich S, Laux G. 50 Jahre Therapie mit Tranylcypromin. Psychopharmakotherapie 2010;17:160–1.
46. Volz HP, Faltus F, Magyar I, Möller HJ. Brofaromine in treatment-resistant depressed patients – a comparative trial versus tranylcypromine. J Affect Disord 1994a;30:209–17.
47. Volz HP, Heimann H, Bellaire J, Laux G, et al. Brofaromine in non-endogenous major depressed inpatients – results of a preliminary dose-finding trial versus tranylcypromine. Pharmacopsychiatry 1994b;27:152–8.
48. White K, Pistole T, Boyd JL. Combined monoamine oxidase inhibitor-tricyclic antidepressant treatment: a pilot study. Am J Psychiatry 1980;137:1422–5.
49. White K, Razani J, Cadow B, Gelfand R, et al. Tranylcypromine vs nortriptyline vs placebo in depressed outpatients: a controlled trial. Psychopharmacology (Berl) 1984;82:258–62.
Dr. rer. nat. Sven Ulrich, Aristo Pharma GmbH, Wallenroder Straße 8–10, 13435 Berlin, E-Mail: sven.ulrich@aristo-pharma.de
Dr. med. Roland Ricken, Klinik für Psychiatrie und Psychotherapie, Charité, Campus Charité Mitte, Charitéplatz 1, 10117 Berlin
Prof. Dr.med. Peter Schlattmann, Institut für Medizinische Statistik, Computerwissenschaften und Dokumentation, Universitätsklinikum Jena, Friedrich-Schiller-Universität Jena, Bachstraße 18, 07743 Jena
Chefarzt Priv.-Doz. Dr. med. Mazda Adli, Fliedner-Kliniken Berlin, Charlottenstraße 65 (Am Gendarmenmarkt), 10117 Berlin-Mitte
Meta-analysis of controlled studies of tranylcypromine in depression and evaluation of quality of study design
The irreversible and nonselective monoamine oxidase (MAO)-A/B inhibitor tranylcypromine (TCP) is used in the therapy of treatment resistant depression (TRD). In view of its clinical application for many years, it was a surprising finding that no meta-analysis is available for controlled studies of TCP in depression. The aim of this study was therefore to identify all controlled studies of TCP in depression as the centerpiece of clinical research of this MAO inhibitor, the evaluation of study-design and the statistical aggregation of study results in a meta-analysis. 23 studies have been found including two studies with simultaneous placebo and active control. This yields six studies (study arms) of the comparison with placebo and 19 studies (study arms) of a comparison with an antidepressant with altogether 664 TCP-patients. Including 15 randomized double-blind studies, study quality according to criteria of the EMA-guideline for antidepressant studies was good to very good, however, with only low sample size in some studies. Early studies (n=7, 1960–1964) had a lower quality than late studies (n=16, 1980–2007). However, the impact of the lower quality on study results is of low importance, because of a conservative orientation of this effect, and because placebo-controlled studies which aimed to show TCP-superiority prevail from 1960 to 1964. A significant and positive effect-size as pooled log (ln) odds ratio (logOR) of 0.509 with 95%-CI =0.026–0.993 was found for four placebo controlled studies. In 10 comparisons with antidepressants, TCP has a pooled logOR of 0.208 with 95%-CI =–0.128–0.544. TCP is also superior to placebo in TRD (one study: logOR =2.826 with 95%-CI =1.494–4.158) and to pseudo-placebos (four studies: pooled logOR =1.976 with 95%-CI =0.907–3.045) as well as equally efficacious as other antidepressants established in TRD (pooled logOR =–0.366 with 95%-CI =–0.869–0.137). This confirms statistically that TCP is superior to placebo and equally efficacious as other antidepressants in depression inclusive TRD.
Key words: Tranylcypromine, depression, MAO inhibitor, treatment resistant depression
Psychopharmakotherapie 2017; 24(06):259-271
