Göran Hajak, Bamberg, Bettina Barthel, München, und Matthias Lemke, Hamburg
Mit einer 12-Monatsprävalenz von 6,9% sind Depressionen häufige Erkrankungen [55]. Gemäß ICD-10 und DSM 5 bestehen die Hauptsymptome der Depression in der Symptomtrias aus depressiver Stimmung, Antriebslosigkeit und der Unfähigkeit, Freude und Interesse zu empfinden – und somit dem Verlust an positiven Emotionen. Dementsprechend kommt der Freudlosigkeit – der sogenannten Anhedonie – im Rahmen der Depression eine besondere Bedeutung zu.
Bei Beurteilung von Response oder Remission wird bislang in erster Linie die Verbesserung von Negativsymptomen als wichtiger Indikator des Therapieverlaufs genutzt. Feldstudien zeigen, dass aus Sicht von Patienten das Wiedererlangen positiver mentaler Gesundheit und die Rückkehr zu Optimismus, Selbstvertrauen, einer positiven Selbsteinschätzung und zu einem normalisierten Funktionsniveau die wichtigsten Remissionskriterien darstellen. Die Abwesenheit der klassischen depressiven Symptome, wie Traurigkeit oder gedrückte Stimmung, stand dagegen für Patienten erst an dritter Stelle [6, 7, 56]. Dies zeigten Demyttenaere und Kollegen in einer Untersuchung mit 426 ambulanten depressiven Patienten. Zu Behandlungsbeginn sowie nach 3-monatiger Behandlung waren sowohl aus Patientensicht als auch aus Sicht der behandelnden Ärzte eine Beurteilung der relevanten Symptome für eine vollständige Remission einer Depression erfasst und ein Ranking durchgeführt worden. Dies beinhaltete depressive und körperliche Symptome, Angst, positive Affekte, funktionelle Beeinträchtigungen und Lebensqualität. Es bestand ein signifikanter Unterschied zwischen der Einschätzung von Ärzten und Patienten, wobei Ärzte primär auf die Erleichterung von depressiven Symptomen fokussierten und Patienten auf die Wiederherstellung des positiven Affekts [7]. Es wurde ferner gezeigt, dass unterschiedliche Einschätzungen zwischen Arzt und Patient das klinische Ergebnis der Behandlung nach sechs Monaten signifikant beeinflussen können [6].
Eine frühzeitige Verbesserung positiver Emotionen ist als relevanter Prädiktor für ein Ansprechen auf eine antidepressive Therapie beschrieben [13, 51]. Andererseits sind anhedone Symptome als Residualsymptom und als Prädiktor für Non-Response und Non-Remission im weiteren Behandlungsverlauf bekannt [45, 50, 53]. Anhedonie kann ebenfalls als unerwünschte Arzneimittelwirkung auftreten, was für primär serotonerg wirkende Substanzen auch als Abflachung von Emotionen (sogenanntes „emotional blunting“) oder defizitäre emotionale Resonanz auf positive und negative Alltagsereignisse beschrieben wird [4, 14, 37, 40]. Die Verbesserung einer vorliegenden Anhedonie rückt damit in den Fokus einer modernen Depressionsbehandlung.
Die Daten direkter Vergleichsstudien weisen darauf hin, dass der melatonerge MT1/MT2-Rezeptoragonist und 5-HT2c-Rezeptorantagonist Agomelatin gegenüber Escitalopram und Venlafaxin XR (extended release) bei vergleichbarer Reduktion der depressiven Symptome zu einer Verbesserung der affektiven Schwingungsfähigkeit und der Anhedonie führt [4, 32]. Eine anti-anhedone Wirkung von Agomelatin wurde ebenfalls im offenen Studiendesign bereits zwei Wochen nach Therapiebeginn dokumentiert [12, 15, 29, 51].
Ziel der nichtinterventionellen Studie VIVID-ON war es, den Effekt von Agomelatin auf die depressive Symptomatik und insbesondere auf Anhedonie, die soziale Funktionsfähigkeit sowie Sexualität unter Praxisbedingungen zu untersuchen. Zusätzlich wurde eine mögliche Korrelation zwischen einer frühzeitigen Verbesserung der Anhedonie und dem Verlauf der depressiven Symptome, der sozialen Funktionsfähigkeit und der Sexualität untersucht.
Patienten und Methoden
In die prospektive, multizentrische, nichtinterventionelle, offene Studie wurden von März bis Oktober 2014 deutschlandweit 970 Patienten einbezogen, die wegen einer Depression ambulant von insgesamt 278 Psychiatern über 12 Wochen mit Agomelatin behandelt wurden. Neben der Eingangsuntersuchung (U1) waren drei Kontrolluntersuchungen vorgesehen (U2 bis U4 nach etwa 3, 6 und 12 Wochen). Bei der Eingangsuntersuchung (Baseline in Woche 0) wurden demographische Daten, Anamnese, Diagnose, Komorbiditäten, eventuelle Vorbehandlungen und die Ausgangswerte der Alanin-Aminotransferase (ALT; syn. GPT), Aspartat-Aminotransferase (AST; syn. GOT) und Gammaglutamyl-Transferase (GGT) dokumentiert. Der Schweregrad der Depression wurde mittels der Hamilton-Depression-Scale-Kurzversion mit 7 Items (HAMD-7) [33, 34] ermittelt. Die validierte Kurzform der HAMD-Skala mit 7 Items erfasst die depressive Stimmung, Schuldgefühle, Arbeit und Aktivität, psychische Angstgefühle, körperliche Angstgefühle, Suizidalität und allgemeine körperliche Beschwerden und wurde gemäß CIPS (Collegium Internationale Psychiatriae Scalarum) ausgewertet. Der Gesamtscore beträgt 0 bis 26 Punkte, wobei höhere Punktwerte einer stärkeren Beeinträchtigung entsprechen [54]. Zusätzlich beurteilten Ärzte den klinischen Gesamteindruck anhand der Clinical Global Impression Scale – Severity (CGI-S); die Veränderung der depressiven Symptomatik bei jeder Folgevisite (U2 bis U4) wurde mit der Clinical Global Impression of Improvement Scale (CGI-I) erfasst [1]. Der Behandlungseffekt auf die soziale Funktionsfähigkeit wurde bei jeder Visite mit der 10-stufigen Selbstbeurteilungsskala Sheehan Disability Scale (SDS; deutsche Version; 0=keine Beeinträchtigungen; 10=maximale Beeinträchtigungen) abgefragt [42]. Die SDS deckt das soziale Funktionsniveau in den drei Domänen Arbeit/Schule, soziale Kontakte und Familienleben/häusliche Verpflichtungen ab; zusätzlich wird die Anzahl an verlorenen bzw. unproduktiven Tagen während der letzten sieben Tage erfragt. Aus den Score-Werten der drei Einzel-Items wird der Gesamtscore berechnet (0=keine Beeinträchtigung bis 30=maximale Beeinträchtigung); die Auswertung des Gesamtscore erfolgte nur für Patienten mit vorliegenden Werten aller drei Einzel-Items. Die Schwere der Anhedonie wurde bei allen vier Visiten mit dem validierten Patientenfragebogen Snaith-Hamilton Pleasure Scale (SHAPS), einer 4-stufigen Likert-Skala („ich stimme überhaupt nicht zu“ bis „ich stimme voll zu“) mit 14 Items erfasst. Der errechnete Punktwert der SHAPS liegt zwischen 0 und 14 Punkten, wobei höhere Werte eine stärkere Anhedonie repräsentieren [11, 44]. Die Definitionen SHAPS-Response (Verbesserung des SHAPS-Gesamtscores um >50%) und Remission (SHAPS-Gesamtscore <3) erfolgten gemäß Auswertungsrichtlinien sowie bisherigen Publikationen, „early improvement“ bezugnehmend auf die Definition der depressiven Symptomatik als 20%ige Verbesserung innerhalb der ersten Wochen [47]. Die frühe Verbesserung wurde aufgrund des Studiendesigns nach drei Wochen erfasst, da unter nichtinterventionellen Bedingungen die Behandlung der alltäglichen ärztlichen Routine entspricht und keine klar definierten Untersuchungszeitpunkte vorgeschrieben werden können. Dementsprechend wurden Patienten gemäß Fachinformation von Agomelatin behandelt, was in der Regel der ersten Kontrolluntersuchung nach etwa drei Wochen entsprach (gemäß der Empfehlungen zu Lebertransaminasenkontrollen).
Da die SHAPS keine Fragen zu Sexualität enthält, wurden zusätzlich zwei Fragen des standardisierten Essener Fragebogens zu Sexualität [3] genutzt (W0 bis W12). Unerwünschte Ereignisse (UE) und unerwünschte Arzneimittelwirkungen (UAW) wurden bei den drei Folgevisiten (W3 bis W12) dokumentiert. Die Verträglichkeit wurde anhand standardisierter Berichtsbögen zu unerwünschten Arzneimittelwirkungen (UAW) dokumentiert und anhand Inzidenz und Art (gemäß MedDRA-Kodierung) ausgewertet.
Alle dokumentierten Daten wurden mittels deskriptiver Statistik analysiert. Die Auswertung erfolgte anhand aller vorliegenden Daten bei der jeweiligen Visite, um Patienten mit vorzeitigem Therapieabbruch in die Analyse einzuschließen, was zu unterschiedlichen Patientenzahlen bei der jeweiligen Visite führen kann (Approach 1). Zusätzlich wurden Patienten mit vorliegenden Daten zu allen Visiten analysiert (Approach 2; entsprechend Per-Protocol-Auswertung). Signifikanztests wurden für zentrale Parameter durchgeführt, sollten aber aufgrund des offenen Studiendesigns und fehlender statistischer Hypothese nur deskriptiv interpretiert werden. Die statistische Korrelationsberechnung zwischen einer frühen Verbesserung der Anhedonie mit weiteren Parametern (depressive Symptomatik, soziale Funktionsfähigkeit, sexuelle Beeinträchtigung) erfolgte mittels „Fisher’s exact test“ und „Jonckheere-Terpstra test“.
Die nichtinterventionelle VIVID-ON-Studie wurde von der Freiburger Ethikkommission positiv bewertet, den zuständigen deutschen Behörden angezeigt (BfArM, KBV, GKV-Spitzenverband) und ist unter www.drks.de in dem nationalen Register (Deutsches Register für klinische Studien) eingetragen. Das Datenmanagement und die statistische Auswertung wurden durch das unabhängige statistische Institut ANFOMED durchgeführt. Die Durchführung der VIVID-ON-Studie erfolgte mit Unterstützung der Servier Deutschland GmbH.
Ergebnisse
Patientencharakteristika
Die insgesamt 970 Studienteilnehmer der untersuchten Kohorte (64,9% Frauen) hatten ein Durchschnittsalter von 48,6±13,7 Jahren (Median 50,0). 53,9% der eingeschlossenen Patienten hatten eine depressive Episode, 46,1% eine rezidivierende depressive Erkrankung. Die Baseline-Charakteristika der Patienten sind in Tabelle 1 zusammengefasst. Zu Studienbeginn wurde der Schweregrad der Depression (nach ICD-10) von den Ärzten überwiegend als mittelgradig (68,3% der Patienten) bis schwer (23,2%) bewertet. 285 Patienten (29,9%) waren in der Vergangenheit aufgrund der Depression bereits in stationärer Behandlung. Neuropsychiatrische Komorbiditäten wurden bei 87,6% aller Patienten (n=850) berichtet. Eine Vorbehandlung mit Antidepressiva wurde für 60,1% der Patienten dokumentiert – überwiegend mit selektiven Serotonin-Wiederaufnahme-Inhibitoren (SSRI; 29,3% der Gesamtpopulation bzw. 50,4% aller vorbehandelten Patienten) – und/oder mit einer Psychotherapie für 25,4% aller Patienten. Bei 222 Patienten (22,9% der Gesamtpopulation) wurde die antidepressive Vortherapie während der 12-wöchigen Beobachtungsdauer fortgesetzt, in den meisten Fällen mit einem SSRI (n=96; 9,9% der Gesamtpopulation) und/oder einem Serotonin-Noradrenalin-Wiederaufnahme-Inhibitor (SNRI; n=59; 6,1%). Insgesamt 347 Patienten (35,8%) erhielten bis zu vier psychotrope Begleitmedikamente, am häufigsten Z-Substanzen (n=111, entsprechend 32,0% aller Patienten mit psychotroper Komedikation).
Tab. 1. Demographische Daten
|
Geschlecht |
Männer |
341 (35,2%) |
|
Frauen |
629 (64,9%) |
|
|
Alter in Jahren (Mittelwert ± SD) |
48,6±13,7 |
|
|
Gewicht (Mittelwert ± SD) |
76,8±15,9 kg |
|
|
Body-Mass-Index (Mittelwert ± SD) |
26,26±4,88 kg/m2 |
|
|
Nikotinkonsum |
Raucher insgesamt |
278 (29,5%) |
|
Nichtraucher |
664 (70,5%) |
|
|
Diagnose |
Depressive Episode (F32) |
522 (53,9%) |
|
Rezidivierende depressive Störung (F33) |
446 (46,1%) |
|
|
Schweregrad der Depression |
Mild |
79 (8,4%) |
|
Moderat |
641 (68,3%) |
|
|
Schwer |
218 (23,2%) |
|
|
Depressive Episoden in der Anamnese (Anzahl als Mittelwert) |
2,8±4,7 (median: 2,0) |
|
|
Dauer der aktuellen Episode (Wochen als Mittelwert) |
12,5±24,6 (median: 8,0) |
|
|
Krankenhausaufenthalt in der Vergangenheit |
Ja |
285 (29,9%) |
|
Nein |
667 (70,1%) |
|
|
Suizidversuche in der Vergangenheit |
Ja |
50 (5,3%) |
|
Nein |
876 (92,3%) |
|
|
Unbekannt |
23 (2,4%) |
|
|
Neuropsychiatrische Komorbiditäten |
850 (87,6%) |
|
|
Schlafstörungen |
654 (76,9/67,4%) |
|
|
Angst-/Panikstörungen |
348 (40,9/35,9%) |
|
|
Schwere Stress-/Anpassungsstörung |
214 (25,2/22,1%) |
|
|
Essstörungen |
120 (14,1/12,4%) |
|
|
Psychotrope Komedikation |
Nein |
623 (64,2%) |
|
Ja*, davon: |
347 (35,8%) |
|
|
111 (32,0/11,4%) |
|
|
76 (21,9/7,8%) |
|
|
69 (19,9/7,1%) |
|
|
56 (16,1/5,8%) |
|
|
Vorbehandlung mit Psychotherapie |
Nein |
724 (74,6%) |
|
Ja*, davon: |
246 (25,4%) |
|
|
153 (62,2/15,8%) |
|
|
78 (31,7/8,1%) |
|
|
7 (2,9/0,7%) |
|
|
Sonstige |
12 (4,9/1,2%) |
|
|
Vorbehandlung mit Antidepressiva |
Nein |
375 (39,9%) |
|
Ja*, davon: |
564 (60,1%) |
|
|
284 (50,4/29,3%) |
|
|
157 (27,8/16,2%) |
|
|
140 (24,8/14,4%) |
|
|
130 (23.1/13,4%) |
|
*Mehrfachnennung möglich; Angaben in Anzahl und (%); Komorbidität, Komedikation und Vorbehandlung angegeben als Anzahl und % (der komorbiden bzw. behandelten Patienten/bzw. der Gesamtpopulation)
Zu Studienbeginn erhielten 96,7% aller Patienten eine Tablette Agomelatin (25 mg/Tag), bei der Abschlussvisite (W12) erhielten 55,6% der Patienten 25 mg/Tag (43,9% nahmen 50 mg/Tag, die restlichen Patienten andere Dosierungen, z.B. ½ Tablette oder >2 Tabletten). Die mittlere Behandlungsdauer betrug 14,1±13,2 Wochen; insgesamt 16,3% aller Patienten (n=154) beendeten die Therapie mit Agomelatin vorzeitig. Als Gründe für einen vorzeitigen Therapieabbruch wurden am häufigsten unzureichende Wirksamkeit (n=47; 30,5% der Patienten mit vorzeitigem Therapieabbruch), mangelnde Compliance (n=41; 26,6%) und mangelnde Verträglichkeit (n=30; 19,5%) beschrieben.
Verlauf der depressiven Symptomatik
Der Schweregrad der Depression zeigt eine kontinuierliche Verbesserung in den Skalen CGI und HAMD-7. Bei der ersten Folgeuntersuchung nach drei Wochen zeigten 15,7% (n=142/905) aller Patienten mit vorliegenden CGI-I-Werten ein Ansprechen (CGI-I ≤2) auf die Therapie mit Agomelatin. Nach sechs Wochen betrug die Responder-Rate 52,4% (n=437/834), nach 12 Wochen 71,5% (n=600/839). Bei der Abschlussvisite hatten 31,7% aller Patienten mit vorliegenden CGI-S-Werten (n=262/827) eine Remission erreicht (CGI-S 1 oder 2). Der HAMD-7-Gesamtscore verringerte sich im Behandlungsverlauf von 11,7 (W0), 9,4 (W3), 6,6 (W6) auf 4,7 Punkte (W12) mit signifikanter Differenz zwischen den einzelnen Visiten. Nach Bewertung gemäß HAMD-7 lag der Anteil der Responder (Verbesserung um >50%) in Woche 12 bei 64,1% (n=534/833) und der Remitter (HAMD-7 ≤3) bei 49,3% (n=412/835) (Tab. 2). Eine frühe Verbesserung („early improvement“), definiert als Reduktion des HAMD-7-Gesamtwerts um >20% in Woche 3, zeigte sich bei 42,8% aller Patienten (n=395/922). Die sieben Einzel-Items der HAMD-7-Skala zeigten ebenfalls eine statistisch signifikante Verbesserung (p<0,0001) im Verlauf der zwölfwöchigen Behandlung (Abb. 1).
Tab. 2. Verbesserung der depressiven Symptomatik mit Response und Remission (anhand Skalen CGI, HAMD-7 und SHAPS)
|
Response |
Remission |
|||||
|
W3 |
W6 |
W12 |
W3 |
W6 |
W12 |
|
|
CGI |
15,7% (n=142) |
52,4% (n=437) |
71,5% (n=600) |
k. A. |
k. A. |
31,7% (n=262) |
|
HAMD-7 |
11,4% (n=105) |
39,8% (n=340) |
64,1% (n=534) |
7,9% (n=73) |
25,0% (n=214) |
49,3% (n=412) |
|
SHAPS |
17,8% (n=150) |
50,3% (n=325) |
70,5% (n=529) |
22,6% (n=203) |
38,6% (n=325) |
63,8% (n=507) |
Ergebnisse angegeben als Patienten in % (Anzahl); W: Woche; CGI: Clinical Global Impression Scale, HAMD-7: Hamilton Depression-Scale – 7 Items, SHAPS: Snaith-Hamilton Pleasure Scale, k. A.: Analyse nicht erfolgt, Auswertung aller Patienten mit vorliegenden Daten zum jeweiligem Untersuchungszeitpunkt
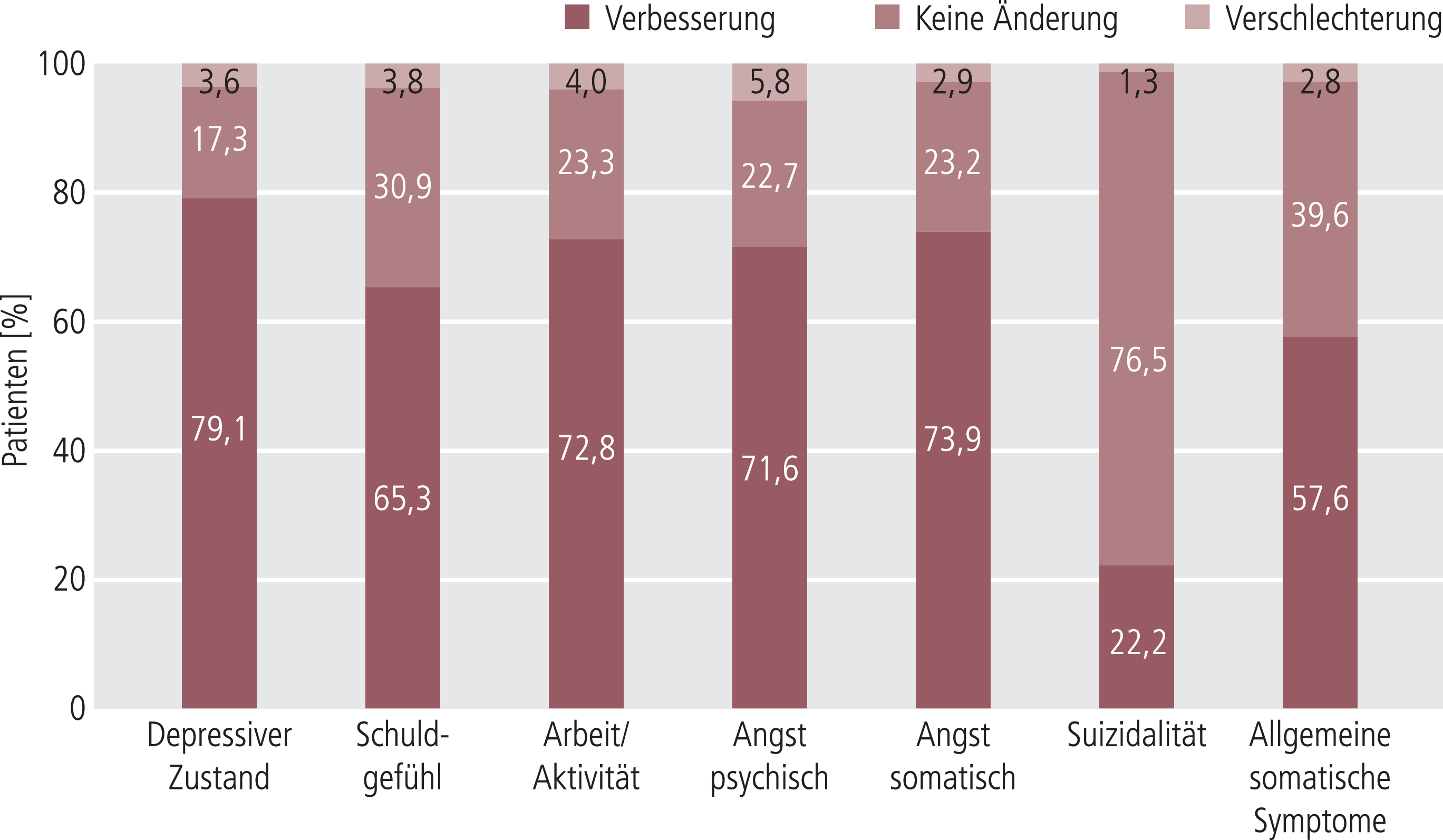
Abb. 1. Verbesserung/Veränderung der depressiven Symptome anhand der Einzel-Items der Depressionsskala HAMD-7 zwischen Baseline und Woche 12; Darstellung der Patienten (in %) mit Verbesserung, ohne Veränderung oder Verschlechterung der sieben erfassten Einzelsymptome (n=833): HAMD-7: Hamilton Depression Scale (7 Items)
Veränderung der sozialen Funktionsfähigkeit
Die Beeinträchtigung der sozialen Funktionsfähigkeit (anhand SDS-Selbstbeurteilungs-Skala) verbesserte sich bis Woche 12 bei 90,8% der Patienten. Der SDS-Gesamtscore (Mittelwert) verringerte sich um 10,9±7,5 Punkte von einem Ausgangswert von 21,3±5,8 (n=913) auf 10,5±7,2 Punkte (n=773) bei der Abschlussuntersuchung (p<0,0001). Die Verbesserung im sozialen Funktionsniveau spiegelt sich ebenfalls in den drei Einzeldomänen (Arbeit/Schule, soziale Kontakte und Familienleben/häusliche Verpflichtungen) der SDS wider (Tab. 3). Die mit dem SDS-Fragebogen ermittelte Anzahl der „verlorenen Tage“ betrug bei Behandlungsbeginn durchschnittlich 3,7±2,9 Tage und verringerte sich auf 1,4±2,4 Tage nach 12 Wochen (p<0,0001 vs. Baseline), die Anzahl der „unproduktiven Tage“ von 4,7±2,6 Tage auf 2,1±2,4 Tage (p<0,0001).
Tab. 3. Verbesserung im sozialen Funktionsniveau gemäß SDS
|
SDS-Score |
W0 |
W3 |
W6 |
W12 |
Differenz W12 – W0 |
Patienten mit Verbesserung in Woche 12 |
|
Arbeit/Schule (0–10) |
7,4±2,2 (n=914) |
6,3±2,3 (n=868) |
4,9±2,6 (n=807) |
3,7±2,7 (n=773) |
–3,7±2,7* (n=760) |
87,1% (n=662/760) |
|
Soziale Kontakte (0–10) |
6,9±2,4 (n=956) |
5,9±2,3 (n=905) |
4,6±2,4 (n=845) |
3,4±2,5 (n=802) |
–3,5±2,8* (n=799) |
85,1% (n=680/799) |
|
Familie/häusliche Verpflichtungen (0–10) |
6,9±2,2 (n=957) |
5,8±2,3 (n=905) |
4,4±2,4 (n=844) |
3,3±2,5 (n=802) |
–3,6±2,7* (n=800) |
85,9% (n=687/800) |
|
SDS-Gesamtwert (0–30) |
21,3±5,8 (n=913) |
18,1±6,2 (n=868) |
13,9±6,9 (n=805) |
(10,5±7,2) (n=773) |
–10,9±7,5* (n=759) |
90,8% (n=689/759) |
|
Anzahl „verlorene“ oder „unproduktive“ Tage |
||||||
|
3,7±2,9 (n=906) |
2,9±2,9 (n=856) |
2,0±2,6 (n=806) |
1,4±2,4 (n=769) |
–2,3±2,8* (n=755) |
k. A. |
|
4,7±2,6 (n=888) |
3,9±2,6 (n=851) |
2,9±2,6 (n=801) |
2,1±2,4 (n=765) |
–2,6±2,9* (n=737) |
k. A. |
Angegeben sind Mittelwerte ± SD und Anzahl der Patienten (n) mit vorliegenden Daten zum jeweiligen Untersuchungszeitpunkt; SDS: Sheehan Disability Scale; k. A.: keine Analyse vorliegend; *p<0,0001
Veränderung der Freudlosigkeit und Sexualität
Zu Studienbeginn waren 16,1% der Patienten (n=153) frei von Anhedonie (SHAPS-Gesamtwert von 0 bis 2), in Woche 12 waren es 63,8% (n=507). Im Behandlungsverlauf verbesserte sich der durchschnittliche SHAPS-Gesamtwert von 7,7±4,3 Punkte (Baseline-Wert, n=952) auf 6,3±4,1 (W3, n=899), 4,0±3,5 (W6, n=841) und 2,5±3,1 (W12, n=795) (p<0,0001 vs. Baseline). Am Studienende zeigten 81,9% der Patienten (n=647/795) eine Verbesserung des SHAPS-Score, 10,1% (n=80/795) eine Verschlechterung und bei 8,0% der Patienten (n=63/795) blieb der SHAPS-Gesamtwert gegenüber dem Ausgangswert unverändert.
Der Anteil an Patienten, der als Responder (Verbesserung des SHAPS-Gesamtscores um >50%) klassifiziert werden konnte, stieg kontinuierlich und lag in Woche 12 bei 70,5% (n=529/750). Eine Remission (SHAPS-Gesamtscore <3) erreichten 63,8% der Patienten (n=507/795) (Tab. 2). Das Kriterium einer frühzeitigen Verbesserung („early improvement“) der Anhedonie (Reduktion des SHAPS-Scores um >20% nach drei Wochen) erfüllten 43,7% (n=369) aller Patienten. Eine Verbesserung der Anhedonie ist in allen 14 Einzel-Items der SHAPS (p<0,0001) nachweisbar (Abb. 2).
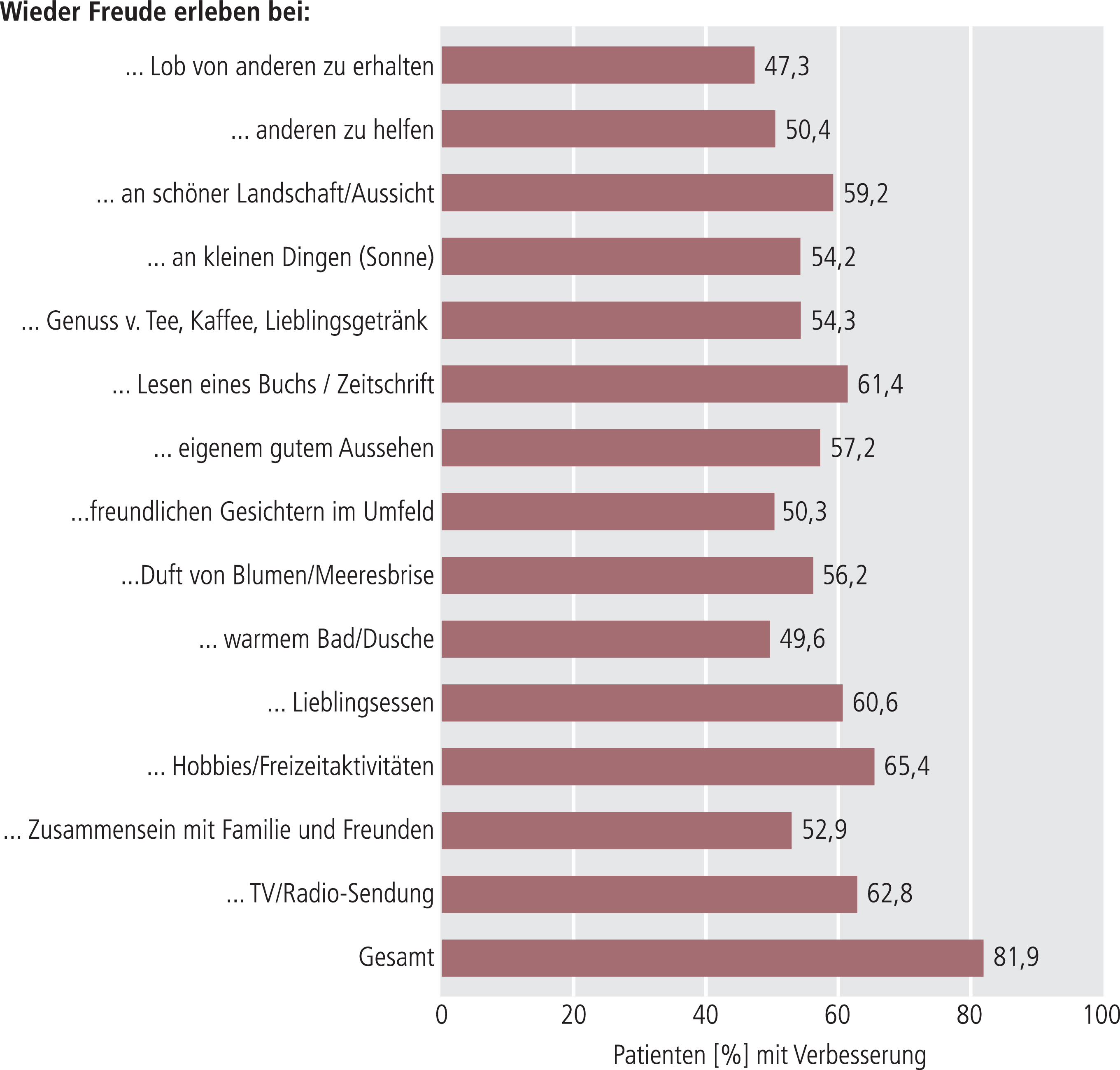
Abb. 2. Verbesserung der Anhedonie mittels Patientenfragebogen SHAPS; Darstellung von Patienten (in %) mit Verbesserung des Gesamtwert sowie der 14 Einzel-Items nach 12 Wochen Behandlung (n=790); SHAPS: Snaith-Hamilton Pleasure Scale
Veränderungen der Sexualität (Verbesserung oder Verschlechterung) wurden zu Studienbeginn von 61,3% der Patienten (n=576/940) dokumentiert. Eine Differenzierung hinsichtlich Verbesserung bzw. Verschlechterung der Sexualfunktion zeigte eine Zunahme der Patienten mit Verbesserung zwischen Baseline und Woche 12 (1,17%/24,97%), während der Anteil an Patienten mit einer Verschlechterung abnahm (55,43%/10,45%).
Eine Analyse der Patienten mit vorbestehender Verschlechterung der Sexualität bei Studienbeginn (n=494) zeigte bei 49,6% dieser Patienten (n=245) im Verlauf der Behandlung eine Verbesserung (W3:13,4%; W6:37,4%; W12:49,6%; Approach 1). Vergleichbare Ergebnisse sind bei der Auswertung von Patienten mit vorliegenden Daten zu allen vier Visiten (n=435) nachweisbar (W3:13,8%; W6:39,8%; W12:53,6%; Approach 2). Die Verbesserung der Sexualität bei vorbestehender Beeinträchtigung trat in dieser Kohorte geschlechtsunabhängig auf, bei Männern jedoch häufiger als bei Frauen (53,8% gegenüber 47,1%) (Abb. 3).
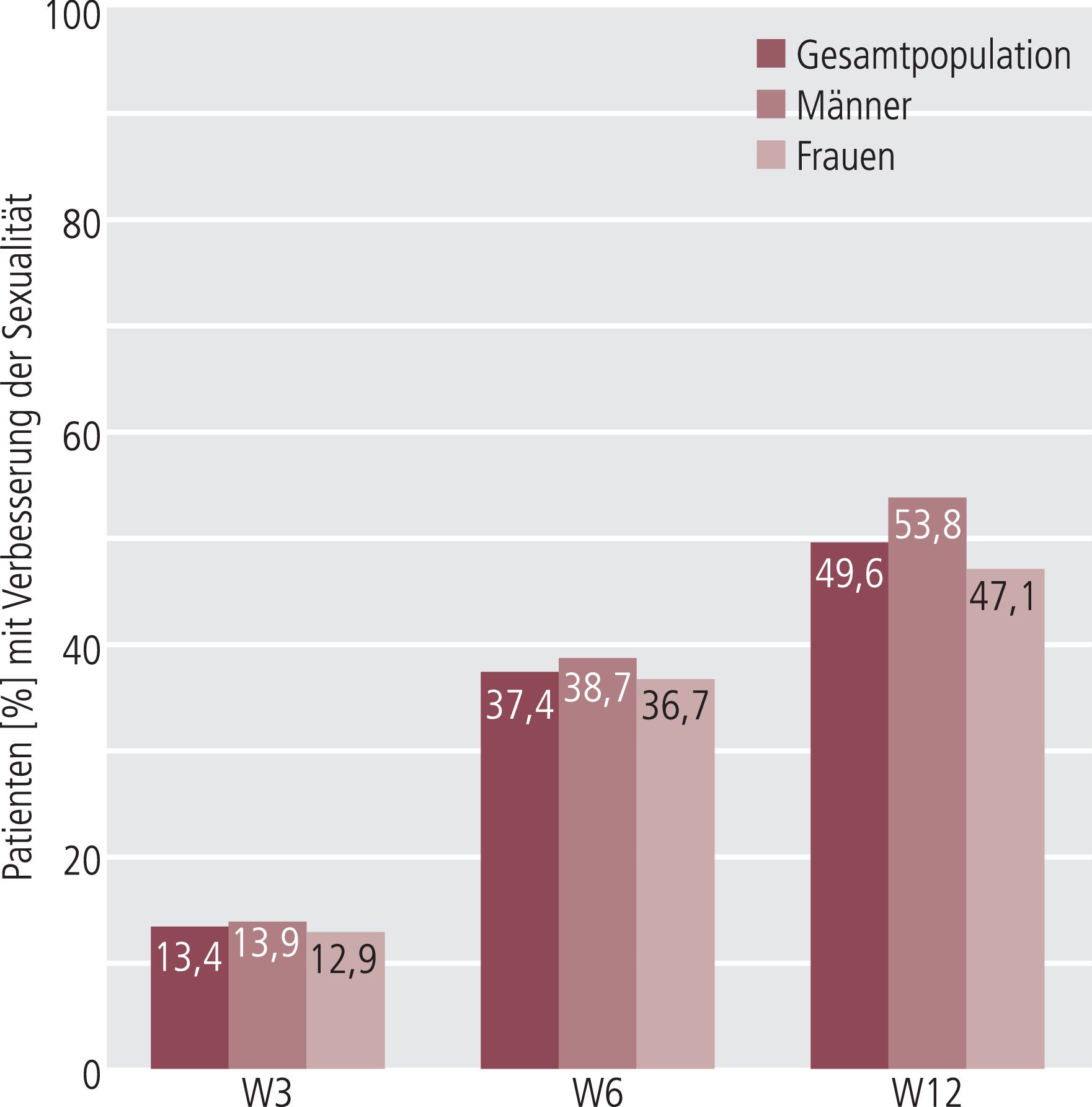
Abb. 3. Geschlechtsspezifische Verbesserung der Sexualität über 12 Wochen bei Patienten mit vorbestehender Verschlechterung der Sexualität zu Studienbeginn; Darstellung kumulativer Werte für Patienten mit Verbesserung in der Gesamtpopulation, bei Männern und Frauen; (n=494)
Korrelation von „early improvement“ und Response/Remission im weiteren Therapieverlauf
Die Auswertung der Daten zeigt eine signifikante Korrelation zwischen einer frühzeitigen Verbesserung (W3) und einer Response und Remission (W12) bezogen auf Depression (HAMD-7; p<0,0001) und Anhedonie (SHAPS; p<0,0001) (Tab. 4a).
Tab. 4a. Korrelation der frühen Verbesserung der Depression (HAMD-7) bzw. Anhedonie (SHAPS) mit Response/Remission im Therapieverlauf
|
Fragebogen/Skalen |
Signifikanz |
|
HAMD-7>20% (W3) vs. HAMD-7-Response (W12) |
p<0,0001a |
|
HAMD-7>20% (W3) vs. HAMD-7-Remission (W12) |
p<0,0001 a |
|
SHAPS >20% (W3) vs. SHAPS-Response (W12) |
p<0,0001a |
|
SHAPS >20% (W3) vs. SHAPS-Remission (W12) |
p<0,0001 a |
Tab. 4b. Korrelation der frühen Verbesserung von Anhedonie (SHAPS) mit Response/Remission (HAMD-7) sowie Verbesserung der Depression (CGI), der sozialen Funktionsfähigkeit (SDS) und Sexualität nach 12 Wochen
|
Fragebogen/Skalen |
Signifikanz |
|
SHAPS >20% (W3) vs. HAMD-7-Response (W12) |
p<0,0001a |
|
SHAPS >20% (W3) vs. HAMD-7-Remission (W12) |
p<0,0001 a |
|
SHAPS >20% (W3) vs. CGI-S (W12) |
p<0,0001b |
|
SHAPS >20% (W3) vs. CGI-I (W12) |
p<0,0001b |
|
SHAPS >20% (W3) vs. SDS-Gesamtscore (W12) |
p<0,0001 a |
|
SHAPS >20% (W3) vs. Verbesserung der Sexualität (W12) |
p<0,0001 a |
Frühe Verbesserung ist definiert als Verbesserung >20% in Woche 3 auf der jeweiligen Skala.
SHAPS: Snaith-Hamilton Pleasure Scale; CGI: Clinical Global Impression Scale (S: Severity; I: Impression); HAMD-7: Hamilton Depression Scale (7 Items); SDS: Sheehan Disability Scale; statistische Korrelationsberechnung mittels Fisher’s-Exact-Test (a) bzw. Jonckheere-Terpstra-Test (b)
Anhand von Korrelationsanalysen (Fisher’s exact test) wurde gemäß der spezifischen Fragestellung zusätzlich die prädiktive Aussagekraft einer frühzeitigen Verbesserung („early improvement“) von Anhedonie (Verbesserung Gesamtscore >20% in W3) für die Verbesserung der depressiven Symptomatik, der sozialen Funktionsfähigkeit und der Sexualität im weiteren Behandlungsverlauf untersucht.
Die Korrelation zwischen SHAPS „early improvement“ (W3) und HAMD-7 Response bzw. Remission (W12) war statistisch signifikant (jeweils p<0,0001). 76,7% der Patienten mit früher Verbesserung der Anhedonie (W3) zeigten eine Response bzw. 64,3% eine Remission nach HAMD-7 (W12) im Vergleich zu 57,7% bzw. 40,2% ohne „early improvement“.
Eine positive Korrelation war ebenfalls nachweisbar zwischen früher Verbesserung von Anhedonie (SHAPS) und Veränderung der Sexualität (p<0,0001) (Tab. 4b) sowie Verbesserung der sozialen Funktionsfähigkeit (SDS-Skala) nach 12 Wochen (r =0,598; p<0,0001) (Abb. 4).
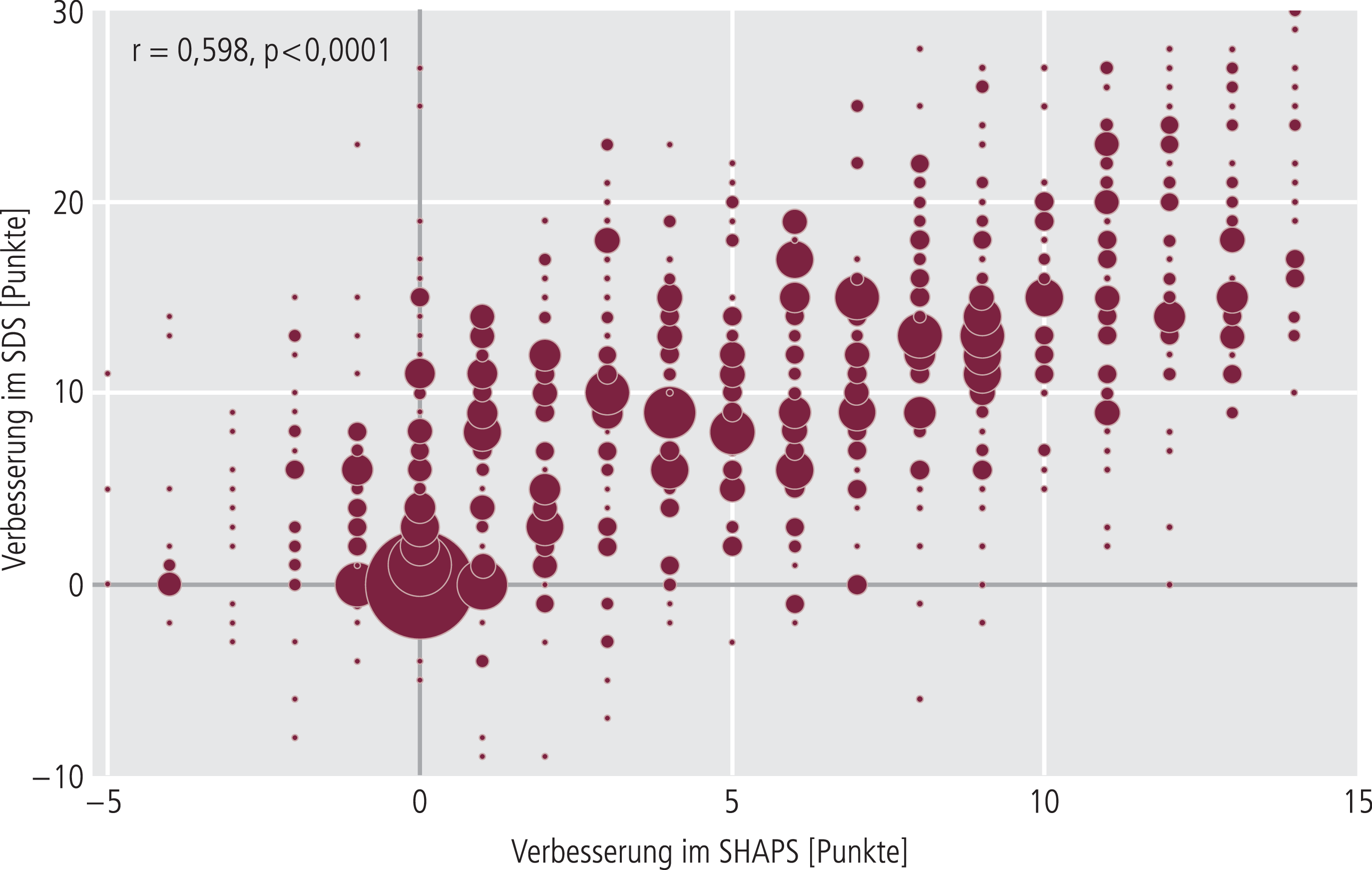
Abb. 4. Positive Korrelation zwischen einer frühen Verbesserung von Anhedonie (SHAPS ≥20% innerhalb drei Wochen) und Verbesserung der sozialen Funktionsfähigkeit (SDS) nach 12 Wochen; SHAPS: Snaith-Hamilton Pleasure Scale; SDS: Sheehan Disability Scale
Verträglichkeit
Die Studien-Ärzte bewerteten die Verträglichkeit von Agomelatin bei 96,5% der Patienten (n=850/881) als „sehr gut/gut“. UAW wurden bei 5,8% der Patienten dokumentiert, am häufigsten in Form von neuropsychiatrischen Symptomen (1,9%) oder gastrointestinalen Beschwerden (1,1%) sowie bei neun Patienten (0,93%) ein Anstieg der Leberwerte um mehr als das 3-Fache über dem Normbereich. Schwerwiegende UAW wurden bei drei Patienten gemeldet (0,31%); hierbei handelte es sich um eine Patientin mit Leberwerterhöhungen (ALT/AST/GGT; bereits vor Behandlungsbeginn dokumentiert), eine Patientin mit GGT-Erhöhung (ebenfalls vorbestehend) und eine Patientin mit Insomnie/Albträumen und Tremor. Das mittlere Gewicht (76,5 vs. 76,3 kg) und der Body-Mass-Index (26,1 vs. 25,8 kg/m2) blieben von Studienbeginn bis zur Abschlussuntersuchung unverändert.
Diskussion
Depression ist nach ICD-10 neben Traurigkeit und gedrückter Stimmung durch die Unfähigkeit, Freude und Interesse zu empfinden, charakterisiert. Bei der klinischen Bewertung des Therapieerfolgs einer Depression liegt der Fokus bei Ärzten bis heute in erster Linie auf einer Verringerung negativer Emotionen, wie gedrückter Stimmung, Traurigkeit oder Schuldgefühlen [6, 7]. Eine Verbesserung der beeinträchtigten Fähigkeit, Freude, Motivation und Interesse zu erleben sowie die Regulation der emotionalen Schwingungsfähigkeit werden bisher in klinischen Studien und im klinischen Alltag bei der Beurteilung des Therapieverlaufs eher vernachlässigt. Als mögliche Erklärung hierfür können die üblicherweise eingesetzten Skalen (z.B. HAMD oder MADRS) dienen, die positive Emotionen wenig erfassen [18, 36].
Der Einfluss einer antidepressiven Pharmakotherapie auf Veränderungen der positiven Emotionsregulation wurde in experimentellen und klinisch-kontrollierten Studien untersucht [4, 19]. Die Literatur zeigt erste Hinweise, dass nicht nur die frühe Verbesserung von negativer Stimmung und Antriebslosigkeit, sondern auch das Wiederauftreten von positiver Stimmung und Interesse einen positiven prädiktiven Wert für Response und Remission im Behandlungsverlauf besitzt [13, 15, 51], wie dies bereits für die frühe Verbesserung der depressiven Symptomatik bekannt ist [20, 46].
Die Überprüfung dieser Hypothese im klinischen Anwendungsbereich von Antidepressiva war Ziel dieser vorliegenden Untersuchung. Der MT1/MT2-Agonist und 5-HT2C-Antagonist Agomelatin wurde für diese Fragestellung als Antidepressivum gewählt, da die Substanz aufgrund der Rezeptorspezifität und des Wirkungsmechanismus im Vergleich zu SSRI und SNRI ein geringes Risiko für „emotional blunting“, ein beschriebenes Phänomen unter antidepressiver Pharmakotherapie, besitzt [14, 37, 40]. Die antidepressive Wirksamkeit und Verträglichkeit von Agomelatin (25–50 mg/Tag) ist in randomisierten, kontrollierten Studien nachgewiesen [5, 16, 23, 25, 48]. Aus kontrollierten sowie offenen Studien liegen zusätzlich Daten zu einem positiven Effekt auf Anhedonie und soziale Funktionsfähigkeit vor [4, 8, 12, 15, 19, 27, 32, 51, 52].
Die vorliegende Studie VIVID-ON untersuchte, neben einer Verbesserung der Symptome Traurigkeit und gedrückte Stimmung den Therapieeffekt auf Freudlosigkeit, soziale Funktionsfähigkeit sowie auf die Sexualität von Patienten am Beispiel einer Therapie mit Agomelatin. Die genutzten Selbst-, und Fremdbeurteilungs-Skalen erfassen neben den gängigen depressiven Symptomen (HAMD-7, CGI) die subjektive Beeinträchtigung der sozialen, häuslichen und beruflichen Funktionsfähigkeit (SDS) und die positiven Emotionen (SHAPS) der Patienten. Das Symptom Anhedonie (erfasst mittels SHAPS) wird häufig mit psychischen Erkrankungen wie beispielsweise einer Schizophrenie in Verbindung gebracht. Als eines der drei Kernsymptome der Depression (ICD-10) ist Anhedonie jedoch ebenfalls als prognostischer Faktor für den weiteren Therapieverlauf einer Depression und als Residualsymptom beschrieben [15, 32, 45, 49, 53], was für die vorliegende Untersuchung im Rahmen der Praxis-Kohorte entscheidend war. Die Kurzversion des HAMD mit sieben Items (HAMD-7) erfasst maßgebliche Symptome der Depression, zeigt Validität gegenüber der Langversion HAMD-17 [33, 34] und wurde aufgrund der Anwenderfreundlichkeit für Patienten in der täglichen Praxis als Depressionsskala gewählt. Vorteilhaft ist zudem, dass die Kurzversion keine Schlaf-Items enthält, wodurch eine Beurteilung des Therapieeffekts von Agomelatin unabhängig von der Wirkung auf den Schlaf ermöglicht wird.
Die demographischen Daten der untersuchten 970 ambulanten Patienten (64,9% Frauen) repräsentieren die allgemeine Geschlechterverteilung depressiver Patienten [22, 31]. Das mittlere Alter (48,6 Jahre) und der Schweregrad der Erkrankung (68,3% mittelgradig depressiv) entsprachen der Patientenpopulation aus klinisch kontrollierten Studien (RCTs) [4, 24, 27, 38]. Mit nahezu vergleichbarem Anteil an Patienten mit depressiver Episode und rezidivierender Erkrankung (53,9% vs. 46,1%) unterschieden sich die hier untersuchten Patienten von der Population aus RCTs (60 bis 75% rezidivierende Episoden) und bisherigen Praxisdaten (etwa 60%) [4, 5, 17, 25, 28]. Die Anzahl vorbehandelter Patienten dieser Kohorte (60%) war im Vergleich zu RCTs [4, 17, 24, 38] geringgradig höher, aber vergleichbar mit bisherigen Studien der breiten praktischen Anwendung [28], was dem nichtinterventionellen Studiendesign und Patienten im Praxisalltag entspricht. Obwohl im Vergleich zu RCTs der Anteil an Patienten mit rezidivierenden Episoden sowie Vorbehandlung mit psychotroper Medikation geringe Unterschiede aufwies, können die Patientencharakteristika als repräsentativ für den Praxisalltag angesehen werden.
Die dargestellten Praxisdaten verdeutlichen neben der Verbesserung depressiver Symptome die Verbesserung einer bestehenden Anhedonie, der sozialen Funktionsfähigkeit und von Störungen der Sexualfunktion bei Behandlung mit Agomelatin.
Die depressive Symptomatik verbesserte sich deutlich im Verlauf hinsichtlich Gesamtscore, Response- und Remissionsraten (CGI, HAMD-7). Zu Studienbeginn waren gemäß CGI 50,2% aller Patienten deutlich erkrankt, nach 12 Wochen waren es lediglich 9,6%; mehr als 70% Responder und 30% Remitter wurden dokumentiert (CGI). Der Gesamtscore des HAMD-7 verbesserte sich im Vergleich zu Baseline signifikant (p<0,0001), Response zeigten nahezu 65% und Remission knapp 49% aller Patienten. Die vorliegenden Ergebnisse sind vergleichbar mit Daten kontrollierter Studien, die anhand der Vollversion des HAMD (HAMD-17) erfasst wurden [4, 24, 25, 27, 38], was die Validität der Kurzversion des HAMD-7 [33, 34] anhand vorliegender Daten der täglichen Praxis nahelegt. Ein „early improvement“ (>20% innerhalb drei Wochen) mittels HAMD-7 wurde für 42,8% der Patienten dokumentiert, was hochsignifikant mit Response bzw. Remission nach 12 Wochen assoziiert war (p<0,0001, Fisher’s exact test).
In einer Untersuchung von Taylor et al. wurde bei 84 respondierten Patienten nach kognitiver Verhaltenstherapie (CBT) gezeigt, dass einzelne Symptome bzw. Residualsymptome, die durch HAMD-17 erfasst werden, prädiktiv für einen Relapse oder eine Wiedererkrankung sein können. Beispielsweise waren verstärkte psychische Angst, Appetitverlust, Libidoverlust oder Hypochondrie unabhängige prädiktive Faktoren [49]. Psychische Angst ist als Symptom ebenfalls in der Kurzversion HAMD-7 (Item 4) enthalten; 68% der Studienpatienten zeigten eine Verbesserung dieses Symptoms nach 12 Wochen. Die Sexualität, die anhand standardisierter Fragen des Essener Sexualitäts-Fragebogens [3] erfasst wurde, verbesserte sich bei 49,6% der Patienten mit vorbestehender Verschlechterung der Sexualität, was als Hinweis auf einen positiven Effekt von Agomelatin auf ein zweites prognostisches Item gewertet werden kann. Der Erhalt der sexuellen Funktion ist für Agomelatin in randomisierten klinischen Studien nachgewiesen [26, 35, 43]. Als Erklärungsansatz dient die antagonistische Wirkung von Agomelatin am 5-HT2C-Rezeptor mit indirekter Erhöhung der Dopamin- und Noradrenalin-Freisetzung im präfrontalen Kortex, ohne den Serotoninspiegel zu beeinflussen, sowie zusätzlich der melatonerge Effekt [21, 41]. Sexuelle Dysfunktion kann als Symptom einer Depression auftreten, ist zusätzlich aber als unerwünschte Arzneimittelwirkung, insbesondere unter serotonergen Substanzen, beschrieben [2, 30, 43]. Dies wird auf einen Anstieg des Serotoninspiegels und einer damit einhergehenden verminderten Aktivierung des dopaminergen Belohnungssystems zurückgeführt. Sexuelle Funktionsstörungen beeinträchtigen nicht nur die Lebensqualität von Patienten, sondern auch deren Therapieadhärenz [2, 10].
90% der untersuchten Studienpatienten zeigten eine Verbesserung der sozialen Funktionsfähigkeit, was für Agomelatin in RCTs und nichtinterventionellen Studien bereits beschrieben ist [12, 27, 39]. Zusätzlich verringerte sich die Anzahl der „verlorenen“ und „unproduktiven Tage“ signifikant über 12 Wochen. Das Ausmaß der funktionellen Verbesserung in den drei Domänen der SDS (Arbeit/Schule, soziale Kontakte und Familienleben/häusliche Verpflichtungen) spiegelt sich für den Bereich Arbeit/Schule im Item 3 der HAMD-7-Skala (Arbeit und Aktivität) wider, was die Konsistenz der erhobenen Ergebnisse bestätigt.
Anhand der Snaith-Hamilton Pleasure Scale (SHAPS) wurde bei insgesamt 80% aller Patienten eine Verbesserung der Anhedonie deutlich. In Bezug auf die vorliegende Anhedonie wurden 70% der Patienten als Responder und 64% als Remitter klassifiziert. Der SHAPS-Gesamtscore verbesserte sich über 12 Wochen um –5,5 Punkte. Im Vergleich zu Martinotti et al. (2012), die eine signifikante Differenz von –3 Punkten beschrieben, war die Verbesserung bei den vorliegenden Patienten deutlicher ausgeprägt [32]. Eine mögliche Erklärung hierfür liefert die unterschiedliche Studiendauer über acht Wochen (Martinotti) gegenüber 12 Wochen (mittlere Behandlungsdauer 14,6 Wochen) in der vorliegenden Kohorte.
Die Verbindung einer bestehenden Anhedonie mit sozialer Funktionsfähigkeit sowie mit Verbesserung der Sexualität ist eine bisher wenig untersuchte Thematik. In der vorliegenden Kohorte des Versorgungsalltags erfolgte zur Untersuchung eines möglichen Zusammenhangs eine Korrelationsberechnung zwischen diesen Variablen. Die Fragestellung war, ob eine frühe Verbesserung der Anhedonie innerhalb von drei Wochen als Prädiktor für eine Response bzw. Remission der Depression, Verbesserung der sozialen Funktionsfähigkeit und der Sexualität nach 12 Wochen genutzt werden kann.
Der positive prädiktive Wert eines „early improvement“ der Depression für den Krankheitsverlauf ist in RCTs beschrieben und wird in der vorliegenden offenen Studie ebenfalls bestätigt. Das Symptom der Freudlosigkeit (Anhedonie) wurde in diesem Zusammenhang allerdings bisher wenig untersucht. Eine frühe Verbesserung („early improvement“) der Anhedonie (>20% auf der SHAPS) innerhalb der ersten drei Wochen wurde in der untersuchten Kohorte bei mehr als 40% aller Patienten nachgewiesen, und zeigte eine signifikante Korrelation mit Response und Remission der Anhedonie (SHAPS; p<0,0001) nach 12 Wochen sowie ebenfalls mit Response und Remission der Depression (HAMD-7; p<0,0001). Zusätzlich wurde eine positive Korrelation zwischen „early improvement“ der Anhedonie und einer Verbesserung der sozialen Funktionsfähigkeit (SDS) deutlich, was bislang nur aus wenigen Untersuchungen bekannt ist [12, 29]. Die dargestellten Praxisversorgungs-Daten geben allerdings erstmals einen Hinweis auf den positiven prädiktiven Wert eines „early improvement“ von Anhedonie für eine Verbesserung der sexuellen Beeinträchtigung (p<0,0001) nach 12 Wochen, was bislang nach den Autoren vorliegenden Informationen in dieser Form nicht beschrieben wurde.
Vor dem Hintergrund der bestehenden Datenlage zu Prädiktion des Therapieverlaufs einer Depression können die vorliegenden Ergebnisse eines „early improvement“ von Anhedonie nicht als spezifischer Prädiktor für die Besserung der depressiven Symptomatik angesehen werden. Weitere Studien zu der Fragestellung des Symptoms Freudlosigkeit erscheinen allerdings sinnvoll, um die mögliche Spezifität eines „early improvement“ von Anhedonie für die Verbesserung der sozialen Funktionsfähigkeit und die Sexualität zu untersuchen, wofür die vorliegenden Daten erste Hinweise liefern.
Da gängige Depressionsskalen die Sexualität von depressiven Patienten nicht erfassen und eine aktive Nachfrage in der Praxisroutine häufig nicht erfolgt, stellt sich die Frage nach geeigneten Beurteilungsinstrumenten. Neben spezifischen Fragebogen zu Sexualität (z.B. Sex-FX nach Kennedy et al., 2001; ASEX nach McGahuey et al., 2000), die wegen Intimität der Thematik teilweise ungern genutzt werden, könnte die Erfassung der Anhedonie hierzu einen indirekten Beitrag leisten, zumal ein bidirektionaler Zusammenhang wahrscheinlich ist.
Das günstige Verträglichkeitsprofil von Agomelatin bestätigte sich in der untersuchten Kohorte (6,8% UE bzw. 5,8% UAW) und die Verträglichkeit wurde von 96,5% als sehr gut/gut bewertet. Es ergaben sich gegenüber klinischen Studien keine zusätzlichen Informationen hinsichtlich Häufigkeiten und Art der unerwünschten Arzneimittelwirkungen [9, 16, 48].
Als Limitation dieser Studie ist das offene, nichtinterventionelle Studiendesign zu nennen, da die fehlende Randomisierung, das Fehlen einer Placebo-Kontrollgruppe und geringes Monitoring zu einer Überschätzung des Behandlungseffekts führen können. Demgegenüber steht allerdings der Vorteil dieses Studiendesigns ohne strenge Ein- und Ausschlusskriterien, um somit praxisrelevante Patienten mit Komorbiditäten und Komedikation in die Untersuchung einschließen zu können. Der Behandlungseffekt ist zudem vergleichbar mit vorliegenden Daten aus klinisch kontrollierten Studien [5, 23, 48]. Eine weitere Limitation ist die kurze Studiendauer von 12 Wochen, da die anhaltende Wirkung auf positive wie negative Emotionen nicht abschließend beurteilt werden kann. Allerdings zeigt sich eine Beobachtungsdauer von drei Monaten zur grundsätzlichen Beurteilung eines Behandlungseffekts in kontrollierten Studien sowie auch in weiteren „Real-Life“-Studien als durchaus geeignet [28, 48]. Eine Studiendauer von 12 Wochen wird außerdem von der europäischen Zulassungsbehörde EMA als geeigneter Zeitrahmen für den Nachweis der Kurzzeitwirksamkeit empfohlen. Als weitere Limitation kann aufgrund der Patientenzahl von 970 Patienten und des nichtinterventionellen Studiendesigns eine Unterschätzung der Häufigkeit von UAWs nicht gänzlich ausgeschlossen werden. Vor dem Hintergrund des günstigen Verträglichkeitsprofils in klinischen Studien bestätigen die vorliegenden Daten aus der täglichen Praxis allerdings Art und Häufigkeit der unerwünschten Arzneimittelwirkungen.
Zusammenfassend geben die vorliegenden Daten aus dem Versorgungsalltag einen Hinweis auf die Bedeutung positiver Emotionen im Sinne von Freude, Motivation und Interesse im Behandlungsverlauf einer Depression. Der antidepressive Effekt von Agomelatin wurde neben einer Verbesserung der gedrückten Stimmung und Traurigkeit durch die positive Wirkung auf eine vorliegende Anhedonie deutlich. Eine frühzeitige Zunahme positiver Emotionen und Verbesserung von Freude und Interesse korrelierte in der untersuchten Kohorte ambulanter Patienten signifikant mit einer Verbesserung der Depression und besitzt einen positiven prädiktiven Wert für Response und Remission der Depression sowie der Verbesserung von sozialer Funktionsfähigkeit und Sexualität im weiteren Behandlungsverlauf. Das günstige Verträglichkeitsprofil bestätigt sich bei den untersuchten Patienten im klinischen Alltag.
Anhand der dargestellten Studiendaten erscheint es sinnvoll, neben der Verbesserung negativer Emotionen die Wiederherstellung positiver Emotionalität und der Fähigkeit, Freude und Interesse zu entwickeln, als zusätzliches Therapieziel für die Psychopharmakotherapie, vermutlich aber auch für nicht medikamentöse Therapieansätze, für depressive Patienten zu nutzen.
Interessenkonflikterklärung
GH: Honorare für die Beratung oder Teilnahme an einem Advisory Board von Actelion, Lundbeck, Merck, Servier, Springer; Honorare für Vorträge, Stellungnahmen oder Artikel von Actelion, Affectis, AstraZeneca, Bayerische Motorenwerke, Bayer Vital, Boehringer Ingelheim, BMBF, Bundesamt für Strahlenschutz, BrainLab, Bristol-Myers Squibb, Cephalon, Daimler Benz, Deutsche Forschungsgemeinschaft, Elsevier, EuMeCom, Georg Thieme, Gerson Lerman Group Council of Healthcare Advisors, GlaxoSmithKline, Janssen-Cilag, Lilly, Lundbeck, McKinsey, Meda, Merck, Merz, Network of Advisors, Neurim, Neurocrine, Novartis, Orphan, Pfizer, Pharmacia, Procter & Gamble, Purdue, Sanofi-Aventis, Sepracor, Servier, Springer, Takeda, Transcept, Urban & Fischer, Volkswagen; Unterstützung für Kongressbesuche von AstraZeneca, GlaxoSmithKline, Janssen-Cilag, Lilly, Lundbeck, Merck, Merz, Pfizer, Sanofi-Aventis, Servier, Springer, Takeda; Forschungsbeihilfe von BMBF, Bundesamt für Strahlenschutz, BrainLab, Janssen-Cilag
BB: Angestellte von Servier Deutschland GmbH
ML: Honorare für die Beratung oder Teilnahme an einem Advisory Board von Eli Lilly; Honorare für Vorträge, Stellungnahmen oder Artikel von Eli Lilly, Lundbeck, Servier; Unterstützung für Kongressbesuche von Lundbeck, Servier; sonstige Unterstützung von Janssen, Otsuka, Servier
Literatur
1. AMDP&CIPS. Rating Scales for psychiatry: European edition. Weinheim: Beltz Test, 1990.
2. Baldwin DS, Foong T. Antidepressant drugs and sexual dysfunction. Br J Psychiatry 2013;202:396–7.
3. Cohen S, Kuhn KU, Bender S, Erfurth A, et al. Sexual impairment in psychiatric inpatients: focus on depression. Pharmacopsychiatry 2007;40:58–63.
4. Corruble E, de Bodinat C, Belaidi C, Goodwin GM. Efficacy of agomelatine and escitalopram on depression, subjective sleep and emotional experiences in patients with major depressive disorder: a 24-week randomized, controlled, double-blind trial. Int J Neuropsychopharmacol 2013;16:2219–34.
5. Demyttenaere K, Corruble E, Hale A, Quera Salva MA, et al. A pooled analysis of six month comparative efficacy and tolerability in four randomized clinical trials: agomelatine versus escitalopram, fluoxetine and sertraline. CNS Spectrums 2013;18:163–70.
6. Demyttenaere K, Donneau AF, Albert A, Ansseau M, et al. What is important in being cured from: does discordance between physicians and patients matter? (2). J Affect Disord 2015;174:372–7.
7. Demyttenaere K, Donneau AF, Albert A, Ansseau M, et al. What is important in being cured from depression? Discordance between physicians and patients (1). J Affect Disord 2015;174:390–6.
8. Di Giannantonio M, Di Iorio G, Guglielmo R, De Berardis D, et al. Major depressive disorder, anhedonia and agomelatine: an open-label study. J Biol Regul Homeost Agents [Clinical Trial Multicenter Study]. 2011;25:109–14.
9. Fachinformation. Valdoxan 25 mg, 2017.
10. Ferguson JM. SSRI antidepressant medications: Adverse effects and tolerability. Prim Care Companion J Clin Psychiatry 2001;3:22–7.
11. Franz M, Lemke MR, Meyer T, Ulferts J, et al. Deutsche Version der Snaith-Hamilton-Pleasure-Scale (SHAPS-D). Fortschr Neurol Psychiat 1998;66:407–13.
12. Gargoloff PD, Corral R, Herbst L, Marquez M, et al. Effectiveness of agomelatine on anhedonia in depressed patients: an outpatient, open-label, real-world study. Hum Psychopharmacol 2016;31:412–8.
13. Geschwind N, Nicolson NA, Peeters F, van Os J, et al. Early improvement in positive rather than negative emotion predicts remission from depression after pharmacotherapy. Eur Neuropsychopharmacol 2011;21:241–7.
14. Goodwin GM, Price J, De Bodinat C, Laredo J. Emotional blunting with antidepressant treatments: A survey among depressed patients. J Affect Disord 2017;221:31–5.
15. Gorwood P, Demyttenare K, Vaiva G, Corruble E, et al. An increase in joy after two weeks is more specific of later antidepressant response than a decrease in sadness. J Affect Disord 2015;185:97–103.
16. Guaiana G, Gupta S, Chiodo D, Davies SJ, et al. Agomelatine versus other antidepressive agents for major depression. Cochrane Database Syst Rev 2013;12:CD008851.
17. Hale A, Corral RM, Mencacci C, Ruiz JS, et al. Superior antidepressant efficacy results of agomelatine versus fluoxetine in severe MDD patients: a randomized, double-blind study. Int Clin Psychopharmacol 2010;25:305–14.
18. Hamilton M. A rating scale for depression. J Neurol Neurosurg Psychiatry 1960;23:56–62.
19. Harmer CJ, de Bodinat C, Dawson GR, Dourish CT, et al. Agomelatine facilitates positive versus negative affective processing in healthy volunteer models. J Psychopharmacol [Randomized Controlled Trial Research Support, Non-U.S. Gov’t] 2011;25:1159–67.
20. Henkel V, Seemüller F, Obermeier M, Adli M, et al. Does early improvement triggered by antidepressants predict response/remission? Analysis of data from a naturalistic study on a large sample of inpatients with major depression. J Affect Disord 2009;115: 439–49.
21. Hickie IB, Rogers NL. Novel melatonin-based therapies: potential advances in the treatment of major depression. Lancet 2011;378:621–31.
22. Jacobi F, Höfler M, Strehle J, Mack S, et al. Psychische Störungen in der Allgemeinbevölkerung. Studie zur Gesundheit Erwachsener in Deutschland und ihr Zusatzmodul Psychische Gesundheit (DEGS1-MH). Nervenarzt 2014;85:77–87.
23. Kasper S, Hale A, Lemoine P. Superior efficacy results of agomelatine versus main current SSRI/SNRI antidepressants
24. Kasper S, Corruble E, Hale A, Lemoine P, et al. Antidepressant efficacy of agomelatine versus SSRI/SNRI: results from a pooled analysis of head-to-head studies without a placebo control. Int Clin Psychopharmacol 2013;28:12–9.
25. Kennedy SH, Rizvi SJ. Agomelatine in the treatment of major depressive disorder – review article. CNS Drugs 2010;24:479–99.
26. Kennedy SH, Rizvi S, Fulton K, Rasmussen J. A double-blind comparison of sexual functioning, antidepressant efficacy, and tolerability between agomelatine and venlafaxine XR. J Clin Psychopharmacol 2008;28: 329–33.
27. Kennedy SH, Avedisova A, Giménez-Montesions N, et al. A placebo-controlled study of three agomelatine dose regimens (10 mg, 25 mg, 25–50 mg) in patients with major depressive disorder. Eur Neuropsychopharmacol 2014;24:553–63.
28. Laux G, Barthel B, Hajak G, Lemke M, et al. Pooled analysis of four non-interventional studies: Effectiveness and tolerability of the antidepressant agomelatine in daily practice. Adv Ther; doi:101007/s12325–017–0485-z. 2017 (Zugriff am 04.09.2017).
29. Llorca P, Gourion D. Course of anhedonia and depressive symptoms in a population of depressed outpatients treated with agomelatine. Eur Neuropsychopharmacol 2014;24(Suppl 2):S468.
30. Malejko K, Abler B, Graf H. Neuronale Korrelate sexueller Funktionen unter Antidepressiva. Nervenheilkunde 2016;35:575–81.
31. Marschall J, Hildebrandt S, Sydow H, Nolting H. DAK Gesundheitsreport 2017 Analyse der Arbeitsunfähigkeitsdaten – Update Schlafstörungen. Storm A (Hrsg.). Heidelberg: medhochzwei-Verlag GmbH, 2017.
32. Martinotti G, Sepede G, Gambi F, Di Iorio G, et al. Agomelatine versus venlafaxine XR in the treatment of anhedonia in major depressive disorder: a pilot study. J clin Psychopharmacol [Randomized Controlled Trial Research Support, Non-U.S. Gov’t] 2012;32:487–91.
33. McIntyre R, Kennedy S, Bagby RM, Bakish D. Assessing full remission. J Psychiatry Neurosci 2002;27:235–9.
34. McIntyre RS, Konarski JZ, Mancini DA, Fulton KA, et al. Measuring the severity of depression and remission in primary care: validation of the HAMD-7 scale. CMAJ 2005;173:1327–34.
35. Montejo A, Majadas S, Rizvi SJ, Kennedy SH. The effects of agomelatine on sexual function in depressed patients and healthy volunteers. Hum Psychopharmacol [Review] 2011;26:537–42.
36. Montgomery SA, Asberg M. A new depression scale designed to be sensitive to change. Br J Psychiatry 1979;134:382–9.
37. Nutt D, Demyttenaere K, Janka Z, Aarre T, et al. The other face of depression, reduced positive affect: the role of catecholamines in causation and cure. J Psychopharmacol (Oxford, England) 2006;21:461–71.
38. Olie JP, Kasper S. Efficacy of agomelatine, a MT1/MT2 receptor agonist with 5-HT2C antagonistic properties in major depressive disorder. Int J Neuropsychopharmacol 2007;10:661–73.
39. Pecenak J, Novotny V. Agomelatine as monotherapy for major depression: an outpatient, open-label study. Neuropsychiatr Dis Treat 2013;9:1595–604.
40. Price J, Cole V, Goodwin GM. Emotional side-effects of selective serotonin reuptake inhibitors: qualitative study. Br J Psychiatry 2009;195:211–7.
41. Racagni G, Riva MA, Molteni R, Musazzi L, et al. Mode of action of agomelatine: synergy between melatonergic and 5-HT2C receptors. World J Biol Psychiatry 2011;12:574–87.
42. Rush J, et al. Handbook of Psychiatric Measures. Washington, DC: American Psychiatric Association, 2000: 113–5.
43. Serretti A, Chiesa A. Treatment-emergent sexual dysfunction related to antidepressants: a meta-analysis. J Clin Psychopharmacol 2009;29:259–66.
44. Snaith RP, Hamilton M, Morley S, Humayan A, et al. A scale for the assessment of hedonic tone the Snaith-Hamilton Pleasure Scale. Br J Psychiatry 1995;167:99–103.
45. Spijker J, Bijl RV, de Graaf R, Nolen WA. Determinants of poor 1-year outcome of DSM-III-R major depression in the general population: results of the Netherlands Mental Health Survey and Incidence Study (NEMESIS). Acta Psychiatr Scand 2001;103:122–30.
46. Szegedi A, Jansen WT, van Willigenburg AP, van der Meulen E, et al. Early improvement in the first 2 weeks as a predictor of treatment outcome in patients with major depressive disorder: a meta-analysis including 6562 patients. J Clin Psychiatry 2009;70:344–53.
47. Tadic A, Helmreich I, Mergl R, Hautzinger M, et al. Early improvement is a predictor of treatment outcome in patients with mild major, minor or subsyndromal depression. J Affect Disord 2010;120:86–93.
48. Taylor D, Sparshatt A, Varma S, Olofinjana O. Antidepressant efficacy of agomelatine: meta-analysis of published and unpublished studies. BMJ 2014;348:g1888.
49. Taylor DJ, Walters HM, Vittengl JR, Krebaum S, et al. Which depressive symptoms remain after response to cognitive therapy of depression and predict relapse and recurrence? J Affect Disord 2010;123:181–7.
50. Uher R, Perlis RH, Henigsberg N, Zobel A, et al. Depression symptom dimensions as predictors of antidepressant treatment outcome: replicable evidence for interest-activity symptoms. Psychol Med 2012;42:967–80.
51. Vinckier F, Gourion D, Mouchabac S. Anhedonia predicts poor psychosocial functioning: Results from a large cohort of patients treated for major depressive disorder by general practitioners. Eur Psychiatry 2017;44:1–8.
52. Volz HP, Escafit-Schülke ML. Effekte von Agomelatin bei depressiven Patienten im Praxisalltag – Ergebnisse der nicht-interventionellen Studie VIVRE. Nervenheilkunde 2015;34:809–17.
53. Vrieze E, Demyttenaere K, Bruffaerts R, Hermans D, et al. Dimensions in major depressive disorder and their relevance for treatment outcome. J Affect Disord 2014;155:35–41.
54. Weyer G. Internationale Skalen für Psychiatrie. 5., vollständig überarbeitete und erweiterte Auflage. Göttingen: Beltz Test, 2005.
55. Wittchen HU, Jacobi F, Rehm J, Gustavsson A, et al. The size and burden of mental disorders and other disorders of the brain in Europe 2010. Eur Neuropsychopharmacol 2011;21:655–79.
56. Zimmerman M, McGlinchey JB, Posternak MA, Friedman M, et al. How should remission from depression be defined? The depressed patient’s perspective. Am J Psychiatry 2006;163:148–50.
Prof. Dr. med. Göran Hajak, Klinik für Psychiatrie, Psychosomatik und Psychotherapie der Sozialstiftung Bamberg, St.-Getreu-Straße 18, 96049 Bamberg, E-Mail: goeran.hajak@solzialstiftung-bamberg.de
Dr. med. Bettina Barthel, Medical Affairs, Servier Deutschland GmbH, Elsenheimerstraße 53, 80687 München
Prof. Dr. med. Matthias Lemke, Evangelische Stiftung Alsterdorf, Hamburg, Heinrich Sengelmann Krankenhaus, Psychiatrie, Psychotherapie und Psychosomatik, Kayhuder Straße 65, 23863 Bargfeld-Stegen, Universität Kiel
Early improvement of emotional regulation as an early predictor for treatment response to antidepressants. Results of the non-interventional study with agomelatine – VIVID-ON
Objective: Anhedonia, the inability to experience joy, is a key symptom of depression and is also described as residual symptom in patients with partial remission. Social functioning is influenced by anhedonia and results in impairment of daily life of depressed patients. Using the example of the non-interventional study VIVID-ON (Valdoxan® improves vitality in depression with anhedonia) the effect of agomelatine on anhedonia was investigated. Furthermore the correlation between early improvement of anhedonia and treatment response concerning depressive symptoms and social functioning was examined in patients with major depression under naturalistic conditions.
Methods: 970 depressive patients were treated with agomelatine (25–50 mg) for 12 weeks. Treatments effects were evaluated by Hamilton Depression Scale short version (HAMD-7), Clinical Global Impression-Scale (CGI), Snaith-Hamilton Pleasure Scale (SHAPS), Sheehan Disability Scale (SDS), and two questions concerning sexuality.
Results: At week 12, response and remission rates according to HAMD-7 were 64.1% and 49.3%, respectively. Social functioning (SDS) improved in 87.9% and anhedonia (SHAPS) in 81.9% of all patients. An early decrease of the SHAPS score (>20% at week 3) shows significant correlation (p<0.0001) with response/remission (HAMD-7) as well as with improvement in social functioning and sexuality.
Conclusion: An early improvement of anhedonia has a predictive value for a positive treatment outcome of depression, social functioning and impairment in sexuality in patients of daily practice. Results of the evaluated cohort suggest that improvement of anhedonic symptoms should be addressed in the treatment of depressive disorder.
Key words: Agomelatine, anhedonia, treatment-outcome, social functioning, sexual function
Psychopharmakotherapie 2017; 24(06):248-258
