Holger Petri, Bad Wildungen*
Aromatasehemmer
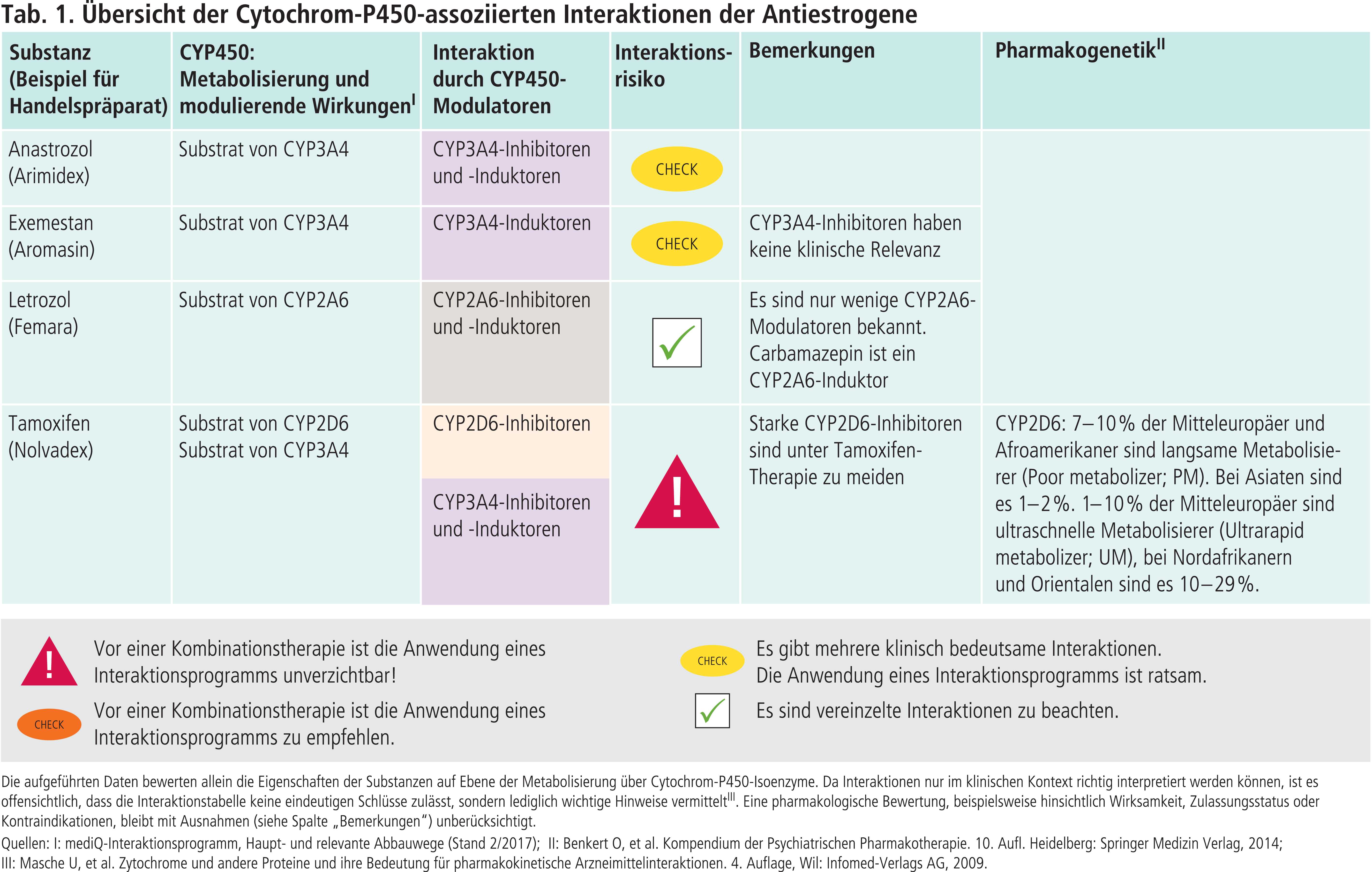
Anastrozol und Exemestan sind steroidale Aromatasehemmer. In-vitro-Untersuchungen zufolge wird Anastrozol primär über CYP3A4 zum inaktiven Metaboliten Hydroxyanastrozol und weiter über die Uridin-5’-diphosphat-Glucuronosyltransferase (UGT) 1A4 abgebaut. Welche klinischen Konsequenzen sich hieraus in Kombination mit potenten CYP3A4-Modulatoren ergeben, ist erst noch durch klinische Studien zu untersuchen [7]. Exemestan wird oxidativ über CYP3A4 zu 6-Hydroxymethylexemestan und über Aldoketoreduktasen zu 17-Hydroexemestan reduziert. Während der starke CYP3A4-Inhibitor Ketoconazol keine bedeutende Wirkung auf die Pharmakokinetik von Exemestan hat, sinkt die AUC (Fläche unter der Konzentrations-Zeit-Kurve) unter dem starken CYP3A4-Induktor Rifampicin um 54%. Nach Herstellerangaben kann ein Verlust der Wirksamkeit auch in Kombination mit anderen starken CYP3A4-Induktoren (Abb. 1) nicht ausgeschlossen werden und die US-amerikanische Fachinformation empfiehlt eine Dosisverdopplung [5, 10].
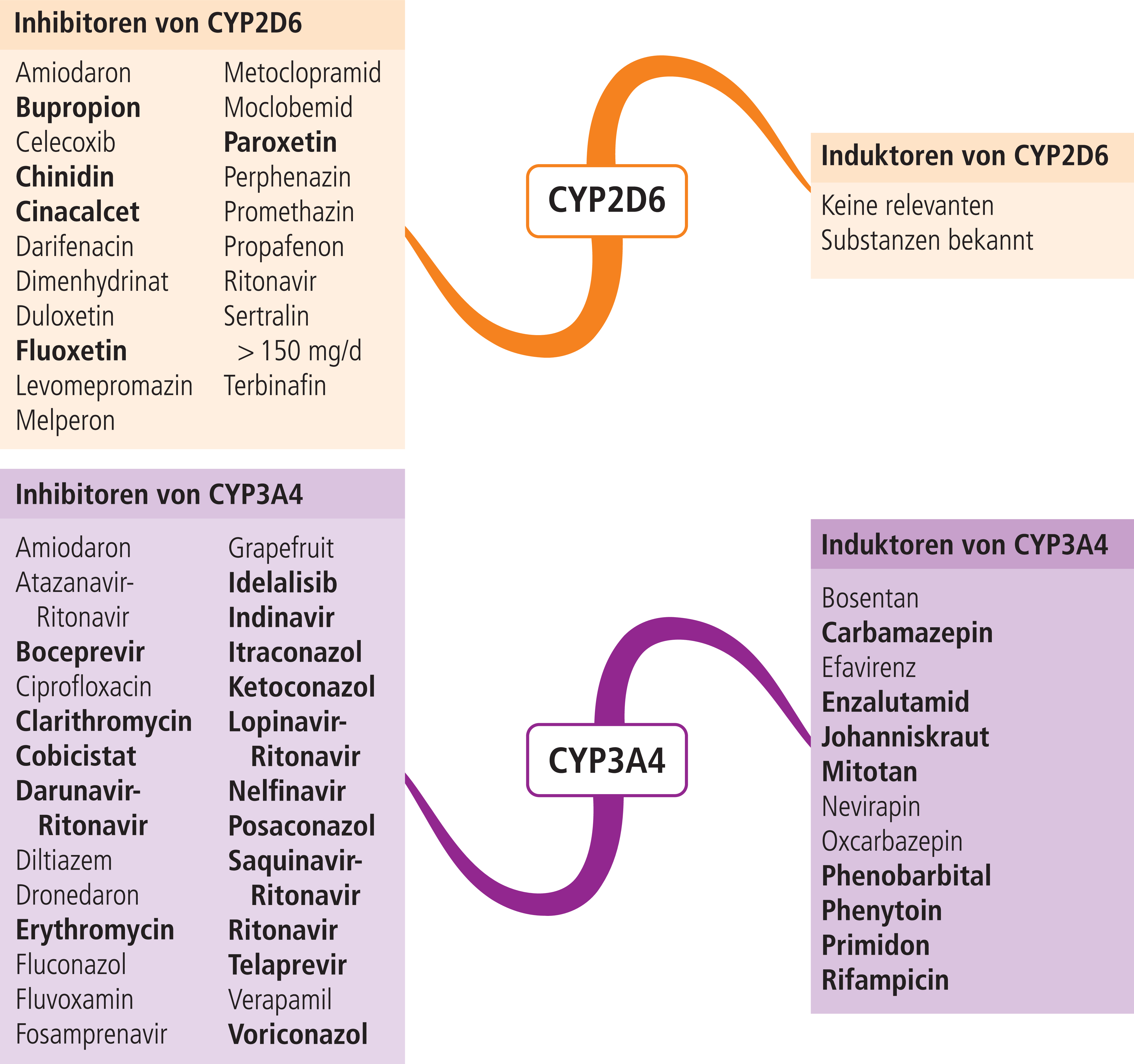
Abb. 1. Auswahl von modulierenden Substanzen (stark wirkende fettgedruckt) mit klinisch relevanter Wirkung auf Cytochrom P450 (CYP) 2D6 und 3A4 (Stand: 2/2017) [Quelle: mediQ-Interaktionsprogramm]
Letrozol wird in vitro über CYP2A6 und 3A4 abgebaut. In vivo hängt der Metabolismus aber wesentlich von der Funktionalität des polymorphen Isoenzyms CYP2A6 ab [3]. Patienten mit einem Poor-Metabolizer-Status haben durchschnittlich 2-fach höhere Talspiegel verglichen mit Patienten mit zwei funktionsfähigen Allelen [9]. Hingegen haben Patienten mit einem oder zwei Allelvarianten, die für CYP2A6-Enzyme mit erhöhter Aktivität kodieren, 84,3% bzw. 44,8% der Estrogenwerte von Frauen mit normaler Enzymaktivität [12]. Carbamazepin ist ein CYP2A6-Induktor [13]. Eine Erniedrigung der Letrozol-Plasmaspiegel ist in Kombination mit dem Antikonvulsivum zu erwarten.
Zusammenfassend sind valide Daten zu pharmakokinetischen Wechselwirkungen auch in Hinsicht harter Endpunkte rar. Im Einzelfall ist zu erwägen, die Estrogen-Spiegel zu messen und ggf. auf einen Aromatasehemmer mit einem anderen Stoffwechselweg zu wechseln.
Tamoxifen
Tamoxifen wird als Prodrug über hepatische Cytochrom-P450(CYP)-Isoenzyme zu wirksamen Metaboliten bioaktiviert. Von diesen ist Endoxifen der wichtigste für die klinische Wirksamkeit des Antiestrogens. Endoxifen hat eine etwa 100-fach höhere Affinität zum Estrogenrezeptor als Tamoxifen und erreicht unter den aktiven Metaboliten die höchsten Plasmaspiegel. In zwei Schritten wird Endoxifen aus Tamoxifen gebildet. Vorrangig über CYP3A4 entsteht N-Desmethyl-Tamoxifen, das weiter über CYP2D6 zu Endoxifen verstoffwechselt wird. Es existieren zahlreiche weitere Abbauwege [1].
Vasomotorische Symptome der Wechseljahre können durch selektive Serotonin-Wiederaufnahmehemmer (SSRI) gelindert werden. Patientinnen unter Tamoxifentherapie wurden zur Behandlung von Hitzewallungen daher über Jahre SSRI-Antidepressiva wie Paroxetin verordnet. Paroxetin hemmt irreversibel CYP2D6 und konsekutiv wird die Bildung von Endoxifen aus Tamoxifen stark reduziert. Gemäß einer kanadischen Kohortenstudie führte die gleichzeitige Verabreichung von Tamoxifen mit Paroxetin zu einer Erhöhung der Brustkrebssterblichkeit [8]. Als Konsequenz dieser „silent drug-drug interaction“ wurde die Tamoxifen-Fachinformation überarbeitet [2]. Tamoxifen soll möglichst nicht mehr mit starken CYP2D6-Hemmern (Abb. 1) kombiniert werden. CYP2D6 wird polymorph exprimiert. Es werden abhängig von der Metabolisierungsaktivität vier Phänotypen unterschieden [11]:
- Langsame Metabolisierer (Poor Metabolizer; PM) → stark reduzierter Stoffwechsel
- Intermediäre Metabolisierer (Intermediate Metabolizer; IM) → reduzierter Stoffwechsel
- Extensive Metabolisierer (Extensive Metabolizer; EM) → normaler Stoffwechsel
- Ultraschnelle Metabolisierer (Ultrarapid Metabolizer; UM) → beschleunigter Stoffwechsel
Frauen mit einem IM- und PM-Status haben bis zu 60% und 74% niedrigere Endoxifen-Konzentrationen verglichen mit Frauen mit einem EM-Phänotyp [1]. Eine spiegelgesteuerte Eskalation der Tamoxifen-Dosis auf bis zu 120 mg pro Tag konnte bei Patientinnen mit einem PM- oder IM-Phänotyp die Endoxifen-Konzentration in einen klinisch wirksamen Bereich erhöhen, ohne dass es zu mehr Nebenwirkungen kam [4]. Inwiefern sich die Studienergebnisse auch auf Patientinnen übertragen lassen, die gleichzeitig starke CYP2D6-Hemmer einnehmen, ist nicht bekannt und bedarf weiterer Untersuchungen.
Unter der Annahme, durch Induktion von CYP3A4 besonders bei CYP2D6-defizienten Patientinnen die Endoxifen-Spiegel zu boostern, wurde Tamoxifen mit dem CYP3A4-Induktor Rifampicin kombiniert. Anders als erwartet, sank die Endoxifen-Exposition um 28 bis 85%. Analog zu Rifampicin fällt die Endoxifen-Konzentration durch den CYP3A4-Induktor Phenytoin um 83%. Somit sollten starke CYP3A4-Induktoren in Kombination mit Tamoxifen gemieden werden [1]. Mechanistisch wird die Plasmaspiegelabsenkung erklärt zum einen durch eine erhöhte Clearance von Tamoxifen und seiner Metaboliten durch die CYP3A4-Induktion, zum anderen durch eine beschleunigte Endoxifen-Ausscheidung aufgrund einer gesteigerten Bildung des Effluxtransporters P-Glykoprotein (P-gp) und von Phase-II-Enzymen wie UGT [6]. Dazu passt, dass homozygote wie heterozytote Trägerinnen der CYP3A4*22-Allele erhöhte Endoxifen-Plasmaspiegel aufweisen. Das Allel CYP3A4*22 kodiert für Enzyme mit verminderter Aktivität. Ob potente CYP3A4-Hemmer auch zu erhöhten Endoxifen-Werten führen, ist nicht bekannt.
Wirkung und Verträglichkeit einer Tamoxifen-Therapie sind maßgeblich abhängig von der Endoxifen-Konzentration. Neben individuellen pharmakogenetischen Besonderheiten führen zum Teil nicht ausreichend untersuchte Arzneimittelinteraktionen neben Alter, Body Mass Index (BMI) und saisonalen Einflüssen zu inter- und intraindividuell unterschiedlichem Behandlungserfolg. Vor diesem Hintergrund sollte besonders bei prämenopausalen Frauen, bei denen Aromatasehemmer keine Alternative darstellen, zur Sicherung der Therapie ein therapeutisches Drug-Monitoring (TDM) von Endoxifen erwogen werden. Entsprechend den Warnhinweisen zur Kombination von Tamoxifen mit CYP2D6-Inhibitoren wäre es wünschenswert, wenn die Fachinformationen auch von der gleichzeitigen Anwendung von CYP3A4-Induktoren abraten würden.
Literatur
1. Binkhorst L, Mathijssen RH, Jager A, et al. Individualization of tamoxifen therapy: much more than just CYP2D6 genotyping. Cancer Treat Rev 2015;41:289–99.
2. Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM). Tamoxifen: Wechselwirkungen mit CYP2D6-Inhibitoren. Bescheid vom 14.11.2012.
3. Desta Z, Kreutz Y, Nguyen AT, et al. Plasma letrozole concentrations in postmenopausal women with breast cancer are associated with CYP2A6 genetic variants, body mass index, and age. Clin Pharmacol Ther 2011;90:693–700.
4. Dezentje VO, Opdam FL, Gelderblom H, et al. CYP2D6 genotype- and endoxifen-guided tamoxifen dose escalation increases endoxifen serum concentrations without increasing side effects. Breast Cancer Res Treat 2015;53:583–90.
5. Fachinformation Aromasin® . Stand: Juni 2016.
6. Henderson SL, Teft WA, Kim RB. Profound reduction in tamoxifen active metabolite endoxifen in a breast cancer patient treated with rifampin prior to initiation of an anti-TNFα biologic for ulcerative colitis: a case report. BMC Cancer DOI 10.1186/s12885–016–2342-x.
7. Kamdem LK, Liu Y, Stearns V, et al. In vitro and in vivo oxidative metabolism and glucuronidation of anastrozole. Br J Clin Pharmacol 2010;70:854–69.
8. Pantke E, Hillen K. Erhöhte Brustkrebssterblichkeit nach gleichzeitiger Anwendung von Tamoxifen und SSRI. Bulletin zur Arzneimittelsicherheit 2010;2:3–6.
9. PharmGKB. Pharmaceuticals and Medical Devices Agency, Japan (PMDA) label information for letrozole and CYP2A6. www.pharmgkb.org/label/PA166160717 (Zugriff am 08.02.2017).
10. Prescribing information Aromasin. Stand: Mai 201411.
11. Reinecke K, Böhm R, Haen E, et al. Arzneimittel und CYP2D6. Dtsch Apo Ztg 2012;47:60–6.
12. Tanii H, Shitara Y, Horie T. Population pharmacokinetic analysis of letrozole in Japanese postmenopausal women. Eur J Clin Pharmacol 2011;67:1017–25.
13. Williams JM, Gandhi KK, Benowitz NL. Carbamazepine but not valproate induces CYP2A6 activity in smokers with mental illness. Cancer Epidemiol Biomarkers Prev 2010;19:2582–9.
*Nachdruck aus Krankenhauspharmazie 2017;38:152–5.
Der Artikel wurde unter Einbeziehung von Diskussionsbeiträgen von Dr. Jörg Brüggmann, Berlin, Prof. Dr. Christoph Hiemke, Mainz, und Dr. Jochen Weber, Bad Wildungen, erstellt.
Holger Petri, Zentral-Apotheke der Wicker Kliniken, Im Kreuzfeld 4, 34537 Bad Wildungen, E-Mail: hpetri@werner-wicker-klinik.de
Psychopharmakotherapie 2017; 24(02)
