Thomas Müller, Berlin
Levodopa ist eine physiologische Aminosäure und der natürliche Vorläufer des Neurotransmitters Dopamin. Im Gegensatz zu Dopamin kann es die Blut-Hirn-Schranke mittels eines aktiven Aminosäure-Transporters gut überwinden. Levodopa wurde zuerst in Japan von Sato oral in niedriger Dosierung gegeben. Dann wurde es von Birkmayer in Wien bei Parkinson-Patienten in klinisch die Motorik verbessernder, höherer Dosis als Infusion und somit kontinuierlicher intravenös verabreicht [4, 33]. Auch wegen seiner guten Verträglichkeit ist Levodopa das wirksamste Arzneimittel zur Behandlung von motorischen Symptomen bei Patienten mit einem idiopathischen Parkinson-Syndrom.
Warum Levodopa mit Enzymhemmern gegeben wird
In der Körperperipherie wird Levodopa schnell zu Dopamin metabolisiert. Deshalb wird es heute in Kombination mit einem Hemmer der Dopadecarboxylase (DDC), beispielsweise Carbidopa (CD) oder Benserazid (BE), verabreicht. Dadurch wird Levodopa in der Peripherie vermehrt über die Catechol-O-Methyltransferase (COMT) abgebaut. Die COMT methyliert Levodopa zu 3-O-Methyldopa (3-OMD) (Abb. 1). COMT-Hemmung führt zur Erhöhung der Bioverfügbarkeit und zur Verlängerung der Halbwertszeit von Levodopa im Blut. Die Bildung von 3-OMD wird verringert. Der Transport von Levodopa über die Blut-Hirn-Schranke wird möglicherweise verbessert. Es gibt Hinweise, dass 3-OMD mit Levodopa am Aminosäure-Transportmechanismus in Konkurrenz steht. Dies wird aber kontrovers beurteilt [3, 39]. Pharmakologisch stellt dieses Konzept eine gewollte Arzneimittelinteraktion dar. Sie verändert die Pharmakokinetik und verbessert die Pharmakodynamik von Levodopa. Als Folge der Hemmung von DDC und COMT wird Levodopa vermehrt über die Tyrosinaminotransferase zu Dihydroxyphenylpyruvat metabolisiert (Abb. 1). Gleichzeitig erreicht aber mehr Levodopa das Gehirn als bei alleiniger Hemmung der DDC [49].
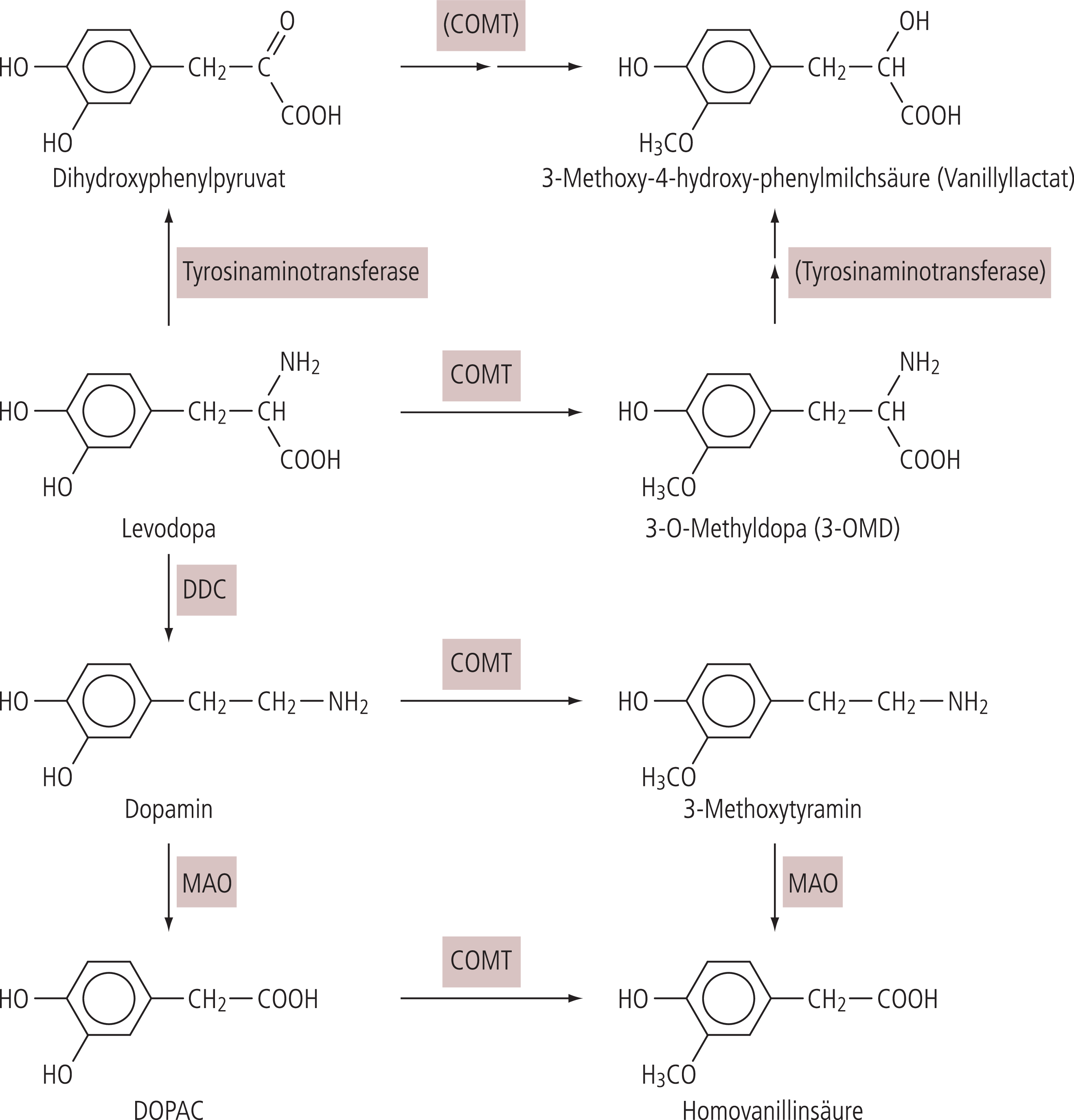
Abb. 1. Abbauwege von Levodopa. COMT: Catechol-O-Methyltransferase, DDC: Dopadecarboxylase, DOPAC: Dihydroxyphenylessigsäure, MAO: Monoaminoxidase
COMT
Die COMT ist beim Menschen peripher vor allem in Leber, Niere und Gastrointestinaltrakt vorhanden. Die physiologische Funktion der COMT ist die Methylierung aktiver oder toxischer Catechole. Zwei Formen der COMT, eine lösliche und eine an Membranen gebundene, sind identifiziert. Die lösliche Form überwiegt. Sie besteht beim Menschen aus 221 Aminosäuren. Die membrangebundene COMT hat 50 zusätzliche Aminosäuren, von denen 30 hydrophobe das Enzym in der Membran verankern, während der Rest der COMT an der zytoplasmatischen Seite der Membran anhängt. Ein einziges Gen auf Chromosom 22 kodiert beide Formen [21, 24].
COMT-Hemmer
Zur Parkinson-Therapie standen bisher zwei reversible COMT-Hemmer zur Verfügung, nämlich das peripher wirksame Entacapon (Comtess®, oder in Kombination mit Levodopa/CD in Stalevo®) und das peripher und zentral wirksame Tolcapon (Tasmar®) [8, 48]. Entacapon hemmt nahezu vollständig die COMT in Duodenum, Erythrozyten und Leber ein bis drei Stunden lang [21, 24]. Acht bis zwölf Stunden nach Gabe von Entacapon ist die COMT-Aktivität wieder hergestellt. Tolcapon inhibiert in einer Dosierung von 100 mg/kg Körpergewicht bei Ratten 15 bis 30 Minuten nach Gabe acht Stunden lang die COMT-Aktivität in Herz und Niere zu 90%, in Leber und Gehirn zu 70%; erst nach 16 Stunden erreicht die COMT-Aktivität wieder die ursprüngliche Stärke [15, 16]. Es gibt klinische Hinweise, dass Tolcapon Entacapon an Effizienz in der Therapie von Parkinson-Patienten überlegen ist. Dies hängt mit den zentralen Effekten von Tolcapon zusammen. Vor allem sie verbessern auch Kognition und Stimmung durch Verringerung des Abbaus biogener Amine in Gliazellen [2, 8, 38, 48].
Durch Zulassung und Einführung des nur peripher, aber lang wirksamen COMT-Hemmers Opicapon wird jetzt die Therapie mit Levodopa/DDC-Hemmer vereinfacht. Seine wesentlichen pharmakologischen Eigenschaften, Ergebnisse aus Studien an Tieren, gesunden Probanden und vor allem an Parkinson-Patienten sollen im Folgenden vorgestellt und seine mögliche, zukünftige Rolle in der realen Welt der Patientenversorgung diskutiert werden.
Opicapon
Opicapon (Entwicklungsbezeichnung: BIA 9–1067; Hersteller: BIAL – Portela & Ca) ist ein lang wirksamer COMT-Hemmer mit einer Nitrocatechol-Struktur (Abb. 2). Es zeigt eine hohe Bindungsaffinität zur COMT (Kd im sub-picomolaren Bereich [45]) und eine langsame Dissoziationskonstante und hat deshalb trotz seines relativ schnellen Abbaus im Körper eine lange Wirkungsdauer.
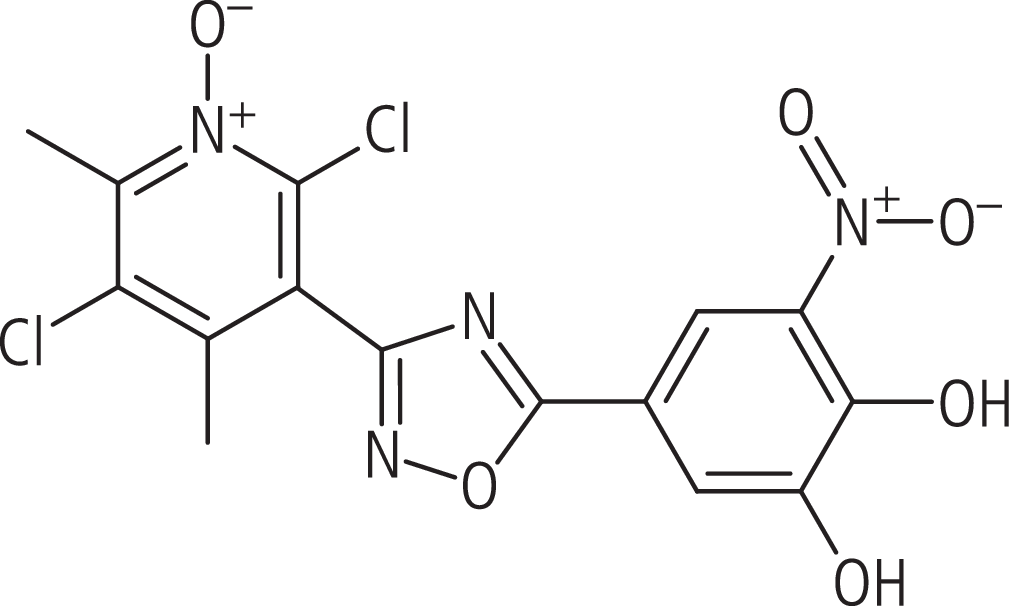
Abb. 2. Opicapon
Opicapon im Tierversuch
Additive Gabe von Opicapon vervielfachte die Bioverfügbarkeit von Levodopa und verzögerte die Zeit bis zum Erreichen der maximalen Konzentration von Levodopa. Die maximale Levodopa-Konzentration erhöhte sich nicht. Während sechs Stunden nach standardisierter Levodopa-Gabe war die systemische 3-OMD-Konzentration bei zusätzlicher Gabe von Opicapon im Vergleich zu der Bedingung ohne Einnahme von Opicapon deutlich erniedrigt (Tab. 1). Opicapon hemmte die lösliche COMT in Erythrozyten länger und stärker als Tolcapon [5, 6]. Design und Messintervalle können die Ergebnisse in Ratten und Affen maßgeblich beeinflussen. Sie wurden aber analog zu ähnlichen pharmakologischen Untersuchungen mit Entacapon und Tolcapon zur pharmakologischen Charakterisierung und des Wirkprinzips von Opicapon durchgeführt.
Tab. 1. Pharmakologische Charakteristika der drei verfügbaren COMT-Hemmer
|
Opicapon |
Entacapon |
Tolcapon |
|
|
Gabe |
Oral |
Oral |
Oral |
|
Einnahmefrequenz (täglich) |
1 |
Bis zu 10 |
3 |
|
Maximale COMT-Hemmung in vivo nach Einnahme [Stunden] |
3 |
0,5 |
1 |
|
COMT-Hemmung |
Peripher |
Peripher |
Peripher und zentral |
|
ED50 [mg·kg–1] 3 Stunden nach Gabe |
1,05±0,04 |
1,77±0,1 |
7,8±0,7 |
COMT: Catechol-O-Methyltransferase ED50: Dosis, die im Tierversuch die Aktivität der löslichen COMT 3 Stunden nach Gabe halbmaximal hemmt
Opicapon bei gesunden Versuchspersonen (Phase I)
Im Rahmen einer doppelblinden, randomisierten Studie wurden steigende Einmaldosen von 10 bis 1200 mg Opicapon der Reihe nach verabreicht. Acht Gruppen mit jeweils acht Teilnehmern wurden untersucht. Jeweils sechs Probanden erhielten Opicapon und zwei Placebo am Morgen nach einer zehnstündigen Nüchternphase. Maximale Konzentration und Bioverfügbarkeit von Opicapon nahmen ungefähr dosisabhängig zu. Trotz der relativ kurzen Halbwertszeit von Opicapon, die zwischen ein und vier Stunden liegt, hielt die Hemmung der löslichen COMT-Aktivität in Erythrozyten lange an. 72 Stunden nach Gabe lag diese immer noch zwischen 6% bei 10 mg Opicapon und 55% bei 1200 mg Opicapon. Die maximale Hemmung der löslichen COMT lag im Zeitraum zwischen einer and sechs Stunden nach Gabe von Opicapon und betrug 34,5% (10 mg), 71,7% (25 mg), 93,8% (50 mg), 96,3% (100 mg) bzw. 100% (200 mg, 400 mg, 800 mg, 1200 mg). Die Konzentrationen von Opicapon und dessen Metaboliten im Urin lagen unter der Nachweisgrenze. Opicapon wurde in allen untersuchten Dosierungen gut vertragen. Weitere 12 Probanden nahmen 50 mg Opicapon einmal nüchtern und nach einer hochkalorischen Mahlzeit ein. Vorherige Nahrungsaufnahme führte zu einer verminderten Resorption [1].
In einer randomisierten, doppelblinden Versuchsanordnung erhielten männliche Probanden acht Tage lang einmal täglich Placebo oder Opicapon in einer Dosierung von 5, 10, 20 oder 30 mg. Abbau und Ausscheidung von Opicapon sowie Hemmung der löslichen COMT-Aktivität in Erythrozyten durch Opicapon wurden untersucht. Dosisabhängig stieg die Bioverfügbarkeit. Die terminale Halbwertszeit von Opicapon war kurz und lag zwischen einer und 1,4 Stunden. Der Abbau von Opicapon erfolgte hauptsächlich über Sulfatierung und Ausscheidung über die Galle. Opicapon hemmte die COMT maximal zu 69,9% bis 98,0%. Diese Werte wurden nach der letzten Gabe erreicht. Die COMT-Hemmung durch Opicapon zeigte eine Halbwertszeit von über 100 Stunden [45].
In einer monozentrischen, randomisierten, doppelblinden, Placebo-kontrollierten Studie wurde der Einfluss verschiedener Opicapon-Dosierungen unter Steady-State-Bedingungen auf die Plasmakonzentration von Levodopa bei Einnahme von dreimal täglich 100/25 mg Levodopa/Carbidopa untersucht. Opicapon wurde elf Tage lang in Dosierungen von 25, 50 oder 75 mg/Tag einmal täglich abends (ca. 10 h vor der ersten Levodopa/CD-Gabe des Folgetags) verabreicht; die Messungen erfolgten an Tag 12. Eine aktive Vergleichsgruppe erhielt nur am letzten Tag 200 mg Entacapon zu jeder Applikation von Levodopa/Carbidopa. Die minimale und mittlere Konzentration von Levodopa im Plasma nahm dosisabhängig unter Opicapon und Entacapon im Vergleich zu Placebo zu. Unterschiede in der maximalen Levodopa-Konzentration fanden sich generell nicht. Die Bioverfügbarkeit von Levodopa stieg dosisabhängig unter Opicapon und unterschied sich jeweils signifikant von der unter Placebo. Die einmalige Gabe von 50 mg und 75 mg, aber nicht von 25 mg Opicapon führte zu einer signifikant höheren Bioverfügbarkeit von Levodopa im Plasma als die dreimalige, zusätzliche Applikation von Entacapon. Unter dieser Konstellation verursachte Entacapon im Vergleich mit Placebo keine erhöhte Bioverfügbarkeit von Levodopa im Plasma. Die maximale Hemmung der löslichen COMT war unter allen Opicapon-Dosierungen höher als unter Entacapon [46]. Die COMT-Hemmung war unter Opicapon im Gegensatz zu Entacapon nicht fluktuierend.
Bei einem Placebo-kontrollierten Vergleich der Pharmakokinetik und der Pharmakodynamik von Opicapon in Dosierungen von 5, 25 und 50 mg zeigte sich nach zehntägiger Gabe bei Asiaten aus Japan und Weißen europäischer Abstammung („Kaukasiern“) kein Unterschied [11]. Auch wurde in einer weiteren Untersuchung zur kardialen Sicherheit gezeigt, dass die einmalige Gabe von Opicapon in einer Dosis von 50 mg bzw. 800 mg keine Verlängerung der QT- bzw. QTc-Zeit bewirkt [43].
Opicapon bei Patienten mit Morbus Parkinson (Phase II und Phase III)
Zehn Parkinson-Patienten erhielten doppelblind in vier unterschiedlichen Behandlungsintervallen mit mindestens zehn Tage andauernden, dazwischen liegenden Auswaschphasen einmalig Placebo, 25, 50 oder 100 mg Opicapon. Die Patienten erhielten Opicapon zusammen mit der morgendlichen Levodopa/Carbidopa- oder Levodopa/Benserazid-Gabe unter standardisierten Bedingungen. Es wurden pharmakokinetische (Levodopa-Plasmaspiegel) und pharmakodynamische Analysen (COMT-Hemmung) durchgeführt. Die Bioverfügbarkeit von Levodopa stieg unter Opicapon im Vergleich zu Placebo um 3,7% (25 mg), 16,4% (50 mg), und 34,8% (100 mg) an. Die maximale Hemmung der COMT lag zwischen 67,8% (25 mg) und 100% (100 mg), abhängig von der verabreichten Dosis von Opicapon. Der 3-OMD-Spiegel sank am meisten nach Einnahme von 100 mg Opicapon [47].
Eine weitere Phase-II-Studie galt mit Levodopa/Carbidopa oder Levodopa/Benserazid behandelten Patienten mit Morbus Parkinson, die unter Fluktuationen der Beweglichkeit litten. Sie erhielten einmal täglich 5, 15 oder 30 mg Opicapon zusätzlich zu ihrer Therapie mit 100/25 mg Levodopa/Carbidopa- oder Levodopa/Benserazid-Tabletten. Die Studie war multizentrisch, doppelblind, randomisiert, Placebo-kontrolliert und vierarmig. Die Studienteilnehmer (n=40) wurden der Reihe nach und zufällig für die zusätzliche Einnahme von 5, 15 oder 30 mg Opicapon oder Placebo (jeweils n=10) eingeteilt. Zweimal wurde jeweils ein Stimulationstest mit Levodopa/DDC-Hemmer standardisiert durchgeführt. Der erste war am Morgen nach Studieneinschluss, der zweite am Ende der Behandlungsphase. Im Vergleich zu Placebo nahm die Bioverfügbarkeit von Levodopa um 24,7% (5 mg Opicapon), 53,9% (15 mg) und 65,6% (30 mg) zu. Die maximale Hemmung der löslichen COMT lag zwischen 52% (5 mg) und 80% (30 mg Opicapon). Die Teilnehmer mussten auch ein Tagebuch zur Dokumentation der „Off“- (Intervalle mit schlechter Beweglichkeit)“ und „On“-Phasen (Zeitabschnitte mit guter Beweglichkeit) ausfüllen. Die Motorik verbesserte sich. Die Off-Zeit nahm dosisabhängig um 0,77% (Placebo), 4,16% (5 mg Opicapon), 29,55% (15 mg) und 32,71% (30 mg) ab [14].
In einer randomisierten, doppelblinden, Placebo-kontrollierten (n=120) Studie (BIPARK I) wurde die einmalige tägliche Einnahme von 5 mg (n=119), 25 mg (n=116) oder 50 mg (n=115) Opicapon mit der Einnahme von jeweils 200 mg Entacapon mit jeder oralen Gabe von Levodopa/Carbidopa oder Levodopa/Benserazid (n=104) bei Patienten mit vorhersagbaren Off-Phasen verglichen. Die Studie dauerte bis zu 15 Wochen. Die anhand von Patiententagebüchern erfasste Off-Zeit verringerte sich im Durchschnitt mit Placebo um 56,0 Minuten (SE [Standardfehler des Mittelwerts] 13,4; 95%-Konfidenzintervall [KI] –82,3 bis –29,7), mit Entacapon um 96,3 Minuten (SE 13,4; 95%-KI –122,6 bis –70,0), mit Opicapon 5 mg um 91,3 Minuten (SE 13,5; 95%-KI –117,7 bis –64,8), mit Opicapon 25 mg um 85,9 Minuten (SE 13,7; 95%-KI –112,8 bis –59,1) und mit Opicapon 50 mg um 116,8 Minuten (SE 14,0; 95%-KI –144,2 bis –89,4). Die Behandlung mit Opicapon 50 mg war Placebo überlegen (p=0,0015) und Entacapon nicht unterlegen (p=0,0051). Opicapon 5 mg (p=0,056) oder 25 mg (p=0,080) unterschied sich nicht signifikant von Placebo. Die häufigste Nebenwirkung war das Auftreten von unkontrollierten Überbewegungen. Diese sogenannten Dyskinesien traten bei fünf Patienten unter Placebo (Behandlungsarm A), bei zehn unter Entacapon (B), bei 17 unter 5 mg Opicapon (C), bei neun unter 25 mg Opicapon (D) und bei 18 unter Opicapon 50 mg (E) auf. Schlaflosigkeit (A: 1; B: 7; C: 2; D: 7; E: 7) und Verstopfung (A: 3; B: 5; C: 4; D: 0; E: 7) wurden auch als Nebenwirkungen berichtet [13].
Eine weitere, internationale, multizentrisch durchgeführte, doppelblinde, randomisierte, dreiarmige Studie (BIPARK II) verglich die Wirkung und Sicherheit einer einmal täglichen Gabe von 25 oder 50 mg Opicapon mit Placebo bei mit Levodopa behandelten Parkinson-Patienten, die unter „Wearing-off“ (vorhersagbaren, von der Medikamenteneinnahme abhängigen Off-Phasen) litten. Placebo erhielten 135 Studienteilnehmer. 25 mg Opicapon bekamen 125 Patienten. 50 mg Opicapon wurde 147 Teilnehmern zusätzlich gegeben. Die doppelblinde Studienphase dauerte bis zu 15 Wochen. Primäres Studienziel war die Änderung der Off-Zeiten im Vergleich zum Studienbeginn. Im Durchschnitt war die Verringerung der anhand von Patiententagebüchern erhobenen Off-Zeiten unter Placebo 1,1 Stunden und unter Opicapon 1,7 Stunden (25 mg) bzw. 2,0 Stunden (50 mg). Trotz der ausgeprägten Wirkung von Placebo war der Unterschied zu dem Arm mit Einnahme von 50 mg Opicapon signifikant (p=0,0084). Bei der Gabe von 25 mg Opicapon war dies nicht der Fall [23].
Opicapon wurde generell gut vertragen und war sicher. Die häufigsten klinisch relevanten Nebenwirkungen in den Phase-III-Studien waren Obstipation, Insomnie, Mundtrockenheit, erhöhte Creatinkinase und Benommenheit. In allen Studien trat keine Diarrhö als Nebenwirkung auf. Dies ist ein Gegensatz zu den Studien und der allgemeinen Erfahrung mit Entacapon oder Tolcapon. Unter beiden Substanzen kann Diarrhö plötzlich auftreten [31], die Ursache dafür ist nicht geklärt.
Opicapon wurde im Juni 2016 von der EMA zugelassen (Ongentys®), und zwar als Zusatztherapie zu Levodopa/DDC-Hemmern bei erwachsenen Patienten mit Morbus Parkinson mit motorischen End-of-Dose-Fluktuationen, bei denen mit Levodopa/DDC-Hemmer keine Stabilisierung erreicht werden kann. Die empfohlene Dosis beträgt 50 mg/Tag.
Therapeutische Bedeutung von COMT-Hemmern
COMT-Hemmer reduzieren Schwankungen der Plasmaspiegel von Levodopa
Levodopa wird innerhalb von 60 bis 90 Minuten abgebaut, wenn es oral in der traditionellen Form mit Inhibition der DDC eingenommen wird. Dies führt zu erheblichen Schwankungen des Plasmaspiegels von Levodopa. Als Folge davon wird Levodopa dem Gehirn pulsatil zur Verfügung gestellt. Klinisch resultiert daraus eine im Tagesverlauf schwankende Ausprägung von motorischen und nichtmotorischen Symptomen. Diese werden auch als motorische und nichtmotorische Komplikationen bezeichnet. Durch jejunale Infusion von Levodopa/Carbidopa werden sie deutlich gebessert. Mit dieser Applikationsform wird ein gleichmäßigerer Plasmaspiegel von Levodopa erreicht. Levodopa wird dann dem Gehirn kontinuierlicher zur Verfügung gestellt [12].
Die Kombination von oral gegebenem Levodopa mit Inhibition der DDC und einem nur in der Peripherie wirksamen COMT-Hemmer verringert das Ausmaß der Schwankungen von Levodopa im Plasma im Vergleich zur traditionellen oralen Gabe von Levodopa mit Carbidopa oder Benserazid [26, 31, 37]. Klinisch kommt es dadurch zu einer verminderten Häufigkeit und Ausprägung motorischer Komplikationen; insbesondere Intensität, Dauer und Häufigkeit vorhersagbarer Off-Phasen verringern sich. Man versuchte diesen Ansatz auch präventiv zu untermauern. Diese Studie scheiterte aber an Konzeptionsfehlern und zeigte, dass es im Behandlungsarm mit Entacapon eher und vermehrt zu Dyskinesien kam. Daher wurde das primäre Studienziel verfehlt. Beim Design der Studie wurden pharmakokinetische Grundlagen der Levodopa-Gabe unterschätzt, beispielsweise die vermehrte Anreicherung von Levodopa im Tagesverlauf unter Entacapon im Vergleich zu Placebo, die die Manifestation von Dyskinesien unterstützt [28, 34, 40, 50]. Seitdem werden als Risikofaktoren für Dyskinesien ein niedriges Gewicht, junges Erkrankungsalter und eine tägliche Levodopa-Dosis über 400 mg postuliert [40]. Dies ist recht einfach dadurch zu erklären, dass die Bioverfügbarkeit von Levodopa negativ mit dem Gewicht korreliert [30]. Junge Parkinson-Patienten wiegen meist weniger als ältere. Daher schwanken Plasmaspiegel gerade unter der Konstellation niedriges Gewicht und hohe orale Levodopa-Dosis am stärksten. Als Folge dessen kommt es dann früher zu Dyskinesien. Dies passt auch zu anderen Studienergebnissen [10]. Hier wurden bei zuvor unbehandelten Parkinson-Patienten vermehrt Dyskinesien innerhalb von 42 Wochen in Relation zur Höhe der verabreichten oralen Dosis von Levodopa/Carbidopa beschrieben.
Verzögerte Freisetzung von Levodopa aus einer Tablette: Ein alternativer Ansatz zur COMT-Hemmung?
Ein alternativer Therapieansatz zum Erreichen gleichmäßigerer Konzentrationen von Levodopa im Plasma war die Entwicklung von Tabletten, die Levodopa verzögert im Gastrointestinaltrakt freisetzen. Diese als „retardiert“ bezeichneten Präparate, die die Gabe von Levodopa ebenfalls nur mit einem DDC-Hemmer kombinierten, scheiterten in entsprechenden Studien. Ein Grund hierfür war, dass motorische Komplikationen nicht detailliert genug erfasst wurden [9, 19]. Auch wurde nicht berücksichtigt, dass bei Retardierung die Bioverfügbarkeit und damit die Wirkung der gegebenen, oralen Dosis von Levodopa und DDC-Hemmer geringer ist als die des zum Vergleich eingesetzten nicht retardierten, traditionellen Präparats mit der gleichen Dosis von Levodopa und DDC-Hemmer. Eine Wirkäquivalenz wird nur durch Gabe einer um etwa 25 bis 33% höheren, oralen Levodopa/DDC-Hemmer-Gabe eines retardierten Präparats erreicht [27]. Die Kombination des COMT-Hemmers Entacapon mit einem retardierten Levodopa/Carbidopa-Präparat verbessert klinisch Off-Phasen länger, ohne Dyskinesien hervorzurufen, als normales Levodopa/Carbidopa [42]. Eine galenische Neuentwicklung diesbezüglich ist Rytary® (IPX066), eine Levodopa/Carbidopa-Formulierung, bei der Levodopa ebenfalls kontinuierlicher dem Gehirn zur Verfügung gestellt wird [18]. Rytary® (IPX066) ist in den USA verfügbar, in der EU zugelassen, wird aber vermutlich als Folge der Preisregulation nach dem Wirkstoffprinzip in der EU nicht vertrieben. Die Kombination von IPX066 mit konstanterer COMT-Hemmung durch Opicapon dürfte das Problem der nächtlichen Akinese, die das Umdrehen im Bett erschwert, vor allem in der ersten Nachthälfte verringern können, wenn IPX066 vor dem Schlafengehen eingenommen wird. Studien hierzu gibt es nicht.
Enzymhemmung bei Levodopa-Gabe: Metabolische Effekte
Das therapeutische Prinzip der dualen Enzymhemmung des Levodopa-Abbaus durch die Kombination mit Hemmern der DDC und der COMT wirkt sich auch langfristig metabolisch aus. Durch die COMT-Inhibition wird zumindest das Ausmaß des mit der Levodopa-Gabe assoziierten Homocystein-Anstiegs verringert (Abb. 3). Homocystein ist eine Aminosäure und ein Biomarker für das Methylierungspotenzial des Organismus. Je höher der Homocystein-Spiegel ist, desto niedriger ist das Methylierungspotenzial. Es stellt die Kapazität für die Entgiftung von endogenen und exogenen Giften durch Übertragung von Methylgruppen dar. Ein medikamentös induzierte Verringerung des Methylierungspotenzials kann für die Pathophysiologie und die Geschwindigkeit des Fortschreitens von chronisch neurodegenerativen und arteriosklerotischen Krankheiten mit entscheidend sein und auch für die sekundäre Manifestation von Symptomen wie Depression, Polyneuropathie oder Beeinträchtigung der Kognition einen Risikofaktor darstellen [7, 20, 22, 29, 32].
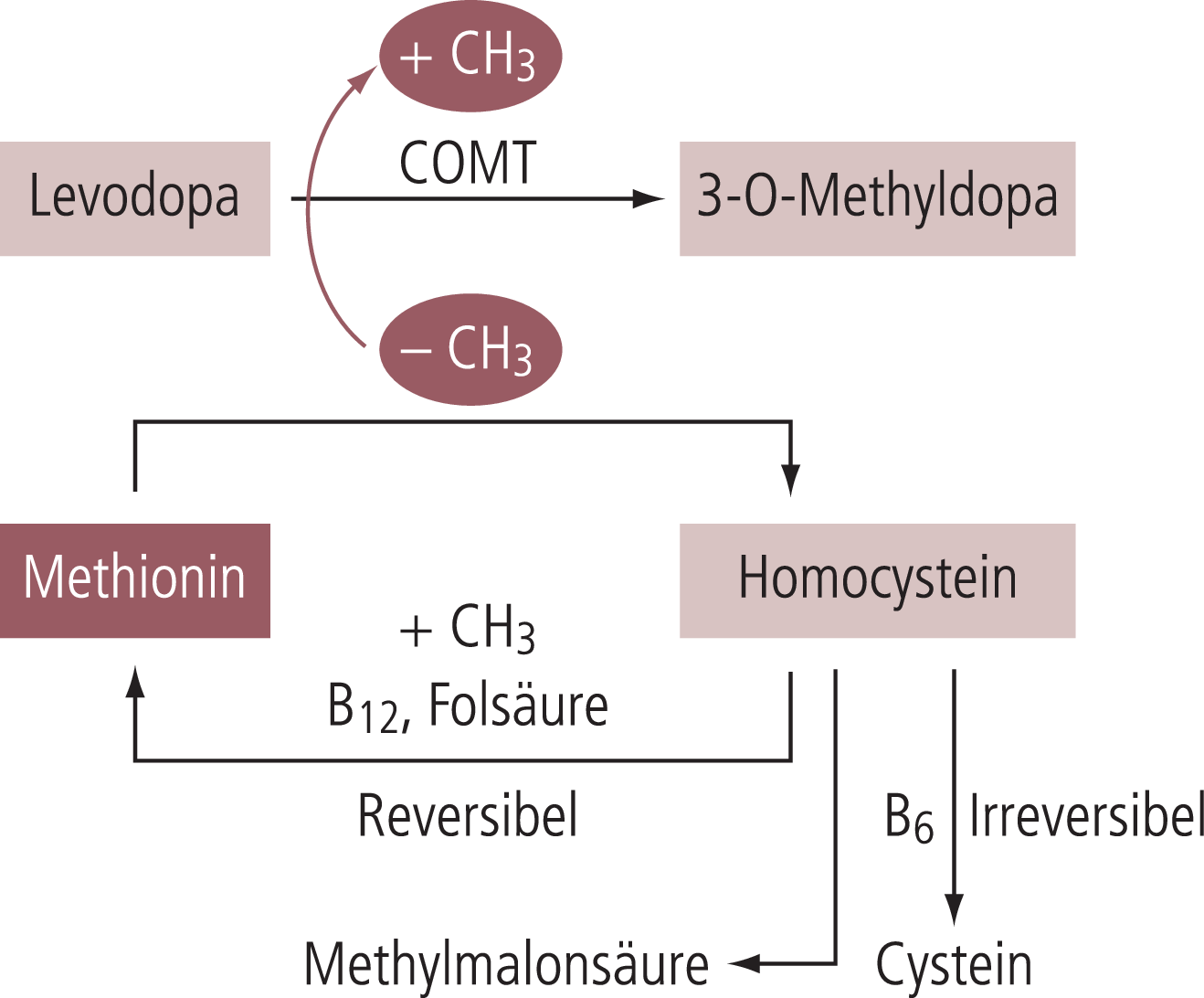
Abb. 3. Vereinfachtes Schaubild der O-Methylierung von Levodopa über die Catechol-O-Methyltransferase und dadurch ausgelöste, metabolische Vorgänge, vor allem bei chronischer Gabe von Levodopa und insbesondere bei alleiniger Hemmung der Dopadecarboxylase. Durch Methylierung von Levodopa über die Catechol-O-Methyltransferase wird Levodopa in 3-O-Methyldopa umgewandelt. Die dazu notwendige Methylgruppe (CH3) wird von Methionin abgegeben, das dabei über die Zwischenstufen S-Adenosylmethionin und S-Adenosylhomocystein in Homocystein umgewandelt wird. Homocystein kann abhängig von Vitamin B12 und Folsäure durch Addition einer Methylgruppe (CH3) reversibel wieder in Methionin umgewandelt werden. Ein Marker für einen funktionellen B12-Mangel ist auch ein Anstieg der Methylmalonsäure. Ein alternativer Abbauweg von Homocystein ist die irreversible Vitamin-B6-abhängige Transformation von Homocystein in Cystein über das Zwischenprodukt Cystathionin.
Praktische Konsequenzen der Einführung von Opicapon
Vor dem Hintergrund der interindividuellen Varianz der gastrointestinalen Resorption und damit Bioverfügbarkeit von Levodopa stellt die jetzige Einführung von Opicapon mit seiner kontinuierlichen COMT-Hemmung eine Innovation dar. Opicapon ist daher nicht mit den bisher eingeführten Wirkstoffen Entacapon und Tolcapon, die die COMT nur fluktuierend hemmen, zu vergleichen. Gerade in der Levodopa-Therapie bei Parkinson-Patienten mit motorischen Fluktuationen in weiter fortgeschrittenen Stadien zeigt sich, dass der nach dem sogenannten „Wirkstoffprinzip“ praktizierte Austausch von Tabletten mit Levodopa und DDC-Hemmer nicht bedenkenlos erfolgen sollte.
Die komplexe Interaktion zwischen Pharmakokinetik, Pharmakodynamik, gastrointestinaler Resorption und Enzymhemmung der Levodopa-Therapie ist bei jedem Patienten einzigartig [36]. Parkinson-Patienten benötigten immer eine individuell angepasste orale Dosierung von Levodopa/DDC-Hemmer. Durch die Teilbarkeit der traditionellen oralen Tabletten mit Levodopa/Carbidopa oder oder Levodopa/Benserazid ist dies leicht möglich. Die Optionen der individuellen Anpassung der erforderlichen Levodopa-Dosis waren durch die fehlende Teilbarkeit von Stalevo®, der Kombination von Levodopa/Carbidopa und dem COMT-Hemmer Entacapon in einer Tablette, auch aus pharmakologischen Gesichtspunkten anfangs begrenzt.
Durch die Einführung unterschiedlich dosierter Stalevo®-Präparate mit 50 bis 200 mg Levodopa wurden dann die therapeutischen Möglichkeiten für die klinische Praxis vereinfacht [35]. Die Problematik der Schwankungen von COMT-Hemmung und Levodopa-Plasmaspiegel blieb aber weiterhin bestehen. Durch Opicapon wird dies jetzt vereinfacht, da die Inhibition der COMT konstanter und länger erfolgt (Abb. 4, Tab. 1). Die hier geschilderten pharmakokinetischen, pharmakodynamischen und metabolischen Vorteile von Opicapon sprechen dafür, orales Levodopa in der traditionellen Form mit Carbidopa oder Benserazid nur noch dann einzusetzen, wenn Patienten es in der Kombination mit dem COMT-Hemmer nicht vertragen. Es bleibt aber abzuwarten, ob das bis heute nicht geklärte Phänomen des Auftretens von Diarrhöen unter Entacapon und Tolcapon nicht auch unter Opicapon zu beobachten sein wird.
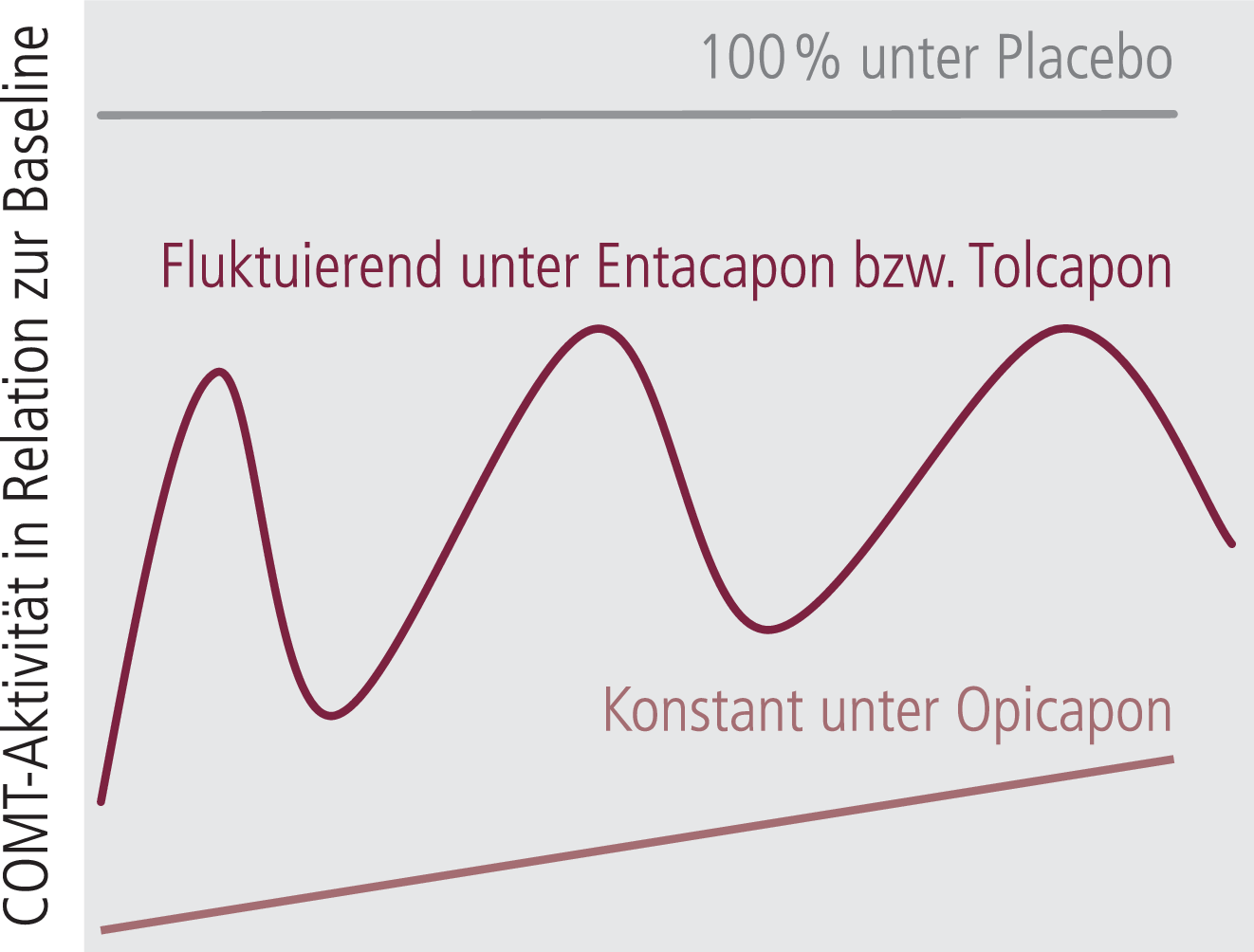
Abb. 4. Schematisierter Verlauf der COMT-Hemmung unter Opicapon, Entacapon, Tolcapon und Placebo
Abschlussbemerkung
Das Prinzip der peripheren COMT-Hemmung wird jetzt mit Gabe einer einzigen Tablette Opicapon pro Tag im Vergleich zur dreimal täglichen Einnahme von Entacapon verbessert und vereinfacht. Vor diesem Hintergrund ist die Kombination von Levodopa/DDC-Hemmer mit Opicapon zukünftig schon bei Beginn der Levodopa-Therapie sinnvoll und nicht erst – wie in der Zulassung beschrieben – bei Auftreten von Wearing-off-Phänomenen bei Patienten in fortgeschrittenen Stadien. Heutzutage müssen Studien in bestimmten Patientengruppen in einer artifiziellen Studienwelt durchgeführt werden, um eine Zulassung zu bekommen. Die Ergebnisse daraus werden überschätzt. Die medikamentöse Therapie von Parkinson-Patienten lässt sich nicht anhand von bürokratischen Kriterien standardisieren [25]. In der realen Welt der Patientenversorgung liegt es immer noch in der Verantwortung des individuell einen Patienten behandelnden Arztes, zu entscheiden, wann der Einsatz eines Medikaments sinnvoll bzw. notwendig ist. Gerade bei der Behandlung des Morbus Parkinson spielen auch langfristige Aspekte eine wesentliche Rolle, zum Beispiel die Vermeidung oder Verringerung von motorischen und nichtmotorischen Komplikationen durch das Prinzip der kontinuierlichen Stimulation [41]. Es ist verwunderlich, dass dies in Zeiten mit hohen Anforderungen an die Durchführung von Studien dann im Rahmen von qualitativ fragwürdigen Untersuchungen verharmlost wird, aber gut publiziert werden kann [17]. Die Nachteile von Levodopa hängen eng mit der aus seinen pharmakokinetischen Eigenschaften resultierenden pulsatilen Stimulation des nigrostriatalen und mesolimbischen, dopaminergen Systems zusammen [41]. Diese Nachteile können jetzt vermutlich besser präventiv aufgefangen werden, und zwar durch die frühzeitige Kombination eines MAO-B-Hemmers wie Rasagilin, Selegilin oder Safinamid, mit der Komponente der zentralen Hemmung des Abbaus von Dopamin in der Glia, und der Komponente der kontinuierlicheren Bioverfügbarkeit von Levodopa im Plasma nach Gabe von Opicapon mit daraus vermehrter Konstanz der COMT-Hemmung [36, 41, 44].
Interessenkonflikterklärung
TM hat Honorare für die Beratung oder Teilnahme an Advisory Boards von Bial und Zambon sowie Vortragshonorare von Zambon erhalten.
Literatur
1. Almeida L, Rocha JF, Falcao A, et al. Pharmacokinetics, pharmacodynamics and tolerability of opicapone, a novel catechol-O-methyltransferase inhibitor, in healthy subjects: prediction of slow enzyme-inhibitor complex dissociation of a short-living and very long-acting inhibitor. Clin Pharmacokinet 2013;52:139–51.
2. Apud JA, Mattay V, Chen J, et al. Tolcapone improves cognition and cortical information processing in normal human subjects. Neuropsychopharmacology 2007;32:1011–20.
3. Benetello P, Furlanut M, Fortunato M, et al. Levodopa and 3-O-methyldopa in cerebrospinal fluid after levodopa-carbidopa association. Pharmacol Res 1997;35:313–5.
4. Birkmayer W, Hornykiewicz O. [The L-3,4-dioxyphenylalanine (DOPA)-effect in Parkinson-akinesia]. Wien Klin Wochenschr 1961;73:787–8.
5. Bonifacio MJ, Sutcliffe JS, Torrao L, et al. Brain and peripheral pharmacokinetics of levodopa in the cynomolgus monkey following administration of opicapone, a third generation nitrocatechol COMT inhibitor. Neuropharmacology 2014;77:334–41.
6. Bonifacio MJ, Torrao L, Loureiro AI, et al. Pharmacological profile of opicapone, a third-generation nitrocatechol catechol-O-methyl transferase inhibitor, in the rat. Br J Pharmacol 2015;172:1739–52.
7. Cacciapuoti F. Hyperhomocysteinemia: a novel risk factor or a powerful marker for cardiovascular diseases? Pathogenetic and therapeutical uncertainties. J Thromb Thrombolysis 2011;32:82–8.
8. Ceravolo R, Piccini P, Bailey DL, et al. 18F-dopa PET evidence that tolcapone acts as a central COMT inhibitor in Parkinson’s disease. Synapse 2002;43:201–7.
9. Dupont E, Andersen A, Boas J, et al. Sustained-release Madopar HBS compared with standard Madopar in the long-term treatment of de novo parkinsonian patients. Acta Neurol Scand 1996;93:14–20.
10. Fahn S, Oakes D, Shoulson I, et al. Levodopa and the progression of Parkinson’s disease. N Engl J Med 2004;351:2498–508.
11. Falcao A, Rocha JF, Santos A, et al. Opicapone pharmacokinetics and pharmacodynamics comparison between healthy Japanese and matched white subjects. Clin Pharmacol Drug Dev 2016;5:150–61.
12. Fernandez HH, Standaert DG, Hauser RA, et al. Levodopa-carbidopa intestinal gel in advanced Parkinson’s disease: final 12-month, open-label results. Mov Disord 2015;30:500–9.
13. Ferreira JJ, Lees A, Rocha JF, et al. Opicapone as an adjunct to levodopa in patients with Parkinson’s disease and end-of-dose motor fluctuations: a randomised, double-blind, controlled trial. Lancet Neurol 2015 Dec 22. pii: S1474–4422(15)00336–1. doi: 10.1016/S1474–4422(15)00336–1. [Epub ahead of print].
14. Ferreira JJ, Rocha JF, Falcao A, et al. Effect of opicapone on levodopa pharmacokinetics, catechol-O-methyltransferase activity and motor fluctuations in patients with Parkinson’s disease. Eur J Neurol 2015;22:815–25, e56.
15. Forsberg M, Lehtonen M, Heikkinen M, et al. Pharmacokinetics and pharmacodynamics of entacapone and tolcapone after acute and repeated administration: a comparative study in the rat. J Pharmacol Exp Ther 2003;304:498–506.
16. Forsberg MM, Huotari M, Savolainen J, et al. The role of physicochemical properties of entacapone and tolcapone on their efficacy during local intrastriatal administration. Eur J Pharm Sci 2005;24:503–11.
17. Gray R, Ives N, Rick C, et al. Long-term effectiveness of dopamine agonists and monoamine oxidase B inhibitors compared with levodopa as initial treatment for Parkinson’s disease (PD MED): a large, open-label, pragmatic randomised trial. Lancet 2014;384: 1196–205.
18. Hauser RA, Hsu A, Kell S, et al. Extended-release carbidopa-levodopa (IPX066) compared with immediate-release carbidopa-levodopa in patients with Parkinson’s disease and motor fluctuations: a phase 3 randomised, double-blind trial. Lancet Neurol 2013;12:346–56.
19. Hutton JT, Morris JL, Bush DF, et al. Multicenter controlled study of Sinemet CR vs Sinemet (25/100) in advanced Parkinson’s disease. Neurology 1989;39:67–72.
20. Jugel C, Ehlen F, Taskin B, et al. Neuropathy in Parkinson’s disease patients with intestinal levodopa infusion versus oral drugs. PLoS One 2013;8:e66639.
21. Kaakkola S, Gordin A, Mannisto PT. General properties and clinical possibilities of new selective inhibitors of catechol O-methyltransferase. Gen Pharmacol 1994;25:813–24.
22. Klostermann F, Jugel C, Müller T, et al. Malnutritional neuropathy under intestinal levodopa infusion. J Neural Transm 2012;119:369–72.
23. Lees AJ, Ferreira JJ, Costa R, et al. Efficacy and safety of opicapone, a new COMT-inhibitor, for the treatment of motor fluctuations in Parkinson’s disease patients: BIPARK-II study. J Neurol Sci 2013;333:e109–51.
24. Mannisto PT. Catechol O-methyltransferase: characterization of the protein, its gene, and the preclinical pharmacology of COMT inhibitors. Adv Pharmacol 1998;42:324–8.
25. Moller JC, Korner Y, Dodel RC, et al. Pharmacotherapy of Parkinson’s disease in Germany. J Neurol 2005;252:926–35.
26. Muhlack S, Herrmann L, Salmen S, et al. Fewer fluctuations, higher maximum concentration and better motor response of levodopa with catechol-O-methyltransferase inhibition. J Neural Transm (Vienna) 2014;121:1357–66.
27. Müller T, Ander L, Kolf K, et al. Comparison of 200 mg retarded release levodopa/carbidopa – with 150 mg levodopa/carbidopa/entacapone application: pharmacokinetics and efficacy in patients with Parkinson’s disease. J Neural Transm 2007;114:1457–62.
28. Müller T, Erdmann C, Muhlack S, et al. Pharmacokinetic behaviour of levodopa and 3-O-methyldopa after repeat administration of levodopa/carbidopa with and without entacapone in patients with Parkinson’s disease. J Neural Transm (Vienna) 2006;113:1441–8.
29. Müller T, Jugel C, Ehret R, et al. Elevation of total homocysteine levels in patients with Parkinson’s disease treated with duodenal levodopa/carbidopa gel. J Neural Transm 2011;118:1329–33.
30. Müller T, Woitalla D, Saft C, et al. Levodopa in plasma correlates with body weight of parkinsonian patients. Parkinsonism Relat Disord 2000;6:171–3.
31. Müller T. Catechol-O-methyltransferase inhibitors in Parkinson’s disease. Drugs 2015;75:157–74.
32. Müller T. Detoxification and antioxidative therapy for levodopa-induced neurodegeneration in Parkinson’s disease. Expert Rev Neurother 2013;13:707–18.
33. Müller T. Dopaminergic substitution in Parkinson’s disease. Expert Opin Pharmacother 2002;3:1393–403.
34. Müller T. Entacapone. Expert Opin Drug Metab Toxicol 2010;6:983–93.
35. Müller T. Levodopa/carbidopa and entacapone in the treatment of Parkinson’s disease: efficacy, safety and patient preference. Patient Prefer Adherence 2009;3:51–9.
36. Müller T. Motor complications, levodopa metabolism and progression of Parkinson’s disease. Expert Opin Drug Metab Toxicol 2011;7:847–55.
37. Müller T. Pharmacokinetic considerations for the use of levodopa in the treatment of Parkinson disease: focus on levodopa/carbidopa/entacapone for treatment of levodopa-associated motor complications. Clin Neuropharmacol 2013;36:84–91.
38. Müller T. Tolcapone addition improves Parkinson’s disease associated nonmotor symptoms. Ther Adv Neurol Disord 2014;7:77–82.
39. Nutt JG, Woodward WR, Gancher ST, et al. 3-O-methyldopa and the response to levodopa in Parkinson’s disease. Ann Neurol 1987;21:584–8.
40. Olanow CW, Kieburtz K, Rascol O, et al. Factors predictive of the development of levodopa-induced dyskinesia and wearing-off in Parkinson’s disease. Mov Disord 2013;28:1064–71.
41. Olanow CW, Obeso JA. Pulsatile stimulation of dopamine receptors and levodopa-induced motor complications in Parkinson’s disease: implications for the early use of COMT inhibitors. Neurology 2000;55:S72–7.
42. Piccini P, Brooks DJ, Korpela K, et al. The catechol-O-methyltransferase (COMT) inhibitor entacapone enhances the pharmacokinetic and clinical response to Sinemet CR in Parkinson’s disease. J Neurol Neurosurg Psychiatry 2000;68:589–94.
43. Pinto R, l’Hostis P, Patat A, et al. Evaluation of opicapone on cardiac repolarization in a thorough QT/QTc study. Clin Pharmacol Drug Dev 2015;4:454–62.
44. Przuntek H, Conrad B, Dichgans J, et al. SELEDO: a 5-year long-term trial on the effect of selegiline in early Parkinsonian patients treated with levodopa. Eur J Neurol 1999;6:141–50.
45. Rocha JF, Almeida L, Falcao A, et al. Opicapone: a short lived and very long acting novel catechol-O-methyltransferase inhibitor following multiple dose administration in healthy subjects. Br J Clin Pharmacol 2013; 76:763–75.
46. Rocha JF, Falcao A, Santos A, et al. Effect of opicapone and entacapone upon levodopa pharmacokinetics during three daily levodopa administrations. Eur J Clin Pharmacol 2014;70:1059–71.
47. Rocha JF, Ferreira JJ, Falcao A, et al. Effect of 3 single-dose regimens of opicapone on levodopa pharmacokinetics, catechol-O-methyltransferase activity and motor response in patients with Parkinson disease. Clin Pharmacol Drug Dev 2016;5:232–40.
48. Russ H, Müller T, Woitalla D, et al. Detection of tolcapone in the cerebrospinal fluid of parkinsonian subjects. Naunyn Schmiedebergs Arch Pharmacol 1999;360:719–20.
49. Sawle GV, Burn DJ, Morrish PK, et al. The effect of entacapone (OR-611) on brain [18F]-6-L-fluorodopa metabolism: implications for levodopa therapy of Parkinson’s disease. Neurology 1994;44:1292–7.
50. Stocchi F, Rascol O, Kieburtz K, et al. Initiating levodopa/carbidopa therapy with and without entacapone in early Parkinson disease: the STRIDE-PD study. Ann Neurol 2010;68:18–27.
Prof. Dr. med. Thomas Müller, Klinik für Neurologie, St. Joseph Krankenhaus Berlin-Weissensee, Gartenstraße 1, 13088 Berlin, E-Mail: th.mueller@alexianer.de; thomas.mueller@ruhr-uni-bochum.de
Opicapone
Levodopa is well tolerated and the most efficacious drug for the treatment of idiopathic Parkinson’s disease. Levodopa is the metabolic precursor of dopamine. Levodopa but not dopamine may trespass the blood brain barrier. Levodopa is quickly metabolised in the periphery. As a result, considerable fluctuations of levodopa plasma levels occur following oral application and levodopa is delivered to the brain in a pulsatile fashion. Inhibition of the enzymes dopadecarboxylase with carbidopa or benserazide and catechol-O-methyltransferase with entacapone or tolcapone is a well known therapeutic principle, which provides more continuous levels in plasma and consecutively in the brain. This review on the new catechol-O-methyltransferase inhibitor opicapone summarizes the essential pharmacologic features and the results from studies in animals, healthy volunteers and patients with Parkinson’s disease, particularly. Opicapone is administered only once daily one hour before food intake, since opicapone provides a constant inhibition of catechol-O-methyltransferase. This is in contrast to entacapone and tolcapone, both of which provide a more fluctuating inhibition of catechol-O-methyltransferase during repeated daily intake. Therefore opicapone improves levodopa therapy due to pharmacokinetic and pharmacodynamic aspects.
Key words: Opicapone, tolcapone, entacapone, continuous dopaminerg stimulation, levodopa, catechol-O-methyltransferase, diarrhea
Psychopharmakotherapie 2016; 23(05)
