Dr. Matthias Herrmann, Berlin
Vor zehn Jahren erhielt Natalizumab (Tysabri®) die Zulassung zur krankheitsmodifizierenden Monotherapie von erwachsenen Patienten mit hochaktiver, schubförmig remittierend verlaufender MS [4]. Bei 942 randomisierten Patienten hatte der gegen Alpha-4-Integrin gerichtete Antikörper die jährliche Schubrate in der Phase-III-Studie AFFIRM über zwei Jahre signifikant um 68% reduziert [7]. Die Zahl sowie die Gesamtlast der mittels Magnetresonanztomographie (MRT) darstellbaren Läsionen im ZNS gingen ebenfalls stark zurück. Der Anteil der Patienten mit bestätigter Behinderungsprogression wurde durch Natalizumab auf 17% gegenüber 29% unter Placebo reduziert. Bei mehr als jedem dritten der Patienten mit hoch aktiver MS kam es dabei sogar zu einer anhaltenden Verbesserung des körperlichen Behinderungsgrads. Damit zeigte das alle vier Wochen als Infusion verabreichte Medikament eine höhere Wirksamkeit als die zur Basistherapie eingesetzten Interferon-beta-Präparate und Glatirameracetat, die die Schubrate um etwa ein Drittel reduzieren.
Natalizumab ist zudem der erste Wirkstoff in der MS-Therapie, unter dem ein relevanter Anteil der Patienten das später formulierte Therapieziel „Freiheit von Krankheitsaktivität“ (no evidence of disease activity, kurz: NEDA [1]) erfüllt. Dieses ist definiert als Schubfreiheit bei gleichzeitig fehlender MRT-Aktivität und ausbleibender Behinderungsprogression und wurde in der AFFIRM-Studie bei 37% der Patienten erreicht (Abb. 1) [5]. In der multinationalen, offenen Beobachtungsstudie TOP zur Wirksamkeit von Natalizumab in der Routineversorgung kam es während der 96-wöchigen Behandlung bei jedem dritten nicht vorbehandelten Patienten mit zuvor hoher Krankheitsaktivität zu einem Rückgang des Behinderungsgrads um mindestens eine Stufe auf der Expanded Disability Status Scale (EDSS) [3]. Von den Patienten, die von Interferon beta/Glatirameracetat oder Fingolimod auf Natalizumab umgestellt worden waren, verbesserten sich 22,1% beziehungsweise 21,4%.
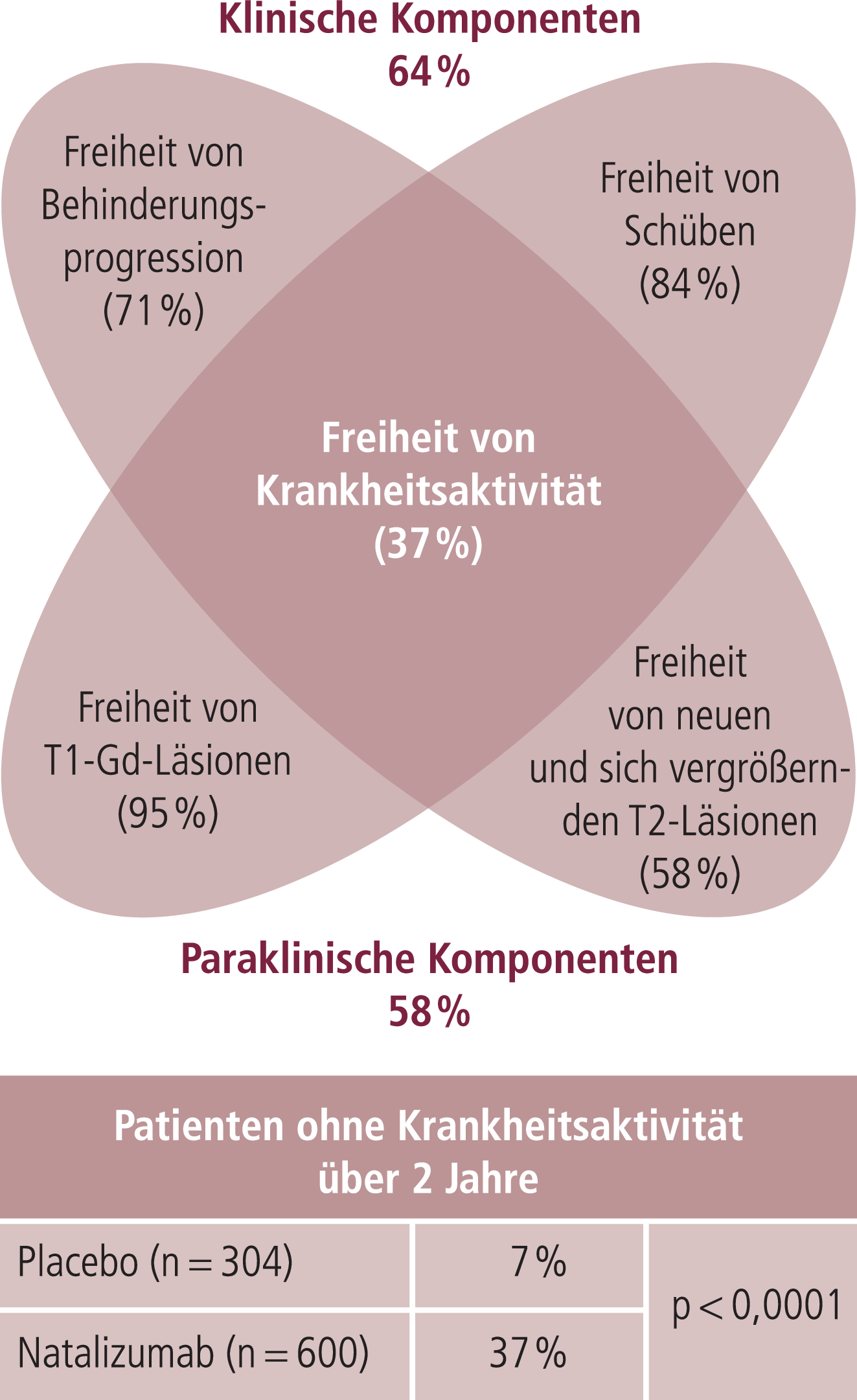
Abb. 1. Freiheit von Krankheitsaktivität unter Natalizumab [mod. nach Havrdova et al. 2009]
Sicherheitsprofil inzwischen gut bekannt
Die grundlegenden Prinzipien der MS-Therapie bestehen heute darin, frühzeitig mit der Behandlung zu beginnen, Patienten bei unzureichender Wirksamkeit rechtzeitig umzustellen und die bestmögliche Krankheitskontrolle zu erreichen. Dass Letzteres mit Natalizumab auch langfristig möglich ist, belegen Daten über einen Zeitraum von bis zu sieben Jahren [8]. Am Ende erfüllte noch jeder dritte Patient alle drei NEDA-Kriterien.
Doch nicht alle Patienten sind für eine Langzeittherapie geeignet. So weist Natalizumab bei weltweit etwa 140000 behandelten Patienten mit mehr als 400000 Patientenjahren ein allgemein gutes Sicherheitsprofil auf [2]. Bei Patienten mit Antikörpern gegen das JC-Virus kann Natalizumab infolge einer Reaktivierung des Virus jedoch als seltene Nebenwirkung eine potenziell lebensbedrohliche progressive multifokale Leukenzephalopathie (PML) verursachen. Neben einem Schub muss sie immer als Ursache in Betracht gezogen werden, wenn ein Patient plötzlich neurologische Symptome entwickelt, nachdem er unter Natalizumab über mehrere Jahre hinweg stabil war. Nach einem Update der Empfehlungen der Europäischen Arzneimittelbehörde (EMA) zum PML-Risikomanagement vom Februar 2016 ist die individuelle Nutzen-Risiko-Abwägung anhand des JC-Virus-Antikörper-Status und der bisherigen Behandlungsdauer aber noch differenzierter möglich [6]. Bei einer Behandlungsdauer von mehr als zwei Jahren sollte das Risiko alle sechs Monate neu berechnet werden, um Patienten mit hohem Risiko nach entsprechender Aufklärung eventuell auf eine andere Therapie umstellen zu können.
Quelle
Prof. Dr.med. Hans-Peter Hartung, Düsseldorf, Prof. Dr.med. Volker Limmroth, Köln; Pressekonferenz „10 Jahre Tysabri® bei RRMS: Patienten erkennen, Freiheit erreichen“, veranstaltet von Biogen GmbH, Frankfurt, 12. Mai 2016.
Literatur
1. Bevan CJ, Cree BA. Disease activity free status: a new end point for a new era in multiple sclerosis clinical research? JAMA Neurol 2014;71:269–70.
2. Biogen, Data on File.
3. Butzkueven H, et al. 67. Jahrestagung der American Academy of Neurology (AAN), Washington, DC, USA, 18.–25. April 2015, Poster P2.069.
4. Fachinformation Tysabri® (Stand: November 2015).
5. Havrdova E, et al. Effect of natalizumab on clinical and radiological disease activity in multiple sclerosis: a retrospective analysis of the Natalizumab Safety and Efficacy in Relapsing-Remitting Multiple Sclerosis (AFFIRM) study. Lancet Neurol 2009;8:254–60.
6. www.ema.europa.eu/ema/index.jsp? curl=pages/news_and_events/news/2016/02/ news_detail_002471.jsp&mid=WC0b01ac05 8004d5c1 (Zugriff am 09.06.2016).
7. Polman CH, et al. A randomized, placebo-controlled trial of natalizumab for relapsing multiple sclerosis. N Engl J Med 2006; 354:899–910.
8. Prosperini L, Fanelli F, Pozzilli C. Long-term assessment of no evidence of disease activity with natalizumab in relapsing multiple sclerosis. J Neurol Sci 2016;364:145–7.
Psychopharmakotherapie 2016; 23(04)
