Mitja Bodatsch, Oberhausen, und Jens Kuhn, Köln und Oberhausen
Der Tatsache zum Trotz, dass sich die Prognose der Schizophrenie dank moderner, multimodaler Behandlungsansätze seit ihrer syndromalen Erstbeschreibung über die letzten 100 Jahre signifikant verbessert hat, bleibt die Schizophrenie eine oftmals chronisch/rezidivierend verlaufende und nachhaltig schwergradig beeinträchtigende Erkrankung [40]. Dies liegt nicht zuletzt darin begründet, dass die klinische Erstmanifestation, die meist erstmals in den kritischen Entwicklungsphasen des jungen Erwachsenenalters in Erscheinung tritt, den Lebensweg unterbricht und die funktionale Bewältigung der lebenszeittypischen Aufgaben verstellt. Aber auch im Vorfeld, in der sogenannten Prodromalphase beziehungsweise in den nicht zwangsläufig in das Vollbild einer Schizophrenie mündenden „attenuiert“-psychotischen und kognitiv-perzeptiven Risikosyndromen, kann die Erkrankung bereits nachhaltig das Funktionsniveau und die Lebensqualität beeinträchtigen [34].
Paradigmatisch für die Schizophrenie ist sicherlich der Verlauf nach einer ersten Episode, wenn nicht nur das Risiko für weitere Episoden dramatisch erhöht ist, sondern wenn insbesondere dauerhafte, oftmals therapieresistente Störungen der Kognition und der seelischen Vitalfunktionen in Erscheinung treten [40].
In allen Erkrankungsphasen stellt die medikamentöse Therapie eine zentrale Säule der Schizophrenie-Behandlung dar [10, 40]. Zu dieser Zentralstellung der medikamentösen Therapie tragen nicht zuletzt verschiedene wissenschaftliche und klinische Aspekte bei: Aus wissenschaftlicher Sicht bietet die Psychopharmakotherapie den unmittelbarsten und pathophysiologisch am besten nachvollziehbaren Zugriff auf die bei der Schizophrenie nachweislich beeinträchtigte Neurotransmission [19, 21], wobei hierdurch eine reine symptomatische und keine kausale Behandlung verwirklicht wird [20]. Aus klinischer Sicht erlaubt die medikamentöse Therapie die rascheste und zuverlässigste Kontrolle der in der Akutphase oftmals auch mit Gefährdung einhergehenden Störung der Realitätsbeurteilung und eine gegenüber Placebo signifikante Senkung der Wahrscheinlichkeit und der Häufigkeit erneuter akutpsychotischer Episoden [10, 40, 46]. Dank dieser zentralen Stellung hängen an der medikamentösen Therapie oftmals auch die Hoffnungen von Patienten und deren Angehörigen, die von der Medikation eine stabile Basis für den ungestörten weiteren Lebensvollzug erwarten.
Gerade weil einerseits die Schizophrenie aber eine heterogen und nur schwer vorhersehbar verlaufende Erkrankung mit allzeitig drohender Chronifizierung darstellt und weil andererseits die medikamentöse Therapie trotz der an sie geknüpften Erwartungen von Ärzten, Patienten und Angehörigen nicht risikofrei und aufgrund von Nebenwirkungen oftmals selbst beeinträchtigend ist, gilt es, die Indikation einer Psychopharmakotherapie nicht nur initial, sondern auch und gerade im Verlauf der Erkrankung wiederholt zu prüfen. Insbesondere muss hierbei die Indikation zur mit besonderen Herausforderungen besetzten medikamentösen Dauerbehandlung kritisch und Krankheitsstadien-gerecht gestellt werden.
In der vorliegenden Arbeit sollen ein kurzer, praktikabler Überblick über die jeweiligen therapeutischen Anforderungen der unterschiedlichen Krankheitsphasen der Schizophrenie gegeben und die Möglichkeiten bzw. Notwendigkeiten der (Langzeit-)Therapie diskutiert werden. Streng davon zu trennen und hier aus Platzgründen nicht besprochen sind Fälle von Therapierefraktarität, die ein eigenes, oftmals hochspezialisiertes therapeutisches Regime erfordern [37]. Die vorliegende Arbeit adressiert vielmehr die im klinischen Alltag häufig anzutreffenden Fälle, in denen eine dauerhafte Remission ungewiss erscheint, ohne dass medikamentöse Refraktarität im engeren Sinne vorliegt. Gerade diese Fälle stellen in psychiatrischen Kliniken und Praxen, auch wenn sie vermeintlich deren „Alltagsgeschäft“ bilden, eine besondere Herausforderung dar, da eine medikamentöse Behandlung über die Leitlinienempfehlung hinaus zwar oft notwendig erscheint, hierfür pauschalierende Ansätze der Lebenssituation der Patienten aber oft unangemessen sind und eher individuelle Lösungen im therapeutischen Bündnis erarbeitet werden müssen. Die vorliegende Arbeit konzentriert sich, wiederum aus Gründen der Übersichtlichkeit, auf die Erhaltungstherapie einer positivsymptomatischen Remission und die damit interagierenden klinischen und sozialen Faktoren.
Klinik, Verlauf und Neurochemie der Schizophrenie
Die Schizophrenie ist eine Erkrankung des jungen Erwachsenenalters mit leichter Präferenz des männlichen Geschlechts [39]. Der klinischen Erstmanifestation geht nicht selten eine bis zu fünf Jahre dauernde Prodromalphase voraus, die initial durch subtile, aber alltags- und lebensqualitätsrelevante Störungen des Denkens und der Wahrnehmung, später durch abgeschwächte charakteristische Störungen der Realitätsbeurteilung und der seelischen Vitalfunktionen gekennzeichnet ist [22]. Die klinische Erstmanifestation gibt dann mit schwerer Beeinträchtigung von Wahrnehmung, Denken, Kognition, Affekt und Psychomotorik das paradigmatische Bild der akuten psychotischen Episode. Symptomatisch kennzeichnend sind hier insbesondere die handlungsrelevanten Positivsymptome mit paranoidem Wahn, akustischen Halluzinationen und Meinhaftigkeitsstörungen (Ich-Störungen). Im Nachgang der ersten Episode kommt es nicht selten zu schweren depressiven Verstimmungen, die dann oftmals mit Suizidgedanken assoziiert sind. In den ersten Jahren nach der Erstmanifestation stellen das Risiko einer erneuten akutpsychotischen Episode, das für die frühe Phase bei bis zu 77% liegt, und Beeinträchtigungen durch die bei einigen Patienten persistierenden kognitiven Störungen und Negativsymptome (Abb. 1) die größten Herausforderungen dar [28, 46]. Im Langzeitverlauf, also insbesondere bei Auftreten mehrerer Episoden und/oder bleibenden kognitiven und Negativsymptomen gilt es, einerseits eine positivsymptomatische Kontrolle zu gewährleisten und andererseits die Lebensqualität zu erhalten [28, 41, 46].
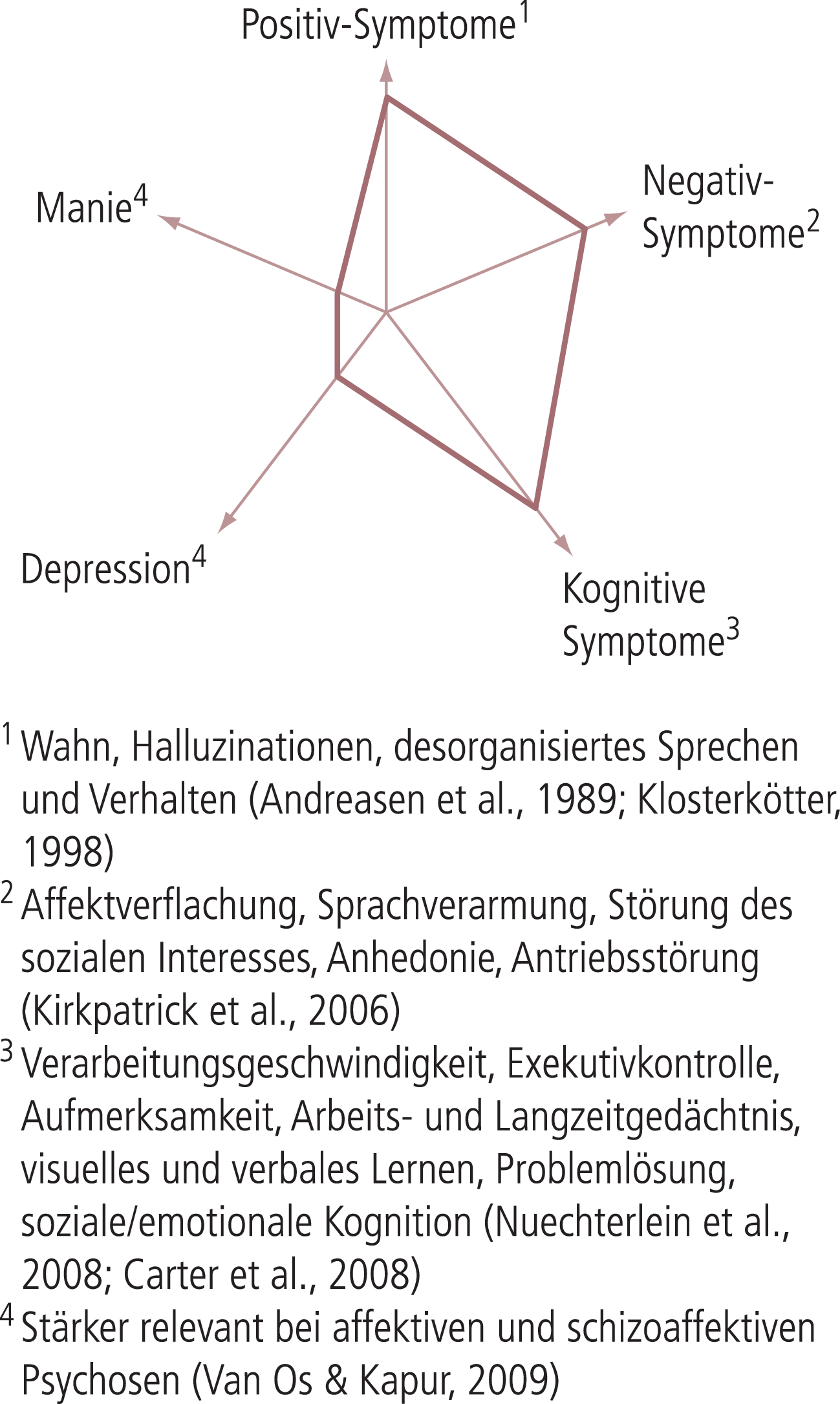
Abb. 1. Symptomdimensionen der Schizophrenie [mod. nach 43]
Pathophysiologisch wird angenommen, dass die dopaminerge Neurotransmission einen zentralen Anteil an der Entstehung von Positiv-, aber auch von Negativsymptomen hat [19, 21]. Diese bedeutsame Hypothese von Carlsson und Lindquist wird durch die Tatsache unterstützt, dass eine experimentelle Stimulation des dopaminergen Systems, beispielsweise durch Amphetamine, bei Gesunden produktivpsychotische Symptome provozieren kann [5]. Ein weiterer Beleg für die Dopamin-Hypothese kommt aus der Schizophrenie-Behandlung: Die zentrale Wirkung von Antipsychotika scheint auf einer Blockade von Dopamin-D2-Rezeptoren zu beruhen [5]. So scheint ein hyperdopaminerger Stoffwechsel in subkortikalen Hirnarealen zwar die Entstehung produktivpsychotischer Symptome hinlänglich zu erklären. In präfrontalen Kortexregionen scheint hingegen ein Mangel an Dopamin vorzuherrschen, der insbesondere für Negativsymptome und kognitive Störungen verantwortlich zeichnet [9]. Dies wird einerseits durch bildgebende Studien, andererseits aber durch die Tatsache unterstützt, dass insbesondere klassische Antipsychotika, die eine ausgeprägte Blockade von D2-Rezeptoren bewirken, kognitive und Negativsymptome sogar verstärken können. Neben dieser möglichen, ungewünschten Symptomakzentuierung hängen auch bedeutsame Nebenwirkungen wie Bewegungs- und hormonelle Störungen von einer „ungewollten“ Dopaminrezeptor-Blockade im nigrostriatalen und tuberoinfundibulären System ab [25]. Dennoch stellt nach wie vor der dopaminerge Stoffwechsel des Gehirns den hauptsächlichen Angriffspunkt von Antipsychotika dar [25]. Hierbei scheint eine weniger intensive Bindung an den D2-Rezeptor (loose binding) bzw. ein partieller D2-Agonismus zwar ein gegenüber den klassischen Antipsychotika günstigeres Nebenwirkungsprofil der atypischen Antipsychotika zu begründen, jedoch konnte eine positive Wirkung auf die anderen Symptomspektren der Schizophrenie nur bei ausgewählten Atypika erreicht werden [24].
Einen möglicherweise vielversprechenden alternativen therapeutischen Zielpunkt stellt der Glutamat-Stoffwechsel dar. Nicht zuletzt aus der Erkenntnis, dass durch eine experimentelle Modifikation des Glutamat-Stoffwechsels durch den NMDA-Antagonisten Ketamin ebenfalls produktivpsychotische Symptome hervorgerufen werden können, konnte geschlossen werden, dass die dopaminerge Störung vielleicht eher als die gemeinsame Endstrecke von Dysfunktionen in unterschiedlichen neuronalen Transmissionswegen zu verstehen ist [5]. Hierfür sprechen nicht nur die phänomenologische Ähnlichkeit der Ketamin-Psychosen mit akuten schizophrenen Episoden hinsichtlich Positiv- und Negativsymptomatik, sondern insbesondere auch, dass Ketamin Störungen des Arbeitsgedächtnisses und der Wortflüssigkeit hervorzurufen vermag, wie sie bei der Schizophrenie typischerweise beobachtet werden können [5]. Medikamente mit glutamatergem Angriffspunkt sind jedoch zur Schizophrenie-Behandlung (noch) nicht etabliert und diesbezüglich aufkeimende Hoffnung hat unlängst durch einen Abbruch bzw. unzureichenden Wirksamkeitsnachweis in den Zulassungsstudien von Bitopertin zweifellos einen starken Dämpfer erfahren [30].
Zielsymptome und therapeutische Herausforderungen der Schizophrenie-Behandlung
Das Symptomprofil der Schizophrenie wandelt sich im Laufe der Erkrankung [40]. Damit wandelt sich auch das Anforderungsprofil, das eine medikamentöse Behandlung zu erfüllen hat. In jeder Erkrankungsphase gilt es nicht zuletzt, die Nebenwirkungen und Risiken einer medikamentösen Behandlung, die nach neueren Erkenntnissen auch mit der Dauer der Behandlung variieren, dem zu erwartenden Nutzen und den Erfordernissen der Erkrankungsphase kritisch gegenüberzustellen (Kurzübersicht in Tab. 1).
Tab. 1. Krankheitsstadien-gerechte Entscheidungsgrundlagen für den Einsatz verschiedener Antipsychotika-Formulierungen
|
Erkrankungsphase |
Entscheidungsgrundlage |
|
|
Orale Antipsychotika |
Depot-Antipsychotika |
|
|
Risikosyndrom |
|
– |
|
Erstmanifestation und frühe Erkrankungsphase |
|
|
|
Erstes Rezidiv |
|
(Wie bei Erstmanifestation, zusätzlich:)
|
|
Zweites Rezidiv |
|
(Wie in der mittleren Erkrankungsphase, zusätzlich:)
|
Risikosyndrom und Prodromalphase
Die Idee einer möglichst früh einsetzenden Behandlung verknüpft sich mit der Hoffnung, die symptomatische Vollmanifestation und den im Anschluss daran oftmals negativen Krankheitsverlauf zu verhindern [34]. Kritisch infrage gestellt wird dieser Ansatz jedoch durch die Tatsache, dass nur eine Minderheit der Patienten, die frühe (kognitiv-perzeptive) oder späte (attenuierte bzw. vorübergehende psychotische Symptome) Risikokriterien erfüllen, überhaupt in absehbarer Zeit das Vollbild einer Schizophrenie entwickelt [13]. Auf ein „Prodrom“ im engeren Sinne kann also nur retrospektiv, nach bereits stattgehabter Erstmanifestation sicher geschlossen werden. Darin begründen sich die Bedenken, eine vermeintlich „falsch-positiv“ identifizierte Person mit Risikosymptomen medikamentös zu behandeln [27]. Dessen ungeachtet bedeutet das Risikosyndrom an sich bereits eine schwere Beeinträchtigung mit subjektivem Leiden und Herabsetzung des sozialen und schulischen/beruflichen Leistungsniveaus, woraus sich eine syndromale Behandlungsindikation ableiten lässt [34]. Für die antipsychotische medikamentöse Therapie kommen dabei vor allem die späten, durch attenuierte oder vorübergehend voll ausgeprägte Positivsymptome geprägten Hochrisikostadien in Betracht. In Studien zeigten sich niedrige Dosen atypischer Antipsychotika auch zur Verhinderung der Vollmanifestation nicht unwirksam [35, 42]. Interessant ist in diesem Zusammenhang die erfolgreiche Anwendung von Omega-3-Fettsäuren in einer kleinen Pilotstudie [2]. Sollten diese Ergebnisse sich in einer derzeitig durchgeführten multizentrischen Studie bestätigen, könnte sich hier eine Alternative zur Anwendung von etablierten Antipsychotika insbesondere in der späten Prodromalphase ergeben. In der klinischen Erstbehandlung und insbesondere in der Praxis stellen Antipsychotika jedoch weiterhin eine praktikable und zielgerichtete Behandlungsmöglichkeit dar. Schwierigkeiten ergeben sich durch die fehlende Zulassung in diesem Erkrankungsstadium, die oftmals geringe Akzeptanz der Patienten, ein Medikament „gegen Schizophrenie“ einzunehmen, und die hochgradige Unsicherheit hinsichtlich der Dauer der Behandlung. Hinsichtlich der Behandlungsdauer gilt es zu beachten, dass eine Kurzzeittherapie zwar wahrscheinlich nicht ausreicht, um eine Vollmanifestation suffizient zu verhindern, dass diese Entwicklung bezogen auf zwei Jahre aber ohnehin nur auf etwa 20% der Risikopersonen zutrifft [13]. Damit ist jedoch eine Dauertherapie, die oftmals durch Depotpräparate am besten gewährleistet wird, nur schwer zu rechtfertigen. Die kurzzeitige Anwendung niedrig dosierter Antipsychotika kann in Abhängigkeit von Symptomschwere, Leidensdruck und der lebensqualitativen Beeinträchtigung erwogen werden.
Erstmanifestation
Bei Auftreten einer akutpsychotischen Episode ist der möglichst frühzeitige Einsatz von Antipsychotika gerechtfertigt [10]. Hierdurch soll nicht nur eine möglichst rasche Remission der mit erheblichem Leiden und oftmals auch Gefährdung (Suizidalität, Aggressivität) verbundenen Positivsymptome erreicht werden, sondern es konnte auch gezeigt werden, dass eine früh einsetzende antipsychotische Behandlung die Prognose nach Erstmanifestation hinsichtlich Lebensqualität und Funktionsniveau signifikant verbessert [33]. Leitliniengerecht sollte die Initialtherapie mit einem atypischen Antipsychotikum in niedrigst möglicher Dosierung in Monotherapie erfolgen [10]. Für die Dauer der Behandlung ist mindestens ein Jahr vorgesehen, was sich aus der hohen Wahrscheinlichkeit einer erneuten Episode in dieser Zeit ableitet, ohne dass jedoch eine wirkliche Evidenz für die Beendigung der Behandlung nach diesem Zeitfenster besteht [23]. Unter der Vorstellung einer „Reifungsstörung“ und mit dem Wissen, dass die derzeitig verfügbaren Medikamente nicht kausal in dieses Modell zur Pathogenese eingreifen, kann sogar eine pauschal dauerhafte Behandlungsnotwendigkeit diskutiert werden [20]. Kritisch ist in dieser Erkrankungsphase insbesondere die Herstellung eines therapeutischen Bündnisses. Nicht nur muss der Patient trotz bestehender Störung der Realitätsbeurteilung dem Arzt soweit vertrauen, dass er die verordnete Medikation einnimmt. Es gilt insbesondere, einem jungen Menschen plausibel zu machen, dass er an einer schweren psychischen Erkrankung leidet, die zumindest für einige Zeit und vielleicht auf Dauer die Einnahme eines Medikaments erfordert. Das kann es für den Patienten auch erforderlich machen, einige Nebenwirkungen zugunsten einer stabilen Remission in Kauf zu nehmen, wobei dieser Aspekt besondere Berücksichtigung im Prozess der partizipativen Entscheidungsfindung (shared decision making) finden sollte. Für die Auswahl und die Applikationsform des Medikaments sind oftmals die individuellen Charakteristika der psychotischen Episode und das individuell antizipierbare Nebenwirkungsprofil maßgebend. So bedeutet die Gabe einer oralen Medikation insbesondere bei verhaltensgestörten und aggressiven Patienten, aber auch bei Auftreten schwerer Nebenwirkungen eine besondere Herausforderung. Eine forcierte Gabe oraler Medikation und/oder die Anwendung beispielsweise intramuskulärer Gaben kann jedoch sehr aversiv erlebt oder wahnhaft verarbeitet werden, was die Behandlungsbereitschaft langfristig nachhaltig beeinträchtigen kann. Auch bei Erstmanifestation kann eine Depot-Formulierung bereits eine sinnvolle Alternative darstellen, insbesondere wenn bereits schwerwiegende Desorganisation (durch Positivsymptome, kognitive Störungen und Negativsymptome) auftritt, die den Patienten eine zuverlässige Einnahme der Medikation unmöglich macht.
Frühe Erkrankungsphase
Nach der Erstmanifestation liegt der Fokus der Behandlung einerseits auf der Verhinderung weiterer Episoden. Hierzu wird in den meisten Leitlinien eine Therapiedauer von zumindest einem Jahr mit einem Antipsychotikum empfohlen (siehe auch „Erstmanifestation“ sowie [22]). Andererseits liegt der Fokus insbesondere auf den in der frühen Erkrankungsphase progressiven kognitiven Störungen und auf persistierenden Negativsymptomen, die regelhaft die Bewältigung lebenszeittypischer Anforderungen in sozialer und beruflicher Hinsicht behindern und reaktiv depressive, nicht selten sogar zum Suizid führende Entwicklungen bedingen können [15]. Die Rolle der Antipsychotika liegt entsprechend ihrer Hauptwirkung in dieser Erkrankungsphase auf der Verhinderung weiterer Episoden. Gleichzeitig gilt es hier umso mehr, eine Medikation auszuwählen, die nicht durch immanente Nebenwirkungen die Lebensqualität bzw. das psychosoziale Funktionsniveau der Patienten vermindert. Diesbezüglich weist eine vielbeachtete Studie der letzten Jahre darauf hin, dass eine ideal austarierte Medikation mit ausreichend hoher Dosis bezüglich eines Rezidivschutzes und gleichzeitig möglichst niedriger Dosis wahrscheinlich die beste Strategie darstellt [45 ]. Aus dieser Perspektive sollte individualitätsbezogen auch nach der ersten Episode die Indikation zur Depot- und zur längerfristigen Behandlung kritisch evaluiert werden. Dies gilt zudem insbesondere bei sehr schweren, mit hoher Gefährdung und langfristig bleibenden, positivsymptomatischen Restsymptomen einhergehenden Fällen oder bei Auftreten von Frühwarnzeichen bei Reduktionsversuchen einer oralen Medikation. Und es erfährt weitere Unterstützung durch die Tatsache, dass in einer jüngst veröffentlichen Studie die Verabreichung von Aripiprazol-Depot zu einer signifikanten Verbesserung der Lebensqualität und des psychosozialen Funktionsniveaus insbesondere bei jüngeren Patienten beitragen konnte [26]. Alltagsorientiert kann gerade auch in dieser Phase Desorganisation (kognitive Störungen, Negativsymptome) eine orale Medikationseinnahme erschweren und daher eine Depot-Gabe empfehlenswert erscheinen lassen. Bei günstigeren Verläufen stellt es zumeist eine besondere Herausforderung für den Arzt dar, selbst bei fehlenden oder subjektiv tolerablen Nebenwirkungen die Medikationseinnahme lebensqualitativ angemessen in den Alltag der zumeist jungen Erwachsenen zu integrieren. So kann bei Menschen, die viel auf Reisen sind, hohe Funktionsanforderungen im Alltag zu bewältigen haben und/oder die tägliche Tabletteneinnahme aus sozialen oder persönlichen Gründen nicht wünschen, auch die Gabe einer Depot-Formulierung im ersten Behandlungsjahr eine entlastende Alternative darstellen. Gleichzeitig gilt es insbesondere in der frühen Erkrankungsphase, eventuellen, aber nicht konstant in allen Untersuchungen gezeigten Langzeitfolgen der Antipsychotika-Gabe für das Hirnvolumen kritisch zu begegnen.
Späte Erkrankungsphase
In den späteren Erkrankungsphasen steht weiterhin die Verhinderung erneuter Episoden zur Minimierung von Gefährdung und nun insbesondere die Vermeidung von Krankenhausaufenthalten und der Autonomieerhalt im Vordergrund [6]. Gleichzeitig gilt es oftmals, eine suffiziente Kontrolle persistierender Positivsymptome sowie schwerer kognitiver und behavioraler Desorganisation zu gewährleisten. Insbesondere bei häufigen Episoden, hoher Gefährdung in der akuten Psychose, persistierenden Positivsymptomen und stabiler medikamentöser Response desorganisierter Symptome erscheint eine Dauerbehandlung unumgänglich. Gerade im Langzeitverlauf muss jedoch die medikamentöse Therapie auf eine Maximierung der Lebensqualität gerichtet sein und damit oftmals hinter die reine Symptomkontrolle zurücktreten. In dieser Erkrankungsphase kommen, vor allem, wenn ein klinischer Nutzen eines Absetzens der Medikation nicht ersichtlich ist, und zur Entlastung des Patientenalltags, Depot-Formulierungen zur Dauerbehandlung in Betracht, zumal in den Leitlinien dann auch eine Langzeitbehandlung über mindestens drei bis fünf Jahre empfohlen wird.
Differenzialindikation medikamentöser Therapiestrategien
Anhand der synoptischen Betrachtung möglicher schizophrener Krankheitsverläufe lässt sich ersehen, dass zumindest ab der Erstmanifestation eine medikamentöse Behandlung unumgänglich erscheint, um die gravierenden Probleme, die mit der Positivsymptomatik assoziiert sind, zu minimieren und zukünftig durch Verhinderung erneuter Episoden und/oder Symptomkontrolle zu erreichen [10, 46]. Aus den Empfehlungen der Fachgesellschaft wird ersichtlich, dass nach Erstmanifestation grundsätzlich eine längerfristige medikamentöse Behandlung zu erwägen ist [10]. Dabei steht der behandelnde Klinikarzt vor der Herausforderung, zusätzlich zur symptomatischen Remission auch die ambulante Behandlung durch die Auswahl eines geeigneten Präparats und durch die Wahl einer geeigneten Applikationsform zu bahnen. Der niedergelassene Psychiater, der Patienten nach einer ersten oder wiederholten Episode nach einem Klinikaufenthalt weiter zu betreuen hat, steht insbesondere vor der Herausforderung, die bestehende Medikation dem vor allem in den ersten Erkrankungsjahren wechselhaften und heterogenen Krankheitsverlauf anzupassen und in den sich dynamisch weiterentwickelnden Lebensweg zumeist junger Patienten unter Berücksichtigung lebensqualitativer Aspekte zu integrieren. Der Niedergelassene noch mehr als der Klinikarzt sieht sich dabei mit der Anforderung konfrontiert, entlang prognostischer Überlegungen zum weiteren Krankheitsverlauf die Medikation in Dosierung und Applikationsform anzupassen. Nach aktueller Literatur erscheint es vor allem unter dem Primat des „non nocere“ geboten, die Dauer der antipsychotisch-medikamentösen Therapie iterativ, Krankheitsstadien-gerecht zu prüfen, um nicht einem Patienten unnötig Nebenwirkungen und Risiken der Behandlung zuzumuten. Bereits anlässlich der Namensgebung „Schizophrenie“ hat Eugen Bleuler festgestellt, dass die Erkrankung in jedem Stadium zurückgehen, zum Stillstand kommen oder fortschreiten kann [4]; diese Aspekte sind der Taktgeber für Intensität und Dauer der medikamentösen Therapie.
Risiken und Nebenwirkungen der Kurz- und Langzeittherapie
Die Nebenwirkungen antipsychotischer Medikamente lassen sich anhand ihrer Adhärenzrelevanz in Gruppen gliedern. Zwar sind – erstens – motorische Nebenwirkungen wie Dyskinesien, Akathisie und Parkinsonoid unter Atypika (zumindest teilweise) weniger relevant als unter klassischen Antipsychotika, jedoch werden insbesondere die letzten beiden auch unter modernen Medikamenten wie Paliperidon, Aripiprazol, Risperidon und Amisulprid nicht selten beobachtet und verursachen erhebliches, die Therapieadhärenz gefährdendes Leiden [8, 11, 36]. Ebenso wirken sich – zweitens – hormonelle und metabolische Störungen, die mit Potenzverlust, Amenorrhö und Gewichtszunahme (Risperidon, Amisulprid, Olanzapin) einhergehen können, aus [8, 11, 36]. Nicht zuletzt werden – drittens – Sedierung und Konzentrationsminderung unter Olanzapin, Clozapin und Quetiapin als lebensqualitativ mindernd erfahren [8, 11, 36].
Bei Erstgabe bestehen besondere und klinisch zu überwachende Risiken insbesondere in der Auslösung eines malignen neuroleptischen Syndroms, in EKG-Veränderungen (QTc-Verlängerung) sowie unter allen Antipsychotika einem erhöhten kardiovaskulären Risiko [12, 18, 38]. In der Langzeittherapie wurde in der letzten Zeit aber auch aufgrund kontroverser Studienergebnisse diskutiert, ob Antipsychotika möglicherweise mit einem signifikanten Verlust von Gehirnsubstanz assoziiert sind [1, 14].
Die Nebenwirkungen und Risiken sind dabei gegenüber dem gerade unter laufender Therapie oft nur schwer zuverlässig zu beurteilenden Erkrankungsverlauf aufzurechnen: So kann es beispielsweise bei einzelnen chronisch Erkrankten sinnvoll sein, die Medikation bei unverändertem Krankheitsverlauf zur Nebenwirkungs- und Risikominimierung zu reduzieren oder sogar abzusetzen, während nach Ersterkrankung auch die Einhaltung einer vermeintlich suffizienten Therapiedauer bei symptomatischer Remission keine ausreichende Gewähr für eine stabile Remission nach Absetzen der Medikation bietet.
Zusammengenommen zeigt sich aber, dass bei einer nennenswerten Anzahl von Patienten eine längerfristige medikamentöse Behandlung notwendig ist. Und selbst im Falle eines günstigen Verlaufs gilt es leitliniengerecht, Ersterkrankte für zumindest ein Jahr nach der akutpsychotischen Episode medikamentös weiter zu behandeln. Unter diesen Bedingungen gewinnt nicht zuletzt die Wahl der Applikationsform eine besondere Bedeutung (s. Kapitel „Indikation und Auswahl eines Depot-Therapeutikums“).
Lebensqualität unter medikamen-töser Therapie
Grundsätzlich ist davon auszugehen, dass die Lebensqualität ohne Erfordernis einer regelmäßigen Medikamenteneinnahme insbesondere in der Zeit des jungen Erwachsenenalters höher ist als im Falle der Notwendigkeit einer medikamentösen Therapie, und sei es auch „nur“ für ein Jahr. Ist aber eine solche medikamentöse Therapie erforderlich, zeigt sich, dass die subjektive Lebensqualität auch, aber nicht ausschließlich von den erlebten Nebenwirkungen abhängig ist [17, 32]. Motorische Einschränkungen und Gewichtszunahme wirken dabei auch nach außen hin stigmatisierend und schränken die Freiheitsgrade der körperlichen Aktivität ein. Sexuelle Dysfunktionen sind meist stark schambesetzt, wirken sich negativ auf das Selbstgefühl aus und interferieren kritisch mit bestehenden oder sich anbahnenden Partnerschaften. Sedierung und Konzentrationsstörungen behindern den freien Lebensvollzug sowohl hinsichtlich der Freizeitgestaltung als auch hinsichtlich der beruflichen Entwicklung. Wenn aber eine medikamentöse Therapie mit zumindest tolerablen Nebenwirkungen etabliert werden konnte, so scheint die Wahl des Applikationswegs für Akzeptanz und Adhärenz der Patienten wenig Gewicht zu haben bzw. sich sogar günstig auszuwirken [3, 7, 8, 44]. Bei Gabe eines Depots in zwei- bis vierwöchigem Abstand liegen die Vorteile hinsichtlich Konstanthaltung der Medikamentenspiegel und der Gewährleistung von Compliance aus klinischer Sicht geradezu auf der Hand. Die Risiken durch die intramuskuläre Gabe selbst (Infektion, Verletzung) erscheinen dabei bei Einhaltung der geltenden Hygienevorschriften und fachgerechter Applikation zwar gering, sind aber unbedingt zu beachten und in die Aufklärung entsprechend einzuschließen. Aus Patientensicht kann die Gabe eines Depots durch Entlastung des Alltags und/oder seltenere Praxiskontakte einen Zugewinn an Lebensqualität schaffen. Zumindest scheinen Depot-Antipsychotika in der Verhinderung von erneuten Episoden niedrigere Numbers needed to treat (NNT) zu erreichen, als sie mit einer oralen Einnahme zu erreichen sind [29, 31]. Auch konnte bisher keine geringere Lebensqualität in Abhängigkeit vom Applikationsweg gezeigt werden [3, 7, 8, 44].
Indikation und Auswahl eines Depot-Therapeutikums
Ist es gelungen, ein gut vertragenes Antipsychotikum in der Behandlung zu etablieren, sollte dieses Präparat leitliniengerecht in der niedrigsten wirksamen Dosierung nach Ersterkrankung für zumindest ein Jahr und nach einer weiteren Episode für zumindest drei bis fünf Jahre fortgeführt werden [10]. Falls eine Depotformulierung des gegebenen Präparats zur Verfügung steht (Aripiprazol, Olanzapin, Risperidon, Paliperidon), so ist in Anbetracht der vorgenannten zeitlichen Empfehlungen der Fachgesellschaft grundsätzlich auch nach Erstmanifestation die intramuskuläre Gabe eine sinnvolle Option [3, 8, 7, 44]. Die Tatsache, dass Depotformulierungen in Deutschland außer in speziellen Kontexten seltener zur Anwendung kommen, scheint dabei weniger auf eine gesicherte Datenbasis oder eine seltenere Verordnung der verfügbaren Medikamente zurückzuführen, als vielmehr der skeptischen Einstellung der Behandler geschuldet zu sein [3, 7, 8, 44]. Hingegen kann es auch und gerade unter klinischen Gesichtspunkten bereits nach einer ersten akutpsychotischen Episode sinnvoll sein, einer Depotformulierung den Vorzug zu geben. Dies erscheint insbesondere rational, wenn die akute Episode mit hoher Gefährdung und/oder ausgeprägt geringer Behandlungseinsicht assoziiert war, sodass die Verhinderung einer erneuten Episode umso mehr geboten erscheint. Auch können früh auftretende kognitive und Negativsymptome sowie Desorganisation, die die Befähigung zur eigenständigen Alltagsbewältigung und zum autonomen Medikationsmanagement kritisch herabsetzen, die Gabe eines Depots sinnvoll erscheinen lassen. Doch auch bei gutem Funktionsniveau und hoher Adhärenz kann die Gabe eines Depots sich lebensqualitativ günstig auswirken, insofern beispielsweise auf Reisen keine Medikamente mitzuführen sind und/oder bei hohen Funktionsanforderungen der Alltag entlastet werden kann. Zumindest nach einer zweiten Episode sollte die Option einer Depot-Gabe zwingend (und nicht nur unter wiederholter Prüfung der vorgenannten Aspekte) erneut evaluiert werden [10]. Nicht nur, dass das Risiko einer weiteren Episode weiter erhöht ist, es können durch eine Depot-Gabe ursachenunabhängig (Incompliance, symptomatische Ursachen) auch Schwankungen der Plasmaspiegel als Bedingung weiterer Episoden zuverlässiger kontrolliert werden. Gerade die eventuell kritisch mit der Alltagsbewältigung interferierenden Störungen von Kognition und seelischen Vitalfunktionen sind nach wiederholten Episoden häufiger und oftmals schwerer ausgeprägt [16]. Die eventuelle Wahl eines Depot-Präparats sollte sich dabei neben grundsätzlichen Erwägungen zur Verträglichkeit und zum Nebenwirkungs- bzw. Risikoprofil auch an weiteren Symptomen und der Lebenssituation des Patienten orientieren. So kann es sinnvoll sein, bei ausgeprägten Störungen auf anderen Symptomdomänen (kognitive Störungen, Negativsymptome, affektive Störungen) und bei dynamischen Lebenssituationen ein Präparat zu wählen, das vergleichsweise kürzere Injektionsintervalle und/oder die Anpassung der Injektionsfrequenz ermöglicht. Hinsichtlich der kurzfristigen Anpassung der Medikation stellt sich jedoch die orale Gabe als klar überlegen dar.
Zusammenfassung
Die Schizophrenie ist eine Erkrankung mit heterogenem und insbesondere in den ersten Erkrankungsjahren nur schwer vorhersehbarem Verlauf. Allzeitig besteht aber ein hohes Risiko für eine Krankheitsprogression und insbesondere erneute akutpsychotische Episoden. In der Verhinderung weiterer akuter Psychosen liegt eine der Hauptaufgaben der medikamentösen Therapie. Dem trägt die Behandlungsleitlinie mit ihren Empfehlungen einer Behandlungsdauer von zumindest einem Jahr nach Erstmanifestation und zumindest drei bis fünf Jahren nach einer zweiten Episode Rechnung. Daraus ergibt sich grundsätzlich die Notwendigkeit einer zumindest für diese Zeiträume, also pauschal mittel- bis längerfristig angelegten medikamentösen Therapie. Dem sind insbesondere Nebenwirkungen und Risiken der Antipsychotika-Therapie aufzurechnen. Zudem muss aus klinisch-praktischer Sicht, aber auch der interferierenden Rolle weiterer Symptomdomänen hinsichtlich Autonomie und Alltagsbewältigung der Patienten sowie der lebensqualitativen Bedeutung einer regelmäßigen Medikamenteneinnahme Rechnung getragen werden. Damit steht der behandelnde Arzt grundsätzlich nicht nur vor der Herausforderung, eine gut verträgliche Medikation auszuwählen und eventuell individuellen Ansprüchen anzupassen, sondern muss auch der Anforderung gerecht werden, die Medikation der Krankheitsstadien-gerechten Symptomenwicklung anzugleichen und in den alltäglichen Lebensvollzug des Patienten angemessen zu integrieren. Hierbei kommt nicht zuletzt den Depotformulierungen, die für Aripiprazol, Olanzapin, Risperidon und Paliperidon zur Verfügung stehen, auch nach einer ersten psychotischen Episode ein besonderer, und in professionellen Kreisen scheinbar unterschätzter Stellenwert zu; zumindest sprechen die verfügbaren Daten nicht für eine lebensqualitative oder klinische Unterlegenheit von Depot-Antipsychotika. Wohl aber gehen die verschiedenen Depot-Antipsychotika mit einem unterschiedlichen Nebenwirkungsspektrum und differenten Veränderungen der Lebensqualität einher, die bei der individuellen Auswahl berücksichtigt werden sollten [26]. In Anbetracht der pauschal empfohlenen Behandlungsdauer von zumindest einem Jahr nach Erstmanifestation und in Abhängigkeit von Individualcharakteristika hinsichtlich symptomatischer und lebenssituativer Anforderungen kann auch und gerade im frühen Erkrankungsverlauf die Gabe eines Depots eine sinnvolle Alternative darstellen. Zumindest aber nach einer zweiten Episode scheint die Evaluation einer Depotverordnung zwingend. Demgegenüber bleibt es in der klinischen Einzelfallverantwortung des Arztes, Krankheitsstadien-gerechte Therapieanforderungen (Tab. 1) gegen die Risiken der Dauertherapie hinsichtlich Mortalität und Morbidität aufzurechnen. Eine Dauerbehandlung gilt es immer dann zu erwägen, wenn die Häufigkeit akutpsychotischer Episoden, hohes Gefährdungspotenzial der akuten Psychose und/oder eine unzureichende Kontrolle desorganisierter Symptome im medikationsfreien Intervall einen Benefit des Absetzens der Antipsychotika unwahrscheinlich erscheinen lassen und die zu erwartenden Nachteile eines Absetzens die Risiken der Dauerbehandlung aufwiegen.
Interessenkonflikterklärung
MB: Vortragshonorare von Lundbeck und Otsuka.
JK: Vortragshonorare von Lundbeck, Otsuka und Schwabe; Honorare für Beratertätigkeit von Lilly, Lundbeck, Otsuka und Schwabe, Studienunterstützung von DFG, BMBF, EKFS, Medtronic AG.
Literatur
1. Aderhold V, Weinmann S, Hägele C, et al. [Can long-term treatment with antipsychotic drugs lead to structural brain damage? Pro]. Nervenarzt 2013;84:1117–9.
2. Amminger GP, Schäfer MR, Papageorgiou K, Klier CM, et al. Long-chain omega-3 fatty acids for indicated prevention of psychotic disorders: a randomized, placebo-controlled trial. Arch Gen Psychiatry 2010;67:146–54.
3. Bera RB. Patient outcomes within schizophrenia treatment: a look at the role of long-acting injectable antipsychotics. J Clin Psychiatry 2014;75(Suppl 2):30–3.
4. Bleuler E. Dementia praecox oder Gruppe der Schizophrenien. Wien: Franz Deuticke Verlag, 1911.
5. Bodatsch M, Klosterkötter J, Daumann J. Contributions of experimental psychiatry to research on the psychosis prodrome. Front Psychiatry 2013;4:170.
6. Buckley LA, Maayan N, Soares-Weiser K, Adams CE. Supportive therapy for schizophrenia. Cochrane Database Syst Rev 2015;4:CD004716.
7. Chue P, Emsley R. Long-acting formulations of atypical antipsychotics: time to reconsider when to introduce depot antipsychotics. CNS Drugs 2007;21:441–8.
8. Correll CU. Recognition of patients who would benefit from LAI antipsychotic treatment: how to assess adherence. J Clin Psychiatry 2014;75:e29.
9. Davis KL, Kahn RS, Ko G, Davidson M. Dopamine in schizophrenia: a review and reconceptualization. Am J Psychiatry 1991;148:1474–86.
10. Deutsche Gesellschaft für Psychiatrie, Psychotherapie und Nervenheilkunde DGPPN (Hrsg.). S3-Praxisleitlinien in Psychiatrie und Psychotherapie. Band 1 – Behandlungsleitlinie Schizophrenie. Darmstadt: Steinkopff-Verlag, 2005.
11. El-Mallakh P, Findlay J. Strategies to improve medication adherence in patients with schizophrenia: the role of support services. Neuropsychiatr Dis Treat 2015;11:1077–90.
12. Frommeyer G, Eckardt L. Drug-induced proarrhythmia: risk factors and electrophysiological mechanisms. Nat Rev Cardiol 2015;doi: 10.1038/nrcardio.2015.110. [Epub ahead of print].
13. Fusar-Poli P, Bonoldi I, Yung AR, Borgwardt S, et al. Predicting psychosis: meta-analysis of transition outcomes in individuals at high clinical risk. Arch Gen Psychiatry 2012;69:220–9.
14. Fusar-Poli P, Smieskova R, Kempton MJ, Ho BC, et al. Progressive brain changes in schizophrenia related to antipsychotic treatment? A meta-analysis of longitudinal MRI studies. Neurosci Biobehav Rev 2013;37:1680–91.
15. Goodby E, MacLeod AK. Future-directed thinking in first-episode psychosis. Br J Clin Psychol 2015;doi: 10.1111/bjc.12096. [Epub ahead of print].
16. Harvey PD. What is the evidence for changes in cognition and functioning over the lifespan in patients with schizophrenia? J Clin Psychiatry 2014;75(Suppl 2):34–8.
17. Hayhurst KP, Massie JA, Dunn G, Lewis SW, et al. Validity of subjective versus objective quality of life assessment in people with schizophrenia. BMC Psychiatry 2014;14:365.
18. Henderson DC, Vincenzi B, Andrea NV, Ulloa M, et al. Pathophysiological mechanisms of increased cardiometabolic risk in people with schizophrenia and other severe mental illnesses. Lancet Psychiatry 2015;2:452–64.
19. Howes OD, Fusar-Poli P, Bloomfield M, Selvaraj S, et al. From the prodrome to chronic schizophrenia: the neurobiology underlying psychotic symptoms and cognitive impairments. Curr Pharm Des 2012;18:459–65.
20. Insel TR. Rethinking schizophrenia. Nature 2010;468:187–93.
21. Keshavan MS, Tandon R, Boutros NN, Nasrallah HA. Schizophrenia, „just the facts“: what we know in 2008 Part 3: neurobiology. Schizophr Res 2008;106:89–107.
22. Klosterkötter J, Schultze-Lutter F, Bechdolf A, Ruhrmann S. Prediction and prevention of schizophrenia: what has been achieved and where to go next? World Psychiatry 2011;10:165–74.
23. Kohl S, Kuhn J, Wiedemann K. Rationale und Zielsetzung der medikamentösen Therapie der Schizophrenie. Psychopharmakotherapie 2014;21:85–95.
24. Leucht S, Cipriani A, Spineli L, Mavridis D, et al. Comparative efficacy and tolerability of 15 antipsychotic drugs in schizophrenia: a multiple-treatments meta-analysis. Lancet 2013;382:951–62.
25. Miyamoto S1, Miyake N, Jarskog LF, Fleischhacker WW, et al. Pharmacological treatment of schizophrenia: a critical review of the pharmacology and clinical effects of current and future therapeutic agents. Mol Psychiatry 2012;17:1206–27.
26. Naber D, Hansen K, Forray C, Baker RA, et al. Qualify: a randomized head-to-head study of aripiprazole once-monthly and paliperidone palmitate in the treatment of schizophrenia. Schizophr Res 2015;168:498–504.
27. Nelson B, Yung AR. Should a risk syndrome for first episode psychosis be included in the DSM-5? Curr Opin Psychiatry 2011;24:128–33.
28. Norman RM, Manchanda R, Harricharan R, Northcott S. The course of negative symptoms over the first five years of treatment: Data from an early intervention program for psychosis. Schizophr Res 2015;doi: 10.1016/j.schres.2015.09.010. [Epub ahead of print].
29. Nussbaum AM, Stroup TS. Paliperidone palmitate for schizophrenia. Cochrane Database Syst Rev 2012;6:CD008296.
30. Okusaga OO1. 6R-l-erythro-5,6,7,8-tetrahydrobiopterin (BH4): a potential treatment for all symptom domains of schizophrenia. Med Hypotheses 2014;82:395–7.
31. Olivares JM, Rodriguez-Martinez A, Burón JA, Alonso-Escolano D, et al. Cost-effectiveness analysis of switching antipsychotic medication to long-acting injectable risperidone in patients with schizophrenia : a 12- and 24-month follow-up from the e-STAR database in Spain. Appl Health Econ Health Policy 2008;6:41–53.
32. Palmer BW, Martin AS, Depp CA, Glorioso DK, et al. Wellness within illness: happiness in schizophrenia. Schizophr Res 2014;159:151–6.
33. Penttilä M, Jääskeläinen E, Hirvonen N, Isohanni M, et al. Duration of untreated psychosis as predictor of long-term outcome in schizophrenia: systematic review and meta-analysis. Br J Psychiatry 2014;205:88–94.
34. Ruhrmann S, Schultze-Lutter F, Klosterkötter J. Probably at-risk, but certainly ill – advocating the introduction of a psychosis spectrum disorder in DSM-V. Schizophr Res 2010;120:23–37.
35. Ruhrmann S, Klosterkötter J, Bodatsch M, Bechdolf A, et al. Pharmacological prevention and treatment in clinical at-risk states for psychosis. Curr Pharm Des 2012;18:550–7.
36. Sendt KV, Tracy DK, Bhattacharyya S. A systematic review of factors influencing adherence to antipsychotic medication in schizophrenia-spectrum disorders. Psychiatry Res 2015;225:14–30.
37. Sinclair D, Adams CE. Treatment resistant schizophrenia: a comprehensive survey of randomised controlled trials. BMC Psychiatry 2014;14:253.
38. Strawn JR, Keck PE Jr., Caroff SN. Neuroleptic malignant syndrome. Am J Psychiatry 2007;164:870–6.
39. Tandon R, Keshavan MS, Nasrallah HA. Schizophrenia, „just the facts“ what we know in 2008. 2. Epidemiology and etiology. Schizophr Res 2008;102:1–18.
40. Tandon R, Nasrallah HA, Keshavan MS. Schizophrenia, „just the facts“ 4. Clinical features and conceptualization. Schizophr Res 2009;110:1–23.
41. Tandon R, Nasrallah HA, Keshavan MS. Schizophrenia, „just the facts“ 5. Treatment and prevention. Past, present, and future. Schizophr Res 2010;122:1–23.
42. van der Gaag M, Smit F, Bechdolf A, French P, et al. Preventing a first episode of psychosis: meta-analysis of randomized controlled prevention trials of 12 month and longer-term follow-ups. Schizophr Res 2013;149:56–62.
43. van Os J, Kapur S. Schizophrenia. Lancet. 2009 Aug 22;374(9690):635–45.
44. Waddell L, Taylor M. Attitudes of patients and mental health staff to antipsychotic long-acting injections: systematic review. Br J Psychiatry Suppl 2009;52:S43–50.
45. Wunderink L, Nieboer RM, Wiersma D, Sytema S, et al. Recovery in remitted first-episode psychosis at 7 years of follow-up of an early dose reduction/discontinuation or maintenance treatment strategy: long-term follow-up of a 2-year randomized clinical trial. JAMA Psychiatry 2013;70:913–20.
46. Zipursky RB, Menezes NM, Streiner DL. Risk of symptom recurrence with medication discontinuation in first-episode psychosis: a systematic review. Schizophr Res 2014;152:408–14.
Dr. med. Mitja Bodatsch, Klinik für Psychiatrie, Psychotherapie und Psychosomatik, Johanniter Krankenhaus Oberhausen, Evangelisches Klinikum Niederrhein gGmbH, Steinbrinkstraße 96a, 46145 Oberhausen
Prof. Dr. med. Jens Kuhn, Klinik für Psychiatrie, Psychotherapie und Psychosomatik, Johanniter Krankenhaus Oberhausen, Steinbrinkstraße 96, 46145 Oberhausen und Leiter Arbeitsgruppe „Neurobiologie und Neuromodulation psychischer Störungen“, Klinik für Psychiatrie und Psychotherapie, Uniklinik Köln, Kerpener Straße 62, 50937 Köln, E-Mail: jens.kuhn@uk-koeln.de
Adapted pharmacotherapy in the maintenance treatment of schizophrenia
The psychopharmacological therapy of schizophrenia represents a major challenge. The heterogeneous course of illness and the different needs in early, recent onset, and chronic stages, respectively, warrant a personalized treatment. The present paper provides an overview of the different requirements that psychopharmacology has to fulfil throughout the course of illness. The focus is on long-term treatment and decision guidance regarding long-acting injectable antipsychotics (LAI).
Key words: Schizophrenia, stages of illness, long-term treatment, long-acting injectable antipsychotics (LAI).
Psychopharmakotherapie 2016; 23(02)
