Holger Petri, Bad Wildungen*
Bezafibrat und Fenofibrat
Bezafibrat und Fenofibrinsäure, der aktive Hauptmetabolit von Fenofibrat (Prodrug), werden größtenteils unverändert oder in Form von Glucuroniden renal ausgeschieden [3, 5]. Klinisch relevante Interaktionen mit CYP-Modulatoren sind nicht zu erwarten. Fenofibrat und Fenofibrinsäure hemmen moderat CYP2C9. Die AUC (Area under the curve) des CYP2C9-Substrats Glimepirid steigt in Kombination um 23% [11]. Patienten unter Fenofibrat-Therapie sind besonders dann sorgfältig zu überwachen, wenn sie gleichzeitig Arzneimittel mit einer geringen therapeutischen Breite einnehmen, die primär über CYP2C9 verstoffwechselt werden. Zu diesen zählen Phenytoin und die Vitamin-K-Antagonisten (VKA) Phenprocoumon und Warfarin [7]. Die Dosis der Antikoagulanzien vom Cumarin-Typ sollte generell zu Beginn einer Fibrattherapie reduziert und unter Kontrolle der Gerinnungsparameter angepasst werden [1, 3–5].
Gemfibrozil
Gemfibrozil wird in Deutschland nicht mehr nennenswert verordnet [12]. In vitro ist Gemfibrozil ein stärkerer Inhibitor von CYP2C9 als von CYP2C8 [14]. In-vivo-Untersuchungen belegen aber, dass der Effekt auf CYP2C9-Substrate nur gering ist [9]. Dagegen wird der Abbau von CYP2C8-Substraten stark gehemmt [10]. Erklärt werden können die paradoxen Wirkungen durch die Bildung des 1-O-β-Glucuronid-Metaboliten, der ein starker CYP2C8-Inhibitor ist. Gemfibrozil ist ein Beispiel dafür, dass die modulatorischen Eigenschaften in vivo von In-vitro-Studien abweichen können, wenn der Metabolit als Modulator nicht betrachtet wird. Deshalb fordern die Zulassungsbehörden EMA und FDA auch von Metaboliten umfangreiche, pharmakokinetische Untersuchungen, wenn sie in definierter Menge gebildet werden [2, 6]. Die regulatorischen Leitlinien beider Behörden führen Gemfibrozil als Beispiel für einen starken CYP2C8-Inhibitor an [2, 6]. Auch für bereits zugelassene Substanzen dient Gemfibrozil bei klinischen Untersuchungen dazu, einen möglichen Abbauweg über CYP2C8 zu detektieren. Beispielsweise konnte für Montelukast in einer Interaktionsstudie mit Gemfibrozil und mit Itraconazol als starkem CYP3A4-Inhibitor gezeigt werden, dass nicht CYP3A4, sondern CYP2C8 das primär verantwortliche Isoenzym für den Abbau des Leukotrienantagonisten ist [8]. Tabelle 1 enthält eine Auswahl an Arzneimitteln, deren Metabolismus von CYP2C8 abhängt.
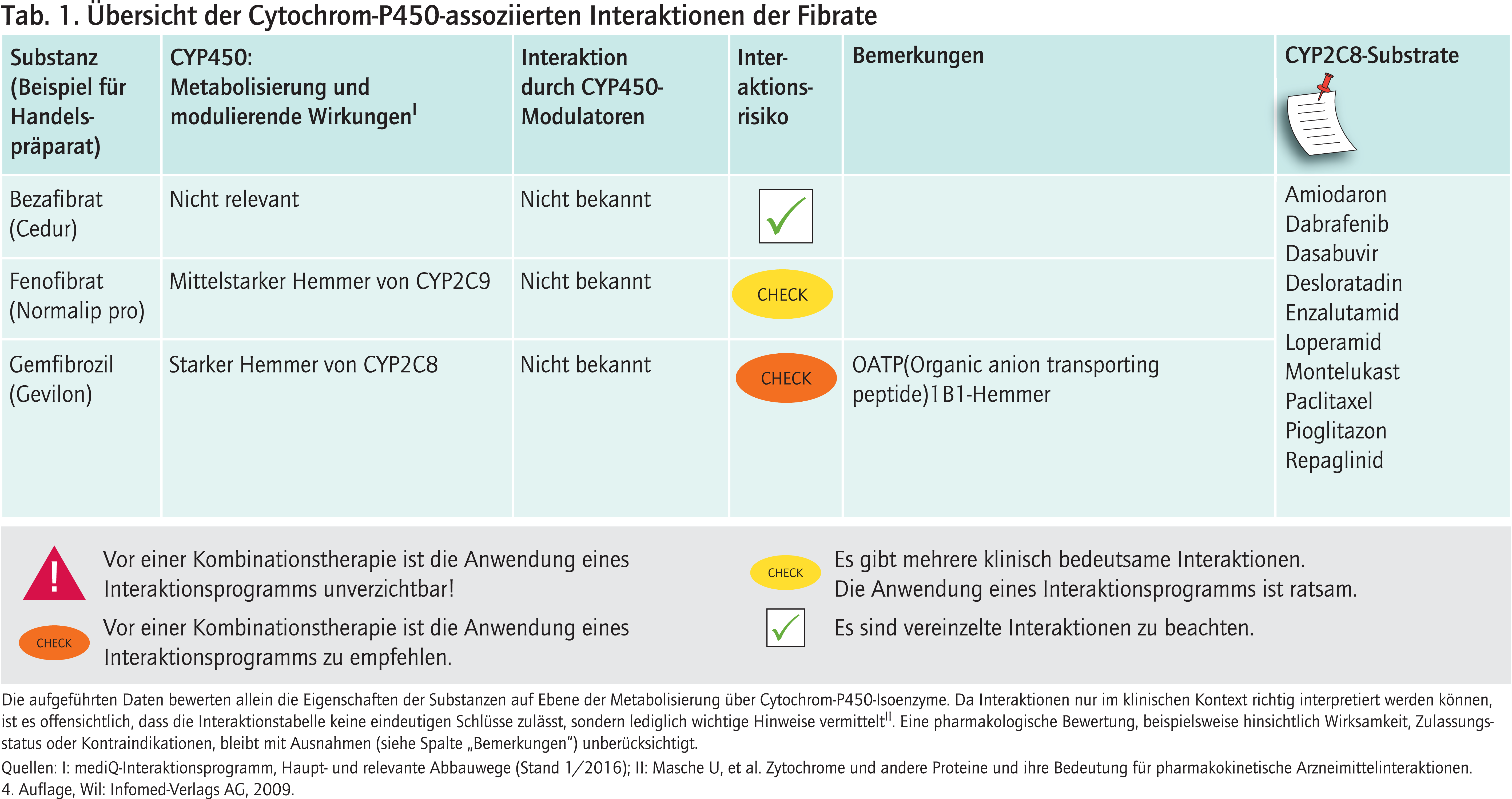
Gemfibrozil hemmt den Arzneimitteltransporter OATP1B1 (Organic anion transporting peptide 1B1). Über OATP1B1 werden die meisten HMG-CoA-Reductasehemmer aus dem Portalvenenblut in die Hepatozyten aufgenommen, was Voraussetzung für die folgenden Metabolisierungsreaktionen ist. Ist der hepatische Influx gehemmt, steigt die systemische Bioverfügbarkeit der Statine. Cerivastatin ist Substrat von CYP2C8 und OATP1B1. Neben der CYP2C8-Hemmung trug die Blockade des Transportproteins zu der hohen Inzidenz von Cerivastatin-induzierten Rhabdomyolysen unter Kombination mit Gemfibrozil bei [13].
Literatur
1. Dixon DL, Williams VG. Interaction between gemfibrozil and warfarin: case report and review of the literature. Pharmacotherapy 2009;29:744–8.
2. European Medicines Agency. Guideline on the investigation of drug interactions. CPMP/EWP/560/95/Rev. 1 Corr. 2**. 21 June 2012. www.ema.europa.eu/docs/en_GB/document_library/Scientific_guideline/2012/07/WC500129606.pdf (Zugriff am 10.02.2016).
3. Fachinformation Bezafibrat-ratiopharm®. Stand: April 2014.
4. Fachinformation Gevilon®. Stand: Februar 2014.
5. Fachinformation Normalip® pro. Stand: Oktober 2008.
6. Food and Drug Administration. Guidance for industry. Drug interaction studies – study design, data analysis, implications for dosing, and labeling recommendations. Draft Guidance. Februar 2012.
7. Kämmerer W. Porträt eines Enzyms – CYP2C9. Arzneimitteltherapie 2012;30:123–5.
8. Karonen T, Neuvonen PJ, Backmann JT. CYP2C8 but not CYP3A4 is important in the pharmacokinetics of montelukast. Br J Clin Pharmacol 2012;72:257–67.
9. Niemi M, Backman JT, Juntti-Patinen L, et al. Coadministration of gemfibrozil and itraconazole has only a minor effect on the pharmacokinetics of the CYP2C9 and CYP3A4 substrate nateglinide. Br J Clin Pharmacol 2005;60:208–17.
10. Ogilvie BW, Zhang D, Li W, et al. Glucuronidation converts gemfibrozil to a potent, metabolism-dependent inhibitor of CYP2C8: implications for drug-drug interactions. Drug Metab Dispos 2006;34:191–7.
11. Prescribing information Triglide®. Stand: April 2015.
12. Schwabe U, Paffrath D. Arzneiverordnungs-Report 2015. Berlin, Heidelberg: Springer, 2015.
13. Tamraz B, Fukushima H, Wolfe AR, et al. OATP1B1-related drug–drug and drug–gene interactions as potential risk factors for cerivastatin-induced rhabdomyolysis. Pharmacogenet Genomics 2013;23:355–64.
14. Wen X, Wang JS, Backmann JT, et al. Gemfibrozil is a potent inhibitor of human cytochrome P4502C9. Drug Metab Dispos 2001;29:1359–61.
*Nachdruck aus Krankenhauspharmazie 2016;37:106–7.
Der Artikel wurde unter Einbeziehung von Diskussionsbeiträgen von Dr. Jörg Brüggmann, Berlin, Prof. Dr. Christoph Hiemke, Mainz, und Dr. Jochen Weber, Bad Wildungen, erstellt.
Holger Petri, Zentral-Apotheke der Wicker Kliniken, Im Kreuzfeld 4, 34537 Bad Wildungen, E-Mail: hpetri@werner-wicker-klinik.de
Psychopharmakotherapie 2016; 23(02)
