Alexander Brunnauer, Wasserburg a.Inn/München/Haag i. OB, Verena Buschert, Guido Distler, Mirjam Fric, Kerstin Sander, Wasserburg a.Inn, Felix Segmiller, München, Peter Zwanzger, Wasserburg a.Inn/München, und Gerd Laux, München/Haag i. OB
Hintergrund
Fragen der Verkehrssicherheit unter medikamentöser Behandlung gewinnen angesichts der demographischen Entwicklung, mit einem immer größeren Anteil älterer Kraftfahrer und steigenden Mobilitätsbedürfnissen in unserer Gesellschaft, zunehmend an Bedeutung. Dies trifft in gleichem Maße für Patienten mit psychischen Erkrankungen zu. Etwa 80% stationär behandelter depressiver Patienten geben an, dass sie einen Führerschein besitzen, und rund 70% hiervon nutzen ihr Auto regelmäßig [9].
Antidepressiva sind die meistverordneten Psychopharmaka. Unterschiede bestehen oftmals im Nebenwirkungsprofil und der Verträglichkeit [1, 11, 22]. Die epidemiologische Datenlage bezüglich Unfallrisiken unter antidepressiver Behandlung ist dünn und inkohärent. In jüngeren Populationen scheint die Unfallwahrscheinlichkeit unter sedierenden oder nichtsedierenden Antidepressiva nicht [2, 12] oder nur leicht erhöht zu sein [3]. Ältere Personen (>60 Jahre) weisen ein zweifach erhöhtes Risiko unter der Behandlung mit Trizyklika auf, wobei das Unfallrisiko mit zunehmender Dosis anstieg [21, 25]. In einer erst kürzlich veröffentlichten Untersuchung konnte ein erhöhtes Unfallrisiko unter selektiven Serotonin(5-HT)-Wiederaufnahmehemmern (SSRI) vor allem für Frauen mittleren Alters (30 bis 60 Jahre) sowie Patienten, die langjährig mit SSRI behandelt wurden, gezeigt werden [24].
Die experimentelle Datenlage zum Einfluss von Antidepressiva auf die Fahrtüchtigkeit ist dünn und von methodischen Problemen gekennzeichnet. Die meisten der bisher veröffentlichten Untersuchungen wurden an jungen, gesunden Probanden unter Einmaldosierungen durchgeführt. Vor allem Trizyklika mit sedierenden Eigenschaften wirkten sich hierbei auf das reale Fahrverhalten negativ aus [23]. SSRI und der Serotonin-Noradrenalin-Wiederaufnahmehemmer (SNRI) Venlafaxin hatten keine negativen Auswirkungen auf die Fahrtüchtigkeit gesunder Probanden [Übersicht in 7].
Ein relativ neuer Ansatz in der Behandlung depressiver Störungen ist Agomelatin, ein Melatonin-Agonist (MT1- und MT2-Rezeptoren) und 5-HT2C-Rezeptorantagonist, der in Studien zu einer Verbesserung der Schlafqualität führte, ohne dass klassisch sedierende Effekte vorherrschend sind [18, 20]. Das ebenfalls neuere, eher aktivierende Antidepressivum Venlafaxin, das in Untersuchungen an Gesunden im Rahmen einer praktischen Fahrprobe keine negativen Auswirkungen auf Psychomotorik und Vigilanz hatte [16], wurde als Vergleichssubstanz gewählt. Um Testwiederholungseffekte zu kontrollieren, wurde eine nach Alter und Geschlecht parallelisierte Gruppe Gesunder im gleichen Zeitschema untersucht.
Ziel der vorliegenden Studie war, folgenden Fragen nachzugehen:
1) Welche Auswirkungen haben Agomelatin und Venlafaxin auf fahrtüchtigkeitsrelevante psychomotorische Leistungsparameter stationär behandelter depressiver Patienten?
2) Inwiefern unterscheiden sich die beiden Antidepressiva hinsichtlich ihrer Effekte auf die Fahrtüchtigkeit?
3) Wie werden Patienten unter Behandlung mit Agomelatin oder Venlafaxin im Rahmen einer Fahrverhaltensbeobachtung, vor der Entlassung aus der stationären Behandlung, durch einen staatlich anerkannten Fahrlehrer in Bezug auf die Fahrtauglichkeit eingeschätzt?
Patienten und Methoden
Die randomisierte klinische Studie wurde von Juli 2011 bis August 2013 im kbo-Inn-Salzach-Klinikum (Wasserburg am Inn) durchgeführt und in einer modifizierten englischsprachigen Version bereits veröffentlicht [8]. Untersucht wurden 40 depressiven Patienten (18 Männer und 22 Frauen), die sich in stationärer Behandlung befanden. Zur Überprüfung von Testwiederholungs-Effekten wurden zusätzlich 20 gesunde Kontrollpersonen (10 Männer und 10 Frauen) untersucht. Die Klassifikation erfolgte nach der Internationalen Klassifikation psychischer Störungen (ICD-10). Das durchschnittliche Alter in der Patientengruppe betrug 50,8±6,6 Jahre (Spannweite 39–62), das in der Kontrollgruppe 46,2±9,2 Jahre (Spannweite 32–63). Das aktuelle Symptomerleben wurde mit der Hamilton-Depressionsskala (HAM-D, 17-Item-Version) und der CGI (Clinical global impression) zu jedem Messzeitpunkt beurteilt. Darüber hinaus erfolgte eine Selbstbeurteilung der Symptombelastung durch die Teilnehmer anhand des Beck-Depressions-Inventars (BDI-II) sowie dem CircScreen (CIRC) [20], einer Selbstbeurteilungsskala zur Erfassung von Schlaf- und zirkadianen Rhythmusstörungen. 20 Patienten erhielten Agomelatin und 20 Venlafaxin. Die mittleren Dosierungen der antidepressiven Behandlung sind in Tabelle 1 aufgeführt.
Die Dosierung der antidepressiven Medikation wurde nach individuellen klinischen Erwägungen durch den jeweils behandelnden Psychiater vorgenommen. Patienten mit neurologischen Erkrankungen in der Vorgeschichte, Substanzmissbrauch oder Intelligenzminderung waren von der Teilnahme an der Studie ausgeschlossen. Alle Patienten waren im Besitz einer gültigen Fahrerlaubnis, nahmen freiwillig an der Studie teil und gaben vor Beginn der Untersuchungen ihr schriftliches Einverständnis zur Teilnahme. Die Studie war von der lokalen Ethikkommission genehmigt (EudraCT:2010–023473–18) und wurde in Übereinstimmung mit der Deklaration von Helsinki durchgeführt.
Tab. 1. Durchschnittlich verabreichte Dosis [mg/Tag]
|
Agomelatin (n=20) |
Venlafaxin (n=20) |
|||
|
Tag 14 (t1) |
Tag 28 (t2) |
Tag 14 (t1) |
Tag 28 (t2) |
|
|
Mittelwert (SD) |
25,0 (0,0) |
46,2 (9,1) |
193,1 (40,8) |
200,6 (50,6) |
|
Spannweite |
25–25 |
25–50 |
150–300 |
150–300 |
Ablauf
Nachdem die Patienten ihre schriftliche Einwilligung zur Studienteilnahme gegeben hatten, erfolgte eine Erstuntersuchung mittels HAM-D und CGI. Im Mittel vergingen sechs Tage zwischen dem Studieneinschluss der Patienten und dem Beginn der medikamentösen Behandlung. Die Einnahme anderer psychoaktiver Substanzen war während des gesamten Untersuchungszeitraums nicht gestattet. Alle Teilnehmer wurden in individuellen Einheiten jeweils gegen 9 Uhr morgens von einer psychologisch-technischen Assistentin (PsTA) mittels computergestützter psychomotorischer Tests untersucht. Die komplette verkehrspsychologische Untersuchung dauerte ungefähr zwei Stunden und wurde jeweils immer in gleicher Abfolge durchgeführt. Am Tag 28 (t2) absolvierten die Teilnehmer zusätzlich eine 50-minütige Fahrverhaltensbeobachtung unter Aufsicht eines staatlich geprüften Fahrlehrers.
Psychomotorische und visuelle Wahrnehmungstests
Gemäß Begutachtungsleitlinien zur Kraftfahreignung der Bundesanstalt für Straßenwesen (bast) [14] wurden unterschiedliche Leistungsbereiche wie visuelle Wahrnehmung, Konzentrationsfähigkeit, Reaktionsfähigkeit/Belastbarkeit und Vigilanz erfasst, die als wesentlich für die Einschätzung der Fahrtüchtigkeit gelten. Die Testleistungen der Teilnehmer wurden mit Normdaten verglichen, die aus einer repräsentativen Normstichprobe der autofahrenden Bevölkerung stammen. Entsprechend den dort festgelegten Beurteilungskriterien muss von Inhabern der Fahrerlaubnisklasse der Gruppe 1 (u.a. PKW) ein Prozentrang von 16, bezogen auf altersunabhängige Normen, in oben genannten Funktionsbereichen erreicht bzw. überschritten werden. Zum Einsatz kamen das computergestützte Act und React Testsystem (ART 90) [19] und das Wiener Testsystem (WTS) [26], welche in Zusammenarbeit mit dem österreichischen Bundesministerium für Verkehr, Innovation und Technologie entwickelt worden waren. Die Zuverlässigkeit dieser Methoden wurde anhand großer Stichproben von sowohl gesunden Kontrollpersonen als auch Patienten bestätigt. Es konnte gezeigt werden, dass mit diesen Methoden eine zu 83% korrekte Zuordnung von angemessenem und nicht angemessenem Fahrverhalten erreicht werden konnte [17].
Die Testbatterie umfasste die nachfolgenden Bereiche. Die visuelle Wahrnehmung wurde mit dem Tachistoskoptest (TAVT) erfasst. Dabei werden nacheinander 20 typische Verkehrssituationen am Bildschirm für jeweils 0,75 Sekunden dargeboten. Nach jeder Darbietung wird der Patient aufgefordert, fünf Multiple-Choice-Fragen zu beantworten, indem er entsprechende Knöpfe auf einer Tastatur drückt. Die Konzentrationsfähigkeit wurde mit dem peripheren Wahrnehmungstest (PVT) gemessen. Dieser Test erfordert vom Probanden die Durchführung einer Trackingaufgabe, während sich gleichzeitig ein Lichtsignal zufällig von der rechten oder der linken Peripherie in das Zentrum des Blickfeldes bewegt. Die entscheidenden Variablen dieser Messung sind die Reaktionszeit und die Ergebnisse der Trackingaufgabe. Der Vigilanztest (VIGIL) erfordert die Aufrechterhaltung der Aufmerksamkeit unter Monotonie. Über einen Zeitraum von 25 Minuten sind auf einer Kreisbahn Unregelmäßigkeiten in einer Bewegungsabfolge zu erkennen, auf die mit Tastendruck zu reagieren ist. Reaktionsfähigkeit und Belastbarkeit wurden mit dem reaktiven Stresstoleranztest (RST3) ermittelt. Farb-, Ton- und Lichtreize werden dabei in drei Testphasen mit je 180 Signalen präsentiert. Im ersten Durchgang werden die Reize mit einem Interstimulusintervall (ISI) von 1,6 Sekunden dargeboten. Die zweite Phase (schnelle Phase) hat ein ISI von 0,9 Sekunden und in der dritten Phase (moderate Phase) erscheinen die Reize alle 1,1 Sekunden. Die Patienten müssen dann entsprechende Tasten und Pedale mit Händen und Füßen betätigen.
Wasserburger Fahrverhaltensbeobachtung
Zum dritten Testzeitpunkt (t2) nahmen die Studienteilnehmer zusätzlich an einer Fahrverhaltensbeobachtung mit einem staatlich geprüften Fahrlehrer teil, der in der Beurteilung von Kraftfahrern mit neurologischen oder psychischen Erkrankungen erfahren war. Die Wasserburger Fahrverhaltensbeobachtung (WAFAB) umfasst eine etwa 50-minütige Fahrt entlang einer festgelegten Route mit definierten Beobachtungspunkten, die in der klinischen Praxis in den letzten zehn Jahren erprobt wurde und sich bewährt hat. Dieser Untersuchung unterzogen sich alle Probanden in einem Standard-Fahrschulfahrzeug. Der Fahrlehrer war bezüglich Diagnosen, Medikation und Testergebnisse der Teilnehmer nicht informiert.
Bei der 50-minütigen Testfahrt im realen Straßenverkehr wurden unterschiedliche Fahrleistungen wie Spurhalten und Spurwechsel (SPUR), Geschwindigkeitskontrolle (GESCH), Verhalten gegenüber anderen Verkehrsteilnehmern (VERH), Entfernung zu anderen Fahrzeugen (ENTF) sowie Verhalten an Kreuzungen und Einmündungen (KREUZ) anhand eines standardisierten Erfassungsbogens bewertet. Zu Beginn der Testfahrt wurde die Fahrvorbereitung vor dem Starten des Motors beurteilt, beispielsweise Sicherheitsgurt anlegen, Außen- und Rückspiegel einstellen sowie die Handbremse lösen (VORB). Darüber hinaus wurde vonseiten des Fahrlehrers zum Ende der Testfahrt eine globale Beurteilung (GLOB) hinsichtlich der Fahrtüchtigkeit abgegeben. Der Fahrlehrer bewertete dabei die Fähigkeiten entlang der standardisierten Strecke auf einer 6-Punkte-Skala von 1 (sehr gut) bis 6 (ungenügend). Ein Testergebnis von 4 (ausreichend) gab nach der Testfahrt Anlass zur individuellen Beratung des Probanden unter Berücksichtigung kompensatorischer Faktoren wie Fahrerfahrung und Einsicht in das eigene Fahrverhalten.
Statistische Analyse
Die statistischen Analysen erfolgten mit dem SPSS-Statistikprogramm (Statistical Package for Social Sciences, Ver. 11.5, SPSS Inc., Chicago III, 2002). Für die psychomotorischen Leistungsparameter wurden Varianzanalysen mit Messwiederholung durchgeführt. Demographische und klinische Daten sowie die Beurteilung der Fahrverhaltensbeobachtung wurden mittels non-parametrischer Verfahren (Chi-Quadrat- und Mann-Whitney-U-Test) analysiert.
Ergebnisse
Soziodemographische Daten
Eine Beschreibung der Gruppen ist in Tabelle 2 dargestellt. Es wurden keine signifikanten Unterschiede zwischen den Behandlungsgruppen hinsichtlich soziodemographischer und klinischer Variablen oder der Fahrbiographie festgestellt. Alle Teilnehmer verfügten über eine gültige Fahrerlaubnis und waren geübte Fahrer, die regelmäßig ihr Fahrzeug nutzten.
Tab. 2. Soziodemographische und klinische Daten
|
Agomelatin (n=20) |
Venlafaxin (n=20) |
Gesunde Kontrollen (n=20) |
Statistische Signifikanz* (p<0,05) |
|
|
Alter [Jahre], MW (SD) |
50,4 (6,1) |
51,1 (7,3) |
46,2 (9,2) |
NS |
|
Geschlecht [n] (M/F) |
10/10 |
8/12 |
10/10 |
NS |
|
Familienstand [n] |
NS |
|||
|
4 |
1 |
8 |
|
|
12 |
13 |
9 |
|
|
4 |
5 |
3 |
|
|
0 |
1 |
0 |
|
|
Diagnosen nach ICD 10 [n] |
NS |
|||
|
4 |
2 |
– |
|
|
9 |
7 |
– |
|
|
1 |
2 |
– |
|
|
6 |
9 |
– |
|
|
Ausbildung [Jahre], MW (SD) |
12,0 (0,6) |
12,6 (1,8) |
14,5 (2,9) |
Agomelatin<gesunde Kontrollen Venlafaxin<gesunde Kontrollen |
|
Tage seit Aufnahme, MW (SD) |
7,2 (4,8) |
4,5 (3,9) |
– |
NS |
|
Fahrerlaubnis |
||||
|
27,4 (8,7) |
30,4 (8,4) |
29,2 (10,3) |
NS |
|
18300 (23128) |
19100 (19563) |
17400 (6064) |
NS |
|
12,6 (11,6) |
13,3 (9,5) |
13,5 (6,6) |
NS |
|
CGI (t0), MW (SD) |
5,6 (0,5) |
5,3 (0,7) |
1,0 (0,0) |
Agomelatin>gesunde Kontrollen Venlafaxin>gesunde Kontrollen |
|
HAM-D (t0), MW (SD) |
19,8 (4,6) |
18,4 (4,1) |
0,9 (1,3) |
Agomelatin>gesunde Kontrollen Venlafaxin>gesunde Kontrollen |
|
BDI-II (t0), MW (SD) |
26,8 (9,2) |
27,6 (9,2) |
1,2 (1,6) |
Agomelatin>gesunde Kontrollen Venlafaxin>gesunde Kontrollen |
|
CIRC (t0), MW (SD) |
12,8 (3,9) |
9,9 (3,4) |
4,1 (2,5) |
Agomelatin>gesunde Kontrollen Venlafaxin>gesunde Kontrollen |
*NS: nicht signifikant; MW: Mittelwert; SD: Standardabweichung; CGI: Clinical Global Impression; HAM-D: Hamilton-Depressionsskala (17-Item-Version); BDI-II: Beck-Depressions-Inventar; CIRC: CircScreen
Globaler Fahrtüchtigkeitsscore
Zunächst wurde die psychomotorische Leistungsfähigkeit gemäß den Begutachtungsleitlinien zur Kraftfahreignung der Bundesanstalt für Straßenwesen (bast) analysiert. Wie in Abbildung 1 dargestellt, erreichten etwa 42% der unbehandelten Patienten nicht die kritische Grenze eines Prozentrangs von 16, das heißt von nicht mehr als einer Standardabweichung unterhalb des Mittelwerts der altersunabhängigen Normstichprobe. Im Gegensatz dazu erfüllten alle gesunden Kontrollpersonen dieses Leistungskriterium. Die Patienten unterschieden sich zu t0 hinsichtlich des globalen Fahrtüchtigkeitsscores nicht signifikant.
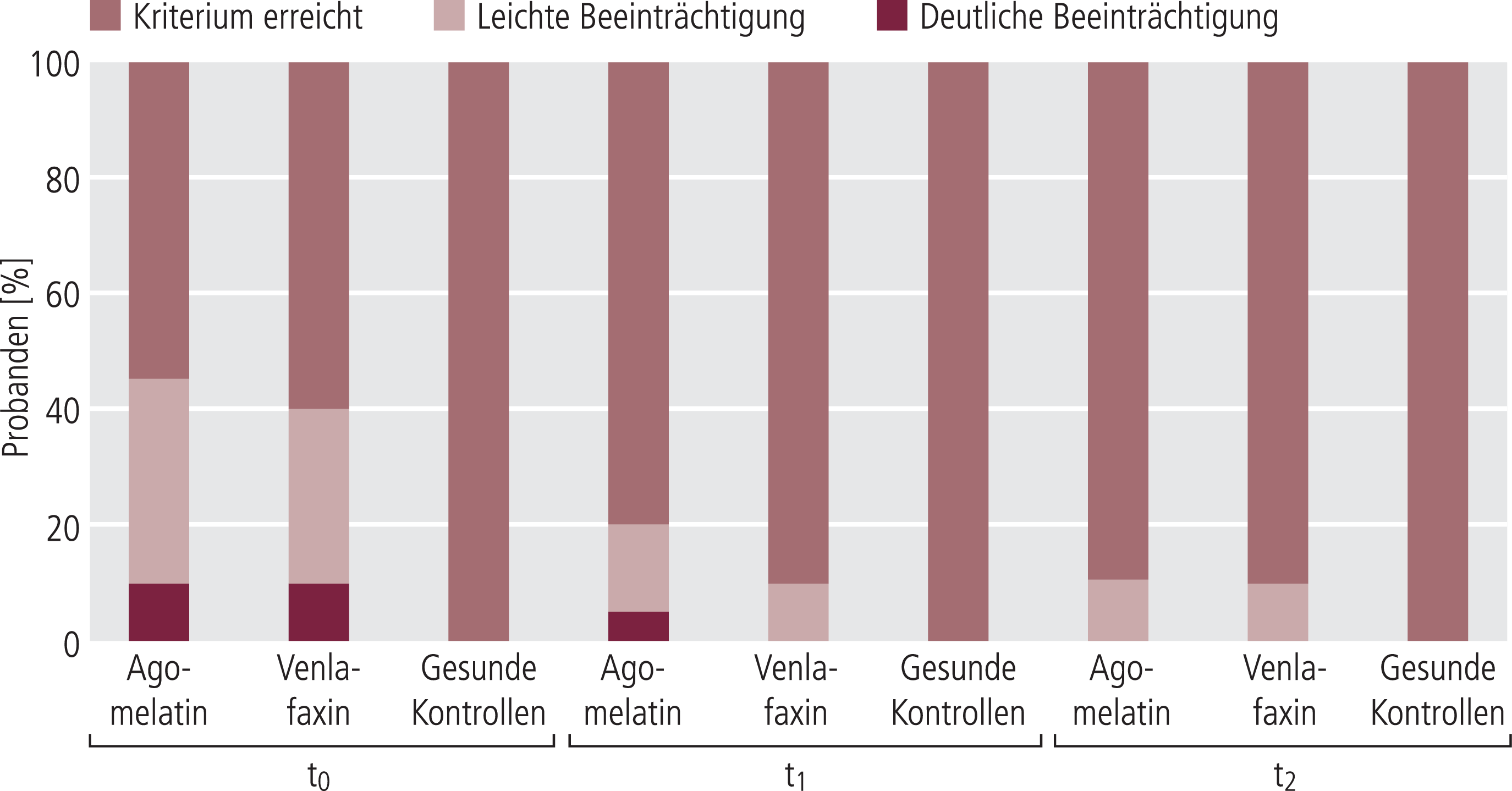
Abb. 1. Globaler Fahrtüchtigkeitsscore entsprechend den Kriterien der Begutachtungsleitlinien zur Kraftfahreignung (verkehrspsychologische Testbatterie) zu t0 (vor medikamentöser Behandlung), t1 (Tag 14) und t2 (Tag 28)
Nach 14-tägiger Behandlung (t1) mit Agomelatin oder Venlafaxin konnten sich beide Patientengruppen deutlich verbessern (Agomelatin: p<0,05; z=–2,16; Venlafaxin: p<0,01; z=–2,74). Zwischen Zeitpunkt t1 und t2 erreichten die Leistungssteigerungen in beiden Behandlungsgruppen keine statistische Signifikanz. Die Behandlungsgruppen unterschieden sich zu t2 nicht signifikant; das psychomotorische Leistungsniveau der gesunden Kontrollpersonen am Tag 28 (t2) erreichten die Patienten, die mit Agomelatin (p<0,01; z=–2,69) oder Venlafaxin (p<0,05; z=–2,35) behandelt wurden, allerdings nicht.
Wie bereits in einer früheren Studie dargestellt [6], wurden Patienten darüber hinaus eingeteilt in „leichte Beeinträchtigung“ (wenn ein Patient in weniger als 40% der kritischen Testvariablen das Kriterium nicht erreichte) und „deutliche Beeinträchtigung“ (wenn in mehr als 40% der Testvariablen das Kriterium unterschritten wurde). Aus klinischer Sicht ist es gerechtfertigt, bei der Einschätzung der Fahrtüchtigkeit in der als „leicht beeinträchtigt“ gekennzeichneten Gruppe kompensatorische Fähigkeiten bei der Bewertung der Fahrtüchtigkeit zu berücksichtigen.
Psychomotorische und visuelle Wahrnehmungsleistungen
In einem zweiten Schritt wurden die Behandlungsgruppen hinsichtlich einzelner Leistungsbereiche verglichen, die sich zu t0 nicht signifikant unterschieden. Mit Ausnahme der Vigilanzleistung verbesserten sich die Patienten über die Messzeitpunkte deutlich (alle p<0,01). Signifikante Interaktions- oder Gruppeneffekte ergaben sich nicht (Tab. 3). Auch hier erreichten die Patienten nicht das Leistungsniveau der gesunden Kontrollpersonen zu t2 (Agomelatin: F=2,73, p<0,05; Venlafaxin: F=4,49, p<0,01).
Tab. 3. Rohwerte der Leistungsuntersuchung (Mittelwerte und Standardabweichung) und Ergebnisse der univariaten Analysen mit Messwiederholung (F-Werte) zwischen den Behandlungsgruppen
|
Agomelatin (n=20) |
Venlafaxin (n=20) |
Gesunde Kontrollen (n=20) |
||||||||||
|
t0 |
t1 |
t2 |
t0 |
t1 |
t2 |
t0 |
t1 |
t2 |
Zeit |
Zeit x Gruppe |
Gruppe |
|
|
Statistik (F-Werte) |
||||||||||||
|
Visuelle Wahrnehmung |
11,1 (2,9) |
12,2 (3,1) |
13,5 (2,8) |
12,6 (3,3) |
13,5 (2,1) |
13,6 (2,5) |
13,6 (2,3) |
14,9 (1,7) |
15,5 (2,3) |
F=11,4** |
F=3,1 |
F=1,5 |
|
Konzentration |
2,8 (0,9) |
2,1 (0,6) |
2,0 (0,5) |
2,5 (0,9) |
1,9 (0,3) |
1,9 (0,4) |
1,9 (0,3) |
1,7 (0,3) |
1,6 (0,3) |
F=13,7** |
F=0,5 |
F=1,7 |
|
Belastbarkeit I |
5,7 (7,1) |
1,8 (3,2) |
1,5 (2,4) |
7,8 (11,4) |
2,6 (4,0) |
1,1 (1,9) |
1,3 (2,0) |
0,6 (1,0) |
0,4 (0,9) |
F=7,2** |
F=1,3 |
F=0,4 |
|
Belastbarkeit II |
39,2 (30,5) |
19,1(16,3) |
12,4 (15,7) |
45,6 (32,3) |
24,0 (26,7) |
16,2 (18,1) |
13,2 (10,9) |
4,6 (6,0) |
1,7 (2,4) |
F=27,4** |
F=0,1 |
F=0,5 |
|
Belastbarkeit III |
17,4 (19,9) |
9,2 (12,1) |
4,9 (8,3) |
23,2 (27,5) |
11,8 (19,5) |
5,8 (8,6) |
5,0 (4,6) |
2,0 (2,3) |
1,1 (1,4) |
F=10,5** |
F=0,4 |
F=0,5 |
|
Vigilanz |
1,5 (1,3) |
1,5 (1,1) |
1,4 (0,9) |
1,7 (1,0) |
1,5 (0,5) |
1,4 (0,9) |
1,4 (0,6) |
1,2 (0,7) |
1,1 (0,8) |
F=1,2 |
F=0,4 |
F=0,1 |
** p<0,01; Standardabweichung in Klammern
Überprüfung von Testwiederholungs-Effekten
Zur Überprüfung von Retest-Effekten wurden Vergleiche mit der Gruppe der gesunden Kontrollen durchgeführt. Dabei konnten signifikante Interaktionseffekte (Zeit × Gruppe) bei den mit Agomelatin behandelten Patienten für den Bereich Konzentrationsfähigkeit (F=4,24; p<0,05) und hinsichtlich Reaktionsfähigkeit/Belastbarkeit (Belastbarkeit I: F=3,84; p<0,05; Belastbarkeit II: F=3,79; p<0,05; Belastbarkeit III: F=3,10; p<0,05) analysiert werden. In der mit Venlafaxin behandelten Patientengruppe zeigten sich ebenfalls signifikante Interaktionseffekte für die Funktionsbereiche Reaktionsfähigkeit/Belastbarkeit (Belastbarkeit I: F=3,41; p<0,05; Belastbarkeit II: F=6,76; p<0,05; Belastbarkeit III: F=3,50; p<0,05).
Psychologische Fahrverhaltensbeobachtung
In den einzelnen Fahrverhaltensbereichen erreichten die Vergleiche mit der Kontrollgruppe keine statistische Signifikanz. Auch zeigten sich keine signifikanten Unterschiede zwischen den Behandlungsgruppen. Es war ein Trend in Richtung signifikanter Unterschied für die Globalbeurteilung (GLOB) beim Vergleich mit der gesunden Kontrollgruppe (Agomelatin: p<0,07; z =–1,83; Venlafaxin: p<0,08; z =–1,75) zu beobachten. 72,5% der Studienpatienten wurden von dem Fahrlehrer als zumindest „gute Fahrer“ vor ihrer Entlassung aus der stationären Behandlung eingestuft im Vergleich zu 85% der gesunden Probanden; in 22,5% der Fälle wurden den Patienten „befriedigende“ Fahrleistungen attestiert – im Vergleich zu 15% bei den Kontrollen. Signifikante Unterschiede zwischen den Behandlungsgruppen zeigten sich auch in der Fahrverhaltensbeobachtung nicht (Abb. 2).
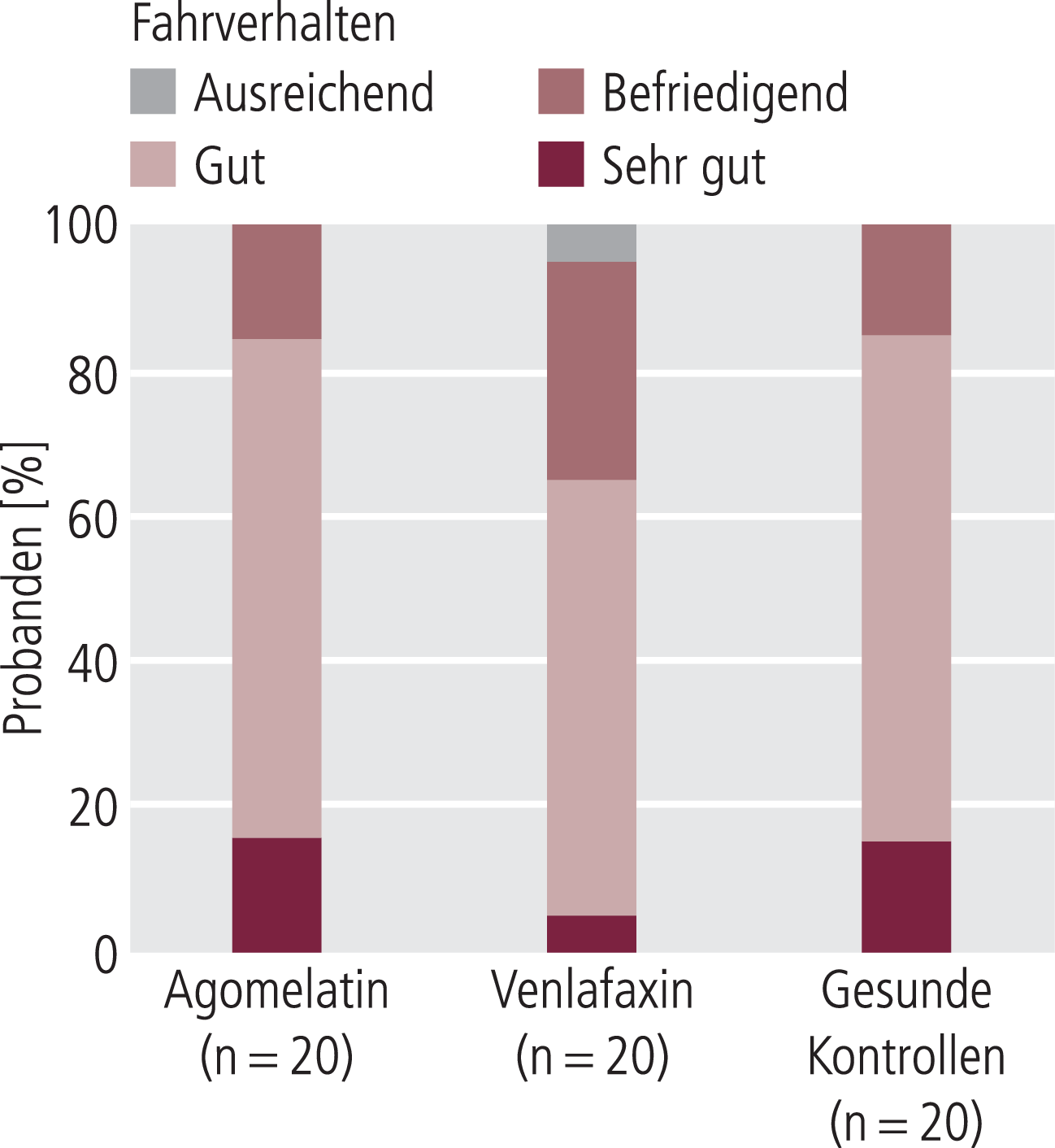
Abb. 2. Fahrverhaltensbeobachtung – Globalbeurteilung des Fahrlehrers zu t2 (Tag 28)
Psychopathologie
Zu t0 unterschieden sich die Patientengruppen nicht im Hinblick auf die Symptombelastung (HAM-D, CGI, CIRC). Wie zu erwarten, unterschieden sie sich signifikant von den gesunden Kontrollpersonen zu t0 (alle p-Werte <0,001). Signifikante Verbesserungen zwischen den Untersuchungen (t0–t2) hinsichtlich depressiver Symptome konnten sowohl für Patienten unter Agomelatin (HAM-D: p<0,001; z=–3,89; CGI: p<0,001; z=–3,78), als auch für diejenigen unter Venlafaxin (HAM-D: p<0,001; z=–3,55; CGI: p<0,001; z=–3,58) ermittelt werden. Dies wurde auch anhand der Selbstbeurteilung mit dem BDI-II deutlich, der mehr auf die Erfassung kognitiver Symptome der Depression fokussiert. Dabei gaben sowohl mit Agomelatin behandelte Patienten (p<0,001; z=–3,34) als auch Patienten unter Venlafaxin p<0,001; z=–3,55) deutliche Verbesserungen in der Symptombelastung an.
Im CircScreen (CIRC) berichteten Patienten unter Agomelatin über Verbesserungen ihrer Schlaf- bzw. zirkadianen Rhythmusstörungen zwischen t0 und t2 (p<0,01; z=–2,70), wohingegen die Selbsteinschätzung von Patienten unter Venlafaxin keine statistische Signifikanz erreichte. Es gab keinen signifikanten Unterschied zwischen den Behandlungsgruppen zu t2. Die Patienten zeigten keine Verbesserungen in diesem Verfahren in Richtung des Niveaus der gesunden Kontrollen zu t2 (Abb. 3).
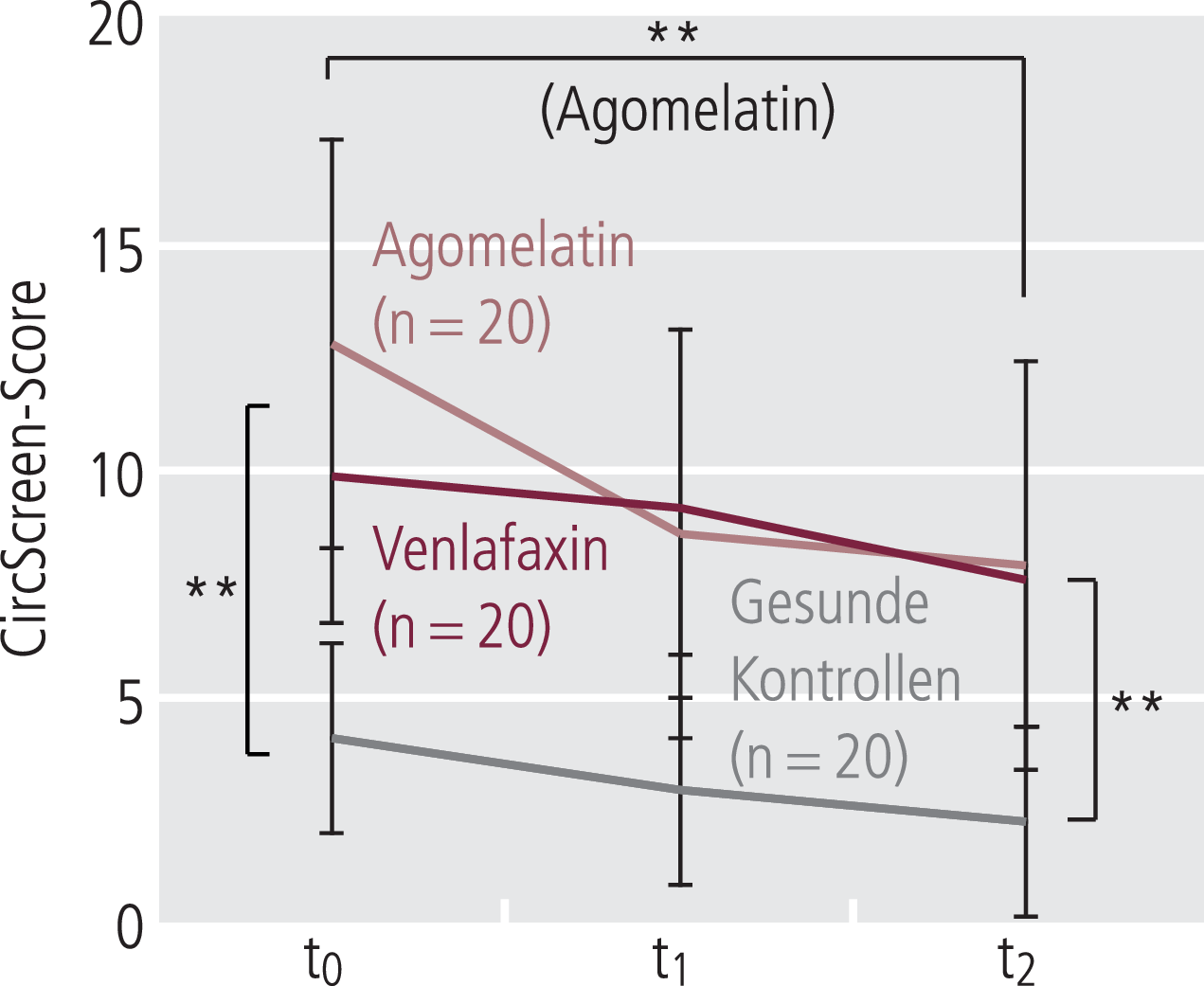
Abb. 3. Selbstbeurteilung von Schlafstörungen (CircScreen) zu t0 (vor medikamentöser Behandlung), t1 (Tag 14) und t2 (Tag 28); ** p<0,01
Diskussion
Sowohl Patienten als auch die Behandelnden stehen häufig vor dem Dilemma, dass die psychopharmakologische Therapie, die oftmals entscheidend für eine Verbesserung der psychopathologischen Symptomatik ist, Veränderungen in Wahrnehmung, Aufmerksamkeit oder Psychomotorik, mit Auswirkungen auf die Fahrtüchtigkeit bewirken kann. Auf der anderen Seite ist die Datenbasis aus klinischen Untersuchungen zum Thema Verkehrssicherheit zu dünn, um Patienten fundiert beraten zu können.
Unsere Daten zeigen, dass die Behandlung mit Agomelatin oder Venlafaxin positive Effekte auf die Fahrtüchtigkeit stationär behandelter depressiver Patienten hat. Innerhalb der vierwöchigen medikamentösen Behandlungsphase zeigten beide Patientengruppen eine signifikante Verringerung psychopathologischer Symptome sowie eine deutliche Verbesserung in verkehrsrelevanten Leistungsbereichen, wie Reaktionsfähigkeit und Belastbarkeit. Die Patienten konnten mehrheitlich entsprechend den Begutachtungsleitlinien zur Kraftfahreignung als „fahrtüchtig“ eingestuft werden. Die meisten Verbesserungen zeigten sich in den ersten beiden Wochen der medikamentösen Behandlung. Diese Ergebnisse werden durch die Resultate der Fahrverhaltensbeobachtung im Realverkehr durch einen zertifizierten Fahrlehrer bestätigt. 72,5% der Patienten wurden hier als „gute Fahrer“ eingestuft, ungefähr 22,5% als „befriedigende Fahrer“ und nur in etwa 5% der Fälle ergaben sich leichte Bedenken hinsichtlich der Fahrtüchtigkeit.
Signifikante Unterschiede zwischen den Patienten, die mit Agomelatin oder Venlafaxin behandelt wurden, konnten weder auf der Ebene einzelner psychomotorischer Funktionen noch in der Fahrverhaltensbeobachtung ermittelt werden. Obwohl sich signifikante Verbesserungen hinsichtlich der Fahrtüchtigkeit zeigten, erreichten die Patienten in den psychomotorischen Tests nicht das Leistungsniveau gesunder Kontrollen innerhalb des untersuchten Behandlungszeitraums. Es scheint, wenn auch nicht in signifikanter Ausprägung, dass dies auch für die Globalbeurteilung der Fahrprobe zutrifft.
Im Hinblick auf die psychopathologische Symptomatik führten beide Antidepressiva – mit Ausnahme einer leichten Überlegenheit der mit Agomelatin behandelten Patienten im Bereich der Schlafstörungen in den ersten beiden Behandlungswochen – zu vergleichbaren Verbesserungen innerhalb des Untersuchungszeitraums. Jedoch konnte in keiner der beiden Behandlungsgruppen das Funktionsniveau der gesunden Kontrollpersonen innerhalb des vierwöchigen Studienzeitraums erreicht werden.
Die Ergebnisse unserer Untersuchung stehen im Einklang mit klinischen Studien, die darauf hinweisen, dass teilremittierte depressive Patienten unter antidepressiver Behandlung bessere Leistungen in psychomotorischen Tests und im Fahrsimulator zeigen als unbehandelte Patienten. In einer früheren Studie konnten wir darstellen, dass depressive Patienten in stationärer Behandlung, die mit Mirtazapin oder Reboxetin behandelt wurden, deutliche Verbesserungen in verkehrsrelevanten Funktionen zeigten, des Weiteren eine signifikante Verringerung der Unfallrate in einem Fahrsimulator-Test nach 14 Tagen Behandlung [6]. Diese Ergebnisse wurden durch eine Untersuchung von Shen et al. [27] bestätigt. Die Autoren beobachteten eine Verbesserung beim Halten der Fahrspur und eine signifikante Verringerung von Unfällen in einem computerisierten Fahrsimulator-Test bei depressiven Patienten während einer 30-tägigen Behandlungsphase mit Mirtazapin. Die unbehandelte klinische Kontrollgruppe zeigte dagegen keine Veränderungen in fahrrelevanten Leistungsbereichen. Es gibt jedoch auch Hinweise, dass die Behandlung mit Antidepressiva, jedenfalls in einer Subgruppe depressiver Patienten, die Fahrtüchtigkeit nicht „normalisiert“. Es wird vermutet, dass Beeinträchtigungen in verkehrsrelevanten Funktionsbereichen unter Langzeitbehandlung eher auf residuale depressive Symptome als auf Medikamenteneffekte zurückzuführen sind [5, 6, 30].
Zur Wirksamkeit von Venlafaxin oder Agomelatin auf attentionale oder kognitive Funktionen liegen kaum Daten vor, dies gilt insbesondere für Untersuchungen zur Fahrtüchtigkeit. Venlafaxin führte bei gesunden Kontrollpersonen zu keinen Beeinträchtigungen in neuropsychologischen Funktionen wie Psychomotorik oder Gedächtnis [28]. Dies konnte ebenfalls bei älteren depressiven Patienten gezeigt werden [29]. Eine randomisierte Placebo-kontrollierte Untersuchung zu Venlafaxin bei gesunden Probanden ergab weder in der akuten Verabreichungsphase noch bei längerfristiger Gabe Auswirkungen auf die Leistungsfähigkeit in einer Fahrprobe [16]. Allerdings gibt es Hinweise auf beeinträchtigende Effekte bei Vigilanzanforderungen unter Venlafaxin [5, 16]. Zu Agomelatin existieren bislang keine Daten in Bezug auf Auswirkungen auf kognitive oder psychomotorische Funktionen oder die Fahrtüchtigkeit depressiver Patienten. In einer aktuellen Studie konnte gezeigt werden, dass Agomelatin keinen signifikanten Einfluss auf exekutive Funktionen bei Patienten mit Fibromyalgie-Syndrom hatte, obgleich insgesamt ein Trend in Richtung Verbesserung der Leistungsfähigkeit zu beobachten war [10].
Folgende Einschränkungen sind bei der Interpretation der Studienergebnisse zu berücksichtigen. In die Studie konnten lediglich Patienten eingeschlossen werden, die in der Lage waren, ohne medikamentöse Behandlung an einer ungefähr 120 Minuten dauernden Testprozedur teilzunehmen. In früher veröffentlichten Querschnittsuntersuchungen zeigten 70 bis 80% der Patienten vor Entlassung in eine ambulante Behandlung leicht- bis schwergradig ausgeprägte Beeinträchtigungen in verkehrsrelevanten psychomotorischen Funktionen [4, 5, 13]; in der vorliegenden Studie erfüllten etwa 55% der Patienten bereits zu Beginn der Untersuchung (t0) die gesetzlichen Mindestanforderungen. Somit kann ein Selektionsbias nicht ausgeschlossen werden. Darüber hinaus untersuchten wir einen relativ kurzen Behandlungszeitraum; damit bleiben Langzeiteffekte der Behandlung mit Antidepressiva auf die untersuchten Leistungsfunktionen ungewiss. Nachdem die Kombinations- bzw. Augmentationstherapie gängige klinische Praxis ist, müssen relevante Medikamenteninteraktionen mit Bezug auf die Verkehrssicherheit in zukünftigen Studien systematisch analysiert werden, um eine bessere Übertragbarkeit auf die klinische Praxis zu erreichen.
Aus unseren Daten lässt sich zusammenfassend ableiten, dass depressive Patienten, die mit Agomelatin oder Venlafaxin behandelt werden, bessere Leistungen in verkehrsrelevanten Tests im Vergleich zu unbehandelten depressiven Patienten erzielen und in einer Fahrverhaltensbeobachtung unter Realbedingungen, vor Entlassung in die ambulante Behandlung, mehrheitlich als fahrtüchtig eingestuft werden können. Um Patienten allerdings umfassend im Hinblick auf die Verkehrssicherheit zu beraten, sind mehr Patientenstudien unter Berücksichtigung der oben genannten klinischen Aspekte erforderlich, um die Beziehungen zwischen Erkrankung, pharmakologischer Behandlung und Fahrtauglichkeit differenziert zu beleuchten.
Danksagung
Wir danken Frau Michaela Wende und Frau Andrea Geidobler für ihre tatkräftige Unterstützung bei diesem Projekt.
Interessenkonflikterklärung
Diese Studie wurde mit finanziellen Mitteln der Firma Servier unterstützt.
Die Autoren erklären im Einzelnen folgende Interessenkonflikte:
AB: Vortrags- oder Publikationshonorar von Otsuka und Servier; Unterstützung für Kongressbesuche und Forschungsbeihilfe (persönlich oder für die Einrichtung) von Servier
VB: Forschungsbeihilfe (persönlich oder für die Einrichtung) von Servier
GD: Forschungsbeihilfe (persönlich oder für die Einrichtung) von Servier
MF: Unterstützung für Kongressbesuch von Merz, Forschungsbeihilfe (persönlich oder für die Einrichtung) von Servier
KS: Forschungsbeihilfe (persönlich oder für die Einrichtung) von Servier
FS: Vortragshonorar von der Klinik für Psychiatrie Bethel
PZ: Beraterhonorar von Lundbeck und Pfizer; Vortrags- oder Publikationshonorar von AstraZeneca, Bristol-Myers Squibb, Lilly, Pfizer, Servier; Unterstützung für Kongressbesuche von Servier; sonstige Unterstützung (persönlich oder für die Einrichtung) von Janssen und Lundbeck
GL: Berater-, Vortrags- und Publikationshonorar sowie Forschungsbeihilfe von AstraZeneca, Bayer, Boehringer Ingelheim, Janssen-Cilag, Lilly, Lundbeck, Merz, Novartis, Pfizer, Servier, Thieme-Verlag Stuttgart, Springer-Verlag Heidelberg/Berlin –Wien, Urban&Fischer/Elsevier Verlag München, Kohlhammer-Verlag Stuttgart
Literatur
1. Anderson IM. Selective serotonin reuptake inhibitors versus tricyclic antidepressants: a meta-analysis of efficacy and tolerability. J Affect Disord 2000;58:19–36.
2. Barbone F, McMahon AD, Davey PG, et al. Association of road traffic accidents with benzodiazepine use. Lancet 1998;352:1331–6.
3. Bramness JG, Skurtveit S, Neutel CI, et al. Minor increase in risk of road traffic accidents after prescriptions of antidepressants: A study of population registry data in Norway. J Clin Psychiatry 2008;69:1099–103.
4. Brunnauer A, Laux G. Driving ability and antidepressants. Psychiat Prax 2003;30(Suppl 2):102–5.
5. Brunnauer A, Laux G, Geiger E, et al. Antidepressants and driving ability: results from a clinical study. J Clin Psychiatry 2006;67: 1776–81.
6. Brunnauer A, Laux G, David I, et al. The impact of reboxetine and mirtazapine on driving simulator performance and psychomotor function in depressed patients. J Clin Psychiatry 2008;69:1880–6.
7. Brunnauer A, Laux G. The effects of most commonly prescribed second generation antidepressants on driving ability: a systematic review. J Neural Transm 2013;1:225–32.
8. Brunnauer A, Buschert V, Distler G, et al. Driving performance and psychomotor function in depressed patients treated with agomelatine or venlafaxine. Pharmacopsychiatry 2015;48:65–71.
9. Brunnauer A, Buschert V, Segmiller F, et al. Mobility behaviour and driving status of patients with mental disorders – an exploratory study. Int J Psychiatry Clin Pract 2015; DOI:10.3109/1365150.2015.1089293.
10. Bruno A, Mico U, Lorusso S, et al. Agomelatine in the treatment of fibromyalgia. A 12-week open-label, uncontrolled preliminary study. J Clin Psychopharmacol 2013;33:507–11.
11. Cipriani A, Furikawa TA, Salanti G, et al. Comparative efficacy and acceptability of 12 new-generation antidepressants: a multiple-treatments meta-analysis. Lancet 2009;373:746–58.
12. Gibson JE, Hubbard RB, Smith CJ, et al. Use of self controlled analytical techniques to assess the association between use of prescription medications and the risk of motor vehicle crashes. Am J Epidemiol 2009;169:761–8.
13. Grabe HJ, Wolf T, Grätz S, et al. The influence of polypharmacological antidepressant treatment on central nervous information processing of depressed patients: Implications for fitness to drive. Neuropsychobiology 1998;37:200–4.
14. Gräcmann N, Albrecht M. Begutachtungsleitlinien zur Kraftfahreignung. Berichte der Bundesanstalt für Straßenwesen. Bergisch Gladbach: Carl Schünemann Verlag GmbH, 2014.
15. Guiano G, Gupta S, Chiodo D, et al. Agomelatine versus other antidepressive agents for major depression. Cochrane Database Syst Rev 2013;12:CD008851. DOI: 10.1002/ 14651858.CD008851.pub2.
16. O’Hanlon JF, Robbe HWJ, Vermeeren A, et al. Venlafaxine’s effects on healthy volunteers’ driving, psychomotor, and vigilance performance during 15-day fixed and incremental dosing regimens. J Clin Psychopharmacol 1998;18:212–21.
17. Karner T, Biehl B. Über die Zusammenhänge verschiedener Versionen von Leistungstests im Rahmen der verkehrspsychologischen Diagnostik. Zeitschrift für Verkehrssicherheit 2001;47:53–63.
18. Kasper S, Hamon M. Beyond the monoaminergic hypothesis: agomelatin, a new antidepressant with an innovative mechanism of action. World J Biol Psychiatry 2009;10:117–26.
19. Kisser R, Wenninger U. Computerunterstütztes Testen im Rahmen der Fahreignungsuntersuchung (Act & React Testsystem ART 90). Kleine Fachbuchreihe des Kuratoriums für Verkehrssicherheit. Wien: Kuratorium für Verkehrssicherheit, 1983.
20. Laredo J, Quera Salva MA, Falissard B, et al. Screening of sleep and circadian rhythms in major depression: Sleep and wake complaints. J Sleep Res 2002;11(Suppl 1):132–3.
21. Leveille SG, Buchner DM, Koepsell TD, et al. Psychoactive medications and injurious motor vehicle collisions involving older drivers. Epidemiology 1994;5:591–8.
22. Möller HJ. Are all antidepressants the same? J Clin Psychiatry 2000;61(Suppl 6):24–8.
23. Ramaekers JG. Antidepressants and driver impairment: empirical evidence from a standard on-the-road test. J Clin Psychiat 2003;64:20–9.
24. Ravera S, van Rein N, de Gier J, et al. Road traffic accidents and psychotropic medication use in the Netherlands: a case-control study. Br J Clin Pharmacol 2011;72:505–13.
25. Ray WA, Fought RL, Decker MD. Psychoactive drugs and the risk of injurious motor vehicle crashes in elderly drivers. Am J Epidemiol 1992;136:873–83.
26. Schuhfried G. Wiener Testsystem (Vienna Test System). Mödling, Austria: Dr. Gernot Schuhfried GmbH, 2000.
27. Shen J, Möller HJ, Wang X, et al. Mirtazapine, a sedating antidepressant, and improved driving safety in patients with major depressive disorder: a prospective, randomized trial of 28 patients. J Clin Psychiatry 2009;70:370–7.
28. Siepmann T, Mueck-Weimann M, Oertel R, et al. The effects of venlafaxine on cognitive function and quantitative EEG in healthy volunteers. Pharmacopsychiatry 2008;41:146–50.
29. Trick L, Stanley N, Rigney U, et al. A double-blind randomized 26-week study comparing the cognitive and psychomotor effects and efficacy of 75 mg (37.5 mg b.i.d.) venlafaxine and 75 mg (25 mg mane and 50 mg nocte) dothiepin in elderly patients with moderate major depression treated in general practice. J Psychopharmacol 2004;18:205–14.
30. Wingen M, Ramaekers JG, Schmitt JA. Driving impairment in depressed patients receiving long-term antidepressant treatment. Psychopharmacology 2006;188:84–91.
Dr. Alexander Brunnauer, kbo-Inn-Salzach-Klinikum, Abteilung Neuropsychologie, Gabersee Haus 13, 83512 Wasserburg am Inn, E-Mail: alexander.brunnauer@kbo.de; Psychiatrische Universitätsklinik der Ludwig-Maximilians-Universität München; Institut für Psychologische Medizin (IPM), Haag i. OB
Dr. Verena Buschert, Guido Distler, Dr. med. Mirjam Fric, Dr. Kerstin Sander, kbo-Inn-Salzach Klinikum, Fachklinikum für Psychiatrie, Psychotherapie, Psychosomatische Medizin, Geriatrie, Neurologie, Wasserburg/Inn
Dr. med. Felix Segmiller, Psychiatrische Universitätsklinik der Ludwig-Maximilians-Universität München
Prof. Dr. med. Peter Zwanzger, kbo-Inn-Salzach Klinikum, Fachklinikum für Psychiatrie, Psychotherapie, Psychosomatische Medizin, Geriatrie, Neurologie, Wasserburg/Inn; Psychiatrische Universitätsklinik der Ludwig-Maximilians-Universität München
Prof. Dr. med. Dipl.-Psych. Gerd Laux, Psychiatrische Universitätsklinik der Ludwig-Maximilians-Universität München; Institut für Psychologische Medizin (IPM), Haag i. OB
Traffic safety of patients treated with agomelatine or venlafaxine
40 inpatients with a major depressive episode were randomly assigned to treatment with either agomelatine (n=20) or venlafaxine (n=20) and investigated concerning their driving ability. Patients were tested before pharmacologic treatment (t0), and on days 14 (t1) and 28 (t2) after initiation of treatment. Data were collected with the computerized Act and React Testsystem (ART 90) and the Wiener Testsystem (WTS) measuring visual perception, reactivity/stress-tolerance, concentration and vigilance. Additionally, participants were rated on an on-road driving test on day 28 by a licensed driving instructor. To control for retest-effects a group of 20 healthy subjects, parallelized for age and gender, was examined in the same time schedule.
Results: Both treatment groups significantly improved in depressive symptoms and in reactivity and stress-tolerance. After four weeks of treatment with antidepressants 87.5% reached the performance criteria according to the German guidelines for road and traffic-safety. In the on-road driving test 72.5% of patients were rated as abundantly fit to drive, in 22.5% of cases a satisfactory performance was certified and in 5% of our sample there were slight concerns with respect to fitness to drive. Significant differences between treatment groups could not be observed. Patients did not reach performance level in functional domains of healthy controls within the study phase.
Conclusions: Our results indicate that partly remitted depressed inpatients treated with agomelatine or venlafaxine significantly improved in psychomotor functions related to driving ability, when compared with the untreated phase and could be predominately classified as fit to drive after the stationary treatment phase.
Key words: Depression, antidepressants, agomelatine, venlafaxine, driving performance, on-road driving test
Psychopharmakotherapie 2016; 23(01)
