Holger Petri, Bad Wildungen*
Eslicarbazepinacetat und Rufinamid
Eslicarbazepinacetat und Rufinamid sind wie Oxcarbazepin Analoga von Carbamazepin [18]. Oxcarbazepin wird in der Leber rasch zum Monohydroxyderivat (MHD) reduziert [14]. MHD besteht aus dem Enantiomerenpaar S-(+)-Licarbazepin oder besser Eslicarbazepin sowie R-(–)-Licarbazepin und wird im Verhältnis 4:1 gebildet (Abb. 1). Pharmakologisch wirksam ist nur Eslicarbazepin. Eslicarbazepinacetat ist wie Oxcarbazepin ein Prodrug. Durch Hydrolyse entsteht zu 95% der aktive Metabolit Eslicarbazepin [3]. CYP-Interaktionen von Eslicarbazepinacetat und Oxcarbazepin sind ähnlich. Eslicarbazepinacetat ist ein moderater Hemmer von CYP2C19 und ein leichter Induktor von CYP3A4 [4, 5, 15]. In der antikonvulsiven Kombinationstherapie sind Wechselwirkungen mit Substanzen zu beachten, die über CYP2C19 (Phenobarbital, Phenytoin und Primidon) oder CYP3A4 (z.B. Ethosuximid, Perampanel und Zonisamid) verstoffwechselt werden. Des Weiteren wird das Risiko für kardiale Nebenwirkungen bei Komedikation mit Citalopram erhöht. Citalopram wird über CYP2C19 abgebaut. Durch klinisch wirksame CYP2C19-Inhibitoren steigen bei gleichbleibender Dosierung die Plasmaspiegel. Der selektive Serotonin-Wiederaufnahmehemmer verlängert dosisabhängig die QTc-Zeit und das Risiko ventrikulärer Arrhythmien, einschließlich Torsade de pointes (TdP), ist erhöht [21]. Eslicarbazepinacetat kann die Wirkung von hormonellen Kontrazeptiva vermindern. Die Hormone werden als CYP3A4-Substrate beschleunigt abgebaut [15].
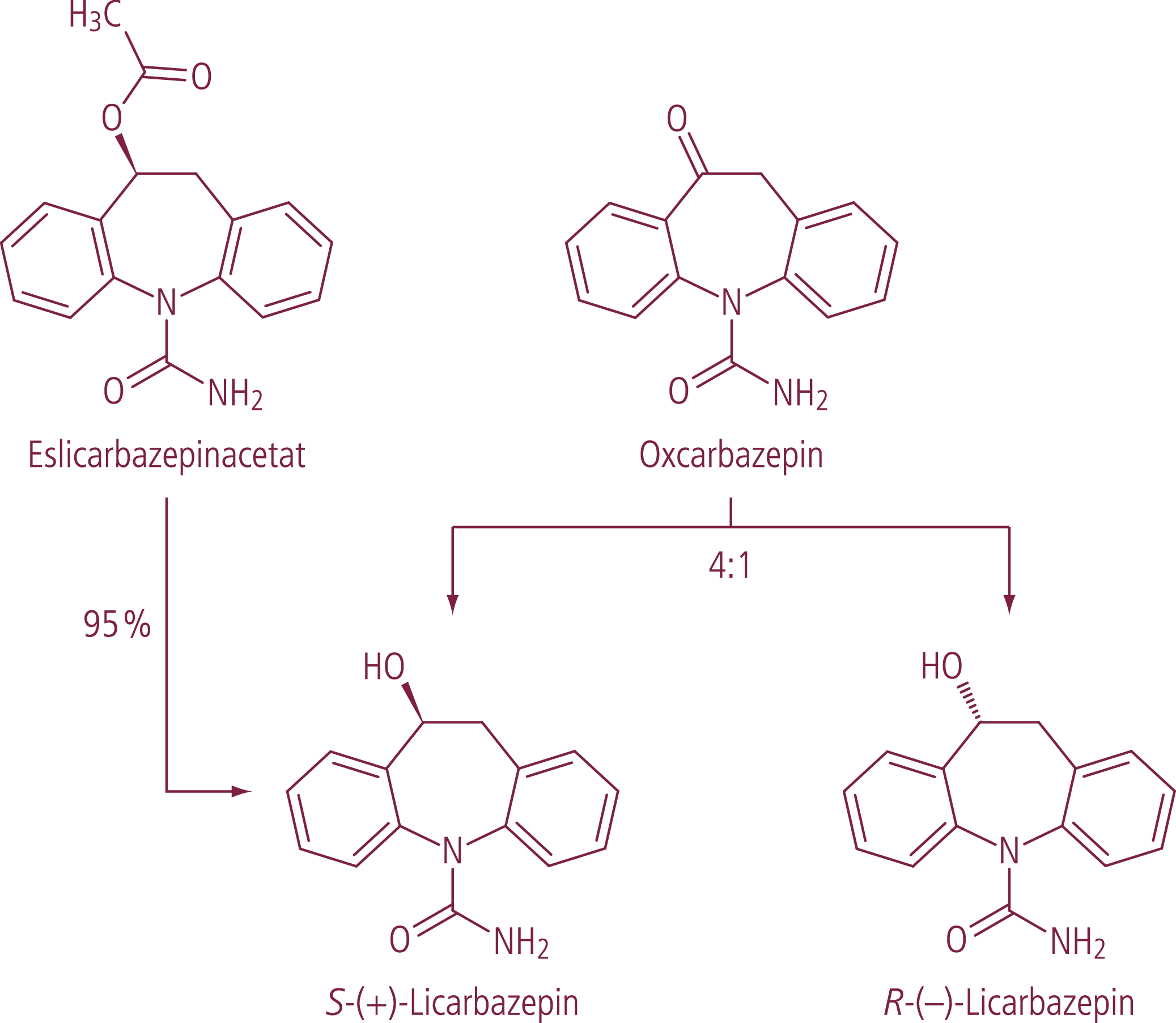
Abb. 1. Metabolimus von Eslicarbazepinacetat und Oxcarbazepin
Rufinamid wird CYP-unabhängig verstoffwechselt. Eine schwache CYP3A4-Induktion kann klinisch relevant werden bei CYP3A4-Substraten mit engem therapeutischen Index. Rufinamid scheint keine klinisch relevante Auswirkung auf die Steady-State-Konzentrationen von Carbamazepin, Lamotrigin, Phenobarbital, Phenytoin, Topiramat oder Valproinsäure zu haben [9].
Ethosuximid und Mesuximid
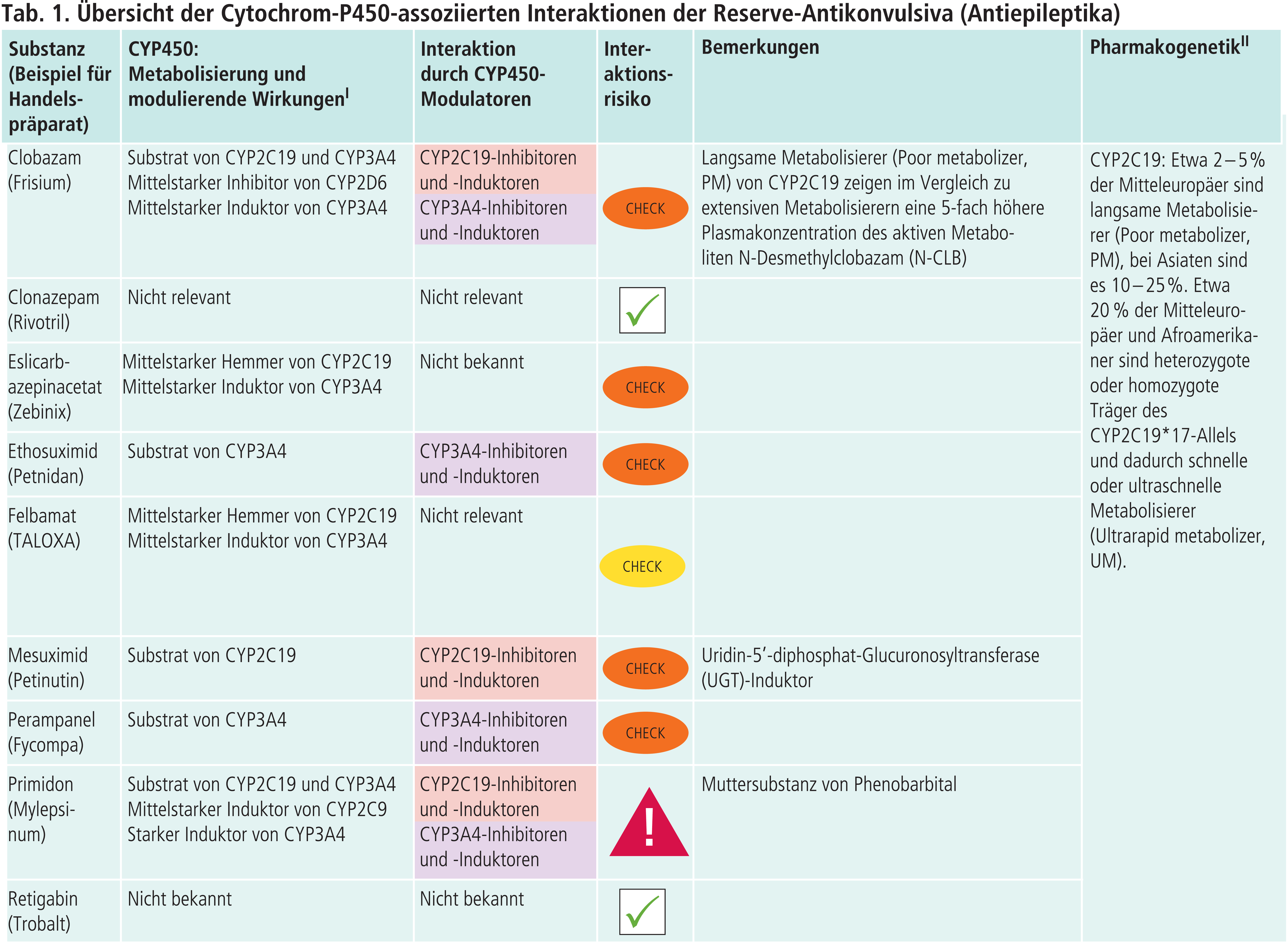
Die beiden Succinimide unterscheiden sich in ihrem Verhalten zu den CYP-Enzymen. Ethosuximid ist ein CYP3A4-Substrat. Die Plasmaspiegel von Ethosuximid sinken in der antikonvulsiven Kombinationstherapie mit potenten CYP3A4-Induktoren wie Carbamazepin, Phenobarbital und Phenytoin (Abb. 2) [16]. Mesuximid kann hingegen pharmakokinetische Interaktionen mit dem CYP2C19-Hemmer Felbamat eingehen (Tab. 1). Eine Verringerung der Mesuximid-Dosis kann notwendig werden [12]. Zudem besitzt Mesuximid induktive Effekte auf die Uridin-5’- diphosphat-Glucuronosyltransferasen (UGT). Die Plasmaspiegel von Lamotrigin und Valproinsäure können sinken [1, 2, 12].
Clobazam und Clonazepam
Benzodiazepine dienen in erster Linie zur akuten Unterbrechung eines epileptischen Geschehens (z.B. Status epilepticus) [18]. Wegen des Risikos von Gewöhnung und Abhängigkeit sollten Benzodiazepin-haltige Arzneimittel nur bei zwingender Indikation und nach sorgfältiger Abwägung des therapeutischen Nutzens in der Langzeitbehandlung eingesetzt werden, zumal bei Dauertherapie die Wirkungsstärke erheblich abnimmt [7, 18]. Eine solche Voraussetzung ist beispielsweise bei der Behandlung der refraktären generalisierten tonisch-klonischen Anfälle bei Patienten mit schwerer myoklonischer Epilepsie im Kindesalter (SMEI, Dravet-Syndrom) gegeben [6]. Clobazam wird durch hepatische Demethylierung unter Beteiligung von CYP3A4 zum aktiven Metaboliten N-Desmethylclobazam (N-CLB) verstoffwechselt. N-CLB wird weiter über CYP2C19 abgebaut. Induktoren von CYP3A4 lassen die Plasmaspiegel von N-CLB steigen. Die Gefahr von Intoxikationen steigt, wenn die Patienten Poor-Metabolizer von CYP2C19 sind. Diese zeigen im Vergleich zu extensiven CYP2C19-Metabolizern eine 5-fach höhere Plasmakonzentration von N-CLB [7]. Vorsicht ist folglich auch geboten, wenn Patienten gleichzeitig potente CYP2C19-Hemmer einnehmen. In der deutschen Fachinformation des Clobazam-haltigen Fertigarzneimittels sind mögliche Wechselwirkungen mit hormonellen Kontrazeptiva nicht erwähnt [7]. Hingegen sollen Patientinnen gemäß der US-amerikanischen Gebrauchsinformation nichthormonale Verhütungsmethoden anwenden. Begründet wird dies mit einer CYP3A4-Induktion, während Interaktionen mit anderen CYP3A4-Substraten als klinisch nicht relevant gewichtet werden [20]. Am Beispiel Clobazam zeigt sich das Problem, dass in klinischen Studien Wechselwirkungen durch weniger potente Induktoren übersehen werden. Zum einen sind Wirkungseintritt und -maximum der Induktion mit mehreren Wochen bis Monaten verglichen mit starken Induktoren deutlich verzögert. Zum anderen ist die Induktion interindividuell unterschiedlich stark ausgeprägt und von der Dosis abhängig. Dies betrifft nicht nur induzierbare CYP-Enzyme, sondern auch die für die Metabolisierung wichtigen Phase-II-Enzyme (z.B. UGT) sowie Transporter (z.B. P-Glykoprotein) [4, 5].
Clonazepam unterliegt nicht relevanten Phase-I-Reaktionen (Tab. 1).
Primidon
Primidon ist die Muttersubstanz von Phenobarbital und wie sein Metabolit ein starker CYP3A4-Induktor (Tab. 1). Zu den Arzneimitteln, die primär über CYP3A4 abgebaut werden, gehören Antiinfektiva, antineoplastische Mittel, Blut-, Herz- und Kreislaufmittel, hormonelle Kontrazeptiva, Immunsuppressiva, Urologika und ZNS-Mittel [19]. Primidon erhöht die hepatische Clearance dieser Substrate („Victim-Drugs“). Es droht ein Therapieversagen wegen erniedrigter AUC-Werte (AUC =Area under the curve, Fläche unter der Konzentrations-Zeit-Kurve) [19]. Auch sollte eine Vitamin-D-Substitution bei Langzeitanwendung von Primidon erwogen werden [10]. Vitamin D wird durch CYP3A4-Induktoren zu inaktiven Metaboliten beschleunigt abgebaut [19].
Sonstige
Felbamat ist zwar ein Substrat von CYP3A4 und CYP2E1, die Hemmung dieser untergeordneten Stoffwechselwege lässt aber keine Folgen in Bezug auf die Pharmakokinetik erwarten [13]. Als mittelstarker Hemmer von CYP2C19 können die Plasmaspiegel von Phenobarbital, Primidon und Phenytoin bei antikonvulsiver Kombinationstherapie steigen. Andererseits beschleunigt Felbamat als CPY3A4-Induktor die Clearance von Carbamazepin und Zonisamid, was gegebenenfalls Dosiserhöhungen zur Folge haben kann.
Perampanel als CYP3A4-Substrat ist ein Victim-Drug, wenn gleichzeitig Induktoren dieses Enzyms verordnet werden. Beispielsweise führte Carbamazepin in einer bei gesunden Probanden durchgeführten Studie zu einer Abnahme der Perampanel-Plasmaspiegel um zwei Drittel [8].
Stiripentol ist indiziert als Zusatztherapie in Verbindung mit Clobazam und Valproinsäure bei Patienten mit Dravet-Syndrom, deren Anfälle mit Clobazam und Valproinsäure nicht angemessen kontrolliert werden können. Metabolisch ist zu beachten, dass Stiripentol als CYP2C19-Inhibitor den Abbau von N-CLB hemmt. Die Interaktion kann zu einem 5-fachen Anstieg des aktiven Metaboliten von Clobazam führen [6].
Sultiam ist ein potenter CYP2C9-Hemmer. In Kombination mit dem CYP2C9-Substrat Phenytoin drohen toxische Plasmaspiegel. Die Komedikation erfordert daher eine besonders strenge Überwachung und häufige Kontrollen des Phenytoin-Plasmaspiegels [11, 17].
Retigabin und Vigabatrin werden CYP-unabhängig metabolisiert (Tab. 1).
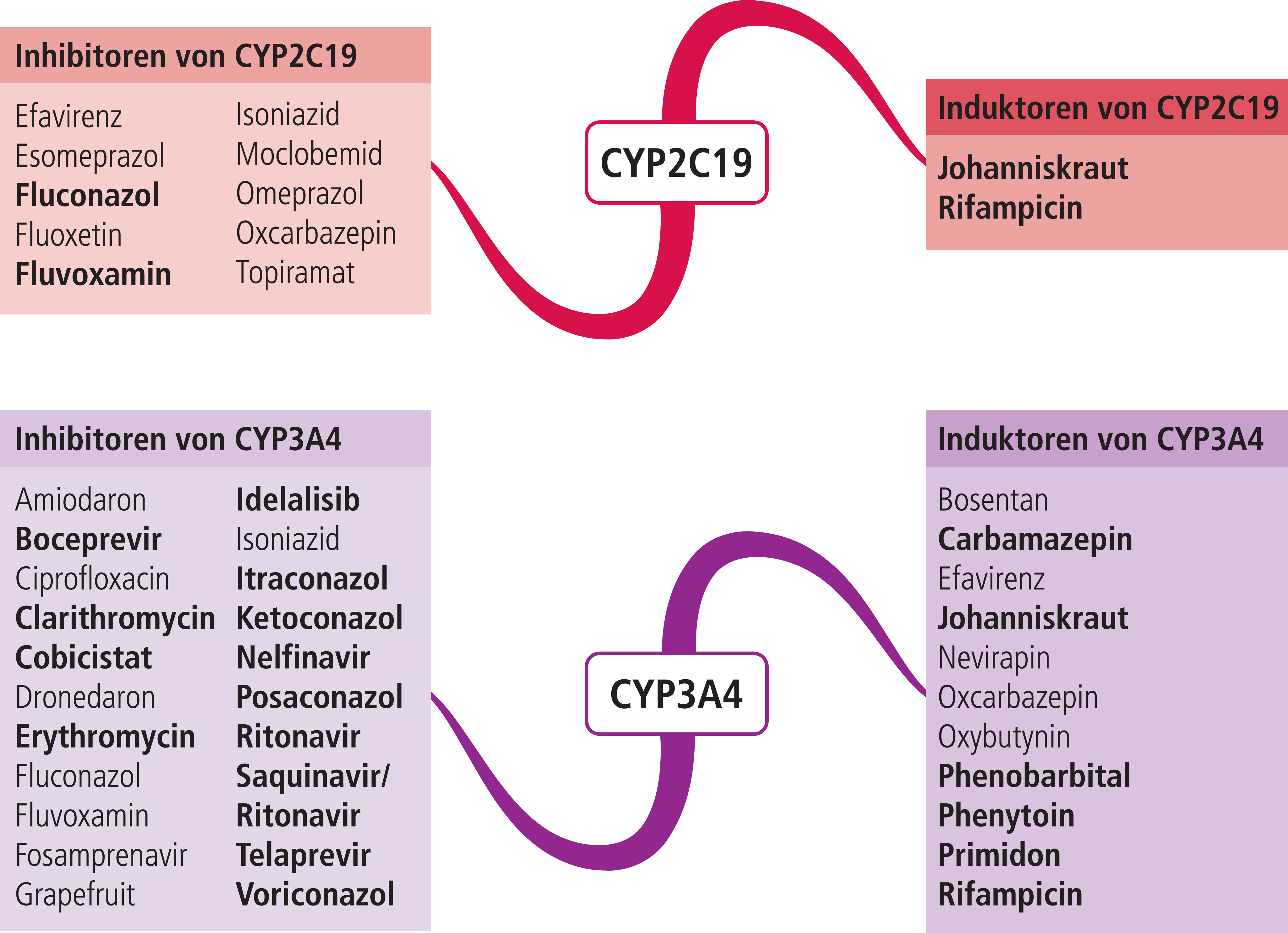
Abb. 2. Auswahl von modulierenden Substanzen (stark wirkende fettgedruckt) mit klinisch relevanter Wirkung auf Cytochrom P450 (CYP) 2C19 und 3A4 (Stand: 12/2015) [Quelle: mediQ-Interaktionsprogramm]

Literatur
1. Besag FM, et al. Methsuximide reduces valproic acid serum levels. Ther Drug Monit 2001;23:694–7.
2. Besag FMC, et al. Methsuximide lowers lamotrigine blood levels: a pharmacokinetic antiepileptic drug interaction. Epilepsia 2000;41:624–7.
3. Brown ME, El Mallakh RS. Role of eslicarbazepine in the treatment of epilepsy in adult patients with partial-onset seizures. Therapeutics and Clinical Risk Management 2010;6:103–9.
4. de Leon J. The effects of antiepileptic inducers in neuropsychopharmacology, a neglected issue. Part I: A summary of the current state for clinicians. Rev Psiquiatr Salud Ment 2015;8:97–115.
5. de Leon J. The effects of antiepileptic inducers in neuropsychopharmacology, a neglected issue. Part II: Pharmacological issues and further understanding. Rev Psiquiatr Salud Ment 2015;8:167–88.
6. Fachinformation Diacomit®. Stand: Juni 2014.
7. Fachinformation Frisium®. Stand: Februar 2015.
8. Fachinformation Fycompa®. Stand: Juni 2015.
9. Fachinformation Inovelon®. Stand: Juni 2013.
10. Fachinformation Mylepsinum®. Stand: November 2014.
11. Fachinformation Ospolot®. Stand: Januar 2014.
12. Fachinformation Petinutin®. Stand: April 2014.
13. Fachinformation Taloxa®. Stand: Dezember 2014.
14. Fachinformation Trileptal®. Stand: September 2014.
15. Fachinformation Zebinix®. Stand: Mai 2015.
16. Giaccone M, Bartolia A, Gatti G, et al. Effect of enzyme inducing anticonvulsants on ethosuximide pharmacokinetics in epileptic patients. Br J Clin Pharmacol 1996;41:575–9.
17. Houghton GW, Richens A. Phenytoin intoxication induced by sulthiame in epileptic patients. J Neurol Neurosurg Psychiatry 1974;37:275–81.
18. Mutschler E, et al. Mutschler Arzneimittelwirkungen. 10. Auflage. Stuttgart: Wissenschaftliche Verlagsgesellschaft Stuttgart, 2013.
19. Petri H. Das Interaktionspotenzial der Antikonvulsiva (Antiepileptika). Krankenhauspharmazie 2015;36:29–33.
20. Prescribing information ONFI®. Stand Dezember 2014.
21. Rocha A, Coelho EB, Sampaio SA, Lanchote VL. Omeprazole preferentially inhibits the metabolism of (+)-(S)-citalopram in healthy volunteers. Br J Clin Pharmacol 2010;70:43–51.
*Nachdruck aus Krankehauspharmazie 2016;37:21–5.
Der Artikel wurde unter Einbeziehung von Diskussionsbeiträgen von Dr. Jörg Brüggmann, Berlin, Prof. Dr. Christoph Hiemke, Mainz, und Dr. Jochen Weber, Bad Wildungen, erstellt.
Holger Petri, Zentral-Apotheke der Wicker Kliniken, Im Kreuzfeld 4, 34537 Bad Wildungen, E-Mail: hpetri@werner-wicker-klinik.de
Psychopharmakotherapie 2016; 23(01)
