Gerd Laux, Haag/München, Bettina Barthel, München, Göran Hajak, Bamberg, Matthias Lemke, Hamburg, und Hans-Peter Volz, Werneck
Depression ist eine komplexe und heterogene Erkrankung mit weitreichenden Folgen für den individuellen Patienten, sein persönliches und berufliches Umfeld und das Gesundheitssystem betreffend. Die 12-Monats-Prävalenz liegt sowohl weltweit als auch in Westeuropa bei etwa 10%, die Lebenszeitprävalenz bei 16 bis 20% mit deutlichen alters- und geschlechtsspezifischen Unterschieden [17, 20, 34, 48]. Als heutiger Therapiestandard gilt neben der Psychotherapie eine individualisierte Pharmakotherapie [7]. 60 bis 70% der Patienten sprechen in der Regel zufriedenstellend auf Antidepressiva an, weniger als 50% erreichen eine Remission [29, 36]. Allerdings setzen etwa 25 bis 50% der Patienten ihre Medikation ohne Wissen des behandelnden Arztes vorzeitig ab [29, 35]. In der Untersuchung von Olfson et al. brachen 42% der amerikanischen Patienten die antidepressive Therapie innerhalb der ersten 30 Tage und 72% innerhalb von 90 Tagen ab [35]. Häufige Ursache für Therapieabbrüche sind unerwünschte Arzneimittelwirkungen wie gastrointestinale Beschwerden, sexuelle Dysfunktion, Gewichtszunahme, das Auftreten anticholinerger Symptome und eine QTc-Verlängerung [3]. Gerade für ältere und komorbide Patienten stellen beispielsweise trizyklische Antidepressiva (TZA) aufgrund ihrer anticholinergen und kardiovaskulären Nebenwirkungen sowie selektive Serotonin-Wiederaufnahmehemmer (SSRI) aufgrund der möglichen Entwicklung einer Hyponatriämie oder Verstärkung der Blutungsgefahr bei Kombinationstherapien ein Risiko dar [1, 7, 32]. Die Verträglichkeit eines Antidepressivums ist daher sowohl für die Behandlungsentscheidung des Arztes als auch für die Compliance der Patienten bedeutsam.
Das Antidepressivum Agomelatin ist ein Melatonin(MT1/MT2-Rezeptor)-Agonist und ein Antagonist am postsynaptischen Serotonin-Subtyp-Rezeptor 5-HT2C [5, 39]. Über die Melatonin-Rezeptoren resynchronisiert das chronobiotisch wirkende Arzneimittel die zirkadiane Rhythmik. Die 5-HT2C-antagonistischen Eigenschaften werden mit einer vermehrten Freisetzung von Dopamin und Noradrenalin spezifisch im frontalen Kortex in Verbindung gebracht. Metaanalysen der Placebo- und aktiv kontrollierten, randomisierten, doppelblinden klinischen Studien (RCTs) bestätigen eine gegenüber Placebo überlegene und mit anderen Antidepressiva vergleichbare antidepressive Wirksamkeit von Agomelatin bei zugleich besserer Verträglichkeit [13, 14, 18, 21, 28, 38, 42, 44].
Die Durchführung von RCTs erfolgt bei eng definierten Patientenkollektiven mit strikten Ein- und Ausschlusskriterien und einem genau festgelegten Therapieregime. In Ergänzung zu den Wirksamkeits- und Verträglichkeitsdaten aus RCTs liefern nichtinterventionelle Studien relevante Informationen für die komplexe Versorgungssituation bei heterogenen Patientenpopulationen, da sie an nichtselektierten Patienten mit der Zieldiagnose unter offenen Bedingungen in der klinischen Praxis durchgeführt werden. Um praxisrelevante Daten an einer großen Zahl komorbider und komedizierter Patienten unter Agomelatin zu sammeln, wurden 2009 bis 2013 vier nichtinterventionelle Studien in fach- und/oder hausärztlichen Arztpraxen in Deutschland durchgeführt: VIVALDI (Valdoxan® improves depressive symptoms and normalizes circadian rhythms) [22–25], VIVALDI-Praxis [26], VITAL (Valdoxan® improves treatment of depression and daytime activity in real life) [27] und VIVRE (Valdoxan® improves depression with anxiety symptoms) [47].
Mit dem Ziel, die Kenntnisse aus der routinemäßigen Anwendung von Agomelatin bei einer großen Patientenzahl der täglichen ärztlichen Praxis zu erweitern, wurden diese vier Studien in einer gepoolten Analyse zusammengefasst. Ein weiteres Ziel der vorliegenden Analyse bestand darin, seltene oder bislang nicht bekannte unerwünschte Arzneimittelwirkungen (UAW) von Agomelatin anhand der großen Patientenzahl besser beurteilen zu können. Aufgrund dosisabhängiger Transaminasenerhöhungen in klinischen Studien wird seit Zulassung von Agomelatin das Monitoring der Lebertransaminasen empfohlen. Als detaillierte Zusatzinformation zu klinischen Studien- und Sicherheitsdaten lag daher ein besonderer Fokus auf der Inzidenz und dem Verlauf von erhöhten Lebertransaminasen unter Behandlung mit Agomelatin.
Patienten und Methoden
In der gepoolten Analyse wurden Daten von insgesamt 9601 Patienten aus vier multizentrischen, nichtinterventionellen Studien mit Agomelatin gepoolt ausgewertet: VIVALDI (Hauptanalyse und Follow-up), VIVALDI-Praxis, VITAL und VIVRE. Diese Studien wurden deutschlandweit in insgesamt 1772 Praxen von Fachärzten für Psychiatrie oder Allgemeinmedizin/praktischen Ärzten/Internisten zwischen 2009 bis 2013 durchgeführt. Die Eckdaten der gepoolten Analyse sind in Tabelle 1 dargestellt. Der Beobachtungszeitraum erstreckte sich in den jeweiligen Studien über mindestens 12 bis maximal 52 Wochen (VIVALDI-Follow-up).
Tab. 1. Eckdaten der gepoolten Analyse und der vier in die Analyse eingeschlossenen, nichtinterventionellen Einzelstudien mit Patientenzahlen der jeweiligen Analyseparameter, Studiendauer, Zeitraum, Arztgruppe und untersuchten Parametern zu antidepressivem Effekt und Verträglichkeit
|
Eckdaten |
Gepoolte Analyse |
Studie |
||||
|
VIVALDI |
VIVALDI-Praxis |
VITAL |
VIVRE |
|||
|
W0–W12 |
Follow-up |
|||||
|
Patientenzahl |
||||||
|
9283 |
3317 |
605 |
1070 |
3005 |
1891 |
|
9283 |
3317 |
605 |
1070 |
3005 |
1891 |
|
9601 |
3324 |
605 |
1070 |
3310 |
1897 |
|
9588 |
3317 |
605 |
1070 |
3310 |
1891 |
|
Beobachtungsdauer |
12 Wo (24 und 52 Wo) |
12 Wo |
52 Wo |
12 Wo |
24 Wo |
12 Wo |
|
Zeitraum |
3/2009–1/2013 |
3/2009–1/2010 |
5/2009–10/2010 |
1/2010–11/2010 |
1/2011–2/2012 |
4/2012–1/2013 |
|
Arztgruppe |
FÄ Spez. HÄ |
FÄ |
Spez. HÄ |
FÄ Spez. HÄ |
FÄ Spez. HÄ |
|
|
Parameter |
||||||
|
Gesamt CGI |
Gesamt CGI svMADRS Circscreen |
Gesamt CGI Circscreen Q-LES-Q-SF |
Gesamt CGI BDI Compliance |
Gesamt CGI PGI SDS COVI |
|
|
Gesamt UAW Labor |
Gesamt UAW Labor |
Gesamt UAW Labor |
Gesamt UAW Labor |
Gesamt UAW Labor |
|
BDI: Beck-Depressionsinventar; CGI: klinischer Gesamteindruck; COVI: Covi-Angst-Skala; FÄ: Fachärzte (Psychiater, Nervenärzte, Neurologen); Gesamt: allgemeine Verträglichkeits-, Effektivitätsbeurteilung durch den Arzt; PGI: Patient Global Impression; Q-LES-Q-SF: Quality of Life Enjoyment and Satisfaction Questionnaire – short form; SDS: Sheehan Disability Scale; spez. HÄ: spezialisierte Hausärzte (Allgemeinmediziner, praktische Ärzte, Internisten); ss: Safety-Set (Sicherheitspopulation); svMADRS: Kurzversion der Montgomery-Åsberg Depression Rating Scale; UAW: unerwünschte Arzneimittelwirkung; UE: unerwünschtes Ereignis
Alle vier nichtinterventionellen Studien wurden von der Freiburger Ethikkommission positiv bewertet, den Bundesbehörden angezeigt, in das internationale Studienregister www.controlled-trials.com eingetragen und publiziert [22–27, 47]. Die Durchführung erfolgte gemäß den Vorgaben des Arzneimittelgesetzes (AMG) und unter Berücksichtigung der Empfehlungen des Bundesinstituts für Arzneimittel und Medizinprodukte (BfArM), der Leitlinien der Deutschen Arbeitsgemeinschaft für Epidemiologie (DAE) zur Sicherung von Guter Epidemiologischer Praxis sowie der Empfehlungen des Verbands der forschenden Arzneimittelunternehmen (VfA) zur Verbesserung der Qualität und Transparenz von nichtinterventionellen Studien. Das Datenmanagement und die Datenanalyse erfolgte durch das unabhängige Statistikinstitut GKM Gesellschaft für Therapieforschung mbH.
In den vier Studien erfolgte jeweils eine prospektive Datenerhebung. In der vorliegenden Analyse wurden ausschließlich solche Daten gepoolt ausgewertet, die in den jeweiligen Einzelstudien in identischer bzw. vergleichbarer Form zu entsprechenden Zeitpunkten erhoben wurden. Bei der Aufnahmevisite (Woche 0) wurden demographische Daten (Alter, Geschlecht, Gewicht, Raucherstatus), die psychiatrische Anamnese (Anzahl bisheriger depressiver Episoden, Dauer der aktuellen Episode, psychiatrische Komorbiditäten und Suizidversuche) und die Therapie (Vorbehandlung mit Antidepressiva, psychotrope Komedikation) dokumentiert. Agomelatin wurde gemäß der Fachinformation in der empfohlenen Dosierung verordnet (25 mg/Tag beim Zubettgehen, bei Bedarf Dosiserhöhung auf 50 mg/Tag) und die Dosierung bei jeder Visite dokumentiert. Der antidepressive Effekt wurde anhand der 7-Punkte-Skala Clinical Global Impression Scale (CGI-I = Improvement bzw. CGI-S = Severity-Scale) beurteilt. Response- (CGI-I ≤2) bzw. Remissionsraten (CGI-S = 1 oder 2) wurden ausgewertet, ebenso die allgemeine Beurteilung des antidepressiven Effekts durch den Arzt. Weiterhin wurden die Daten zur Verträglichkeit einschließlich Inzidenz und Art von UAW analysiert. Auftreten oder Fehlen von UAW wurde bei jeder Visite durch den Arzt dokumentiert. In einem Meldebogen entsprechend geltenden Bestimmungen wurden auftretende UAW an die Arzneimittelsicherheit weitergeleitet und dem BfArM gemeldet. Mit unklaren Eintragungen im Beobachtungsbogen wurde nach Rücksprache mit den behandelnden Ärzten gleichermaßen verfahren. Soweit vorliegend wurden die Lebertransaminasen Alanin-Aminotransferase (ALT = GPT) und Aspartat-Aminotransferase (AST = GOT) gemäß der zum jeweiligen Studienzeitpunkt gültigen Fachinformation zu Studienbeginn, in Woche 6, 12, 24 und 52 inklusive der laborspezifischen Normwerte dokumentiert, sowie zusätzlich nach drei Wochen (VIVRE-Studie). Bei fehlender Eintragung der Labornormwerte wurden empfohlene Normwerte für die Lebertransaminasen ALT und AST mit 50 U/l bzw. 0,83 µmol/l für Männer und 35 U/l bzw. 0,58 µmol/l für Frauen verwendet.
Die Transaminasenwerte ALT (GPT) und AST (GOT) wurden folgendermaßen klassifiziert:
- Normal, innerhalb des Normbereichs (≤ULN [ULN=upper limit of normal range])
- Oberhalb der Norm, aber nicht klinisch relevant (>ULN und ≤3 ULN)
- Oberhalb des 3-fachen Normbereichs und klinisch relevant (>3 ULN)
Der Grenzwert für eine klinisch relevante Erhöhung der Transaminasen (>3 ULN) wurde entsprechend den FDA-Empfehlungen festgelegt [10], was auftretenden, potenziell klinisch signifikanten, abnormen Werten entspricht. Die Transaminasenwerte wurden analog zu den UAW für die drei Behandlungsphasen (W0–12; W12–24 und W24–52) separat ausgewertet.
In die vorliegende Analyse wurden jeweils alle Daten der vier Einzelstudien eingeschlossen, die für einzelne Auswertungen (z.B. Baseline-Daten, Transaminasenwerte, UAW) zum jeweiligen Untersuchungszeitpunkt vorlagen. Hierdurch ergeben sich unterschiedliche Patientenzahlen für die entsprechenden Auswertungen. Baseline-Daten lagen von insgesamt 9283 Patienten vor, dokumentierte Leberwerte zu mindestens einem Untersuchungszeitpunkt im Studienverlauf von insgesamt 9588 Patienten. In die Sicherheitsanalyse (UAW-Erfassung) wurden alle 9601 Patienten eingeschlossen, für die Erfassungsbögen vorlagen, um aufgetretene mögliche UAW bei allen Patienten zu erfassen.
Tabelle 2 gibt eine Übersicht über die in der gepoolten Analyse ausgewerteten Parameter und die Patientenzahlen mit vorliegenden Daten zum jeweiligen Auswertungszeitpunkt.
Tab. 2. Gesamtpopulation der gepoolten Analyse und Anzahl (n) vorliegender Patientendaten zu ausgewerteten Parametern und jeweiligem Untersuchungszeitpunkt in der Hauptanalyse (nach 12 Wochen) sowie der Zusatzauswertungen bei Teilpopulationen (nach 24 bzw. 52 Wochen)
|
Ausgewertete Parameter |
Aufnahmevisite |
Woche 2* |
Woche 6 |
Woche 12# |
Woche 24 |
Woche 52 |
|
Baseline-/Demographische Daten |
n=9283 |
– |
– |
– |
– |
– |
|
Dosierung von Agomelatin |
n=9067 |
n=8654 |
n=8026 |
n=7805 |
n=3202 |
n=539 |
|
Laborparameter |
||||||
|
n=9588 |
n=1324 |
n=6286 |
n=5834 |
n=2547 |
n=315 |
|
n=1305 |
n=6175 |
n=5755 |
n=2505 |
n=312 |
|
|
Unerwünschte Arzneimittelwirkungen |
n=9601 |
n=9601 |
n=9601 |
n=9601 |
n=3915 |
n=605 |
|
Bewertung durch den Arzt |
||||||
|
– |
– |
– |
n=5897 |
n=2882 |
n=579 |
|
– |
– |
– |
n=5793 |
n=2882 |
n=568 |
|
n=9283 +, ++ |
++ n=8996 |
++ n=8501 |
+ n=5497 ++ n=7932 |
+ n=3350 ++ n=3320 |
+ n=562 ++ n=557 |
* VIVRE: W3 anstatt W2, ab 2012 erfolgten gemäß Fachinformation (Stand 3/2012) ALT/AST-Kontrollen zusätzlich nach 3 Wochen (somit erstmalig erfasst in VIVRE); + CGI-S (Clinical Global Impression–Severity Scale); ++ CGI-I (Clinical Global Impression-Improvement Scale); # Bewertung der Effektivität und Verträglichkeit sowie CGI-S erfolgten in der VITAL-Studie bei Studienende (W24) anstatt bei W12
Die Hauptanalyse umfasst die Behandlung über 12 Wochen und schließt die Daten aller vier Studien ein. Aufgrund der unterschiedlichen Studiendauer der Einzelstudien wurden zusätzliche Analysen über 24 Wochen (VIVALDI-Follow-up/VITAL; n=3610) sowie 52 Wochen (VIVALDI-Follow-up; n=605) bei entsprechenden Teilpopulationen durchgeführt. Körpergewicht bzw. BMI wurden gepoolt über 12 Wochen (VIVALDI/VIVALDI-Praxis/VIVRE; n=6217) sowie über 24 Wochen (VITAL; n=2972) analysiert. Für die Zusatzanalysen zur Langzeitverträglichkeit wurde der Zeitraum von Woche 12 bis 24 (VIVALDI-Follow-up/VITAL; n=3915) und von Woche 24 bis 52 (VIVALDI-Follow-up; n=605) ausgewertet.
Die statistische Analyse der gepoolten Daten erfolgte deskriptiv mit SAS® (Version 9.2). Quantitative Variablen wurden durch basisstatistische Kenngrößen wie Mittelwert, Standardabweichung und Median (50%-Quantil) ausgewertet. Für qualitative Daten (z.B. Geschlecht) und kategoriale Variablen (z.B. Skalen-Werte) wurden Häufigkeitsverteilungen (absolute und relative Häufigkeit) berechnet. Nebenwirkungen wurden gemäß MedDRA® kodiert und auf Basis der Kodierungsebenen „system organ class“ und „preferred terms“ ausgewertet. Die gepoolte Analyse der Response- und Remissionsraten gemäß CGI erfolgte in Bezug auf die Gesamtheit aller Patienten mit validen Daten zum jeweiligen Untersuchungszeitpunkt.
Ergebnisse
Patientencharakteristika
In der gepoolten Analyse wurden Baseline-Daten von 9283 Patienten ausgewertet. Die Patientencharakteristika und demographischen Daten sind in Tabelle 3 aufgeführt. Zwei Drittel der Patienten waren Frauen, das mittlere Alter betrug 50,5 Jahre, wobei die Mehrzahl (68,9%) der Patienten älter als 45 Jahre war. Bei knapp zwei Drittel der Patienten lag eine rezidivierende Depression vor. Die aktuelle Episode bestand im Mittel länger als zehn Wochen. In VIVALDI-Praxis war die Episodendauer mit sechs Wochen am kürzesten, in VIVALDI mit knapp 14 Wochen am längsten. 6674 der insgesamt 9283 Patienten (71,9%) hatten eine psychiatrische Komorbidität, in hausärztlichen Praxen war dies am seltensten (8,2% in VIVALDI-Praxis).
Tab. 3. Demographische Daten der in die gepoolte Analyse einbezogenen Patienten (n=9283) im Vergleich zu den Einzelstudien
|
Parameter |
Gepoolte Analyse (n=9283) |
VIVALDI |
VIVALDI-Praxis (n=1070) |
VITAL |
VIVRE |
|
Geschlecht [%] |
|||||
|
34,7 |
35,5 |
34,1 |
34,0 |
35,1 |
|
65,3 |
64,5 |
65,9 |
66,0 |
64,9 |
|
Alter [Jahre] (Mittelwert ± SD) |
50,5±13,4 |
50,5±13,0 |
52,7±14,2 |
50,5±13,6 |
50,3±13,3 |
|
Altersgruppen [%] |
|||||
|
2,9 |
3,1 |
2,2 |
3,1 |
2,8 |
|
28,2 |
29,1 |
26,8 |
27,6 |
28,8 |
|
54,5 |
54,4 |
50,7 |
55,3 |
55,5 |
|
10,2 |
11,0 |
13,0 |
9,3 |
8,4 |
|
4,2 |
2,5 |
7,3 |
4,7 |
4,4 |
|
BMI [kg/m2] (Mittelwert ± SD) |
26,4±4,9 |
26,4±4,9 |
26,6±4,8 |
26,4±4,8 |
26,5±4,9 |
|
Raucherstatus [%] |
|||||
|
27,2 |
28,2 |
29,4 |
25,3 |
27,6 |
|
58,9 |
60,2 |
55,5 |
59,7 |
57,3 |
|
13,9 |
11,7 |
15,1 |
14,9 |
15,0 |
|
Diagnose [%] |
|||||
|
39,8 |
36,4 |
40,6 |
52,9 |
24,8 |
|
60,2 |
63,6 |
59,4 |
47,1 |
75,2 |
|
Anzahl depressiver Episoden in der Anamnese |
|||||
|
3,9±6,1 |
4,5±7,2 |
4,2±7,2 |
3,6±5,4 |
3,2±4,2 |
|
2 |
3 |
2 |
2 |
2 |
|
Dauer der aktuellen depressiven Episode [Wochen] |
|||||
|
10,6±16,4 |
13,9±21,3 |
6,1±7,4 |
8,9±11,1 |
9,8±15,9 |
|
6 |
8 |
4 |
6 |
6 |
|
Suizidversuche [%] |
|||||
|
5,9 |
8,0 |
2,9 |
5,1 |
5,8 |
|
89,6 |
87,5 |
89,9 |
91,5 |
89,8 |
|
4,4 |
4,5 |
7,2 |
3,5 |
4,4 |
|
Begleitende psychiatrische Erkrankungen [%] |
|||||
|
71,9 |
70,4 |
8,2 |
84,4 |
90,7 |
|
28,1 |
29,6 |
91,8 |
15,6 |
9,3 |
|
Vorbehandlung [%]* |
|||||
|
60,1 |
70,2 |
45,0 |
58,2 |
54,0 |
|
31,4 |
49,1 |
19,7 |
27,1 |
28,5 |
|
23,2 |
32,1 |
17,0 |
20,7 |
15,7 |
|
15,2 |
21,0 |
9,6 |
13,2 |
11,5 |
|
14,3 |
24,9 |
7,5 |
10,3 |
11,7 |
|
8,1 |
6,5 |
11,9 |
9,6 |
6,3 |
|
1,6 |
2,9 |
0,6 |
1,4 |
0,5 |
|
Komedikation [%] |
|||||
|
18,9 |
25,8 |
9,1 |
13,1 |
19,9 |
|
31,9 |
30,1 |
31,7 |
4,1 |
39,1 |
Berechnung erfolgt anhand der Patienten mit vorliegenden Daten bei Studienbeginn
*Mehrfachnennung möglich
Psychotrope Komedikation
Von den 9283 Patienten der Gesamtpopulation waren 60,1% (n=5581) bereits mit Antidepressiva vorbehandelt. Der höchste Anteil vorbehandelter Patienten zeigt sich in der Studie VIVALDI (70,2%), der niedrigste in VIVALDI-Praxis (45,0%). Von den vorbehandelten Patienten hatten 31,4% SSRI und 23,2% trizyklische Antidepressiva erhalten. Mirtazapin, SSNRI (selektive Serotonin-Noradrenalin-Wiederaufnahmehemmer), Johanniskraut und MAO-(Monoaminoxidase-)Inhibitoren wurden seltener verwendet. Bei 18,9% der Gesamtpopulation wurden die zuvor verordneten Antidepressiva zusätzlich zu Agomelatin weitergeführt.
Insgesamt ein Drittel aller Patienten erhielt zu Studienbeginn weitere psychotrope Substanzen, am häufigsten sogenannte Z-Substanzen wie beispielsweise Zolpidem oder Zopiclon (13,0%; n=1204), gefolgt von Benzodiazepinen (10,1%; n=933), Antipsychotika/Neuroleptika (5,7%; n=531) und Antikonvulsiva (2,2%; n=205).
Dosierung von Agomelatin im Therapieverlauf
Bei nahezu allen Patienten (98,4%; n=8922) wurde die Behandlung mit Agomelatin 25 mg/Tag begonnen. 1,4% der Patienten (n=125) erhielten bereits bei Therapiebeginn zwei Tabletten Agomelatin (50 mg/Tag). Der Anteil der mit zwei Tabletten behandelten Patienten stieg im weiteren Verlauf auf 25,4% (n=2197) in Woche 2 und 31,8% (n=2549) in Woche 6. Ab Woche 6 blieb dieser Anteil nahezu unverändert (Abb. 1).
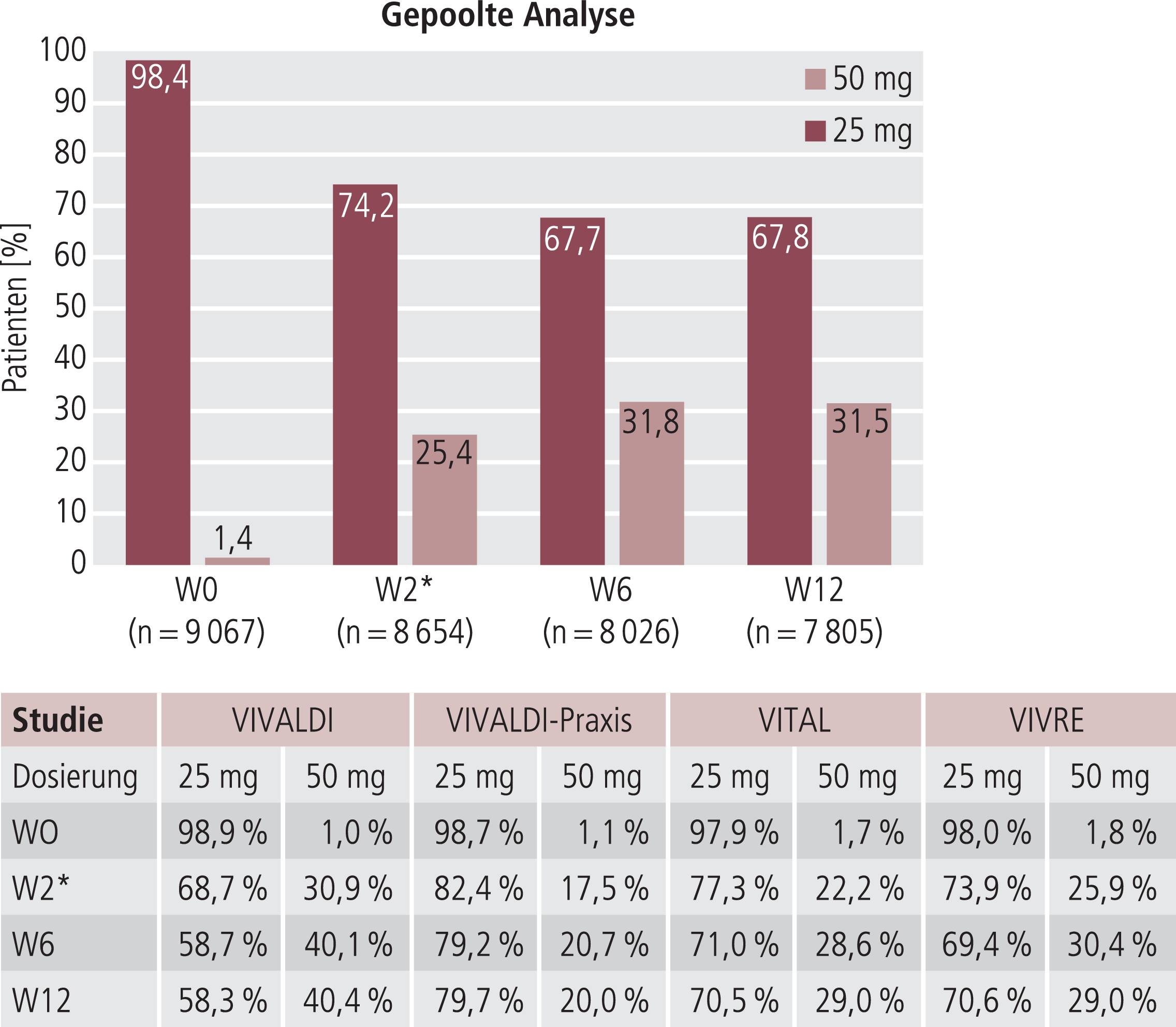
Abb. 1. Dosierung von Agomelatin mit Anteil an Patienten unter 25 mg bzw. 50 mg (1 bzw. 2 Tabletten) im Therapieverlauf über 12 Wochen gepoolt sowie in den Einzelstudien. * In der VIVRE-Studie Dokumentation in W3 statt in W2 (VIVALDI, VIVALDI-Praxis, VITAL). (Differenz zu 100% = andere Dosierung [z.B. 1/2 Tbl, 1 1/2 oder >2 Tbl.])
Verträglichkeit
Für die gepoolte Analyse konnten Daten von insgesamt 9601 Patienten zu Häufigkeit und Art der UAW einschließlich der schwerwiegenden UAW (sUAW) und von 9588 Patienten die Laborparameter ausgewertet werden (Tab. 1). Im Zeitraum von Woche 0 bis 12 wurden bei 5,32% aller Patienten (511 von 9601) insgesamt 859 UAW (8,9%) dokumentiert (Tab. 4a). Bei Patienten mit psychotroper Komedikation (n=3048) trat dies bei 5,28% (n=161), ohne psychotrope Komedikation (n=6553) bei 5,34% (n=350) der Patienten auf. Die in der Gesamtpopulation am häufigsten beobachteten UAW waren Kopfschmerz, Übelkeit, Schwindel und Unruhe. Die Häufigkeit dieser UAW war bei Patienten mit und ohne psychotrope Komedikation vergleichbar. Ein Anstieg der Lebertransaminasen unter Behandlung mit Agomelatin wurde bei 30 Patienten (0,3%) dokumentiert und hiervon bei 23 Patienten als UAW klassifiziert (Patienten mit bzw. ohne psychotrope Komedikation in 0,33% bzw. 0,32%).
Während der Therapie über 12 Wochen wurden bei 18 Patienten (0,19%) insgesamt 33 sUAW (0,3%) dokumentiert (Tab. 4b). Suizidale Gedanken wurden in 0,09% (n=9) angegeben, in vielen Fällen ohne kausalen Zusammenhang zur Medikation [23]. In der Gesamtpopulation der vorliegenden Analyse trat kein Todesfall auf und es kam zu keiner dauerhaften Beeinträchtigung.
Tab. 4. Verträglichkeit von Agomelatin in der gepoolten Auswertung des Safety-Analysis-Set (SAS) in der Gesamtpopulation (Woche 0–12) sowie den jeweiligen Teilpopulationen (Woche 12–24 und Woche 24–52) im Behandlungsverlauf
a) Anzahl (n) und Anteil (%) der Patienten mit den häufigsten gemeldeten unerwünschten Arzneimittelwirkungen (UAW)
|
UAW* sortiert nach PT (Preferred Term) |
W0–W12 |
W12–W24 |
W24–W52 |
|||
|
Patienten |
Patienten |
Patienten |
||||
|
[n] |
[%] |
[n] |
[%] |
[n] |
[%] |
|
|
Gesamt |
511 |
5,32 |
19 |
0,49 |
6 |
0,99 |
|
Kopfschmerz |
88 |
0,92 |
4 |
0,10 |
– |
– |
|
Übelkeit |
72 |
0,75 |
1 |
0,03 |
1 |
0,17 |
|
Schwindel |
52 |
0,54 |
4 |
0,10 |
– |
– |
|
Unruhe |
43 |
0,45 |
1 |
0,03 |
– |
– |
|
Diarrhö |
35 |
0,36 |
– |
– |
– |
– |
|
Transaminasenerhöhungen (>3 ULN) |
30 |
0,30 |
1 |
0,03 |
1 |
0,17 |
|
Müdigkeit |
29 |
0,30 |
1 |
0,03 |
1 |
0,17 |
|
Schwitzen |
26 |
0,27 |
– |
– |
1 |
0,17 |
|
Schlafstörungen |
26 |
0,27 |
3 |
0,08 |
1 |
0,17 |
|
Oberbauchbeschwerden |
18 |
0,19 |
2 |
0,05 |
– |
– |
|
Suizidgedanken |
18 |
0,19 |
– |
– |
– |
– |
|
Gamma-GT |
5 |
0,05 |
1 |
0,03 |
1 |
0,17 |
* Mehrfachnennungen möglich; W: Woche; ULN: Upper limit of normal range (Normalbereich)
b) Anzahl (n) und Anteil (%) aller Patienten mit schwerwiegender unerwünschter Arzneimittelwirkung (sUAW) sowie Anzahl der dokumentierten sUAW
|
sUAW * |
W0–W12 |
W12–W24 |
W24–W52 |
||||||
|
sUAW [n] |
Patienten |
sUAW [n] |
Patienten |
sUAW [n] |
Patienten |
||||
|
[n] |
[%] |
[n] |
[%] |
[n] |
[%] |
||||
|
Gesamt |
33 |
18 |
0,19 |
3 |
2 |
0,05 |
– |
– |
– |
|
Durchfall |
1 |
1 |
0,01 |
– |
– |
– |
– |
– |
– |
|
Allgemeine Beschwerden |
2 |
2 |
0,01 |
– |
– |
– |
– |
– |
– |
|
Leberwerterhöhungen |
2 |
2 |
0,01 |
– |
– |
– |
– |
– |
– |
|
Kopfschmerz |
1 |
1 |
0,01 |
– |
– |
– |
– |
– |
– |
|
Schläfrigkeit |
1 |
1 |
0,01 |
– |
– |
– |
– |
– |
– |
|
Psychiatrische Beschwerden |
25 |
13 |
0,14 |
– |
– |
– |
– |
– |
– |
|
Angst |
2 |
2 |
0,02 |
– |
– |
– |
– |
– |
– |
|
Depression |
2 |
2 |
0,02 |
– |
– |
– |
– |
– |
– |
|
Ruhelosigkeit |
2 |
2 |
0,02 |
– |
– |
– |
– |
– |
– |
|
Schlafstörungen |
2 |
2 |
0,02 |
– |
– |
– |
– |
– |
– |
|
Suizidale Gedanken |
9 |
9 |
0,09 |
– |
– |
– |
– |
– |
– |
|
Andere# |
8 |
8 |
0,08 |
– |
– |
– |
– |
– |
– |
|
Hospitalisierung |
1 |
1 |
0,01 |
– |
– |
– |
– |
– |
– |
|
Bradykardie |
– |
– |
– |
1 |
1 |
0,03 |
– |
– |
– |
|
Hepatobiliäre Störung |
1 |
0,03 |
|||||||
|
Hepatitis |
– |
– |
– |
1 |
– |
– |
– |
||
|
Ikterus |
1 |
||||||||
* Mehrfachnennungen möglich; W: Woche; #Jeweils eine sUAW-Meldung (entspr. 0,01%) zu Aggression, Verwirrtheit, Halluzination, dissoziativen Gedanken, Schlaflosigkeit, manische Stimmung, Albträume, Zwangsgedanken
Zur Beurteilung des zeitlichen Auftretens von unerwünschten Arzneimittelwirkungen unter Agomelatin wurden Inzidenz und Art der UAW/sUAW sowie die Laborparameter zusätzlich zur Hauptanalyse über 12 Wochen ebenfalls im Zeitraum von Woche 12 bis 24 (VIVALDI-Follow-up und VITAL; n=3915) und Woche 24 bis 52 (VIVALDI-Follow-up, n=605) ausgewertet. Die in den drei unterschiedlichen Zeiträumen aufgetretenen UAW und sUAW sind in Tabelle 4 dargestellt. Die Häufigkeit der meisten UAW nahm nach Woche 12 deutlich ab; viele der in der Akuttherapie berichteten UAW traten im weiteren Verlauf nicht mehr auf. Von Woche 12 bis 24 wurden bei 19 Patienten (0,49% von 3915) insgesamt 28 UAW dokumentiert. Bei zwei Patienten (0,05% von 3915) traten in dieser Zeit drei schwerwiegende UAW auf, ein Fall einer Bradykardie (0,03%) und eine hepatobiliäre Störung (0,03%) mit Hepatitis und Ikterus. Der Fall der hepatobiliären Störung wurde bei einer 52-jährigen Frau berichtet. Als Differenzialdiagnose wurde eine Medikamenten-induzierte- oder Autoimmunhepatitis angegeben. Nach Absetzen von Agomelatin war die Symptomatik reversibel. Die Patientin erholte sich ohne weiter bestehende Beeinträchtigung.
Die optionale Verlängerungsphase der VIVALDI-Studie (Follow-up) erfolgte über 12 bis 52 Wochen. Im Behandlungszeitraum von Woche 24 bis 52 wurden bei sechs Patienten (0,99% von 605) UAW beschrieben. Kopfschmerz, Schwindel und Unruhe wurden nicht mehr beobachtet. Zudem traten zwischen Woche 24 bis 52 keine sUAW auf.
Unter Behandlung mit Agomelatin traten keine relevanten Gewichtsveränderungen auf. Sowohl über 12 Wochen als auch im weiteren Verlauf der Behandlung blieben Körpergewicht und BMI annähernd stabil. Bei Studienbeginn betrug das mittlere Gewicht 76,9±15,7 kg, nach 12 Wochen 77,0±15,5 kg (Median jeweils 75). Die entsprechenden Werte für den BMI lagen bei 26,4±4,9 kg/m2 (W0) bzw. 26,5±4,8 kg/m2 (W12). Auch nach 24-wöchiger Behandlung in der VITAL-Studie zeigten Körpergewicht (76,8±15,0 kg) und BMI (26,4±4,6 kg/m2) keine relevanten Veränderungen gegenüber Baseline (76,7±15,5 kg bzw. 26,3±4,7 kg/m2).
Veränderung der Leberwerte
Die Lebertransaminasen wurden bei Studienbeginn für 78,4% (ALT-Werte) bzw. 76,4% (AST-Werte) aller Patienten dokumentiert. Hiervon waren ALT und AST bei 88,4% bzw. 90,8% der Patienten im Normbereich (≤ULN), bei 11,4% bzw. 9,0% zeigte sich eine leichte Erhöhung unterhalb der 3-fachen Norm (≤3 ULN), bei 0,2% bzw. 0,1% wurde eine klinisch relevante Erhöhung bereits vor Behandlungsbeginn dokumentiert (≥3 ULN). Der Anteil an Patienten mit normalen Transaminasenwerten blieb im Behandlungsverlauf über 12 Wochen sowie 6 bzw. 12 Monaten weitgehend stabil. In Tabelle 5 sind die Transaminasenwerte im Verlauf der Behandlung dargestellt.
Tab. 5. Patienten mit dokumentierten Lebertransaminasenwerten (ALT =GPT bzw. AST =GOT) im Behandlungsverlauf sowie Anzahl (n) und Anteil (%) der Patienten mit Normwerten, leicht erhöhten oder klinisch relevant erhöhten Transaminasenwerten
|
ALT (GPT) |
W0 |
W3 * |
W6 |
W12 |
W24 |
W52 |
||||||
|
n |
% |
n |
% |
n |
% |
n |
% |
n |
% |
n |
% |
|
|
ALT ≤ULN |
6644 |
88,4 |
1191 |
90,0 |
5482 |
87,2 |
5057 |
86,7 |
2232 |
87,6 |
289 |
91,7 |
|
ULN<ALT ≤3 ULN |
860 |
11,4 |
128 |
9,7 |
788 |
12,5 |
761 |
13,0 |
311 |
12,2 |
25 |
7,9 |
|
ALT >3 ULN |
13 |
0,2 |
5 |
0,4 |
16 |
0,3 |
16 |
0,3 |
4 |
0,2 |
1 |
0,3 |
|
AST (GOT) |
W0 |
W3 * |
W6 |
W12 |
W24 |
W52 |
||||||
|
n |
% |
n |
% |
n |
% |
n |
% |
n |
% |
n |
% |
|
|
AST ≤ULN |
6651 |
90,8 |
1194 |
91,5 |
5506 |
89,2 |
5080 |
88,3 |
2280 |
91,0 |
289 |
92,6 |
|
ULN<ALT ≤3 ULN |
660 |
9,0 |
111 |
8,5 |
659 |
10,7 |
667 |
11,6 |
224 |
8,9 |
23 |
7,4 |
|
AST >3 ULN |
10 |
0,1 |
0 |
0,0 |
10 |
0,2 |
8 |
0,1 |
1 |
0,0 |
0 |
0,0 |
ULN: Upper limit of normal range (oberer Normbereich); >ULN und ≤3 ULN: Oberhalb der Norm aber nicht klinisch relevant; >3 ULN: Oberhalb des 3-fachen Normbereichs gilt als klinisch relevante Erhöhung. * Transaminasenkontrollen nach 3 Wochen wurden erstmalig in VIVRE gemäß Fachinformation (3/2012) erfasst.
Insgesamt wurden bei 0,5% (n=49) aller Patienten erhöhte Transaminasenwerte >3 ULN dokumentiert, wovon bei 0,2% (n=19) bereits klinisch relevant erhöhte ALT/AST-Werte bei Studienbeginn vorlagen (Tab. 6a). Somit zeigten unter Agomelatin 0,3% (n=30) aller Patienten einen ALT- und/oder AST-Anstieg (>3 ULN). Bei 23 dieser Patienten (0,24%) wurde ein kausaler Zusammenhang durch den behandelnden Arzt zumindest als möglich eingestuft (klassifiziert als UAW). Von diesen 23 Patienten waren 78,2% zwischen 25 bis 65 Jahre und 4,4% älter als 75 Jahre. Transaminasenerhöhungen traten vorwiegend innerhalb der ersten 12 Wochen auf, mehr als zwei Drittel dieser Patienten (69,6%) erhielten eine Komedikation (Tab. 6b).
Tab. 6. Patienten mit dokumentierten unerwünschten Arzneimittelwirkungen (UAW) einer Leberschädigung in Form von Transaminasenerhöhungen (ALT und/oder AST >3-fach über dem Normbereich [>3 ULN]).
Tab. 6a. Gesamtzahl an Patienten mit Transaminasenerhöhungen (ALT/AST >3 ULN), Patienten mit vorbestehenden Erhöhungen (bereits bei Baseline) sowie unter Agomelatin-Behandlung auftretende Erhöhungen (mit/ohne kausalen Zusammenhang). Berechnung als Anteil (%) bezogen auf die Gesamtpopulation sowie ausschließlich auf Patienten mit allen vorliegenden Transaminasenwerten im Behandlungsverlauf (W0–12) („per Protokoll“)
|
ALT- und/oder AST-Erhöhungen >3 ULN |
Patienten |
Bezugspopulation für %-Berechnung |
|
|
Gesamtpopulation |
Per Protokoll (ALT =5061; AST =4956) |
||
|
Unter Behandlung |
30 |
0,31% |
0,60% |
|
UAW (mit zumindest möglicher Kausalität) |
23 |
0,24% |
0,46% |
|
Keine UAW (ohne Kausalitätsbeziehung) |
7 |
0,07% |
0,14% |
|
Bereits bei Baseline |
19 |
0,19% |
0,38% |
|
Gesamtanzahl |
49 |
0,51% |
0,98% |
UAW: Unerwünschte Arzneimittelwirkung; >3 ULN: oberhalb des 3-fachen Normbereichs gilt als klinisch relevant
Tab. 6b. Charakteristika der 23 Patienten mit dokumentierten UAW einer Leberschädigung in Form von Transaminasenerhöhungen (>3-fach oberhalb Normbereich [>3 ULN]); Berechnung auf Datenbasis der Pharmakovigilanz-Patientenberichte
|
Patientencharakteristika (n=23) |
n |
% |
|
|
Geschlecht |
|
3 |
13,0 |
|
20 |
87,0 |
|
|
Alter [Jahre] |
|
0 |
– |
|
7 |
30,4 |
|
|
11 |
47,8 |
|
|
4 |
17,4 |
|
|
1 |
4,4 |
|
|
Dosierung |
|
13 |
56,5 |
|
6 |
26,1 |
|
|
3 |
13,0 |
|
|
1 |
4,4 |
|
|
Einnahmedauer bis zum Auftreten der UAW |
|
2 |
8,7 |
|
1 |
4,4 |
|
|
7 |
30,4 |
|
|
2 |
8,7 |
|
|
9 |
39,1 |
|
|
1 |
4,4 |
|
|
1 |
4,4 |
|
|
Komedikation |
|
16 |
69,6 |
|
3 |
13,0 |
|
|
4 |
17,4 |
|
|
Reversibilität |
|
19 |
82,6 |
|
1 |
4,4 |
|
|
3 |
13,0 |
|
k. A.: Keine Angabe
Ab Behandlungswoche 12 zeigte sich bei keinem Patienten mit normalen oder leicht erhöhten Werten ein klinisch relevanter Anstieg von ALT oder AST auf >3 ULN.
Die Verträglichkeit von Agomelatin wurde bei 95,5% der Patienten in Woche 12 als sehr gut oder gut bewertet, in Woche 24 auf der Basis der VITAL-Daten bei 97,3% und nach 12 Monaten (Vivaldi-Follow-up) bei 97,5% der Patienten.
Veränderung der depressiven Symptomatik
Für die gepoolte Analyse der Effektivitätsdaten wurden die zu jedem Untersuchungszeitpunkt erhältlichen Daten ausgewertet. Im Behandlungszeitraum Woche 0 bis 12 kam es zu einer kontinuierlichen Verbesserung des Schweregrads der Depression (CGI-S-Gesamtwert). Nach 12 Wochen konnten Daten von 5497 Patienten (VIVALDI, VIVALDI-Praxis und VIVRE) eingeschlossen werden, da in der VITAL-Studie nach 12 Wochen lediglich der CGI-I erhoben wurde. Nach 12-wöchiger Behandlung mit Agomelatin verbessert sich der mittlere CGI-S-Wert von 4,7±0,8 zu Beginn (5=Patient ist krank) auf 3,0±1,3 (3=Patient ist nur leicht krank) (Abb. 2a). Insgesamt zeigt sich bei 81% der Patienten eine Verbesserung des CGI-S-Mittelwerts. Die gepoolten Daten von VIVALDI-Follow-up und VITAL (n=3340) zeigen nach sechs Monaten (W24) eine Verbesserung bei 82,4% der Patienten entsprechend einer Abnahme von 4,7±0,8 (W0) auf 2,8±1,3 (Abb. 2).
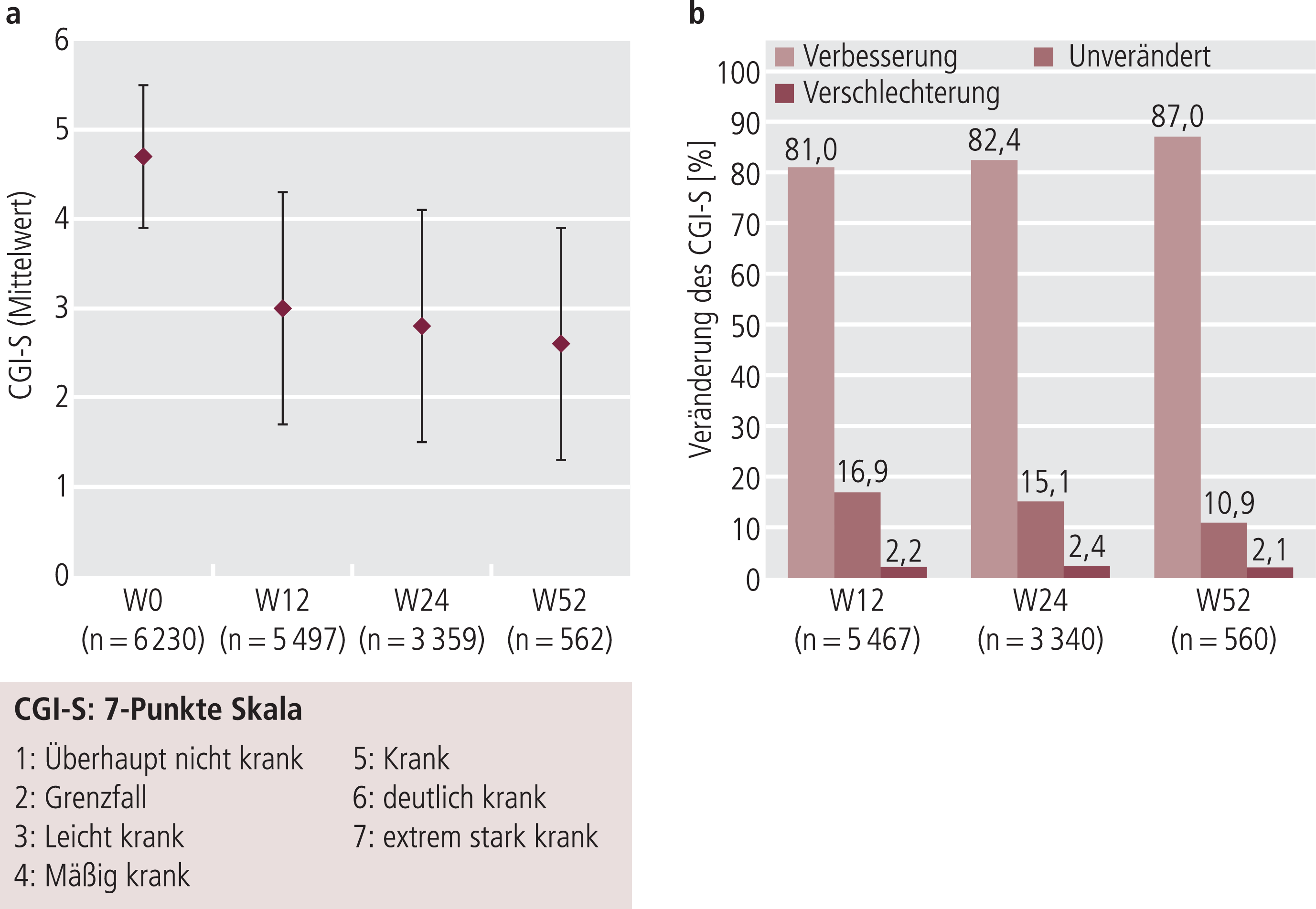
Abb. 2. Verbesserung des Schweregrades der Depression (mittels CGI-S) unter Agomelatin im Therapieverlauf über 12 Wochen (VIVALDI, VIVALDI-Praxis, VIVRE), 24 Wochen (VITAL, VIVALDI-Follow-up) und 52 Wochen (Follow-up); Auswertung anhand vorliegender Patientendaten zu jeweiligem Untersuchungszeitpunkt; a) Abnahme des CGI-S-Gesamtwerts von 4,7 (krank) zu 2,6 (leicht krank – grenzwertig erkrankt); b) Anteil der Patienten (%) mit Verbesserung, ohne Veränderung oder Verschlechterung der Symptomatik im Vergleich zu Studienbeginn (Woche 0)
24,3% der Patienten wurden nach zwei Wochen, 63,0% nach 6 und 78,7% nach 12 Wochen als Responder (CGI-I ≤2) klassifiziert. 12 Wochen nach Therapiebeginn erfüllten 34,5% der Patienten die Kriterien einer Remission (CGI-S: 1 oder 2). In Woche 24 betrug die Remissionsrate 38,1% (Abb. 3).
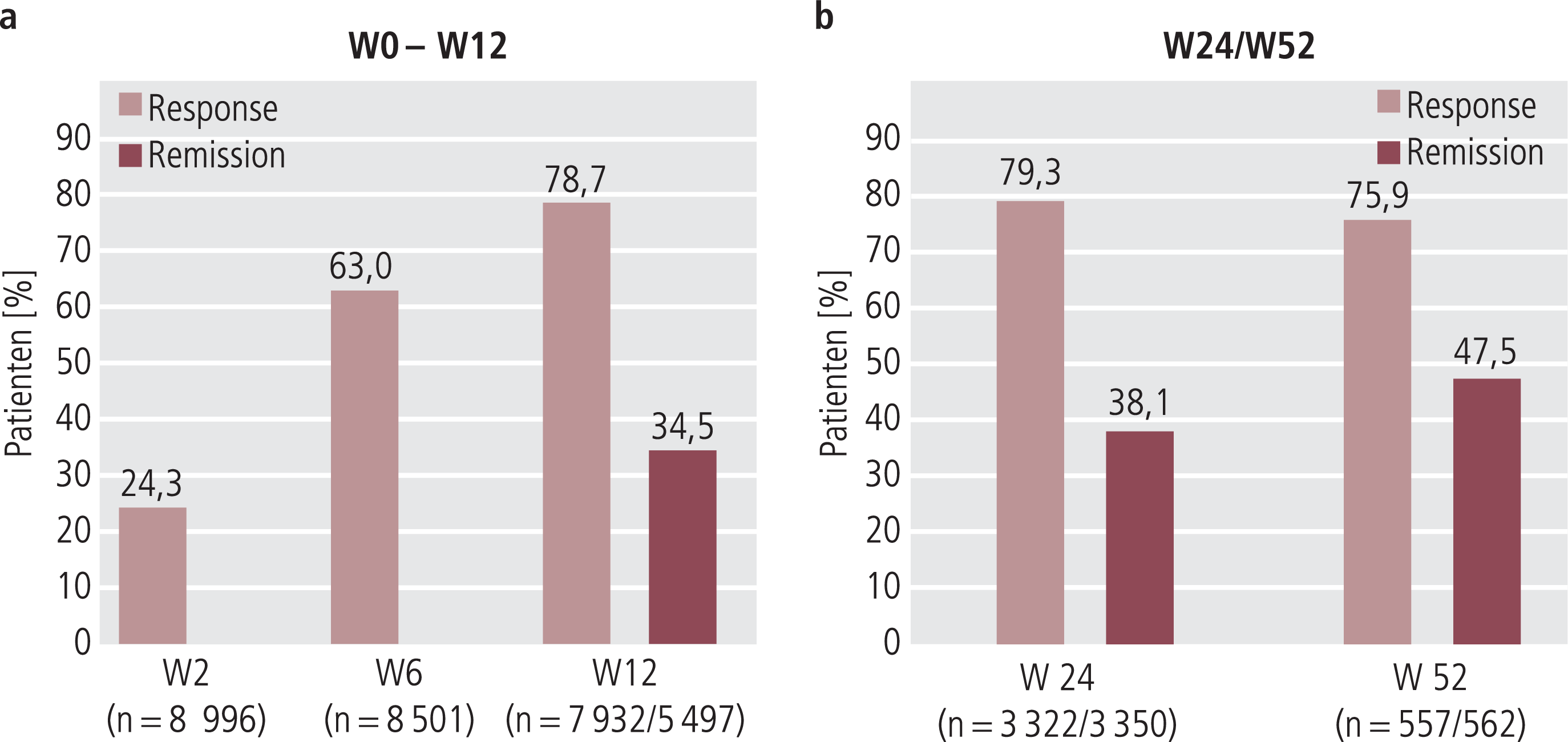
Abb. 3. Antidepressiver Effekt von Agomelatin anhand von Response und Remissionsraten (CGI) im Behandlungsverlauf (Response: CGI-I ≤2; Remission: CGI-S =1 oder 2). Auswertung anhand vorliegender Patientendaten zu jeweiligem Untersuchungszeitpunkt. a) In der Gesamtpopulation über 12 Wochen und b) in Teilpopulationen über 24 und 52 Wochen
Nach 12 Wochen bewerteten die behandelnden Ärzte den antidepressiven Effekt von Agomelatin bei 76,6% der Patienten als sehr gut oder gut. Auch im Langzeitverlauf zeigte sich auf Basis der VITAL-Daten nach 24 Wochen bei 84,1% der Patienten eine sehr gute/gute Effektivität, ebenso nach 52 Wochen in der Follow-up-Phase der VIVALDI-Studie (84,5%).
Diskussion
In der vorliegenden gepoolten Analyse wurden vier nichtinterventionelle Studien zwischen 2009 und 2013 [22–27, 47] zusammengefasst ausgewertet, um anhand der großen Patientenzahl – einschließlich älterer, komorbider und komedizierter Patienten – Erkenntnisse aus dem Praxisalltag über einen Zeitraum von bis zu 52 Wochen zu gewinnen.
Anhand der demographischen Daten wird deutlich, dass es sich um eine für die ärztliche Praxis repräsentative Population handelt. Die Patienten waren überwiegend vorbehandelt und etwa drei Viertel litten an mindestens einer psychiatrischen Komorbidität. Im Vergleich der Einzelstudien wird der ausgeprägtere Schweregrad der Depression in Facharztpraxen deutlich, was sich an psychiatrischer Komorbidität, Anzahl und Dauer der depressiven Episoden sowie vorangegangenen Suizidversuchen zeigt (Tab. 3).
Verträglichkeitsprofil – Leberfunktion
In allen vier in die vorliegende Analyse einbezogenen Studien wurden Transaminasenwerte dokumentiert, um einen möglichen Einfluss von Agomelatin auf die Leberfunktion zu untersuchen. Wie die gepoolte Auswertung der Daten zeigt, liegen alle entsprechend der Fachinformation empfohlenen Transaminasenwerte bei gut der Hälfte aller Patienten vor, ein Baseline- und mindestens ein Folgewert bei etwa zwei Drittel der Patienten. Klinisch relevante Transaminasenerhöhungen (>3 ULN) werden nach 6 bzw. 12 Wochen mit jeweils 0,3% (ALT) und 0,2% bzw. 0,1% (AST) gelegentlich beobachtet, bei Patienten mit normalen Ausgangswerten ist die Häufigkeit noch geringer (ALT: 0,2%; AST: 0,1%). Bei insgesamt 0,5% aller Patienten (n=49) wurden Erhöhungen der ALT- und/oder AST-Werte (>3 ULN) dokumentiert, wovon allerdings 19 Patienten (0,2%) diese bereits vor Behandlungsbeginn aufwiesen. Gemäß aktualisierter Fachinformation besteht inzwischen eine Kontraindikation für diese Patienten [9]. Erhöhte Transaminasen normalisierten sich in der Regel nach Absetzen von Agomelatin, teilweise auch bei weiterer Einnahme, was Daten aus RCTs bestätigen [42, 49]. Die bei einem Patienten dokumentierte Hepatitis mit Ikterus trat nach insgesamt 10-wöchiger Behandlung mit Agomelatin 50 mg/Tag auf (Dosiserhöhung erfolgte nach zweieinhalb Wochen). Außer zu Therapiebeginn mit leicht auffälligen Laborwerten (Cholesterol- und LDH-Erhöhungen, AST im Normbereich und ALT-Wert nicht vorliegend) erfolgten Laborkontrollen erst bei Auftreten klinischer Symptome. Die Symptomatik der Hepatitis war nach Absetzen von Agomelatin ohne fortbestehende Beeinträchtigungen der Patientin vollständig reversibel. Dieser Fall verdeutlicht, dass Transaminasenbestimmungen bei Patienten als frühes Anzeichen einer Leberfunktionsbeeinträchtigung genutzt werden sollten und im Zeitverlauf einer medikamentösen Behandlung als Risikoindikator dienen und eine schwere Leberschädigung verhindern können. In klinisch-kontrollierten Studien an nahezu 8000 Patienten unter Agomelatin trat kein Fall von Hepatitis auf, was die Bedeutung der Transaminasenkontrollen ebenfalls unterstreicht.
Der Vergleich der aus Zulassungsdaten und zahlreichen weiteren RCTs ermittelten Transaminasenerhöhungen mit den vorliegenden gepoolten Daten eines großen Patientenkollektivs zeigt, dass die Inzidenz potenziell leberschädigender UAW unter Agomelatin im Versorgungsalltag, insbesondere auch in Form von reversiblen Transaminasenerhöhungen, seltener beobachtet wird. Die Rekrutierungspraxis von Studienpatienten mit vorbestehenden Risikofaktoren in RCTs, beispielsweise in US-amerikanischen Studien, könnte für die höheren Inzidenzen mitverantwortlich sein [31, 49]. Als weitere Erklärung wird das enge klinische Monitoring bei RCTs und die damit verbundene höhere Melderate genannt. Die geringere Häufigkeit von Transaminasenerhöhungen in der vorliegenden Analyse bestätigt sich allerdings auch bei einer Berechnung bezogen auf Patienten mit vollständig vorliegenden Transaminasenwerten gemäß Fachinformationsempfehlung (ALT: n=5061; AST: n=4956). Bei dieser Berechnung (entsprechend „per Protokoll“) ergibt das für Patienten mit dokumentierter UAW einer Transaminasenerhöhung (n=23 [0,46%]) sowie für die Gesamtzahl einschließlich aller Patienten mit Baseline-Erhöhungen (n=49 [0,98%]) (Tab. 6a) eine unter der in klinischen Studien beobachteten Häufigkeit.
Noch seltenere Meldungen von Leberwertveränderungen ergab eine Analyse von Spontanmeldungen [11]. Gahr et al. führten eine Datenbank-Recherche des Bundesinstituts für Arzneimittel und Medizinprodukte (BfArM) durch, um Spontanmeldungen zu leberschädigenden Nebenwirkungen unter Agomelatin-Behandlung zu untersuchen. In diese Datenbank-Analyse wurden nur Patienten mit Normwerten vor Therapiebeginn eingeschlossen. Im Zeitraum von Mai/2009 bis Januar/2013 erfolgten 58 Spontanmeldungen zu hepatischen UAW im Zusammenhang mit Agomelatin. Bei 79% der Fälle (n=46) handelte es sich um einen asymptomatischen Anstieg der Lebertransaminasen, bei 10% (n=6) wurde eine Hepatitis gemeldet [11], davon ein Fall einer toxischen Hepatitis. Eine Bewertung der Kausalität ist anhand dieser Datenbankanalyse schwierig, worauf die Autoren selbst hinweisen. Da es sich laut BfArM bei gelisteten Spontanmeldungen um „Rohdaten“ handelt und kein Bezug zur Verordnungshäufigkeit stattfindet, können auf dieser Datenbasis keine Aussagen über Häufigkeiten einer UAW getroffen oder valide Beurteilungen einer Kausalität durchgeführt werden [2].
Die UAW bezüglich hepatischer Effekte (v.a. Transaminasenerhöhungen) traten nach Gahr et al. vorwiegend in der Anfangszeit der Behandlung auf. Als mögliche Risikofaktoren identifizierten die Autoren Polypharmazie, weibliches Geschlecht und ein Alter über 50 Jahren [11]. Anhand der vorliegenden, aktuellen Analyse bestätigten sich das Auftreten der Transaminasenerhöhungen zu Beginn der Behandlung, die Reversibilität der Transaminasenerhöhungen sowie das vermehrte Auftreten bei Frauen und bei bestehender Komedikation. Klinisch relevante Transaminasenerhöhungen wurden in dieser gepoolten Analyse allerdings in zwei Drittel der Fälle bei Patienten jünger als 55 Jahre beobachtet, was somit im Gegensatz zu der Datenbankanalyse von Gahr et al. kein erhöhtes Risiko mit höherem Lebensalter zeigt. Bestätigt wird dies durch klinische Studiendaten, die bei älteren eine vergleichbare Verträglichkeit wie bei jüngeren Erwachsenen belegen [15, 16].
In einer weiteren Datenbankanalyse von Pharmakovigilanz-Daten des Uppsala Monitoring Centers (VigiBase) werden Melde-Daten zu potenziell leberschädigenden UAW bei unterschiedlichen Antidepressiva (Zeitraum:1968 bis Mai 2014) verglichen (Gahr et al., 2015) [12]. Diese Analyse dient nach Aussage der Autoren primär der explorativen quantitativen Signalerfassung zu Meldehäufigkeiten, ohne jedoch definitive Aussagen zu einem tatsächlichen Risiko für eine Leberschädigung unter bestimmten Antidepressiva zu ermöglichen oder Häufigkeiten bzw. Kausalitätsbewertungen darzustellen. Es erscheint in diesem Zusammenhang erwähnenswert, dass im Gegensatz hierzu bei der regelmäßigen Nutzen-Risiko-Bewertung von Arzneimitteln durch Zulassungsbehörden neben der weltweiten Signalerfassung auch eine Kausalitätsbewertung durchgeführt wird, welche bei begründetem Verdacht zu Anpassungen der Fachinformation oder weiteren Interventionen führt.
Das in der Analyse von Gahr et al. (2015) beschriebene erhöhte Risiko für Meldungen von UAW im Zusammenhang mit einer Leberschädigung unter Agomelatin (v.a. Transaminasenerhöhungen) wird durch den „reporting bias“ und die falsch-positiven Ergebnisse durch transiente Transaminasenerhöhungen relativiert, wie von den Autoren dargestellt [12]. Entscheidend bei dieser Datenbankanalyse erscheint jedoch die Methodik der Berechnung des Reporting Odds-Ratio (ROR). Das ROR ermöglicht keinen Rückschluss auf das tatsächliche Risiko einer möglichen Leberschädigung, sondern gibt an, wie hoch das OR für ein „reporting“ ist, berechnet aus dem Anteil von „Leber-UAW“ an „Gesamt-UAW“ eines Medikaments, was zu einer deutlichen Verzerrung der Ergebnisse führt. Somit wird für Agomelatin aufgrund der, seit Zulassung, empfohlenen Transaminasenkontrollen und daraus resultierender vermehrter Wachsamkeit der Ärzte bezüglich dieses Parameters ein höherer Wert (n=334) bezogen auf eine insgesamt niedrige Gesamtzahl an UAW-Meldungen (n=1758) errechnet.
Bei dieser Berechnungsart ist der Zeitfaktor ebenfalls sehr bedeutsam, da in den 1960er- bis 1990er-Jahren (bei Zulassung älterer Antidepressiva) die Pharmakovigilanz noch einen geringeren Stellenwert hatte und erst in den letzten fünf bis zehn Jahren mit Novellierungen des Arzneimittelgesetzes (AMG) die Pharmakovigilanz deutlich gestärkt wurde. In diesen letzten Jahren hat die europäische Zulassungsbehörde EMA mit dem Ziel, eine möglichst hohe Therapiesicherheit zu gewährleisten, bei Neuzulassungen zunehmend strengere Kriterien hinsichtlich Studienqualität und insbesondere Arzneimittelsicherheit formuliert. Sie fordert inzwischen für viele Medikamente ein regelmäßiges Monitoring unterschiedlicher Laborparameter, EKG-/EEG-Kontrollen oder ähnliches. Aufgrund der in RCTs zu Agomelatin beobachteten Fälle von Transaminasenerhöhungen (1,4% unter 25 mg, 2,5% unter 50 mg Agomelatin gegenüber 0,6% unter Placebo) werden in diesem Zusammenhang Leberwertkontrollen empfohlen. Transaminasentests sollen vor Behandlungsbeginn, nach etwa 3, 6, 12 und 24 Wochen, sowie bei vorliegenden klinischen Symptomen einer Leberfunktionsstörung durchgeführt werden. Nach Dosiserhöhung sollen die Kontrollen in derselben Häufigkeit erfolgen [9], was, bei einer im klinischen Alltag üblichen Dosiserhöhung nach zwei bis drei Wochen, einer zusätzlichen Transaminasenkontrolle entspricht. Im Gegensatz zu älteren Wirkstoffen ist diese Empfehlung eines sorgfältigen Monitorings in der Fachinformation von Agomelatin gelistet [9], für ältere Antidepressiva und Psychopharmaka wird dies in Leitlinien und Lehrbüchern ebenfalls empfohlen [1, 7]. Regelmäßige Kontrollen gewährleisten somit eine hohe Therapiesicherheit, insbesondere aufgrund der Reversibilität der Transaminasenerhöhungen [23, 42, 49].
Eine Veränderung der Transaminasen ist ein häufig beschriebenes Phänomen unter Psychopharmaka [37, 46], Laborkontrollen werden empfohlen [1, 7]. Ebenso sind selten auftretende Medikamenten-induzierte Leberschädigungen (z.B. Hepatitis, Ikterus, Leberversagen) bei vielen unterschiedlichen allgemein-internistischen Arzneimitteln, wie beispielsweise auch Antibiotika [33], nichtsteroidalen Antirheumatika (NSAR) oder Paracetamol [40] beschrieben. Die klinische Symptomatik arzneimittelbedingter Leberfunktionsstörungen ist komplex und zugleich uncharakteristisch. Im Einzelfall können der Nachweis eines Kausalzusammenhangs und die Diagnose einer Medikamenten-assoziierten Leberschädigung schwierig sein. Hierbei sind vorbestehende Erkrankungen oder Risikofaktoren sowie potenzielle pharmakokinetische und -dynamische Wechselwirkungen bedeutsam [7, 34]. Das frühzeitige Erkennen einer potenziell hepatotoxischen Wirkung unter Ausschluss anderer Ursachen und das Absetzen der verdächtigen Medikamente ist eine wichtige Voraussetzung für das Vermeiden schwerwiegender Leberschädigungen [7, 37, 43, 45, 46].
In Anbetracht eines generell bestehenden Risikos einer möglichen Leberschädigung durch Arzneimittel erscheint es grundsätzlich sinnvoll, Leberwerte vor und während einer medikamentösen Behandlung, insbesondere bei Polypharmazie, regelmäßig zu kontrollieren, und auf Symptome einer Leberfunktionsstörung zu achten, um Risikopatienten frühzeitig zu erkennen [1, 7, 37, 46].
Verträglichkeitsprofil – weitere Aspekte
Aufgrund seines spezifischen Rezeptorprofils hat Agomelatin im Vergleich zu anderen Antidepressiva keine Auswirkungen auf Serotoninspiegel, Blutgerinnung oder Elektrolyte. Sexuelle Funktion, Körpergewicht, Blutdruck, Herzfrequenz und QTc-Zeit werden nicht beeinflusst [4, 8, 9, 13, 19, 30, 41, 44]. Die gute Verträglichkeit spiegelt sich in den geringen Therapieabbruchraten aufgrund von UAW wider, die in klinischen Studien vergleichbar dem Placebo-Arm und signifikant niedriger als unter SSRI/SSNRI sind [6, 13, 19, 44].
Die Daten der aktuell vorliegenden Analyse aus dem Praxisalltag liefern die erforderlichen und gewünschten epidemiologischen Daten an einer großen Patientenzahl, um eine Bewertung des Verträglichkeitsprofils von Agomelatin mit Daten der Versorgungsrealität zu unterstützen.
Wie diese Daten zeigen, traten UAW unter Agomelatin insgesamt mit einer geringen Inzidenz auf, bei bekanntem Nebenwirkungsprofil (v.a. Kopfschmerz, Übelkeit, Schwindel) und nahezu unabhängig von einer psychotropen Komedikation. Sie beschränkten sich überwiegend auf die ersten 12 Behandlungswochen. Schwerwiegende UAW wurden nach Woche 24 nicht mehr berichtet. Dies bestätigt die bisherigen Erkenntnisse aus klinischen Studien hinsichtlich guter Verträglichkeit von Agomelatin, dem günstigen Nebenwirkungs- und Interaktionsprofil sowie dem Auftreten von UAW vorwiegend bei Behandlungsbeginn [9].
Antidepressive Wirkung
Der mittels CGI erhobene antidepressive Effekt wird als Hinweis auf die Effektivität von Agomelatin gewertet, und entspricht der allgemeinen Einschätzung der behandelnden Ärzte im Praxisalltag. Die hier gezeigten Response- und Remissionsraten decken sich allerdings mit den Ergebnissen aus RCTs anhand von differenzierten Skalen (MADRS, HAM-D) [13, 44].
Limitationen
Als Limitationen werden bei naturalistischen Studien im Vergleich zu RCTs häufig die fehlende Randomisierung und Verblindung sowie nicht vorhandene Vergleichsgruppen beschrieben. Außerdem wird als Schwäche bei naturalistischem Studiendesign das fehlende Monitoring und damit verbundene niedrigere UAW-Melderaten diskutiert. Auch wenn nichtinterventionelle Studien aus methodologischen Gründen keinen Wirksamkeitsnachweis erbringen können, liefern sie dennoch für den Praxisalltag relevante Informationen zu Therapieeffekt und Verträglichkeit von Arzneimitteln, was in RCTs aufgrund der strengen Ein- und Ausschlusskriterien nicht abgebildet werden kann und somit die Bedeutung und Relevanz nichtinterventionell erhobener Daten unterstreicht. Hinsichtlich der Verträglichkeitserfassung ist erwähnenswert, dass in RCTs unerwünschte Ereignisse, unabhängig von Kausalitätsbeziehungen, erfasst werden, wohingegen in naturalistischen Studien UAW mit zumindest einem möglichen Kausalzusammenhang ausgewertet werden. Einer möglicherweise Studiendesign-bedingten niedrigeren Melderate steht bei Agomelatin allerdings die erhöhte Wachsamkeit bei Ärzten hinsichtlich hepatischer Effekte entgegen, da auf das Monitoring der Transaminasen seit Zulassung kontinuierlich hingewiesen wurde, und die Aufmerksamkeit durch Informationsbriefe an verschreibende Ärzte weiter zugenommen hat.
Als Stärke der hier präsentierten Daten ist die große Anzahl an nicht selektierten Patienten des Praxisalltags zu nennen.
Fazit
Zusammengefasst bestätigt die vorliegende gepoolte Analyse der vier nichtinterventionellen Studien VIVALDI, VIVALDI-Praxis, VITAL und VIVRE an insgesamt 9601 Patienten, dass Agomelatin bei heterogenen und für den Praxisalltag typischen Patienten mit Depression, einschließlich älterer, komorbider und komedizierter Patienten, effektiv und gut verträglich ist. Die Nebenwirkungsrate ist niedrig (5,3%) und nimmt im Behandlungsverlauf deutlich ab. Das potenzielle Risiko einer Leberschädigung ist bei diesen Patienten unter Praxisbedingungen gering und wird meist in Form von reversiblen Transaminasenerhöhungen, vorwiegend innerhalb der ersten zwölf Behandlungswochen, beobachtet. Mit den empfohlenen Transaminasenkontrollen, die ein frühzeitiges Erkennen von Risikopatienten ermöglichen, ist Agomelatin aufgrund des günstigen Nebenwirkungs- und Interaktionsprofils ein gut verträgliches und sicheres Antidepressivum.
Interessenkonflikterklärung
GL: Beratung oder Teilnahme an einem Expertenbeirat: Janssen-Cilag, Lundbeck, Otsuka, Servier; Honorare für Vorträge, Stellungnahmen oder Artikel: Bayer, GlaxoSmithKline, Lundbeck, Servier; Unterstützung für Kongressbersuche: Lundbeck
BB: Angestellte von Servier Deutschland GmbH, Medical Affairs
GH: Beratung oder Teilnahme an einem Expertenbeirat: Actelion, Lundbeck, Merck, Servier; Honorare für Vorträge, Stellungnahmen oder Artikel: Actelion, Affectis, AstraZeneca, Bayer Vital, Boehringer Ingelheim, Bundesministerium für Bildung und Forschung, Bundesamt für Strahlenschutz, BrainLab, Bristol-Myers Squibb, Cephalon, Deutsche Forschungsgesellschaft, Essex, EuMeCom, Gerson Lerman Group Council of Healthcare Advisors, GlaxoSmithKline, Janssen-Cilag, Lilly, Lundbeck, McKinsey, Meda, Merck, Merz, Network of Advisors, Neurim, Neurocrine, Novartis, Organon, Orphan, Pfizer, Procter & Gamble, Purdue, Sanofi, Schering-Plough, Sepracor, Servier, Takeda, Transcept, Wyeth; Unterstützung für Kongressbesuche: AstraZeneca, GlaxoSmithKline, Janssen-Cilag, Lilly, Lundbeck, Merck, Merz, Pfizer, Sanofi, Servier, Takeda; Forschungsbeihilfe: BMBF, Bundesamt für Strahlenschutz, BrainLab, Janssen-Cilag
ML: Honorare für Vorträge, Stellungnahmen oder Artikel: Boehringer Ingelheim, Forum für medizinische Fortbildung, Lundbeck, Servier; Unterstützung für Kongressbesuche: Lundbeck, Servier; sonstige Unterstützung (z.B. Ausrüstung, Personal, Veranstaltungsausrichtung): Janssen-Cilag, Lilly, Lundbeck
H-PV: Beratung oder Teilnahme an einem Expertenbeirat: AstraZeneca, Janssen-Cilag, Lilly Deutschland, Lundbeck, Neuraxpharm, Otsuka Pharma, Pfizer Pharma, Dr. Willmar Schwabe, Steigerwald Arzneimittelwerk; Vortragshonorare: AstraZeneca, Bristol-Myers Squibb, Janssen-Cilag, Lilly Deutschland, Lundbeck, Neuraxpharm, Otsuka Pharma, Pfizer Pharma, Dr. Willmar Schwabe, Servier Deutschland, Spitzner Arzneimittelwerke, Steigerwald Arzneimittelwerk, Trommsdorff
Literatur
1. Benkert O, Hippius H (Hrsg.). Kompendium der Psychiatrischen Pharmakotherapie. 10. Auflage. Berlin: Springer, 2014.
2. BfArM. Pharmakovigilanz – Datenbank unerwünschter Arzneimittelwirkungen. 2013. www.bfarm.de/DE/Arzneimittel/Pharmakovigilanz/Risikoinformationen/uawDB/_node.html (Zugriff am 13.03.2015).
3. Brambilla P, Cipriani A, Hotopf M, Barbui C. Side-effect profile of fluoxetine in comparison with other SSRIs, tricyclic and newer antidepressants: a meta-analysis of clinical trial data. Pharmacopsychiatry 2005;38:69–77.
4. De Berardis D, Di lorio G, Acciavatti T, Conti CM. The emerging role of melatonin agonists in the treatment of major depression: focus on agomelatine. CNS Neurol Disord Drug Targets 2011;10:119–32.
5. De Bodinat C, Guardiola-Lemaitre B, Mocaer E, Renard P, et al. Agomelatine, the first melatonergic antidepressant: discovery, characterization and development. Nat Rev Drug Discov [Review] 2010;9:628–42.
6. Demyttenaere K, Corruble E, Hale A, Quera Salva MA, et al. A pooled analysis of six month comparative efficacy and tolerability in four randomized clinical trials: agomelatine versus escitalopram, fluoxetine and sertraline. CNS Spectrums 2013;18:163–70.
7. DGPPN, Leitliniengruppe. S3-Leitlinie/Nationale Versorgungsleitlinie Unipolare Depression. DGPPN, ÄZQ, AWMF; 2012.
8. Donazzolo Y, Latreille M, Caillaud M, Mocaer E, et al. Evaluation of the effects of therapeutic and supratherapeutic doses of agomelatine on the QT/QTc interval: A phase I, randomized, double-blind, placebo-controlled and positive-controlled, crossover thotough QT/QTc study conducted in healthy volunteers. J Cardiovasc Pharmacol 2014;64:440–51.
9. Fachinformation. Valdoxan 25 mg. 2014.
10. FDA. Clinical White Paper. CDER-PHRMA-AASLD Conference 2000; www.fda.gov/downloads/drugs/scienceresearch/researchareas/ucm091457.pdf (Zugriff am 13.03.2015).
11. Gahr M, Freudenmann R, Connemann B, Hiemke C, et al. Agomelatine and hepatotoxicity: Implications of cumulated data derived from spontaneous reports of adverse drug reactions. Pharmacopsychiatry 2013;46:214–20.
12. Gahr M, Zeiss R, Lang D, Connemann BJ, et al. Hepatotoxicity associated with agomelatine and other antidepressants: disproportionality analysis using pooled pharmacovigilance data from the Uppsala Monitoring Centre. J Clin Pharmacol 2015; DOI 10.1002/jcph.475.
13. Guaiana G, Gupta S, Chiodo D, Davies SJ, et al. Agomelatine versus other antidepressive agents for major depression. Cochrane Database Syst Rev 2013;12:CD008851.
14. Hale A, Corral RM, Mencacci C, Ruiz JS, et al. Superior antidepressant efficacy results of agomelatine versus fluoxetine in severe MDD patients: a randomized, double-blind study. Int Clin Psychopharmacol 2010;25:305–14.
15. Heun R, Corral R, Ahokas A, Nicolini H, et al. Sustained efficacy and safety of agomelatine versus placebo over 24 weeks in elderly out-patients suffering from major depressive disorder. Eur Neuropsychopharmacol 2014;24(Suppl 2):S403 P.2.b.042.
16. Heun R, Ahokas A, Boyer P, Giménez-Montesions N, et al. The efficacy of agomelatine in elderly patiens with recurrent major depressive disorder: A placebo-controlled study. J Clin Psychiatry 2013;74:587–94.
17. Jacobi F, Höfler M, Strehle J, Mack S, et al. Psychische Störungen in der Allgemeinbevölkerung. Studie zur Gesundheit Erwachsener in Deutschland und ihr Zusatzmodul psychische Gesundheit (DEGS1-MH). Nervenarzt 2014;85:77–87.
18. Kasper S, Hajak G, Wulff K, Hoogendijk WJ, et al. Efficacy of the novel antidepressant agomelatine on the circadian rest-activity cycle and depressive and anxiety symptoms in patients with major depressive disorder: a randomized, double-blind comparison with sertraline. J Clin Psychiatry 2010;71: 109–20.
19. Kennedy SH, Rizvi S, Fulton K, Rasmussen J. A double-blind comparison of sexual functioning, antidepressant efficacy, and tolerability between agomelatine and venlafaxine XR. J Clin Psychopharmacol 2008;28:329–33.
20. Kessler R, Aguilar-Gaxiola S, Alonso J, Chatterji S, et al. The global burden of mental disorders: an update from the WHO World Mental Health (WMH) surveys. Epidemiol Psychiatri Soc 2009;18:23–33.
21. Koesters M, Guaiana G, Cipriani A, Becker T, et al. Agomelatine efficacy and acceptability revisited: systematic review and meta-analysis of published and unpublished randomised trials. Br J Clin Pharmacol 2013;203: 179–87.
22. Laux G. The antidepressant agomelatine in daily practice: results of the non-interventional study VIVALDI. Pharmacopsychiatry 2012;45:284–91.
23. Laux G, VIVALDI S. Antidepressive Therapie mit Agomelatin in der Facharztpraxis. Ergebnisse der VIVALDI-Studie. Psychopharmakotherapie 2011;18:18–26.
24. Laux G, Huttner N. Agomelatin in der Depressionsbehandlung über 12 Monate – Follow-up der VIVALDI-Studie. Psychopharmakotherapie 2013;20:119–27.
25. Laux G, Huttner NA. Subgroup analysis of the non-interventional study VIVALDI: agomelatine in treatment-naive patients, in combination therapy and after treatment switch. Int J Psychiatry Clin Pract 2014;18:86–96.
26. Laux G, Steinmann C. Antidepressive Behandlung mit Agomelatin in der Hausarztpraxis: Ergebnisse der Studie VIVALDI-Praxis [Poster]. DGPPN 2011, P-011-008
27. Lemke M, Barthel B. Results of the German non-interventional study VITAL over 6 months: Effect of agomelatine on depressive symptoms and patientsʼ compliance [Poster Abstract]. Eur Neuropsychopharmacol 2013;23(Suppl 2):S327.
28. Lemoine P, Guilleminault C, Alvarez E. Improvement in subjective sleep in major depressive disorder with a novel antidepressant, agomelatine: randomized, double-blind comparison with venlafaxine. J Clin Psychiatry 2007;68:1723–32 .
29. Machado M, Iskedjian M, Ruiz I, Einarson TR. Remission, dropouts and adverse drug reaction rates in major depressive disorder: a meta-analysis of head-to-head trials. Curr Med Res Opin 2006;22:1825–37.
30. Marx U, Picarel-Blanchot F, Mocaer E, Seguin L. Neutrality of agomelatine on QT/QTc interval in healthy young volunteers: Results from a randomized double-blind cross-over phase I study. Eur Neuropsychopharmacol 2013;23(Suppl): P.2.h.007.
31. Möller HJ. Das Problem der Heterogenität zwischen in den USA und nicht in den USA durchgeführten Antidepressiva Studien. Psychopharmakotherapie 2014;21:211–8.
32. Möller HJ, Laux G, Kapfhammer H (Hrsg.). Psychiatrie, Psychosomatik, Psychotherapie. 4. Auflage. Berlin: Springer, 2011.
33. Navano VJ, Senior JR. Drug-related hepatotoxicity. N Engl J Med 2006;354:731–9.
34. Olesen J, Gustavsson A, Svensson M, Wittchen HU, et al. The economic cost of brain disorders in Europe. Eur J Neurol 2012;19:155–62.
35. Olfson M, Marcus SC, Tedeschi M, Wan GJ. Continuity of antidepressant treatment for adults with depression in the United States. Am J Psychiatry 2006;163:101–8.
36. Papakostas G, Homberger C, Fava M. A meta-analysis of clinical trials comparing mirtazapine with selective serotonin reuptake inhibitors for the treatment of major depressive disorder. J Psychopharmacol (Oxford, England) 2008;22:843–8.
37. Park SH, Ishino R. Liver injury associated with antidepressants. Curr Drug Saf 2013;8:207–23.
38. Quera Salva MA, Hajak G, Philip P, Montplaisir J, et al. Comparison of agomelatine and escitalopram on nighttime sleep and daytime condition and efficacy in major depressive disorder patients. Int Clin Psychopharmacol 2011;26:252–62.
39. Racagni G, Riva MA, Molteni R, Musazzi L, et al. Mode of action of agomelatine: synergy between melatonergic and 5-HT2C receptors. World J Biol Psychiatry 2011;12:574–87.
40. Rotthauwe J. Bulletin zur Arzneimittelsicherheit 2012;3:11–3.
41. Serretti A, Chiesa A. Treatment-emergent sexual dysfunction related to antidepressants: a meta-analysis. J Clin Psychopharmacol 2009;29:259–66.
42. Stahl SM, Fava M, Trivedi MH, Caputo A, et al. Agomelatine in the treatment of major depressive disorder: an 8-week, multicenter, randomized, placebo-controlled trial. J Clin Psychiatry 2010;71:616–26.
43. Tajiri K, Shimizu Y. Practical guidelines for diagnosis and early management of drug-induced liver injury. World J Gastroenterol 2008;14:6774–85.
44. Taylor D, Sparshatt A, Varma S, Olofinjana O. Antidepressant efficacy of agomelatine: meta-analysis of published and unpublished studies. BMJ 2014;348:g1888.
45. US Departement of Health and Human Services, Food and Drug Administration (FDA), Center for Drug Evaluation and Research (CDER), Center for Biologics Evaluation and Research (CBER). Guidance for Industry Drug-Induced Liver Injury. FDA; 2009.
46. Voican C, Corruble E, Naveau S, Perlemuter G. Antidepressant-induced liver injury: A review for clinicans. Am J Psychiatry 2014;171:404–15.
47. Volz H, Barthel B. Results of the non-interventional study VIVRE: Treatment effect of agomelatine on depressive symptoms, anxiety symptoms within depression and social and emotional functioning over 3 months. J Eur Psychiatry 2014;29(Suppl 1):P-0397.
48. Wittchen HU, Jacobi F, Rehm J, Gustavsson A, et al. The size and burden of mental disorders and other disorders of the brain in Europe 2010. Eur Neuropsychopharmacol 2011;21:655–79.
49. Zajecka J, Schatzberg A, Stahl S, Shah A, et al. Efficacy and safety of agomelatine in the treatment of major depressive disorder: a multicenter, randomized, double-blind, placebo-controlled trial. J Clin Psychopharmacol 2010;30:135–44.
Prof. Dr. med. Dipl.-Psych. Gerd Laux, Institut für Psychologische Medizin (IPM), Oberwallnerweg 7, 83527 Haag i. Ob., E-Mail: ipm@ipm-laux.de
Dr. med. Bettina Barthel, Medical Affairs, Servier Deutschland GmbH, Elsenheimerstraße 53, 80687 München
Prof. Dr. med. Göran Hajak, Klinik für Psychiatrie, Psychotherapie und Psychosomatik der Sozialstiftung Bamberg, St.-Getreu-Straße 14–18, 96049 Bamberg
Prof. Dr. med. Matthias Lemke, Evangelisches Krankenhaus Alsterdorf, Psychiatrie und Psychotherapie, Alsterdorfer Markt 8, 22297 Hamburg, Universität Kiel
Prof. Dr. med. Hans-Peter Volz, Krankenhaus für Psychiatrie, Schloss Werneck, Balthasar-Neumann-Platz 1, 97440 Werneck
Effectiveness and tolerability of the antidepressant agomelatine in daily practice – Pooled analysis of four non-interventional studies
In randomized, double-blind, placebo-controlled and head-to-head studies the melatonergic MT1-/MT2-agonist and selective 5-HT2C-antagonist agomelatine has shown antidepressant efficacy and a favorable tolerability profile. In order to provide further evidence concerning the antidepressant effect and tolerability in daily practice, a pooled analysis was performed, based on the data of four non-interventional-studies with agomelatine (25–50 mg/day) in Germany (2009–2013). In total, the data of 9,601 patients with the diagnosis of major depression, treated by psychiatrists and general practitioners, were included into the analysis. Main analysis of the total population was performed after 12 weeks, subpopulations were analyzed after 24 and 52 weeks.
71.9% of the patients had concomitant psychiatric diseases, 60.1% were already pretreated with other antidepressant drugs. 18.9% of patients had co-medication with other antidepressants, 31.9% with other psychotropic medication. 67.8% were treated with 25 mg agomelatine after 12 weeks, 31.5% received 2 tablets (50 mg). Depression improved according to Clinical Global Impression (CGI) with response in 78.7% (CGI-I ≤2) and remission in 34.5% (CGI-S =1 or 2) of patients. During 12 weeks of treatment, adverse drug-reactions (ADR) were reported in 5.32% of the patients (n=511), with headache (0.92%), nausea (0.75%), dizziness (0.54%) and restlessness (0.45%) being the most frequently reported ADR. For 18 patients (0.19%) serious adverse drug-reactions (sADR) were documented. Overall 49 patients (0.5%) of the total population showed transaminase-elevations (ASAT/ALAT >3 times upper normal value), thereof 19 patients (0.2%) already had preexisting elevations at study-start. One patient (0.03%) developed hepatitis with jaundice (week 12–24), which was reversible after discontinuation of agomelatine. ADR and liver-enzyme-elevations predominantly occurred within the first weeks of treatment. Mean weight and body mass index (BMI) remained unchanged.
The presented pooled data confirm that agomelatine is well tolerated and effective in treating a heterogeneous population of depressed patients which are representative for daily practice.
Key words: Agomelatine, major depression, pooled-analysis, effectiveness, tolerability, transaminases
Psychopharmakotherapie 2015; 22(03)
