Tillmann H. C. Krüger, Hannover
Warum Sexualität bei Patienten mit Depressionen evaluieren?
Sexuelle Dysfunktionen sind in der Normalbevölkerung häufig und können je nach Studie bei Männern zwischen 10 und 52% und bei Frauen bei 25 bis 63% liegen [17]. Das Vorliegen einer Depression kann das Risiko für eine sexuelle Dysfunktion um 50 bis 70% erhöhen [2]. Neben der hohen Prävalenz sind drei wichtige Gründe zu nennen, sexuelle Probleme bei Patienten mit Depressionen zu evaluieren:
- Es existiert ein gut dokumentierter Zusammenhang zwischen sexueller Gesundheit und Lebensqualität – auch unabhängig von der Stimmung (Übersicht bei [9]).
- Sexuelle Probleme können bei Depressionen ein zusätzlicher Stressor sein und den weiteren Krankheitsverlauf ungünstig beeinflussen.
- Medikamenten-induzierte sexuelle Dysfunktionen können die Adhärenz erheblich beeinträchtigen. Analysen zu Gründen für Therapieabbrüche ergaben, dass Nebenwirkungen auf sexuelle Funktionen als einer der wichtigsten Gründe von Patienten aufgeführt wurde [1, 18]. Ein Großteil der Patienten (85%) schätzt sexuelle Gesundheit als wichtig oder sehr wichtig ein [11, 39].
Entgegen weit verbreiteter Vorurteile sind Sexualprobleme kein besonders heikles, schwieriges und „undankbares“ Thema der Medizin und klinischen Psychologie. Im Gegenteil: Es gibt nicht viele andere Bereiche in Psychiatrie und Psychotherapie, in denen man Patienten so wirkungsvoll helfen kann (auch in Kombination mit Pharmakotherapie). Patienten sind in der Regel sehr dankbar, wenn ihr Behandler auch sexuelle Probleme ernst nimmt oder aktiv anspricht.
Für viele sexuelle Probleme braucht es kein hochspezialisiertes Expertenwissen, sondern der Arzt oder Therapeut kann mit seinen Fertigkeiten plus einigen sexualmedizinischen Basiskenntnissen bereits viel erreichen. Und nicht zuletzt hat sexuelle Gesundheit und Partnerschaft ein großes salutogenes Potenzial wie eine Vielzahl von Untersuchungen belegt [12, 15, 22, 24, 26].
Neurobiologie sexueller Funktionen und präklinisches Profil von Vortioxetin
Neurobiologie sexueller Funktionen
Sexuelle Funktionen werden durch eine Reihe von Hormonen, Neuromodulatoren und Neurotransmittern maßgeblich moduliert. Ein Grundverständnis der neurochemischen Vorgänge ist vor dem Hintergrund der komplexen Interaktionen mit pharmakologischen Substanzen essenziell. Die unterschiedlichen Substanzen können dabei primär inhibitorische oder exzitatorische Effekte auf sexuelles Verlangen und Funktionen ausüben. Das von Bancroft und Janssen (2000) beschriebene „Dual Control Model“ [4], welches primär exzitatorische und inhibitorische Faktoren auf einer psychologischen Ebene beschrieb, lässt sich auch in diesem Kontext nutzen, um sich das Wechselspiel der verschiedenen Botenstoffe zu vergegenwärtigen. Auch während der Erhebung der Anamnese kann das Modell helfen, neben psychologischen Bedingungsfaktoren auch ein eventuelles Ungleichgewicht aufgrund pharmakologischer Faktoren (Arzneimitteleinnahme) zu identifizieren.
Die wesentlichen neurochemischen Substanzen sind in Tabelle 1 aufgeführt. Die als erstes aufgeführte Gruppe der Sexualsteroide repräsentiert die für Kliniker bekannteste Gruppe der Substanzen. Im zentralen Nervensystems (ZNS) sind intrazellulär insbesondere die Metaboliten des Testosterons, Dihydrotestosteron (DHT) und 17-beta-Estradiol, von Relevanz und schaffen die Grundvoraussetzungen dafür, dass bestimmte neuronale Schaltkreise auf interne und externe sexuelle Stimuli ansprechen und psychische und somatische sexuelle Reaktionen initiiert werden können (Priming). Insbesondere die Wichtigkeit von Estradiol für die zentralnervöse Prozessierung von sexueller Appetenz und Erektionsfähigkeit konnte in einer großen klinischen Studie an Männern gezeigt werden [13]. Die Wirkorte von Testosteron und seinen Metaboliten umfassen sowohl subkortikale (Hypothalamus, Amygdala mit Nucleus striae terminalis, Mamillarkörper) als auch kortikale Strukturen (präfrontal, temporal). Über non-genomische Mechanismen können kurzfristige Effekte im Bereich von Sekunden bis Minuten hervorgerufen werden, wohingegen über die klinisch oftmals prominenteren genomischen Mechanismen Effekte im Bereich von Stunden bis Tagen induziert werden [3]. Letzteres kann auch die Synthese von Neurotransmittern oder Neurotransmitter-Rezeptoren beinhalten. Hier existiert insbesondere auch eine Schnittstelle zum monoaminergen System. Die chirurgische oder pharmakologische Supprimierung von Sexualsteroiden (z.B. durch die Gabe von Testosteron-Antagonisten oder Gonadorelin-(GnRH-)Agonisten (syn.: LHRH-Agonisten) inhibiert sexuelles Verlangen und Funktionen in erheblichem Ausmaß, ähnlich wie es auch bei einem klinisch manifesten Hypogonadismus beobachtet werden kann. Erste bildgebende Untersuchungen zeigen, dass unter der Behandlung mit GnRH-Agonisten, die nach einer mehrwöchigen Latenz zu einer Inhibition der Testosteronsynthese führen, wesentliche neuronale Strukturen des limbischen Systems und auch kortikale Areale bei der Betrachtung von visuellen sexuellen Reizen nicht mehr oder deutlich geringer aktivieren und auf der subjektiven Ebene mit einer deutlichen Reduktion von sexueller Lust und Erregung einhergehen [30, 34].
Tab. 1. Taxonomie von für sexuelle Funktionen relevanten Substanzen. Die wesentlichen Hormone bzw. Neuromodulatoren und Neurotransmitter (und deren primärer Synthese- und Sekretionsort in Klammern), die exzitatorische oder inhibitorische Effekte auf sexuelle Funktionen ausüben.
|
Sexualsteroide
|
|
Zerebrale Monoamine
|
|
Neuropeptide
|
DHEA-S: Dehydroepiandrosteronsulfat; POMC: Pro-Opiomelanocortin; ACTH: Adrenocorticotropin; MSH: Melanotropin
Die zerebralen Monoamine fallen im klinischen Alltag vor allem in das Arbeitsgebiet der Neurologen und Psychiater, die diese Systeme durch unterschiedliche pharmakologische Interventionen maßgeblich beeinflussen können. Im ZNS spielen in erster Hinsicht Noradrenalin, Dopamin und Serotonin eine Rolle. Allen drei Substanzen haben gemeinsam, dass sie primär in Kerngebieten des Hirnstamms synthetisiert werden und durch umfassende Projektionen zum limbische System, zum Kortex und zum Teil auch zum Rückenmark (Serotonin, Noradrenalin) zahlreiche neuromodulatorische Effekte auf Verhalten und Befinden ausüben [32].
Das noradrenerge System sorgt dabei für ein ausreichendes Maß an psychophysiologischer Aktivierung, die für sexuelle Lust und Funktion benötigt wird. Das Kerngebiet wird durch den Locus coeruleus repräsentiert und hat Projektionen ins Cerebellum, Rückenmark, Hypothalamus, limbische System und kortikale Areale [32]. Dieses System kontrolliert eine Reihe weiterer Funktionen des autonomen Nervensystems wie die Atmung. Die Funktionsweise des noradrenergen Systems verhält sich dabei wie eine umgekehrte U-Kurve. Ein Mangel an Noradrenalin sorgt für Müdigkeit und Desinteresse, was sich ungünstig auf die sexuelle Aktivität auswirkt. Ein Noradrenalin-Überschuss findet sich in Stresssituationen, die nur in Ausnahmefällen mit Sexualverhalten kompatibel sind. Ein zu hohes Erregungsniveau dieses Systems wird auch im Zusammenhang mit Ejaculatio praecox diskutiert, insbesondere in Fällen, die situativ auftreten und mit Versagensängsten und/oder mangelnder sexueller Erfahrung einhergehen. Das noradrenerge System hat eine Schnittstelle mit den Sexualsteroiden. Estradiol beispielsweise kann im Tiermodell die Synthese von Noradrenalin erhöhen und sorgt auch für eine erhöhte Transmission im ventromedialen Hypothalamus, was das Lordose-Verhalten in weiblichen Ratten fördert.
Eine spezifischere sexualphysiologische Bedeutung haben die zerebralen Monoamine im dopaminergen System, das insbesondere für appetitive und konsumatorische Komponenten verantwortlich ist, die das sexuelle Verlangen, sexuelle Reaktionen und Teilaspekte des Belohnungserlebens umfassen. Es gliedert sich in drei Teilsysteme, die anatomisch in mesolimbischen/mesokortikalen Arealen, nigrostriatalen Arealen und im Hypothalamus verortet sind. Das erste System unterhält weitläufige Projektionen von Kerngebieten im ventralen tegmentalen Areal zum Nucleus accumbens, weiteren limbischen Regionen inklusive der Amygdala und dem präfrontalen Kortex. Das ventrale tegmentale Areal steht aber auch unter dem Einfluss des medial präoptischen Areals (MPOA) des Hypothalamus, welches für die Sexualität zweifelsohne eine Kernstruktur repräsentiert. Das nigrostriatale System hat funktionelle Verbindungen zwischen Kerngebieten in der Substantia nigra mit den Striatum (Nucleus caudatus und Putamen). Dieses System ist insbesondere für die Modulation von motorischen Mustern bedeutsam, beispielsweise beim Morbus Parkinson. Im sexualphysiologischen Kontext steuern beide Systeme selektive Aufmerksamkeit gegenüber relevanten Reizen, motivationales Verhalten in Richtung eines sexuellen Reizes sowie Aufbau eines autonomen Erregungsniveaus, wobei es hier Überschneidungen mit dem noradrenergen System gibt. Das im Hypothalamus lokalisierte Dopamin-System ist vor allem über inhibitorische Eigenschaften an der Kontrolle der Prolactinsekretion der Adenohypophyse beteiligt.
Ein Gegenspieler der oben genannten Substanzgruppen ist das serotonerge System, das in Abhängigkeit von den sieben Rezeptorklassen sowie weiteren Rezeptorsubtypen mehrheitlich inhibitorische Funktionen ausübt. Insbesondere über den 5-HT2C-Rezeptorsubtyp können ausgeprägte inhibitorische Effekte induziert werden, während die Stimulation des 5-HT1A-Rezeptorsubtyps (ein Autorezeptor, dessen Stimulation eine verminderte Serotonintransmission bewirkt) exzitatorische Auswirkungen haben kann. Serotonin wird in den Raphe-Kernen im Hirnstamm synthetisiert. Umfassende Projektionen reichen in das Rückenmark und zum Hypothalamus sowie zu limbischen (MPOA, Nucleus accumbens) und kortikalen Arealen. Serotonerge Transmission moduliert Sättigung, Entspannung und Zufriedenheit. Es scheint in reger Wechselbeziehung zum dopaminergen System zu stehen und kann die mesolimbische und hypothalamische Dopamin-Sekretion inhibieren, während in Abhängigkeit von Rezeptorsubtyp in anderen Arealen die Sekretion von Dopamin gefördert wird. Über deszendierende Bahnen im Rückenmark übt Serotonin einen inhibierenden Einfluss auf spinale Sexualreflexe aus. Steroidhormone scheinen keinen wesentlichen Einfluss auf dieses System auszuüben, sodass die serotonerge Transmission relativ unabhängig von hormoneller Regulation funktioniert [32].
Die dritte wichtige Gruppe wird durch Neuropeptide repräsentiert, die weniger schnell als die monoaminergen Substanzen zu agieren scheinen. Es sind ausgeprägte Verhaltensmodulatoren und bei Substanzen wie Oxytocin oder Vasopressin kann man von „sozialen Neuropeptiden“ sprechen, da sie Aspekte des Sozialverhaltens regulieren [27, 23]. Prolactin sind überwiegend inhibitorische Effekte zuzuschreiben, insbesondere bei klinischen Zuständen von chronischer Hyperprolaktinämie, wie sie nach der Gabe von D2-Rezeptorantagonisten (bestimmte Neuroleptika) gesehen werden können. Dauerhafte Einnahme von Opioidrezeptoragonisten sorgt für eine deutliche Reduktion von sexueller Lust, Erregungs- und Orgasmusfähigkeit.
Präklinisches Profil von Vortioxetin
Vortioxetin wird als ein multimodales Antidepressivum bezeichnet [31], das mittels einer Kombination von pharmakologischen Wirkweisen arbeitet: Rezeptoraktivität und Wiederaufnahmehemmung sowie Modulierung der Neurotransmission in mehreren Systemen (Abb. 1). In-vitro-Studien zeigen, dass Vortioxetin ein 5-HT3-, 5-HT7- und 5-HT1D-Rezeptorantagonist, ein 5-HT1B-Rezeptorpartialagonist, ein 5-HT1A-Rezeptoragonist und ein Inhibitor des Serotonintransporters ist [5, 29]. Hier wird bereits deutlich, dass es zu keiner unmittelbaren Stimulation des für sexuelle Funktionen inhibitorisch wirkenden 5-HT2C-Rezeptors kommt, wohingegen eine agonistische Wirkung am 5-HT1A-Rezeptor in diesem Kontext unproblematisch oder sogar erwünscht ist. Nichtklinische In-vivo-Studien zeigen, dass Vortioxetin die Spiegel der Neurotransmittersysteme von Serotonin, Noradrenalin, Dopamin, Histamin, Acetylcholin, Gamma-Aminobuttersäure (GABA) und Glutamat moduliert – dies vor allem im Bereich des Vorderhirns. Die Erhöhung der Verfügbarkeit von Serotonin ist von sexualmedizinischer Seite prinzipiell als ungünstig zu werten. Vermutlich kann dieser Effekt aber über den gleichzeitigen 5-HT1A-Rezeptoragonismus kompensiert werden [36, 37].
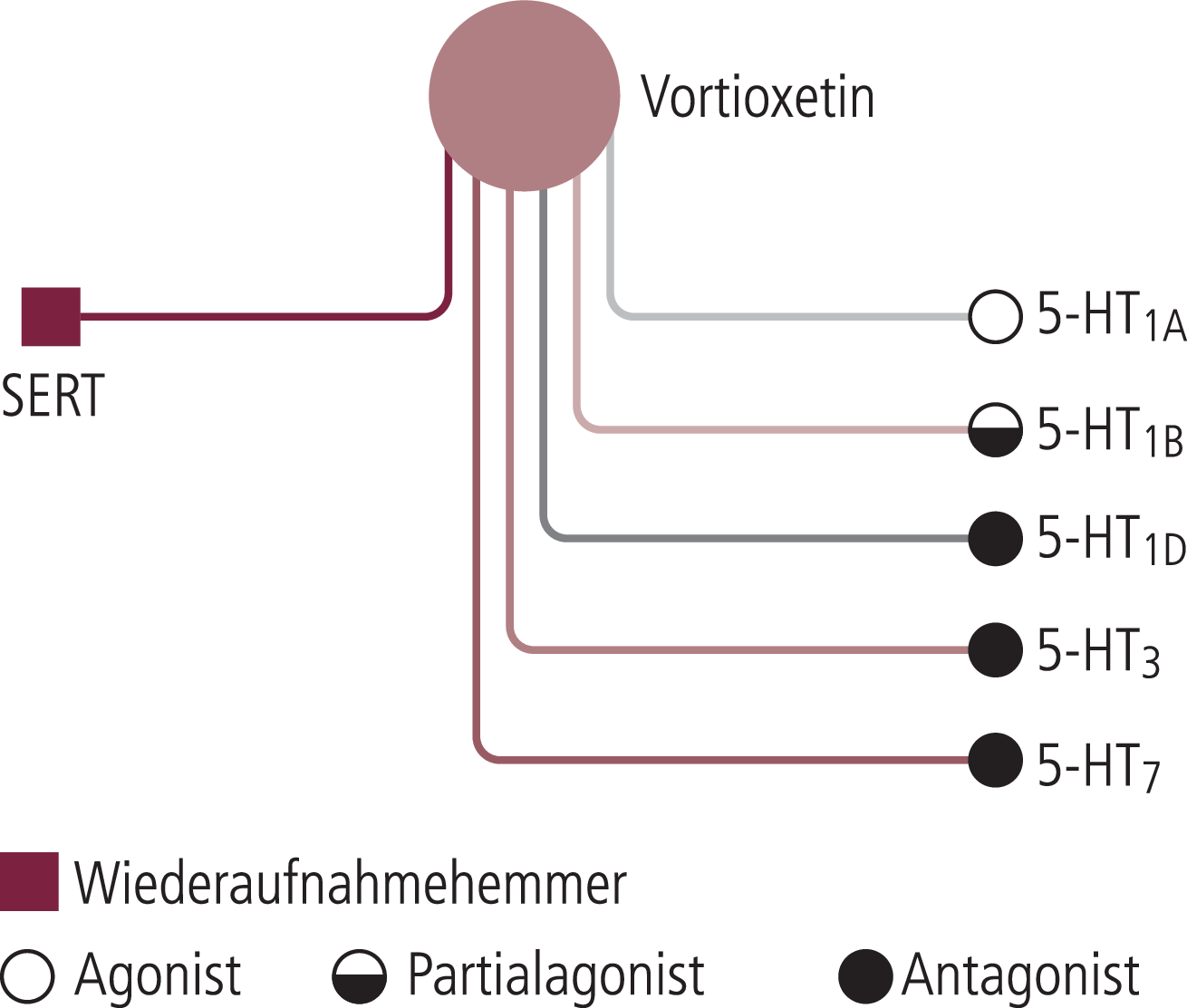
Abb. 1. Pharmakologisches Profil von Vortioxetin. SERT: Serotonintransporter
Sexuelle Dysfunktionen: Definition, Epidemiologie und Erhebung
Die ICD-10-Klassifikation führt die entsprechenden Kriterien für die unterschiedlichen sexuellen Funktionsstörungen auf, die sich im Wesentlichen in Störungen der Motivation und der Funktion unterteilen lassen (Tab. 2).
Tab. 2. Klassifikation sexueller Funktionsstörungen gemäß ICD-10
|
Sexuelle Funktionsstörungen F52 |
|
F52.0 Mangel oder Verlust von sexuellem Verlangen |
|
F52.1 Sexuelle Aversion und mangelnde sexuelle Befriedigung |
|
F52.2 Versagen genitaler Reaktionen |
|
F52.3 Orgasmusstörungen |
|
F52.4 Ejaculatio praecox |
|
F52.2 Vaginismus |
|
F52.3 Dyspareunie |
|
F52.7 Gesteigertes sexuelles Verlangen |
Das in seiner Beschreibung etwas ausführlichere DSM-5 gibt störungsübergreifend ein Zeitkriterium von sechs Monaten an sowie das Vorliegen von Leidensdruck und/oder interpersoneller Schwierigkeiten aufgrund der sexuellen Störung. Zudem beinhaltet es Vorschläge zu formalen Beschreibungskriterien sexueller Funktionsstörungen, die für das Verständnis des Krankheitsbildes und der Behandlung bedeutsam sind (Tab. 3).
Tab. 3. Formale Beschreibungskriterien sexueller Funktionsstörungen im DSM-5
|
Kriterium |
Ausprägungsmöglichkeiten |
|
Beginn |
|
|
Kontext des Auftretens |
|
|
Ätiologische Faktoren |
|
Für die Angaben von Häufigkeiten sexueller Funktionsstörungen findet sich eine große Streubreite, die in der unterschiedlichen Methodik der Erhebung begründet ist. Bei Männern dominieren Erektionsstörungen und die Ejaculatio praecox. Eine manifeste Störung der sexuellen Lust ist bei jüngeren Männern (16–44 Jahre) mit 1,8% sehr selten. Die hohen Prävalenzen von bis zu 41% beziehen sich eher auf ältere Männer (66–74 Jahre), erfüllen in den Studien aber nicht immer die Kriterien eines Störungsbildes. Bei Frauen stehen Störungen von Lust und Erregung im Vordergrund (Tab. 4). Einige Funktionsstörungen sind stark altersabhängig; der Leidensdruck ist vor allem in den mittleren Lebensjahren am höchsten.
Tab. 4. Prävalenzraten sexueller Funktionsstörungen in Prozent [DSM-5]
|
Luststörung* |
Lubrikationsstörung* |
Schmerz |
Orgasmusstörung |
Erektionsstörung |
Ejaculatio praecox |
|
|
Männer |
1,8–41 |
– |
3,0 |
8,3 |
13–21 |
20–30** |
|
Frauen |
7–34 |
12–21 |
15 |
10–42 |
– |
– |
*Im DSM-5 sind diese beiden Störungsbilder in einer gemeinsamen Kategorie zusammengefasst, für die noch keine Prävalenzangaben vorliegen. **Bei Anwendung der neuen Definition mit nur einminütiger intravaginaler Ejakulationslatenz läge die Prävalenz nur bei 1–3%.
Für die klinische Erhebung sexueller Funktionsstörungen braucht es zunächst die Bereitschaft des Behandlers, auch über sexuelle Probleme sprechen zu wollen und zu können. Die meisten Patienten sind dankbar, wenn ihr Behandler auch für sexuelle Themen Offenheit signalisiert und zumindest eine Basiskompetenz vorweisen kann. Dafür braucht es ein Grundverständnis der Sexualphysiologie, das von jedem Mediziner erwartet werden darf. Eine entsprechend feinfühlige Anamnese und Exploration genügt in der Regel, die entsprechenden diagnostischen Kriterien zu erfragen, wobei ein besonderes Augenmerk auf die Kontextfaktoren bzw. Beschreibungskriterien gelegt werden sollte.
Darüber hinaus existieren weitere Instrumente zur Selbst- und Fremdbeurteilung, die sich für klinische und wissenschaftliche Zwecke bewährt haben und gute psychometrische Kennwerte vorweisen können:
- Die Arizona Sexual Experience Scale (ASEX) umfasst 5 Items mit 6-Punkt-Likert-Skalen, die Auskunft zu sexueller Lust, Erregung, Erektion/Lubrikation, Orgasmusfähigkeit und Befriedigung geben (Punktzahl 5–30) [25]. Aufgrund der Kürze eignet sie sich auch gut für die Anwendung in der Praxis oder Klinik.
- Der Changes in Sexual Functioning Questionnaire (CSFQ) ist in einer Lang- und Kurzversion erhältlich und ermöglicht eine etwas genauere Erfassung der unterschiedlichen Dimensionen sexuellen Erlebens [10]. Die Kurzversion beinhaltet 14 Items mit 5-stufigen Likert-Skalen, für die bei unbeeinträchtigter Sexualfunktion ein Maximalwert von 70 erreicht werden kann [21]. Für Frauen wird ein Summenwert von <41 bzw. für Männer <47 angeben, der indikativ für sexuelle Störungsbilder ist.
Diese beiden Skalen sind von der Food and Drug Administration (FDA) für klinische Studien zu Antidepressiva empfohlen worden. Des Weiteren sind Fremdbeurteilungsverfahren speziell für die Erhebung Medikamenten-assoziierter sexueller Dysfunktionen entwickelt worden, beispielsweise der Psychotropic-Related Sexual Questionnaire und der Sex Effects Scale.
Depressionen als Ursache sexueller Dysfunktionen
Etwa 50 bis 70% der depressiven Patienten leiden an sexuellen Dysfunktionen. Es ist gut nachvollziehbar, dass während schwerer depressiver Episoden nahezu alle Betroffenen kein sexuelles Verlangen verspüren. Eine Beeinträchtigung sexueller Funktion kann also als Teil der depressiven Erkrankung gesehen werden bzw. hat dann eine morbogene Ursache. Dabei kann jede einzelne Phasen des sexuellen Reaktionszyklus betroffen sein: sexuelle Lust, sexuelle Erregung und Orgasmusfähigkeit. Einer Metaanalyse zufolge erhöht Depression das Risiko für eine sexuelle Dysfunktion um 52 bis 71% [2]. Umgekehrt erhöht auch das Vorliegen einer sexuellen Dysfunktion das Risiko für eine depressive Störung um 130 bis 210%. Die Elixier-Studie hat in Frankreich an einem Kollektiv von 4557 Patienten mit Depression die Prävalenz sexueller Dysfunktionen erhoben [7]. 35% der Patienten berichteten spontan über sexuelle Probleme, während insgesamt 69% der Patienten dies taten, wenn sie auch vom Arzt darauf angesprochen wurden. Neben der hohen Prävalenz macht dies deutlich, wie wichtig es ist, Patienten auf sexuelle Probleme aktiv anzusprechen oder spezielle Erhebungsinstrumente einzusetzen. Bei Patienten, die bislang keine antidepressive Medikation erhalten hatten, lag die Prävalenz sexueller Dysfunktionen bei 65%, während Patienten unter antidepressiver Medikation in 71% der Fälle entsprechende Störungen angaben. Eine andere Studie ermittelte etwas höhere Prävalenzen von 86% bei Patienten ohne Medikation und 73% bei Patienten mit antidepressiver Behandlung [8].
Die zugrundeliegenden Mechanismen für sexuelle Dysfunktionen sind vielfältig und sollen hier nicht im Detail erörtert werden. Neben der ohnehin reduzierten Appetenz und der ausgeprägten Anhedonie in Bezug auf viele Tätigkeiten des täglichen Lebens gesellen sich sicher depressionstypische Veränderungen wie vermehrte Aktivierung der HPA-Achse, Überaktivierung des sympathischen Nervensystems und damit einhergehender Dysbalance der zentralen Exzitations- und Inhibitionszentren (verstärkte Amygdala-Aktivierung, Hippocampusatrophie etc.). Auf psychologischer Ebene sind die für sexuelle Dysfunktionen charakteristischen Verhaltensmuster wie Selbstbeobachtung, Versagensangst oder Ablenkung bei depressiven Patienten besonders stark ausgeprägt.
Antidepressiva als Ursache sexueller Dysfunktionen
Die Mehrzahl der Patienten mit Depressionen erachten sexuelle Gesundheit und Zufriedenheit als wichtig, auch wenn dies in der Akutphase der Erkrankung zunächst nicht im Vordergrund stehen mag. In einer Erhebung an 6000 Patienten mit Depression beurteilten 85% sexuelle Funktionsfähigkeit als wichtig bis extrem wichtig; lediglich 3% empfanden diesen Aspekt als nicht wichtig [11]. Abhängig vom Antidepressivum kann es bei bis zu 80% der Fälle zu Medikamenten-induzierten Nebenwirkungen bezüglich der Sexualität kommen, was Compliance und Patientenzufriedenheit zum Teil erheblich beeinträchtigt. Patienten werten sexuelle Dysfunktionen und Benommenheit/Schläfrigkeit unter Behandlung mit selektiven Serotonin-Wiederaufnahmehemmern (SSRI) als am störendsten [18] und sexuelle Dysfunktionen waren selbst nach drei Monaten Behandlung in 83% der Fälle noch vorhanden. Rosenberg et al. (2003) berichten, dass 42% der Männer und 15% der Frauen ihre antidepressive Medikation absetzten, da sie sexuelle Dysfunktionen als Nebenwirkung befürchteten oder bereits hatten [33].
Das Auftreten von sexuellen Dysfunktionen hängt ganz maßgeblich von dem pharmakologischen Profil der eingesetzten Substanz ab. Eine sehr hilfreiche Metaanalyse zu den meisten gängigen Antidepressiva ist von Serretti und Chiesa (2009) durchgeführt worden (Abb. 2).
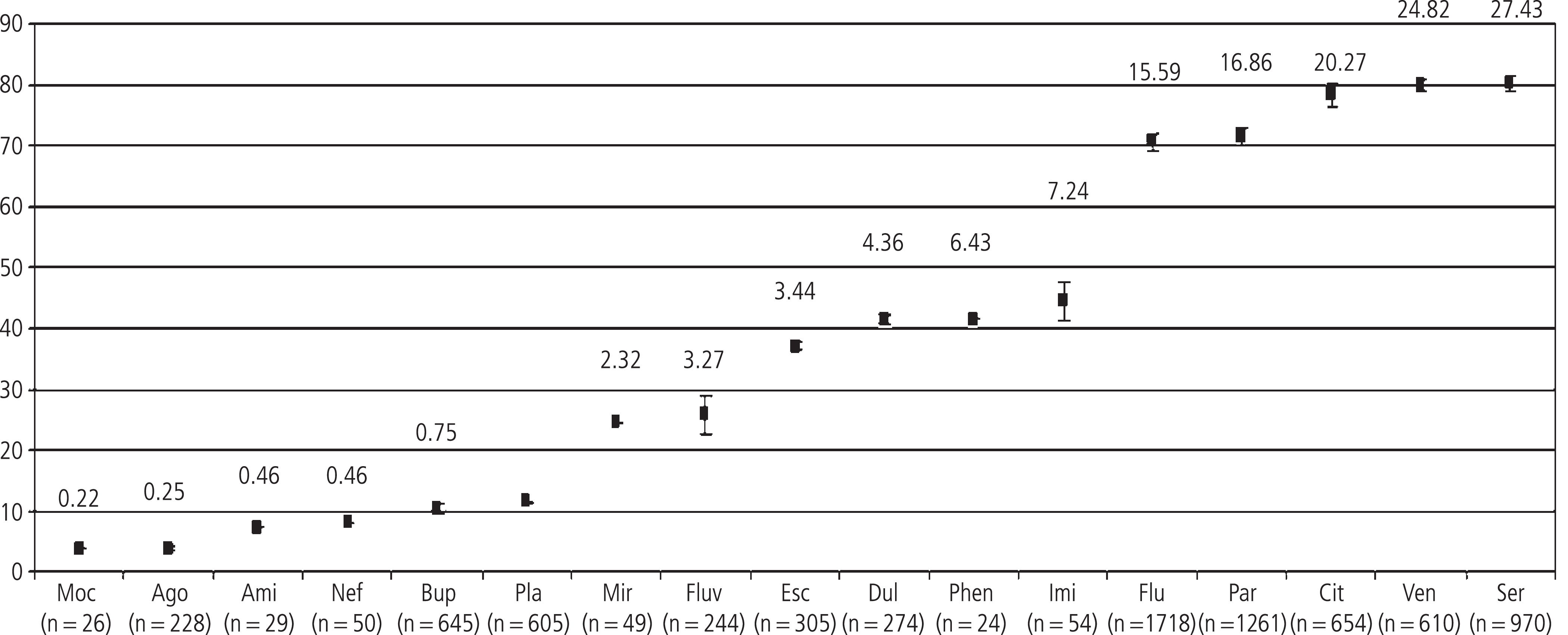
Abb. 2. Antidepressiva-induzierte sexuelle Dysfunktionen. Metaanalyse (Serretti & Chiesa 2009) zu Antidepressiva-induzierten sexuellen Dysfunktionen (Angabe in % und als Odds-Ratio) [35]. Risiko für sexuelle Dysfunktionen auf Placebo-Niveau oder im niedrigen Bereich: Moc, Ago, Ami, Nef, Bup, Mir; Arzneistoffe mit moderatem Risiko: Fluv, Esc, Dul, Phen, Imi; Arzneistoffe mit hohem Risiko: Flu, Par, Cit, Ven, Ser Ago: Agomelatin; Ami: Amineptin; Bup: Bupropion; Cit: Citalopram; Dul: Duloxetin; Esc: Escitalopram; Flu: Fluoxetin; Fluv: Fluvoxamin; Imi: Imipramin; Mir: Mirtazapin; Moc: Moclobemid; Nef: Nefazodon; Par: Paroxetin; Phe: Phenelzin; Pla: Placebo; Ser: Sertralin; Ven: Venlafaxin. (Mit freundlicher Genehmigung von Wolters Kluwer Health, Inc.)
Substanzen mit primär serotonerger Komponente (SSRI) haben demgemäß die stärksten negativen Effekte auf sexuelle Funktionen. Beeinträchtigungen von sexueller Lust und Erregung sind am ehesten über zentralnervöse Effekte vermittelt, wobei eine Veränderung der dopaminergen Transmission in Hypothalamus und mesolimbischen System angenommen werden [6]. Zudem wird von einer Hemmung der spinal lokalisierten Ejakulationszentren (Nucleus Onuf) ausgegangen, was bei Ejaculatio praecox erwünscht sein kann. Die stärksten inhibitorischen Effekte werden wahrscheinlich über 5-HT2-Rezeptoren, vor allem 5-HT2C-Subrezeptoren, vermittelt. Weitere Mechanismen kommen infrage, beispielsweise anticholinerge Effekte und eine Hemmung der NO-Synthese durch Paroxetin. In der Metaanalyse von Serretti und Chiesa findet sich das Enantiomer Escitalopram, im Gegensatz zum Racemat Citalopram, in einer Gruppe mit moderaten Risiko für sexuelle Dysfunktionen wieder – ein interessanter Befund, der aber sicher weiterer Untersuchungen im direkten Vergleich bedarf.
Substanzen mit primär noradrenerger Komponente (NRI) wie Reboxetin verhalten sich weitgehend neutral auf sexuelle Funktionen, können bei Männern jedoch zu Störungen der Ejakulation führen (möglicherweise durch Überangebot von Noradrenalin bedingt). Wie weiter oben ausgeführt, zählen Noradrenalin und Dopamin in physiologischen Konzentrationen zu den Neurotransmittern bzw. -modulatoren, die im Rahmen der sexuellen Phasen wichtige Funktionen übernehmen (z.B. psychophysiologische Erregung, Motivation).
Substanzen mit serotonerger und noradrenerger Komponente (SNRI) bleiben aufgrund der Erhöhung des serotonergen Tonus trotz der günstigen noradrenergen Effekte problematisch. Venlafaxin scheint hier ungünstiger als Duloxetin abzuschneiden, was mit der höheren Affinität zu den Serotonin-Transportern erklärt werden kann (v.a. in niedrigen Dosen). Auch Mirtazapin stimuliert die noradrenerge und serotonerge Aktivität, hat aber zugleich 5-HT1A-agonistische und 5-HT2- und 5-HT3-antagonistische Effekte, was klinisch mit einer deutlich reduzierten Rate an sexuellen Dysfunktion im Vergleich zu SSRI und SNRI einhergeht.
Substanzen mit primär noradrenerger und dopaminerger Komponente wie Bupropion verhalten sich überwiegend neutral auf sexuelle Funktionsfähigkeit und konnten sich daher im direkten Vergleich zu SSRI (Orgasmusstörungen 40% vs. 11%) oder SNRI (z.B. Venlafaxin) deutlich abgrenzen und bezüglich einiger Subskalen auf dem CSFQ sogar eine Verbesserung vorweisen [16, 38].
Weitere Substanzgruppen: Zum Zeitpunkt der klinischen Studien zu trizyklischen Substanzen sind sexuelle Funktionen selten berücksichtigt worden. Die verfügbaren Daten und die klinische Erfahrung lassen jedoch keinen Zweifel an den zum Teil erheblichen Nebenwirkungen auf sexuelle Funktionen aufkommen, die sich über serotonerge und anticholinerge Effekte erklären lassen. Die Datenlage ist ebenso mäßig umfangreich für MAO-Hemmer, unten denen Phenelzin (in Deutschland nicht zugelassen) gelegentlich bis häufig, Tranylcypromin selten und Moclobemid nicht häufiger als Placebo zu sexuellen Dysfunktionen führt [35, 14]. Agomelatin mit seinen MT1- und MT2-Rezeptor-agonistischen und 5-HT2C-Rezeptor-antagonistischen Eigenschaften weist im Vergleich zu SSRI hinsichtlich sexueller Funktionen ein günstiges Nebenwirkungsprofil auf [28].
Aktuelle Entwicklungen: Vortioxetin und Sexualität
Neue Antidepressiva müssen hinsichtlich Wirksamkeit und Nebenwirkungsprofil mit bereits zur Verfügung stehenden Substanzen vergleichbar oder besser sein. Mit Blick auf das präklinische Profil von Vortioxetin wäre zu vermuten, dass es im Vergleich zu Placebo nicht häufiger zu sexuellen Dysfunktionen kommt. Vortioxetin erhöht zwar den serotonergen Tonus im synaptischen Spalt, aufgrund eines gleichzeitigen 5-HT1A-Rezeptor-Agonismus (mit fazilitatorischen Effekten auf sexuelle Funktionen) wäre aber eine Nivellierung des Effekts zu erwarten.
Spontan berichtete sexuelle Dysfunktionen waren in einer Analyse von 14 Studien (total n=6514) bei einer Vortioxetin-Dosierung zwischen 5 und 20 mg vergleichbar mit Placebo (2,2% vs. 1,0%) und niedriger als bei Gabe von 60 mg Duloxetin (5,7%) [19]. Für Vortioxetin fand sich in dieser Analyse keine Dosisabhängigkeit. Die Mehrheit der Nebenwirkungen umfasste reduzierte sexuelle Lust und Orgasmusstörungen.
In sieben Kurzzeitstudien über einen Zeitraum von acht Wochen wurden sexuelle Funktionen mit Hilfe des ASEX-Selbstbeurteilungsfragebogens erfasst [19]. Eine dieser Studien war an Patienten mit generalisierter Angststörung durchgeführt worden. Der Einsatz eines validierten Messinstruments zur Erfassung sexueller Dysfunktionen ist positiv hervorzuheben. Nur etwa 30% der randomisierten Patienten hatten zu Beginn der Studie (Baseline) keine sexuellen Dysfunktionen, was nochmals die hohe Prävalenz von sexuellen Störungen bei Patienten mit Depression belegt. In die weiteren Analysen wurden nur die Patienten ohne initiale sexuelle Dysfunktionen einbezogen. Die gepoolten Inzidenzraten für sexuelle Dysfunktionen lagen für Placebo bei 32,0%, für Vortioxetin (5–20 mg) bei 37,1% und für Duloxetin (60 mg) bei 48,2% [19]. Die Schätzung der gemeinsamen Risikodifferenz für substanzinduzierte sexuelle Dysfunktionen erhöhte sich mit der Dosierung von Vortioxetin (5 mg: –4,6%; 20 mg: 9,9%), war aber im Vergleich zu Placebo nicht signifikant unterschiedlich (4,2%; 95%-Konfidenzintervall [KI] –2,4 bis 10,7). Für die Dosierung von 5 mg erreichte Vortioxetin das Non-Inferioritätskriterium im Placebo-Vergleich. Dosierungen von 10 und 15 mg waren hinsichtlich der Inzidenz substanzinduzierter sexueller Dysfunktionen statistisch nicht signifikant höher als Placebo. Eine Dosierung von 20 mg Vortioxetin führte zu einem Anstieg therapiebedingter sexueller Dysfunktionen (TESD). Duloxetin in einer Dosierung von 60 mg hatte eine signifikant höhere Risikodifferenz für sexuelle Dysfunktionen im Vergleich zu Placebo (15%; 95%-KI 5,8–24,1).
In einer Langzeitstudie (n=396) zur Rückfallprophylaxe über einen Zeitraum von 24 bis 64 Wochen lagen spontan berichtetet TESD bei einer Vortioxetin-Dosierung von 5 bis 10 mg auf Placebo-Niveau.
Es existieren insgesamt nur wenige klinische Studien zur Pharmakotherapie von Depressionen, die sexuelle Funktionen als primären Endpunkt definiert haben. Hierzu haben Jacobsen et al. (2014) eine Studie durchgeführt, die aufgrund ihrer Besonderheit ausführlicher dargestellt werden soll [20]. Zielsetzung dieser Studie war die Untersuchung der klinischen Auswirkungen von Vortioxetin auf die sexuelle Funktionsfähigkeit im Vergleich zu Escitalopram über acht Behandlungswochen bei Patienten, deren Depression medikamentös gut eingestellt war, die jedoch an SSRI-induzierten sexuellen Funktionsstörungen litten. Der Studienansatz umfasst zwei klinisch relevante Fragestellungen – nämlich die Frage, ob Patienten von einer Umstellung hinsichtlich ihrer sexuellen Funktionen profitieren und die Frage, ob die Umstellung ohne Komplikationen bzw. Verschlechterung der depressiven Symptomatik durchgeführt werden kann. Die Erfassung sexueller Funktionen erfolgte mittels der Kurzfassung des Changes-in-Sexual-Functioning-Fragebogens (CSFQ-14), der jedoch mehr Informationen erhebt als der ASEX-Fragebogen mit nur fünf Items.
Die Studie umfasste 447 Patienten und wurde in den USA und Kanada durchgeführt. Patienten mit der Diagnose einer depressiven Episode gemäß DSM-IV-TR (TR: Textrevision), die mindestens acht Wochen vor dem Screening-Termin eine SSRI-Monotherapie erhielten (Citalopram, Paroxetin oder Sertralin, nicht jedoch Escitalopram) und die unter sexuellen Funktionsstörungen litten, wurden eingeschlossen. Die depressive Episode musste gut eingestellt sein, das heißt, der Patient musste stabil sein (ohne klinisch relevante Schwankungen des Niveaus der Depressionssymptome) – dies wurde durch den Studienleiter mittels eines Gesamtscores der klinischen Gesamteindruck-Schwere-Skala von ≤3 beurteilt. Zudem musste die sexuelle Funktionsstörung SSRI-induziert sein (vom Studienleiter überprüft) und den Schwellenwert für sexuelle Funktionsstörungen, gemessen mittels des CSFQ-14-Gesamtscores (≤41 Frauen; ≤47 Männer), erreichen. Nach Randomisierung wurde bei alle Patienten die bisherige Medikation beendet und in der ersten Woche eine neue Behandlung mit entweder 10 mg Vortioxetin oder 10 mg Escitalopram initiiert, die nach der ersten Woche bei allen Patienten auf jeweils 20 mg erhöht wurde. Bei den Terminen der Wochen 2, 4 und 6 konnten die Dosierungen je nach Beurteilung des Studienleiters auf 10 oder 20 mg sowohl für Vortioxetin als auch für Escitalopram flexibel angepasst werden. Die sexuelle Funktionsfähigkeit (CSFQ-14) wurde in den Wochen 1, 2, 4, 6 und 8 beurteilt. Weitere Endpunkte beinhalteten die Beurteilung der Depressionssymptome nach dem Medikamentenwechsel zu Vortioxetin oder Escitalopram, bewertet durch Veränderung zum Behandlungsbeginn in der Montgomery-Åsberg Depression Rating Scale (MADRS) und Veränderung in der Clinical Global Impression Scale (CGI).
Es gab keine klinisch relevanten Unterschiede zwischen den beiden Behandlungsgruppen bezüglich der demographischen und klinischen Parameter. Die meisten Patienten befanden sich bei Behandlungsbeginn in partieller oder vollständiger Remission (durchschnittlicher MADRS: 7,9 [Vortioxetin-Gruppe] bzw. 8,3 [Escitalopram-Gruppe]), litten jedoch an erheblichen sexuellen Funktionsstörungen (durchschnittlicher CSFQ-14: 36,5 bzw. 36,3 ).
Unter beiden Behandlungsformen war eine Verbesserung der sexuellen Funktionsfähigkeit zu beobachten. Die Behandlung mit Vortioxetin brachte einen statistisch signifikanten Behandlungseffekt bezüglich des primären Endpunkts der Veränderung im CSFQ-14-Gesamtscore von Behandlungsbeginn bis zur achten Woche im Vergleich zur Behandlung mit Escitalopram (Differenz Vortioxetin vs. Escitalopram in Woche 8: 2,2 [95%-KI 0,48–4,02], p=0,013, MMRM [mixed-effects model for repeated measures]) (Abb. 3a). Behandlungsvorteile, die numerisch zugunsten von Vortioxetin ausfielen, wurden bereits in der zweiten Woche vermerkt und über die gesamten acht Wochen der Studiendauer aufrecht erhalten (statistisch signifikant in den Wochen 4 und 8). Ein ähnliches Bild zeigt sich bei der Betrachtung der CSFQ-14-Subskalen, für die mehrheitlich ein signifikanter Vorteil für Vortioxetin gezeigt werden konnte (Abb. 3b). Während der Studie kehrten mehr Patienten unter Vortioxetin zu einer normalen sexuellen Funktionsfähigkeit zurück als unter Escitalopram (52,1% vs. 44,2%; Odds-Ratio [OR] 1,37; p=0,112). Ferner sprachen mehr mit Vortioxetin behandelte Patienten auf die Therapie an (74,7% vs. 66,2%; OR 1,51; p=0,057). Response auf die Behandlung wurde definiert als Veränderung zum Baseline-CSFQ-14-Gesamtscore von mehr als drei Punkten. Während des achtwöchigen Behandlungszeitraums war keine Verschlechterung der depressiven Symptomatik (MADRS) und der klinischen Gesamtsymptomatik zu beobachten.
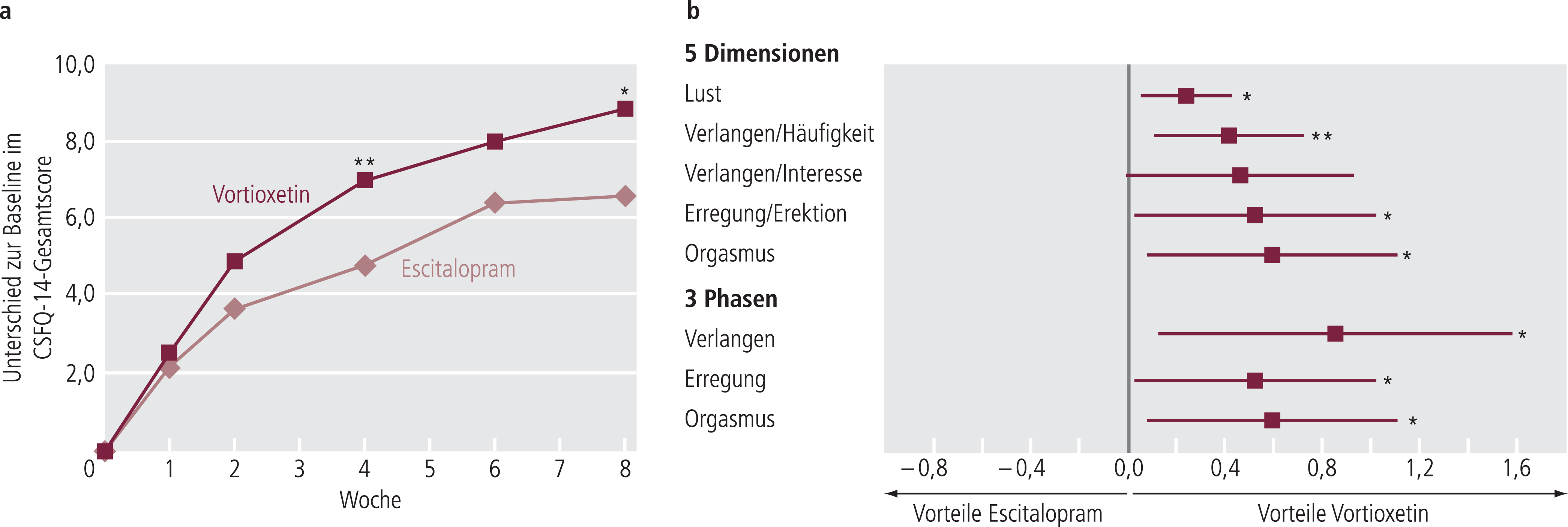
Abb. 3. Vortioxetin und sexuelle Funktionen im Vergleich zu Escitalopram bei Depressionspatienten, die unter einer vorangehenden wirksamen antidepressiven Therapie unter sexuellen Funktionsstörungen litten [20]. a) Veränderungen des CSFQ-14-Gesamtscores über den 8-wöchigen Behandlungsverlauf mit Vortioxetin (10–20 mg) und Escitalopram (10–20 mg) im Vergleich zum Ausgangswert; b) Veränderung der einzelnen Subskalen des CSFQ-14-Fragebogens unter Vortioxetin im Vergleich zu Escitalopram; *p< 0,05; **p<0,01
Insgesamt scheint sich gemäß dieser Studie eine Umstellung der antidepressiven Medikation bei Patienten mit SSRI-induzierten sexuellen Dysfunktionen auf Escitalopram oder Vortioxetin zu lohnen, wobei die Effekte für Vortioxetin größer waren. Gemäß der Metaanalyse von Serretti und Chiesa (2009) [35] hat man mit Escitalopram in Bezug auf sexuelle Funktionen möglicherweise ein verhältnismäßig nebenwirkungsarmes Antidepressivum als Vergleichstherapie gewählt. Im Vergleich zu beispielsweise Fluoxetin hätten die Unterschiede möglicherweise noch stärker ausfallen können. Das methodische Vorgehen berücksichtigt leider nicht die Kontrolle von Placebo-Effekten, von denen sowohl für Escitalopram als auch Vortioxetin auszugehen ist. Hierfür hätte man eine weitere Randomisierungsgruppe einführen müssen, die beispielsweise die alte Medikation fortführt.
Fazit und therapeutische Implikationen
Depressionen gehen häufig mit sexuellen Dysfunktionen einher – diese können sowohl morbogen als auch pharmakogen bedingt sein. Was ist zu tun und womit können Compliance und Lebensqualität unserer Patienten verbessert werden? Folgender Maßnahmenkatalog kann nützlich sein:
- Dran denken und beraten! Eventuell Einsatz von psychometrischen Screeningverfahren (ASEX, CSFQ, Derogatis Interview u.a.). Die meisten Patienten sind dankbar, wenn sich ihr Behandler auch sexueller und/oder partnerschaftlicher Probleme annimmt und zumindest eine Basiskompetenz vorweist. Dies erhöht bereits Compliance und Patientenzufriedenheit.
- Sinnhaftigkeit der Pharmakotherapie überprüfen, Dosisreduktion oder Wechsel auf ein anderes Antidepressivum. Zum Zeitpunkt der Initiierung einer antidepressiven Medikation sollten mögliche Nebenwirkungen mit dem Patienten besprochen und eine partizipative Entscheidungsfindung angestrebt werden. Wenn eine unbeeinträchtigte Sexualität als wichtig erachtet wird oder bereits sexuelle Dysfunktionen vorliegen, kann eine Ein- oder Umstellung auf Agomelatin, Bupropion, Hypericum, Moclobemid, Mirtazapin, Tianeptin oder Vortioxetin erwogen werden. Auch eine Dosisreduktion kommt unter Umständen infrage, muss aber mit dem klinischen Bild vertretbar sein.
- „Drug Holiday“ oder abwarten? Eine Unterbrechung der antidepressiven Medikation (z.B. SSRI) während des Wochenendes oder anderer Zeiten ist mit Blick auf Compliance und Absetzphänomene eher kritisch zu sehen. Bestimmte Nebenwirkungen (insbesondere gastrointestinale) können nach einigen Tagen oder wenigen Wochen zurückgehen. Dieser Effekt ist für sexuelle Funktionen aber nicht sicher belegt, außerdem könnten Patienten ungeduldig werden. Zum Teil wird sogar eine Zunahme von sexuellen Nebenwirkungen über einen Zeitraum von drei Monaten beschrieben (von initial 70% auf 83%, [18]), möglicherweise weil sich manche Patienten erst später dessen bewusst werden.
- Gegenmittel oder Augmentation? Der Markt an sexualmedizinisch verfügbaren Substanzen ist überschaubar und umfasst vorwiegend PDE-5-Inhibitoren (Sildenafil, Tadalafil, Vardenafil, Avanafil) für die erektile Dysfunktion, Androgensubstitution bei nachgewiesenem Hypogonadismus oder Dapoxetin bei Ejaculatio praecox. Fast die Hälfte der Männer mit sexueller Appetenzproblematik haben auch Erektionsprobleme und können von einem PDE-5-Hemmer profitieren. Insbesondere das positive Feedback durch eine verbesserte Erektion kann bei Männern auch lustfördernd wirken. Dieser Effekt scheint bei Frauen, bei denen PDE-5-Hemmer ebenfalls untersucht wurde, deutlich schwächer zu sein. Die zusätzliche Gabe anderer Pharmaka muss ins klinische Gesamtkonzept passen. Sowohl für Bupropion als auch für Mirtazapin liegen positive Hinweise vor, letztere Substanz sicher bedingt durch den Antagonismus am 5-HT2C-Rezeptor.
- Stellenwert von Vortioxetin: Gemäß pharmakologischem Profil und aktueller Studienlage ist aus sexualmedizinischer Sicht Vortioxetin zum gegenwärtigen Zeitpunkt als günstig einzustufen und fügt sich damit in die Reihe an Substanzen, die die sexuelle Funktionsfähigkeit weitgehend unbeeinträchtigt lassen.
Interessenkonflikterklärung
TK hat Honorare für die Beratung oder Teilnahme an einem Expertenbeirat von Allergan und Lundbeck, Honorare für Vorträge, Stellungnahmen oder Artikel von Allergan, Lilly, Lundbeck, Schwabe und Servier, Unterstützung für Kongressbesuche von Lundbeck und Otsuka sowie Forschungsbeihilfe von Trommsdorff erhalten.
Literatur
1. Ashton AK, Jamerson BD, Weinstein WL, Wagoner C. Antidepressant-related adverse effects impacting treatment compliance: Results of a patient survey. Curr Ther Res Clin Exp 2005;66:96–106.
2. Atlantis E, Sullivan T. Bidirectional association between depression and sexual dysfunction: a systematic review and meta-analysis. J Sex Med 2012;9:1497–507.
3. Balthazart J, Ball GF. Is brain estradiol a hormone or a neurotransmitter? Trends Neurosci 2006;29:241–9.
4. Bancroft J, Janssen E. The dual control model of male sexual response: a theoretical approach to centrally mediated erectile dysfunction. Neurosci Biobehav Rev 2000;24:571–9.
5. Bang-Andersen B, Ruhland T, Jorgensen M, Smith G, et al. Discovery of 1-[2-(2,4-dimethylphenylsulfanyl)phenyl]piperazine (Lu AA21004): a novel multimodal compound for the treatment of major depressive disorder. J Med Chem 2011;54:3206–21.
6. Bijlsma EY, Chan JS, Olivier B, Veening JG, et al. Sexual side effects of serotonergic antidepressants: mediated by inhibition of serotonin on central dopamine release? Pharmacol Biochem Behav 2014;121:88–101.
7. Bonierbale M, Lancon C, Tignol J. The ELIXIR study: evaluation of sexual dysfunction in 4557 depressed patients in France. Curr Med Res Opin 2003;19:114–24.
8. Bossini L, Fagiolini A, Valdagno M, Polizzotto NR, et al. Sexual disorders in subjects treated for mood and anxiety diseases. J Clin Psychopharmacol 2007;27:310–2.
9. Clayton AH, El Haddad S, Iluonakhamhe JP, Ponce Martinez C, et al. Sexual dysfunction associated with major depressive disorder and antidepressant treatment. Expert Opin Drug Saf 2014;13:1361–74.
10. Clayton AH, McGarvey EL, Clavet GJ. The changes in sexual functioning questionnaire (CSFQ): development, reliability, and validity. Psychopharmacol Bull 1997;33:731–45.
11. Clayton AH, Pradko JF, Croft HA, Montano CB, et al. Prevalence of sexual dysfunction among newer antidepressants. J Clin Psychiatry 2002;63:357–66.
12. Davison SL, Bell RJ, LaChina M, Holden SL, et al. The relationship between self-reported sexual satisfaction and general well-being in women. J Sex Med 2009;6:2690–7.
13. Finkelstein JS, Lee H, Burnett-Bowie SA, Pallais JC, et al. Gonadal steroids and body composition, strength, and sexual function in men. N Engl J Med 2013;369:1011–22.
14. Gillman PK. Advances pertaining to the pharmacology and interactions of irreversible nonselective monoamine oxidase inhibitors. J Clin Psychopharmacol 2011;31:66–74.
15. Haake P, Krueger TH, Goebel MU, Heberling KM, et al. Effects of sexual arousal on lymphocyte subset circulation and cytokine production in man. Neuroimmunomodulation 2004;11:293–8.
16. Hartmann UH, Ruffer-Hesse C, Kruger TH, Philippsohn S. Individual and dyadic barriers to a pharmacotherapeutic treatment of hypoactive sexual desire disorders: results and implications from a small-scale study with bupropion. J Sex Marital Ther 2012;38:325–48.
17. Heiman JR. Sexual dysfunction: overview of prevalence, etiological factors, and treatments. J Sex Res 2002;39:73–8.
18. Hu XH, Bull SA, Hunkeler EM, Ming E, et al. Incidence and duration of side effects and those rated as bothersome with selective serotonin reuptake inhibitor treatment for depression: patient report versus physician estimate. J Clin Psychiatry 2004;65:959–65.
19. Jacobsen PL, Clayton AH, Mahableshwarkar AR, Palo W, et al. The effect of vortioxetine on sexual dysfunction in adults with major depressive disorder or generalized anxiety disorder. Poster presented at Annual Meeting of the American Society of Clinical Psychopharmacology; 16th–19th June 2014; Hollywood, USA,2014.
20. Jacobsen PL, Mahableshwarkar AR, Chen Y, Chrones L, et al. A randomized, double-blind, head-to-head, flexible-dose study on vortioxetine vs. escitalopram on sexual functioning in adults with well-treated major depressive disorder experiencing treatment-emergent sexual dysfuntion. Poster presented at Annual Meeting of American Society of Clinical Psychopharmacology 16th–19th June 2014; Hollywood, USA, 2014.
21. Keller A, McGarvey EL, Clayton AH. Reliability and construct validity of the changes in sexual functioning questionnaire short-form (CSFQ-14). J Sex Marital Ther 2006;32:43–52.
22. Klapilova K, Brody S, Krejcova L, Husarova B, et al. Sexual satisfaction, sexual compatibility, and relationship adjustment in couples: The role of sexual behaviors, orgasm, and men‘s discernment of womenʼ’’s intercourse orgasm. J Sex Med 2015;12:667–75.
23. Lee HJ, Macbeth AH, Pagani JH, Young WS, 3rd. Oxytocin: the great facilitator of life. Prog Neurobiol 2009;88:127–51.
24. Levin RJ. Recreation and procreation: A critical view of sex in the human female. Clin Anat 2015;28:339–54.
25. McGahuey CA, Gelenberg AJ, Laukes CA, Moreno FA, et al. The Arizona Sexual Experience Scale (ASEX): reliability and validity. J Sex Marital Ther 2000;26:25–40.
26. McNulty JK, Russell VM. When „negative“ behaviors are positive: a contextual analysis of the long-term effects of problem-solving behaviors on changes in relationship satisfaction. J Pers Soc Psychol 2010;98:587–604.
27. Meyer-Lindenberg A, Domes G, Kirsch P, Heinrichs M. Oxytocin and vasopressin in the human brain: social neuropeptides for translational medicine. Nat Rev Neurosci 2011;12:524–38.
28. Montejo A, Majadas S, Rizvi SJ, Kennedy SH. The effects of agomelatine on sexual function in depressed patients and healthy volunteers. Hum Psychopharmacol 2011;26:537–42.
29. Mork A, Pehrson A, Brennum LT, Nielsen SM, et al. Pharmacological effects of Lu AA21004: a novel multimodal compound for the treatment of major depressive disorder. J Pharmacol Exp Ther 2012;340:666–75.
30. Moulier V, Fonteille V, Pelegrini-Issac M, Cordier B, et al. A pilot study of the effects of gonadotropin-releasing hormone agonist therapy on brain activation pattern in a man with pedophilia. Int J Offender Ther Comp Criminol 2012;56:50–60.
31. Nutt DJ. Beyond psychoanaleptics – can we improve antidepressant drug nomenclature? J Psychopharmacol 2009;23:343–5.
32. Pfaus JG. Pathways of sexual desire. J Sex Med 2009;6:1506–33.
33. Rosenberg KP, Bleiberg KL, Koscis J, Gross C. A survey of sexual side effects among severely mentally ill patients taking psychotropic medications: impact on compliance. J Sex Marital Ther 2003;29:289–96.
34. Schiffer B, Gizewski E, Kruger T. Reduced neuronal responsiveness to visual sexual stimuli in a pedophile treated with a long-acting LH-RH agonist. J Sex Med 2009;6:892–4.
35. Serretti A, Chiesa A. Treatment-emergent sexual dysfunction related to antidepressants: a meta-analysis. J Clin Psychopharmacol 2009;29:259–66.
36. Snoeren EM, Veening JG, Olivier B, Oosting RS. Serotonin 1A receptors and sexual behavior in female rats: a review. Pharmacol Biochem Behav 2014;121:43–52.
37. Snoeren EM, Veening JG, Olivier B, Oosting RS. Serotonin 1A receptors and sexual behavior in male rats: a review. Pharmacol Biochem Behav 2014;121:102–14.
38. Thase ME, Clayton AH, Haight BR, Thompson AH, et al. A double-blind comparison between bupropion XL and venlafaxine XR: sexual functioning, antidepressant efficacy, and tolerability. J Clin Psychopharmacol 2006;26:482–8.
39. Williams VS, Baldwin DS, Hogue SL, Fehnel SE, et al. Estimating the prevalence and impact of antidepressant-induced sexual dysfunction in 2 European countries: a cross-sectional patient survey. J Clin Psychiatry 2006;67:204–10.
Prof. Dr. med. Tillmann H.C. Krüger, Medizinische Hochschule Hannover, Klinik für Psychiatrie, Sozialpsychiatrie, und Psychotherapie, Carl-Neuberg-Straße 1, 30625 Hannover, E-Mail: krueger.tillmann@mh-hannover.de
Antidepressant treatment and sexual functions: The role of the novel antidepressant Vortioxetin
Depressive disorders are of considerable health, social, and economic relevance. The lifetime prevalence of these disorders is at least 16%. Often noticed beside loss of interest and motivation is the loss of interest in sexual activities and disturbed sexual functions. Depending on the study and severity of depressive disorder assessed, between 50–70% of cases also present with associated sexual disorders. An improvement in associated sexual dysfunction can be expected through successful treatment of the overlying depressive disorder. In many cases however this does not occur and treatment with antidepressants can cause further difficulties in sexual function. These difficulties are often experienced as disturbing by the patients and result in treatment non-compliance. Sexual disorders are of a sensitive nature and are often challenging to discuss. To that effect, special attention should be paid to an appropriate and personal antidepressant therapy, as antidepressants can affect sexual function in patients differently. Agonists on the 5HT2C-receptors, and anticholinergic and α1-antogonistic effects were proven to have negative side effects on sexual functioning. Several new antidepressants avoid these side effects by functioning through the dopaminergic and noradrenergic transmitter systems. Recently the new multimodal antidepressant Vortioxetine was introduced on the market. It has differential serotonergic properties with agonistic and antagonistic effects as well as serotonine reuptake inhibition and shows beneficial properties with regard to sexual functions.
Key words: Vortioxetine, antidepressants, sexuality, sexual dysfunction
Psychopharmakotherapie 2015; 22(03)
