Holger Petri, Bad Wildungen*
Substrate von CYP2D6
Codein und Dihydrocodein
Codein und sein Derivat Dihydrocodein entfalten ihre hustenstillende Wirkung durch Bindung an die µ-Opioid-Rezeptoren im supraspinalen Hustenzentrum [7]. Aus Codein entsteht über das Cytochrom-P450(CYP)-Isoenzym 2D6 der pharmakologisch aktive Metabolit Morphin [10]. Unabhängig von weiteren Medikamenten ist das Ansprechen auf die Therapie mit Codein individuell verschieden.
CYP2D6 besitzt eine ausgeprägte pharmakogenetische Variabilität. Es werden abhängig von der Metabolisierungsaktivität vier Phänoytpen unterschieden [11].
- Langsame Metabolisierer (Poor metabolizer; PM) → stark reduzierter Stoffwechsel
- Intermediäre Metabolisierer (Intermediate metabolizer; IM) → reduzierter Stoffwechsel
- Extensive Metabolisierer (Extensive metabolizer; EM) → normaler Stoffwechsel
- Ultraschnelle Metabolisierer (Ultrarapid metabolizer; UM) → beschleunigter Stoffwechsel
Vor dem Hintergrund des Intoxikationsrisikos (Atemstillstand) bei Patienten mit UM-Phänotyp hat das Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM) im August 2013 die Anwendung von Codein als Analgetikum bei Kindern eingeschränkt und weitere sicherheitsrelevante Aktualisierungen der Produktinformationen angeordnet [1]. Zur Zeit können Codein-haltige Arzneimittel in Deutschland als Hustentherapeutikum Kindern über zwei Jahren noch verordnet werden. Das beschriebene Risiko einer tödlichen Atemdepression besteht aber unabhängig der Indikation. Das BfArM sieht die Notwendigkeit der Nutzen-Risiko-Bewertung auch für diese Indikation und hat deshalb ein europäisches Folgeverfahren zur Beurteilung der Sicherheit von Codein bei der Behandlung von Husten veranlasst [8].
Nicht nur die ausgeprägte pharmakogenetische Variabilität unterscheidet CYP2D6 von anderen CYP-Isoenzymen. Es ist auch durch Xenobiotika kaum induzierbar [11]. Morphin-Intoxikationen durch die Komedikation mit anderen Substanzen sind somit nicht zu befürchten.
Bei extensiven Metabolisierern wird in Kombination mit potenten CYP2D6-Hemmern (Abb. 1) wie bei Patienten mit PM- oder IM-Status die Konversion des Prodrugs Codein zu Morphin unterdrückt und es besteht die Gefahr des Therapieversagens, da hauptsächlich Morphin für die antitussive Wirksamkeit verantwortlich ist [8].
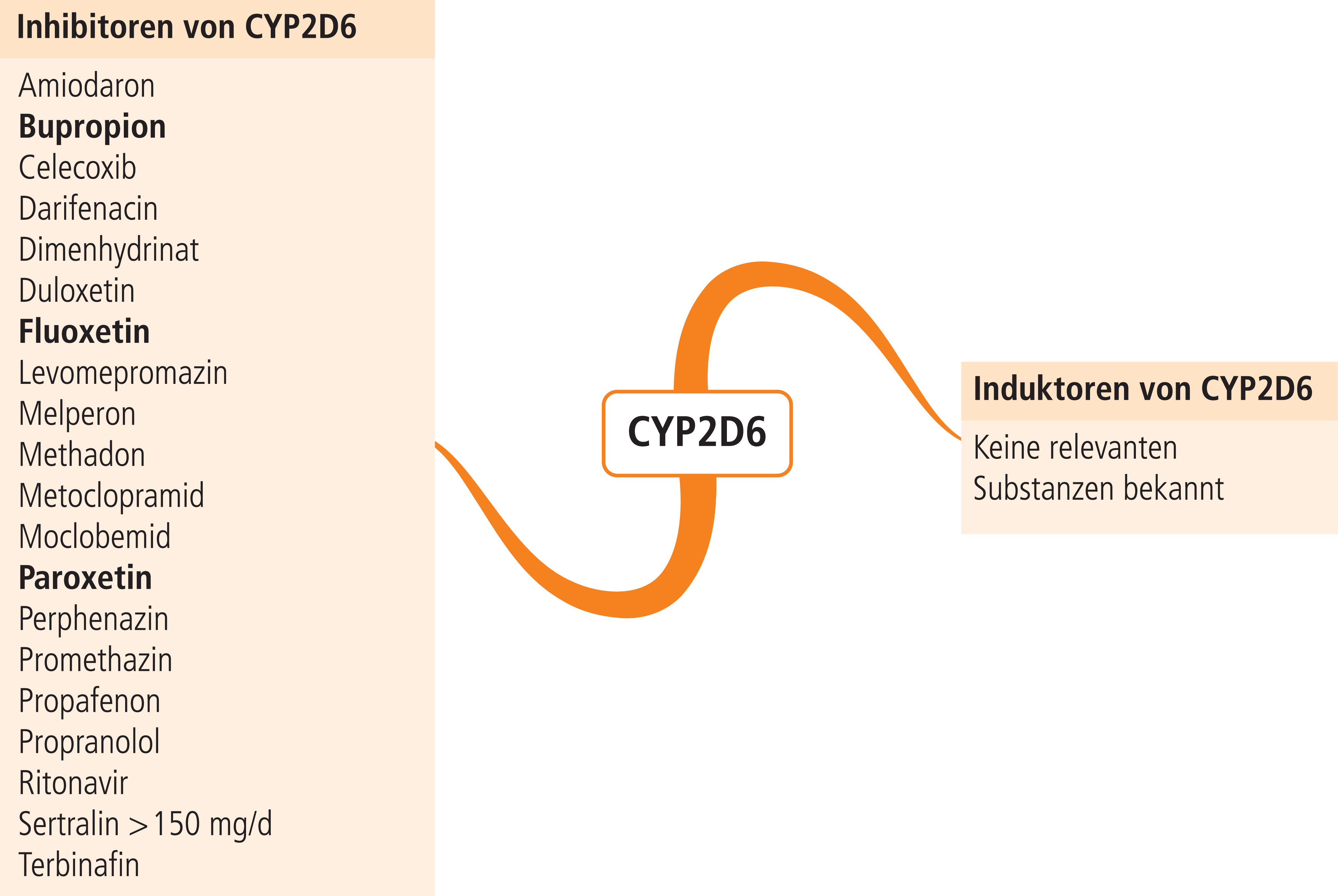
Abb. 1. Auswahl von modulierenden Substanzen (stark wirkende fettgedruckt) mit klinisch relevanter Wirkung auf Cytochrom P450 2D6 (Stand: 08/2014) [Quelle: mediQ-Interaktionsprogramm]
Der CYP2D6-Phänotyp und die Komedikation mit CYP2D6-hemmenden Substanzen spielen für das therapeutische Ansprechen von Dihydrocodein eine untergeordnete Rolle, da anders als bei Codein, die Muttersubstanz selbst pharmakologisch wirksam ist [10].
Dextromethorphan
Die Bedeutung von CYP2D6 für den Metabolismus von Dextromethorphan (DMP) zeigt sich schon daran, dass das Antitussivum als Modellsubstanz zur Phänotypisierung des CYP2D6-Phänotyps Verwendung findet [11]. Als aktiver Metabolit entsteht über CYP2D6 Dextrorphan (DO). Im Gegensatz zu Codein und Dihydrocodein kommt die antitussive Wirkung von DMP und DO nicht über µ-Opioid-Rezeptoren, sondern durch die antagonistische Wirkung an NMDA- und agonistische Wirkung an Sigma-Rezeptoren zustande [12]. Die hustenstillende Wirkung ist unabhängig vom CYP2D6-Phänotyp oder der Komedikation mit CYP2D6-Hemmern, jedoch unterscheidet sich das Nebenwirkungsprofil. Probanden mit PM- bzw. IM-Phänotyp hatten unter DMP in üblicher Einmal- oder Doppeldosis gegenüber normalen Metabolisierern (EM) ein vierfach bzw. dreifach erhöhtes Risiko für unerwünschte Arzneimittelwirkungen wie Schlaflosigkeit, Übelkeit, Schwindel und Kopfschmerzen [13]. DO besitzt eine höhere Affinität zum NMDA-Rezeptor und blockiert diesen stärker als die Muttersubstanz. Die Hemmung von NMDA-Rezeptoren birgt das Risiko für psychotische Nebenwirkungen ebenso wie für Missbrauch. Schnelle Metabolisierer (UM) besitzen für diese Nebenwirkungen wegen der höheren DO-Plasmaspiegel gegenüber normalen Metabolisierern ein erhöhtes Risiko [11].
Die Abbauhemmung von DMP wird therapeutisch genutzt zur symptomatischen Behandlung der pseudobulbären Affektstörung bei Erwachsenen. DMP ist in einer Fixkombination mit Chinidin verfügbar (Nuedexta®; seit Juni 2013 in der EU zugelassen), wodurch der DMP-Abbau zu DO gehemmt wird [3].
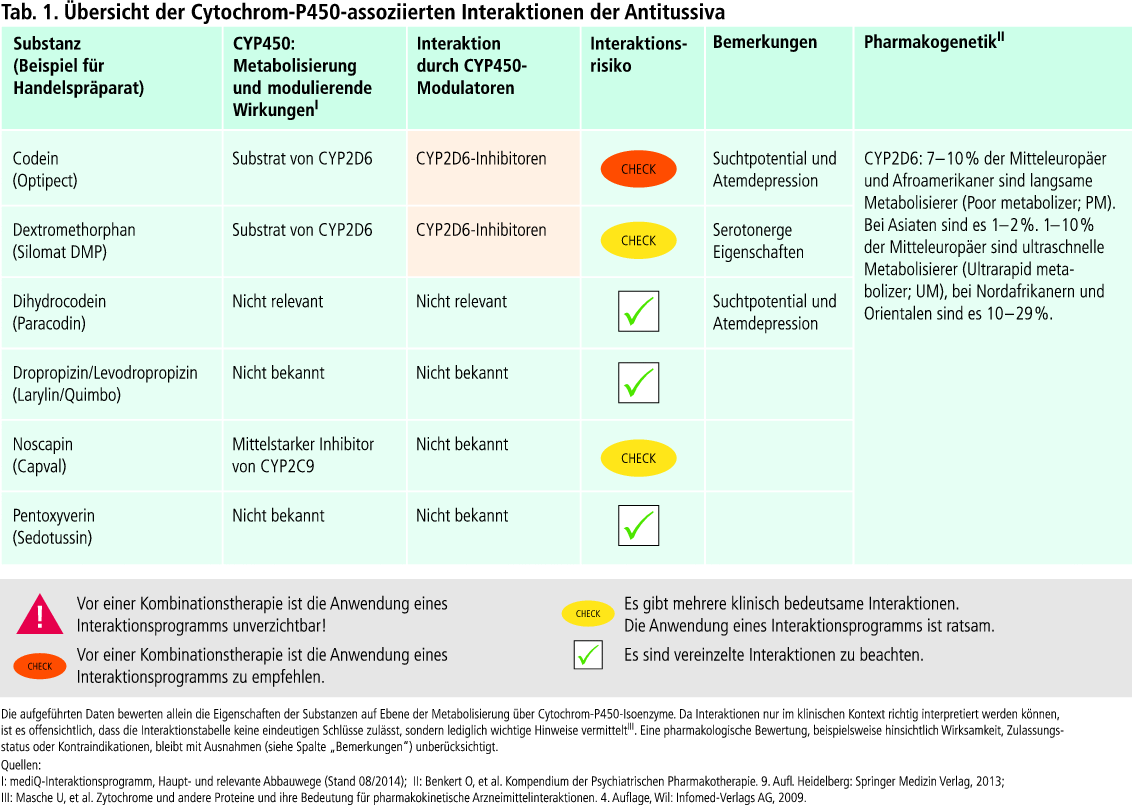
Tabelle 1 enthält Angaben zur Häufigkeit von genetischen Polymorphismen, auch unter Berücksichtigung ethnischer Gruppen.
Hemmung von CYP2C9
Noscapin
Noscapin ist ein Isochinolinderivat und nicht strukturverwandt mit Morphin [4]. Analog zu Dextromethorphan wird unter anderem eine agonistische Wirkung an Sigma-Rezeptoren für die Wirkung angenommen [12]. Noscapin ist kein Substrat der Cytochrom-P450-Isoenyzme. Verschiedene Fallberichte von schwerwiegenden Blutungen und erhöhten INR-Werten bei Komedikation mit Warfarin deuten darauf hin, dass Noscapin insbesondere CYP2C9 hemmt, über das das primär wirksame S-Enantiomer des Vitamin-K-Antagonisten abgebaut wird [9]. Deshalb ist Vorsicht geboten bei Patienten, die mit Vitamin-K-Antagonisten behandelt werden oder Medikamente mit einer engen therapeutischen Breite einnehmen, deren Abbau wesentlich von CYP2C9 abhängt [6].
Leitlinienempfehlungen zur Hustentherapie
Die Leitlinie der Deutschen Gesellschaft für Allgemeinmedizin und Familienmedizin (DEGAM) empfiehlt bei akutem Husten im Rahmen eines Infekts nur in Ausnahmefällen den Einsatz von Antitussiva. Antitussiva wirken gegen den Hustenreiz nicht besser als Plazebo [2]. Plazebo hat gegenüber „Nichtbehandlung“ beim Husten einen starken Effekt, der auf eine zentrale Hustenregulation über endogene Opioide zurückgeführt wird [7]. Somit ist erklärbar, dass sie die Fähigkeit zu schlafen verbessern. Bei akutem Husten sollte sich die Anwendung von Antitussiva auf die abendliche Einnahme bei nichtproduktivem und quälendem Reizhusten für maximal 14 Tage beschränken.
Zur Behandlung von chronischem Husten (>8 Wochen) ist die Verwendung von Präparaten, die kein Codein enthalten, der Gabe von Codein-Derivaten (Codein und Dihydrocodein) vorzuziehen (cave: Suchtpotenzial und Atemdepression durch Codein-haltige Präparate) [2].
Zu den Nicht-Opioid-Antitussiva (Dropropizin, Levodropropizin und Pentoxyverin) findet sich zur Indikation akuter Husten beim Erwachsenen und chronischer Husten kaum wissenschaftliche Evidenz [5]. Klinisch relevante Interaktionen auf Ebene der Cytochrom-P450-Enzyme mit anderen Substanzen sind nicht zu erwarten (Tab. 1).
Literatur
1. BfArM. Codein: Anwendungsbeschränkung bei der Schmerzbehandlung von Kindern, 22. August 2013. www.bfarm.de/SharedDocs/Risikoinformationen/DE/TA/PRAC-Referrral/TA-codein.html (Zugriff am 02.04.2014).
2. DEGAM-Leitlinie Nr. 11: Husten. Stand Februar 2014.
3. European Medicine Agency. Zusammenfassung des EPAR für Nuedexta. Stand: Juni 2013.
4. Fachinformation Capval®. Stand: Dezember 2012.
5. Holzinger F. Persönliche Korrespondenz vom 17. Juni 2014.
6. Kämmerer W. Portrait eines Enzyms – CYP2C9. Arzneimitteltherapie 2012;30:123–5.
7. Kardos P, et al. Leitlinie der Deutschen Gesellschaft für Pneumologie und Beatmungsmedizin zur Diagnostik und Therapie von erwachsenen Patienten mit akutem und chronischem Husten. Pneumologie 2010;64:336–73.
8. Lauktien G (BfArM). Codein: Risiko der Morphinintoxikation bei der Behandlung von Husten und Erkältungskrankheiten bei Kindern und Jugendlichen. Bulletin zur Arzneimittelsicherheit 2014; Ausgabe 2:03–06.
9. Ohlsson S, et al. Noscapine may increase the effect of warfarin. Br J Clin Pharmacol 2007;65:277–8.
10. Petri H. Das Interaktionspotenzial niederpotenter Opioide. Krankenhauspharmazie 2014;35:161–3.
11. Reinecke K, Böhm R, Haen E, Cascorbi I, et al. Arzneimittel und CYP2D6. Dtsch Apo Ztg 2012;152:5762-8.
12. Reynolds SM, et al. The pharmacology of cough. Trends Pharmacol Sci 2004;25:569–76.
13. Röhm S. Arzneimitteltherapiesicherheit für Dextromethorphan in der Selbstmedikation – ein Beitrag des Apothekers zur personalisierten Arzneimitteltherapie. Inauguraldissertation, Universität Düsseldorf. Februar 2010.
*Nachdruck aus Krankenhauspharmazie 2014;35:353–6.
Der Artikel wurde unter Einbeziehung von Diskussionsbeiträgen von Dr. Jörg Brüggmann, Berlin, Prof. Dr. Christoph Hiemke, Mainz, und Dr. Jochen Weber, Bad Wildungen, erstellt.
Holger Petri, Zentral-Apotheke der Wicker Kliniken, Im Kreuzfeld 4, 34537 Bad Wildungen, E-Mail: hpetri@werner-wicker-klinik.de
Psychopharmakotherapie 2014; 21(05)
