Holger Petri, Bad Wildungen*
Substrate von CYP3A4
Buprenorphin ist ein Substrat des Cytochrom-P450(CYP)-Isoenzyms 3A4. Ketoconazol, ein starker CYP3A4-Inhibitor, erhöhte in einer Studie zu Wechselwirkungen die Plasmaspiegel von Buprenorphin [8]. Bei transdermaler Anwendung von Buprenorphin wurde kein klinisch relevanter Hemmeffekt von Ketoconazol festgestellt [10]. Bei sublingualer Anwendung von Buprenorphin wird daher empfohlen, Patienten, die mit CYP3A4-Hemmern behandelt werden, genau zu überwachen und gegebenenfalls die Dosis zu reduzieren. Buprenorphin wirkt als Partialagonist an den µ-Opioid-Rezeptoren (Ceiling-Effekt). Bei Opioid-toleranten Patienten ist eine klinische Relevanz der Kombination von Buprenorphin mit Proteasehemmern, geboostert mit dem starken CYP3A4-Hemmer Ritonavir (Abb. 1), nicht nachgewiesen [6].
Die Auswirkungen der gleichzeitigen Gabe mit CYP3A4-Induktoren, zum Beispiel Carbamazepin oder Johanniskraut, sind nicht näher untersucht worden. Mit einer Absenkung der Plasmaspiegel in den subtherapeutischen Bereich ist aber zu rechnen.
Fentanyl wird hauptsächlich über CYP3A4 metabolisiert. Die gleichzeitige Anwendung von transdermal appliziertem Fentanyl und CYP3A4-Inhibitoren wird nicht empfohlen, es sei denn, der Patient wird engmaschig auf Anzeichen einer Atemdepression überwacht. Die Fachinformation führt hierbei nicht nur starke CYP3A4-Hemmer wie Clarithromycin, Itraconazol oder Ritonavir auf, sondern auch moderat hemmende Substanzen wie Amiodaron, Fluconazol oder Verapamil.
Bei gleichzeitiger Gabe von CYP3A4-Induktoren kann die therapeutische Wirkung ausbleiben und eine Dosiserhöhung notwendig werden [16]. Nach Absetzen des CYP3A4-Induktors steigen allmählich (Deinduktionszeit) die Fentanyl-Plasmaspiegel mit der Gefahr einer schweren Atemdepression. In diesem Fall wird eine spezielle Patientenüberwachung gefordert [1].
Fentanyl als Phenylpiperidin-Opioid hat serotonerge Eigenschaften und wird vor allem bei Kombination mit weiteren serotonerg wirksamen Substanzen als Auslöser eines Serotonin-Syndroms beschrieben (pharmakodynamische Interaktion). Das Risiko dieser dosisabhängigen Nebenwirkung steigt durch die Komedikation mit CYP3A4-Hemmern.
Oxycodon wurde 1916 entwickelt und ein Jahr später als schmerz- und hustenstillendes Mittel auf den Markt gebracht. Trotzdem ist der Metabolismus von Oxycodon über die Cytochrom-P450-Enzyme erst in den letzten Jahren intensiv erforscht worden. Dabei wurde festgestellt, dass CYP3A4 das Hauptenzym und CYP2D6 ein Nebenenzym für den Abbau ist [15]. Während in der Fachinformation von Oxycodon noch behauptet wird, dass die Hemmung von CYP2D6 und CYP3A4 keine klinische Relevanz hat, wird in der von Oxycodon/Naloxon auf veränderte Plasmakonzentrationen in Kombination mit CYP3A4-Modulatoren hingewiesen, die unter Umständen eine Dosisanpassung erforderlich machen [3, 7]. Hingegen wird in einer „black box warning“ sogar vor einer potenziell lebensbedrohlichen Atemdepression bei gleichzeitiger Anwendung von CYP3A4-Hemmern gewarnt [13]. Untersuchungen mit den beiden starken CYP3A4-Modulatoren Voriconazol und Rifampicin bestätigen den Einfluss von CYP3A4 als Hauptabbauweg von Oxycodon [9, 12].
Inwiefern eine Hemmung oder der Phänotyp von CYP2D6 von klinischer Relevanz ist, wird in den Studien unterschiedlich betrachtet und bedarf weiterer Forschung [11, 14].
Der Metabolismus von Hydromorphon, Morphin und Tapentadol ist unabhängig von Cytochrom-P450-Enzymen. Die Opioide werden primär durch Konjugation mit Glucuronsäure zu Glucuroniden metabolisiert [2, 4, 5]. Diese Phase-II-Reaktion der Biotransformation wird über Uridin-Diphosphat-Glucuronyl-Transferasen (UGT) katalysiert. Aus Morphin entsteht beispielsweise über UGT2B7 ein 6-Glucuronid (M6G), das zum therapeutischen Effekt maßgeblich beiträgt. Auf Ebene der Cytochrom-P450-Enyzme sind klinisch relevante Wechselwirkungen von Hydromorphon, Morphin und Tapentadol mit anderen Substanzen nicht zu erwarten.
Tapentadol birgt in Kombination mit serotonergen Arzneimitteln das Risiko für ein Serotonin-Syndrom [4].
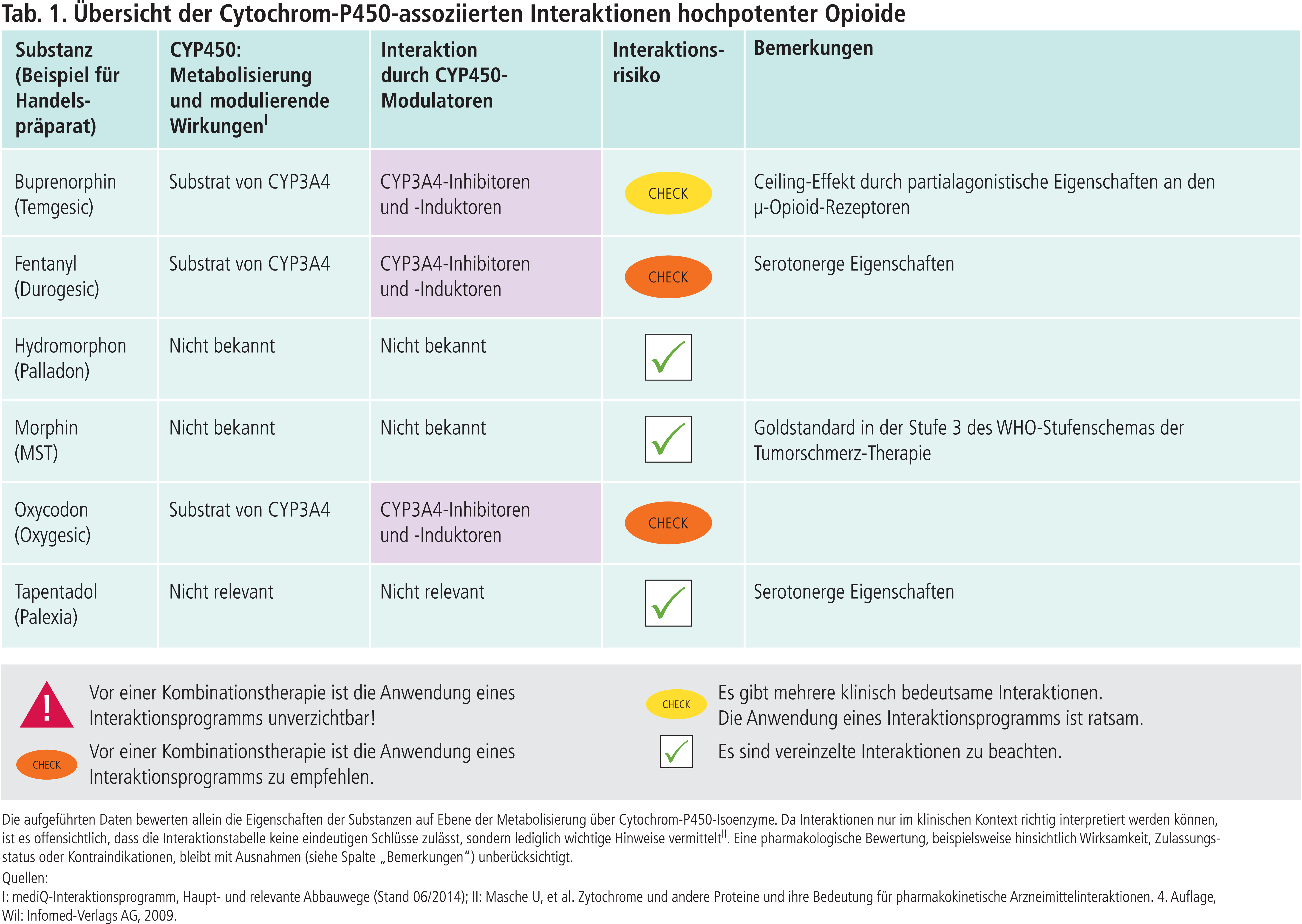
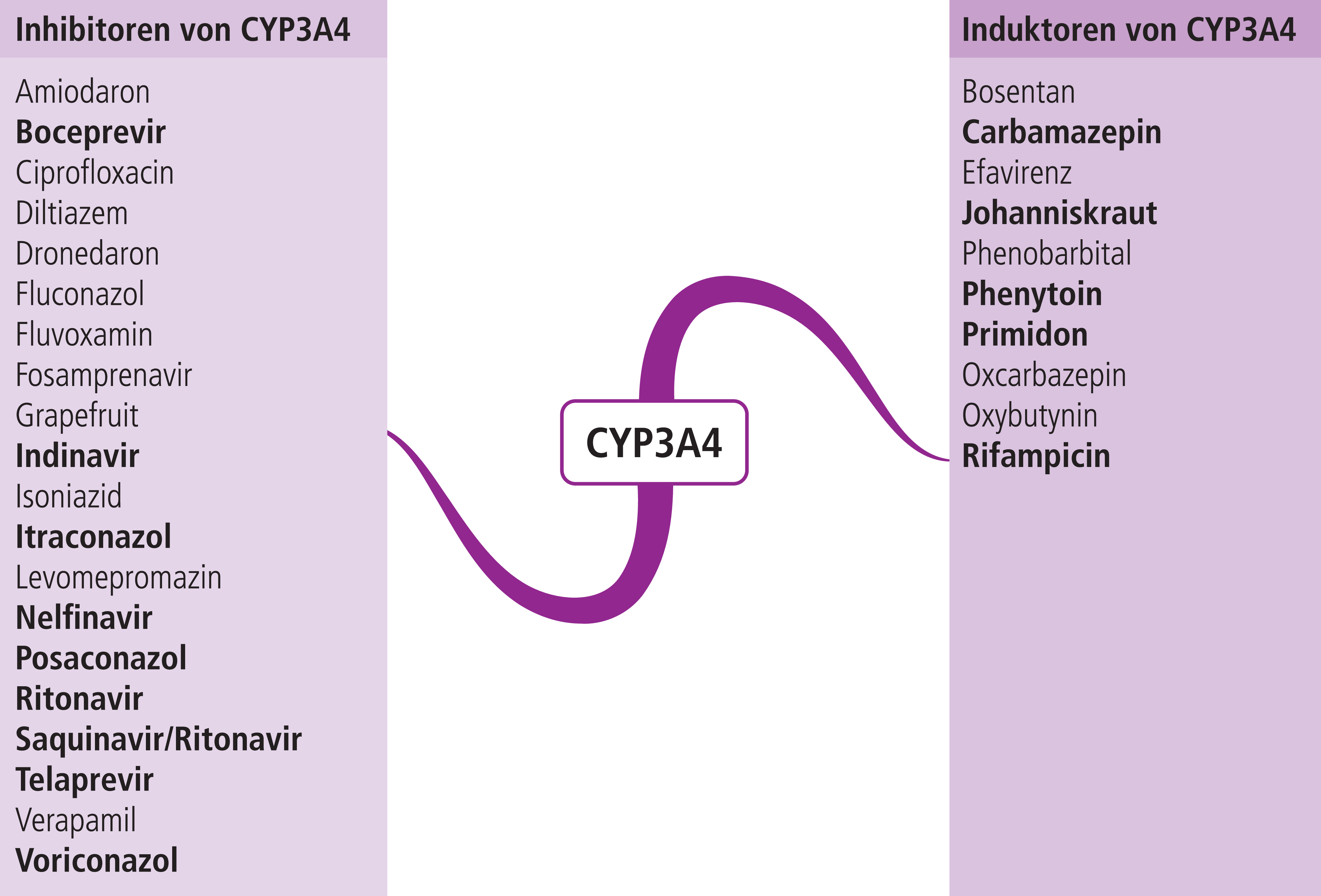
Abb. 1. Auswahl der modulierenden Substanzen (stark wirkende fettgedruckt) mit klinisch relevanter Wirkung auf Cytochrom P450-3A4 (Stand 06/2014) [Quelle: mediQ-Interaktionsprogramm]
Literatur
1. Fachinformation Durogesic®. Stand: Januar 2013.
2. Fachinformation MST Mundipharma®. Stand: Oktober 2013.
3. Fachinformation Oxygesic®. Stand: August 2011.
4. Fachinformation Palexia®. Stand: Oktober 2013.
5. Fachinformation Palladon®. Stand: August 2011.
6. Fachinformation Prezista®. Stand: Oktober 2013.
7. Fachinformation Targin®. Stand: Januar 2013.
8. Fachinformation Temgesic®. Stand: April 2012.
9. Hagelberg NM, Nieminen TH, Saari TI, et al. Voriconazole drastically increases exposure to oral oxycodone. Eur J Clin Pharmacol 2009;65:263–71.
10. Kapil RP, et al. Effect of ketoconazole on the pharmacokinetic profile of buprenorphine following administration of a once-weekly buprenorphine transdermal system. Clin Drug Investig;32:583–92.
11. Klimas R, Witticke D, El Fallah S, Mikus G. Contribution of oxycodone and its metabolites to the overall analgesic effect after oxycodone administration. Expert Opin Drug Metab Toxicol 2013;9:517–28.
12. Nieminen TH, Hagelberg NM, Saari TI, et al. Rifampicin greatly reduces the plasma concentrations of intravenous and oral oxycodone. Anesthesiology 2009;110:1371–8.
13. Prescribing information OxyContin®. Stand: 2010.
14. Samer CF, Daali Y, Wagner M, et al. Genetic polymorphisms and drug interactions modulating CYP2D6 und CYP3A4 activities have a major effect on oxycodone analgesic efficacy and safety. Br J Pharmacol 2010;160:919–30.
15. Söderberg Löfdal KC, et al. Cytochrome P450-mediated changes in oxycodone pharmacokinetics/pharmacodynamics and their clinical implications. Drugs 2013;73:533–43.
16. Tempelhoff R, et al. Anticonvulsant therapy increases fentanyl requirements during anaesthesia for craniotomy. Can J Anaesth 1990;37:327–32.
*Nachdruck aus Krankenhauspharmazie 2014;35:283–5.
Der Artikel wurde unter Einbeziehung von Diskussionsbeiträgen von Dr. Jörg Brüggmann, Berlin, Prof. Dr. Christoph Hiemke, Mainz, und Dr. Jochen Weber, Bad Wildungen, erstellt.
Holger Petri, Zentral-Apotheke der Wicker Kliniken, Im Kreuzfeld 4, 34537 Bad Wildungen, E-Mail: hpetri@werner-wicker-klinik.de
Psychopharmakotherapie 2014; 21(04)
