Gerd Laux, Soyen/München, und Christoph Goemann, Hamburg
Epidemiologie der Depression
Depressionen gehören weltweit zu den häufigsten psychischen Störungen. Die durchschnittliche Lebenszeit-Prävalenz der Depression (depressive Episode, Major Depression) liegt in zehn Ländern mit den höchsten Einkommen bei 14,6%, die durchschnittliche 12-Monats-Prävalenz bei 5,5%. Die entsprechenden Werte für Deutschland liegen bei 9,9% für die Lebenszeitprävalenz und bei 3% für die 12-Monats-Prävalenz. Dabei ist für Frauen die Prävalenz etwa doppelt so hoch wie für Männer; das durchschnittliche Alter der Patienten bei der ersten Diagnose liegt in Deutschland bei 27,6 Jahren [3]. Erweitert man die Definition der Erkrankung auf „Depressionen und depressive Verstimmungen“, wie in der Studie zur Gesundheit Erwachsener in Deutschland (DEGS), ergibt sich für Deutschland eine 12-Monats-Prävalenz von etwa 8% (Frauen 10%, Männer 6%) und eine Lebenszeitprävalenz diagnostizierter Depressionen von knapp 12% (Frauen 15%, Männer 8%) [9]. Die WHO schätzt, dass im Jahre 2030 Depressionen zu den drei führenden volkswirtschaftlichen Krankheitsbelastungen weltweit gehören werden [26].
Der Verlauf der Erkrankung ist gekennzeichnet durch ein hohes Rückfallrisiko: mindestens 50% der Patienten, die eine depressive Episode durchgemacht haben, erleben ein oder mehrere weitere Episoden in ihrem Leben. Jede weitere Episode erhöht die Wahrscheinlichkeit eines Rückfalls [4]. Depressionen führen zu erheblichen sozialen und physischen Störungen bis hin zur Invalidität. Gleichzeitig beginnt die Erkrankung häufig schon bei Jugendlichen oder jungen Erwachsenen, sodass Depressionen heute ein führender Grund für Invalidität bei Patienten mitten im Arbeitsleben sind [35, 36]. Etwa 10 bis 15% der Patienten mit schweren Depressionen begehen Suizid; insgesamt sinkt die Lebenserwartung von Patienten mit Depressionen um etwa zehn Jahre; einerseits durch das erhöhte Suizidrisiko, aber auch durch die negativen Auswirkungen der Depression auf Begleiterkrankungen [1] oder durch das erhöhte Risiko, weitere Erkrankungen, beispielsweise Herz-Kreislauf-Krankheiten, zu entwickeln [39].
Schon dieser sehr kurze Blick auf die Epidemiologie der Depression und die Folgen der Erkrankung für Patienten, ihre Angehörigen und die Volkswirtschaft macht deutlich, welche Bedeutung der erfolgreichen Behandlung dieser Erkrankung zukommt.
Entwicklung der Antidepressiva
Seit den 1960er-Jahren stehen neben psychotherapeutischen Methoden wirksame Medikamente zur Behandlung der Depression zur Verfügung. Die ältesten unter diesen Medikamenten sind die sogenannten trizyklischen Antidepressiva (TZA) – nichtselektive Monoamin-Rückaufnahme-Inhibitoren (NSMRI) – und die Monoaminoxidase(MAO)-Hemmer basierend auf den Neurotransmitter-Hypothesen der Depression („Noradrenalin-, Serotonin-Mangel“). Beide Substanzklassen weisen zahlreiche Nebenwirkungen auf. Es wurden dann selektive neue Antidepressiva entwickelt, die Serotonin(SSRI)- bzw. Serotonin/Noradrenalin-Wiederaufnahmehemmer (SNRI) sowie Noradrenalin-Dopamin-Wiederaufnahmehemmer (selektive bzw. sogenannte duale Substanzen) [24]. Auch ein selektiver Melatoninagonist und Serotonin-Rezeptorsubtyp-Antagonist ist inzwischen verfügbar [8].
Die erhoffte Verbesserung der antidepressiven Wirksamkeit konnte mit diesen Substanzen nicht erreicht werden. Ältere wie neuere Antidepressiva haben die Wirklatenz sowie klinisch relevante unerwünschte Wirkungen gemeinsam, bei den SSRI und SNRI insbesondere Übelkeit, Gewichtszunahme und gestörte Sexualfunktion, was zu Therapieabbrüchen führt.
Studien in der Primärversorgung zeigten, dass weniger als 50% der depressiven Patienten ihre Medikamente länger als 12 Wochen gemäß den Therapieempfehlungen einnehmen. Als Hauptursachen hierfür werden Nebenwirkungen oder mangelnde Wirksamkeit angegeben [10]. Alle Antidepressiva wirken nur bei einem Teil der Patienten: nur 25 bis 40% der Patienten erlangen mit dem ersten eingesetzten Antidepressivum volle Remission [6, 41].
„Unmet needs“
In den letzten Jahren ist das Bewusstsein der schwerwiegenden Folgen und der unbefriedigenden Situation der Behandlung von Depressionen gewachsen. Unter der Überschrift „unmet needs – unbefriedigte Bedürfnisse“ werden die unterschiedlichsten Faktoren diskutiert: vom Fehlen einer Behandlung für viele Patienten [33] über Forderungen nach neuen und besseren Diagnosekriterien [10, 21] oder neuen Behandlungszielen [28] bis zu den psychosozialen Funktionsaspekten der betroffenen Patienten („patientenrelevanten Endpunkten“, „social functioning“) [20]. Formuliert werden „unmet needs“ heute nicht nur von Ärzten und dem Pflegepersonal, sondern auch von Behörden, Patienten und ihren Angehörigen, wobei die Anforderungen der verschiedenen Interessensgruppen nicht unbedingt identisch sind (Tab. 1).
Tab. 1. „Unmet needs“ depressiver Patienten aus Sicht der Ärzte und Patienten
|
|
Arzt |
Patient |
|
Sartorius (2005) |
Verminderung der Suizidalität |
Involvierung in die Therapie |
|
Schneller Wirkungseintritt |
Vollständige Remission |
|
|
Verkürzte Interventionsphase |
Keine Beeinträchtigung der Funktionalität |
|
|
Kennedy (2008) |
Verminderung der Nebenwirkungen |
Verminderung der Nebenwirkungen |
|
Schneller Wirkungseintritt |
Erhöhung der Compliance |
|
|
Erhöhung der Response |
Erhöhung der Response |
|
|
Danner (2011) |
Verbesserung der Remissionsrate |
Erhöhung der Response |
|
Verhinderung eines Rezidivs |
Reduktion der Angst |
|
|
Verbesserung der sozialen Funktionalität |
Verbesserung der Kognition |
|
|
Fazit: |
1. Arzt und Patient haben spezifische Anforderungen an eine antidepressive Therapie |
|
|
2. Arzt und Patient benennen Schwerpunkte in |
||
Als patientenrelevante Outcome-Maße werden von Ärzten und Patienten Response, Besserung von kognitiven Funktionen, Angstreduktion, Besserung sozialer Funktionseinbußen und die wirksame Rezidivprophylaxe priorisiert [7].
Hier soll es im Folgenden in erster Linie um die „unmet needs“ in der Arzneimitteltherapie der Depression gehen, um die Anforderungen, die wir an zukünftige Antidepressiva stellen.
Die meisten der heute eingesetzten Substanzen haben jeweils nur einen pharmakologischen Wirkungsmechanismus, nämlich die Hemmung des Serotonin-Transporters (SERT) beziehungsweise der Serotonin- und Noradrenalin-Transporter (NAT). Die älteren TZA und MAO-Hemmer, die bezüglich der Wirksamkeit durchaus mit der neuen Generation von Antidepressiva vergleichbar sind, besitzen mehrere Mechanismen, die jedoch nicht alle therapeutisch erwünscht sind und zu zahlreichen Nebenwirkungen führen können. Vor allem um die Verträglichkeit zu verbessern, wurde daher bei der Entwicklung der heutigen Generation von Antidepressiva ganz bewusst nach hochselektiven Substanzen mit nur einem Wirkungsmechanismus gesucht; Substanzen mit multiplen Mechanismen gerieten für viele Jahre in den Ruf, „dirty drugs“ zu sein. Der Einsatz der neueren Antidepressiva (SSRI, SNRI) hat insgesamt zu einer Verbesserung der Verträglichkeit der Therapien geführt und daraus resultierend auch zu einer leichte Verbesserung der Compliance. Nach wie vor bestehen aber folgende Problemfelder in der Antidepressiva-Therapie:
- Relativ hohe Non-Response-/Non-Remissions-Raten
- „Residualsymptome“
- Wirklatenz
- Unerwünschte Arzneimittelwirkungen (UAW)
- Non-Compliance
- Interaktionen
- Negativ-Image
Depression – eine Spektrums-Störung
Depressionen sind ein sehr heterogenes Krankheitsbild. Sowohl genetische Faktoren als auch Umwelteinflüsse spielen bei der Entstehung eine Rolle und es ist eine ganze Reihe von (neuro-)biologischen Prozessen involviert, von denen nur ein Teil bekannt ist. Die Fülle der Faktoren, die zur Ätiologie der Depression beitragen können, legt nahe, dass es nicht nur einen Entstehungsmechanismus gibt [2, 23]. Es ist daher unwahrscheinlich, dass Medikamente mit nur einem Wirkungsmechanismus alle oder auch nur einen großen Teil der Patienten erfolgreich behandeln können.
Die heutige Antidepressiva-Therapie zielt in erster Linie auf die Behandlung der Stimmungsstörungen, die auch als „Hauptsymptome“ bei der Diagnose der Depression gelten [11]. Die gleiche Diagnose „Depression“ kann aber fast ohne gemeinsame Symptome gestellt werden, wie Abbildung 1 illustriert.
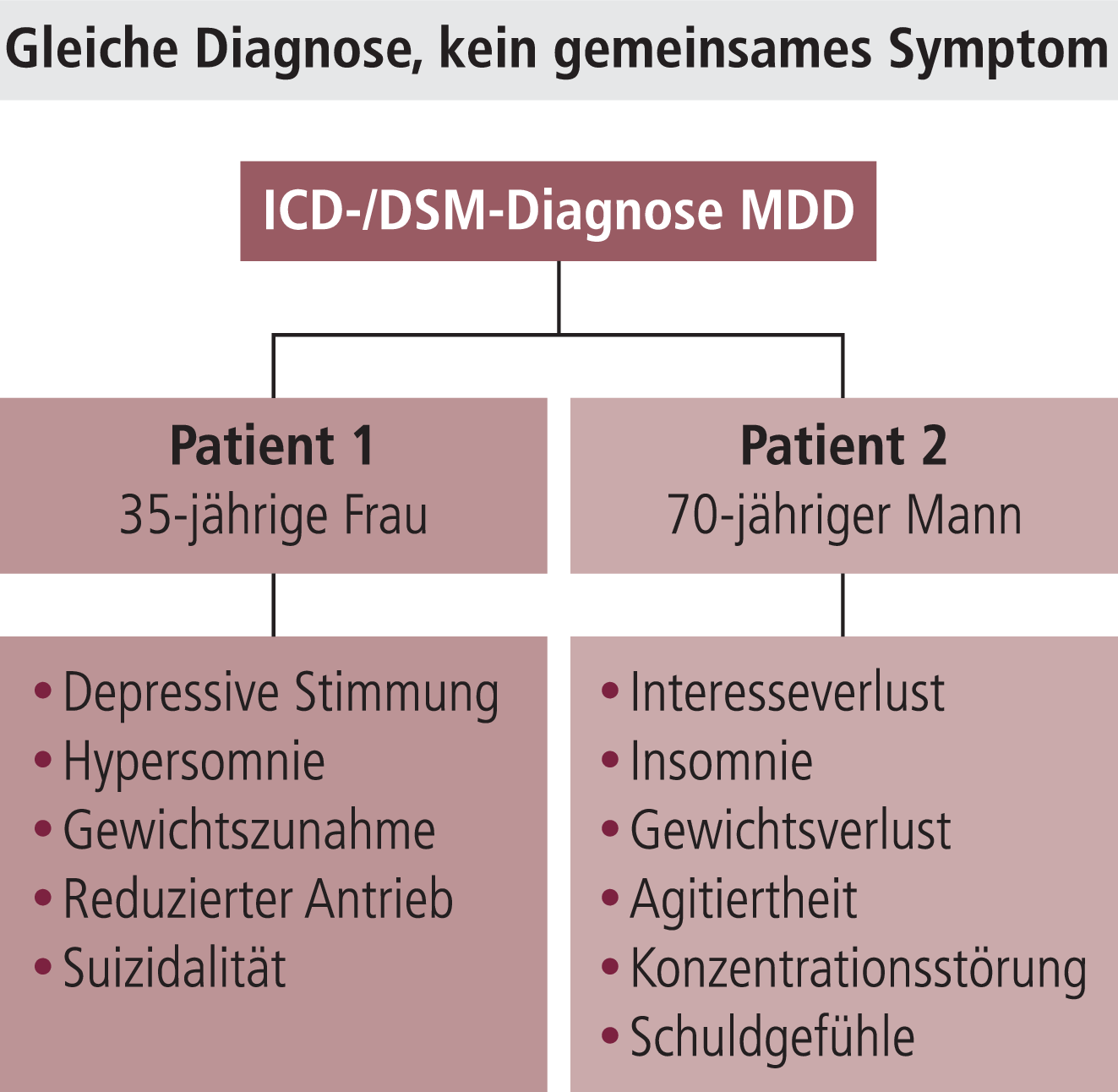
Abb. 1. Gesichter der Depression. MDD: major depressive disorder (depressive Episode)
Zu den Depressions-assoziierten nichtaffektiven Symptomen zählen vor allem Kognitions-, Schlaf- oder Angststörungen, die die Lebensqualität und das Funktionieren der Patienten im Alltagsleben stark beeinträchtigen können [28].
Als Komorbidität sind Angststörungen häufig, die schon Jahre vor Einsetzen der Depression beobachtet werden können, differenzialdiagnostisch schwierig sind und einen negativen Einfluss auf den Krankheitsverlauf der Depression haben [29].
Schlafstörungen sind bei Patienten mit Depression so häufig, dass manche Autoren davor warnen, die Diagnose „Major Depression“ in Abwesenheit von Schlafstörungen zu stellen [25]. Störungen des zirkadianen Rhythmus und des Schlaf-Wach-Rhythmus, die häufig Ursache von Schlafstörungen sind, stellen eine mögliche Ätiologie von Depressionen dar. Untermauert wird diese Hypothese unter anderem durch den erfolgreichen Einsatz von Schlafentzug oder Verschiebung des Schlafrhythmus [10].
Besonders interessant in diesem Zusammenhang sind die kognitiven Defizite, die in Verbindung mit Depressionen beobachtet werden. Diese tragen maßgeblich zu der hohen Invalidität bei [37] und haben dadurch eine große Bedeutung sowohl für betroffene Patienten und ihre Ärzte [6] als auch in volkswirtschaftlicher Hinsicht [35]. In einer Studie, die die Prioritäten von Patienten und Ärzte bei der Antidepressiva-Behandlung miteinander verglich, lag die Beseitigung kognitiver Störungen bei beiden Gruppen weit vorn, bei den Patienten sogar auf dem zweiten Rang gleich nach „Response“ allgemein [6].
Die kognitive Beeinträchtigung kann unterschiedliche Ausprägungen haben wie Störungen der Konzentrationsfähigkeit, des Gedächtnisses, der Lernfähigkeit, der Psychomotorik bis hin zu Störungen der exekutiven Funktionen im Sinne von Planen und Entscheidungen treffen. Solche Symptome werden inzwischen weitgehend als charakteristisch für die akute Phase einer Depression angesehen.
Lange Zeit wurde angenommen, dass kognitive Defizite eine direkte Folge der Stimmungsstörungen seien und somit bei erfolgreicher Therapie „automatisch“ abklingen würden [14]. Studien zeigen jedoch, dass kognitive Symptome auch zwischen akuten Phasen der Erkrankung oder in Remission weiter bestehen [7]. Es scheint sogar, dass sich die kognitive Leistungsfähigkeit bei Patienten mit rezidivierender Depression mit jeder akuten Episode verschlechtert [14].
Ob alle oder einige der oben beschriebenen Symptome als Teil der Depression anzusehen sind oder als Komorbiditäten, wird unterschiedlich diskutiert; immerhin erscheinen sie zumindest als „Zusatzsymptome“ auch unter den offiziellen Diagnosekriterien für Depressionen [11]. Aber gleichgültig wie man diese Beschwerden einordnen will, auch sie benötigen eine Therapie, da sie großen Einfluss auf die Schwere der Depression und die Rezidivrate haben. Das Vorhandensein von Restsymptomen wurde als wichtiger Faktor und Prädiktor für einen Rückfall identifiziert. Kognitive Störungen gehören dabei zusammen mit Schlafstörungen und persistierenden Stimmungsstörungen zu den am häufigsten genannten Symptomen [27].
Neue Ansätze
Für zukünftige Antidepressiva ergibt sich damit eine lange Wunschliste: Sie sollten nicht nur schneller und effektiver wirken als die bisherigen Medikamente, besser verträglich sein und zu verbesserter Compliance führen, sondern auch nichtaffektive Symptome, wie beispielsweise kognitive Störungen, bessern. Wenn man diese Anforderungen betrachtet und gleichzeitig das heterogene Krankheitsbild der Depression berücksichtigt, ist es unwahrscheinlich, dass ein Medikament mit nur einem Wirkungsmechanismus diese Aufgaben erfüllen kann. Benötigt werden einerseits Medikamente, die denjenigen Patienten helfen, die auf die heute zugelassenen Substanzen nicht ansprechen oder diese nicht vertragen, und andererseits Medikamente, die nichtaffektive Symptome behandeln, die heute nicht im Zentrum der antidepressiven Therapie stehen. Die zukünftige medikamentöse Therapie der Depression muss alternative Wirkungsmechanismen zu den heute verbreiteten SSRI und SNRI anbieten, beispielsweise durch die Kombination mehrerer pharmakologischer Mechanismen.
Eine Möglichkeit, mehrere Wirkungsmechanismen miteinander zu kombinieren, die auch heute schon häufig bei der Behandlung sogenannter therapieresistenter Depressionen angewandt wird, ist die Kombination mehrerer Antidepressiva oder die Augmentation eines Antidepressivums mit Medikamenten aus anderen Substanzklassen, zum Beispiel Lithium, Levothyroxin, atypischen Antipsychotika oder dopaminergen Stimulanzien wie Methylphenidat oder Dexamphetamin [12, 13, 38]. Solche Kombinationen können wirksam sein, allerdings bringt das zusätzliche Medikament neue Nebenwirkungen mit sich, abgesehen vom Interaktionsrisiko. Nicht vergessen sollte man auch die Komplexität des Regimes (Anzahl der täglich einzunehmenden Tabletten) hinsichtlich der Compliance. Nur für wenige Antidepressiva-Kombinationen gibt es kontrollierte klinische Studien zur Sicherheit und Wirksamkeit, in Klinik und Praxis hat dieses Vorgehen aber zunehmende Bedeutung erlangt („Polypharmazie“) [31, 32].
Für die beiden atypischen Antipsychotika Aripiprazol und Quetiapin liegt eine Zulassung der US Food and Drug Administration (FDA) für den Einsatz in Kombination mit einem SSRI oder SNRI bei therapieresistenter Major Depression vor, ebenso für die Fixkombination Olanzapin/Fluoxetin. In Deutschland ist zurzeit Quetiapin als Add-on zugelassen. Atypische Antipsychotika sind jedoch durch eine Reihe von metabolischen Nebenwirkungen belastet, die eine Langzeitbehandlung fragwürdig machen [38].
Multimodale Antidepressiva
Die Alternative zur Kombination verschiedener Medikamente sind Substanzen, die mehrere synergistische Wirkungsmechanismen in einem Molekül vereinen. Nach einer langen Phase, in der nach hochselektiven Substanzen geforscht wurde, sind in den letzten Jahren solche multimodale Antidepressiva in Entwicklung [40]. Ein in den USA kürzlich zugelassenes Medikament zur Behandlung der Major Depression ist das Antidepressivum Vortioxetin. Diese Substanz blockiert nicht nur wie ein SSRI den Serotonin-Transporter, sondern hat auch Rezeptoraktivitäten als 5-HT3-, 5-HT7-, 5-HT1D-Antagonist, als 5-HT1B-Partialagonist und 5-HT1A-Agonist. Vortioxetin hat also Affinität zu einer Reihe von Serotoninrezeptoren: einerseits zu präsynaptischen Serotoninautorezeptoren, die zumindest teilweise für den verzögerten Wirkungseintritt der SSRI verantwortlich gemacht werden, andererseits zu Rezeptoren, die mit kognitiven Leistungen assoziiert sind [34].
Optimierungsspielräume
Weitere Substanzen mit neuen pharmakologischen Wirkungsmechanismen sind in Entwicklung, zum Beispiel Substanzen mit Einfluss auf die glutamaterge oder GABAerge Neurotransmission, auf Neurokininrezeptoren, das Opioidsystem oder das peptiderge System sowie neurotrophe Substanzen (BDNF, IGF). Sie befinden sich jedoch noch in frühen Phasen der Entwicklung, ihre zukünftige Bedeutung ist noch nicht abzuschätzen [5].
Vieles spricht dafür, dass zukünftige Antidepressiva multimodale Medikamente sein werden, die nicht nur auf die Behandlung des Affekts abzielen, sondern auch bei Patienten wirksam sind, die nichtaffektive Symptome aufweisen.
Die herausragende Bedeutung depressiver Störungen auch in gesundheitsökonomischer Sicht sollte zu einer konsequenten Nutzung vorhandener Behandlungsoptionen und zur Intensivierung der Pharmaforschung trotz hoher Aufwendungen und verbreiterter Ressentiments führen [16].
Interessenkonflikterklärung
GL hat Honorare für Vorträge, wissenschaftliche Tätigkeit in Advisory/Expert Boards und Drittmittelforschungsmittel erhalten von den Firmen Janssen-Cilag, Lilly, Lundbeck, Merz, Otsuka und Servier.
CG ist Medical Advisor der Scientific Unit bei Lundbeck GmbH, Deutschland.
Literatur
1. Angst F, Stassen HH, Clayton PJ, Angst J. Mortality of patients with mood disorders: follow-up over 34–38 years. J Affect Disord 2002;68:167–81.
2. Belmaker RH, Agam G. Major depressive disorder. N Engl J Med 2008;358:55–68.
3. Bromet E, Andrade LH, Hwang I, et al. Cross-national epidemiology of DSM-IV major depressive episode. BMC Med 2011;9:90.
4. Burcusa SL, Iacono WG. Risk for recurrence in depression. Clin Psychol Rev 2007;27:959–85.
5. Connolly KR, Thase ME. Emerging drugs for major depressive disorder. Expert Opin Emerg Drugs 2012;17:105–26.
6. Cuffel BJ, Azocar F, Tomlin M, Greenfield SF, et al. Remission, residual symptoms, and non-response in the usual treatment of major depression in managed clinical practice. J Clin Psychiatry 2003;64:397–402.
7. Danner M, Hummel JM, Volz F, et al. Integrating patients’ views into health technology assessment: Analytic hierarchy process (AHP) as a method to elicit patient preferences. Int J Technol Assess Health Care 2011;27: 369–75.
8. De Berardis D, Marini S, Fornaro M, et al. The melatonergic system in mood and anxiety disorders and the role of agomelatine: implications for clinical practice. Int J Mol Sci 2013;13;14:12458–83.
9. DEGS. Studie zur Gesundheit Erwachsener in Deutschland. Bundesgesundheitsbl 2013;56:609–893.
10. Demyttenaere K, Enzlin P, Dewé W, et al. Compliance with antidepressants in a primary care setting, 1: Beyond lack of efficacy and adverse events. J Clin Psychiatry 2001;62(Suppl 22):30–3.
11. DGPPN, BÄK, KBV, AWMF, AkdÄ, BPtK, BApK, DAGSHG, DEGAM, DGPM, DGPs, DGRW (Hrsg.) für die Leitliniengruppe Unipolare Depression. S3-Leitlinie/Nationale VersorgungsLeitlinie Unipolare Depression-Kurzfassung, 1. Auflage. Berlin, Düsseldorf: DGPPN, ÄZQ, AWMF, 2009.
12. Garcia-Toro M, Medina E, Galan JL, Gonzalez MA, et al. Treatment patterns in major depressive disorder after an inadequate response to first-line antidepressant treatment. BMC Psychiatry 2012;12:143.
13. Gitlin M. Augmentation strategies for major depressive disorder. CNS Spectrums 2010;15(Suppl 7):8–10.
14. Hammar A, Ardal G. Cognitive functioning in major depression –a summary. Front Hum Neurosci 2009;3:26.
15. Hasselbalch BJ, Knorr U, Hasselbalch SG, Gade A, et al. Cognitive deficits in the remitted state of unipolar depressive disorder. Neuropsychology 2012;26:642–51.
16. Hegerl U, Friede M. Psychische Erkrankungen in Deutschland. Optimierungsspielräume und Handlungsbedarf. Nervenheilkunde 2013;32:762–5.
17. Henigsberg N, Mahableshwarkar AR, Jacobsen P, et al. A randomized, double-blind, placebo-controlled 8-week trial of the efficacy and tolerability of multiple doses of Lu AA21004 in adults with major depressive disorder. J Clin Psychiatry 2012;73:953–9.
18. Hickie IB, Naismith SL, Robillard R, et al. Manipulating the sleep-wake cycle and circadian rhythms to improve clinical management of major depression. BMC Med 2013; 11:79.
19. Hickie IB, Scott J, Hermens DF, et al. Clinical classification in mental health at the cross-roads: which direction next? BMC Med 2013;11:125.
20. Houtjes W, van Meijel B, Deeg DJ, Beekman AT. Unmet needs of outpatients with late-life depression; a comparison of patient, staff and carer perceptions. J Affect Disord 2011;134:242–8.
21. Kennedy SH. Core symptoms of major depressive disorder: relevance to diagnosis and treatment. Dialogues Clin Neurosci 2008;10:271–7.
22. Langlieb AM, Guico-Pabia CJ. Beyond symptomatic improvement: assessing real-world outcomes in patients with major depressive disorder. Prim Care Companion J Clin Psychiatry 2010;12.
23. Laux G. Depressive Störungen. In: Möller HJ, Laux G, Kapfhammer HP (Hrsg.) Psychiatrie, Psychosomatik, Psychotherapie. Bd. 2 Spezielle Psychiatrie. 4. Aufl. Berlin: Springer, 2011.
24. Laux G, Dietmaier O. Praktische Psychopharmakotherapie. 6. Aufl. München: Elsevier, 2012.
25. Luca A, Luca M, Calandra C. Sleep disorders and depression: brief review of the literature, case report, and nonpharmacologic interventions for depression. Clin Interv Aging 2013;8:1033–9.
26. Mathers CD, Loncar D. Projections of global mortality and burden of disease from 2002 to 2030. PLoS Med 2006;3:e442.
27. McClintock SM, Husain MM, Wisniewski SR, Nierenberg AA, et al. Residual symptoms in depressed outpatients who respond by 50% but do not remit to antidepressant medication. J Clin Psychopharmacol 2011;31:180–6.
28. McKnight PE, Kashdan TB. The importance of functional impairment to mental health outcomes: a case for reassessing our goals in depression treatment research. Clin Psychol Rev 2009;29:243–59.
29. McLaughlin TP, Khandker RK, Kruzikas DT, Tummala R. Overlap of anxiety and depression in a managed care population: Prevalence and association with resource utilization. J Clin Psychiatry 2006;67:1187–93.
30. Melartin T, Rytsälä H, Leskelä U, et al. Continuity is the main challenge in treating major depressive disorder in psychiatric care. J Clin Psychiatry 2005;66:220–7.
31. Messer Th, Schmauß M. Polypharmazie in der Psychopharmakotherapie. 2. Aufl. Wien: Springer, 2012.
32. Mojtabai R, Olfson M. National trends in psychotropic medication polypharmacy in office-based psychiatry. Arch Gen Psychiatry 2010;67:26–36.
33. Mojtabai R. Unmet need for treatment of major depression in the United States. Psychiatr Serv 2009;60:297–305.
34. Mørk A, Pehrson A, Brennum LT, Nielsen SM, et al. Pharmacological effects of Lu AA21004: a novel multimodal compound for the treatment of major depressive disorder. J Pharmacol Exp Ther 2012;340:666–75. doi: 10.1124/jpet.111.189068.
35. Murray CJL, Lopez AD (eds). The Global Burden of Disease: A comprehensive assessment of mortality and disability from diseases, injuries and risk factors in 1990 and projected to 2020. Cambridge, MA: Harvard University Press on behalf of the World Health Organization, 1996.
36. Murray CJL, Vos T, Lozano R, et al. Disability-adjusted life years (DALYs) for 291 diseases and injuries in 21 regions, 1990–2010: a systematic analysis for the Global Burden of Disease Study 2010. Lancet 2012;380:2197–223.
37. Naismith SL, Longley WA, Scott EM, Hickie IB. Disability in major depression related to self-rated and objectively-measured cognitive deficits: a preliminary study. BMC Psychiatry 2007;7:32.
38. Nelson JC. Adjunctive atypical antipsychotics in medication-resistant depression. CNS Spectrums 2010;15(Suppl 7):10–3.
39. Penninx BW, Milaneschi Y, Lamers F, Vogelzangs N. Understanding the somatic consequences of depression: biological mechanisms and the role of depression symptom profile. BMC Med 2013;11:129.
40. Richelson E. Multi-modality: a new approach for the treatment of major depressive disorder. Int J Neuropsychopharmacol 2013;16:1433–42.
41. Rush AJ, Trivedi MH, Wisniewski SR, Nierenberg AA, et al. Acute and longer-term outcomes in depressed outpatients requiring one or several treatment steps: a STAR*D report. Am J Psychiatry 2006;163:1905–17.
42. Sartorius N. Unmet needs in depression (and other mental disorders). Medicographia 2005; 27:270–2.
43. Ten Doesschate MC, Bockting CL, Schoene AH, et al. Adherence to continuation and maintenance antidepressant use in recurrent depression. J Affect Disord 2009;115:167–70.
Prof. Dr. med. Dipl.-Psych. Gerd Laux, Institut für evidenzbasierte Medizin in der Psychopharmakotherapie (IEP), Nussbaumstraße 9, 83564 Soyen, E-Mail: Dr.g.laux@t-online.de
Dr. med. Christoph Goemann, Lundbeck GmbH, Ericusspitze 2, 20457 Hamburg, E-Mail: GOEM@Lundbeck.com
Unmet needs in treatment with antidepressants
Major depression is a common disorder worldwide, which severely affects patient’s quality of life, leads to disability and shortens life expectancy. Progress in treatment with antidepressants is stagnating while we are confronted with a number of unmet needs. Future drugs should work faster and in more patients than present antidepressants available, as well as being better tolerable and providing better compliance. In addition to treating mood symptoms, future antidepressants should also treat non-affective symptoms like disturbed sleep or cognition functions. Considering this task list as well as the heterogeneous pathophysiology of major depression, it is unlikely that any drug with just one mechanism can meet all these unmet needs. Needed are drugs with new, alternative and multimodal mechanisms, which combine several synergistic pharmacological mechanisms.
Key words: Major depression, unmet needs, antidepressants, multimodal drugs
Psychopharmakotherapie 2014; 21(01)
