Günter Niklewski und Teresa Biermann, Nürnberg
Die Psychoonkologie umfasst definitionsgemäß „das gesamte Spektrum von psychosozialer Beratung bis hin zu einer spezifischen Psychotherapie. Die psychoonkologische Behandlung ist dem supportiven Psychotherapiekonzept zuzuordnen“, wobei sie in verschiedenen Aspekten der Behandlung bestehend aus Akutbehandlung, Rehabilitation und ambulanter Nachsorge in unterschiedlichem Maße ausgebaut ist [32]. Die vorliegende Darstellung befasst sich vor allem mit pharmakologischen Aspekten dieses sehr komplexen Themas:
Zunächst sind einige generelle Aspekte zu erwähnen, die in der Pharmakotherapie von onkologischen Patienten berücksichtigt werden müssen.
- In den meisten Fällen handelt es sich um sogenannte Off-Label-Verschreibungen von Psychopharmaka im Rahmen einer Chemotherapie oder einer syndromalen Therapie bei eher diffusen psychiatrischen Symptomen. Es gibt nur wenige Daten zu spezifischen psychotropen Medikamenten in der supportiven Behandlung, sodass sich die Therapieentscheidungen meist eher auf klinische Erfahrungen oder Schlussfolgerungen stützen denn auf publizierte Evidenz [10].
- Die Pharmakokinetik verschiedenster Medikamente kann bei Patienten mit fortgeschrittenen Tumorerkrankungen dramatisch verändert sein. Die Absorption mag entweder vermindert sein, durch eine Gastroparese oder Achlorhydrie, oder erhöht durch Störung des hepatischen First-Pass-Metabolismus. Die Verteilung verändert sich darüber hinaus durch Hypoproteinämie, Kachexie, Dehydratation oder Ödeme. Durch Leber- oder Nierenversagen kann es zur Akkumulation verschiedener Substanzen kommen [10, 37].
- Die Rate an Neben- und Wechselwirkungen psychotroper Substanzen kann erhöht sein durch Hypoxie, metabolische Störungen oder eine paraneoplastische Sekretion verschiedener Transmitter [16]. Hierdurch kann es entweder zu einer Über- oder Unterdosierung kommen [8].
- Die Praktikabilität einer jeweiligen Behandlung kann deutlich durch die Darreichungsform gestört sein, zum Beispiel beim Vorliegen von Schluckstörungen oder Inkompatibilität mit der enteralen Ernährung [27].
- Die Evaluation des Behandlungserfolgs kann durch starke Fluktuationen und eine progressive allgemeine Zustandsverschlechterung erschwert werden, mitunter fällt die Unterscheidung zwischen Nichtansprechen auf die Medikation, Nebenwirkungen und klinischen Auffälligkeiten in Relation zur zugrunde liegenden Erkrankung schwer [10].
Aus den genannten Überlegungen lassen sich allgemeine Empfehlungen ableiten, zum Beispiel das regelmäßige und standardisierte Erfassen von klinischen Variablen der Befindlichkeit wie Stimmung, Antrieb und kognitive Leistungsfähigkeit, entsprechende Laborkontrollen, das frühe Beginnen mit einer psychotropen Medikation, wenn die Beurteilung noch leichter fällt als im Verlauf der Erkrankung, sowie den Einstieg mit einer möglichst niedrigen Dosis mit langsamer Dosistitration [49]. In diesem Sinne lässt sich nach Grassi zitieren: “There is still a lack of robust information on the mutual influence between medications used to treat cancer and those used to treat comorbid psychiatric disorders” [28].
Epidemiologie von psychischen Erkrankungen bei onkologischen Patienten
Die Angaben zur Häufigkeit psychiatrischer Erkrankungen bei onkologischen Patienten variieren in der Literatur erheblich. Zu erwähnen sind hier insbesondere Angststörungen (1–48%) und posttraumatische Belastungsstörungen (0–35%), Anpassungsstörungen (2–52%) und schwere depressive Episoden (0–58%) [48]. Erkrankungen aus dem schizophrenen Formenkreis und bipolare Störungen kommen mit 0,4 bis 1,5% deutlich seltener vor [50, 72]. Insgesamt sind Angsterkrankungen und Depressionen die häufigsten psychischen Störungen bei Tumorpatienten, eine aktuelle Studie von Brown und Mitarbeitern mit 397 Patienten ergab bei 63% das Vorliegen einer behandlungsbedürftigen Angsterkrankung, 78% der Patienten litten an einem depressiven Syndrom, bei 46% dieser Patienten lag eine komorbide Angststörung vor [9]. Allerdings variieren die Zahlen zum Teil erheblich. In einer anderen aktuellen Studie aus Deutschland wurden Patienten während der Akutbehandlung mit Patienten in der Rehabilitation verglichen. Die Prävalenz akuter psychiatrisch relevanter Störungen betrug während eines Zeitraums von vier Wochen 34% in der Rehabilitation und 24% in der Akutversorgung. Innerhalb eines Zeitraums von sechs Monaten berichteten bis zu 45% der Teilnehmer der Studie während der Rehabilitation von behandlungsbedürftigen psychischen Störungen. Die häufigsten aktuellen psychischen Störungen sind dabei depressive Störungen mit bis zu 13% und Angsterkrankungen mit bis zu 17% [31].
Die Raten klinisch relevanter psychischer Störungen sind wesentlich höher als Prävalenzen in methodisch vergleichbaren epidemiologischen Untersuchungen aus der Allgemeinbevölkerung in Deutschland. Hierbei war die Wahrscheinlichkeit, an einer behandlungsbedürftigen psychischen Störung zu leiden, erhöht, wenn zum Zeitpunkt der onkologischen Diagnosestellung der Patient oder die Patientin arbeitslos war, an Fatigue oder Schmerzen litt [51, 63]. Bei affektiven Erkrankungen ist der größte Risikofaktor für das Auftreten einer Depression eine positive Vorgeschichte. Weitere Risikofaktoren sind starke Schmerzen, ein schlechter funktionaler Status, ein schlechtes soziales Netzwerk sowie jüngeres Lebensalter [42]. Darüber hinaus werden häufig Einzelsymptome beschrieben, die einen hohen Leidensdruck verursachen, zum Beispiel Insomnie, Appetitverlust, Übelkeit mit Erbrechen und chronische Fatigue.
Es wird zudem beschrieben, dass Onkologen vorwiegend auf Schmerzen fokussieren und weniger auf Symptome einer psychischen Erkrankung [28]. Selbst wenn eine Depression erkannt wird, nehmen nur 25 bis 30% ambulant behandelter onkologischer Patienten mit einer Depression eine Überweisung zum Psychiater an, sodass nur die wenigsten Patienten angemessen psychopharmakologisch behandelt werden [62].
Eigene Daten aus dem Konsiliardienst der psychiatrischen Klinik des Klinikums Nürnberg Nord zeigen jedoch eine andere Verteilung von psychiatrischen Diagnosen anhand von 322 Konsilen bei onkologischen Patienten während der Jahre 2009 und 2010 (Abb. 1). Diese konsiliarische Mitbeurteilung führte in 18% der Fälle sogar zu einer Übernahme in die psychiatrische Klinik, in 22,5% zur Einrichtung einer gesetzlichen Betreuung und in 24% zu einer Behandlung mit einem Antidepressivum (eigene Daten, bislang unveröffentlicht).
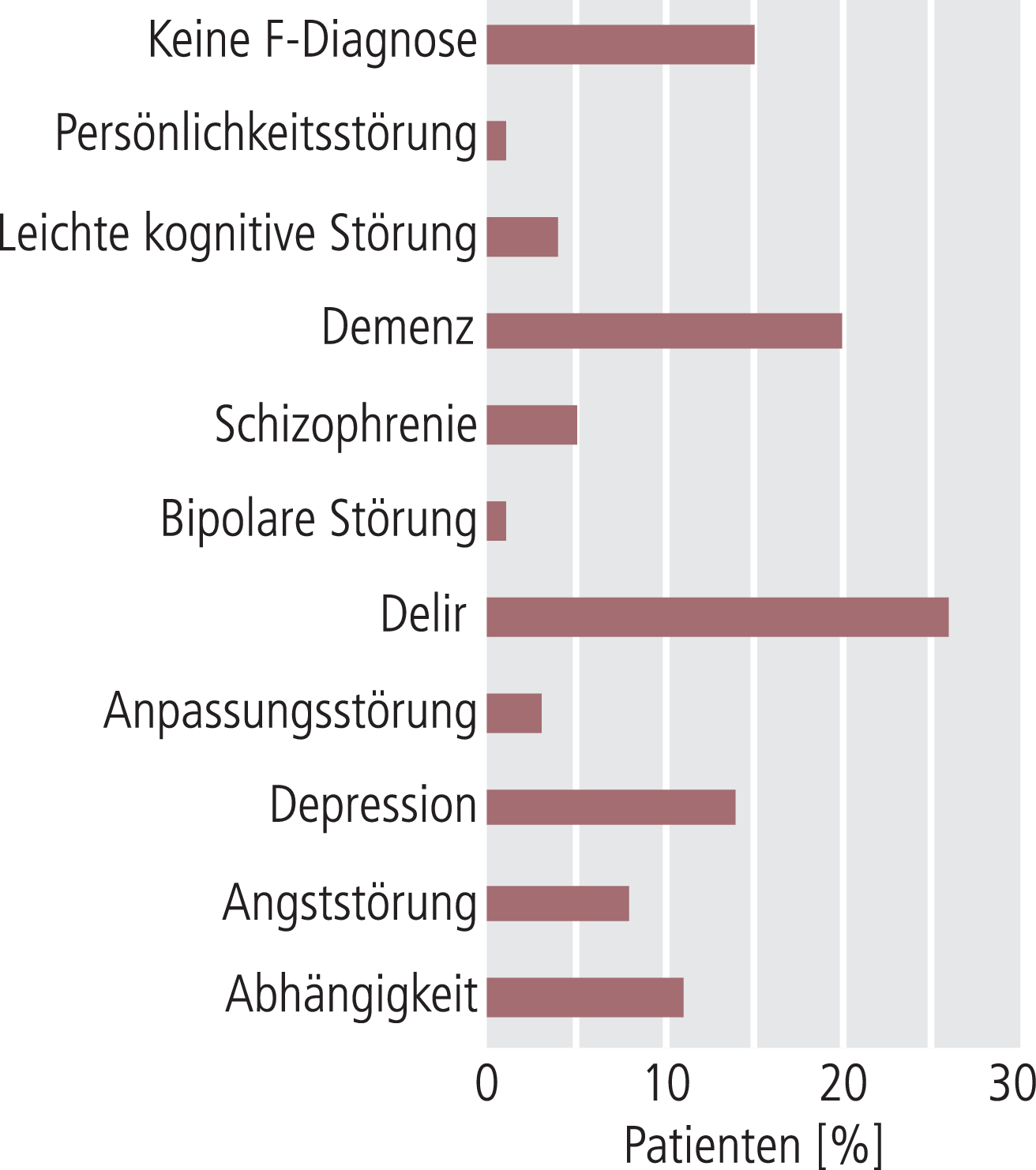
Abb. 1. Verteilung psychiatrischer Diagnosen bei 322 onkologischen Patienten, die während psychiatrischer Konsile während der Jahre 2009 und 2010 erhoben wurden
Bei der Behandlung von onkologischen Patienten mit Psychopharmaka kann man sich die bekannten Nebenwirkungen durchaus zunutze machen: Bei einem Patienten mit Schlafstörungen ist es sinnvoll, ein Medikament anzusetzen, das einen sedierenden Effekt haben kann (z.B. Mirtazapin). Da Angst ein häufiges Symptom im Rahmen einer Tumorerkrankung ist, können hier vorwiegend Substanzen mit anxiolytischer Wirkung eingesetzt werden (z.B. Venlafaxin). Patienten mit größerem Gewichtsverlust können von der appetitsteigernden Wirkung von beispielsweise Mirtazapin oder Olanzapin profitieren. Bei psychomotorischer Verlangsamung kann eine stimulierend wirkende Substanz wie Bupropion sinnvoll sein; ähnliche Überlegungen gelten für Patienten mit neuropathischen Schmerzen [42].
Es finden sich Zahlen in der Literatur, dass bis zu 80% aller onkologischen Patienten mindestens ein Psychopharmakon erhalten, ungeachtet der beschriebenen Inzidenzen psychiatrischer Störungen bei onkologischen Patienten. 36% der Betroffenen erhielten sogar mehr als drei psychotrope Medikamente [66]. Schätzungsweise 60 bis 80% aller Psychopharmaka werden über die Enzyme der Cytochrom-P450-(CYP-)Familie in der Leber abgebaut. Dabei exprimieren 10 bis 20% aller Kaukasier kein funktionsfähiges CYP2D6, was die Metabolisierung verschiedener psychotroper Medikamente verändern und damit zu erhöhten oder erniedrigten Plasmaspiegeln und zur Zunahme unerwünschter Wirkungen und Interaktionen führen kann [12]. Weiterhin können Unterschiede bei Transportproteinen wie dem P-Glykoprotein (P-gp) die Entstehung von Wechselwirkungen erklären [69].
Aus diesen Überlegungen wird deutlich, dass die Wechselwirkungen zwischen psychiatrischen und onkologischen Erkrankungen unter Einbeziehung der vielschichtigen Medikationen mehr als komplex ist, sodass im Folgenden lediglich auf einige wichtige Aspekte fokussiert werden kann.
Immunmodulatoren und Kinaseinhibitoren stellen neuartige Substanzen dar, die ebenfalls eine große Wirkung auf das ZNS haben können, ohne dass allerdings hierzu Näheres bekannt ist. Aufgrund dessen soll hier nicht näher darauf eingegangen werden.
Hämatologische Nebenwirkungen von Psychopharmaka
Generell kann nicht vorhergesagt werden, wie der einzelne Patient auf eine Medikation reagieren wird [67]. Hämatologische Abnormitäten werden oft im Rahmen einer psychiatrischen Medikation entdeckt, meist sind sie moderat und nicht von besonderer klinischer Bedeutung. Oft lässt sich nur schwer ein kausaler Zusammenhang feststellen [30].
Schwerwiegende und klinisch relevante Nebenwirkungen treten meist zu Beginn einer Behandlung auf. Eine Agranulozytose beginnt meist 21 bis 28 Tage nach Beginn der Behandlung und kann bis zu drei Monate anhalten, bis auf die aplastische Anämie bilden sich die meisten Auffälligkeiten nach Absetzen der Substanz zurück [56]. Zu den Psychopharmaka-induzierten Störungen gehören seltene, aber ernst zu nehmende hämatologische Komplikationen, deren Häufigkeit sich je nach Studie zwischen 1 bis 2/100000/Jahr bewegt; die Mortalität fluktuiert zwischen 8 bis 17% [25]. Prinzipiell können alle Klassen psychiatrischer Medikamente (typische und atypische Antipsychotika, Antidepressiva, Stimmungsstabilisatoren und Benzodiazepine) hämatotoxisch wirken. Zu den möglichen Nebenwirkungen gehören in absteigender Häufigkeit Neutropenie, Agranulozytose, Eosinophilie, Thrombozytopenie sowie Purpura und Anämie [47]. Darüber hinaus wird auch regelmäßig von Leukozytose, Thrombozytose und gestörter Plättchenfunktion berichtet [38]. Es werden verschiedene Ursachen hierfür diskutiert von einer Knochenmarkssuppression, einer immunvermittelten Zellzerstörung bis hin zu einer direkten Knochenmarkstoxizität [4]. Das größte Risiko für derartige Nebenwirkungen haben kaukasische Frauen und Patienten mittleren Alters [56].
Eine Übersicht über die bekannten hämatologischen Nebenwirkungen findet sich in Tabelle 1.
Tab. 1. Übersicht über hämatologische Nebenwirkungen von Psychopharmaka in absteigender Reihenfolge
|
Substanzklasse |
Nebenwirkung |
|
Typische Neuroleptika |
Gesamtrisiko Agranulozytose 0,1% |
|
Chlorpromazin Thioridazin Fluphenazin Haloperidol |
Agranulozytose Anämie Eosinophilie Leukopenie Thrombozytopenie |
|
Atypische Neuroleptika |
|
|
Clozapin Remoxiprid1 |
Agranulozytose 1–2% Eosinophilie (eosinophile Kardiomyopathie) |
|
Olanzapin Quetiapin |
Leukozytose Thrombozytopenie |
|
Risperidon |
Anämie Leukozytose Leukopenie Thrombozytopenie |
|
Antidepressiva |
|
|
Trizyklika |
|
|
Amitriptylin Nortriptylin Imipramin Clomipramin |
Agranulozytose (0,1–0,2%) Eosinophilie Thrombozytopenie Panzytopenie (Clomipramin) |
|
SSRI/NSSRI/Tetrazyklika |
Erhöhtes Blutungsrisiko unter SSRI Vor allem in Kombination mit NSAID |
|
Citalopram Sertralin |
Anämie Leukopenie Thrombozytopenie |
|
Mirtazapin Mianserin |
Agranulozytose |
|
Benzodiazepine |
Thrombozytopenie Agranulozytose |
|
Clonazepam Diazepam |
Thrombozytopenie Anämie Eosinophilie Leukopenie |
|
Stimmungsstabilisatoren |
|
|
Lithium |
Leukozytose Thrombozytose Inhibition Blutkoagulation und Fibrinogenpräzipitation |
|
Carbamazepin |
Agranulozytose Leukopenie |
|
Valproinsäure |
Neutropenie Thrombozytopenie Makrozytäre Anämie |
|
Lamotrigin |
Makrozytäre Anämie |
|
Andere |
|
|
Cholinesterasehemmer |
Erhöhtes relatives Blutungsrisiko Anämie Thrombozythämie Thrombozytopenie Ekchymose |
1Vom Markt genommen
Typische Neuroleptika
Generell ist die Agranulozytose die häufigste Nebenwirkung mit weniger als 0,1%. Darüber hinaus gibt es vorwiegend Einzelberichte für Chlorpromazin, Fluphenazin und Haloperidol über Agranulozytosen, Anämien, Eosinophilien, Leukopenien und Thrombozytopenien [56]. Nach Clozapin und Remoxiprid (bereits wegen Hämatotoxizität vom Markt genommen) scheint das höchste Risiko für hämatologische Nebenwirkungen mit den aliphatischen Phenotiazinderivaten Thioridazin und Chlorpromazin assoziiert zu sein [40]. Je höher die neuroleptische Potenz, desto geringer scheint das Risiko für das Auftreten einer Agranulozytose [56].
Atypische Neuroleptika
Die Substanz, die am häufigsten bei der Erwähnung hämatologischer Nebenwirkungen in den Sinn kommt, ist Clozapin, ein atypisches Neuroleptikum mit einem sehr guten Wirkungsprofil, dessen Anwendung jedoch durch das häufigere Vorkommen einer Agranulozytose im Vergleich mit anderen Psychopharmaka eingeschränkt wird. Die Entstehung dieser doch sehr heterogen verlaufenden Agranulozytose scheint auf einem hoch spezifischen immunogenen Prozess zu beruhen [45]. Die Häufigkeit einer Agranulozytose liegt bei 1 bis 2%, wobei auch das – jedoch geringere – Risiko einer Eosinophilie mit beispielsweise einer eosinophilen Kardiomyopathie zu beachten ist [56]. Entsprechend haben die beiden Neuroleptika Olanzapin und Quetiapin auch ein erhöhtes Risiko für die Entwicklung einer Leukozytose und Thrombozytopenie, wohingegen Risperidon das Auftreten einer Anämie, Leukozytose sowie Leukopenie und das Auftreten einer Thrombopenie begünstigt [56].
Trizyklika
Antidepressiva können eine Reihe hämatologischer Nebnwirkungen verursachen, die zu Beginn oft schwer von den Symptomen einer Depression mit Müdigkeit und Krankheitsgefühl unterschieden werden können. Für Amitriptylin, Nortriptylin, Imipramin und Clomipramin ist die Gefahr einer Agranulozytose durch direkte Knochenmarkstoxizität beschrieben, allerdings mit geringerer Häufigkeit (zum Teil bis zu zehnfach geringer) als bei Neuroleptika [56]. Darüber hinaus sind Eosinophilien und Thrombozytopenien beschrieben, unter Clomipramin ist es auch zu Panzytopenien gekommen [56].
SSRI/NSSRI/Tetrazyklika
Die meisten Angaben zu anderen hämatologischen Nebenwirkungen gibt es bezüglich eines erhöhten Blutungsrisikos unter verschiedenen Psychopharmaka, da vor allem Serotonin-Wiederaufnahmehemmer (SSRI) die Thrombozytenfunktion beeinträchtigen: Unter SSRI ist eine verlängerte Blutungszeit beschrieben, insbesondere im gastrointestinalen Trakt mit einer Verdoppelung der Blutungsneigung, dieses Risiko wird potenziert bei gleichzeitiger Gabe von nichtsteroidalen Antiphlogistika oder Antikoagulanzien [11, 35]. SSRI können im ZNS die Serotoninkonzentration im synaptischen Spalt erhöhen, wohingegen diese in den Thrombozyten vermindert wird, sodass es zu einer gestörten Plättchenaggregation, einer verlängerten Blutungszeit und erhöhter Prothrombinzeit kommt [64].
Unter Citalopram und Sertralin kam es zu Anämien, aber auch Leukopenien und Thrombozytopenien [56]. Darüber hinaus ist die Gefahr einer Agranulozytose für Mirtazapin mit einer Häufigkeit von 1,1‰ beschrieben [53, 56]. Das Vorkommen von Agranulozytosen unter Mianserin wurde mit etwas unter 1‰ angegeben [21].
Benzodiazepine
Es wird in der Literatur über Einzelfälle von Thrombozytopenien und Agranulozytose berichtet, wobei kein kausaler Zusammenhang, eine Dosis-Wirkungs-Beziehung oder eine pathophysiologische Erklärung hierfür bekannt sind [3]. Eine Thrombozytopenie ist vor allem für Clonazepam und Diazepam beschrieben, wobei Clonazepam auch eine Anämie, Eosinophilie und Leukopenie hervorrufen kann [18].
Stimmungsstabilisatoren
Unter Lithium wird regelmäßig von reproduzierbaren hämatologischen Nebenwirkungen berichtet. Unter Lithium kann eine Proliferation der Leukozyten beobachtet werden, ferner kommt es zur Thrombozytose mit Inhibition der Blutkoagulation und Fibrinogenpräzipitation [23]. Aufgrund dessen kann Lithium auch im Management einer hämatologischen Toxizität im Rahmen anderer Erkrankungen eingesetzt werden, beispielsweise die Nutzung der Lithium-induzierten Neutrophilie im Rahmen der Behandlung von Lymphomen oder Leukämien [56].
Darüber hinaus können Stimmungsstabilisatoren, hier vor allem Antiepileptika wie Carbamazepin, Valproinsäure und Lamotrigin, am häufigsten hämatologische Nebenwirkungen verursachen. Carbamazepin kann eine Agranulozytose verursachen und kann in bis zu 10% der Fälle in den ersten vier Behandlungsmonaten eine transiente Reduktion der weißen Blutkörperchen hervorrufen [59]. Valproinsäure hat Einfluss auf die Phospholipide der Erythrozytenmembran, allerdings sind auch Neutropenie, Thrombopenie und makrozytäre Anämie unter der Einnahme von Valproinsäure beschrieben, Letztere wurde auch unter Lamotrigin beobachtet [19, 57].
Andere
Weiterhin zu beachten ist ein erhöhtes relatives Blutungsrisiko unter Cholinesterasehemmern. Vor allem Donepezil scheint mit hämatologischen Nebenwirkungen wie Anämie, Thrombozythämie, Thrombozytopenie und Ekchymose (4%) assoziiert zu sein [56]. Dahingegen findet sich für Ginkgo-biloba-Extrakte kein erhöhtes Risiko; sogar in Kombination mit anderen Antikoagulanzien wie Acetylsalicylsäure oder Phenprocoumon [26].
Psychiatrische Nebenwirkungen von Zytostatika
Jeder Konsiliararzt, der onkologische Patienten versorgt, sollte sich mit den lokalen Besonderheiten der in dem jeweiligen Klinikum gebräuchlichen Zytostatika und speziell deren zerebralen Nebenwirkungen vertraut machen:
Zytostatika sind natürliche oder synthetische Substanzen, die das Zellwachstum beziehungsweise die Zellteilung hemmen. Sie werden vor allem zur Behandlung von Tumorerkrankungen eingesetzt. Eine Übersicht über Angriffspunkte und Wirkungsmechanismen der häufigsten Substanzen findet sich in Tabelle 2.
Tab. 2. Angriffspunkte und Wirkungsmechanismen einer Auswahl von Zytostatika [52]
|
Substanzgruppe |
Wirkungsmechanismus |
Beispiele |
|
Antimetabolitem |
Hemmung der Purinsynthese |
6-Mercaptopurin, Methrotrexat |
|
Alkylanzien |
DNS-Interkalation |
Cyclophosphamid, Cisplatin, Doxorubicin |
|
Topoisomerase-Hemmstoffe |
Hemmung der DNS-Replikation |
Etoposid |
|
Enzyme |
Abbau wichtiger Substanzen |
Asparaginase |
|
Hormonantagonisten |
Hemmung des hormonabhängigen Wachstums |
Tamoxifen, Aromatasehemmer |
|
Mitosehemmstoffe |
Hemmung der Mikrotubuli-funktion |
Vinca-Alkaloide, Taxane |
Im Folgenden werden einige der Präparate näher mit ihren potenziellen Komplikationen im Hinblick auf neuropsychiatrische Neben- und Wechselwirkungen beschrieben. Eine Übersicht findet sich in Tabelle 3.
Tab. 3. Psychiatrische Nebenwirkungen von Zytostatika
|
Zytostatikum |
Nebenwirkung |
|
Methotrexat |
Leukenzephalopathie Transientes Delir nach 1–2 Wochen Reversible ZNS-Toxizität in Kombination mit Bestrahlung |
|
Procarbazin |
Delir Somnolenz Psychotische Zustände Cave: Wechselwirkung mit SSRI und Trizyklika, kein Alkohol und tyraminhaltige Speisen |
|
Irinotecan |
Cholinerges Syndrom Delir Cave: Kombination mit SSRI und Johanniskraut |
|
Glucocorticoide |
„Cortisonpsychose“ Hyperaktivität Insomnie Angst Affektlabilität Psychomotorische Unruhe Manische und depressive Episoden |
Methotrexat
Methotrexat (MTX) ist ein Analogon der Folsäure (Vitamin B9) und inhibiert als Folsäure-Antagonist kompetitiv und reversibel das Enzym Dihydrofolatreduktase. Es wird meist in Kombination als Zytostatikum in der Chemotherapie verschiedener Tumorerkrankungen, aber auch beispielsweise zur Behandlung von Autoimmunerkrankungen eingesetzt.
Unter einer Therapie mit Methotrexat wurden einzelne Fälle von Leukenzephalopathien berichtet. Darüber hinaus kann es nach ein bis zwei Wochen unter der Behandlung zu einem transienten Delir kommen [13]. Die zentralnervöse Toxizität ist in Kombination mit gleichzeitiger Bestrahlung deutlich erhöht, allerdings scheint es im Verlauf zu einer vollständigen Erholung des ZNS zu kommen [46].
Procarbazin
Procarbazin ist ein Chemotherapeutikum, das zur Gruppe der Alkylanzien gehört. Diese verändern die Ablesbarkeit der DNS durch den Einbau von Alkylgruppen, wodurch meist die Zellteilung verhindert werden kann. Es handelt sich um ein sogenanntes Prodrug, das in Azoprocarbazin umgewandelt wird. Die Metabolisierung erfolgt hepatisch und in den Erythrozyten. Der Arzneistoff wird unter anderem eingesetzt zur Behandlung von Morbus Hodgkin, Non-Hodgkin-Lymphomen, zerebralen Neoplasien und dem kleinzelligen Bronchialkarzinom [52].
Alkylanzien wie Busulfan, Cyclophosphamid oder Procarbazin sind in moderater Dosis gut zentralnervös verträglich [54]. Allerdings kann es zu einem Delir mit abruptem Beginn kommen, ferner sind Somnolenz und psychotische Zustände beschrieben [55]. Procarbazin hat eine zwar schwache, aber dennoch relevante Wirkung auf die Monoaminoxidase, weswegen potenzielle Wechselwirkungen mit SSRI und Trizyklika beachtet werden müssen [36]. Darüber hinaus sollte auf tyraminhaltige Speisen verzichtet werden. Ferner kann der Metabolismus von Phenothiazinen und Alkohol vermindert sein, zudem hat Procarbazin eine Disulfiram-ähnliche Wirkung [44].
Irinotecan
Irinotecan wird zur Behandlung verschiedener Tumorerkrankungen eingesetzt, vor allem zur Behandlung des Kolonkarzinoms. Es gehört zur Gruppe der Topoisomerasehemmer. Irinotecan bewirkt eine Apoptose durch Hemmung des Enzyms DNS-Topoisomerase I, das die räumliche Anordnung der DNS reguliert und in vielen Tumoren gesteigert aktiv ist. Aufgrund seiner ausgeprägten cholinergen Wirkungen kann es je nach Dosis und Infusionsgeschwindigkeit zu Diarrhöen und im Verlauf zu einem cholinergen Syndrom mit Bradykardie und Delir kommen, das durch die Elektrolytverschiebungen im Rahmen der unter Umständen schwerwiegenden Diarrhöen erschwert werden kann [15]. Da Irinotecan wie auch einige Psychopharmaka, allen voran SSRI und Johanniskraut, über das hepatische CYP3A4 und CYP2B6 verstoffwechselt wird, ist Vorsicht bei der Kombinationsbehandlung geboten [65]. Johanniskraut führt zu einer Enzyminduktion des entsprechenden Enzyms und kann dadurch die Wirksamkeit von Irinotecan fast vollständig aufheben, wohingegen SSRI, eher Inhibitoren des entsprechenden Enzyms, zu einer unter Umständen dramatischen Erhöhung der Plasmaspiegel führen können. Entsprechend können gastrointestinale Nebenwirkungen wie Übelkeit, Diarrhöen und Obstipation verstärkt auftreten. Sogar Fälle tödlicher Rhabdomyolysen unter der Kombination von SSRI und Irinotecan sind beschrieben [61].
Glucocorticoide
Diese Substanzklasse gehört sicherlich zu den häufigsten adjuvanten Medikamenten im Rahmen einer Behandlung von verschiedensten Tumorerkrankungen. Sie können zahlreiche neuropsychiatrische Nebenwirkungen auslösen, die allerdings bei jedem Therapiezyklus erheblich variieren können. Zu nennen sind vor allem Hyperaktivität und Insomnie sowie Angst, Affektlabilität und psychomotorische Unruhe. Darüber hinaus können sogenannte „Cortisonpsychosen“ mit affektiver Betonung ausgelöst werden sowie depressive und auch manische Episoden [24]. Diese treten zumeist in den ersten Behandlungswochen auf. Allerdings kann es beispielsweise unter der Behandlung mit Methylprednisolon zu Beginn zu einem antiemetischen, analgetischen und appetitsteigernden Effekt kommen, der durch die Interaktion mit spezifischen Rezeptoren im Gehirn erklärt wird. Die sedativen, antidepressiven und anxiolytischen Fähigkeiten können die Lebensqualität von Tumorpatienten auch deutlich verbessern [10].
Wechselwirkungen zwischen Psychopharmaka und Chemotherapeutika
Auch hier soll lediglich eine relevante Auswahl möglicher Wechselwirkungen dargestellt werden. Wie bereits oben erwähnt, werden die meisten Psychopharmaka über das hepatische Cytochrom-P450-Enzymsystem abgebaut. Hierdurch können Wechselwirkungen entstehen, die bei Kenntnis der Metabolisierung vermeidbar sind. Zu erwähnen ist hierbei Tamoxifen, ein selektiver Estrogen-Rezeptormodulator, der als Arzneistoff zur Therapie von Brustkrebs eingesetzt wird. Tamoxifen ist für die adjuvante Therapie nach Primärbehandlung des Mammakarzinoms und zur Behandlung des metastasierenden Mammakarzinoms zugelassen. Darüber hinaus gibt es Studien, die auf eine Wirksamkeit bei Manie hindeuten [5].
Bis zu 25% der Patientinnen mit Brustkrebs erleiden eine depressive Episode. Neuere Antidepressiva, allen voran die SSRI, werden weit gefächert zur Behandlung der Depression, aber auch zur Verbesserung von Tamoxifen-assoziierten Nebenwirkungen wie Hitzewallungen und anderen Wechseljahr-ähnlichen Beschwerden eingesetzt [60]. Tamoxifen reduziert bei Frauen mit Estrogenrezeptor-positivem Karzinom das Rezidivrisiko um 50% und die Mortalität um ein Drittel.
Tamoxifen ist ein Prodrug, das in der Leber durch CYP2D6 zum pharmakologisch aktiven Endoxifen metabolisiert wird, dadurch kann es in Kombination mit CYP2D6-Inhibitoren zu einer deutlichen Reduktion der Wirksamkeit von Tamoxifen kommen [39]. Zu den relevantesten CYP2D6-Inhibitoren gehören die SSRI Fluoxetin, Paroxetin, Sertralin und weniger stark der dual wirksame Noradrenalin- und Dopamin-Wiederaufnahmehemmer Bupropion [7]. Eine populationsbasierte Kohortenstudie von Kelly et al. mit 2430 Brustkrebspatientinnen konnte diese Wechselwirkung für Paroxetin und Tamoxifen zeigen: Innerhalb des Follow-up-Zeitraums von 2,38 Jahren starben 15,4% der Patientinnen an Brustkrebs. Die Komedikation mit Paroxetin für etwa 41% des Behandlungszeitraums (1,31 Jahre während der Tamoxifen-Behandlung) führte zu einem zusätzlichen Todesfall pro 19,7 Patientinnen. Je länger die gleichzeitige Einnahme von Tamoxifen mit Paroxetin dauerte, desto größer war die Einschränkung des Nutzens der Therapie mit Tamoxifen und desto höher auch die Mortalität durch die Tumorerkrankung [39].
Kognitive Störungen „Chemobrain?“
Speziell in der letzten Dekade wurde vermehrt Augenmerk auf die im Rahmen verschiedener chemotherapeutischer Regime auftretende Neurotoxizität gelegt. Zunächst beklagten die Patienten subjektive kognitive Beschwerden, die mittels neuropsychologischer Testungen für verschiedene Erkrankungen validiert werden konnten. Es findet sich klinisch das Bild einer leichten kognitiven Störung mit Konzentrationsstörungen, Problemen mit der Planung komplexer Handlungsabläufe und Einschränkungen des Kurzzeitgedächtnisses. Dieses Phänomen wurde in der Literatur als „Chemobrain“ bzw. „Chemofog“ umschrieben [22]. Viele, vor allem junge Patientinnen und Patienten, vor allem mit prämorbidem hohem Bildungsstand, berichten über zum Teil stark ausgeprägte kognitive Störungen während und auch längere Zeit nach einer Chemotherapie; derartige neuropsychologische Störungen wurden berichtet für Brustkrebserkrankungen, Hodenkrebs, Lymphome, Leukämien und nach Stamm- und Knochenmarkstransplantationen [1, 20, 34, 70]. Insgesamt ist jedoch die Erfassung der subtilen Störungen schwierig, es gibt wenig geeignete Testbatterien, die auch eine longitudinale Erhebung von Problemen ermöglichen, zumeist kombiniert man neuropsychologische Testverfahren mit zerebraler Bildgebung und phänomenologischen Aspekten.
Die Ergebnisse bezüglich kognitiver Störungen sind uneinheitlich. Meist wird ein diffuses Bild beschrieben mit gestörten Funktionen im Bereich des verbalen Lernens und des verbalen Gedächtnisses, der Aufmerksamkeit und Konzentration sowie von gestörten frontostriatalen Funktionen [6, 58], wohingegen andere Studien keine anhaltenden kognitiven Störungen sogar unter einer Kombinationstherapie zeigen [14, 34]. So zeigte eine Studie von Hermelink et al. mit 101 Brustkrebspatientinnen keine objektivierbaren Störungen in 12 kognitiven Leistungstests, aber deutliche subjektive kognitive Beeinträchtigungen, als deren Prädiktor eine depressive Stimmungslage, ein negativer Affekt als Charaktereigenschaft und ein intensiviertes Therapieregime identifiziert werden konnten [34]. Allerdings sind viele der berichteten subjektiven kognitiven Störungen mit Symptomen wie psychischem Stress, Fatigue und Angst mit der Diagnose einer Tumorerkrankung assoziiert, was weit über die einfache Erfassbarkeit kognitiver Störungen hinausgeht [22]. Viele Studien zeigten dementsprechend zwar objektivierbare kognitive Störungen im Verlauf der Behandlung; wurden diese aber für Angst, Depressivität und Fatigue korrigiert, so waren sie oft nicht mehr nachweisbar oder wesentlich schwächer als erwartet [6].
Als ursächlich für die Entstehung der kognitiven Störungen werden verschiedene Befunde diskutiert. Untersuchungen anhand bildgebender Verfahren konnten eine Verminderung der grauen Substanz vor allem im Bereich der Amygdala, dem parahippokampalen Gyrus und dem Hippokampus, aber auch im Bereich der Basalganglien vor allem bei Brustkrebspatientinnen zeigen [22]. Da es eine Dosis-Wirkungsbeziehung von Chemotherapie und kognitiven Störungen zu geben scheint, vermutet man darüber hinaus eine Störung des zerebralen Metabolismus durch die medikamentöse Behandlung der Krebserkrankung. Diese Störung neuronaler Fasern geht vermutlich auf eine Erhöhung proinflammatorischer Zytokine wie Tumornekrosefaktor(TNF)-α zurück, kann aber auch durch DNS-Schäden, verursacht durch die Chemotherapie, oder auch psychischen Stress hervorgerufen werden [17, 68]. Chronischer Stress kann wiederum Störungen der Hypothalamus-Hypophysen-Nebennierenachse über dauerhaft erhöhte Glucocorticoidspiegel hervorrufen, die strukturelle und funktionelle Einschränkungen der Hirnfunktion hervorrufen können [71]. In einer Studie zu kognitiven Störungen bei der Behandlung des kolorektalen Karzinoms mit Oxaliplatin, 5-Fluoruracil und Leukovorin konnte lediglich eine Verbesserung der emotionalen Verarbeitung während der Chemotherapie nachgewiesen werden, nicht jedoch messbare Auffälligkeiten der mentalen Leistungsfähigkeiten. Die Autoren vermuten, dass das genannte Therapieregime wenig Toxizität auf hormonelle Systeme, beispielsweise den Estrogenhaushalt, hat, da die meisten positiven Studien mit Patienten mit Prostatakarzinom oder Patientinnen mit Brustkrebs durchgeführt wurden [2].
Mögliche Behandlungen verfolgen verschiedene Ansätze. So soll die Behandlung mit einem Stimulans wie Modafinil Erfolg versprechend sein [43]. Andere Forschungsgruppen wiederum empfehlen Gedächtnistraining und die Verbesserung von mentalen Bewältigungsstrategien, moderates Sporttraining und Meditation, wobei die wissenschaftliche Validierung der verschiedenen Methoden noch aussteht [33].
Psychiatrische Psychoonkologie?
Zusammenfassend soll auf einige wichtige Punkte hingewiesen werden.
Zentral bei der Behandlung von psychiatrischen Problemen onkologischer Patienten sind sicherlich die Beachtung von Nebenwirkungen der einzelnen Substanzklassen und die Berücksichtigung von Wechselwirkungen zwischen Psychopharmaka und Chemotherapeutika vor dem Hintergrund der persönlichen Situation des einzelnen Patienten. Womöglich wäre es hilfreich, bereits deutlich früher auch nichtmedikamentöse Behandlungsstrategien zu implementieren, beispielsweise Entspannungsverfahren, Verbesserung von Copingstrategien und sportliche Betätigung.
Darüber hinaus weisen erste experimentelle Daten auf einen Vorteil einer Behandlung mit Antidepressiva bei der Tumorerkrankung hin: SSRI und Trizyklika scheinen das generelle Tumorrisiko zu senken. SSRI sind in der Lage, das Wachstum kolorektaler Tumorzellen zu verlangsamen, und reduzieren sogar die Zytotoxizität von Doxorubicin und verbessern dessen Ansprechen bei der Tumorprogression [42].
Eine weitere Besonderheit stellen jedoch auch Tumorerkrankungen bei psychiatrischen Patienten dar. Die Inzidenz von Tumorerkrankungen scheint bei psychiatrischen Patienten nicht höher zu sein als in der Normalbevölkerung, allerdings haben psychiatrische Patienten eine höhere Mortalität, da sie meist später zur Diagnose gelangen und weniger Zugang zu spezialisierten Therapien haben [41].
Von großer Relevanz für die Lebensqualität sind die sachgerechte Behandlung der zentralnervösen Toxizität von Chemotherapeutika mit Therapie der kognitiven und affektiven Störungen sowie die Handhabung deliranter Syndrome.
Wichtiges für die Praxis
- Antidepressiva sollten in niedriger Dosis langsam eintitriert werden und haben eine Wirklatenz von durchschnittlich zwei Wochen.
- Bei der Behandlung deliranter Syndrome sind hochpotente Neuroleptika niedrigpotenten vorzuziehen. Gegebenenfalls sollte in einer niedrigen Dosis begonnen werden.
- Die Metabolisierung einiger Pharmaka muss bei der Verordnung von Psychopharmaka bedacht werden; allen voran ist an die Cytochrom-P450-Enzyme zu denken.
- SSRI sollten wegen der Wirklatenz und den Interaktionen nur zurückhaltend eingesetzt werden. Erfahrungen zu Alternativen wie Bupropion stehen noch aus.
- Der Einsatz von Benzodiazepinen kann sinnvoll sein, allerdings sollten diese in möglichst niedriger Dosis in einem festen Schema über einen begrenzten Zeitraum eingesetzt werden. Lediglich bei Delirien im Rahmen einer Antibiotikatherapie sind sie in erster Linie indiziert.
- Bei der Behandlung von Fatigue kann der Einsatz von Stimulanzien wie Modafinil oder Methylphenidat erwogen werden.
Literatur
1. Ahles TA, Saykin AJ, McDonald BC, Li Y, et al. Longitudinal assessment of cognitive changes associated with adjuvant treatment for breast cancer: impact of age and cognitive reserve. J Clin Oncol 2010;28:4434–40.
2. Andreis F, Ferri M, Mazzocchi M, Meriggi F, et al. Lack of a chemobrain effect for adjuvant FOLFOX chemotherapy in colon cancer patients. A pilot study. Support Care Cancer 2012.
3. Baldessarini RJ. Drugs and the treatment of psychiatric disorders. In: Gilman AG, Goodman LS, Gilman A (eds.). The Pharmacological Basis of Therapeutics. 6th edition. New York: Macmillan, 1980:391–447.
4. Balon R, Berchou R. Hematologic side effects of psychotropic drugs. Psychosomatics 1986;27:119–20,125–7.
5. Bebchuk JM, Arfken CL, Dolan-Manji S, Murphy J, et al. A preliminary investigation of a proteinkinase C inhibitor in the treatment of acute mania. Arch Gen Psychiatry 2000;57:95–7.
6. Bender CM, Pacella ML, Sereika SM, Brufsky AM, et al. What do perceived cognitive problems reflect? J Support Oncol 2008;6:238–42.
7. Benkert O, Hippius H. Kompendium der Psychiatrischen Pharmakotherapie. 9th edition. Heidelberg: Springer, 2012.
8. Bernard SA, Bruera E. Drug interactions in palliative care. J Clin Oncol 2000;18:1780–99.
9. Brown LF, Kroenke K, Theobald DE, Wu J, et al. The association of depression and anxiety with health-related quality of life in cancer patients with depression and/or pain. Psychooncology 2010;19:734–41.
10. Buclin T, Mazzocato C, Berney A, Stiefel F. Psychopharmacology in supportive care of cancer: a review for the clinician. IV. Other psychotropic agents. Support Care Cancer 2001;9:213–22.
11. Buhre K, de Rossi L, Buhre W. [Preoperative long-term therapy]. Anaesthesist 2005;54:902–13.
12. Cacabelos R. Pharmacogenomics and therapeutic strategies for dementia. Expert Rev Mol Diagn 2009;9:567–611.
13. Carey ME, Hockenberry MJ, Moore IM, Hutter JJ, et al. Brief report: effect of intravenous methotrexate dose and infusion rate on neuropsychological function one year after diagnosis of acute lymphoblastic leukemia. J Pediatr Psychol 2007;32:189–93.
14. Castellon SA, Ganz PA, Bower JE, Petersen L, et al. Neurocognitive performance in breast cancer survivors exposed to adjuvant chemotherapy and tamoxifen. J Clin Exp Neuropsychol 2004;26:955–69.
15. Chabot GG. Clinical pharmacology and pharmacodynamics of irinotecan. A review. Ann N Y Acad Sci 1996;803:164–72.
16. Chan A, Yap KY, Koh D, Low XH, et al. Electronic database to detect drug-drug interactions between antidepressants and oral anticancer drugs from a cancer center in Singapore: implications to clinicians. Pharmacoepidemiol Drug Saf 2011;20:939–47.
17. Chandrashekara S, Jayashree K, Veeranna HB, Vadiraj HS, et al. Effects of anxiety on TNF-α levels during psychological stress. J Psychosom Res 2007;63:65–9.
18. Cimo PL, Pisciotta AV, Desai RG, Pino JL, et al. Detection of drug-dependent antibodies by the 51Cr platelet lysis test: documentation of immune thrombocytopenia induced by diphenylhydantoin, diazepam, and sulfisoxazole. Am J Hematol 1977;2:65–72.
19. Cocito L, Maffini M, Loeb C. Long-term observations on the clinical use of lamotrigine as add-on drug in patients with epilepsy. Epilepsy Res 1994;19:123–7.
20. Correa DD, Ahles TA. Cognitive adverse effects of chemotherapy in breast cancer patients. Curr Opin Support Palliat Care 2007;1:57–62.
21. Coulter DM, Edwards IR. Mianserin and agranulocytosis in New Zealand. Lancet 1990;336:785–7.
22. Dutta V. Psychostimulants for chemotherapy induced cognitive changes in cancer, Ockham’s razor, anyone? J Cancer Res Ther 2011;7:264–9.
23. Focosi D, Azzara A, Kast RE, Carulli G, et al. Lithium and hematology: established and proposed uses. J Leukoc Biol 2009;85: 20–8.
24. Frahm AW, Hager HHJ, Bruchhausen F von, Hager H. Folgeband 4: Stoffe A–K. In: Birkhäuser (ed.). Hagers Handbuch der pharmazeutischen Praxis, 1999:1099.
25. Galbaud du Fort G. [Hematologic toxicity of antidepressive agents]. Encephale 1988;14:307–18.
26. Gaus W, Westendorf J, Diebow R, Kieser M. Identification of adverse drug reactions by evaluation of a prescription database, demonstrated for “risk of bleeding”. Methods Inf Med 2005;44:697–703.
27. Gilbar PJ. A guide to enternal drug administration in palliative care. J Pain Symptom Manage 1999;17:197–207.
28. Grassi L, Rossi E, Caruso R, Nanni MG, et al. Educational intervention in cancer outpatient clinics on routine screening for emotional distress: an observational study. Psychooncology 2011;20:669–74.
29. Guan NC, Termorshuizen F, Laan W, Smeets HM, et al. Cancer mortality in patients with psychiatric diagnoses: a higher hazard of cancer death does not lead to a higher cumulative risk of dying from cancer. Soc Psychiatry Psychiatr Epidemiol 2012.
30. Hall RL, Smith AG, Edwards JG. Haematological safety of antipsychotic drugs. Expert Opin Drug Saf 2003;2:395–9.
31. Harter M, Reuter K, Schretzmann B, Hasenburg A, et al. [Comorbid psychiatric disorders in cancer patients in acute inpatient treatment and medical rehabilitation]. Rehabilitation (Stuttg) 2000;39:317–23.
32. Heckl U, Singer S, Wickert M, Weis J. Aktuelle Versorgungsstrukturen in der Psychoonkologie. Nervenheilkunde 2011;3:124–30.
33. Hede K. Chemobrain is real but may need new name. J Natl Cancer Inst 2008;100:162–3, 169.
34. Hermelink K. Acute and late onset cognitive dysfunction associated with chemotherapy in women with breast cancer. Cancer 2010;117:1103; author reply 1103–4.
35. Huyse FJ, Touw DJ, van Schijndel RS, de Lange JJ, et al. Psychotropic drugs and the perioperative period: a proposal for a guideline in elective surgery. Psychosomatics 2006;47:8–22.
36. Illiger HJ, Hartlapp JH. [Pharmaceutical, pharmacokinetic and dynamic interactions in tumor drug therapy]. Onkologie 1984;7(Suppl 1):10–8.
37. Joerger M. Covariate pharmacokinetic model building in oncology and its potential clinical relevance. Aaps J 2012;14:119–32.
38. Joffe RT, Kellner CH, Post RM, Uhde TW. Lithium increases platelet count. N Engl J Med 1984;311:674–5.
39. Kelly CM, Juurlink DN, Gomes T, Duong-Hua M, et al. Selective serotonin reuptake inhibitors and breast cancer mortality in women receiving tamoxifen: a population based cohort study. BMJ 2010;340:c693.
40. King DJ, Wager E. Haematological safety of antipsychotic drugs. J Psychopharmacol 1998;12:283–8.
41. Kisely S, Crowe E, Lawrence D. Cancer-related mortality in people with mental illness. Arch Gen Psychiatry 2012;1–9.
42. Kissane DW, Haj M, Sartorius N. Depression and Cancer (World Psychiatric Association). 2nd edition. New York: John Wiley & Sons, 2010.
43. Kohli S, Fisher SG, Tra Y, Adams MJ, et al. The effect of modafinil on cognitive function in breast cancer survivors. Cancer 2009;115:2605–16.
44. Kroner T, Margulies A, Taverna C. Medikamente in der Tumortherapie: Handbuch für die Pflegepraxis. 3. Auflage. Berlin: Springer, 2011.
45. Lieberman JA, Johns CA, Kane JM, Rai K, et al. Clozapine-induced agranulocytosis: non-cross-reactivity with other psychotropic drugs. J Clin Psychiatry 1988;49:271–7.
46. Lindae ML, Luy J, Abel EA, Kaplan R. Mycosis fungoides with CNS involvement: neuropsychiatric manifestations and complications of treatment with intrathecal methotrexate and whole-brain irradiation. J Dermatol Surg Oncol 1990;16:550–3.
47. Mazaira S. [Haematological adverse effects caused by psychiatric drugs]. Vertex 2008;19:378–86.
48. Mehnert A, Veers S, Howaldt D, Braumann KM, et al. Effects of a physical exercise rehabilitation group program on anxiety, depression, body image, and health-related quality of life among breast cancer patients. Onkologie 2012;34:248–53.
49. Meyboom RH, Hekster YA, Egberts AC, Gribnau FW, et al. Causal or casual? The role of causality assessment in pharmacovigilance. Drug Saf 1997;17:374–89.
50. Miovic M, Block S. Psychiatric disorders in advanced cancer. Cancer 2007;110:1665–76.
51. Mitchell AJ, Chan M, Bhatti H, Halton M, et al. Prevalence of depression, anxiety, and adjustment disorder in oncological, haematological, and palliative-care settings: a meta-analysis of 94 interview-based studies. Lancet Oncol 2011;12:160–74.
52. Mutschler E, Geisslinger G, Kroemer HK, Menzel S, et al. Mutschler Arzneimittelwirkungen: Pharmakologie – Klinische Pharmakologie – Toxikologie. 10. Auflage. Stuttgart: Wissenschaftliche Verlagsgesellschaft, 2012.
53. Nazer LH, Shankar G, Ali BA, Al-Najjar T. Fatal agranulocytosis associated with psychotropic medication use. Am J Health Syst Pharm 2012;69:863–7.
54. Newton HB. Neurological complications of hemotherapy to the central nervous system. Handb Clin Neurol 2012;105:903–16.
55. Osoba D, Brada M, Yung WK, Prados M. Health-related quality of life in patients treated with temozolomide versus procarbazine for recurrent glioblastoma multiforme. J Clin Oncol 2000;18:1481–91.
56. Oyesanmi O, Kunkel EJ, Monti DA, Field HL. Hematologic side effects of psychotropics. Psychosomatics 1999;40:414–21.
57. Ozkara C, Dreifuss FE, Apperson Hansen C. Changes in red blood cells with valproate therapy. Acta Neurol Scand 1993;88:210–2.
58. Poppelreuter M, Weis J, Kulz AK, Tucha O, et al. Cognitive dysfunction and subjective complaints of cancer patients. a cross-sectional study in a cancer rehabilitation centre. Eur J Cancer 2004;40:43–9.
59. Rall TW, Schleifer LS. Drugs effective in the therapy of the epilepsies. In: Gilman AG GL, Gilman A (ed.). The Pharmacological Basis of Therapeutics. 6th edition. New York: Macmillan, 1980:448–74.
60. Reich M, Lesur A, Perdrizet-Chevallier C. Depression, quality of life and breast cancer: a review of the literature. Breast Cancer Res Treat 2008;110:9–17.
61. Richards S, Umbreit JN, Fanucchi MP, Giblin J, et al. Selective serotonin reuptake inhibitor-induced rhabdomyolysis associated with irinotecan. South Med J 2003;96:1031–3.
62. Shimizu K, Ishibashi Y, Umezawa S, Izumi H, et al. Feasibility and usefulness of the “Distress Screening Program in Ambulatory Care” in clinical oncology practice. Psychooncology 2010;19:718–25.
63. Singer S, Bringmann H, Hauss J, Kortmann RD, et al. [Prevalence of concomitant psychiatric disorders and the desire for psychosocial help in patients with malignant tumors in an acute hospital]. Dtsch Med Wochenschr 2007;132:2071–6.
64. Skop BP, Brown TM. Potential vascular and bleeding complications of treatment with selective serotonin reuptake inhibitors. Psychosomatics 1996;37:12–6.
65. Slatter JG, Schaaf LJ, Sams JP, Feenstra KL, et al. Pharmacokinetics, metabolism, and excretion of irinotecan (CPT-11) following i.v. infusion of [(14)C]CPT-11 in cancer patients. Drug Metab Dispos 2000;28:423–33.
66. Stiefel FC, Kornblith AB, Holland JC. Changes in the prescription patterns of psychotropic drugs for cancer patients during a 10-year period. Cancer 1990;65:1048–53.
67. Stubner S, Grohmann R, Schmauss M. [Drug safety in clinical practice – part 1: psychopharmacological treatment]. Fortschr Neurol Psychiatr 2012;80:468–80, quiz 481.
68. Tangpong J, Cole MP, Sultana R, Joshi G, et al. Adriamycin-induced, TNF-alpha-mediated central nervous system toxicity. Neurobiol Dis 2006;23:127–39.
69. Uhr M, Grauer MT, Holsboer F. Differential enhancement of antidepressant penetration into the brain in mice with abcb1ab (mdr1ab) P-glycoprotein gene disruption. Biol Psychiatry 2003;54:840–6.
70. Vardy J, Rourke S, Tannock IF. Evaluation of cognitive function associated with chemotherapy: a review of published studies and recommendations for future research. J Clin Oncol 2007;25:2455–63.
71. Wiedenmayer CP, Bansal R, Anderson GM, Zhu H, et al. Cortisol levels and hippocampus volumes in healthy preadolescent children. Biol Psychiatry 2006;60:856–61.
72. Zabora J, BrintzenhofeSzoc K, Curbow B, Hooker C, et al. The prevalence of psychological distress by cancer site. Psychooncology 2001;10:19–28.
Dr. Dr. med. Günter Niklewski, Klinik für Psychiatrie und Psychotherapie, Klinikum Nürnberg Nord, Prof.-Ernst-Nathan-Straße 1, 90419 Nürnberg, E-Mail: Niklewski@klinikum-nuernberg.de
Priv.-Doz. Dr. Teresa Biermann, Klinik für Psychiatrie und Psychotherapie, Klinikum Nürnberg Nord, Prof.-Ernst-Nathan-Straße 1, 90419 Nürnberg
Special aspects of psychopharmacotherapy in an oncological setting
The specialty of psychooncology comprises the entire spectrum of psychosocial counselling up to a specialized psychotherapy including psychopharmacotherapy.
In order to treat mental disorders in oncological patients, several special aspects have to be taken into account as follows: Many psychopharmacotherapeutics have potential hematological side effects themselves that might have a serious impact on the oncological disease and its treatment. The most important side effects of the most common psychiatric drugs are described. Furthermore, some side effects of chemotherapeutics relevant for psychiatrists are mentioned. Due to the different metabolism of various categories of drugs there is a variety of possible interactions that have to be thought of as they might diminish the effectivity of each drug. An example of an interaction with a serious impact on mortality is the reduced effect of tamoxifen in combination with paroxetine through inhibition of the cytochrome P450 enzyme 2D6.
Also of relevance are affective and cognitive disturbances due to chemotherapy in terms of the so called “chemobrain” in certain groups of cancer patients. The assumed causes of chemobrain and possible ways of treatment are described here.
In sum, further research is still required to better understand and treat the complex interactions of the psyche and the body in oncologic patients.
Key words: psychopharmacotherapy, oncology, psychooncology, chemobrain
Psychopharmakotherapie 2013; 20(03)
