Priv.-Doz. Dr. Dieter Angersbach, Wolfratshausen
Der Wirkstoff Lurasidon gehört zu den sogenannten atypischen Antipsychotika. Charakteristisch für diese Substanzen ist, dass sie potentere Serotonin-5-HT2- als Dopamin-D2-Antagonisten sind. In Rezeptorstudien war auch Lurasidon ein potenter Antagonist des 5-HT2A-Rezeptors mit einer Inhibitionskonstante (Ki) von 0,47 und ein schwächerer Antagonist des D2-Rezeptors (Ki 0,99). Die Affinität für den 5-HT7-Rezeptor (Ki 0,49) ist nahezu ebenso hoch wie für den 5-HT2A-Rezeptor, die Bindung an den 5-HT1A-Rezeptor dagegen deutlich schwächer (Ki 6,4).
Lurasidon wurde im November 2010 in den USA zur Behandlung der Schizophrenie zugelassen (Latuda®). Bei der vorliegenden 6-wöchigen Doppelblindstudie handelt es sich um eine Phase-III-Studie mit dem primären Ziel, die Wirksamkeit zweier Dosen von Lurasidon (40 und 120 mg/Tag) im Vergleich mit Plazebo zu untersuchen. Die Studie wurde von Januar 2008 bis Juni 2009 von 52 Zentren in Kolumbien, Litauen, Asien (Indien, Philippinen) und den USA durchgeführt.
Studiendesign
Eingeschlossen wurden stationäre männliche und weibliche Patienten im Alter von 18 bis 75 Jahren mit der Diagnose einer Schizophrenie nach DSM-IV. Die Erkrankung musste seit mindestens einem Jahr bestehen und die Dauer des Klinikaufenthalts wegen der akuten Exazerbation durfte nicht länger als zwei Wochen sein. Weitere Einschlusskriterien waren: ein CGI-S-Score von ≥4 (mäßig krank und schwerer) und ein PANSS-Gesamtscore von ≥80, wobei wenigstens zwei der folgenden Items einen Score von ≥4 haben mussten: Wahnvorstellungen, formale Denkstörung, Halluzination, ungewöhnliche Denkinhalte und Misstrauen/Verfolgungswahn.
Die Patienten wurden im Verhältnis von 1:1:1:1 randomisiert einem der vier Behandlungsarme zugewiesen: 40 mg/Tag Lurasidon, 120 mg/Tag Lurasidon, 15 mg/Tag Olanzapin und Plazebo. Der Olanzapin-Arm wurde zur Überprüfung der Testempfindlichkeit einbezogen.
Die Patienten der beiden Lurasidon-Arme erhielten zu Behandlungsbeginn die Zieldosis (40 bzw. 120 mg/Tag); Olanzapin wurde an den Tagen 1 bis 7 mit 10 mg/Tag dosiert, danach mit 15 mg/Tag. Die Studienmedikation wurde einmal täglich (mit dem Frühstück) eingenommen. Eine begrenzte Einnahme von Benzodiazepinen gegen schwere Angst, Agitiertheit oder Schlaflosigkeit war möglich. Nach drei Wochen der Behandlung wurde erwogen, Patienten mit einem CGI-S-Score von ≤3 nach Hause zu entlassen.
Die Wirksamkeit wurde mithilfe des PANSS-Gesamtscores und der Scores der Subskalen (Positivskala, Negativskala, psychopathologische Globalskala), der CGI-S-Skala und der Montgomery-Åsberg-Depressionsskala (MADRS) beurteilt. Primärer Wirksamkeitsparameter war die mittlere Änderung des PANSS-Scores vom Einschluss bis Woche 6 der Behandlung. Extrapyramidal-motorische Symptome wurden eingestuft mit der Simpson-Angus Extrapyramidal Side Effect Scale, der Barnes Akathisia Scale und der Abnormal Involuntary Movement Scale. Zur Kontrolle der Sicherheit wurden Vitalparameter gemessen, verschiedene Laborparameter untersucht und die unerwünschten Ereignisse registriert.
Ergebnisse
Patienten. Von den 781 gescreenten Patienten konnten 478 randomisiert der 6-wöchigen Behandlung zugewiesen werden (Lurasidon 40 mg: n=120; Lurasidon 120 mg: n=119; Olanzapin: n=123; Plazebo: n=116). Der PANSS-Gesamtscore lag bei Randomisierung zwischen 95,8 (Plazebo) und 97,9 Punkten (Lurasidon 120 mg; Olanzapin: 96,3; Lurasidon 40 mg: 96,6). Der Anteil der Patienten, der die Studie protokollgemäß nach sechs Behandlungswochen beendete, war in der Lurasidon-40-mg-Gruppe etwa ebenso hoch (64,2%) wie in der Plazebo-Gruppe (61,2%). In der Olanzapin-Gruppe lag dieser Anteil bei 68,3% und in der Lurasidon-120-mg-Gruppe bei 55,5%.
Wirksamkeit. Die Änderung im PANSS-Gesamtscore vom Einschluss bis Woche 6 war unter Lurasidon 40 mg (–25,7; p=0,002) und 120 mg (–23,6; p=0,022) signifikant größer als unter Plazebo (–16,0). Auch unter der Olanzapin-Behandlung waren die Änderungen signifikant größer als in der Plazebo-Gruppe (–28,7; p=0,001) – eine Bestätigung der Empfindlichkeit des Testdesigns (Abb. 1). Bereits nach einer Woche waren die Lurasidon-40-mg- und die Olanzapin-Gruppe signifikant von Plazebo verschieden (p=0,022 bzw. p=0,008) und ab Woche 3 war dies auch die Lurasidon-120-mg-Gruppe (p=0,004).
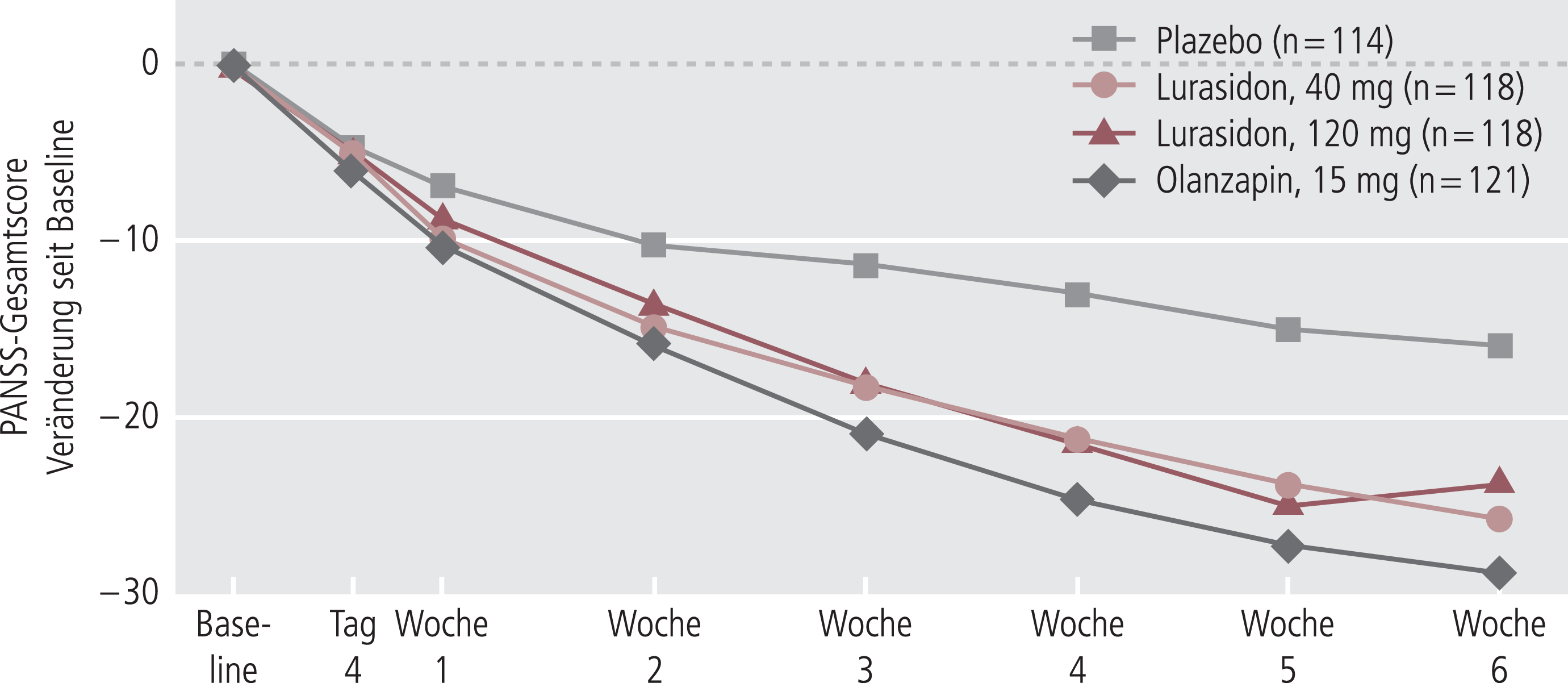
Abb. 1. Änderung des mittleren PANSS-Gesamtscores vom Einschluss bis zum Studienende. Signifikanzen im Vergleich zu Plazebo nach Woche 6: Olanzapin: p<0,001, Lurasidon 40 mg: p<0,001, Lurasidon 120 mg: p=0,011 (ein statistisch signifikanter Unterschied zu Plazebo bestand für Olanzapin und Lurasidon 40 mg ab Woche 1, für Lurasidon 120 mg ab Woche 3).
Sowohl beide Lurasidon-Dosen als auch Olanzapin verbesserten die Scores der drei PANSS-Subskalen gegenüber Plazebo signifikant. Die Änderung des CGI-S-Scores war unter Lurasidon 40 mg (–1,5; p=0,011) und Lurasidon 120 mg (–1,4; p=0,040) signifikant größer als unter Plazebo. Auch in der Olanzapin-Gruppe waren die Änderungen signifikant (–1,5; p<0,001). Ein Vergleich der PANSS-Gesamtscores und der CGI-S-Scores der drei aktiven Therapien nach Woche 6 ergab keine statistisch signifikanten Unterschiede.
Die Verbesserungen im MADRS waren unter beiden Lurasidon-Dosen statistisch nicht vom Plazebo-Effekt verschieden. Unter Olanzapin war die Verbesserung gegenüber Plazebo jedoch signifikant (p=0,003).
Sicherheit. Mindestens ein unerwünschtes Ereignis hatten 72 bis 82% der Patienten (Tab. 1); 6 bis 12% beendeten deshalb die Studie vorzeitig. Die häufigste Ursache für den Abbruch war unter Lurasidon Akathisie, die dosisabhängig bei über 10% der Patienten auftrat (Tab. 1), und unter Olanzapin Gewichtszunahme (20%). Die häufigsten unerwünschten Wirkungen waren unter Lurasidon Kopfschmerz, Akathisie und Somnolenz. Unter Olanzapin traten am häufigsten Sedierung, Kopfschmerz und Insomnie auf.
Tab. 1. Unerwünschte Ereignisse (UE) während der sechswöchigen Studie
|
Ereignis |
Lurasidon 40 mg/Tag |
Lurasidon 120 mg/Tag |
Olanzapin 15 mg/Tag |
Plazebo |
|
Patienten mit wenigstens einem UE [%] |
75,6 |
82,2 |
82,0 |
72,4 |
|
Vorzeitiger Studienabbruch wegen UE [%] |
6,7 |
11,8 |
6,5 |
8,6 |
|
Akathisie [%] |
11,8 |
22,9 |
7,4 |
0,9 |
Anticholinergika zur Behandlung extrapyramidal-motorischer Symptome nahmen 18% der Olanzapin- und 20% der Lurasidon-40-mg-Patienten, aber 41% der Patienten mit Lurasidon 120 mg/Tag.
Bei den Änderungen im Körpergewicht und den metabolischen Parametern bestand unter Lurasidon kein signifikanter Unterschied zu Plazebo. Dagegen wurden unter Olanzapin eine signifikante Zunahme des Körpergewichts (im Mittel 4,1 kg; p<0,001) und ein signifikanter Anstieg des Cholesterol- (p<0,001), des LDL- (p=0,010) und des Triglycerid-Spiegels (p<0,001) festgestellt.
Kommentar
Ein wichtiges Ergebnis dieser Studie ist, dass Lurasidon in der Akutbehandlung der Schizophrenie wirksam war. Auch wenn Olanzapin nur als Testkontrolle diente, scheint die Wirksamkeit von Lurasidon mit der von Olanzapin vergleichbar zu sein. Ein weiteres Ergebnis ist, dass sich in Bezug auf die antipsychotische Wirkung keine Dosisabhängigkeit zeigen ließ. Eine Dosis-Wirkungs-Beziehung wurde auch in einer anderen Phase-III-Studie nicht gefunden. Dort waren 80 mg/Tag die optimale Dosis, während sich 40 und 120 mg nicht signifikant von Plazebo unterschieden. Auch in einem weiteren Vergleich waren 80 mg Lurasidon der Plazebo-Behandlung signifikant überlegen, so dass man insgesamt den Eindruck gewinnt, dass 40 mg/Tag eine geeignete Startdosis sein könnte und mit 80 mg eine Steigerung der Wirksamkeit möglich ist. Dagegen scheinen 120 mg/Tag keinen zusätzlich Nutzen, sondern nur mehr Nebenwirkungen zu haben.
Quelle
Meltzer HY, et al. Lurasidone in the treatment of schizophrenia: A randomized, double-blind, placebo- and olanzapine-controlled study. Am J Psychiatry 2011;168:957–67.
Psychopharmakotherapie 2012; 19(04)
