Ortwin Pfeiffer, Bad Emstal, Detlef Degner, Göttingen, Eveline Jaquenoud Sirot, Brugg (Schweiz), Eckart Rüther, Göttingen/München, Christoph Schmid und Michael Franz, Bad Emstal
Kasuistik
Der nach fremdanamnestischen Angaben seit fünf bis sechs Jahren demente Patient war bis zu seiner erstmaligen Aufnahme in eine psychiatrische Klinik von der Ehefrau zu Hause versorgt worden. Der behandelnde niedergelassene Psychiater wies ihn zur stationären Behandlung ein, als dies wegen anhaltender Situationsverkennung mit gehäuften tätlich aggressiven Impulsdurchbrüchen, ausgeprägter Unruhe und Wachrhythmusstörung nicht mehr zu bewältigen war.
Gemäß hausärztlichem Medikamentenplan hatte er zuletzt täglich 50 mg Captopril, 25 mg Hydrochlorothiazid, 5 mg Bisoprolol, 120 mg Isosorbiddinitrat, 100 mg Acetylsalicylsäure, 10 mg Alfuzosin, 16 mg Galantamin und 1 mg (möglicherweise früher auch 1,5 mg) Risperidon als Regelmedikation erhalten, zusätzlich als Bedarfsmedikation 4-mal täglich 25 bis 50 mg Melperon und bis 2 mg Lorazepam.
Somatoananmnestisch waren bei Aufnahme eine arterielle Hypertonie, koronare Herzkrankheit, Prostatahyperplasie und eine etwa fünf Jahre zurückliegende Knieprothesenimplantation bekannt.
Bei der Aufnahmediagnostik fand sich im EKG ein Rechtsschenkelblock. Die QT-Zeit von 390 ms ergab bei einem RR-Abstand von 714 ms und einer QRS-Dauer von 140 ms eine niedrig-normale korrigierte QT-Zeit von 411 ms nach der QTRR,QRS-Formel von Rautaharju [5, 6] für intraventrikuläre Leitungsstörungen mit verlängerter QRS-Zeit.
Bei der Laboruntersuchung fielen eine Niereninsuffizienz mit einer nach CKD-EPI bzw. MDRD geschätzten glomerulären Filtrationsrate (GFR) von 30,6 bzw. 32,7 ml/min (bei einem Serumcreatinin-Wert von 1,5 mg/dl) und eine normochrome Anämie mit einem Hämoglobin-Wert von 12,8 g/dl auf; der Serumkaliumspiegel lag mit 4,0 mmol/l im mittleren Referenzbereich. Die Creatinkinase war leicht erhöht mit 207 U/l (Referenzbereich bis 174) bei normaler CK-MB (Creatinkinase-Myokardtyp). Die Werte der Transaminasen und Gamma-Glutamyltransferase lagen im Referenzbereich. Der Bilirubin-Wert und International normalized Ratio (INR) wurden – bei anamnestisch und klinisch fehlenden Anhaltspunkten für eine Leberfunktionsstörung – nicht bestimmt.
Die native craniale Computertomographie (CCT) erbrachte keinen auffälligen Befund außer einer Erweiterung der inneren und äußeren Liquorräume, die keine Progredienz im Vergleich mit dreieinhalb Jahre zurückliegenden Voraufnahmen zeigte.
Im stationären Verlauf bestätigten sich die fremdanamnestischen Angaben massiver Unruhe mit vollständig aufgehobenem Tag-Nacht-Rhythmus und über längere Phasen lautem nächtlichen Rufen; aggressive Verhaltensstörungen sind nicht dokumentiert. Neben zeitweiser Einzelbetreuung wurde zusätzlich zur Vormedikation Haloperidol in einer Dosis von 5 mg eingesetzt und Lorazepam durch Oxazepam (feste Dosis von 20 bzw. ab dem zweiten Tag 15 mg zur Schlafinduktion) ersetzt. Melperon wurde als Regelmedikation mit 250 mg und Bedarfsmedikation mit bis 6-mal 25 mg belassen. Ab dem vierten Behandlungstag ließ das Ausmaß der Unruhe etwas nach, worauf unter der Vorstellung eines vollständigen Umsetzens von Haloperidol auf Risperidon Ersteres von 5 auf 2,5 mg reduziert und Letzteres von 1 auf 1,5 mg erhöht wurde. Der Medikationsverlauf ist in Tabelle 1 im Überblick dargestellt.
Tab. 1. Medikationsverlauf (Tagesdosis [mg]); Tag 0 = stationäre Aufnahme
|
Arzneistoff |
Tag |
||||||||||||
|
–1 |
0 |
1 |
2 |
3 |
4 |
5 |
6 |
7 |
8 |
9 |
10 |
11 |
|
|
Galantamin |
16 |
" |
" |
" |
" |
" |
" |
" |
" |
" |
" |
" |
" |
|
Haloperidol |
5 |
" |
" |
" |
" |
3 |
3 |
2,5 |
" |
" |
" |
||
|
Lorazepam |
Bis 2* |
– |
– |
– |
– |
– |
– |
– |
– |
– |
– |
– |
– |
|
Melperon |
100–200* |
200 |
300 |
225 |
200 |
300 |
275 |
250 |
250 |
225 |
250 |
250 |
250 |
|
Oxazepam |
20 |
15 |
" |
" |
" |
" |
" |
" |
" |
" |
" |
||
|
Risperidon |
1(–1,5) |
1 |
" |
" |
" |
" |
" |
" |
" |
1,5 |
" |
" |
" |
|
Acetylsalicylsäure |
100 |
" |
" |
" |
" |
" |
" |
" |
" |
" |
" |
" |
" |
|
Alfuzosin |
10 |
" |
" |
" |
" |
" |
" |
" |
" |
" |
" |
" |
" |
|
Bisoprolol |
5 |
" |
" |
" |
" |
" |
" |
" |
" |
" |
" |
" |
" |
|
Captopril |
50 |
" |
" |
" |
" |
" |
" |
" |
" |
" |
" |
" |
" |
|
Hydrochlorothiazid |
25 |
" |
" |
" |
" |
" |
" |
" |
" |
" |
" |
" |
" |
|
Isosorbiddinitrat |
120 |
" |
" |
" |
" |
" |
" |
" |
" |
" |
" |
" |
" |
": letztgenannte Dosis weitergeführt; *: Bedarfsmedikation; –: abgesetzt
Am elften Behandlungstag war der Patient vor dem Frühstück sehr müde, konnte aber danach „in Begleitung den gesamten Stationsflur entlang gehen“. Am nächsten Tag ist der Patient „nach dem begleiteten Toilettengang um 16:05 Uhr kollabiert und zusammengebrochen“. Das wenige Minuten später eingetroffene Reanimationsteam brach die Wiederbelebungsmaßnahmen ab, nachdem die Patientenverfügung eingesehen worden war, die eine Reanimation ausschloss. Das Ergebnis der EKG-Ableitung ist dem Notfallprotokoll nicht zu entnehmen. Der Patient wurde nicht obduziert.
Interaktionspharmakologie
Die nachträgliche Überprüfung der möglichen Interaktionen mithilfe der Internet-basierten Datenbank mediQ [11] zeigte ein komplexes Geflecht möglicher Interaktionen. Es fand sich bei fünf Wirkstoffen der Hinweis „QT-Verlängerung“, bei fünf Wirkstoffen der Hinweis „Dosisanpassung bei Niereninsuffizienz“ (Tab. 2) und bei sechs Wirkstoffen der Hinweis „Dosisanpassung bei Leberinsuffizienz“.
Tab. 2. Erforderlichkeit einer Dosisanpassung bei Niereninsuffizienz (nach [11])
|
Wirkstoff |
Dosisanpassung bei Niereninsuffizienz |
|
Haloperidol |
Nein |
|
Risperidon |
Ja/halbieren |
|
Melperon |
Nein/vorsichtig dosieren |
|
Galantamin |
Nein/nur unter 9 ml/min |
|
Captopril |
Ja/nach Creatinin-Clearance |
|
Bisoprolol |
Ja/nach Creatinin-Clearance |
|
Alfuzosin |
Nein |
|
Hydrochlorothiazid |
Ja |
In der Einstellung „ab durchschnittliche Interaktion“ wurden fünf klinisch relevante Interaktionen über das Cytochrom P450 (präziser CYP2D6) gezeigt, die die QT-Zeit-verlängernden Wirkstoffe Galantamin, Melperon, Risperidon und Haloperidol betreffen. Neun der elf eingenommenen Arzneistoffe können allein oder in gegenseitiger Wirkungsverstärkung blutdrucksenkend wirken.
Abbildung 1 stellt die hinsichtlich der erwogenen Todesursachen relevanten Teile dieses Interaktionsgeflechts vereinfacht dar (die Zahlen an den Pfeilen beziehen sich auf das Risiko für Torsades de Pointes (nach [10]). Denkbare Interaktionen bei nicht ausgeschlossener weniger schwerer Leberfunktionsbeeinträchtigung sind nicht berücksichtigt.
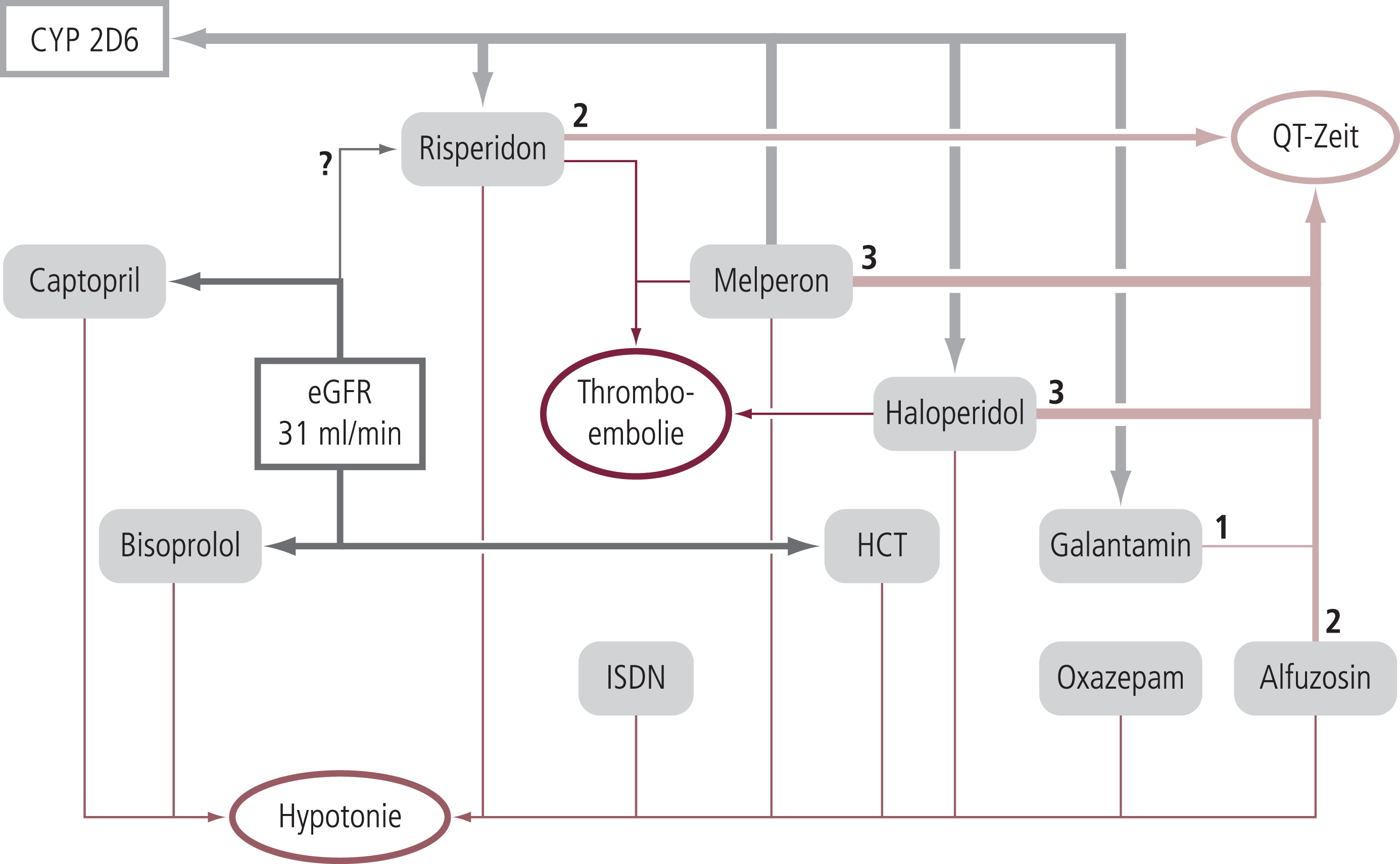
Abb. 1. Schematisierte Darstellung der bezüglich der erwogenen Todesursachen relevanten Arzneimittelinteraktionen. Zahlen an den rosa Pfeilen geben das Risiko für Torsades des Pointes (TdP) an (1: Risiko für TdP [risk of torsades]; 2: mögliches Risiko für TdP [possible risk of torsades]; 3: bedingtes Risiko für TdP [conditional risk of torsades]) (nach [10])
Die eGFR (geschätzte glomeruläre Filtrationsrate) liegt im Grenzbereich zur schweren Nierenfunktionseinschränkung; Q0 (extrarenale Dosisfraktion) beträgt 0,5 für Bisoprolol, 0,55 für Captopril, und 0,05 für HCT (nach [4]). Angaben zur Dosisreduzierung von Risperidon lassen Fragen offen. Galantamin, Risperidon und Haloperidol sind Substrate von CYP2D6, Melperon und Haloperidol mittelstarke CYP2D6-Inhibitoren.
HCT: Hydrochlorothiazid, ISDN: Isosorbiddinitrat
Diskussion
Als wahrscheinlichste Ursachen des plötzlichen Exitus letalis kommen eine kardiale Arrhythmie, eine thromboembolische Komplikation oder eine hypotone Kreislaufdysregulation in Betracht. Die zwei in den letzten fünf Lebenstagen bei bis zum Exitus konstanter Medikation dokumentierten Blutdruckmessungen ergaben normotone Werte, obwohl (bei insgesamt 10 Messungen im Behandlungsverlauf) zuvor auch hypotone Werte gemessen wurden (Tab. 3). Somit ist ein Blutdruckabfall als Todesursache nicht auszuschließen, aber ein Zusammenhang mit der Psychopharmakotherapie weniger plausibel.
Tab. 3. Vollständige Liste der gemessenen Kreislaufwerte des Patienten im Verlauf der stationären Behandlung
|
Behandlungstag |
Uhrzeit |
Blutdruck systolisch |
Blutdruck diastol. |
|
1 |
14:30 |
95 |
50 |
|
1 |
19:15 |
90 |
55 |
|
2 |
18:30 |
100 |
60 |
|
3 |
09:00 |
90 |
60 |
|
3 |
19:30 |
115 |
55 |
|
4 |
18:30 |
75 |
50 |
|
4 |
19:15 |
90 |
60 |
|
9 |
09:00 |
120 |
70 |
|
11 |
09:00 |
120 |
80 |
Angesichts der Vielzahl und des Interaktionspotenzials der Wirkstoffe mit bekanntem Risiko für eine QT-Zeit-Verlängerung erscheint der Verdacht einer kardialen Rhythmusstörung als Todesursache nahe liegend, wenn auch das EKG bei Aufnahme außer einem Rechtsschenkelblock keinen Anlass zu erhöhter Vorsicht in dieser Richtung zu geben schien. Da der Patient kurz vor der beim behandelnden Kollegen routinemäßig nach zwei Wochen eingeplanten EKG-Kontrolle verstarb, bleibt allerdings selbst die Überlegung einer QT-Zeit-Verlängerung hypothetisch. Schlussendlich steht nur fest, dass ein Zusammenhang zwischen der Psychopharmakotherapie und dem unerwarteten plötzlichen Ableben des Patienten nicht auszuschließen ist. Um einen „wahrscheinlichen“ Zusammenhang nach AMSP-Kriterien zu postulieren, müsste durch entsprechende Messergebnisse eindeutig eine zeitlich korrelierende Hypotonie-Entwicklung oder Reizleitungsstörung dokumentiert sein. Im Fall eines thromboembolischen Ereignisses würde man selbst bei gesicherter Diagnose nur einen „möglichen“ Zusammenhang sehen können. In diesem Sinne wurde in der AMSP-Fallkonferenz ein gemeinsamer mitursächlicher Zusammenhang mit dem plötzlichen Versterben des Patienten nach AMSP-Kriterien als „möglich“ für die Wirkstoffe Haloperidol, Risperidon, Melperon, Galantamin und Alfuzosin eingestuft.
Neben den offen bleibenden Fragen nach Todesursache und Zusammenhang derselben mit der Psychopharmakotherapie wirft die Betrachtung dieses Falls weitere Fragen zum Risikomanagement in der gerontopsychiatrischen Pharmakotherapie auf.
Aus informationstheoretisch-algorithmischer Sicht ist zu konstatieren, dass ohne EDV-gestützte Interaktionsprüfung ein solches Risikomanagement nicht implementiert werden kann, da mit der Zahl der verordneten Wirkstoffe die Komplexität jedes denkbaren Abgleichalgorithmus mit exponentieller Ordnung steigt und „von Hand“ nicht zu bewältigen ist.
Dieser Fall zeigt sogar, dass bei einer größeren Zahl zu prüfender Substanzen selbst die Ausgabe eines aktuellen Werkzeugs zur Interaktionsprüfung schon wieder einen Komplexitätsgrad aufweisen kann, der im Arbeitsalltag auf Station oder in der Praxis kaum in der zur Verfügung stehenden Zeit zu erfassen ist. Alle den Autoren bekannten aktuellen Werkzeuge zur Interaktionsprüfung liefern Listen von Interaktionen jeweils zweier Substanzen. Ob es zukünftig Möglichkeiten geben wird, komplex kaskadierende und zirkuläre bis vernetzte Interaktionsmechanismen, wie sie in diesem Fall eine Rolle spielen können, informationstechnologisch berechenbar zu machen und für menschliche Auffassung überschaubar darzustellen, ist zur Zeit noch nicht absehbar.
Gegenwärtig ist in solchen Fällen die Hinzuziehung von Interaktionsexperten hilfreich, wenn auch im klinischen gerontopsychiatrischen Alltag bei Knappheit von Ressourcen nicht in dem Umfang realisierbar, wie die Häufigkeit von Polypharmazie bei alten Patienten es als ratsam erscheinen ließe.
Beim Verfolgen von Angaben zur Dosisreduzierung bei eingeschränkter Nierenfunktion erwiesen sich pharmakokinetische Informationen teilweise als nicht oder lückenhaft verfügbar oder inkonsistent. Beispielsweise führte die Interaktionsrecherche in diesem Fall zu dem Hinweis, dass die Risperidon-Dosis nach Herstellerangaben bei Niereninsuffizienz halbiert werden soll [11, 12]. Differenziertere Angaben, die eine individuelle Dosisanpassung nach Ausmaß der Nierenfunktionseinschränkung ermöglichen würden, fanden sich in der Fachinformation des Herstellers nicht. Nach [4] beträgt die extrarenale Dosisfraktion Q0 für Risperidon 0,95 bzw. 0,8 für „Risperidon-Metaboliten“, wobei Daten für Paliperidon selbst nicht explizit angegeben sind. Eine nach der geschätzten glomerulären Filtrationsrate (eGFR, estimated GFR) zu berechnende Dosisreduzierung bzw. alternativ Verlängerung des Dosierungsintervalls wird aber erst bei einer Q0 von kleiner als 0,8 empfohlen [4]. In Hersteller-Fachinformationen zu Paliperidon fand sich schließlich die Angabe, dass Paliperidon überwiegend renal eliminiert wird [13, 14], was einer Q0 von deutlich unter 0,5 entsprechen sollte.
Auch die Frage, wie sich weniger schwere Einschränkungen der Leberfunktion quantifizieren und in differenzierte Dosisanpassungen der überwiegend hepatisch metabolisierten Psychopharmaka umsetzen lassen, ist gegenwärtig für den klinischen Alltag noch nicht gelöst [9].
In der gerontopsychiatrischen klinischen Alltagssituation steht sehr häufig dem zuweilen unberechenbar erscheinenden Risiko der Behandlung deren unabweisbare Notwendigkeit aufgrund gravierender, die Versorgung der Patienten gefährdender Verhaltensauffälligkeiten gegenüber.
Der Ausweg aus diesem Dilemma sollte, solange keine praktikablen risikoärmeren Alternativen existieren, nicht darin bestehen, die Anwendung oder Kombination von Substanzen mit potenziellen Risiken in der Gerontopsychiatrie rigide einzuschränken. Vielmehr sollten diese Risiken durch entsprechend engmaschige Überwachung der relevanten Parameter kontrolliert werden.
Werkzeuge zur Aufdeckung von Interaktions- und Nebenwirkungsrisiken sind hierbei gerade für gerontopsychiatrische Abteilungen von zentraler Bedeutung.
Wünschenswert wäre auch eine noch deutlich verbesserte Verfügbarkeit klinisch entscheidungsrelevanter pharmakologischer Daten. Denkbar wären verbindliche und konsistente Pflichtangaben der Hersteller, die in zentralen nationalen oder internationalen Datenbanken zusammengefasst werden und dort von klinischen entscheidungsunterstützenden Informationssystemen abgerufen werden können.
Behandlungsversuche mit potenziell QT-Zeit-verlängernden Antipsychotika bei schweren Unruhezuständen und aggressiven Tendenzen halten wir bei ausgeschöpften nichtpharmakologischen Interventionen und ausbleibendem Effekt pharmakologischer Alternativen gegenwärtig für unverzichtbar [1–3, 7]. Die Risiko-Nutzen-Abwägung und eventuelle begründete Überschreitungen des Indikationsgebiets sollten individuell mit den Angehörigen oder Betreuern erörtert und dies dokumentiert werden [8].
Im vorliegenden Fall hätte man rückblickend in Kenntnis der Interaktionsmechanismen das CYP2D6 hemmende Melperon gegen Pipamperon austauschen können, um sowohl die Risiken einer CYP2D6-Inhibition als auch der QT-Zeit-Verlängerung auszuschalten. Würde man außerdem Risperidon und Haloperidol durch Quetiapin oder die Kombination von Haloperidol mit Quetiapin ersetzen, hätte man zwar weiterhin eine Häufung von Substanzen mit einem Risiko für Torsades des Pointes. Es gäbe aber keine relevanten Interaktionen mehr durch CYP2D6, das in unserer Bevölkerung stark variabel exprimiert ist und durch dessen Inhibition die Serumspiegel dieser Substanzen stark erhöht werden können. Wollte oder könnte man nicht auf die übergangsweise Kombination von Risperidon und Haloperidol verzichten, wäre es denkbar, bei sich manifestierender QT-Zeit-Verlängerung Alfuzosin und Galantamin abzusetzen und den Effekt auf das EKG zu beobachten. Unbedingt werden bei solcher Häufung von Risiken engmaschige Kontrollen der betroffenen Parameter (hier QT-Zeit und Kreislaufwerte) benötigt.
Literatur
1. Ballard C, Corbett A, Chitramohan R, Aarsland D. Management of agitation and aggression associated with Alzheimer’s disease: controversies and possible solutions. Curr Opin Psychiatry 2009;22:532–40.
2. Deutsche Gesellschaft für Psychiatrie, Psychotherapie und Nervenheilkunde (DGPPN), Deutsche Gesellschaft für Neurologie (DGN). S3-Leitlinie „Demenzen“ (Langversion 23.11.2009). www.dgn.org/images/stories/dgn/pdf/s3_leitlinie_demenzen.pdf (Zugriff am 12.02.2012).
3. National Institute for Health and Clinical Excellence. Dementia: Supporting People with Dementia and their Carers in Health and Social Care. NICE, 2006 (www.nice.org.uk/guidance/cg42) (Zugriff am 15.04.2012).
4. Pham VV, Stichtenoth DO. Arzneimitteldosierung bei eingeschränkter Nierenfunktion. Stand: April 2011. www.mh-hannover.de/fileadmin/institute/klinische_pharmakologie/downloads/Q0_2011.pdf (Zugriff am 15.04.2012).
5. Rautaharju PM, Surawicz B, Leonard SG. AHA/ACCF/HRS recommendations for the standardization and interpretation of the electrocardiogram. Part IV: The ST segment, T and U waves, and the QT interval. J Am Coll Cardiol 2009;53:982–91.
6. Rautaharju PM, Zhang ZM, Prineas R, Heiss G. Assessment of prolonged QT and JT intervals in ventricular conduction defects. Am J Cardiol 2004;93:1017–21.
7. Treloar A, Crugel M, Prasanna A, Solomons L, et al. Ethical dilemmas: should antipsychotics ever be prescribed for people with dementia? Br J Psychiatry 2010;197:88–90.
8. Wightman R, Fielding J, Green S. Audit of antipsychotic prescribing in dementia: Cambridgeshire results and lessons learnt. Psychiatr Danub 2011;23(Suppl 1):S126–9.
9. Verbeeck RK. Pharmacokinetics and dosage adjustment in patients with hepatic dysfunction. Eur J Clin Pharmacol 2008;64:1147–61.
10. www.azcert.org/medical-pros/drug-lists/bycategory.cfm (Zugriff am 15.04.2012). Critical Path Institute, Tucson, Arizona and Rockville, Maryland.
11. www.mediq.ch. mediQ – Qualitätszentrum für Medikamentensicherheit und Diagnostik, Klinik Königsfelden, Psychiatrische Dienste Aargau AG, CH-5201 Brugg. (Zugriff am 15.04.2012).
12. Fachinformation Risperdal®, Stand März 2011.
13. Fachinformation Invega®, Stand Oktober 2011.
14. Fachinformation Xeplion®, Stand Oktober 2011.
Ortwin Pfeiffer, Dr. med. Christoph Schmid, Priv.-Doz. Dr. med. Michael Franz, Vitos Klinikum Kurhessen, 34306 Bad Emstal, E-Mail: ortwin.pfeiffer@vitos-kuhessen.de
Dr. med. Detlef Degner, Psychiatrische Klinik der Universität, Von-Siebold-Straße 5, 37075 Göttingen
Dr. Eveline Jaquenoud Sirot, mediQ – Qualitätszentrum für Medikamentensicherheit und Diagnostik, Klinik Königsfelden, Psychiatrische Dienste Aargau AG, 5201 Brugg, Schweiz
Prof. Dr. med. Eckart Rüther, Psychiatrische Klinik der Universität, Von-Siebold-Straße 5, 37075 Göttingen und Klinikum der Ludwig-Maximilians-Universität München, Klinik für Psychiatrie und Psychotherapie, Nussbaumstraße 7, 80336 München
Risks of a multiple drug combination in geriatric psychiatry
An 89 year old demented man under inpatient treatment for symptoms of delirium died unexpectedly under therapy with haloperidol, risperidone, melperone, galantamine, alfuzosine, oxazepam, bisoprolol, captopril, hydrochlorothiazide, isosorbide dinitrate and acetylsalicylic acid.
The potential causes of his death were assessed within the drug safety project AMSP (Arzneimittelsicherheit in der Psychiatrie – Drug Safety in Psychiatry). An ex post drug interaction check with a web-based program revealed complex pharmacokinetic and pharmacodynamic interaction risks. A combined adverse drug reaction causality for the first five of the aforementioned drugs was rated as „possible” in terms of AMSP criteria.
This case study illustrates the difficult risk management of a psychopharmacologic treatment of severe agitation in demented patients.
Key words: Combination therapy, adverse drug reactions (ADR), drug interaction risks, antipsychotic agents, AMSP, behavioural and psychological symptoms in dementia (BPSD)
Psychopharmakotherapie 2012; 19(03)
