Dr. Claudia Bruhn, Schmölln
In Abhängigkeit von Ort und Größe der Läsion im zentralen Nervensystem variiert die klinische Ausprägung der dadurch hervorgerufenen Spastik. So ist nach einem Schlaganfall vor allem die Beugemuskulatur der oberen Extremitäten betroffen: zu den typischen Fehlstellungen zählen die gefaustete Hand, die Daumen-in-Hand-Stellung, eine Ellenbogen- und Handgelenkbeugung und die Unterarmpronation. Die verminderte Bewegungsfähigkeit ist oftmals von Schmerzen begleitet, schränkt alltägliche Verrichtungen ein und erschwert die Pflege der Patienten.
Für die Behandlung spastischer Symptome wird eine interdisziplinäre Zusammenarbeit von Neurologen, Physio- und Ergotherapeuten, Orthopäden, Neurochirurgen und Pflegekräften empfohlen. In der medikamentösen Therapie kommen systemische Antispastika wie Tizanidin, Baclofen, Tetrazepam und Flupirtin zum Einsatz.
Zur Behandlung fokaler Spastiken sind drei Präparate mit Botulinumtoxin Typ A zur Injektion in die betroffenen Muskeln zugelassen. Sie unterscheiden sich in den Indikationen (zu behandelnde Muskelgruppen), Dosierungen und Lagerungsvorschriften (Tab. 1).
Tab. 1. Botulinumtoxin-Typ-A-Präparate zur Behandlung fokaler Spastik nach Schlaganfall im Vergleich [Fachinformationen]
|
Xeomin® |
Botox® |
Dysport® |
|
|
Anwendungsgebiete |
Spastik der oberen Extremitäten nach Schlaganfall mit Handgelenkbeugung und gefausteter Hand bei Erwachsenen |
Fokale Spastizität des Handgelenks und der Hand bei erwachsenen Schlaganfallpatienten |
Armspastik bei Erwachsenen infolge eines Schlaganfalls |
|
Dosierung |
Maximal 400 Einheiten pro Behandlung |
200–240 Einheiten pro Behandlung |
1000 Einheiten intramuskulär in den Arm |
|
Lagerung |
Bei Raumtemperatur |
Bei 2 bis 8°C |
Bei 2 bis 8°C |
Botulinumtoxin blockiert die cholinerge Signalübertragung durch Hemmung der präsynaptischen Acetylcholin-Freisetzung; die Signalübertragung auf die postsynaptische Zelle unterbleibt. Handelt es sich dabei um eine Muskelzelle, führt dies zur Lähmung der entsprechenden Muskelgruppe beziehungsweise einer Reduktion des Muskeltonus.
Die Wirkung von Botulinumtoxin Typ A setzt in der Regel nach etwa vier Tagen ein und erreicht innerhalb von vier Wochen ein Maximum. Der Therapieeffekt hält etwa drei bis vier Monate an.
In der nativen Form ist das eigentliche Neurotoxin umgeben von weiteren Proteinen, den sogenannten Komplexproteinen, die an der pharmakologischen Wirkung nicht beteiligt sind. Tierexperimente lieferten Hinweise, dass diese die Bildung neutralisierender Antikörper gegen das Botulinumtoxin stimulieren könnten. Deshalb werden die Komplexproteine bei der Herstellung des Präparats Xeomin® durch einen spezifischen Reinigungsprozess entfernt.
Zulassungsstudie
Bisher war Xeomin® zugelassen zur symptomatischen Behandlung von Blepharospasmus und zervikaler Dystonie mit überwiegend rotatorischer Komponente (Torticollis spasmodicus). Im Dezember 2009 erfolgte die Indikationserweiterung auf die Spastik der oberen Extremitäten nach Schlaganfall.
Grundlage der Zulassungerweiterung war eine randomisierte, Plazebo-kontrollierte doppelblinde Phase-III-Studie: 148 Patienten mit einer Spastik der Handgelenk- oder Fingerbeugemuskulatur nach Schlaganfall erhielten eine einmalige Behandlung mit dem Botulinumtoxin-Typ-A-Präparat oder Plazebo. Die Injektion erfolgte in verschiedene Muskelgruppen, je nach Ausprägung der Spastik. Anschließend wurden die Patienten über einen Zeitraum von 12 Wochen beobachtet.
Eine zusätzliche Behandlung mit oralen Antispastika sowie Physio- und Ergotherapie war erlaubt, wenn die Patienten stabil darauf eingestellt waren und während der Studie keine Veränderungen erfolgten. Primäres Studienziel war die Wirkung auf die Beugemuskeln des Handgelenks vier Wochen nach der Behandlung, als Instrument hierfür diente die Ashworth-Skala (Skala von 0–4 zur Erfassung des Muskeltonus). Als Responder wurden diejenigen Patienten definiert, die sich auf der Ashworth-Skala um mindestens einen Punkt verbesserten. Daneben wurde die Beeinträchtigung der Patienten bezüglich alltagsrelevanter Bereiche erfasst: funktionelle Beeinträchtigung (Hygiene, Ankleiden, Gliedmaßenstellung, Schmerz) und Schwierigkeiten bei der Pflege.
Ergebnisse der Studie waren eine signifikante und klinisch relevante Reduktion des Muskeltonus der Handbeugemuskulatur (primäres Studienziel, Odds-Ratio [OR] 3,97; 95%-KI 1,9–8,3; p<0,001), aber auch anderer Muskelgruppen (OR=3,12–13,43; p≤0,009) nach 4 Wochen (Abb. 1). Nach 8 Wochen waren in Bezug auf alle Muskelgruppen noch mindestens 50,0% (maximal 67,1%) der Patienten Responder, in der Plazebo-Gruppe waren es 28,9% bis 45,2%. Die Wirkung des Botulinumtoxins setzte im Median 4 Tage nach der Injektion ein, ein Nachlassen der Wirkung wurde im Median nach 10 Wochen berichtet.
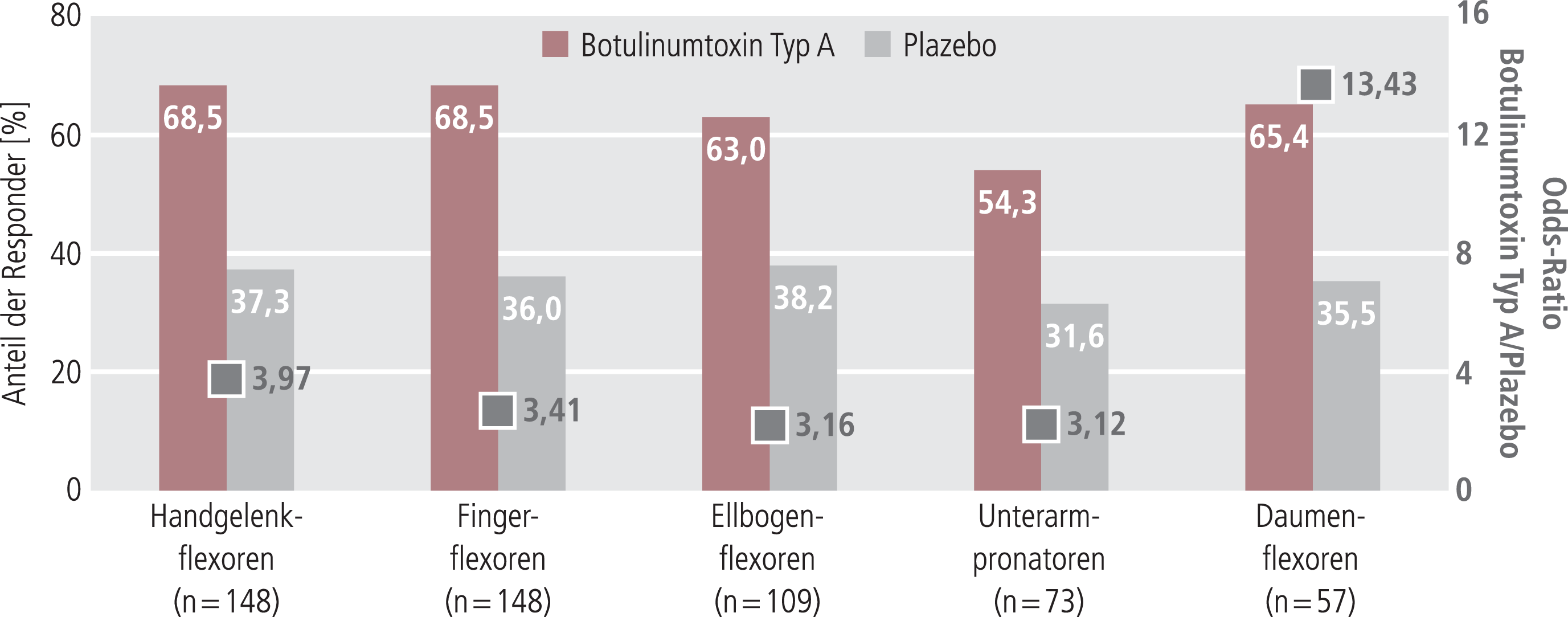
Abb. 1. Reduktion des Tonus verschiedener Muskelgruppen durch komplexproteinfreies Botulinumtoxin Typ A verglichen mit Plazebo 4 Wochen nach der Behandlung: Responder waren Patienten mit einer Verbesserung auf der Ashworth-Skala um mindestens 1 Punkt (p<0,001 bis p=0,057) [modifiziert nach Kanovsky et al., 2009]
Die Verbesserung bezüglich der funktionellen Beeinträchtigungen war in der Behandlungs-Gruppe größer als unter Plazebo, auch noch nach 12 Wochen zeigten sich signifikante Unterschiede. Nach Beurteilung der Pfleger war die Verbesserung in den Kriterien Ankleiden und Reinigung der betroffenen Hand (p=0,021/p=0,028) nach 4 Wochen in der Verum-Gruppe größer als nach Plazebo-Injektion.
Unerwünschte Ereignisse traten in der Behandlungs-Gruppe bei 28,8% der Patienten auf, in der Plazebo-Gruppe bei 26,7%; sie waren meist von leichter Natur und wurden nicht in kausalen Zusammenhang mit der Behandlung gebracht. Im Anschluss an die Studie folgte eine offene Verlängerungsphase. Neutralisierende Antikörper wurden bei keinem der Patienten festgestellt. Auch über einen längeren Beobachtungszeitraum und bei mehrmaliger Applikation (bis zu 5 Behandlungen im Abstand von mindestens 12 Wochen; bis zu insgesamt 89 Wochen) reduzierte das Botulinumtoxin-Präparat die Beschwerden der Patienten und war gut verträglich.
Quellen
Prof. Dr. Jörg Wissel, Beelitz, Prof. Dr. Wolfgang Jost, Wiesbaden, Dr. Jürgen Frevert, Potsdam, Fachpressekonferenz „Neu zugelassen: Mit Xeomin® mehr Optionen in der Spastik-Therapie“, Beelitz, 9. Februar 2010, veranstaltet von der Merz Pharmaceuticals GmbH, Frankfurt/Main.
Kanovsky P, et al. Efficacy and safety of botulinum neurotoxin NT 201 in poststroke upper limb spasticity. Clin Neuropharm 2009;32:259–65.
Kanovsky P, et al. Repeated injections of NT 201 (Xeomin® – Botulinum neurotoxin type A free from complexing proteins) in upper limb post-stroke spasticity patients. Mov Disord 2009;24 (Suppl 1):S452
Fachinformationen Xeomin® (Stand 12/2009), Botox® (Stand 04/2009) und Dysport® (Stand 06/2009)
Psychopharmakotherapie 2010; 17(02)
