Christoph Schrader, Reinhard Dengler und Dirk Dressler, Hannover
Als sich in den 1950er Jahren die Pharmakotherapie der Schizophrenie zu entwickeln begann, wurde Tetrabenazin (TBZ) von der Firma Hoffmann-La Roche als Antipsychotikum in der Schweiz auf den Markt gebracht. Allerdings stellte sich rasch heraus, dass Dopaminrezeptorblocker, die als Neuroleptika bekannt wurden, zur Schizophreniebehandlung effektiver waren [2]. Daraufhin wurde der Einsatz von Tetrabenazin bei anderen Indikationen untersucht. Dabei zeichnete sich eine Wirksamkeit von Tetrabenazin bei hyperkinetischen Bewegungsstörungen ab. Bereits in den 1960er Jahren wurden positive Ergebnisse bei der Behandlung der Chorea der Huntington-Krankheit (HK) beobachtet [3, 41, 47]. Erst vor kurzem jedoch wurde diese antichoreatische Wirksamkeit in größeren kontrollierten Studien bestätigt [1, 8, 29, 42]. Daneben wurde die Wirksamkeit auch bei weiteren hyperkinetischen Bewegungsstörungen untersucht. Bereits 1971 erfolgte die Zulassung von Tetrabenazin zur Behandlung von HK-Chorea in Großbritannien und Australien, später in weiteren europäischen Ländern, in Kanada und den USA. Im März 2007 schließlich wurde Tetrabenazin in Deutschland unter dem Namen Nitoman® zur Behandlung von HK-Chorea und tardiven Dyskinesien zugelassen, Letzteres unter der Auflage, dass andere Therapieverfahren zuvor erfolglos waren. Wegen seiner Wirksamkeit und der fehlenden Auslösung von tardiver Dyskinesie verzeichnet Tetrabenazin seither eine stetig steigende Verwendung.
Pharmakologische Eigenschaften
Substanz
Tetrabenazin (Ro 1-9569) ist ein Benzochinolinderivat mit dem chemischen Namen 3-Isobutyl-9,10-dimethoxy-2,3,4,6,7,11b-hexahydro-1H-benzo[a]chinolizin-2-on (Abb. 1). Im Gegensatz zu Reserpin besitzt Tetrabenazin keine Indolstruktur [37] und reagiert daher nicht alkalisch: Tetrabenazin einen pKa-Wert von 6,0 [44]. In der chromatographischen Analyse zeigt es einen Fluoreszenzgipfel bei 282 nm [40]. In Deutschland wird die Substanz seit 2007 als Nitoman® von der Firma Temmler-Pharma als Filmtabletten mit 25 mg Wirkstoffmenge angeboten.
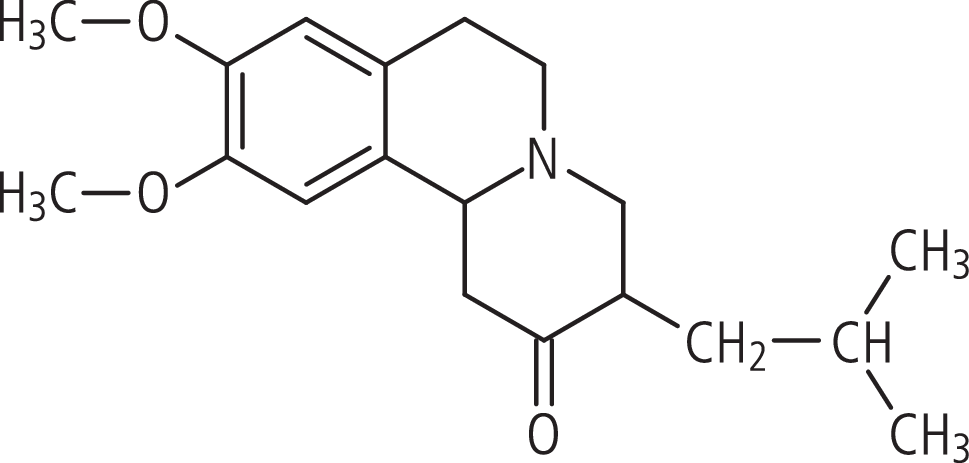
Abb. 1. Tetrabenazin
Wirkungsmechanismus
Die Monoamine Dopamin, Noradrenalin und Serotonin werden im neuronalen Zytoplasma synthetisiert und in Vesikeln gespeichert. Nach der Sekretion der Monoamine in den synaptischen Spalt erfolgt die Signalbeendigung durch eine präsynaptische Wiederaufnahme über die spezifischen Monoamintransporter für Dopamin (DAT), Noradrenalin (NART) und Serotonin (SERT). In der präsynaptischen Nervterminale werden die Monoamine über verschiedene vesikuläre Monoamintransporter (VMAT) in die Speichervesikel zurücktransportiert. VMAT existiert in zwei Formen: VMAT-1 wird zum größten Teil außerhalb des Gehirns exprimiert [11], während VMAT-2 vorwiegend im Gehirn vorkommt [34].
Tetrabenazin weist zwei Wirkungsmechanismen auf (Abb. 2). Zum einen bindet es reversibel an VMAT-2 und inhibiert damit kompetitiv den Rücktransport der Monoamine in die präsynaptischen Speichervesikel [37]. Dies führt zu einem verstärkten Monoamin-Abbau, da die Monoamine außerhalb dieser Vesikel im Zytoplasma einem raschen Abbau durch diverse Monoaminoxidasen unterliegen. Weil über 90% der in den synaptischen Spalt ausgeschütteten Monoamine weiterhin über die präsynaptischen Monoamintransporter DAT, NART und SERT wieder in die Nervterminale aufgenommen werden, führt Tetrabenazin letztlich zu einer präsynaptischen Entspeicherung („Depletion“) der Monoamine.
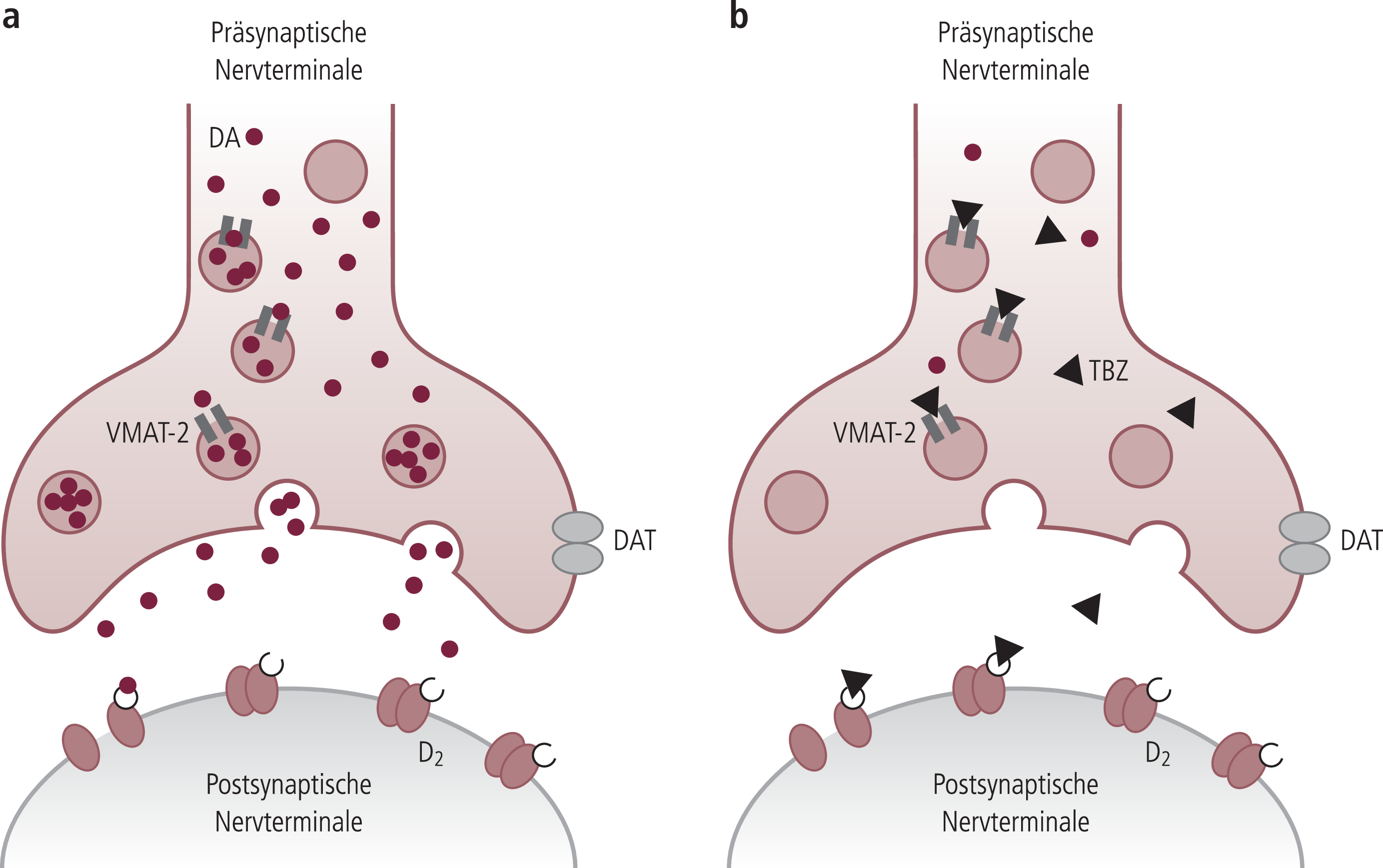
Abb. 2. Wirkungsmechanismus von Tetrabenazin am Beispiel der dopaminergen Synapse
D2: Dopamin-2-Rezeptor, DA: Dopamin, DAT: Dopamintransporter, TBZ: Tetrabenazin, VMAT-2: vesikulärer Monoamintransporter
a) DA wird präsynaptisch in Vesikeln gespeichert, die bei einem Aktionspotenzial mit der Synapsenmembran verschmelzen. Das in den synaptischen Spalt ausgeschüttete DA bindet postsynaptisch an den D2-Rezeptor und wird über den DAT in die präsynaptische Nervterminale wiederaufgenommen. Es gelangt durch VMAT-2 zurück in die Vesikel
b) TBZ bindet reversibel an den VMAT-2 und verhindert die präsynaptische Speicherung monoaminerger Catecholamine, die dann von zytosolischen Monoaminoxidasen abgebaut werden, und führt damit – indirekt – zur Catecholamindepletion. Außerdem blockiert TBZ schwach den postsynaptischen D2-Rezeptor.
Im Gehirn von Ratten verringerte Tetrabenazin den Gehalt von Dopamin um 40%, von Noradrenalin um 41% und von Serotonin um 44% [20]. Daneben wird auch der Gehalt von Acetylcholin, Aspartat und Glutamat gesenkt, allerdings in deutlich geringerem Maße.
In einer Autopsie-Studie an 18 Patienten mit Huntington-Krankheit, die zu Lebzeiten Tetrabenazin erhalten hatten, fand man im Vergleich zu einer Kontroll-Gruppe eine Monoamindepletion im Nucleus caudatus, in den Amygdalae, im Hippocampus und im Temporallappen [9, 33]. Die Depletion von Dopamin im Nucleus caudatus war dabei am stärksten betroffen.
Daneben blockiert Tetrabenazin in vitro auch direkt D2-Rezeptoren, und zwar mit einer Ki von etwa 2,1 x 10–6 M. Diese Affinität ist aber etwa 1000-fach geringer als die zu VMAT-2 [21, 38]. Damit ist diese D2-Rezeptorblockade zu schwach, um sich klinisch zu manifestieren und tardive Dyskinesien auszulösen. Akute dystone Reaktionen treten unter Tetrabenazin extrem selten auf [5].
Die präsynaptische Monoamindepletion und die schwache D2-Rezeptorblockade sind möglicherweise die Ursache für einen gesteigerten Dopaminumsatz, der sich durch eine Erhöhung der Homovanillinsäure im Liquor von HK-Patienten nachweisen lässt [24].
Das dem Tetrabenazin sehr ähnliche Reserpin wirkt zentral ebenfalls am VMAT-2 [7, 43]. Es blockiert jedoch zusätzlich VMAT-1 in der Peripherie und führt zu einer peripheren Monoamindepletion, was vermutlich die bei Reserpin erhöhte Inzidenz von Hypotonie und gastrointestinalen Nebenwirkungen wie epigastrischen Schmerzen und Diarrhö erklärt. Während die Bindung von Tetrabenazin an VMAT-2 reversibel ist, bindet Reserpin irreversibel an VMAT-1 und VMAT-2. Daneben zeigt Tetrabenazin einen rascheren Wirkungseintritt und eine kürzere Halbwertszeit, wodurch es besser gesteuert werden kann als Reserpin.
Pharmakokinetik
Tetrabenazin wird oral eingenommen, hepatisch metabolisiert und renal ausgeschieden. Es weist eine interindividuell stark schwankende, aber kurze Halbwertszeit von etwa 6 Stunden, eine vergleichsweise geringe relative Bioverfügbarkeit von 4,9%±3,2% und eine Plasmaproteinbindung von 83 bis 88% auf [39].
Wegen der relativ kurzen Halbwertszeit wird rasch ein stabiler Wirkspiegel erreicht. Damit kann die klinische Wirksamkeit einer bestimmten Dosierung nach sieben Tagen beurteilt werden. Bei Dosen zwischen 37,5 und 112,5 mg/Tag ist die Kinetik von Tetrabenazin und seinen Hauptmetaboliten linear [25].
Nach oraler Einnahme wird Tetrabenazin zu mindestens 75% resorbiert. Nach Einmalgabe in Dosen zwischen 12,5 und 50 mg liegt seine Plasmakonzentration aufgrund einer raschen und ausgeprägten hepatischen Metabolisierung normalerweise unter der Nachweisgrenze. Tetrabenazin wird in einem hepatischen First-Pass-Effekt durch Reduktion der Ketogruppe zu einer Hydroxylgruppe zu α- und β-Dihydrotetrabenazin verstoffwechselt. Während α-Dihydrotetrabenazin ein aktiver Metabolit ist, verhält sich β-Dihydrotetrabenazin biochemisch inert. Im Vergleich zu Tetrabenazin ist die Proteinbindung von Dihydro-tetrabenazin mit 44 bis 59% deutlich niedriger [39], seine Plasmaspiegel sind höher und seine Halbwertszeit ist mit 10 Stunden länger [40, 39]. Die Plasmaspitzenkonzentrationen (Cmax) von α- und β-Dihydrotetrabenazin werden nach einer Stunde erreicht. Nahrungsaufnahme hat keinen Einfluss auf die mittlere Plasmakonzentration, Cmax oder AUC (Area under curve), weshalb Tetrabenazin ohne Rücksicht auf Mahlzeiten eingenommen werden kann. Tetrabenazin wird zu mindestens 19 Metaboliten abgebaut. Die Hauptmetaboliten α- und β-Dihydrotetrabenazin werden über Cytochrom P450 (CYP) 2D6 O-dealkyliert; eine klinisch signifikante Induktion von CYP1A2, CYP3A4, CYP2C8, CYP2C9 oder CYP2C19 wurde nicht nachgewiesen. Die Ausscheidung der Metaboliten erfolgt renal.
Dosierung und unerwünschte Arzneimittelwirkungen (UAW)
Tetrabenazin wurde in Dosisbereichen zwischen 25 und 200 mg/Tag eingesetzt, wobei die typische therapeutische Dosis zwischen 50 und 75 mg/Tag liegt. In den Studien sowie in der täglichen Praxis wird Tetrabenazin langsam beginnend mit 25 mg verteilt auf zwei bis drei Einzeldosen eintitriert. Die Steigerung erfolgt in der Regel in Schritten von 25 mg/Woche. Die kurze Halbwertszeit erfordert manchmal drei Einzeldosen am Tag. Die Tetrabenazin-Dosis wird gesteigert, bis entweder die klinische Wirkung oder nicht zu tolerierende UAW eintreten. Fast alle UAW können durch Reduktion der Dosis behoben werden. Tatsächlich waren die meisten Studien so angelegt, dass die Dosis bis zum Auftreten von nicht tolerierbaren UAW gesteigert und dann wieder unter die UAW-Schwelle gesenkt wurde. Vor diesem Hintergrund ist es nicht verwunderlich, dass fast alle Studienpatienten über UAW berichteten. Diese UAW-Dosisabhängigkeit ist zum Verständnis des Nebenwirkungsprofils von Tetrabenazin wichtig [13, 27]. Einmalig appliziert scheinen selbst Dosen von 1000 mg außer einer Sedierung keine anderen nennenswerten Effekte auszulösen [18].
Eine Zusammenfassung typischer UAW findet sich in Tabelle 1. Die häufigsten Nebenwirkungen umfassen Sedierung, Parkinsonismus, Depression, Schlaflosigkeit und Akathisie; sie sind alle reversibel [13]. Viele Autoren beschreiben eine generell bessere Verträglichkeit bei jungen Menschen. Bei Patienten mit einem Lebensalter von weniger als 50 Jahren dominieren Schlaflosigkeit und Depression. Ältere Patienten haben ein höheres Risiko, ein medikamenteninduziertes Parkinson-Syndrom zu entwickeln [13, 16].
Tab. 1. Unerwünschte Arzneimittelwirkungen von Tetrabenazin bei 400 Patienten, die wegen tardiver Stereotypie (n=93), Myoklonus (n=12), Huntington-Krankheit (n=29), tardiver Dystonie (n=82), idiopathischer Dystonie (n=108), Tourette-Syndrom (n=47) und anderen Bewegungsstörungen (n=29) behandelt wurden [nach 13]
|
Unerwünschte Wirkung |
Häufigkeit [%] |
|
Müdigkeit, Schläfrigkeit |
37 |
|
Parkinsonismus |
30 |
|
Depression |
15 |
|
Schlaflosigkeit |
11 |
|
Nervosität, Angst |
10 |
|
Akathisie |
10 |
|
Übelkeit, Erbrechen |
5 |
|
Dystone Reaktionen, |
3 |
|
Tremor |
3 |
|
Vergesslichkeit, Verwirrtheit |
2 |
|
Orthostatische Hypotonie |
3 |
|
Benommenheit, Sedierung |
1 |
|
Gleichgewichts-, Gangstörung |
1 |
|
Schwindel |
1 |
|
Durchfall |
<1 |
|
Kopfschmerz |
<1 |
|
Halluzinationen |
<1 |
|
Parästhesien |
<1 |
|
Pharyngeale Spasmen, |
<1 |
|
Verschwommensehen |
<1 |
|
Panikattacken |
<1 |
|
Dysphagie |
<1 |
|
Wahn |
<1 |
Sehr seltene, aber schwerwiegende UAW von Tetrabenazin sind maligne Hyperthermie [46], das maligne Neuroleptika-Syndrom [4, 22, 30, 35], akute dystone Reaktionen [5], Pneumonie [23], schwere Dysphagie [13] und Suizid [10]. Das maligne Neuroleptika-Syndrom tritt in aller Regel innerhalb der ersten vier Wochen der Behandlung auf, kann in seltenen Fällen aber auch nach Jahren in Erscheinung treten [35].
Unter Einnahme von Tetrabenazin bei Huntington-Krankheit sind ungeklärte Todesfälle aufgetreten: die Häufigkeit liegt zwischen 2,5% [32] und 7,5% [19]. Snaith et al. nahmen an, dass die Todesfälle Folgen von Tetrabenazin-induzierter Dysphagie mit nachfolgender Aspirationspneumonie sein könnten [35, 45]. Allerdings gehören Dysphagie, Suizid und früher Tod auch zum Krankheitsbild der Huntington-Krankheit. Die meisten Autoren sahen die Todesfälle nicht in direktem Zusammenhang mit der Einnahme von Tetrabenazin.
Klinische Wirksamkeit
Die überwiegende Zahl der Studien zur Wirksamkeit von Tetrabenazin sind bei Patientengruppen mit gemischten hyperkinetischen Bewegungsstörungen durchgeführt worden. Allerdings sind fast alle retrospektive Analysen. Ferner wurden meist keine einheitlichen Messinstrumente verwendet. Eine Auswahl von Studien mit objektivierbaren Messinstrumenten zu Tetrabenazin findet sich in Tabelle 2. Verwendet wurden die Abnormal Involuntary Movement Scale (AIMS), die besonders gut rasche, phasische Bewegungen wie Chorea, Dyskinesien und Myoklonien erfasst und deren Bereich von 0 (keine abnormen Bewegungen) bis 40 (schwerste abnorme Bewegungen am gesamten Körper) reicht, die Clinical Global Impression of Change (CGIC; –3=schwere Verschlechterung bis +3=starke Verbesserung) und die Global Rating Scale (GRS; 1=deutliche Reduktion unwillkürlicher Bewegungen, exzellente funktionelle Besserung, 2=mäßige Reduktion unwillkürlicher Bewegungen, sehr gute funktionelle Besserung, 3=mäßige Besserung unwillkürlicher Bewegungen, leichte oder keine funktionelle Besserung, 4=keine Änderung, 5=Verschlechterung) [13].
Tab. 2. Klinische Studien über Tetrabenazin (TBZ) bei verschiedenen hyperkinetischen Bewegungsstörungen
|
Autoren |
Design |
n |
Behandlungsdauer [Monate] |
TBZ-Dosis (Bereich) [mg/Tag] |
Responder- Rate [%] |
Ausmaß der Besserung |
|
Huntington-Krankheit |
||||||
|
HD-Study Group (2006) [1] |
Doppelblind, plazebokontrolliert |
54 |
3 |
25–100 |
69 |
–3,5 Punkte (UHDRS) 24% weniger Chorea |
|
Paleacu et al. (2004) [31] |
Retrospektiv, open-label |
28 |
22 |
76 (25–175) |
68 |
≥1 Punkt (CGIC) |
|
Ondo et al. (2002) [29] |
Prospektiv, einfachblind, open-label |
19 |
6 |
62 (25–150) |
79 |
–3,4 Punkte (AIMS) |
|
Jankovic & Orman (1988) [15] |
Retrospektiv, open-label |
10 |
14 |
145 (75–300) |
2,6 (GRS 1–5) |
|
|
Jankovic & Beach (1997) [13] |
Retrospektiv, open-label |
29 |
28 |
109 (37,5–250) |
97 |
1,3 (GRS 1–5) |
|
Tardive Dyskinesie |
||||||
|
Paleacu et al. (2004) [31] |
Retrospektiv, open-label |
17 |
22 |
76 (25–175) |
59 |
≥1 Punkt (CGIC ) |
|
Ondo et al. (1999) [28] |
Einfachblind, randomisiert |
20 |
20 |
58 |
95 |
–9,7 Punkte (AIMS) |
|
Jankovic & Orman (1988) [15] |
Retrospektiv, open-label |
44 |
21 |
97 (25–200) |
91 |
2,3 (GRS 1–5) tardive Dyskinesie |
|
Jankovic & Orman (1988) [15] |
Retrospektiv, open-label |
15 |
16 |
155 (75–250) |
93 |
2,6 (GRS 1–5) tardive Dystonie |
|
Jankovic & Beach (1997) [13] |
Retrospektiv, open-label |
94 |
35 |
97 (25–400) |
91 |
1,3 (GRS 1–5) tardive Dyskinesie |
|
Jankovic & Beach (1997) [13] |
Retrospektiv, open-label |
82 |
32 |
125 (37,5–400) |
94 |
1,5 (GRS 1–5) tardive Dystonie |
|
Tourette-Syndrom |
||||||
|
Paleacu et al. (2004) [31] |
Retrospektiv, open-label |
9 |
22 |
76 (25–175) |
33 |
≥1 Punkt (CGIC) |
|
Kenney et al. (2007) [17] |
Retrospektiv, open-label |
77 |
24 |
50 (6,25–125) |
83 |
1,8 (GRS 1–5) |
|
Jankovic & Orman (1988) [15] |
Retrospektiv, open-label |
17 |
14 |
82 (37,5–150) |
64 |
2,7 (GRS 1–5) |
|
Jankovic & Beach (1997) [13] |
Retrospektiv, open-label |
47 |
20 |
84 (12,5–200) |
76 |
2,1 (GRS 1–5) |
|
Porta et al. (2008) [36] |
Retrospektiv, open-label |
77 |
19 |
76 |
≥1 Punkt (CGIC) |
|
|
Dystonie |
||||||
|
Jankovic & Orman (1988) [15] |
Retrospektiv, open-label |
19 |
14 |
115 (50–200) |
89 |
2,8 (GRS 1–5) trunkal |
|
Jankovic & Orman (1988) [15] |
Retrospektiv, open-label |
57 |
15 |
109 (37,5–250) |
84 |
2,8 (GRS 1–5) fazial |
|
Jankovic & Beach (1997) [13] |
Retrospektiv, open-label |
108 |
29 |
112 (25–400) |
77 |
2,2 (GRS 1–5) |
|
Paleacu et al. (2004) [31] |
Retrospektiv, open-label |
26 |
22 |
76 (25–175) |
46 |
≥1 Punkt (CGIC) trunkal |
|
Paleacu et al. (2004) [31] |
Retrospektiv, open-label |
34 |
22 |
76 (25–175) |
76 |
≥1 Punkt (CGIC) orofazial |
UHDRS: Unified Huntington´s Disease Rating Scale, CGI-C: Clinical Global Impression of Change (–3 bis +3), AIMS: Abnormal Involuntary Movement Scale, GRS: Global Response Scale (1–5) (siehe Text)
Huntington-Krankheit (HK)
Zahlreiche klinische Studien haben die Wirksamkeit von Tetrabenazin auf die hyperkinetischen Bewegungsstörungen der Huntington-Krankheit nachgewiesen. Aus diesem Grunde empfahl bereits 1974 McLellan Tetrabenazin als Mittel der Wahl für die Behandlung der Chorea [24].
Tetrabenazin hat bei Huntington-Krankheit eine gute antichoreatische Wirkung mit Ansprechraten zwischen 68 und 97%. Die verwendeten Dosen reichten von 25 bis 250 mg/Tag. In den in Tabelle 2 aufgeführten Studien wurden keine HK-spezifischen UAW beschrieben; das Spektrum glich dem von Patienten mit anderen Bewegungsstörungen.
Es gibt nur eine einzige doppelblinde, randomisierte Studie („TETRA-HD“), die die antichoreatische Wirkung von Tetrabenazin bei Huntington-Krankheit untersucht [1]. Dabei wurden 84 HK-Patienten für drei Monate mit bis zu 100 mg/Tag Tetrabenazin (n=54) oder mit Plazebo (n=30) behandelt. Bereits ab der ersten Woche übertraf Tetrabenazin die Wirksamkeit von Plazebo in Bezug auf Senkung des motorischen Teils der Unified Huntington’s Disease Rating Scale (UHDRS). Die maximale Besserung unter Tetrabenazin betrug im Vergleich zu Plazebo 3,5 Punkte auf der UHDRS, was einer Reduktion der Chorea um etwa 24% entsprach. Das Ausmaß der Reduktion der Chorea war unabhängig von dem Schweregrad der Chorea, dem Alter, dem Geschlecht beziehungsweise der Genmutation (CAG-Replikationslänge). Dabei führte Tetrabenazin zu keiner Verschlechterung des Hamilton-Depression-Scores (HAM-D). In der Verum-Gruppe kam es nicht zu einer Verschlechterung der Dysphagie und der Sprache im UHDRS. Eine Woche nach Auswaschen des Tetrabenazins war das Ausmaß der Chorea wieder auf dem Ausgangsniveau.
UAW waren Sedierung (27%), Akathisie (8%), sowie Parkinsonismus und Depression (jeweils 4%). Bei vier Patienten wurde die Behandlung wegen schwerwiegender unerwünschter Ereignisse ausgesetzt (ein Suizid, ein Suizidversuch, eine intrakranielle Blutung nach Sturz und eine Erstdiagnose Brustkrebs). In der Plazebo-Gruppe traten keine schwerwiegenden unerwünschten Ereignisse auf. Tetrabenazin ist damit das bislang einzige Medikament, für das eine Wirksamkeit bei HK-Chorea nachgewiesen worden ist [26].
Tardive Dyskinesien (TD)
Tetrabenazin ist bei tardiver Dyskinesie das am besten wirksame orale Medikament. Die ersten Beobachtungen hierzu machte Brandrup bereits 1960 [3]. Seither erschienen viele Fallserien und retrospektive Analysen zur Wirksamkeit von Tetrabenazin bei tardiver Dyskinesie. Einige Studien unterschieden zwischen verschiedenen tardiven Phänomen wie Akathisie, orofazialen Dyskinesien und (trunkal betonter) Dystonie. Verglichen mit der Wirksamkeit bei Huntington-Krankheit scheint bei tardiver Dyskinesie sowohl der Prozentsatz der profitierenden Patienten als auch das Ausmaß der Besserung größer zu sein. Orofaziale Dyskinesien beziehungsweise phasische, schnelle Komponenten wurden in fast allen Studien besser und effektiver sowie in kleineren Dosen durch Tetrabenazin gedämpft als trunkale Dystonie beziehungsweise tonische, langsame Komponenten. Die mittleren therapeutischen Dosen lagen zwischen 50 und 125 mg und damit in ähnlichen Bereichen wie bei Huntington-Krankheit. In den Studien wurden keine TD-spezifischen UAW beobachtet.
Tourette-Syndrom
In den USA sind Haloperidol und Pimozid für die Behandlung von Tics bei Tourette-Patienten zugelassen. Besonders bei Kindern und Jugendlichen werden diese Medikamente jedoch oft nicht gut vertragen. Daneben können sie tardive Dyskinesien verursachen. Tetrabenazin erweitert das therapeutische Spektrum der Therapie von Tics. Allerdings gibt es keine doppelblinden, randomisierten und Plazebo-kontrollierten Studien zur Wirksamkeit und Sicherheit von Tetrabenazin bei Tourette-Syndrom. Alle bislang publizierten Daten sind Fallberichte oder retrospektive Analysen vergleichsweise kleiner Patientengruppen.
Die Daten zur Wirksamkeit von Tetrabenazin bei Tourette-Syndrom sind deutlich heterogener als die zur tardiven Dyskinesie oder Chorea bei Huntington-Krankheit. Zielsymptom waren bei fast allen Studien motorische Tics. Die Verträglichkeit war in den Studien im Schnitt etwas schlechter als bei Huntington-Krankheit und tardiver Dyskinesie. Auch das Ausmaß der Tic-Reduktion war nicht ganz so gut wie der anti-choreatische beziehungsweise anti-dyskinetische Effekt. Kinder und Jugendliche scheinen den Studien zufolge etwas besser als Erwachsene auf Tetrabenazin zu reagieren.
Pädiatrische Patienten
Im Gegensatz zu vielen neuropsychiatrischen Pharmaka gibt es für Tetrabenazin Erfahrung bei Kindern und Jugendlichen mit hyperkinetischen Erkrankungen. Die Erkrankungen, bei denen es zum Einsatz kommt, reichen von der infantilen Zerebralparese über akute Enzephalopathien, Down-Syndrom, Chorea Sydenham, Lesch-Nyhan-Syndrom, Leigh-Syndrom bis hin zum Tourette-Syndrom und der Huntington-Krankheit [6, 12, 14, 17]. Allerdings sind alle Studien klein und nicht randomisiert. In keiner dieser Studien wurden standardisierte Instrumente als Messparameter für die klinische Wirksamkeit verwendet. Sie zeigen aber, dass Tetrabenazin auch von Kindern und Jugendlichen (22 Monate bis 18 Jahre) vertragen wird. Dabei liegen die tolerablen Tetrabenazin-Dosen häufig deutlich höher als bei Erwachsenen. Die eingesetzten Dosen lagen zwischen 0,8 und 25 mg/kg Körpergewicht. Kinder und Jugendliche haben als Hauptnebenwirkungen Sedierung (etwa 30%) und Verhaltensauffälligkeiten (etwa 20%). Letztere äußerten sich in Unruhe, Reizbarkeit und Angst und waren in der größten rein pädiatrischen Studie zu Tetrabenazin der Hauptgrund für das Absetzen der Substanz [12].
Dystonie, Myoklonus und Chorea bei anderen Erkrankungen
Tetrabenazin wurde in einer Vielzahl von kleinen und mittelgroßen Studien bei weiteren hyperkinetischen Bewegungsstörungen, wie Meige-Syndrom, Bruxismus, Torticollis spasmodicus, Blepharospasmus, Akathisie, generalisierter Dystonie, infantiler Zerebralparese und Myoklonus untersucht, aber oftmals ohne einheitliche Messinstrumente.
In Tabelle 2 sind Studien aufgeführt, in denen neben den klassischen Indikationen auch Patienten mit Dystonie behandelt wurden. Die Ansprechraten waren geringer als bei tardiver Dyskinesie. Wiederum wirkte Tetrabenazin bei phasischen fazialen Bewegungen besser als bei tonischen Bewegungen, besonders wenn diese Rumpf oder Extremitäten betrafen. Die größte Therapietreue (als Maß für die Wirksamkeit beziehungsweise das Wirkungs-Nebenwirkungs-Verhältnis) zeigten Patienten mit Huntington-Krankheit und tardiver Dyskinesie (63,3% beziehungsweise 60,4%). Die übrigen Patienten brachen häufiger ab (Therapietreue bei Dystonie 43,9%, bei Tics 48,9% und bei Myoklonus 52,6%) [16].
Schlussbemerkungen
Tetrabenazin ist ein Catecholamin-Depletor und D2-Antagonist, mit dem es weltweit fast 50 Jahre klinische Erfahrung gibt. Es weist einen einzigartigen pharmakologischen Mechanismus auf, der sich bei einer Reihe von Indikationen bewährt hat. Nach den Kriterien der evidenzbasierten Medizin erreicht der Einsatz von Tetrabenazin bei Huntington-Krankheit den Grad B, bei tardiver Dyskinesie und Tics den Grad C. Es ist meist gut verträglich, allerdings sollte auf Depression, Parkinsonismus und Dysphagie geachtet werden.
Obwohl die meisten Studien nicht doppelblind und Plazebo-kontrolliert waren, sprechen das Ausmaß des klinischen Nutzens, der auch langfristig stabil ist, sowie das Wiederauftreten von Symptomen nach Dosisreduktion klar für eine klinische Wirksamkeit. Neben der Reduktion von hyperkinetischen Bewegungsstörungen ist der größte Vorteil von Tetrabenazin das Fehlen tardiver UAW. Seit März 2007 ist Tetrabenazin als Nitoman® nun auch in Deutschland für die Behandlung der Chorea im Rahmen der Huntington-Krankheit und für die Behandlung tardiver Dyskinesien zugelassen.
Literatur
1. Huntington Study Group. Tetrabenazine as antichorea therapy in Huntington disease: a randomized controlled trial. Neurology 2006;66:366–72.
2. Ashcroft GW, MacDougall EJ, Barker PA. A comparison of tetrabenazine and chlorpromazine in chronic schizophrenia. J Ment Sci 1961;107:287–93.
3. Brandrup E. Reserpin og tetrabenacin ved chorea Huntington. Nord Med 1960;4:968–9.
4. Burke RE, Fahn S, et al. Neuroleptic malignant syndrome caused by dopamine-depleting drugs in a patient with Huntington disease. Neurology 1981;31:1022–5.
5. Burke RE, Reches A, Traub MM, Ilson J, et al. Tetrabenazine induces acute dystonic reactions. Ann Neurol 1985;17:200–2.
6. Chatterjee A, Frucht SJ. Tetrabenazine in the treatment of severe pediatric chorea. Mov Disord 2003;18:703–6.
7. Erickson JD, Schafer MK, Bonner TI, Eiden LE, et al. Distinct pharmacological properties and distribution in neurons and endocrine cells of two isoforms of the human vesicular monoamine transporter. Proc Natl Acad Sci U S A 1996;93:5166–71.
8. Frank S, Ondo W, Fahn S, Hunter C, et al. A study of chorea after tetrabenazine withdrawal in patients with Huntington disease. Clin Neuropharmacol 2008;31:127–33.
9. Garcia Ruiz PJ, Mena MA, Sanchez BV, Diaz NW, et al. Cerebrospinal fluid homovanillic acid is reduced in untreated Huntington’s disease. Clin Neuropharmacol 1995;18:58–63.
10. Gimenez-Roldan S, Mateo D. Huntington disease: tetrabenazine compared to haloperidol in the reduction of involuntary movements. Neurologia 1989;4:282–7.
11. Gonzalez AM, Walther D, Pazos A, Uhl GR. Synaptic vesicular monoamine transporter expression: distribution and pharmacologic profile. Brain Res Mol Brain Res 1994;22:219–26.
12. Jain S, Greene PE, Frucht SJ. Tetrabenazine therapy of pediatric hyperkinetic movement disorders. Mov Disord 2006;21:1966–72.
13. Jankovic J, Beach J. Long-term effects of tetrabenazine in hyperkinetic movement disorders. Neurology 1997;48:358–62.
14. Jankovic J, Caskey TC, Stout JT, Butler IJ. Lesch-Nyhan syndrome: a study of motor behaviour and cerebrospinal fluid neurotransmitters. Ann Neurol 1988;23:466–9.
15. Jankovic J, Orman J. Tetrabenazine therapy of dystonia, chorea, tics, and other dyskinesias. Neurology 1988;38:391–4.
16. Kenney C, Hunter C, Jankovic J. Long-term tolerability of tetrabenazine in the treatment of hyperkinetic movement disorders. Mov Disord 2007;22:193–7.
17. Kenney C, Hunter C, Mejia N, Jankovic J. Tetrabenazine in the treatment of Tourette syndrome. J Ped Neurol 2007;5:9–13.
18. Kidd DW, McLellan DL. Self-poisoning with tetrabenazine. Br J Clin Pract 1972;26:179–80.
19. Kingston D. Tetrabenazine for involuntary movement disorders. Med J Aust 1979;1:628–30.
20. Lane JD, Smith JE, Shea PA, McBride WJ. Neurochemical changes following the administration of depleters of biogenic monoamines. Life Sci 1976;19:1663–7.
21. Login IS, Cronin MJ, MacLeod RM. Tetrabenazine has properties of a dopamine receptor antagonist. Ann Neurol 1982;12:257–62.
22. Mateo D, Munoz-Blanco JL, Gimenez-Roldan S. Neuroleptic malignant syndrome related to tetrabenazine introduction and haloperidol discontinuation in Huntington’s disease. Clin Neuropharmacol 1992;15:63–8.
23. McLellan DL. The suppression of involuntary movements with tetrabenazine. Scott Med J 1972;17:367–70.
24. McLellan DL, et al. A double-blind trial of tetrabenazine, thiopropazate, and placebo in patients with chorea. Lancet 1974;1:104–7.
25. Mehvar R, Jamali F, Watson MW, Skelton D. Pharmacokinetics of tetrabenazine and its major metabolite in man and rat. Bioavailability and dose dependency studies. Drug Metab Dispos 1987;15:250–5.
26. Mestre T, Ferreira J, Coelho MM, Rosa M, et al. Therapeutic interventions for symptomatic treatment in Huntington’s disease. Cochrane Database Syst Rev 2009;CD006456.
27. Mikkelsen BO. Tolerance of tetrabenazine during long-term treatment. Acta Neurol Scand 1983;68:57–60.
28. Ondo WG, Hanna PA, Jankovic J. Tetrabenazine treatment for tardive dyskinesia: assessment by randomized videotape protocol. Am J Psychiatry 1999;156:1279–81.
29. Ondo WG, Tintner R, Thomas M, Jankovic J. Tetrabenazine treatment for Huntington’s disease-associated chorea. Clin Neuropharmacol 2002;25:300–2.
30. Ossemann M, Sindic CJ, Laterre C. Tetrabenazine as a cause of neuroleptic malignant syndrome. Mov Disord 1996;11:95.
31. Paleacu D. Tetrabenazine in the treatment of Huntington’s disease. Neuropsychiatr Dis Treat 2007;3:545–51.
32. Paleacu D, Giladi N, Moore O, Stern A, et al. Tetrabenazine treatment in movement disorders. Clin Neuropharmacol 2004;27:230–3.
33. Pearson SJ, Reynolds GP. Depletion of monoamine transmitters by tetrabenazine in brain tissue in Huntington’s disease. Neuropharmacology 1988;27:717–9.
34. Pettibone DJ, et al. Tetrabenazine-induced depletion of brain monoamines: characterization and interaction with selected antidepressants. Eur J Pharmacol 1984;102:425–30.
35. Petzinger GM, Bressman SB. A case of tetrabenazine-induced neuroleptic malignant syndrome after prolonged treatment. Mov Disord 1997;12:246–8.
36. Porta M, Sassi M, Cavallazzi M, Fornari M, et al. Tourette’s syndrome and role of tetrabenazine: review and personal experience. Clin Drug Investig 2008;28:443–59.
37. Quinn GP, Shore PA, Brodie BB. Biochemical and pharmacological studies of RO 1-9569 (tetrabenazine), a nonindole tranquilizing agent with reserpine-like effects. J Pharmacol Exp Ther 1959;127:103–9.
38. Reches A, Burke RE, Kuhn CM, Hassan MN, et al. Tetrabenazine, an amine-depleting drug, also blocks dopamine receptors in rat brain. J Pharmacol Exp Ther 1983;225:515–21.
39. Roberts MS, McLean S, Millingen KS, Galloway HM. The pharmacokinetics of tetrabenazine and its hydroxy metabolite in patients treated for involuntary movement disorders. Eur J Clin Pharmacol 1986;29:703–8.
40. Roberts MS, Watson HM, McLean S, Millingen KS. Determination of therapeutic plasma concentrations of tetrabenazine and an active metabolite by high-performance liquid chromatography. J Chromatogr 1981;226:175–82.
41. Sattes H. The treatment of chorea minor with the monoamine liberator “Nitoman”. Psychiatr Neurol (Basel) 1960;140:13–9.
42. Savani AA, Login IS. Tetrabenazine as antichorea therapy in Huntington disease: a randomized controlled trial. Neurology 2007;68:797.
43. Scherman D. Dihydrotetrabenazine binding and monoamine uptake in mouse brain regions. J Neurochem 1986;47:331–9.
44. Scherman D, Henry JP. Acido-basic properties of the catecholamine uptake inhibitors tetrabenazine and dihydrotetrabenazine. Biochimie 1982;64:915–21.
45. Snaith RP, Warren HD. Letter: Treatment of Huntington’s chorea with tetrabenazine. Lancet 1974;1:413–4.
46. Stevens E, et al. Severe hyperthermia during tetrabenazine therapy for tardive dyskinesia. Intensive Care Med 1998;24:369–71.
47. Stumpf W. Untersuchungen über „Nitoman“. Psychiatr Neurol (Basel) 1960;140:63–8.
Dr. med. Christoph Schrader, Prof. Dr. med. Reinhard Dengler, Prof. Dr. med. Dirk Dressler, Klinik für Neurologie und Klinische Neurophysiologie, Medizinische Hochschule, Carl-Neuberg-Str. 1, 30625 Hannover, E-Mail: dressler.dirk@mh-hannover.de
Tetrabenazine in the treatment of hyperkinetic movement disorders
Tetrabenazine (TBZ) is a centrally acting depletor of the monoamines dopamine, norepinephrine, and serotonin. It reversibly blocks the vesicular monoamine transporter VMAT-2 and has only mild D2-receptor blocking properties. It is used successfully in hyperkinetic movement disorders including chorea as in Huntington’s disease (HD) and other aetiologies, tardive dyskinesias (TD), tics, dystonias, myoclonus and cerebral palsy. Chorea and TD are studied best and yield best therapeutic results. In 2007 tetrabenazine was approved in Germany as Nitoman® for the treatment of HD-chorea and TD.
Tetrabenazine is generally well tolerated. However, depression, parkinsonism, and dysphagia can occur. Tetrabenazine is the only drug that offers robust therapeutic efficacy based upon indirect D2-antagonism, lack of TD risk and lack of peripheral adverse effects.
Key words: Tetrabenazine, hyperkinetic movement disorders, chorea, Huntington’s disease, tardive dyskinesias, tic, myoclonus, dystonia, pharmacology
Psychopharmakotherapie 2010; 17(02)
