Michael A. Rapp, Berlin
Bei etwa 25 bis 30% der über 60-Jährigen liegen psychische Störungen im weitesten Sinne vor [22]. Die Prävalenz der majoren Depression wird bei etwa 5% vermutet; weit häufiger kommen subdiagnostische depressive Symptome vor [22]. Letztere zeigen jedoch signifikante Einflüsse auf die Alltagsfähigkeiten, können das Risiko für Gedächtnisstörungen erhöhen und sind mit einer erhöhten Morbidität und Mortalität assoziiert [33, 34].
Angst berichtet eine Punktprävalenz für depressive Episoden jenseits des 65. Lebensjahrs von etwa 2%, für leichtere und sekundäre depressive Störungen von 5% bis 15% [4]. Neben mittelschweren und schweren Depressionen spielen also im hohen Alter insbesondere leichtere und altersspezifische Unterformen der Depression eine wichtige Rolle. So nimmt mit dem Alter die Variabilität des Erscheinungsbilds, nicht aber die Prävalenz beziehungsweise die Häufigkeit von Depressionen zu [24, 34]. Die Abgrenzung depressiver Störungen mit Beginn im jungen Erwachsenenalter und Erstmanifestationen im höheren Lebensalter [34] kann insbesondere im Hinblick auf eine vermehrte kardiovaskuläre Komorbidität bei Erstmanifestationen im höheren Lebensalter von Bedeutung sein; therapeutische Konsequenzen ergeben sich hier aber nur im Hinblick auf das Nebenwirkungsprofil der antidepressiven Medikation sowie eine zu bedenkende ungünstigere Prognose bei Vorliegen zerebrovaskulärer Läsionen [43]. Differenzialdiagnostisch sind hier auch depressive Störungen in der Prodromalphase einer neurodegenerativen Erkrankung abzugrenzen [35], wobei hier neben neuropsychologischen und bildgebenden Verfahren liquorchemische Untersuchungen hilfreich sein können [45]. Bei Depressionen im Alter ist neben kognitiven Störungen und funktionellen Einbußen vor allem auf die erhöhte Suizidgefahr, insbesondere für Männer, zu achten [13].
Mit den heute zur Verfügung stehenden kombinierten Therapieverfahren aus Pharmako-, Psycho- und Sozio-(Sozial-) therapie kann für die Mehrzahl der depressiven alten Patienten grundsätzlich ein günstiger Therapieverlauf erwartet werden. Im Vergleich zu jüngeren Erwachsenen liegen jedoch für die antidepressive Pharmakotherapie im Alter wenige Studien vor. Anhand systematischer evidenzbasierter Übersichtsarbeiten, Konsensusleitlinien und neuerer Studien zur Wirksamkeit und Sicherheit antidepressiver Pharmakotherapie im Alter wird hier die Evidenzbasis für die Pharmakotherapie depressiver Erkrankungen im Alter dargestellt. Weiterhin wird analog zu bekannten Therapiealgorithmen für jüngere Erwachsene ein Therapiealgorithmus für die spezifische Pharmakotherapie der Depressionen im höheren Lebensalter entwickelt und vorgestellt. Die Ergebnisse werden kritisch diskutiert.
Konsensusleitlinien
Für die Therapie der Altersdepression liegen spezifische Leitlinien bisher nur aus dem angloamerikanischen Raum vor [2, 49].
In der britischen Leitlinie des National Institute for Clinical Excellence (NICE) [49] wurden zunächst sämtliche Studien zur antidepressiven Pharmakotherapie, in denen mehr als 80% der Studienteilnehmer älter als 65 Jahre waren, aufgenommen. Insgesamt schlossen 15 Studien Teilnehmer ein, die mindestens 60 Jahre alt waren [3, 11, 12, 14–18, 20–23, 27, 28, 31–33, 41], davon waren zehn randomisierte, Plazebo-kontrollierte Studien zu Serotonin-Wiederaufnahmehemmern (SSRI), zwei zu Venlafaxin, je eine zu Mirtazapin, Phenelzin und Johanniskraut. Wirksamkeitsdaten waren von 1083 Patienten und Verträglichkeitsdaten von 1620 Patienten vorhanden. Die Studiendauer reichte von fünf bis acht Wochen. Alle eingeschlossenen Studien wurden zwischen 1984 und 2003 veröffentlicht. Es zeigte sich für alle Monotherapiestudien zusammen eine Wirksamkeit, die mit den Daten bei jüngeren Erwachsenen durchaus vergleichbar war, aber mit einer höheren Nebenwirkungsrate einherging [49].
In Vergleichsstudien ergaben sich keine Unterschiede in der Wirksamkeit zwischen Amitriptylin und Paroxetin, zwischen SSRI und allen anderen Antidepressiva, zwischen Venlafaxin und trizyklischen Antidepressiva (TZA), zwischen allen anderen Antidepressiva und TZA sowie zwischen Mirtazapin und Paroxetin. Es ergaben sich jedoch hier Hinweise, dass Mirtazapin gegenüber Paroxetin und TZA bei älteren Patienten, die früh im Verlauf über starke Nebenwirkungen klagen, auch in der Wirksamkeit überlegen ist [49]. Insgesamt ergab sich aber kein signifikanter Unterschied bezüglich der Wirksamkeit und der Häufigkeit der aufgetretenen Nebenwirkungen zwischen den untersuchten Antidepressiva. Durch Augmentierung eines Antidepressivums mit Lithium wiesen ältere Patienten, die bereits mehrere erfolglose Therapieversuche hinter sich gebracht hatten, eine höhere Remissionsrate auf [26].
Die NICE-Empfehlungen (Tab. 1) [49] umfassen deshalb zunächst die antidepressive Monotherapie in einer altersangepassten Dosierung für mindestens sechs Wochen sowie bei einer teilweisen Remission in den ersten sechs Wochen eine Weiterbehandlung für weitere sechs Wochen. Insbesondere bei TZA wird die genaue Beobachtung von Nebenwirkungen empfohlen; für alle Antidepressiva wird die genaue Beachtung von Wechselwirkungen mit anderen Pharmaka gefordert. Bei zwei erfolglosen Therapieversuchen mit einer antidepressiven Monotherapie wird eine Augmentierung mit Lithium empfohlen. Depressionen bei Demenz sollten pharmakotherapeutisch genauso behandelt werden wie Depressionen bei anderen älteren Erwachsenen. Weitere Studien werden für alle Aspekte der antidepressiven Pharmakotherapie empfohlen, insbesondere in der Gruppe der über 80-Jährigen.
Tab. 1. Konsensusempfehlungen des National Institute for Clinical Excellence (NICE) [49]
|
Leichte depressive Episode |
Mittelschwere und schwere depressive Episode |
||
|
Pharmakotherapie nicht zwingend indiziert |
SSRI |
SSRI |
Amitriptylin Andere TZA |
|
Mirtazapin |
Venlafaxin |
Mirtazapin |
|
|
Bei Therapieversagen (sechs Wochen): |
|||
|
Nach zwei erfolglosen Monotherapieversuchen: Lithium-Augmentierung |
|||
SSRI: selektive Serotonin-Wiederaufnahmehemmer; TZA: trizyklische Antidepressiva
Fett und kursiv dargestellt sind Medikamente der ersten Wahl. Die NICE-Leitlinien empfehlen zunächst eine Monotherapie für mindestens sechs Wochen sowie deren Fortführung bei Teilremission für weitere sechs Wochen. Bei Therapieversagen wird der Wechsel auf eine andere Substanzklasse und erneut eine Monotherapie für sechs Wochen (bei Teilremission für weitere sechs Wochen) vorgeschlagen, und erst dann die Augmentierung mit Lithium [49].
Die älteren amerikanischen Konsensusleitlinien [2], die nicht auf einer systematischen Übersichtsarbeit beruhen, kommen insgesamt zu einem vergleichbaren Ergebnis, differenzieren jedoch nach Depressionschweregrad; auch werden TZA nicht als Initialtherapie bei leichter bis mittelschwerer depressiver Episode empfohlen und sind aufgrund des vermuteten ungünstigeren Nebenwirkungsprofils auch bei schwerer depressiver Episode nicht Medikamente der ersten Wahl. Eine Augmentierung mit Lithium wird hier allerdings nicht spezifisch empfohlen. Die Konsensusempfehlungen der American Association for Geriatric Psychiatry bezüglich antidepressiver Pharmakotherapie im Alter sind in Tabelle 2 dargestellt [2].
Tab. 2. Konsensusempfehlungen der American Association for Geriatric Psychiatry [2]
|
Leichte depressive Episode |
Mittelschwere und schwere depressive Episode |
||
|
SSRI |
Bupropion |
SSRI |
TZA |
|
Venlafaxin |
Mirtazapin |
Venlafaxin |
Mirtazapin Bupropion |
Fett und kursiv dargestellt sind Medikamente der ersten Wahl [2].
Cochrane-Übersichten
Die Cochrane Database of Systematic Reviews [46] auf Grundlage der evidenzbasierten Medizin [8] stellt seit nunmehr 1995 systematische Übersichtsarbeiten und Metaanalysen zur Verfügung [41]. Für den Bereich der antidepressiven Pharmakotherapie im Alter liegen derzeit drei Übersichtsarbeiten in der Cochrane-Datenbank vor [5, 30, 44].
Wilson und Kollegen [44] untersuchten die Wirksamkeit und Sicherheit der Behandlung mit antidepressiven Medikamenten im höheren Lebensalter. Geeignete Studien wurden über die Cochrane Collaboration Depression, Anxiety and Neurosis Review Group (CCDAN) gesucht. Es fanden sich insgesamt 7000 Studien zur Depressionsbehandlung im Verzeichnis, von denen 366 aufgrund ihres Designs, der Zielerkrankung und der untersuchten Altersgruppe in die engere Auswahl kamen. Letztlich erfüllten aber nur 17 Studien die Qualitätskriterien, die in erster Linie auf Randomisierung, Plazebo-Kontrolle, objektivierte und standardisierte Zielkriterien sowie die systematische Erfassung der Sicherheit abzielten. Aus allen randomisierten, Plazebo-kontrollierten Studien zu Antidepressiva in der Behandlung älterer Patienten wurden sowohl dichotome Daten zur Remission als auch kontinuierliche Daten anhand gebräuchlicher Skalen wie der Hamilton-Depressionsskala (HAMD) und der Montgomery-Åsberg-Skala (MADRS) eingeschlossen. 17 Studien lieferten Daten zur Wirksamkeitsanalyse von 245 Patienten, die mit trizyklischen Antidepressiva (223 mit Plazebo) behandelt wurden, 365 Patienten, die mit SSRI (372 mit Plazebo) behandelt wurden, und 58 Patienten, die mit Monoaminoxidase-(MAO-)Hemmern (63 mit Plazebo) behandelt wurden. Für eine Remission ergaben sich aus den Studien folgende Odds-Ratios (OR):
- TZA: OR=3,13 (95%-Konfidenzintervall [95%-KI] 1,32–4,76)
- SSRI: OR=1,97 (95%-KI 1,39–2,78)
- MAO-Hemmer: OR=5,88 (95%-KI 2,56–14,29)
Es ergab sich somit kein statistisch bedeutsamer Unterschied in der Wirksamkeit zwischen SSRI und TZA, während MAO-Hemmer den SSRI, nicht aber den TZA überlegen waren [44].
In einer zweiten Studie, ebenfalls aus der Arbeitsgruppe um Wilson und Nightingale [30], ging es um die Frage, ob SSRI gegenüber TZA ein günstigeres Nebenwirkungsprofil, insbesondere hinsichtlich der Häufigkeit des Behandlungsabbruchs im Rahmen randomisierter, Plazebo-kontrollierter Studien aufweisen. Eingeschlossen wurden hier alle randomisierten, kontrollierten Studien, die zwei oder mehrere Antidepressiva bei Patienten über 55 Jahren hinsichtlich einer Depressionsbehandlung miteinander verglichen. Anhand der Datenbank Cochrane Collaboration Depression, Anxiety and Neurosis Controlled Trials Register (CCDANCTR) wurden 163 Studien gefunden, von denen 32 den Qualitäts- und Zielkriterien entsprachen. TZA zeigten gegenüber SSRI eine höhere Nebenwirkungsrate (OR=1,23; 95%-KI 1,05–1,43) und eine höhere Abbruchrate wegen Nebenwirkungen (OR=1,36; 95%-KI 1,09–1,70). Die qualitative Analyse von Nebenwirkungen zeigte ein gering erhöhtes Risiko für gastrointestinale und neuropsychiatrische Nebenwirkungen bei TZA [30].
Eine neuere Studie zur Wirksamkeit von Antidepressiva im niedergelassenen Bereich bestätigt die Ergebnisse der beiden beschriebenen systematischen Übersichtsarbeiten [5]. Hier wurden Studien ausgewählt, wenn sie in randomisierten kontrollierten Designs die Wirksamkeit von TZA oder SSRI gegenüber Plazebo bei älteren Patienten (über 65 Jahren) mithilfe validierter Depressionsskalen erfassten. Primäres Zielkriterium war die Remission, und auch hier wurden Odds-Ratios mit Konfidenzintervallen berichtet. Von 16 ausgewählten Studien untersuchten zehn TZA, zwei SSRI und zwei schlossen beide Medikamentengruppen ein. In den Interventionsgruppen gab es insgesamt 1364 Teilnehmer, in den Plazebo-Gruppen 919 Teilnehmer. Fast alle Studien waren von kurzer Dauer, gewöhnlich sechs bis acht Wochen. Die zusammengefassten Daten ergaben ein Odds-Ratio von OR=1,24 (95%-KI 1,11–1,38) zugunsten von TZA gegen Plazebo. Für SSRI war dieses OR=1,28 (95%-KI 1,15–1,43). Die Fallzahlen, die benötigt wurden, um zu schädigen (number needed to harm [NNH] für die Abbruchrate wegen Nebenwirkungen), reichten von 4 bis 30 für TZA und von 20 bis 90 für SSRI [5].
Zusammenfassend lässt sich sagen, dass sowohl TZA als auch SSRI in der Behandlung von Depressionen bei älteren Menschen wirksam sind. Die Behandlungsdauer sollte mindestens sechs Wochen betragen, um eine effektive Behandlung sicherzustellen. TZA und SSRI sind von gleicher Wirksamkeit, SSRI haben aber geringere Abbruchraten aufgrund von Nebenwirkungen als die TZA. Die hier vorgestellten Studien umfassen für die SSRI und TZA jedoch nur Monotherapie- und Vergleichsstudien, die bis September 2007 publiziert wurden, und für alle Substanzen nur Monotherapiestudien, die bis Herbst 2002 publiziert wurden. Sie geben auch keine Hinweise auf Behandlungsstrategien zur Erhaltungstherapie und bei therapierefraktärer Depression. Im Folgenden sollen daher weitere Studien berichtet werden, die für die Depressionsbehandlung im Alter zusätzliche Informationen liefern können.
Monotherapiestudien
Schatzberg und Kollegen [40] verglichen in einer randomisierten, Plazebo-kontrollierten, doppelblinden Studie die Wirksamkeit von Mirtazapin mit der von Paroxetin bei 256 älteren Patienten (mittleres Alter 71,8±5,3 Jahre; Mirtazapin: n=126; Paroxetin: n=120) und konnten für Mirtazapin gegenüber Paroxetin eine signifikante Verbesserung auf der Hamilton-Depressionsskala sowie in der Remissionsrate und der Dauer bis zur Remission (Mirtazapin: Median 26 Tage; Paroxetin: Median 40 Tage) zeigen.
Allard und Kollegen [3] verglichen in einer randomisierten doppelblinden Studie die Wirksamkeit von Citalopram und Venlafaxin bei 148 älteren Depressionspatienten (mittleres Alter 72,9±5,9 Jahre) und konnten hinsichtlich Wirksamkeit und Nebenwirkungen vergleichbare Effekte zeigen. Die Remissionsrate betrug hier 19% für Venlafaxin and 23% für Citalopram.
Katona und Kollegen [25] untersuchten die Wirksamkeit von Reboxetin im Vergleich zu Trimipramin im Rahmen einer Plazebo-kontrollierten randomisierten Studie bei 347 älteren Patienten (mittleres Alter 74,2±7,0 Jahre) und konnten hinsichtlich Wirksamkeit und Nebenwirkungen vergleichbare Effekte zeigen. Allerdings zeigen neuere Metaanalysen auch unveröffentlichter Daten zumindest bei jungen Erwachsenen angesichts einer erhöhten Nebenwirkungsrate keine ausreichende Evidenz für den Nutzen von Reboxetin [47].
Zielsetzung der Studie von Raskin et al. [37] war die Untersuchung der Wirksamkeit von Duloxetin (60 mg/Tag) in Bezug auf Depressivität und Schmerzerleben bei älteren Patienten (mittleres Alter 72 Jahre, Streubreite 65–90 Jahre) mit rückläufigen schweren depressiven Episoden. In einer doppelblinden randomisierten Studie zeigten die 207 Patienten in der Verum-Gruppe gegenüber Plazebo (n=104) über einen Zeitraum von acht Wochen signifikante Verbesserungen in der Hamilton-Depressionsskala (standardisierte Mittelwertsdifferenz [SMD] –6,49 gegenüber –3,72). Remissionen waren in der Duloxetin-Gruppe signifikant häufiger (27,4% gegenüber 14,7%), und auch hinsichtlich subjektiv erlebter Schmerzen ergab sich ein signifikanter Behandlungseffekt [37].
Monotherapiestudien zur Erhaltungstherapie
Reynolds und Kollegen [38] prüften die Wirksamkeit von Paroxetin (20–40 mg/Tag), kombiniert mit interpersoneller Psychotherapie (IPT), gegenüber Plazebo und Psychotherapie bei Patienten über 70 Lebensjahren (mittleres Alter 77,1±5,6 Jahre) hinsichtlich der Rezidivrate nach initialer Remission einer schweren depressiven Episode über zwei Jahre. In der Paroxetin-Gruppe erlitten 37% der Patienten im Beboachtungszeitraum ein Rezidiv, in der Kontrollgruppe hingegen 68%. Das relative Risiko für ein Rezidiv war somit in der Plazebo-Gruppe 2,4-fach (95%-KI 1,4–4,2) erhöht [38].
Gorwood et al. [18] untersuchten die Wirksamkeit und die Verträglichkeit von Escitalopram zur Rezidivprophylaxe bei 305 älteren Patienten, die nach einer ersten Behandlung mit Escitalopram remittiert waren, über 24 Wochen. Dabei wurden 152 Patienten mit Escitalopram und 153 Patienten mit Plazebo behandelt. Das Rezidivrisiko war 4,4-fach höher für Plazebo- als für Escitalopram-behandelte Patienten (95%-KI 1,34–12,32) [18].
Kombinationsstudien
Dew und Kollegen untersuchten im Rahmen der STAR*D-Studie [11] die Augmentierung mit Bupropion, Lithium oder Nortriptylin bei 105 Patienten und konnten bei etwa 50% der Patienten, die vorher nicht von einer Kombinationsbehandlung aus Paroxetin und IPT profitiert hatten, eine klinische Remission erreichen. Dabei zeigten sich ähnliche Effekte für alle drei Augmentierungsstrategien, allerdings bei kleinen Fallzahlen. Die Dauer bis zur Remission betrug dabei bis zu 12 Wochen; es war jedoch ebenfalls eine erhöhte Nebenwirkungsrate feststellbar [11].
Carpenter und Kollegen [7] untersuchten in einer doppelblinden Studie die Augmentierung einer antidepressiven Monotherapie mit Mirtazapin bei 26 ambulanten jüngeren Patienten (mittleres Alter 46,3±9,7 Jahre) mit therapierefraktärer Depression in einer Dosis von 15–30 mg/Tag. 64% in der Verum-Gruppe, aber nur 20% in der Plazebo-Gruppe waren nach vier Wochen Augmentierungsbehandlung remittiert. Es gab keine signifikanten Gruppenunterschiede hinsichtlich Nebenwirkungen. Obgleich für die Wirksamkeit der Augmentierung mit Mirtazapin im höheren Lebensalter bisher keinen kontrollierten Studien vorliegen, scheint sie doch im klinischen Alltag bereits gängige Routine zu sein. Vergleichsdaten fehlen hier aber insbesondere auch zu Nebenwirkungen wie etwa der Hyponatriämie.
Für das atypische Neuroleptikum Aripiprazol liegen jetzt ebenfalls erste Daten aus einer offenen Studie zur Augmentierung einer SSRI-Therapie vor, die jedoch zunächst repliziert werden sollten [39].
Wechsel zu einem MAO-Hemmer
In einer Open-Label-Studie lag die Remissionsrate bei einem Wechsel zu Phenelzin nach erfolgloser Augmentierung bei 50% [15]. In einer randomisierten, doppelblinden, Plazebo-kontrollierten Studie des Wechsels zu Selegilin nach zwei erfolglosen Monotherapieversuchen wurden Remissionsraten von bis zu 50% berichtet [42]. Jedoch ist die Generalisierbarkeit dieser Studie durch ihre kleine Fallzahl (n=16) und die kurze Dauer der Behandlung (drei Wochen) begrenzt [42]. Kok und Kollegen verglichen die Wirksamkeit der Lithiumaugmentierung mit dem Wechsel zu einem MAO-Hemmer in einer sechswöchigen Open-Label-Studie (n=29) bei älteren Patienten (mittleres Alter 73,1±7,7 Jahre) mit therapierefraktärer schwerer depressiver Episode [26] und berichteten für die Lithiumaugmentation Remissionsraten von 33%, während beim Wechsel zu Phenelzin kein Patient remittierte [26].
Versuch eines evidenzbasierten Therapiealgorithmus
Ausgehend von den vorliegenden Konsensusempfehlungen [2, 49], den drei Metaanalysen der Cochrane-Datenbank [5, 30, 46] sowie neueren Studien zur Monotherapie [3, 25, 37, 40], Studien zur Erhaltungs- [18, 37] und Kombinationstherapie [7, 11] und Studien zum Wechsel zu einem MAO-Hemmer bei therapierefraktärer Depression [15, 26, 42] im höheren Lebensalter stellen wir anhand der Vorlagen des Texas Algorithm Project [10] und des Berliner Stufenplans zur Depressionsbehandlung [1] ein evidenzbasiertes Therapieschema für die Pharmakotherapie depressiver Erkrankungen im höheren Lebensalter vor (Abb. 1). Dabei sind die Evidenzgrade wie folgt definiert:
- Evidenzgrad I: Metaanalyse oder mehrere randomisierte kontrollierte Studien
- Evidenzgrad II: eine randomisierte kontrollierte Studie oder mehrere Open-Label-Studien
- Evidenzgrad III: einzelne Berichte
- Evidenzgrad IV: Konsensus ohne Evidenz
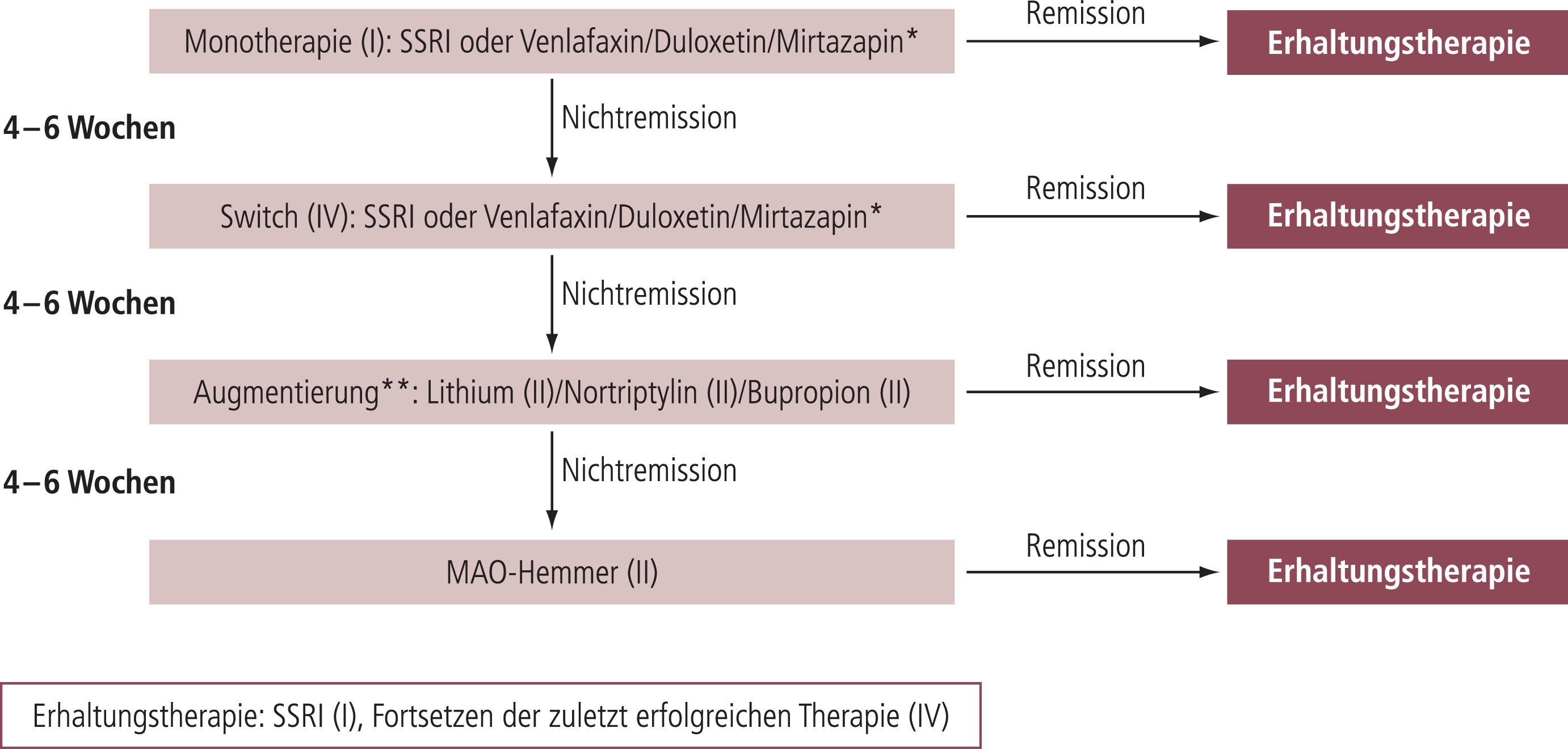
Abb. 1. Versuch eines evidenzbasierten Therapiealgorithmus für die antidepressive Pharmakotherapie im Alter
* TZA sind angesichts der erhöhten Nebenwirkungsraten im Alter [29] möglich, jedoch nicht Medikamente der ersten Wahl. ** Mirtazapin ist als Augmentierungsstrategie im Alter noch nicht untersucht, angesichts der guten Daten bei jüngeren Erwachsenen jedoch vielerorts gängige Praxis [7]. Evidenzgrade: I = Metaanalyse oder mehrere randomisierte kontrollierte Studien; II = eine randomisierte kontrollierte Studie oder mehrere Open-Label-Studien; III = einzelne Berichte; IV = Konsensus ohne Evidenz
Der hier vorgestellte Algorithmus schließt die wahnhafte Depression nicht explizit mit ein. Konsensusleitlinien [2, 49] empfehlen hier die interkurrente Komedikation mit einem atypischen Neuroleptikum, welches nach Abklingen der affektiven Symptomatik ausgeschlichen werden sollte. Auch beschreibt der vorliegende Therapiealgorithmus lediglich pharmakotherapeutische Interventionen. Der Nutzen anderer Verfahren, wie etwa psychotherapeutischer Interventionen (in Kombination mit pharmakotherapeutischen Ansätzen) [39] und insbesondere bei der therapierefraktären Depression unter strikter Beachtung der Kontraindikationen auch der Elektrokrampftherapie [19] hat jedoch ebenfalls eine gute Evidenzbasis.
In der Monotherapie depressiver Erkrankungen haben TZA und SSRI den Evidenzgrad I [5, 30, 44]. Die neueren Antidepressiva Duloxetin [37], Venlafaxin [3] und Mirtazapin [40] als Monotherapie haben Evidenzgrad II. Dabei basiert das Therapieschema zunächst auf einer zentralen Prämisse, die sich aus den hier vorgestellten Metaanalysen ergibt. So zeigen zwar sowohl SSRI als auch TZA in der antidepressiven Pharmakotherapie älterer Patienten Evidenz für die Wirksamkeit, für die TZA ist jedoch eine signifikant höhere Nebenwirkungs- und Abbruchrate beschrieben worden [5, 30]. Angesichts der klinischen Konsensusempfehlungen, die eine antidepressive Pharmakotherapie mit TZA bei älteren Patienten nicht [2] oder nur eingeschränkt [49] empfehlen, werden TZA im hier vorgestellten Stufenplan (analog zum Berliner Stufenplan [1]) nicht als Medikamente der ersten Wahl aufgeführt. Ihre Einsatzmöglichkeit unter Berücksichtigung von Nebenwirkungen auch als Monotherapie wird jedoch bestätigt.
Die Dauer bis zu einem Wechsel entbehrt ebenfalls einer gesicherten Evidenzbasis. Während die NICE-Leitlinien [49] anhand der dort vorgestellten Übersichtsarbeiten eine Therapiedauer von mindestens sechs Wochen empfehlen, konnten Mulsant und Kollegen [29] in einer prospektiven Studie mit wöchentlichen Assessments mittels der Hamilton-Depressionsskala bei 472 älteren Patienten (mittleres Alter 72,5±7,4 Jahre) zeigen, dass das Vorliegen und aber insbesondere die Abwesenheit einer Teilremission bereits nach vier Wochen für den Therapieerfolg aussagekräftig ist. Die Patienten hatten randomisiert entweder Paroxetin oder Nortriptylin erhalten. Bei den Patienten (n=168), die nach vier Wochen keine Teilremission zeigten, erreichten nur 21,6% bei Weiterbehandlung eine Remission. Bei den Patienten, die nach vier Wochen eine Teilremission aufwiesen (n=149), erreichten hingegen 50,2% eine volle Remission. Nach sechs Wochen zeigte sich ein ähnliches Bild: Bei den Patienten, die nach sechs Wochen keine Teilremission zeigten (n=107), erreichten nur 25,7% bei Weiterbehandlung eine Remission. Bei den Patienten, die nach vier Wochen eine Teilremission aufwiesen (n=168), erreichten hingegen 60,3% eine volle Remission [29]. Die Autoren schlagen deshalb vor, bei Ausbleiben einer Teilremission nach vier Wochen zu wechseln; diese Evidenz geht in den hier vorgeschlagenen Stufenplan mit ein.
Das hier vorgeschlagene Therapieschema weist Lücken auf, die in bisher fehlender Evidenz begründet sind, die jedoch nicht die Abwesenheit der Wirksamkeit für bestimmte Therapieansätze belegt. So stehen sowohl für Augmentierungsstrategien bei Teilremission (die sogenannte „frühe“ Augmentierung) als auch für den Wechsel auf ein Antidepressivum einer anderen Klasse nach erfolgloser Therapie nach mindestens sechs Wochen keine spezifischen Daten für ältere Patienten zur Verfügung. Der Wechsel auf ein Antidepressivum einer anderen Klasse wird jedoch in den spezifischen Konsensusleitlinien explizit empfohlen [2, 49], so dass er mit Evidenzgrad IV Aufnahme in das hier vorgeschlagene Therapieschema findet.
Für die Augmentierung einer antidepressiven Therapie liegen aus der STAR*D-Studie [11] – sowie einer weiteren Studie zur Lithiumaugmentierung [26] – Daten vor, die die Augmentierung mit den Substanzen Lithium, Nortriptylin und Bupropion mit Evidenzgrad II empfehlen. Für die Erhaltungstherapie liegen lediglich Daten für SSRI vor (Evidenzgrad I), die Konsensusempfehlung des Fortführens der zuletzt erfolgreichen Therapie [2] scheint hier jedoch plausibel (Evidenzgrad IV).
Insgesamt ist die Studienlage zur antidepressiven Pharmakotherapie im Alter weiterhin als unbefriedigend zu bewerten. Neben den genannten Lücken fehlen insbesondere auch weiterführende Daten zur Kombinationstherapie aus Pharmako- und Psychotherapie (siehe auch [38]), die aber in den Konsensusleitlinien empfohlen wird [2, 49]. Weiterhin liegen keine Studien für die rasch wachsende Zahl hochaltriger Patienten (z.B. über 80 Jahre) vor, und auch Studien zum Therapieeffekt auf die im Alter erhöhte Suizidalität fehlen bislang. Schließlich liegen keine Studien zur Wirksamkeit bei altersadjustierten Dosierungen vor, und auch empirische Studien zum therapeutischen Drug-Monitoring (TDM) fehlen im Alter. Die Arbeitsgemeinschaft TDM der Arbeitsgemeinschaft für Neuropsychopharmakologie und Pharmakopsychiatrie empfiehlt jedoch bei Patienten über 65 Jahren grundsätzlich das TDM, spezifisch bei einigen TZA (z.B. Nortriptylin, Despiramin: dringende Empfehlung), SSRI (Citalopram, Paroxetin, Sertralin mit dem Empfehlungsgrad „nützlich“) und anderen Antidepressiva (Mirtazapin, Mianserin mit dem Empfehlungsgrad „nützlich“) [6]. Angesichts der häufigen Komorbiditäten und möglichen Wechselwirkungen mit anderen Pharmaka kommt einer individuellen Therapieplanung bei der pharmakotherapeutischen Behandlung der Depression im höheren Lebensalter deshalb auch jenseits der vorliegenden und hier zusammengefassten Evidenz eine zentrale Bedeutung zu.
Literatur
1. Adli M, Rush AJ, Möller HJ, Bauer M. Algorithms for optimizing the treatment of depression: making the right decision at the right time. Pharmacopsychiatry 2003;36(Suppl 3):S222–9.
2. Alexopoulos GS, Katz IR, Reynolds CF 3rd, Carpenter D, et al. The expert consensus guideline series. Pharmacotherapy of depressive disorders in older patients. Postgrad Med 2001; Spec No Pharmacotherapy:1–86.
3. Allard P, Gram L, Timdahl K, Behnke K, et al. Efficacy and tolerability of venlafaxine in geriatric outpatients with major depression: a double-blind, randomised 6-month comparative trial with citalopram. Int J Geriatr Psychiatry 2004;19:1123–30.
4. Angst J. The course of affective disorders. Psychopathology 1986;19(Suppl 2):47–52.
5. Arroll B, Elley CR, Fishman T, Goodyear-Smith FA, et al. Antidepressants versus placebo for depression in primary care. Cochrane Database of Systematic Reviews 2009; Issue 3.
6. Baumann P, Hiemke C, Ulrich S, Eckermann G, et al. The AGN-TDM Expert Group Consensus Guidelines: Therapeutic drug monitoring in psychiatry. Pharmacopsychiatry 2004;37:243–65.
7. Carpenter LL, Yasmin S, Price LH. A double-blind, placebo-controlled study of antidepressant augmentation with mirtazapine. Biol Psychiatry 2002;51:183–8.
8. Cochrane A. Effectiveness and Efficiency – Random Reflections on Health Services. London: Royal Society of Medicine Press, 1997.
9. Cohn CK, Shrivastava R, Mendels J, Cohn JB, et al. Double-blind, multicenter comparison of sertraline and amitriptyline in elderly depressed patients. J Clin Psychiatry 1990;51(Suppl B):28–33.
10. Crismon ML, Trivedi M, Pigott TA, Rush AJ, et al. The Texas Medication Algorithm Project: report of the Texas Consensus Conference Panel on Medication Treatment of Major Depressive Disorder. J Clin Psychiatry 1999;60:142–56.
11. Dew MA, Whyte EM, Lenze EJ, Houck PR, et al. Recovery from major depression in older adults receiving augmentation of antidepressant pharmacotherapy. Am J Psychiatry 2007;164:892–9.
12. Dorman T. Sleep and paroxetine: a comparison with mianserin in elderly depressed patients. Int Clin Psychopharmacol 1992;6(Suppl 4):53–8.
13. Erlenmeier N. Suizidalität im Alter. Stuttgart: Kohlhammer, 1992.
14. Feighner JP. A comparative trial of fluoxetine and amitriptyline in patients with major depressive disorder. J Clin Psychiatry 1985;46:369–72.
15. Flint AJ, Rifat SL. The effect of sequential antidepressant treatment on geriatric depression. J Affect Disord 1996;36:95–105.
16. Georgotas A, McCue RE, Hapworth W, Friedman E, et al. Comparative efficacy and safety of MAOIs versus TCAs in treating depression in the elderly. Biol Psychiatry 1986;21:1155–66.
17. Geretsegger C, Stuppaeck CH, Mair M, Platz T, et al. Multicenter double blind study of paroxetine and amitriptyline in elderly depressed inpatients. Psychopharmacology (Berl) 1995;119:277–81.
18. Gorwood P, Weiller E, Lemming O, Katona C. Escitalopram prevents relapse in older patients with major depressive disorder. Am J Geriatr Psychiatry 2007;15:581–93.
19. Greenberg RM, Kellner CH. Electroconvulsive therapy: a selected review. Am J Geriatr Psychiatry 2005;13:268–81.
20. Guillibert E, Pelicier Y, Archambault JC, Chabannes JP, et al. A double-blind, multicentre study of paroxetine versus clomipramine in depressed elderly patients. Acta Psychiatr Scand Suppl 1989;350:132–4.
21. Harrer G, Schmidt U, Kuhn U, Biller A. Comparison of equivalence between the St. John’s wort extract LoHyp-57 and fluoxetine. Arzneimittelforschung 1999;49:289–96.
22. Helmchen H, Linden M. Subthreshold disorders in psychiatry: Clinical reality, methodological artifact, and the double-threshold problem. Compr Psychiatry 2000;41(Suppl 1):1–7.
23. Hutchinson DR, Tong S, Moon CA, Vince M, et al. Paroxetine in the treatment of elderly depressed patients in general practice: a double-blind comparison with amitriptyline. Int Clin Psychopharmacol 1992;6(Suppl 4): 43–51.
24. Jorm AF. Does old age reduce the risk of anxiety and depression? A review of epidemiological studies across the adult life span. Psychol Med 2000;30:11.
25. Katona CL, Abou-Saleh MT, Harrison DA, Nairac BA, et al. Placebo-controlled trial of lithium augmentation of fluoxetine and lofepramine. Br J Psychiatry 1995;166:80–6.
26. Kok RM, Vink D, Heeren TJ, Nolen WA. Lithium augmentation compared with phenelzine in treatment-resistant depression in the elderly: an open, randomized, controlled trial. J Clin Psychiatry 2007;68:1177–85.
27. La Pia S, Giorgio D, Ciriello R, Sannino A, et al. Double blind controlled study to evaluate the effectiveness and tolerability of fluoxetine versus mianserin in the treatment of depressive disorders among the elderly and their effects on cognitive behavioral parameters. New Trends Exp Clin Psychiatry 1992;8:139–46.
28. Mahapatra SN, Hackett D. A randomised, double-blind, parallel-group comparison of venlafaxine and dothiepin in geriatric patients with major depression. Int J Clin Pract 1997;51(4):209-13.
29. Mulsant BH, Houck PR, Gildengers AG, Andreescu C, et al. What is the optimal duration of a short-term antidepressant trial when treating geriatric depression? J Clin Psychopharmacol 2006;26:113–20.
30. Mottram P, Wilson K, Strobl P. Antidepressants for depressed elderly. Cochrane Database of Systematic Reviews 2003; Issue 2.
31. Pélicier Y, Schaeffer P. Multicenter double-blind study comparing the efficacy and tolerance of paroxetine and clomipramine in reactive depression in the elderly patient. Encephale 1993;19:257–61.
32. Phanjoo AL, Wonnacott S, Hodgson A. Double-blind comparative multicentre study of fluvoxamine and mianserin in the treatment of major depressive episode in elderly people. Acta Psychiatr Scand 1991;83:476–9.
33. Rahman MK, Akhtar MJ, Savla NC, Sharma RR, et al. A double-blind, randomised comparison of fluvoxamine with dothiepin in the treatment of depression in elderly patients. Br J Clin Prac 1991;45:255–8.
34. Rapp MA, Dahlman K, Sano M, Grossman HT, et al. Neuropsychological differences between late-onset and recurrent geriatric major depression. Am J Psychiatry 2005;162: 691–8.
35. Rapp MA, Schnaider-Beeri M, Grossman HT, Sano M, et al. Increased hippocampal plaques and tangles in patients with Alzheimer disease with a lifetime history of major depression. Arch Gen Psychiatry 2006;63:161–7.
36. Rapp MA, Gerstorf D, Helmchen H, Smith J. Depression predicts mortality in the young old, but not in the oldest old: results from the Berlin Aging Study. Am J Geriatr Psychiatry 2008;16:844–52.
37. Raskin J, Wiltse CG, Siegal A, Sheikh J, et al. Efficacy of duloxetine on cognition, depression, and pain in elderly patients with major depressive disorder: an 8-week, double-blind, placebo-controlled trial. Am J Psychiatry 2007;164:900–9.
38. Reynolds CF 3rd, Dew MA, Pollock BG, Mulsant BH, et al. Maintenance treatment of major depression in old age. N Engl J Med 2006;354:1130–8.
39. Rutherford B, Sneed J, Miyazaki M, Eisenstadt R, et al. An open trial of aripiprazole augmentation for SSRI non-remitters with late-life depression. Int J Geriatr Psychiatry 2007;22:986–91.
40. Schatzberg AF, Kremer C, Rodrigues HE, Murphy GM Jr, et al. Double-blind, randomized comparison of mirtazapine and paroxetine in elderly depressed patients. Am J Geriatr Psychiatry 2002;10:541–50.
41. Smeraldi E. Amisulpride versus fluoxetine in patients with dysthymia or major depression in partial remission: a double-blind, comparative study. J Affect Disord 1998;48:47–56.
42. Sunderland T, Cohen RM, Molchan S, Lawlor BA, et al. High-dose selegiline in treatment-resistant older depressive patients. Arch Gen Psychiatry 1994;51:607–15.
43. Taylor WD, Steffens DC, Krishnan KR. Psychiatric disease in the twenty-first century: The case for subcortical ischemic depression. Biol Psychiatry 2006;60:1299–303.
44. Wilson K, Mottram P, Sivanranthan A, Nightingale A. Antidepressants versus placebo for the depressed elderly. Cochrane Database of Systematic Reviews 2001; Issue 3.
45. Wiltfang J, Lewczuk P, Riederer P, Grünblatt E, et al. Consensus paper of the WFSBP Task Force on Biological Markers of Dementia: the role of CSF and blood analysis in the early and differential diagnosis of dementia. World J Biol Psychiatry 2005;6:69–84.
47. www.iqwig.de/index.981.html/
48. www.nice.org.uk/CG023NICEguideline
Dr. phil. Dr. med. Michael A. Rapp, Klinik für Psychiatrie und Psychotherapie, Charité Campus Mitte, Berlin und Gerontopsychiatrisches Zentrum, Psychiatrische Universitätsklinik der Charité im St. Hedwigs Krankenhaus, Große Hamburger Straße 5–11, 10115 Berlin, E-Mail: Michael.Rapp@charite.de
Antidepressant treatment in old age: what is the evidence base?
Compared to young adults, data on antidepressant treatment in older adults are sparse. Following established consensus guidelines, systematic evidence-based reviews, and recent studies, we present the evidence base for the pharmacotherapy of depression in older adults. In addition, following established treatment algorithms in younger adults, we develop a specific treatment algorithm for depression in later life. Results are being discussed.
Key words: Depression, pharmacotherapy, evidence base, treatment algorithms, old age
Psychopharmakotherapie 2010; 17(02)
