Reimund Freye, Baden-Baden
Das Nucleosid-Analogon Cladribin (Abb. 1) wird bereits seit mehreren Jahren erfolgreich parenteral (Leustatin®, Litak®) zur Behandlung der Haarzell-Leukämie eingesetzt. Cladribin ist ein Prodrug, das vor allem in Lymphozyten und Monozyten durch Phosporylierung in seine aktive Form umgewandelt wird. Die Selektivität für diese Zelltypen resultiert daraus, dass diese Immunzellen eine hohe Phosphorylierungsrate und gleichzeitig eine geringe Dephosphorylierungsaktivität aufweisen. Weil in Cladribin am Purin-Ringsystem ein Wasserstoff- durch ein Chloratom ersetzt wurde, ist es gegen das Enzym Adenosindeaminase resistent. Dadurch kommt es intrazellulär zur Akkumulation der aktiven Substanz.
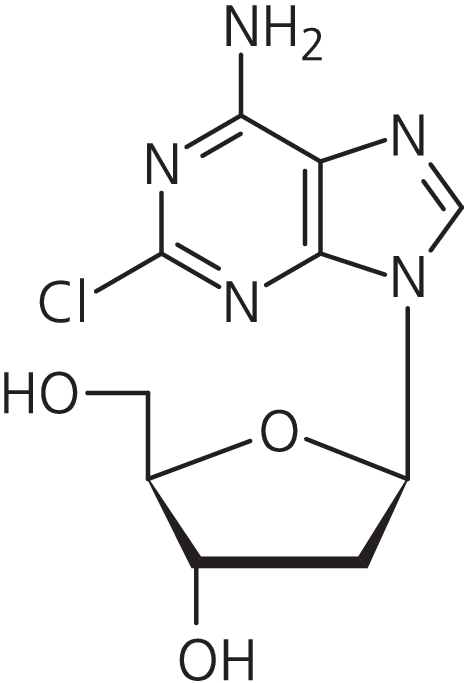
Abb. 1. Cladribin
Cladribin wirkt sowohl in sich teilenden als auch ruhenden Lymphozyten. In den ruhenden Zellen bewirkt es eine defiziente Reparatur von DNS-Strangbrüchen, in sich teilenden Zellen eine Hemmung der DNS-Polymerase. Der depletive Effekt auf CD4-positive T-Zellen scheint wesentlich ausgeprägter zu sein als auf CD8-positive T-Zellen. Da aber ein hoher CD4/CD8-Quotient mit einer stärkeren MS-Aktivität in Zusammenhang gebracht wird, könnte gerade diese Selektivität in einer besonderen Wirksamkeit resultieren.
Für die Behandlung der multiplen Sklerose wurde Cladribin als orale Darreichungsform entwickelt. Der Vorteil einer oralen Einnahme wird noch ergänzt durch ein Therapieregime, das es erlaubt, die Substanz lediglich während eines Monats pro Jahr einzunehmen. Die T-Lymphozyten benötigen nämlich fast ein ganzes Jahr, um sich von dieser Reduktion ihrer Anzahl zu erholen. Wie Prof. Kieseier betonte, bestehen bei anderen neurologischen Autoimmunerkrankungen bereits gute Erfahrungen mit einer Absenkung der Lymphozyten-Konzentration auf deutlich unter 109/l. Es werden dadurch keine gravierenden Infektionen generiert.
In ersten Studien konnte die verträgliche Dosis von 2,1 mg/kg Körpergewicht den Anteil der Patienten mit Gadolinium-aufnehmenden, also aktiv entzündlichen, Läsionen um 85% senken.
Aktuell wird Cladribin in der Phase-III-Studie CLARITY (Cladribine tablets in treating MS orally) bei 1348 Patienten mit schubförmiger MS getestet. Die Ergebnisse dieser Studie werden 2009 erwartet. In einer weiteren Untersuchung (ONWARD) soll geklärt werden, ob die Add-on-Gabe von Cladribin zur Standardtherapie mit Interferon beta-1a einen zusätzlichen Nutzen bringt.
B-Zellen als Zielpunkt der MS-Therapie
Standen bei der Pathogenese der multiplen Sklerose bislang die T-Zellen im Fokus des Interesses, so verdichten sich die Hinweise darauf, dass auch die B-Lymphozyten eine wesentliche Rolle bei der Entstehung und Aufrechterhaltung des Autoimmunprozesses spielen. Dies ist zumindest vornehmlich bei einem Subtyp der Erkrankung, der sogenannten Pattern-II-MS der Fall.
Die Beteiligung von B-Zellen an der Pathogenese der MS läuft vermutlich zum einen über die Sezernierung von (Auto-) Antikörpern, die direkt demyelinisierend wirken, andererseits aber auch über interne Kommunikation im Immunsystem via Antigen-Präsentation gegenüber T-Zellen.
Im Verlauf der Erkrankung wechselt offenbar die autoimmunologische Aktivität der B-Zellen im ZNS. In früh aktiven MS-Läsionen lassen sich vor allem CD20-positive B-Zellen nachweisen. In chronifizierten MS-Läsionen jedoch sind hohe Konzentrationen von ausgereiften Plasmazellen feststellbar, die Immunglobuline sezernieren. Hierbei war lange Zeit unklar, warum die B-Zellen so lange im ZNS überleben konnten. Neuere Forschungen machen hierfür unter anderen den Faktor BAFF (B-cell-activating factor belonging to the TNF family) verantwortlich, der von Astrozyten produziert wird.
Als therapeutische Optionen ergeben sich daraus einerseits eine Elimination von Autoantikörpern durch Plasmapherese und andererseits eine B-Zell-Depletion. Für Letztere stehen zurzeit zwei Strategien zur Verfügung. Rituximab, ein monoklonaler Antikörper, der bereits beim Non-Hodgkin-Lymphom und der rheumatoiden Arthritis eingesetzt wird (MabThera®), bindet an das CD20-Antigen auf B-Zellen und induziert dadurch deren Zerstörung. Der zweite Ansatz besteht in der subkutanen Gabe von Atacicept. Dies ist ein Fusionsprotein aus der Fc-Domäne von menschlichem Immunglobulin G und dem extrazellulären Anteil des TACI-Rezeptors, eines auf B-Zellen liegenden Rezeptors, über den normalerweise unter anderem BAFF seine stimulierende Wirkung entfaltet. Als löslicher TACI-Rezeptor blockiert Atacicept die BAFF-Signalübertragung. Die Folge ist eine Hemmung der B-Zell-Proliferation und der weiteren Differenzierung. Im Moment laufen mit Atacicept Phase-II-Studien.
Quelle
Prof. Dr. med. Hans-Peter Hartung, Düsseldorf, Prof. Dr. med. Bernd Kieseier, Düsseldorf, Priv.-Doz. Dr. med. Andreas Steinbrecher, Regensburg, Satellitensymposium „Perspektiven in der Multiplen Sklerose-Therapie“, veranstaltet von Merck Serono im Rahmen des 81. Kongresses der DGN, Hamburg, 12. September 2008.
Psychopharmakotherapie 2009; 16(02)
