Dr. Tanja Saußele, Stuttgart
In Deutschland leiden ungefähr 600000 bis 800000 Menschen an Epilepsie. Fokale Anfälle sind bei den Patienten am häufigsten und noch dazu am schwersten zu behandeln. Die meisten Patienten müssen dauerhaft Medikamente einnehmen, aber nur 70 bis 80% der Epilepsie-Patienten können dabei anfallsfrei werden. Antiepileptika dienen der symptomatischen Behandlung verschiedener Epilepsieformen. Sie wirken entweder hemmend auf die Erregbarkeit von Neuronen und/oder dämpfend auf die räumliche Ausbreitung der Erregung. Angriffspunkte sind dabei Ionenkanäle (z.B. Kalium-, Natrium-, oder Calciumionenkanäle) oder Neurotransmitter-Rezeptoren (z.B. NMDA- oder GABA-Rezeptoren).
Die antiepileptische Wirksamkeit von Lacosamid beruht zum einen auf einer Steigerung der langsamen Inaktivierung spannungsabhängiger Natriumkanäle, ohne dabei die schnelle Inaktivierung zu beeinflussen, die beispielsweise den Angriffspunkt für Carbamazepin, Phenytoin und Lamotrigin darstellt. Dadurch kommt es zu einer Herabsetzung der pathophysiologisch erhöhten neuronalen Aktivität, einer Normalisierung der Aktivierungsschwelle und dadurch zu einer Stabilisierung des Membranpotenzials. Zum anderen bindet Lacosamid an CRMP(Collapsin response mediator protein)-2, ein Phosphoprotein, das an der neuronalen Differenzierung und Netzwerkbildung beteiligt ist.
Klinische Studien
Bislang wurden drei große, Plazebo-kontrollierte, randomisierte und doppelblinde Studien mit jeweils über 400 Epilepsie-Patienten durchgeführt, die an fokalen Anfällen mit oder ohne sekundäre Generalisierung litten (Tab. 1). Die Patienten litten durchschnittlich 20 Jahre an Epilepsie und nahmen bereits ein bis drei Antiepileptika ein. Die Patienten hatten durchschnittlich vier fokale Anfälle innerhalb von 28 Tagen. Während einer achtwöchigen Beobachtungsphase zu Beginn der Studien war der anfallsfreie Zeitraum der Patienten kürzer als 21 Tage. Danach erhielten die Patienten entweder Lacosamid (je nach Studie: 200 mg, 400 mg oder 600 mg) oder Plazebo. Die Lacosamid-Dosis wurde dabei innerhalb von sechs Wochen einmal pro Woche um 100 mg/d bis zur jeweiligen Zieldosis erhöht. Bei einer Lacosamid-Zieldosis unter 600 mg erfolgte die Titration in den ersten Wochen mit Plazebo. Im Anschluss an die Titrationsphase folgte eine zwölfwöchige Erhaltungsphase.
Tab. 1. Überblick über Plazebo-kontrollierte, randomisierte und doppelblinde Lacosamid-Studien der Phasen II und III
|
Studie, Ort |
Lacosamid-Dosen |
Patienten [n] (ITT) |
|
SP667 (Phase II) USA, Europa |
200 mg/d 400 mg/d 600 mg/d |
421 |
|
SP755 (Phase III) Europa, Australien |
200 mg/d 400 mg/d |
477 |
|
SP754 (Phase III) USA |
400 mg/d 600 mg/d |
402 |
ITT = Anzahl der Patienten, die in die Intention-to-treat-Analyse eingegangen ist
In den drei Studien konnte jeweils eine signifikante Reduktion der Anfallshäufigkeit durch Lacosamid bei den Patienten gezeigt werden, die die Studien bis zum Ende durchführten (Abb. 1). Eine 50%ige Reduktion der Anfallshäufigkeit erreichten in der Phase-II-Studie, die in den USA und Europa durchgeführt wurde (SP667), 38% der Patienten, die 200 mg Lacosamid einnahmen, jeweils 49% der 400-mg- und 600-mg-Lacosamid-Gruppe und 21% der Plazebo-Gruppe. In der Phase-III-Studie SP755 erreichten nur die Patienten der 400-mg-Lacosamid-Gruppe signifikant häufiger eine 50%ige Reduktion der Anfallshäufigkeit (46%) als Patienten, die 200 mg Lacosamid (35%) oder Plazebo (38%) einnahmen. In der Studie SP754, in der die 400-mg- und 600-mg-Lacosamid-Dosis untersucht wurde, erreichten 40% der 400-mg-Gruppe und 51% der 600-mg-Gruppe eine 50%ige Reduktion der Anfallshäufigkeit, dies war signifikant häufiger als in der Plazebo-Gruppe (18%).
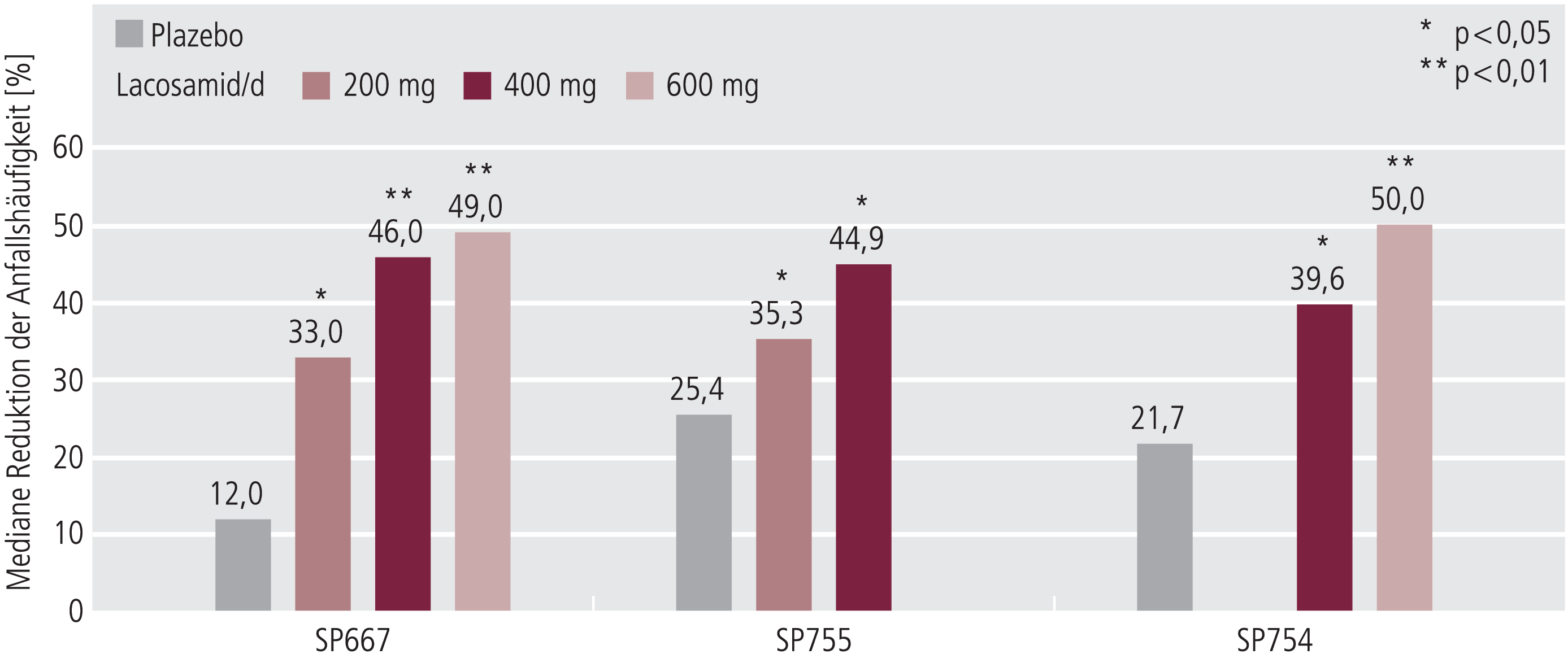
Abb. 1. Mediane Reduktion der Anfallshäufigkeit seit Studienbeginn in den Phase-II- und Phase-III-Studien SP667, SP755 und SP754 (Per-Protocol-Analyse)
Die häufigsten unerwünschten Wirkungen, die bei mehr als 10% der Patienten während den Behandlungsphasen dosisabhängig auftraten, waren Schwindel, Kopfschmerzen, Diplopie und Übelkeit. Das Körpergewicht oder Laborparameter wurden durch Lacosamid nicht verändert. Im EKG wurde hingegen eine dosisabhängige geringfügige Verlängerung des PR-Intervalls beobachtet.
Klinische Interaktionsstudien haben ergeben, dass die Pharmakokinetik anderer Antiepileptika oder beispielsweise oraler Kontrazeptiva durch Lacosamid nicht beeinflusst wird. Die Pharmakokinetik von Lacosamid kann jedoch durch die gleichzeitige Anwendung anderer, enzyminduzierender Antiepileptika wie Carbamazepin, Phenytoin und Phenobarbital verändert werden; in einer Populationsanalyse wurde eine 25%ige Verringerung der systemischen Lacosamid-Exposition beobachtet.
Zusammenfassung
Lacosamid ist seit Anfang September für Patienten ab 16 Jahre zugelassen für eine ergänzende Behandlung bei fokalen Anfällen mit oder ohne sekundäre Generalisierung. Zu Behandlungsbeginn wird eine Dosis von zweimal täglich 50 mg Lacosamid empfohlen, die dann wöchentlich in Schritten von zweimal täglich 50 mg Lacosamid erhöht werden kann. Die empfohlene Tageshöchstdosis beträgt 400 mg Lacosamid (zweimal 200 mg). Der Wirkstoff ist sowohl in Tablettenform (50 mg, 100 mg, 150 mg und 200 mg) als auch in Sirupform und als Infusionslösung erhältlich. In klinischen Studien konnte bereits gezeigt werden, dass die kurzfristige parenterale Gabe von Lacosamid bioäquivalent zur oralen Gabe war und auch die Sicherheit und Verträglichkeit beider Applikationsformen vergleichbar waren. Somit stellt die parenterale Gabe eine Alternative für Patienten dar, die vorüberghend nicht in der Lage sind, Lacosamid oral einzunehmen, beispielsweise nach einer Operation.
Quellen
Dr. Stephan Arnold, München, Prof. Dr. Bernhard J. Steinhoff, Kehl-Kork, Dr. Mischa Uebachs, Bonn. Journalisten-Workshop Lacosamid „Epilepsiemangagement 2008“, Monheim, 5. August 2008, veranstaltet von UCB Pharma.
Dr. Stephan Arnold, München, Dr. Günther Krämer, Zürich, Prof. Dr. Christian E. Elger, Bonn. 4. Turmgespräch Epilepsie „Epilepsiemanagement 2008“, Köln, 5. September 2008, veranstaltet von UCB Pharma.
Fachinformation Vimpat®. Stand: August 2008.
Psychopharmakotherapie 2009; 16(01)
