Jörg Wissel, Beelitz-Heilstätten
Die Basis der Behandlung der Spastizität bildet die krankengymnastische und physikalische Behandlung [17]. Lassen sich jedoch Behinderungen und Schmerzen durch eine Spastik so nicht beherrschen, so sind Botulinumtoxin-Typ-A(BoNT A)-Injektionen die Behandlung der Wahl bei spastischen Syndromen mit fokalen Behinderungen. Die Begründung für den Einsatz von BoNT A ergibt sich aus einer bei intramuskulärer Injektion auftretenden lokalisierten und dosisabhängigen Wirkung. Es kommt nach Injektion zu einer rezeptorvermittelten Bindung und Aufnahme von BoNT A in aktive motorische Endplatten. Hier induziert BoNT A eine hochselektive neuromuskuläre Blockade durch Blockierung der Freisetzung von Acetylcholin und dadurch eine dosisabhängige Tonusreduktion der injizierten Muskeln [1, 10]. Wie eine Reihe kontrollierter Studien zeigen konnte, bewirken Injektionen bei Patienten mit Spastizität eine lokale Reduktion des Muskeltonus und Vergrößerung des passiven Bewegungsausmaßes von betroffenen Gelenken [2, 13, 15, 18]. Zudem konnte in kontrollierten Studien gezeigt werden, dass Schlaganfallpatienten von der Injektion einer adäquaten BoNT-A-Dosis eine signifikante Abnahme ihres funktionellen Behinderungsgrads und der Pflegeabhängigkeit erreichen können [3].
Evidenzbasierte Empfehlungen zur Botulinumtoxin-A-Behandlung der Spastizität
Evidenzklasse I (mehrere große kontrollierte Studien und ein systematischer Review): BoNT A mindert den spastischen Muskeltonus dosisabhängig, auch nach wiederholten Behandlungszyklen [14]. Die Behandlung zeigt kaum relevante Nebenwirkungen [14]. BoNT A kann in moderater Dosierung (250 MU Botox®) bei der Behandlung der oberen Extremität zu alltagsrelevanten Verbesserungen der Funktion führen [3] und die Belastung von pflegenden Angehörigen signifikant mindern (500–1000 MU Dysport®) [2].
Evidenzklasse II–III (wenige kleine kontrollierte Studien und Fallsammlungen, Fallberichte): BoNT A mindert Spastik-assoziierte Schmerzen [18]. Die tonussenkende Wirkung von BoNT A kann durch Taping [4] und Elektrostimulation günstig beeinflusst werden [9].
Evidenzklasse IV (Expertenmeinung):Injektionskontrolltechniken wie elektrophysiologische Verfahren (EMG und Elektrostimulation) und Ultraschall steigern die Genauigkeit der Injektionslokalisation von BoNT A [19].
Praxis der Botulinumtoxin-Behandlung in Deutschland
In Deutschland ist aktuell nur ein BoNT-A-Präparat (Botox®) zur Behandlung des dynamischen Spitzfußes bei Kindern mit Zerebralparese ab zwei Jahren zugelassen. Bis Ende 2008 waren Botox® und Dysport® die beiden zugelassenen BoNT-A-Produkte zur Behandlung der Armspastik nach Schlaganfall. Für das dritte Produkt, Xeomin®, ist die Zulassung zur Behandlung der oberen Extremität nach Schlaganfall beantragt. In der auf der Jahrestagung 2008 der Deutschen Gesellschaft für Neurologie in Hamburg vorgestellten Zulassungsstudie zeigte Xeomin®, dass es in dieser Indikation wie die anderen Produkte hoch wirksam und nebenwirkungsarm ist.
Die Gabe einer adäquaten Dosis (Tab. 1 und 2) eines der drei Produkte erzielt eine hohe lokale Wirksamkeit und kann bei Spastizität mit fokaler Behinderung die Motilität von betroffenen Gelenken verbessern, den Tonus reduzieren und begleitende Schmerzen lindern [14, 20]. Zudem kann BoNT A mit allen anderen medikamentösen und nichtmedikamentösen Therapieverfahren der Spastizität kombiniert werden, ohne dass Interaktionen befürchtet werden müssen [17, 21]. Dies sind gute Argumente, eines der BoNT-A-Produkte auch bei lokalen Schwerpunkten einer generalisierten Spastik nach Schlaganfall in Kombination mit oralen oder intrathekalen Antispastika einzusetzen.
Tab. 1. Dosierung von Botulinumtoxin A bei Spastizität der oberen Extremität
|
Muskel |
Anzahl Injektionsstellen |
Dosis Botox® Xeomin® [Units] |
Dosis Dysport® [Units] |
|
M. deltoideus |
2 |
25–50 |
125–250 |
|
M. pectoralis major |
1–3 |
50–75 |
250–375 |
|
M. teres major |
1–2 |
25–50 |
125–250 |
|
M. biceps brachii |
3–4 |
50–100 |
250–500 |
|
M. brachialis |
1–2 |
25–50 |
125–250 |
|
M. brachioradialis |
1–2 |
25–50 |
125–250 |
|
M. flex. carpi radialis |
1–2 |
25–50 |
125–250 |
|
M. flex. carpi ulnaris |
1–2 |
25–50 |
125–250 |
|
M. flex. dig. profundus |
2–3 |
25–50 |
125–250 |
|
M. flex. dig. superficialis |
2–3 |
25–50 |
125–250 |
|
M. flexor pollicis longus |
1–2 |
25–50 |
75–250 |
|
M. adductor pollicis |
1 |
15–25 |
75–125 |
|
M. flexor pollicis brevis |
1 |
15–25 |
75–125 |
|
Gesamtdosis pro Sitzung |
<500 |
<1500 |
|
|
Empfohlene Verdünnung |
2–5 ml/100 Units |
2–4 ml/500 Units |
|
Tab. 2. Dosierung von Botulinumtoxin A bei Spastizität der unteren Extremität
|
Muskel |
Anzahl |
Dosis Botox® |
Dosis |
|
M. iliopsoas |
2–3 |
50–100 |
250–500 |
|
M. adductor longus |
1–2 |
50–75 |
250–375 |
|
M. adductor brevis |
1–2 |
50–75 |
250–375 |
|
M. adductor magnus |
1–3 |
50–75 |
250–375 |
|
M. gracilis |
1–2 |
50–75 |
250–375 |
|
M. biceps femoris |
2–3 |
50–75 |
250–375 |
|
M. semitendinosus |
1–2 |
50–75 |
250–375 |
|
M. semimembranosus |
1–2 |
50–75 |
250–375 |
|
M. soleus |
2 |
25–75 |
125–375 |
|
M. gastrocnemius |
4 (2x2) |
50–100 |
250–500 |
|
M. tibialis posterior |
2–3 |
50–75 |
125–375 |
|
M. flex. dig. longus |
2 |
50–75 |
125–250 |
|
M. tibialis anterior |
2 |
25–50 |
125–250 |
|
M. extensor hallucis |
1–2 |
25–50 |
100–150 |
|
M. flex. hall. longus |
1 |
20–30 |
100–150 |
|
M. flex. dig. brevis |
1 |
20–30 |
100–150 |
|
Gesamtdosis pro Sitzung |
< 500 |
<1500 |
|
|
Empfohlene Verdünnung |
2–5 ml/100 Units |
2–4 ml/500 Units |
|
Die Therapie mit BoNT A wird aufgrund der aktuellen Studienlage von der Deutschen Gesellschaft für Neurologie (DGN-Leitlinien) und dem Arbeitskreis Botulinumtoxin der Deutschen Gesellschaft für Neurologie für die lokale Behandlung behindernder oder schmerzhafter Auswirkungen von Spastik neben den zugelassenen Indikationen für folgende Bereiche empfohlen [20]:
- Bei spastischer Spitzfuß- und Inversionsstellung, die sich durch Schienen, orale Antispastika und physikalische Maßnahmen nicht beheben lässt
- Bei spinaler Adduktorenspastik, beispielsweise bei multipler Sklerose, zur Erleichterung pflegerischer Maßnahmen
- Bei der Spastik von Kindern mit kindlicher Zerebralparese zur Verbesserung des Stehens, Gehens und der Greiffunktion der Hände
- Zur Frührehabilitation der spastischen Fehlstellung an den Beinen, um dauerhafte Kontrakturen, Schmerzen und Sekundärschäden zu vermeiden
Idealerweise sollte BoNT A eingesetzt werden, bevor sich bei Spastizität eine behindernde Abnahme der Muskellänge mit Kontrakturen und Schmerzen in betroffenen Gelenken entwickeln kann [17].
Für den Erfolg einer BoNT-A-Behandlung sind allerdings neben der adäquaten Dosierung von BoNT A weitere Faktoren relevant: So ist die symptomadäquate Muskelauswahl für die BoNT-A-Injektion auf der Grundlage der Analyse des spastischen Bewegungs- oder Haltungsmusters essenziell. Es bedarf hierfür sowohl einer ausreichenden Erfahrung des behandelnden Arztes als auch ergänzend häufig der Kommunikation des Arztes mit den Physio- oder Ergotherapeuten und Pflegenden des Patienten. An den Zielen des Patienten orientiert sollte dann der Arzt auf der Basis seiner klinischen Untersuchung unter Einbezug der zur Verfügung stehenden Informationen die Muskelauswahl treffen und die Dosierungen festlegen. Für die genaue Lokalisation der Injektionen von BoNT A können dann Kontrollverfahren wie eine Sonographie oder Elektrostimulation notwendig sein, des Weiteren sollten zeitlich koordiniert synergistisch wirkende Therapiemaßnahmen zum Einsatz kommen.
Symptomadäquate Auswahl der Zielmuskeln für Botulinumtoxin A
Bei der Auswahl der Zielmuskeln kann wie bei BoNT-A-Injektionen zur Behandlung der fokalen Dystonien vorgegangen werden. Wie beim Torticollis spasmodicus analysiert der Behandler auch bei spastischen Bewegungsstörungen die auftretenden Bewegungen oder die bestehenden Haltungen und wählt aufgrund seiner funktionell anatomischen Kenntnisse die verursachenden Muskeln aus. Durch passives oder aktiv/passives Bewegen der entsprechenden spastischen Bewegungssegmente können weitere Zielmuskeln identifiziert werden. Muskeln, die bei dieser Tonusprüfung spastisch-rigid erscheinen, sind weitere Zielmuskeln für eine BoNT-A-Injektion. Zu berücksichtigen ist, dass die Ausprägung der Symptome nicht nur durch das individuelle Schädigungsmuster, sondern auch durch die Untersuchungssituation (horizontale vs. vertikale Position bei der Untersuchung) bestimmt wird, so dass eine Untersuchung in verschiedenen Ausgangslagen empfohlen wird [12, 17, 21].
Bei der in Deutschland zugelassenen Indikation der Behandlung einer Spastizität der oberen Extremität nach Schlaganfall ist die Auswahl der Muskeln nach folgendem Schema möglich: Beurteilt werden die passive und aktive Schulter-, Ellenbogen- und Handgelenksbewegung sowie die Pro- und Supination. Zusätzlich ist relevant, wie und ob der Daumen und die Langfinger mit in das spastische Muster einbezogen sind, ob eine spastische Faust, eine Krallenhand oder eine sogenannte Lumbrikalhand vorliegt und welche Bewegungen Schmerzen in dadurch gedehnten Muskeln auslösen [21].
Dosierung und Lokalisationskontrolle der Botulinumtoxin-Injektionen
Mit den drei BoNT-A-Produkten stehen hoch effektive Substanzen zur Verfügung, die bei ausreichender Dosierung (s. Tab. 1 und 2) und zielgerichteter Injektion den Tonus spastischer Muskeln dosisabhängig reduzieren können. Bei gewünschter hoher Selektivität der Injektion wird daher eine Injektionskontrolle, beispielsweise durch Elektrostimulation oder Sonographie, empfohlen [19]. Ausnahmen bilden etwa Patienten mit spastisch fixierter Faust, bei denen eine Differenzierung der am Unterarm zu injizierenden Fingerflexoren nicht zwingend erforderlich ist. In dieser Situation erscheint es gerechtfertigt, auf der Basis einer anatomisch lokalisierten Injektion beispielsweise den M. flexor digitorum superficialis und M. flexor digitorum profundus mit einer adäquaten BoNT-A-Dosis zu versorgen. Die exakte Lokalisation der BoNT-A-Injektion ist aber immer dann von Bedeutung, wenn eine funktionelle Verbesserung durch selektive Muskelblockaden angestrebt wird [19, 21].
Bei der sonographiegesteuerten Injektionstechnik besteht schon vor dem Einstich der Kanüle eine Übersicht über das Injektionsgebiet und erlaubt, den Einstich zu planen. Hier kann das Toxin unter visueller Kontrolle zielgenau auch in schwer erreichbare, tiefer gelegene Muskeln wie beispielsweise den M. flexor pollicis longus injiziert werden [19, 21]. Das injizierte Volumen und der Injektionsort lassen sich dabei zeitsynchron verfolgen und exakt dokumentieren (Sonobild vor und nach Injektion). Eine zielgenaue Injektion hat möglicherweise auch den grundsätzlichen Vorteil, dass über die Injektion in die Mitte des Muskelbauches und Verwendung kleinerer Injektionsvolumina die Diffusion von BoNT A besser abgeschätzt/gesteuert werden kann. Je größer die injizierten Volumina sind und je ungenauer die Injektion im Muskel lokalisiert wurde, desto höher ist die Wahrscheinlichkeit der Wirkungsausbreitung von BoNT A am Injektionsort, aber auch über den Injektionsort hinaus [1].
Nebenwirkungen einer Behandlung mit Botulinumtoxin A
Aufgrund kontrollierter randomisierter Studien zur Behandlung der Spastizität kann die BoNT-A-Behandlung als sicher und nebenwirkungsarm bezeichnet werden [14]. In diesen Untersuchungen zeigte sich, dass BoNT A im Vergleich zu Plazebo nur lokale Paresen im Injektionsareal bei höherer Dosierung als lokale Nebenwirkung signifikant häufiger aufwies. Wie bei allen intramuskulären Injektionen können diese selbst schmerzhaft sein und sie können zu kleineren Hämatomen führen. In Einzelfällen wurde bei sehr hohen Dosierungen (Dosis pro Sitzung von über 500 Units Botox® und 1500 Units Dysport®) oder fakultativ nicht intramuskulären Injektionen von BoNT A über Zeichen einer systemischen Verteilung wie Schluckstörungen, Mund- und Augentrockenheit, Blasenentleerungsstörungen, Motilitätsstörungen der Gallenblase und eine allgemeine Muskelschwäche berichtet.
Bisher sind keine prospektiven Zahlen zur Antikörperbildung (AK) gegen BoNT bei der Behandlung der spastischen Bewegungsstörung mitgeteilt worden. Bei zervikaler Dystonie wird aufgrund von retrospektiven Analysen berichtet, dass in Abhängigkeit von der kumulativen Gesamtdosis (je höher die kumulative Gesamtdosis, desto höher das AK-Risiko) und sogenannten Boosterinjektionen (Injektionsintervalle von unter 6 Wochen) im Durchschnitt bei etwa 2 bis 5% der behandelten Patienten eine Antikörperbildung auftritt [14]. Es wird prospektiven Studien vorbehalten bleiben, zur Klärung der Frage beizutragen, wie häufig neutralisierende Antikörper mit den verschiedenen Produkten bei der Spastizitätsbehandlung auftreten.
Wirksamkeitssteigerung durch adjuvante Therapien
Die Effizienz des injizierten BoNT A scheint sich durch zeitlich abgestimmte Therapien und Maßnahmen noch weiter verbessern zu lassen. Der wissenschaftliche Hintergrund dieser Empfehlungen basiert auf den Erkenntnissen zum BoNT-A-Rezeptor namens SV2. Dieser ist in der motorischen Endplatte im Acetylcholin-tragenden Vesikel lokalisiert und wird erst bei Verschmelzung des Vesikels mit der Membran an der Oberfläche präsentiert. Daraus ergibt sich, dass nur Synapsen, die Acetylcholin abgeben, also aktiv sind, BoNT A binden und damit aufnehmen können. Demzufolge ist die Kooperation mit Physio- und Ergotherapeuten zunehmend wichtiger, da diese beispielsweise angehalten werden können, das pathologische spastische Muster unmittelbar nach der BoNT-A-Injektion zu provozieren, um so zur Steigerung der BoNT-Bindung am Rezeptor, der Aufnahme und damit Wirksamkeit des injizierten Toxins beizutragen. Auf der Basis der Erkenntnis, dass nur aktive Synapsen BoNT A aufnehmen [10], erklären sich auch Ergebnisse einer Studie mit Schreibkrampfpatienten, die zeigt, dass das injizierte Toxin bei der Sicherstellung einer Muskelaktivität direkt nach der Injektion effektiver wirksam werden kann [5]. In weiteren Arbeiten konnte unter anderem gezeigt werden, dass durch Elektrostimulation der injizierten Muskeln mehr Toxin aufgenommen wird. So zeigten Hesse et al., dass zeitlich um die Injektion applizierte Elektrostimulation der behandelten Muskulatur die Effektivität des injizierten Toxins steigern kann [9]. Im direkten Vergleich zeigte jedoch die dynamische Redression eine Überlegenheit gegenüber der alleinigen Elektrostimulation [4].
Synergistische Wirkung von Botulinumtoxin A und Redressionsmaßnahmen
Spastische Muskeln zeigen bereits nach kurzer Zeit biomechanische Veränderungen mit einer Tendenz zur Muskelverkürzung und Erhöhung des viskoelastischen Widerstands bei passiver Dehnung [7]. Auf der Basis dieser bereits in den 80er Jahren des 20. Jahrhunderts publizierten Ergebnisse hat die Kombination einer Redression (Dehnung im Kunststoff-Cast) mit BoNT-A-Injektionen möglicherweise einen besonderen Stellenwert. Für den kombinierten Einsatz der Redression und BoNT-A-Injektionen kann ein synergistischer Effekt angenommen werden. Diese Vermutung stützt sich auf pathophysiologische Überlegungen zur Spastizität, nach denen unterschiedliche „Spastik-Komponenten“ (Abb. 1a) zu der komplexen Bewegungsstörung beitragen und daher auch differenziert zu behandeln sein könnten [6, 8].
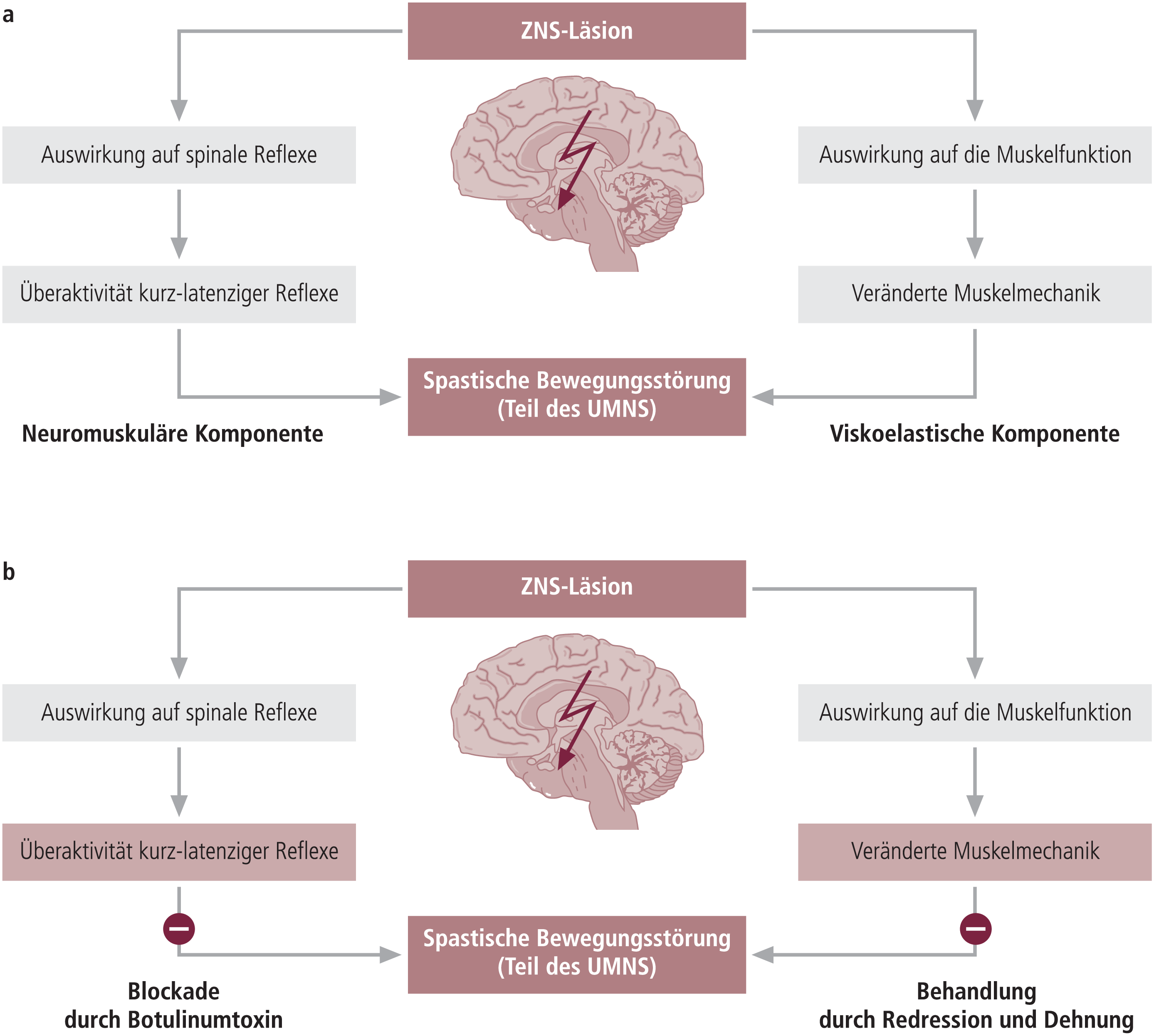
Abb. 1. Spastik-Komponenten und deren Behandlung
Ausgehend von der Definition von Lance [11] handelt es sich bei der Spastik um eine Bewegungsstörung, die eine geschwindigkeitsabhängige Übererregbarkeit der muskulären Reaktion auf passive Muskeldehnung zeigt [16]. Dabei wird diese spastische Bewegungsstörung als Teil des Pyramidenbahnsyndroms (Upper motor neuron syndrome = UMNS) charakterisiert [22]. Diese Definition fokussiert auf die sogenannte neuromuskuläre Reflexkomponente, die aus einer Enthemmung von kurz-latenzigen spinalen Reflexen beim UMNS resultiert. Aus heutiger Sicht erscheint es erforderlich, in die Überlegungen zur Therapie der Spastizität auch die auftretenden Veränderungen der passiv-mechanischen (viskoelastischen) Eigenschaften der Muskulatur zu integrieren [7]. Bei chronischer Spastizität resultieren langfristig immer auch strukturelle Veränderungen der Muskulatur, die zu veränderten viskösen Eigenschaften und potenziell zu einer Muskelverkürzung („viskoelastische Komponente“) führen [6]. Als Ursache dieser viskösen Veränderungen wird derzeit unter anderem eine dauerhaft pathologisch veränderte Aktivierung des Muskels über das Alpha-Motorneuron diskutiert.
Für funktionelle Verbesserungen sind demnach neben der Reduktion des gesteigerten Muskeltonus bei passiver Dehnung („neuromuskuläre Komponente“) auch Verbesserungen der muskulo-skelettalen Voraussetzungen (Behandlung der „viskoelastischen Komponente“) bedeutsam [4, 6, 21]. Die kombinierte Therapie BoNT A und Redression will beide Komponenten beeinflussen (Abb. 1b). So könnte beispielsweise eine Injektion von BoNT A die Folgen einer dauerhaft pathologischen Information zum Muskel korrigieren und die gesteigerten Muskeleigenreflexe sowie die Muskeltonuserhöhung (die „neuromuskuläre Komponente“ des spastischen Syndroms) abschwächen. Mindestens gleich bedeutsam erscheint die Behandlung einer zunehmenden Behinderung durch eine spastische Muskelverkürzung mit einer adäquaten Redression [6]. Durch eine kombinierte und frühe Behandlung können möglicherweise negative Auswirkungen wie Kontraktions-Dekontraktions-Verlangsamungen beeinflusst und ein höherer Grad der Funktionsbesserung im Verlauf erzielt werden. Zusammenfassend erscheint die Kombination von BoNT A mit Redressionen in der differenziellen Behandlung der Spastizität sinnvoll und wird sowohl für die ambulante als auch die stationäre Behandlung empfohlen [20, 21].
Behandlung der Spastizität im multiprofessionellen Team
Im Lichte des Ausgeführten sollte die fokale Behandlung von Behinderungen durch Spastizität am besten durch ein multiprofessionelles Team erfolgen, das neben dem auf die Behandlung der Spastik und Botulinumtoxin spezialisierten Arzt den Ergo- und Physiotherapeuten, das Pflegepersonal oder die pflegenden Angehörigen sowie einen spezialisierten Therapeuten für die Redressionsbehandlung integriert (Abb. 2) [20]. Im Mittelpunkt dieses Behandlungskonzepts stehen die mit dem Patienten erarbeiteten realistischen Behandlungsziele, die durch Umsetzung eines über 24 Stunden pro Tag geplanten Behandlungskonzepts erreicht werden sollen. Alle Therapieziele sollten gemeinsam mit dem Patienten, den Pflegenden und dem multiprofessionellen Team definiert werden. Dabei sollte ein realistisches kurz- bis mittelfristig erreichbares Ziel, beispielsweise die Reduktion begleitender Schmerzen, mit übergeordneten Zielen, wie der Verbesserung der passiven Gelenkbeweglichkeit und Erleichterung des Ankleidens, verständlich mit Patient und Angehörigen vereinbart werden.
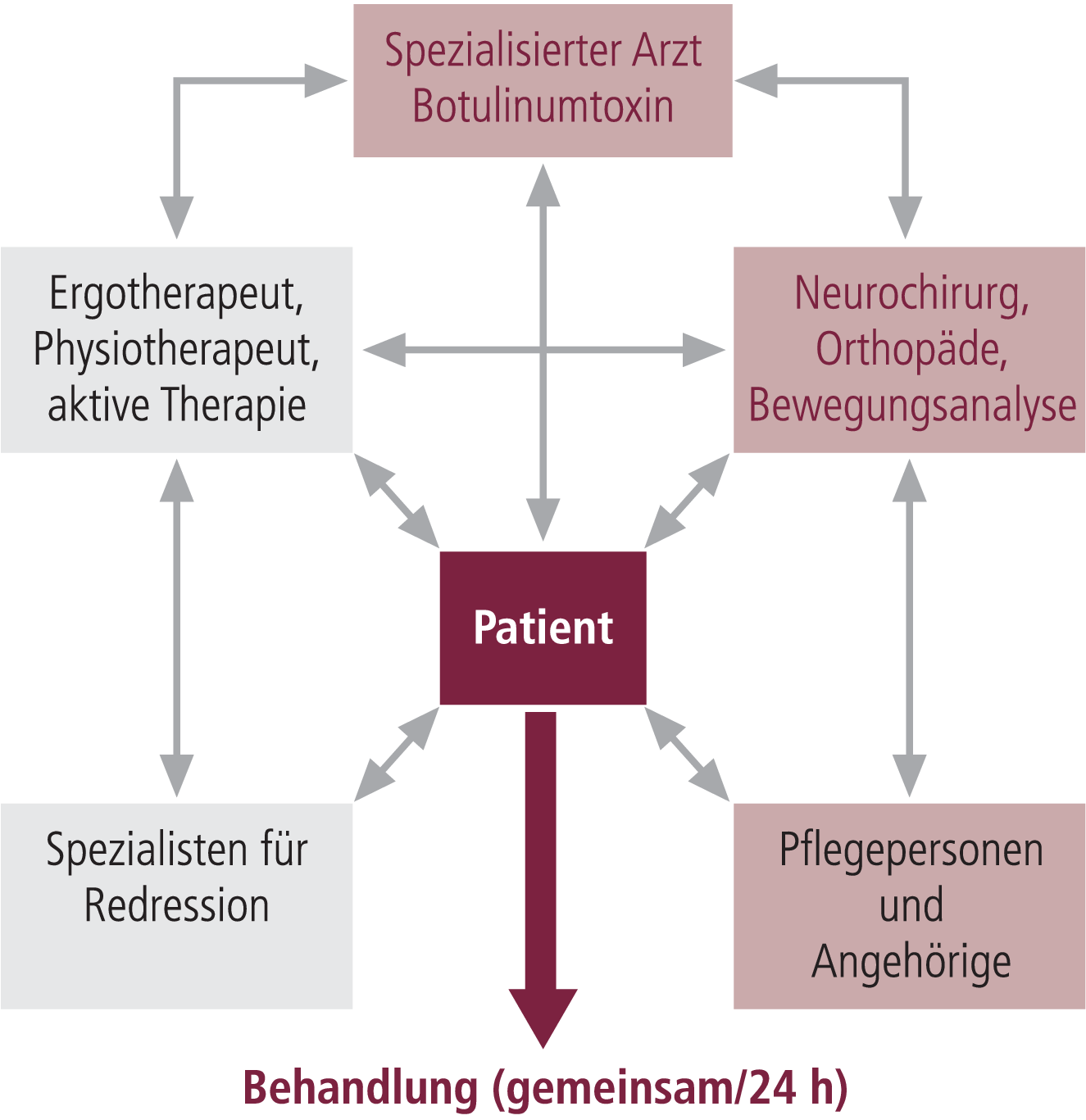
Abb. 2. Das multiprofessionelle Team zur Spastik-Behandlung
Die Erleichterung der Pflege und Körperhygiene, die Verbesserung der passiven und aktiven Gelenkbeweglichkeiten und die Verbesserung von motorischen Funktionen können dabei fokussiert werden. Im Vorfeld einer lokalen Behandlung der Spastizität mit BoNT A sollte außerdem sichergestellt werden, dass der Patient ausreichend für die Behandlungsschritte motiviert ist [20, 21].
Interessenkonflikt
Der Autor hat Förderungen für klinische Studien und Honorierungen von Vorträgen durch alle Botulinumtoxin-A-Hersteller (Pharm Allergan, Ipsen Pharma, Merz Pharma) erhalten.
Literatur
1. Aoki KR. Pharmacology and immunology of botulinum toxin serotypes. J Neurol 2001;248(Suppl 1):3–10.
2. Bakheit M, Thilmann AF, Ward AB, et al. A randomised, double blind, placebo controlled, dose ranging study to compare the efficacy and safety of three doses of botulinum toxin type A (Dysport) with placebo in upper limb spasticity after stroke. Stroke 2000;31:2402–6.
3. Brashear A, Gordon MF, Elovic E, et al. Intramuscular injection of botulinum toxin for the treatment of wrist and finger spasticity after stroke. N Engl J Med 2002;347:395–400.
4. Carda S, Molteni F. Taping versus electrical stimulation after botulinum toxin type A injection for wrist and finger spasticity. A case-control study. Clin Rehabil 2005;19:621–6.
5. Chen R, Karp BI, Goldstein SR, et al. Effect of muscle activity immediately after botulinum toxin injection for writer’s cramp. Mov Disord 1999;14:307–12.
6. Dietz V. Proprioception and locomotor disorders. Nat Rev Neurosci 2002;3:781–90.
7. Dietz V, Berger W. Normal and impaired regulation of muscle stiffness in gait: a new hypothesis about muscle hypertonia. Exp Neurol 1983;79:680–7.
8. O’Dwyer NJ, Ada L, Neilson PD. Spasticity and muscle contracture following stroke. Brain 1996;119:1737–49.
9. Hesse S, Reiter F, Konrad M, et al. Botulinum toxin type A and short-term electrical stimulation in the treatment of upper limb flexor spasticity after stroke: a randomised, double-blind, placebo-controlled trial. Clin Rehabil 1998;12:381–8.
10. Jahn R. A neuronal receptor for Botulinum toxin. Science 2006;312:S40–1.
11. Lance JW. Symposium synopsis. In: Feldman RG, Young RR, Koella WP (eds.). Spasticity: disordered motor control. Chicago: Year Book Medical Publishers, 1980:485–94.
12. Sheean GL. Pathophysiology of spasticity. In: Sheean G (ed.). Spasticity rehabilitation. London: Churchill Communications Europe Ltd., 1998:17–38.
13. Simpson DM, Alexander DN, O’Brin CF, et al. Botulinum toxin type A in the treatment of upper extremity spasticity: a randomised, double-blind, placebo-controlled trial. Neurology 1996;46:1306–10.
14. Simpson DM, Gracies JM, Graham HK, et al. Assessment: Botulinum neurotoxin for the treatment of spasticity (an evidence-based review): Report of the Therapeutics and Technology Assessment Subcommittee of the American Academy of Neurology. Neurology 2008;70:1691–8.
15. Snow BJ, Tsui JKC, Bhatt MH, et al. Treatment of spasticity with botulinum toxin A: double-blind study. Ann Neurol 1990;28:512–5.
16. Thilmann AF, Fellows SJ, Garms E. The mechanism of spastic muscle hypertonus: variation in reflex gain over the time course of spasticity. Brain 1991;114:233–44.
17. Ward AB. A summary of spasticity management – a treatment algorithm. Eur J Neurol 2002;9(Suppl 1):48–52.
18. Wissel J, Müller J, Dressnandt J, et al. Management of spasticity associated pain with botulinum toxin A. J Pain Symptom Manage 2000;20:44–9.
19. Wissel J, Müller J, Poewe W. Electromyography for identification of dystonic and spastic muscles and techniques for guidance of injections. In: Moore AP, Naumann M (eds.). Handbook of botulinum toxin treatment. 2nd edition. Oxford: Blackwell Science, 2002.
20. Wissel J, Benecke R, Erbguth F, et al. Konsensus-Statement des Arbeitskreises Botulinumtoxin e. V. der DGN (AkBoTx) zur fokalen Therapie der Spastizität mit Botulinumtoxin Typ A. Neurol Rehabil 2003;9:242–3.
21. Wissel J, Fheodoroff K, Huber M. Blue Book Spasticity: Behandlung der Spastizität mit Botulinumtoxin. Grundlagen – Klinik – Atlas – Skalen. München, Potsdam: Child & Brain, 2004.
22. Young RR. Spasticity: a review. Neurology 1994;44(Suppl 9):12–20.
Ao. Univ.-Prof. Dr. med. Jörg Wissel, Neurologische Rehabilitationsklinik Beelitz-Heilstätten, Kliniken Beelitz GmbH, Paracelsusring 6A, 14547 Beelitz-Heilstätten, E-Mail: wissel@rehaklinik-beelitz.de
Botulinum toxin A injection – method of choice in the therapy of focally disabling spasticity
Intramuscular botulinum toxin A (BoNT A) injections are the method of choice in the treatment of spastic and dystonic syndromes with focally disabling consequences. Their main aims are to relieve disabling spastic disturbances of posture and movement as well as accompanying pain, to overcome obstacles to care and hygiene, and thus to improve the quality of life of the patient. Prior to treatment, realistic treatment aims should be discussed with the patient or the caring relatives.
The muscles to be injected are selected due to clinical features; accuracy of the injections should be controlled by sonography or electrical stimulation. The therapeutic aims must be adjusted with the accompanying therapeutic team in oder to achieve maximum efficiency by coordinated treatment measures. By temporally coordinated action, the efficacy may be improved further. Based on the knowledge of receptor-mediated binding and cellular entry of BoNT A, it is recommended to provoke spasticity in the injected segment in close temporal association (within minutes of hours after injection), e.g. by passive distension or activation of the antagonistic muscle, in order to achieve binding of the toxin at the “spasticity-eliciting synapses”. Furthermore, in the weeks after BoNT A injection, distensions should be applied by splints or bandages and active neurorehabilitative therapies (physical therapy, occupational therapy, electrical stimulation) in order to invigorate antagonist coordination. The coordinated application of local BoNT A injections and modern neurorehabilitative therapies may allow to achieve a functionally relevant outcome more often.
Key words: Spasticity, stroke, focal therapy, botulinum toxin type A, multiprofessional team, sonographically navigated injection technique
Psychopharmakotherapie 2009; 16(01)
