Walter S. Fuchs, Roland Seifert, Erich Schneider, David Schnell und Ekkehard Haen, Regensburg, für die AGATE*
Schwer wiegende Blutbildveränderungen wie Granulozytopenien und Agranulozytosen sind als bekannte Nebenwirkungen verschiedener Psychopharmaka einzustufen. Speziell das atypische Neuroleptikum Clozapin, aber auch die gesamte Klasse der Phenothiazine stehen mit einer Inzidenz von etwa 0,8% für Agranulozytosen und rund 3% für Leukopenien im Mittelpunkt einer kritischen Therapieüberwachung durch den Arzt [13]. Beobachtet wird in diesen Fällen im Laufe der Medikation ein drastisches Absinken der Leukozytenzahlen auf unter 3000 Leukozyten/µl Blut bei der Leukopenie und im Extremfall auf unter 500 Leukozyten/µl Blut im Fall der Agranulozytose [12]. Mit dem Zusammenbruch der körpereigenen Abwehr gehen dann bakterielle und virale Infektionen sowie ein Pilzbefall bis hin zur Sepsis einher [3].
Aufgrund dieses lebensbedrohlichen Risikos und seiner kreislaufdepressiven Wirkung sind bei der Einstellung eines Patienten auf Clozapin regelmäßige Blutbildkontrollen und eine Dosistitration beginnend mit einer „Testdosis“ von 12,5 mg mit schrittweiser Erhöhung von 25 bis 50 mg/d bis zu einer maximalen Tagesdosis von 1000 mg zwingende Notwendigkeit [10]. Als Voraussetzung für einen Therapiebeginn schreibt das Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM) ein Differenzialblutbild mit unauffälligen Leukozytenzahlen (>3500/µl Blut) vor. Im weiteren Therapieverlauf wird eine wöchentliche Kontrolle der Leukozyten und neutrophilen Granulozyten während der ersten 18 Wochen und danach mindestens alle 4 Wochen während der gesamten Therapiedauer gefordert [13]. Analog dazu schreibt die amerikanische Gesundheitsbehörde (FDA) wöchtliche Kontrollen über die ersten 24 Wochen gefolgt von zweiwöchentlichen Kontrollen für weitere 6 Monate und danach monatliche Blutbildkontrollen für Leukozyten und neutrophile Granulozyten vor [4, 13].
Bedingt durch diese engmaschigen Blutbildkontrollen, eine strenge Indikationsstellung und die Verfügbarkeit der Granulozyten-koloniestimulierenden Faktoren (G-CSF) sind heute schwerwiegende unerwünschte Arzneimittelwirkungen seltener und gut therapierbar geworden. Durch eine gelockerte Verschreibungspraxis, eine Öffnung der Vertriebskanäle und die neuerliche generische Verfügbarkeit hat Clozapin den Weg vom psychiatrischen Krankenhaus in die allgemeinmedizinische Praxis gefunden. Ziel dieser Arbeit ist es deshalb, aktuelle und an einem größeren Patientenkollektiv erhobene Daten über Häufigkeit und zeitlichen Verlauf dieser lebensbedrohlichen Nebenwirkung zu sammeln um daraus aktualisierte Sicherheitshinweise für die Therapie abzuleiten.
Patienten und Methoden
Im Rahmen eines Qualitätssicherungsprogramms für die Psychopharmakotherapie erfasst und dokumentiert die AGATE (Arbeitsgemeinschaft Arzneimitteltherapie bei psychiatrischen Erkrankungen) schwere unerwünschte Wirkungen von Arzneimitteln (UAW). Insgesamt partizipieren derzeit 32 psychiatrische Versorgungskrankenhäuser und 2 Qualitätszirkel niedergelassener Psychiater an diesem Verbundsystem zur Verbesserung der Sicherheit der Arzneimitteltherapie. Die monatlich stattfindende Auswertung und Bewertung der gemeldeten UAW wird in einer Datenbank hinterlegt. Dokumentiert sind neben personenbezogenen Daten Zeitpunkt, Dauer der UAW, Name und Tagesdosis der applizierten Pharmaka, Grund- und Begleiterkrankungen des Patienten, anamnestische Besonderheiten, Veränderungen von Laborparametern, Verlauf und Therapie der UAW. Als Definition der Leukopenie und der Agranulozytose wurde eine Leukozytenzahl von weniger als 3000 bzw. weniger als 500 Leukozyten/µl Blut im peripheren Blutbild herangezogen und entspricht damit allgemein anerkannten Kriterien [3, 12]. Die Messung der Leukozytenzahlen erfolgte mit allgemein üblichen Laborverfahren.
Die Definition des Wahrscheinlichkeitsgrads der UAW zeigt Tabelle 1.
Tab. 1. Definition des Wahrscheinlichkeitsgrads für UAW
|
Zusammenhang mit der |
Kriterien |
|
Kein Zusammenhang |
|
|
Möglich |
Für das in Frage kommende Medikament: –ungewöhnliche UAW –ungewöhnlicher Zeitverlauf Wahrscheinlichkeit einer anderen Ursache >50% |
|
Wahrscheinlich |
Für das in Frage kommende Medikament: –Bekannte UAW –Mit der bisherigen Erfahrung übereinstimmender Zeitverlauf Wahrscheinlichkeit einer anderen Ursache <50% |
|
Sicher |
Analog „wahrscheinlich“, aber zusätzlich: Erneutes Auftreten der UAW nach Reexposition |
|
Nicht beurteilbar |
Ergebnisse, deren Zusammenhang völlig unklar ist und die damit nicht beurteilbar sind |
|
Wirkstoffkombination |
Obige Ereignisse aufgrund der Kombination mehrerer Wirkstoffe |
Ergebnisse
Im untersuchten Zeitrahmen von 1992 bis 2005 erfolgte die Meldung von insgesamt 2002 Fällen unerwünschter Arzneimittelwirkungen durch die AGATE-Kooperationspartner. Der Anteil der UAW „Leukopenie“ und „Agranulozytose“ lag bei diesem Gesamtkollektiv bei 43 bzw. 28 Fällen. Abbildung 1 zeigt alle Psychopharmaka, die für die beiden Nebenwirkungen nach Beurteilung der AGATE als „wahrscheinlich“ oder „möglich“ ursächlich verantwortlich eingestuft wurden. Sowohl hinsichtlich der Gesamtzahl der Blutbildveränderungen von 21 UAW als auch hinsichtlich der schwerwiegenden Agranulozytose mit insgesamt 13 Fällen nahm Clozapin eine exponierte Position innerhalb der verordneten Medikation der psychiatrischen Patienten ein. Eine Auswertung der eingesetzten Komedikation zeigte, dass das Ereignis „Agranulozytose“ in allen Fällen durch die AGATE-Fachgutachter auf Clozapin zurückgeführt wurde. Im Fall von Clozapin wurde in allen Fällen der Wahrscheinlichkeitsgrad für die UAW mit „wahrscheinlich“ angegeben. In absteigender Reihenfolge bezüglich beider UAW folgten die Substanzen Carba- mazepin, Olanzapin, Mianserin, Levomepromazin und Quetiapin. Auffällig oft waren hier schwerwiegende Agranulozytosen für die Substanzen Carbamazepin und Mianserin mit vier bzw. sechs Fällen zu beobachten. Als Verursacher von ein bis maximal drei Ereignissen wurde eine Vielzahl von Psychopharmaka identifiziert. Nicht in der Grafik gezeigt sind Einzelfälle, bei denen Antibiotika, Schilddrüsentherapeutika und Sulfonamide die beiden UAW auslösten.
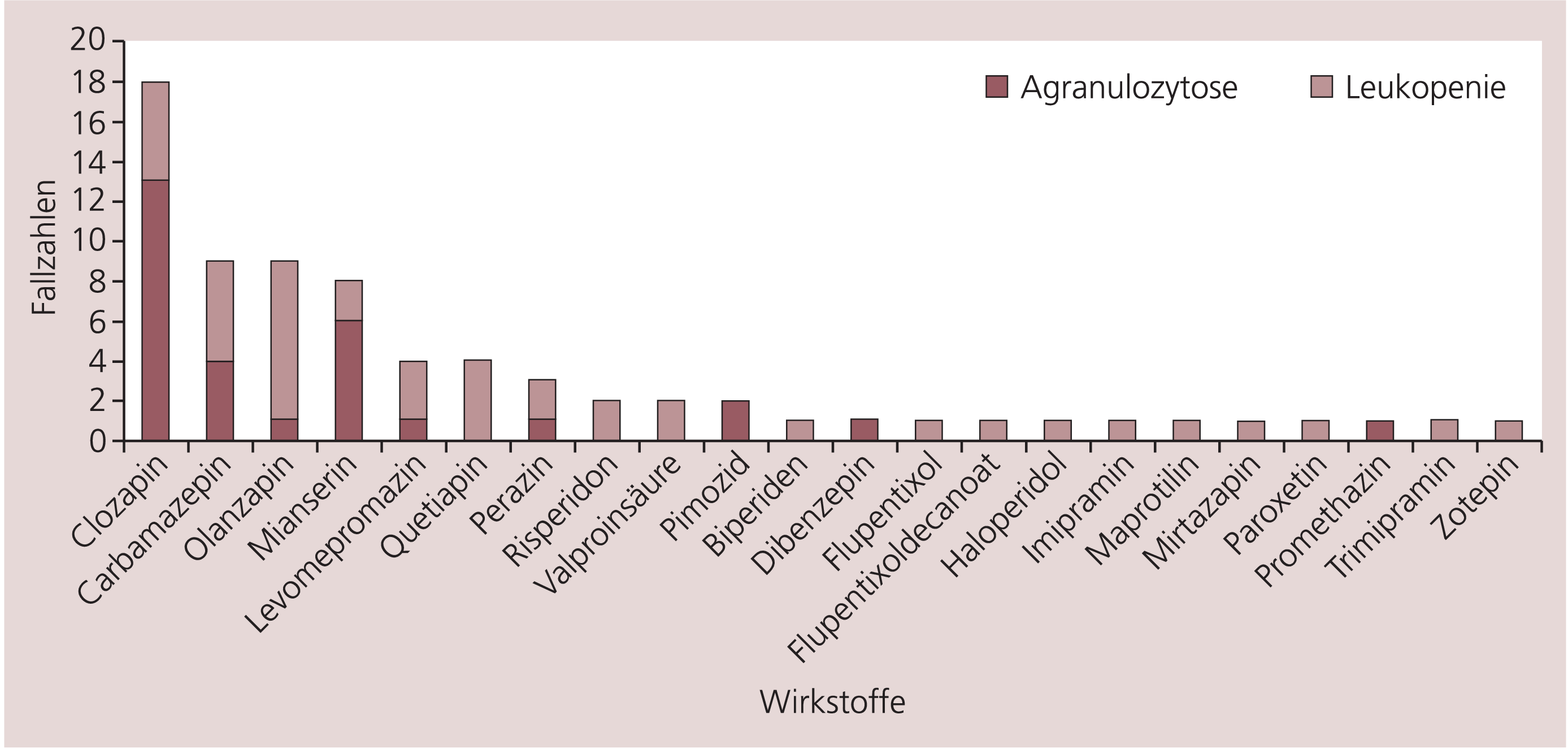
Abb. 1. Agranulozytose und Leukopenie unter Psychopharmaka in den AGATE-Kliniken 1992 bis 2005
Bezüglich des zeitlichen Verlaufs der durch Clozapin induzierten Agranulozytose ergab sich ein heterogenes Bild (Tab. 2). In zwei Fällen trat die Diagnose „Agranulozytose“ innerhalb des ersten Therapiemonates auf, während die meisten Fälle ein bis zwei Monate nach Therapiebeginn beobachtet wurden. Nach diesem zeitlichen Maximum löste Clozapin auch in den folgenden Monaten in Einzelfällen Agranulozytosen aus. Im beobachteten Extremfall vergingen seit der erstmaligen Einnahme 22 Monate bis zur Diagnose der UAW. Als Tagesdosis wurde in allen Fällen mindestens 200 mg/d appliziert (Tab. 3). Ab dieser Schwellendosis war diese UAW in allen höheren Dosierungsstufen anzutreffen. Eine Kumulation der Fälle bei den höheren Dosierungen konnte nicht festgestellt werden.
Tab. 2. Einnahmedauer von Clozapin bis zur UAW Agranulozytose
|
Einnahmedauer [Monate] |
Neue Agranulozytose-Fälle [n] |
|
1 |
2 |
|
2 |
6 |
|
4 |
1 |
|
7 |
1 |
|
10 |
1 |
|
17 |
1 |
|
>17 |
1 |
Tab. 3. Clozapin-Tagesdosis bis zur UAW Agranulozytose
|
Tagesdosis |
Agranulozytose-Fälle |
|
200 |
3 |
|
201–400 |
5 |
|
401–600 |
4 |
|
601–800 |
1 |
Die eingeleiteten klinischen Maßnahmen nach der Diagnose Leukopenie (Tab. 4) und Agranulozytose (Tab. 5) unterschieden sich deutlich. In 2% der Fälle konnte die Therapie mit Clozapin bei einer Leukopenie fortgeführt werden. Ein Absetzen der Medikation war in 89% der Fälle ausreichend, die Leukozytenzahlen zu normalisieren. Eine engmaschige Überwachung nach Absetzen der Medikation durch einen stationären Aufenthalt oder medikamentöse Gegenmaßnahmen waren dagegen in 2% bzw. 7% der Fälle angezeigt.
Tab. 4. Klinische Maßnahmen nach Leukopenie
|
Absetzen, kein stationärer Aufenthalt |
89% |
|
Absetzen, medikamentöse Gegenmaßnahmen |
7% |
|
Absetzen, stationärer Aufenthalt |
2% |
|
Weiterbehandlung mit dem jeweiligen Medikament |
2% |
Tab. 5. Klinische Maßnahmen nach Agranulozytose
|
Absetzen, kein stationärer Aufenthalt |
29% |
|
Absetzen, medikamentöse Gegenmaßnahmen |
21% |
|
Absetzen, stationärer Aufenthalt |
46% |
|
Medikamentöse Gegenmaßnahmen, Intensivstation |
4% |
Bei einer aufgetretenen Agranulozytose erwies sich ein singuläres Absetzen der Medikation in 29% der Fälle als therapeutisch ausreichend. Eine medikamentöse Intervention nach Absetzen war in 21% erforderlich. Mit 46% der Fälle mussten allerdings fast die Hälfte der Patienten stationär behandelt werden oder in 4% der Fälle auf die Intensivstation verlegt werden.
Als Therapie für beide UAW wurde in 36,5% der Fälle eine symptomorientierte Therapie mit verschiedenen Antibiotika gewählt, während eine kausale Therapie mit Granulozyten-koloniestimulierendem Faktor (G-CSF) in 69,2% der Fälle zur Anwendung kam.
Diskussion
Arzneimittelinduzierte Leukopenien oder im Extremfall Agranulozytosen sind besonders für Analgetika (Metamizol, Paracetamol), Sulfonamide, Schilddrüsentherapeutika und Psychopharmaka bekannte unerwünschte Arzneimittelwirkungen [3]. Durch das infektionsbedingte erhöhte Gefährdungspotenzial der Patienten geht man bei diesen arzneimittelinduzierten Blutbildveränderungen von einer Sterblichkeit von bis zu 10% aus. Speziell im Fall von Clozapin wurde das Risiko als so gravierend eingeschätzt, dass die Substanz in den USA zeitweise vom Markt genommen wurde [9]. Die überlegene antipsychotische Wirkung ohne extrapyramidal-motorische Nebenwirkungen und der sehr geringe Prolactin-Anstieg dieser Substanz haben aber zum erneuten Markteintritt geführt. In Europa ist eine Renaissance dieses ersten „atypischen“ Neuroleptikums durch den inzwischen erfolgten Patentablauf und die Verfügbarkeit als Generikum zu erwarten.
Untersuchungen über die Pathogenese dieser arzneimittelinduzierten Agranulozytosen werden dadurch erschwert, dass oft nur einzelne Kasuistiken für weitergehende Untersuchungen zur Verfügung stehen oder die Besserung des Patienten Untersuchungen unmöglich macht [3]. Die Daten aus dem großen Kollektiv aller süddeutschen Bezirkskrankenhäuser mit über 2000 Meldungen an unerwünschten Arzneimittelwirkungen ist daher von großem Wert für die Einschätzung des diesbezüglichen Gefährdungspotenzials. Das Risiko einer Agranulozytose nach Clozapin ist gut belegt und variiert in der Literatur zwischen 0,05% und 2% der Patienten [1, 5]; aktuelle Daten ermitteln einen noch engeren Bereich zwischen 0,5% [8] und 1% [3] der behandelten Patienten. Dieses hohe Risikopotenzial findet sich auch in unseren Daten wieder. Mit insgesamt 18 Fällen führt das Dibenzodiazepin Clozapin die Liste der kritischen Substanzen im beobachteten Zeitraum an. Auch bezüglich der schwerwiegenden Agranulozytosen nimmt Clozapin mit 13 Fällen eine exponierte Position ein.
Für die strukturverwandten Substanzen Olanzapin als Thienobenzodiazepin und Mianserin [8] wurde mit insgesamt 9 bzw. 8 Fällen ebenfalls eine Häufung beider unerwünschten Arzneimittelwirkungen registriert. Diese Daten stehen allerdings im Widerspruch zur Literatur, die zumindest für Olanzapin ein erhöhtes Risiko einer Agranulozytose – auch bei hohen Behandlungszahlen – negiert [8]. Allerdings konnte für Olanzapin nur in einem Fall eine schwerwiegende Agranulozytose und in den 8 verbleibenden Fällen Leukopenien festgestellt werden. Zu berücksichtigen ist außerdem, dass Olanzapin nicht im Rahmen einer Monotherapie eingesetzt wurde.
Die Mehrzahl der Agranulozytosefälle bei Clozapin wurden 1 bis 2 Monate nach Therapiebeginn diagnostiziert. Ein annähernd analoges Zeitfenster von 1 bis 3 Monaten beschreiben auch andere Autoren, die allerdings nur ein geringes Risikopotenzial für diese unerwünschte Arzneimittelwirkung nach einer Einnahmedauer von mehr als 6 Monaten sehen [5]. Bei den Patienten dieser Untersuchung waren auch noch zu späteren Zeitpunkten bis maximal 22 Monate nach Therapiebeginn Einzelfälle mit der Nebenwirkung Agranulozytose festzustellen. Dieses Ergebnis unterstreicht die Notwendigkeit einer regelmäßigen Kontrolle der Leukozyten und neutrophilen Granulozyten alle 4 Wochen während der gesamten Behandlungszeit.
Festgestellt wurde in allen Fällen eine Koinzidenz zwischen einer Dosissteigerung im Rahmen der Neueinstellung oder Therapieoptimierung und dem Auftreten einer Agranulozytose. Abbildung 2 zeigt eine repräsentative Kasuistik für die Entwicklung der Leukozytenzahlen unter einer Clozapin-Therapie. Die Leukozytenzahlen blieben während der Dosistitration beginnend mit 12,5 mg/d bis hin zur optimalen Therapiedosis annähernd konstant und brachen erst nach Erreichen einer „Schwellendosis“ von 200 mg/d dramatisch ein. Diese Schwellendosis war auch in allen anderen Fällen bei dem Auftreten der Agranulozytose erreicht oder überschritten. Bei Annahme einer linearen Beziehung zwischen Dosis und resultierenden Blutspiegeln [2, 9] lassen diese Daten einen Zusammenhang zwischen Clozapin-Serumkonzentration und Agranulozytose vermuten. Dieses Ergebnis steht allerdings im Widerspruch zu Daten, die keinen Zusammenhang zwischen Agranulozytose und Clozapin-Serumkonzentration sehen [6]. Eine endgültige Klärung dieser Frage erschwert die nur geringe Dosislinearität bedingt durch große interindividuelle Varianz der Clozapin-Pharmakokinetik sowie das Fehlen einer systematischen Bestimmung von Clozapin-Blutspiegeln in dieser Untersuchung. Dosissteigerungen über 200 mg/d sollten in jedem Fall unter engmaschiger Kontrolle der Leukozytenzahlen durchgeführt werden. Problematisch ist in diesem Zusammenhang, dass die ermittelte „kritische Schwellendosis“ für die UAW Agranulozytose am unteren Rand des optimalen therapeutischen Dosisbereichs von 200 bis 400 mg/d Clozapin [11] liegt und damit die Dosis bis hin zur Maximaldosis von 1000 mg/d nicht optimal ausgenutzt werden kann.
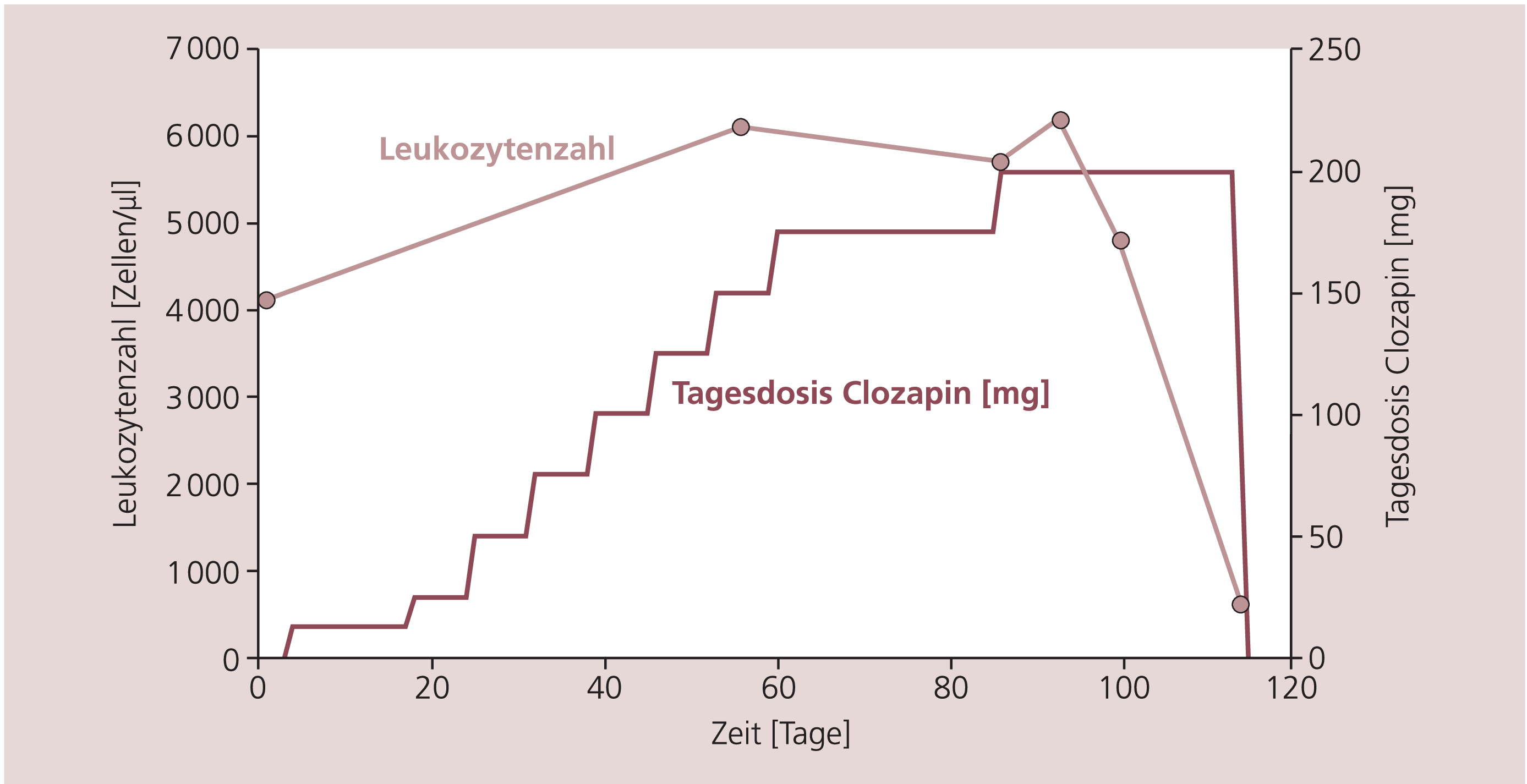
Abb. 2. Entwicklung der Leukozytenzahl nach Clozapin-Gabe (Fallbeispiel)
Die Therapie der arzneimittelinduzierten Agranulozytose konzentriert sich heute auf die Gabe von Granulozyten-koloniestimulierenden Faktoren, die eine Zeitverkürzung bis zur Erholung der Leukozytenzahlen sicherstellen. Aufgrund der geringen Patientenzahlen fehlt zwar bisher der Beleg der Wirksamkeit einer derartigen Therapie, die hohe Todesrate in dieser Indikation rechtfertigt allerdings den Einsatz dieser Substanz [3]. Bei einer Mehrheit der Patienten (69,2%) kam diese moderne Therapieoption auch zum Einsatz, so dass Todesfälle in den Krankenhäusern der AGATE nicht gemeldet wurden. Zusätzlich oder allein symptomorientiert mit Antibiotika wurde in 36,5% der Fälle therapiert.
Die Pathogenese dieser arzneimittelinduzierten Blutbildveränderung bleibt trotz intensiver Bemühungen nach wie vor ungeklärt. Ein immunologischer Hintergrund mit der Bildung spezifischer Antikörper kann heute bedingt durch die große zeitliche Verzögerung dieser Nebenwirkung bei Clozapin-Reexposition ausgeschlossen werden [9]. Auch die toxische, apoptotische Wirkung eines reaktiven Clozapin-Metaboliten konnte nicht überzeugend belegt werden [13]. Als neuer Mechanismus wird derzeit über einen Zusammenhang zwischen Clozapin als Partial-Agonisten am Histamin-H4-Rezeptor und der UAW Agranulozytose diskutiert [7].
Danksagung
Die Autoren danken der Dr. August und Dr. Anni Lesmüller Stiftung für die großzügige Unterstützung dieses Projekts.
Herzlich danken möchten die Autoren auch Herrn Schiller vom Rechenzentrum der Universität Regensburg für die Programmierung und Betreuung der AGATE Datenbank.
Frau A. Bindl gebührt Dank für ihre Mithilfe bei der Auswertung der Daten.
Literatur
1. Atkin K, Kendall F, Gould D, Freemann H, et al. The incidence of neutropenia and agranulocytosis in patients treated with clozapine in the UK and Ireland Br J Psychiatry 1996;169:483–8.
2. Bell R, McLaren A, Galanos J, Copolov D. The clinical use of plasma clozapine levels. Austral New Zealand J Psychiatry 1998;32: 567–74.
3. Berliner N, Horwitz M, Loughran TP. Congenital and acquired neutropenia. Hematology 2004:63–79.
4. FDA Safety Information and Adverse Event Reporting: Clozaril (clozapine) tablets: revision to WBC monitoring schedule and other safety labelling, 2006.
5. Guest I, Sokoluk B, MacCrimmon J, Uetrecht J. Examination of possible toxic and immune mechanisms of clozapine-induced agranulocytosis. Toxicology 1998;131:53–65.
6. Härtter S, Hiemke C. Wichtig bei atypischen Antipsychotika: Pharmakokinetik, Interaktionspotential und TDM. Pharmazie in unserer Zeit 2002;6:546–57.
7. Hough LB. Genomics meets histamine receptors: New subtypes, new receptors. Mol Pharmacol 2001;59:415–9.
8. Iverson S, Zahid N, Uetrecht JP. Predicting drug-induced agranulocytosis: characterizing neutrophil-generated metabolites of a model compound DMP 406, and assessing the relevance of an in vitro apoptosis assay for identifying drugs that may cause agranulocytosis. Chemico-Biological Interactions 2002;142:175–99.
9. Jann MW, Grimsley SR, Gray EC, Chang WH Pharmacokinetics and pharmacodynamics of clozapine. Clin Pharmacokinet 1993;24:161–76.
10. Müller N, Riedel M, Möller HJ. Atypische Neuroleptika: Wirkstoffe gegen Wahn und Rückzug. Pharm Ztg 2000;43:3583–8.
11. Müller N, Riedel M. Therapie mit atypischen Neuroleptika. Pharmazie in unserer Zeit 2002;6:558–65.
12. Palmblad J, Papadaki HA, Eliopoulos G. Acute and chronic neutropenias. What is new? J Int Med 2001;250:476–91.
13. Williams DP, Pirmohamed M, Naisbitt DJ, Uetrecht JP, et al. Induction of metabolism-dependent and -independent neutrophil apoptosis by clozapine. Mol Pharmacol 2000;58:207–16.
* KH Agatharied (Fr. Dr. I. Lemke), SKH Arnsdorf (Hr. CA Dr. DP. H. Heilemann), BK Ansbach (Fr. Dr. B. Mößner-Haug), BKH Augsburg, (Hr. Dr. T. Messer), BKH Bamberg (Fr. Dr. C. Bauer), BKH Bayreuth (Hr. Dr. C. Franke), Bavaria Klinik Kreischa (Fr. Dr. P. Behnert), Tagesklinik Cham (Hr. Dr. M. Dobmeier), Danuvius Klinik (OA Dr. R. Doerr), Klinikum am Europakanal Erlangen (Hr. CA Prof. Schneider), Frankenalb Klinik Engelthal (Fr. Dr. U. Reichert), Furtbacher Krankenhaus (Fr. Dr. D. Gangnus), Inn-Salzach-Klinikum gGmbH, Wasserburg (Hr. Dr. C. Steinmann), BKH Günzburg (Hr. Dr. M. Jäger), Christophsbad Göppingen (CA PD Dr. L. Hermle), Isar-Amper-Klinikum gGmbH Klinikum München Ost (Hr. Dr. Pfeiffer), NLK Hildesheim (Hr. Dr. Andreas Töpperwien), Klinik Höhenried (Hr. Dr. T. Leitz), BKH Ingolstadt (Fr. Dr. I. Mußmächer u. Hr. Dr. R. Schuler), BKH Kaufbeuren (Hr. Dr. G. Eckermann), BKH Kempten (CA PD Dr. P. Brieger), Waldkrankenhaus Köppern (Hr. CA Prof. Dr. Schiller), Lech-Mangfall-Kliniken gGmbH am Klinikum Landsberg am Lech (Hr. Dr. P. Lauer), BKH Landshut (Hr. Dr. H. Haag), BKH Lohr (Hr. Dr. W. Gsell), BKH Mainkofen (Hr. Dr. Groß), BKH Memmingen (Hr. Dr. T. Möller), Klinikum Nürnberg Nord (Hr. Dr. Waimer), BKH Obermain (Hr. Dr. Baumann), BZK Regensburg (Hr. Dr. M. Wittmann u. Hr. Dr. H. Hausner), BKH Rehau (Hr. Dr. Moder), Reha Zentrum Isarwinkel Bad Tölz (Hr. G. Winkler), Klinikum Schwerin (Hr. Dr. L. Drach), BKH Straubing (Hr. Dr. R. Müller), Krankenhaus St. Elisabeth (Hr. Dr. W. Paulus), Isar-Amper-Klinikum gGmbH Klinikum Taufkirchen (Fr. Dr. S. Apelt), ZfP Weißenau (Prof. Dr. T. Steinert), BKH Werneck (Hr. Dr. C.-P. Ostermeier), BKH Wöllershof (Fr. Dr. T. Kirchner)
Dr. rer.nat. Walter S. Fuchs, Dr. med. Roland Seifert, Dr. rer.nat. Erich Schneider, David Schnell, Lehrstuhl für Pharmakologie und Toxikologie, Naturwissenschaftliche Fakultät IV und Medizinische Fakultät, Universität Regensburg, Waldweg 27, 93055 Regensburg, E-Mail: roland.seifert@chemie.uni-regensburg.de Prof. Dr. Dr. Ekkehard Haen, Klinische Pharmakologie, Klinik und Poliklinik für Psychiatrie, Psychosomatik und Psychotherapie der Universität Regensburg, Universitätsstraße 84, 93053 Regensburg, E-Mail: ekkehard.haen@klinik.uni-regensburg.de
Agranulocytosis and neutropenia in patients treated with antipsychotic drugs with focus on clozapine
A total of 2002 cases of drug-induced adverse events were reported from AGATE (working group drugs in psychiatry) in the years 1992 to 2005 including 28 cases of agranulocytosis and 43 cases of leukopenia. Clozapine was most often rated responsible for both adverse events followed by carbamazepin, olanzapin and mianserin. In most cases clozapine-induced agranulocytosis (CIA) was reported within two months after starting therapy, whereas single cases still occurred up to 17 months after initiation of therapy. Daily doses of at least 200 mg clozapine were given before CIA developed. These data point to a dose-dependent phenomenon and support a stringent monitoring of leucocyte counts during clozapine treatment and dosing at the lower end of the effective dosage range.
Keywords: Agranulocytosis, neutropenia, antipsychotic drugs, clozapine
Psychopharmakotherapie 2008; 15(03)
