Daniela Eser, Thomas C. Baghai und Hans-Jürgen Möller, München
Die endogene Melatoninausschüttung unterliegt einer strengen zirkadianen Rhythmik [11] und wird über die cAMP-Signaltranduktionskaskade gesteuert [4]. Positive Effekte von Melatonin bei der Behandlung von Schlafstörungen konnten in verschiedenen Untersuchungen belegt werden. Allerdings ist die therapeutische Anwendung von Melatonin, das beispielsweise in den USA als Nahrungsergänzungsmittel zur Verfügung steht, durch die geringe orale Bioverfügbarkeit eingeschränkt. Deswegen wurden in den letzten Jahren verschiedene Melatoninagonisten synthetisiert und auf ihre mögliche therapeutische Wirkung bei der Behandlung von Schlafstörungen untersucht (für eine aktuelle Übersicht des Entwicklungsstandes verschiedener Melatoninrezeptoragonisten vgl. Turek et al., 2004 [24]). Agomelatin (S-20098; Abb. 1), ein Agonist für zentrale Melatonin(M1 und M2)-Rezeptoren, ist dabei die bislang tierexperimentell am besten charakterisierte Substanz [24]. Im Gegensatz zu Melatonin besitzt Agomelatin nicht nur eine Melatonin-agonistische, sondern gleichzeitig eine 5-HT2C-Rezeptor-antagonistische Wirkung. In zahlreichen tierexperimentellen Untersuchungen fanden sich Hinweise auf eine antidepressive Wirksamkeit von Agomelatin, wobei die therapeutische Wirkung von Agomelatin in diesen Studien, der Wirkung etablierter Antidepressiva vergleichbar war [2, 3, 20]. Zudem konnten im Tiermodell anxiolytische Effekte von Agomelatin nachgewiesen werden [5, 15]. Außerdem wurde gezeigt, dass Agomelatin, ähnlich wie Melatonin, zu einer Resynchronisation gestörter zirkadianer Rhythmen beiträgt [1, 22, 25, 26].
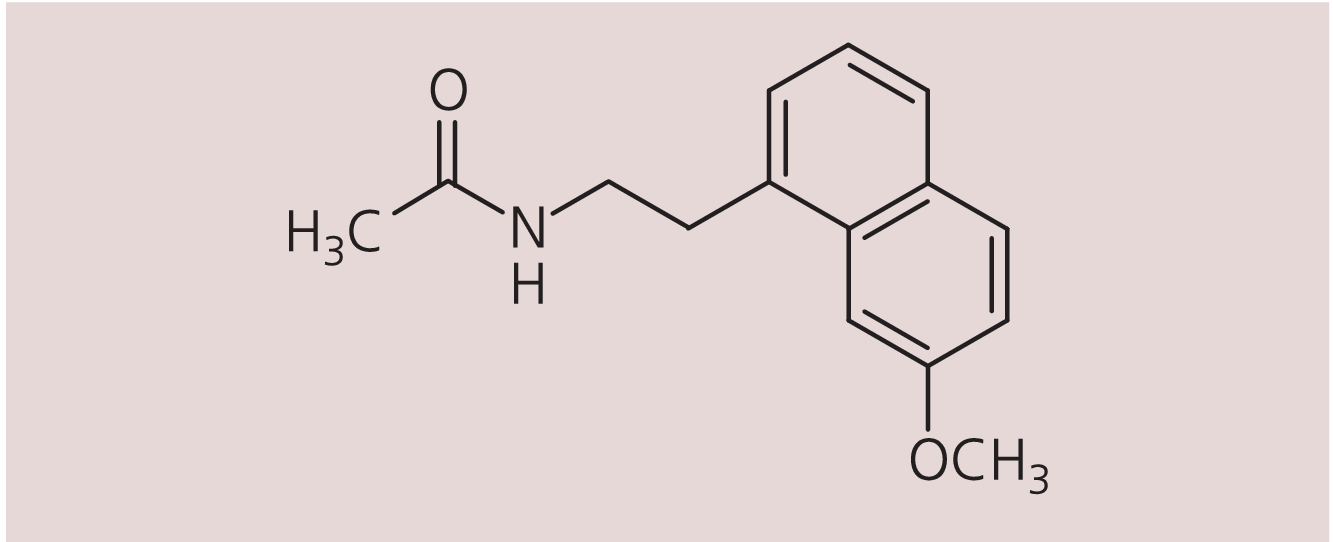
Abb. 1. Agomelatin
Auf Grundlage dieser vielversprechenden tierexperimentellen Befunde wurde Agomelatin in den letzten Jahren als mögliche neue Therapieoption bei der Behandlung depressiver Störungen untersucht. Dabei wurde die klinische Wirksamkeit und Verträglichkeit in kontrollierten klinischen Studien belegt. Im Folgenden sollen die bislang veröffentlichten klinischen Studienergebnisse zur Wirksamkeit und Verträglichkeit von Agomelatin dargestellt werden.
Antidepressive Wirkung von Agomelatin
In einer ersten doppelblinden, Plazebo-kontrollierten, internationalen Dosisfindungsstudie [14] wurde die klinische Wirksamkeit dreier unterschiedlicher Dosierungen von Agomelatin mit der Wirksamkeit von Paroxetin bei der Behandlung depressiver Störungen verglichen. Dabei wurden 711 Patienten, im Alter von 18 bis 65 Jahren, die unter einer depressiven Episode im Rahmen einer unipolar depressiven Störung (n=698) oder einer bipolaren Störung (n=13) (bipolar II nach DSM-IV [16]) litten, untersucht. Eingeschlossen wurden Patienten, die mindestens 22 Punkte im Summenscore der 17-Itemversion der Hamilton-Depressionsskala (HAMD17) [7] erreichten. Als Hauptwirksamkeitskriterium wurde der HAMD17-Wert bei Behandlungsende in der Gesamtanalyse (Full analysis set [FAS]) definiert. Nach einer obligatorischen einwöchigen Plazebo-Behandlungsphase wurden diejenigen Patienten, die bereits auf die Plazebo-Behandlung angesprochen hatten (definiert durch eine Reduktion in der HAMD17-Skala um mehr als 20%), von der weiteren Studienteilnahme ausgeschlossen. Die verbleibenden Patienten wurden randomisiert den verschiedenen Behandlungskonditionen zugeordnet. Die achtwöchige Behandlung erfolgte unter doppelblinden Bedingungen mit 1 mg, 5 mg oder 25 mg/d Agomelatin in einer einmaligen Abenddosis, mit 20 mg/d Paroxetin, welches morgens verabreicht wurde, oder mit Plazebo.
Vor der ersten aktiven Behandlung betrug der mittlere HAMD17-Wert 27,4 Punkte, in der Montgomery-Åsberg Depressionsskala (MADRS) [16] wiesen die eingeschlossenen Patienten einen mittleren Wert von 31,5 auf. Somit handelte es sich um mittelgradig bis schwer depressive Patienten. Ein Drittel der Patienten litt an einer schweren depressiven Episode, die durch einen HAMD17-Wert ≥25 definiert wurde. Die Behandlungsgruppen unterschieden sich bei Baseline statistisch nicht in den demographischen oder klinischen Variablen.
In der Intent-to-treat-Analyse wurden alle Patienten berücksichtigt, die nach Randomisierung mindestens einmalig aktiv behandelt und nach dem Baselinezeitpunkt mindestens einmal untersucht wurden. In der LOCF(Last observation carried forward)-Analyse zeigte sich im Vergleich der mittleren Skalenwerte zwischen der Gruppe aller mit Agomelatin behandelten Patienten und der Plazebo-Gruppe eine signifikant bessere Wirksamkeit von Agomelatin. Auch für die aktive Vergleichssubstanz Paroxetin konnte eine signifikante Überlegenheit gegenüber Plazebo nachgewiesen werden. In einer zusätzlich durchgeführten statistischen Analyse (Dunett’s t-Test, korrigiert für multiples Testen) war Agomelatin nur in einer Dosierung von 25 mg signifikant wirksamer als Plazebo. Die Zeit bis zum ersten Ansprechen war unter Agomelatin 25 mg signifikant kürzer als unter der Plazebo-Behandlung. Zudem wurde im Gegensatz zu Paroxetin, das erst nach einer Behandlungsdauer von vier Wochen einer Plazebo-Behandlung überlegen war, unter Agomelatin 25 mg bereits nach zwei Behandlungswochen ein signifikanter Unterschied zur Plazebo-Behandlung erreicht.
In der Responderanalyse zeigte sich eine Verbesserung der depressiven Symptomatik um mindestens 50% signifikant häufiger unter Agomelatin 25 mg (61,5%) als unter Plazebo (46,3%). In einer ergänzenden statistischen Analyse (paarweiser Bonferroni-korrigierter Vergleich) wurden im Vergleich zu Plazebo signifikant höhere Responseraten unter Agomelatin 25 mg und Agomelatin 1 mg (62,5%) nachgewiesen, während sich die Responseraten von 51,4% unter Agomelatin 5 mg und 56,3% unter Paroxetin nicht signifikant von der Plazebo-Behandlung unterschieden.
In Bezug auf die Remission der depressiven Symptomatik, die durch einen HAMD17-Wert unterhalb 7 definiert wurde, zeigten sich Agomelatin 25 mg und Paroxetin der Therapie mit Plazebo signifikant überlegen. In der Subgruppenanalyse der schwer depressiven Patienten (HAMD17-Score ≥25) zeigte sich dagegen, dass sich nur die mit Agomelatin 25 mg behandelten Patienten, jedoch nicht die Patienten, die mit niedrigerer Dosis behandelt wurden, signifikant von der Plazebo-Gruppe unterschieden. Auch eine Behandlung mit Paroxetin unterschied sich dabei nicht von der Plazebo-Behandlung.
In zwei weiteren randomisierten doppelblinden Plazebo-kontrollierten Studien wurde die antidepressive Wirksamkeit von 25 mg Agomelatin bestätigt [19]. In beiden Studien erwies sich Agomelatin auch bei der Behandlung schwerer depressiver Episoden als wirksam [9, 17]. Dabei wurden, in der aktuell von Kennedy et al. publizierten Studie [9], 212 ambulante depressive Patienten zunächst mit 25 mg/d Agomelatin behandelt, bei unzureichender Besserung der depressiven Symptomatik nach der zweiten Behandlungswoche war eine Dosissteigerung auf 50 mg/d (n=36) möglich. Im Vergleich zu Plazebo war Agomelatin nach einer Behandlungsdauer von sechs Wochen signifikant wirksamer, was sich in einer signifikanten Reduktion der HAMD-Werte, einer signifikant höheren Ansprechrate von 49,1% und signifikant niedrigeren CGI-Werten (Clinical global impressions) ausdrückte.
Zudem konnte die klinische Wirksamkeit von Agomelatin in einer weiteren randomisierten doppelblinden Multicenterstudie belegt werden, die als primäres Ziel anstrebte, mögliche Absetzsymptome nach Therapie mit Agomelatin oder Paroxetin bei anhaltend remittierten depressiven Patienten zu vergleichen [18] (siehe auch Unterpunkt Sicherheit und Verträglichkeit). In dieser Untersuchung wurden 335 ambulante Patienten mit der Diagnose einer „Major Depression“ (nach DSM-IV) und einem mittleren MADRS-Wert von 23 über einen Zeitraum von 12 Wochen mit 25 mg/d Agomelatin oder 20 mg/d Paroxetin behandelt. Insgesamt respondierten 192 Patienten auf die Studienbehandlung und wiesen in der 8., 10. und 12. Behandlungswoche einen MADRS-Score ≤12 auf. Die Remissionsrate betrug in der Agomelatin-Gruppe 52,7% und in der Paroxetin-Gruppe 61,9%. Zu Beginn der Absetzphase zeigten sich zwischen den remittierten Patienten beider Behandlungsgruppen keine signifikanten Unterschiede in der Hamilton-Angstskala (HAMA) und im MADRS-Score. Auch diese Ergebnisse belegen, dass Agomelatin antidepressiv wirksam ist und zu einer hohen Ansprechrate führt. Ähnliche Ergebnisse zeigten sich in einer Untersuchung von Kennedy et al. [8], deren primäres Ziel darin bestand, sexuelle Funktionsstörungen unter Therapie mit Agomelatin und Venlafaxin zu vergleichen. Ambulante depressive Patienten wurden über einen Zeitraum von 12 Wochen mit 50 mg Agomelatin oder 150 mg Venlafaxin behandelt. Auch in dieser Studie wurden nicht nur eine vergleichbar gute antidepressive Wirksamkeit, sondern auch vergleichbar hohe Remissionsraten von 56,9% unter Agomelatin und 59,7% unter Venlafaxin beobachtet.
In Tabelle 1 sind die klinischen Studienergebnisse zur Wirksamkeit von Agomelatin dargestellt.
Tab. 1. Antidepressive Wirksamkeit von Agomelatin. Übersicht klinischer Untersuchungsergebnisse
|
Autor |
Studienart |
Patientenkollektiv |
Patienten |
Agomelatin-Tagesdosis |
Behandlungs-dauer |
Wirksamkeit |
|
Loo 2002 [14] |
Dosisfindungsstudie doppelblind, Plazebo-kontrolliert |
Depressive Episode i. R. unipolarer (n=698) oder bipolarer (n=13) Störung |
711 |
1 mg (n=141) |
49±15 Tage |
HAMD-Reduktion |
|
Loo 2002 [14] |
Dosisfindungsstudie doppelblind, Plazebo-kontrolliert |
Schwere depressive Episode (HAMD ≥25 bei Studieneinschluss) |
586 |
25 mg (n=120) |
49±15 Tage |
HAMD-Reduktion |
|
Kennedy 2006 [9] |
Doppelblind, Plazebo-kontrolliert |
Ambulante depressive Patienten |
212 |
25–50 mg (n=106) |
6 Wochen |
HAMD-Reduktion |
|
Kennedy 2006 [9] |
Doppelblind, Plazebo-kontrolliert |
Schwere depressive Episode (HAMD ≥25 bei Studieneinschluss) |
151 |
25–50 mg (n=16) |
6 Wochen |
HAMD-Reduktion |
|
Montgomery 2004 [18] |
Studie zu Absetzsymptomen, doppelblind, Plazebo-kontrolliert |
Ambulante depressive Patienten |
335 |
25 mg (n=167) |
12 Wochen |
Remissionsrate 52,7% |
|
Kennedy 2005 [8] |
Studie zu sexuellen Funktionsstörungen doppelblind, Plazebo-kontrolliert |
Ambulante depressive Patienten |
276 |
50 mg (n=137) |
12 Wochen |
Remissionsrate 56,9% |
Für die Zulassung des Präparats auf dem europäischen Markt stehen derzeit allerdings noch Ergebnisse aus klinischen Langzeitstudien aus, so dass die Wirksamkeit von Agomelatin bei der effektiven Erhaltungstherapie und Rückfallprophylaxe depressiver Episoden aktuell noch nicht abschließend beurteilt werden kann.
Anxiolytische Wirkung von Agomelatin
In tierexperimentellen Untersuchungen konnten neben Hinweisen auf antidepressive Effekte auch Hinweise auf anxiolytische Wirkungen von Agomelatin gefunden werden. Ähnlich wie Imipramin, Fluoxetin und Diazepam vermindert Agomelatin angstassoziiertes Verhalten im Tiermodell [5]. Im Gegensatz zu Melatonin ist die anxiolytische Wirkung von Agomelatin jedoch vom Tageszeitpunkt der Verabreichung unabhängig [5]. Zudem wurde im Elevated-plus-maze-Test gezeigt, dass die Vorbehandlung mit einem Melatoninantagonisten zwar die anxiolytische Wirkung einer abendlichen Gabe von Melatonin oder Agomelatin aufhebt, die anxiolytische Wirkung der morgendlichen Agomelatin-Gabe jedoch erhalten bleibt [5]. Dementsprechend wurde gefolgert, dass die anxiolytische Wirkung von Agomelatin nicht nur auf die Melatonin-agonistische, sondern auch auf die 5-HT2C-Rezeptor-antagonistische Wirkung zurückzuführen ist [5].
Obwohl bislang keine Untersuchungen zur Wirksamkeit von Agomelatin bei der Behandlung von Angsterkrankungen vorliegen, wurde in der eingangs dargestellten Dosisfindungsstudie [14] ein signifikanter Rückgang depressionsassoziierter Angstsymptome nachgewiesen. Sowohl bei Behandlung mit 25 mg/d Agomelatin als auch mit Paroxetin zeigten sich im Vergleich zur Plazebo-Behandlung signifikant niedrigere Mittelwerte in der Hamilton-Angstskala, die auf eine gute anxiolytische Wirksamkeit von Agomelatin schließen lassen.
Einfluss von Agomelatin auf die zirkadiane Rhythmik
Der Einfluss von Agomelatin auf die zirkadiane Rhythmik wurde sowohl bei gesunden Probanden, als auch bei depressiven Patienten untersucht. In einer doppelblinden, Plazebo-kontrollierten Cross-over-Studie an gesunden älteren Männern [10] zeigte sich nach 15-tägiger Behandlung mit 15 mg/d Agomelatin eine signifikante, annähernd 2-stündige, Phasenvorverlagerung des zirkadianen Körpertemperaturverlaufs und der zirkadianen Cortisolausschüttung. Ein vergleichbarer Trend konnte für die Ausschüttung von Thyreotropin (TSH) nachgewiesen werden. Außerdem stimulierte Agomelatin sowohl die pulsatile Wachstumshormonsekretion während der Wachphase als auch die Prolactinausschüttung. Allerdings veränderte Agomelatin dabei nicht das normale Schlafprofil der gesunden Probanden [10]. Bei depressiven Patienten trägt die Behandlung mit 25 mg Agomelatin dagegen zu einer Normalisierung des gestörten Schlaf-Wach-Rhythmus bei [21]. In polysomnographischen Untersuchungen zeigte sich, dass es sowohl zu einer Verlängerung der Slow-Wave-Phasen als auch zu einer Normalisierung der Slow-Wave-Phasenverteilung im Nachtverlauf kommt [21].
Außerdem konnte in den bereits dargestellten Dosisfindungsstudien [12, 13] gezeigt werden, dass sich unter Therapie mit Agomelatin sowohl somatische Beschwerden als auch depressionsassoziierte Schlafstörungen signifikant verbessern. Erste Ergebnisse einer ambulanten Untersuchung, in der die Wirksamkeit von Agomelatin (25–50 mg/d) und Venlafaxin (75–150 mg/d) bei der Behandlung depressiver Störungen verglichen wurde, zeigten unter Agomelatin eine signifikante subjektive Verbesserung von Einschlafstörungen und der Schlafqualität bei gleichzeitigem Rückgang der Tagesmüdigkeit [6].
Zusammenfassend zeigen diese Ergebnisse, dass Agomelatin bei depressiven Patienten durch Induktion einer Phasenverlagerung zu einer Normalisierung gestörter Schlaf-Nacht-Rhythmen beitragen kann, ohne jedoch gleichzeitig durch sedierende Eigenschaften den normalen Schlaf-Wach-Rhythmus zu stören.
Sicherheit und Verträglichkeit von Agomelatin
In allen bislang publizierten Studien zeigte sich, dass Agomelatin in seiner Anwendung sicher und im Vergleich zu etablierten Antidepressiva, insbesondere selektiven Serotonin-Wiederaufnahmehemmern (SSRI) und kombinierten selektiven Serotonin- und Noradrenalin-Wiederaufnahmehemmern (SSNRI), besser verträglich ist. In einer ersten Pilotstudie zur Dosisfindung wurden 28 Patienten mit Agomelatin 5 mg/d oder 100 mg/d behandelt. Nach 4- bis 8-wöchiger Therapie wurden keine klinisch relevanten Veränderungen von kardiovaskulären oder laborchemischen Parametern festgestellt [12, 13], wenngleich die Hochdosisbehandlung mit einer etwas höheren Rate unerwünschter Wirkungen sowie behandlungsassoziierter Nebenwirkungen (z.B. Kopfschmerzen, Angstsymptome, Bauchschmerzen, Diarrhö) einherging. Im Rahmen der großen doppelblinden Dosisfindungsstudie [14] berichteten insgesamt 56,5% der 711 behandelten Patienten über mindestens eine Nebenwirkung, die entweder erstmalig während der Behandlung aufgetreten war oder sich im Verlauf der Behandlung verschlimmerte. Die Nebenwirkungsrate unterschied sich jedoch nicht zwischen der Plazebo-Gruppe (54,7%) und der Agomelatin-Gruppe (51,1%). Im Gegensatz dazu traten unter Paroxetin signifikant häufiger gastrointestinale Nebenwirkungen, insbesondere Übelkeit auf. Auch hier kam es während der Behandlung mit Agomelatin nicht zu klinisch relevanten Veränderungen der Vitalparameter, des Gewichts oder kardiovaskulärer Parameter. Insbesondere traten keine EKG-Veränderungen auf. Des Weiteren konnte in den beiden bereits erwähnten randomisierten doppelblinden Studien [19] neben der klinischen Wirksamkeit auch die gute Verträglichkeit von Agomelatin in Tagesdosierungen von 25 mg und 50 mg belegt werden, welche der Verträglichkeit von Plazebo vergleichbar war. Eine Übersicht behandlungsassoziierter Nebenwirkungen unter Agomelatin-Therapie kann aus Tabelle 2 entnommen werden.
Tab. 2. Beobachtete Nebenwirkungen (UAW) unter Agomelatin-Therapie
|
Studie |
Dosis |
Therapie-dauer |
Beobachtete Nebenwirkungen |
Kommentar |
|
Loo 2002 [14] |
25 mg |
8 Wochen |
Kopfschmerzen (6,6%)* Bauchschmerzen (3,6%)* Diarrhö (3,6%)* Angstsymptome (3,6%)* Übelkeit (2,9%)* Müdigkeit (2,9%)* Depression (2,9%)* Schlafstörungen (2,9%)* Schnupfen (2,2%)* Mundtrockenheit (0,7%)* |
UAW seltener unter Agomelatin (51,1%) als unter Plazebo (54,7%) und Paroxetin (66%) |
|
Kennedy 2005 [8] |
25–50 mg |
6 Wochen |
Häufiger unter Agomelatin: Schwindel (9,3% vs. 4,8%)° Nasopharyngitis (6,5% vs. 3,8%)° Grippesymptome (6,5% vs. 2,9%)° Häufiger unter Plazebo: Kopfschmerzen Übelkeit Müdigkeit Mundtrockenheit Diarrhö |
UAW seltener unter Agomelatin (30,2%) als unter Plazebo (36,2%) |
* Prozent der mit Agomelatin (25 mg/d) behandelten Patienten (n=137)
° Prozent der mit Agomelatin (n=61) und mit Plazebo (n=66) behandelten Patienten
Sexuelle Funktionsstörungen, die häufig als Nebenwirkungen einer antidepressiven Pharmakotherapie auftreten, stellen eine häufige Ursache für die Noncompliance der Patienten dar [23]. In einer eigens dafür konzipierten Untersuchung von Kennedy et al. [8] wurde die Wirkung von Agomelatin auf sexuelle Funktionen und mögliche Funktionsstörungen untersucht. Sexuelle Funktionsstörungen wurden mit Hilfe eines Fragebogens unter Therapie mit Agomelatin oder Venlafaxin verglichen. Im Vergleich zur Venlafaxin-Gruppe wurden von Patienten, die mit Agomelatin 50 mg behandelt wurden, sowohl Libido als auch Orgasmusfähigkeit signifikant besser bewertet. Das Fehlen sexueller Funktionsstörungen stellt einen besonders wichtigen und klinisch relevanten Vorteil von Agomelatin bei depressiven Patienten im Vergleich zu SSRI dar.
In einer weiteren randomisierten, Plazebo-kontrollierten, internationalen doppelblinden Studie wurden gezielt Absetzsymptome nach abrupter Beendigung der Agomelatin-Therapie erfasst, wobei als aktive Vergleichssubstanz Paroxetin verwendet wurde [18]. Dabei wurden in der ersten Studienphase 335 ambulante depressive Patienten für die Dauer von 12 Wochen mit 25 mg/d Agomelatin (n=167) oder mit 20 mg/d Paroxetin (n=168) behandelt. Diejenigen Patienten, die im Rahmen der Behandlung eine anhaltende Remission der depressiven Störung erreicht hatten (definiert durch einen MADRS-Wert ≤12 in der 8., 10., und 12. Behandlungswoche), wurden randomisiert in die zweite, ebenfalls doppelblinde Studienphase eingeschlossen. In dieser Phase wurden die Patienten über einen Zeitraum von zwei Wochen entweder mit der aktiven Studienmedikation oder mit Plazebo weiterbehandelt. Absetzsymptome wurden ein und zwei Wochen nach erneuter Randomisierung mit der Discontinuation-Emergent-Signs-and-Symptoms(DESS)-Skala erfasst.
In die zweite Studienphase wurden insgesamt 192 anhaltend remittierte Patienten eingeschlossen. Dabei hatten 88 Patienten unter Behandlung mit Agomelatin und 104 Patienten unter Behandlung mit Paroxetin die Kriterien einer anhaltenden Remission erreicht.
Bei 61 Patienten der jeweiligen Behandlungsgruppe wurde die aktive Studienbehandlung mit Agomelatin 25 mg/d oder Paroxetin 20 mg/d unverändert fortgeführt. Im Gegensatz dazu wurde bei 27 Patienten der Agomelatin-Behandlungsgruppe und bei 43 Patienten der Paroxetin-Behandlungsgruppe die aktive Behandlung abrupt beendet und mit Plazebo weiterbehandelt. Die unterschiedlichen Patientenzahlen in den jeweiligen Absetzgruppen resultierten aus dem gewählten Randomisierungsverfahren [18].
Eine Woche nach Absetzen zeigte sich in der Anzahl von Absetzsymptomen kein statistisch signifikanter Unterschied zwischen der Agomelatin-Absetzgruppe (3,0±4,2) und der Gruppe, bei der Agomelatin weiter verabreicht wurde (4,4±5,7). Im Gegensatz dazu traten in der Paroxetin-Absetzgruppe im Vergleich zur Weiterbehandlungsgruppe signifikant mehr Absetzsymptome (7,3±7,1 vs. 3,5±4,1), wie beispielsweise Schlafsstörungen, Muskelschmerzen, Schwindel und Übelkeit, auf. Zwei Wochen nach Absetzen unterschieden sich die jeweiligen Weiterbehandlungs- und Absetzgruppen dagegen nicht in der Anzahl von Absetzsymptomen. Im Gegensatz dazu klagten diejenigen Patienten, bei denen bereits in der ersten Woche nach Absetzen von Paroxetin Absetzsymptome aufgetreten waren, auch in der zweiten Woche über signifikant mehr Symptome als diejenigen Patienten, bei denen die Paroxetin-Behandlung fortgeführt wurde.
Zudem wurde bei der Paroxetin-Absetzgruppe während der ersten Beobachtungswoche eine signifikante Zunahme depressiver Symptome im CGI und der MADRS-Skala verzeichnet, während sich die entsprechenden Skalenwerte zwischen der Agomelatin-Absetz- und Agomelatin-Weiterbehandlungsgruppe nicht signifikant unterschieden.
Somit konnte mit dieser Studie belegt werden, dass nach abruptem Absetzen von Agomelatin innerhalb eines zweiwöchigen Beobachtungszeitraums keine Absetzsymptome auftreten. Somit geht Agomelatin, insbesondere auch bei nicht-complianten Patienten, nach abrupter Beendigung der Therapie mit einem sehr geringen Risiko des Auftretens von Absetzsymtomen einher. Dementsprechend stellt Agomelatin auch unter diesem Gesichtspunkt eine neue Therapieoption mit deutlichem Sicherheitsvorteil im Vergleich zu etablierten Antidepressiva dar.
Zusammenfassung
Agomelatin ist das erste melatonerge Antidepressivum. In allen bislang veröffentlichten klinischen Untersuchungen, einschließlich Studien der Phase III, zeigt Agomelatin eine sehr gute Wirksamkeit bei der Behandlung depressiver Störungen. Dabei ist Agomelatin wirksamer als eine Plazebo-Behandlung und in seiner Wirksamkeit vergleichbar mit aktiven Vergleichssubstanzen wie SSRI und SSNRI. Agomelatin ist zudem auch zur Behandlung schwerer depressiver Episoden geeignet. Des Weiteren verbessert Agomelatin depressionsassoziierte Schlafstörungen, ohne eine Tagesmüdigkeit hervorzurufen. Die Verträglichkeit von Agomelatin ist sehr gut, klinisch relevante Veränderungen von Labor- oder Vitalparametern traten nicht auf. Blutdruck, Herzfrequenz oder QTc-Zeitintervalle werden durch Agomelatin nicht verändert. Die Rate behandlungsassoziierter Nebenwirkungen ist nicht höher als unter einer Plazebo-Behandlung. Das Fehlen sexueller Funktionsstörungen unter Agomelatin-Therapie sowie das Fehlen von Absetzsymptomen nach abrupter Beendigung der Behandlung bieten weitere klinische Vorteile. Für den Kliniker wird Agomelatin eine neue Therapieoption bei der Behandlung depressiver Störungen darstellen, die vermutlich auch in der täglichen Praxis bei einem Großteil der depressiven Patienten gute klinische Wirksamkeit mit gleichzeitig ausgezeichneter Verträglichkeit verbindet. Aktuell fehlen für eine Zulassung durch die europäische Zulassungsbehörde noch die Ergebnisse einer derzeit laufenden Langzeitstudie.
Literatur
1. Armstrong SM, McNulty OM, Guardiola-Lemaitre B, Redman JR. Successful use of S 20098 and melatonin in an animal model of delayed sleep-phase syndrome (DSPS). Pharmacol Biochem Behav 1993;46:45–9.
2. Barden N, Shink E, Labbe M, Vacher R, et al. Antidepressant action of agomelatine (S 20098) in a transgenic mouse model. Prog Neuropsychopharmacol Biol Psychiatry 2005;29:908–16.
3. Bourin M, Mocaer E, Porsolt R. Antidepressant-like activity of S 20098 (agomelatine) in the forced swimming test in rodents: involvement of melatonin and serotonin receptors. J Psychiatry Neurosci 2004;29:126–33.
4. Foulkes NS, Borjigin J, Snyder SH, Sassone-Corsi P. Rhythmic transcription: the molecular basis of circadian melatonin synthesis. Trends Neurosci 1997;20:487–92.
5. Gruca P, Przegalisnki E, Mrowiec S, Lason M, et al. P.1.127 Evidence for antidepressant- and anxiolytic-like activities of melatonin and agomelatine in animal models. Eur Neuropsychopharmacol 2004;14(Suppl 3):S230.
6. Guilleminault C. Sleep as a marker of dirupted circadian rhythms in depression. Eur Neuropsychopharmacol 2005;20(Suppl 1):S151.
7. Hamilton M. The Hamilton rating scale for depression. In: Sartorius N, Ban TA (ed.). Assessment of depression. Berlin: Springer, 1986:143–52.
8. Kennedy SH. Sexual function in remitted depressed patients following agomelatine and venlafaxine XR treatment. Eur Neuropsychopharmacol 2005;15(Suppl 3):S440.
9. Kennedy SH, Emsley R. Placebo-controlled trial of agomelatine in the treatment of major depressive disorder. Eur Neuropsychopharmacol 2006;16:93–100.
10. Leproult R, Van OA, L’hermite-Baleriaux M, Van CE, et al. Phase-shifts of 24-h rhythms of hormonal release and body temperature following early evening administration of the melatonin agonist agomelatine in healthy older men. Clin Endocrinol (Oxf) 2005;63:298–304.
11. Lesieur D, Leclerc V, Chavatte P, Marcot C, et al. Melatonin: a pertinent prototype for therapeutic intervention. Therapie 1998;53:429–37.
12. Loo H, Dalery J, Macher JP, Payen A. Pilot study comparing in blind the therapeutic effect of two doses of agomelatine, melatoninergic agonist and selective 5-HT2C-receptors antagonist, in the treatment of major depressive disorders. Encephale 2002;28:356–62.
13. Loo H, Dalery J, Macher JP, Payen A. Pilot study comparing in blind the therapeutic effect of two doses of agomelatine, melatonin-agonist and selective 5-HT2C-receptors antagonist, in the treatment of major depressive disorders. Encephale 2003;29:165–71.
14. Loo H, Hale A, D’haenen H. Determination of the dose of agomelatine, a melatoninergic agonist and selective 5-HT2C-antagonist, in the treatment of major depressive disorder: a placebo-controlled dose range study. Int Clin Psychopharmacol 2002;17:239–47.
15. Millan MJ, Brocco M, Gobert A, Dekeyne A. Anxiolytic properties of agomelatine, an antidepressant with melatoninergic and serotonergic properties: role of 5-HT2C receptor blockade. Psychopharmacology (Berl) 2005;177:448–58.
16. Montgomery SA, Asberg M. A new depression scale designed to be sensitive to change. Br J Psychiatry 1979;134:382–9.
17. Montgomery SA, Kasper S. Persönliche Mitteilung. ECNP 2005.
18. Montgomery SA, Kennedy SH, Burrows GD, Lejoyeux M, et al. Absence of discontinuation symptoms with agomelatine and occurrence of discontinuation symptoms with paroxetine: a randomized, double-blind, placebo-controlled discontinuation study. Int Clin Psychopharmacol 2004;19:271–80.
19. Olie JP, Emsley R. Confirmed clinical efficacy of agomelatine (25–50 mg) in major depression: two randomized, double-blind, placebo-controlled studies. Eur Neuropsychopharmacol 2005;15(Suppl 3):S416.
20. Papp M, Gruca P, Boyer PA, Mocaer E. Effect of agomelatine in the chronic mild stress model of depression in the rat. Neuropsychopharmacology 2003;28:694–703.
21. Quera-Salva MA, Vanier B, Chapotot F, Bohic M et al. Effect of agomelatine on the sleep EEG in patients with major depressive disorder (MDD). Sleep Med 2005;6(Suppl 2):S1–215.
22. Redman JR, Guardiola-Lemaitre B, Brown M, Delagrange P, et al. Dose dependent effects of S 20098, a melatonin agonist, on direction of re-entrainment of rat circadian activity rhythms. Psychopharmacology (Berl) 1995;118:385–90.
23. Rosen RC, Lane RM, Menza M. Effects of SSRIs on sexual function: a critical review. J Clin Psychopharmacol 1999;19:67–85.
24. Turek FW, Gillette MU. Melatonin, sleep, and circadian rhythms: rationale for development of specific melatonin agonists. Sleep Med 2004;5:523–32.
25. Van RO, Olivares E, Turek FW, Granjon L, et al. Resynchronisation of a diurnal rodent circadian clock accelerated by a melatonin agonist. Neuroreport 1998;9:1901–5.
26. Van RO, Olivares E, Zhang Y, Zee PC et al. Comparative effects of a melatonin agonist on the circadian system in mice and Syrian hamsters. Brain Res 1997;762:185–94.
Prof. Dr. med. Hans-Jürgen Möller, Dr. med. Daniela Eser, Priv.-Doz. Dr. med. Thomas C. Baghai, Klinik für Psychiatrie und Psychotherapie, Ludwig-Maximilian-Universität München, Nussbaumstraße 7, 80336 München, E-Mail: hans-juergen.moeller@med.uni-muenchen.de
Efficacy and safety of agomelatine in the treatment of depression
Melatonin secretion underlies strict circadian rhythms and is regulated via the cAMP signal transduction cascade. In the last years a variety of melatonin receptor agonists have been synthesized and evaluated for the treatment of sleep disorders. Animal studies suggested that agomelatine (S-20098), a synthetic melatonergic MT1 and MT2 receptor agonist with 5-HT2C receptor antagonistic properties could represent a new approach for the treatment of depression. In clinical trials, including phase III studies, superior efficacy was shown for agomelatine in comparison to placebo, and at least equal efficacy in comparison to active comparators for the acute treatment of major depression, even in severely depressed patients. In all studies published today agomelatine was safe and the overall tolerability profile was superior to serotonin reuptake-inhibitors (SSRIs) or selective serotonin and noradrenalin reuptake inhibitors (SNRIs). In summary agomelatine may represent a novel strategy in the acute treatment of depression.
Keywords: Agomelatine, antidepressants, melatonin, major depression
Psychopharmakotherapie 2008; 15(02)
