Hjördis Hentschel und Georg Gahn, Dresden
Primärprävention
Weltweit ereignen sich 100 bis 700 Schlaganfälle pro 100000 Menschen und Jahr, wobei die höchste Inzidenz in Osteuropa zu beobachten ist, die niedrigste Inzidenz in Skandinavien und Nordamerika [49].
Das Ziel der primären Prävention ist die Vermeidung zerebraler Ischämien bei Patienten ohne bisherige zerebrovaskuläre Erkrankungen.
Sekundärprävention
Einen ersten Schlaganfall überleben etwa 80 bis 85% der Patienten in der Akutphase [35, 92]. Davon erleiden 8 bis 15% im ersten Jahr ein Zweitereignis. Hierbei ist das Risiko in den ersten Wochen besonders hoch [54, 90], am größten ist es in den ersten drei Tagen. Besonders gefährdet für Rezidivschlaganfälle sind Patienten mit multiplen vaskulären Risikofaktoren oder solche mit begleitender koronarer Herzkrankheit (KHK) oder peripherer arterieller Verschlusskrankheit (pAVK).
Zur Erfassung des Risikoprofils sind folgende Untersuchungen obligat: eine neurologische und internistische Untersuchung, Computertomographie (CT) oder Magnetresonanztomographie (MRT) des Gehirns zur Abgrenzung von Differenzialdiagnosen (z. B. Blutung, Subarachnoidalblutung, post-paroxysmale Lähmung, Migräne) und Abklärung der Schlaganfallätiologie (embolisch, hämodynamisch, lakunär), Ultraschalluntersuchung der hirnversorgenden Gefäße (alternativ dazu oder bei unklarem Befund: CT- oder MR-Angiographie), Labor (inkl. Blutzucker, Cholesterol), Echokardiographie, EKG. Fakultativ sollten Langzeit-EKG, Langzeit-Blutdruckmessung sowie spezielle Labortests (Ausschluss Vaskulitis, Gerinnungsstörung) ergänzt werden.
Der Schwerpunkt der Sekundärprävention liegt neben der Behandlung der Risikofaktoren auf der Thrombozytenfunktionshemmung [5, 6] und der Antikoagulation.
Thrombozytenfunktionshemmung
Zu den Thrombozytenfunktionshemmern gehören die Acetylsalicylsäure (ASS), Clopidogrel, Dipyridamol in Kombination mit ASS sowie Ticlopidin. In Deutschland kommt Letzteres nur in Ausnahmefällen (Kontraindikation gegenüber ASS und Wirkungsversagen von Clopidogrel) zur Anwendung.
Thrombozytenfunktionshemmer führten in mehreren Studien zu einer Reduktion des relativen Risikos für einen nicht tödlichen Rezidiv-Schlaganfall um 23% (von einem relativen Risiko von 10,8% auf 8,3% über 3 Jahre) [6]. Patienten mit zusätzlicher KHK oder pAVK erreichten sogar eine relative Risikoreduktion (RRR) von 31%.
Die Sekundärprophylaxe mit einem Thrombozytenfunktionshemmer sollte bei sonst fehlenden Kontraindikationen lebenslang fortgeführt werden, wenngleich Studien über das 4. Anwendungsjahr hinaus fehlen.
Acetylsalicylsäure
Die Acetylsalicylsäure (ASS; Aspirin® u.v.a.) führt zur irreversiblen Hemmung der Cyclooxygenase. Die Bildung von Thromboxan A2 bleibt aus, welches normalerweise die Thrombozytenaggregation und Vasokonstriktion fördert.
Für ASS konnte ein primär vorbeugender Effekt in der Verhütung von Herzinfarkten nachgewiesen werden [64, 87]. Für den Schlaganfall konnte ein primärpräventiver Effekt für ASS nur bei Frauen gezeigt werden, die älter als 45 Jahre waren und zusätzliche vaskuläre Risikofaktoren hatten [67]. Für Männer und Patienten mit einem niedrigen zerebrovaskulären Risikoprofil konnte der Effekt nicht belegt werden [40].
Unter den ersten Sekundärpräventionsstudien, in denen ASS gegen Plazebo verglichen wurde, sind der International Stroke Trial (IST) und die chinesische Aspirin-Studie (CAST) zu erwähnen [15, 45], weitere folgten. In den Untersuchungen konnte eine durchschnittliche RRR von 13% gegenüber Plazebo ermittelt werden. Die absolute Risikoreduktion für einen erneuten Schlaganfall betrug 1% [22]. Durch Metaanalysen konnte gezeigt werden, dass die RRR dosisunabhängig war [2, 6]. Die gastrointestinalen Nebenwirkungen wie Dyspepsie, Übelkeit, Magen-/Duodenalulkus nehmen jedoch mit steigender Dosis zu. Zudem erhöht sich mit Dosen >150 mg die Anzahl der Blutungskomplikationen [94].
Derzeit hat sich in Deutschland, wie in den meisten europäischen Ländern, eine Therapie mit 100 mg ASS pro Tag durchgesetzt. Treten unter ASS Nebenwirkungen auf, kann ein anderer Thrombozytenfunktionshemmer (z.B. Clopidogrel) gegeben werden. Bei Magen- oder Duodenalulkus unter ASS kann alternativ nach einer Karenzzeit die Prophylaxe mit ASS in Kombination mit einem Protonenpumpen-Hemmer fortgeführt werden [16].
Ticlopidin
Ticlopidin (z.B. Tiklyd®) wirkt wohl als irreversibler Antagonist am Adenosindiphosphat-(ADP-)Rezeptor. Der genaue Wirkungsmechanismus ist jedoch unklar. ADP seinerseits stimuliert die Thrombozytenaggregation.
In der CATS-Studie wurde für Ticlopidin eine RRR von 21% für Schlaganfall und tödliche Ereignisse ermittelt, die damit über der RRR von Acetylsalicylsäure lag [31]. Aufgrund der häufigen und zum Teil schweren Nebenwirkungen (20% Durchfall, 0,9% Neutropenie, mehrere Fälle einer thrombotischen thrombozytopenischen Purpura) wird Ticlopidin in Deutschland dennoch praktisch nicht verwendet.
Clopidogrel
Clopidogrel (Iscover®, Plavix®) wirkt wie das aus der gleichen Substanzgruppe der Thienopyridine stammende Ticlopidin über eine irreversible Hemmung des ADP-Rezeptors. Die vollständige Wirkung setzt erst nach etwa drei bis vier Tagen ein.
In die CAPRIE-Studie wurden zu gleichen Teilen Patienten mit zerebraler Ischämie, mit Myokardinfarkt und mit einer pAVK eingeschlossen. Getestet wurde ASS 325 mg gegen Clopidogrel 75 mg. Die RRR in Bezug auf einen ischämischen Schlaganfall, Myokardinfarkt und vaskulären Tod betrug für Clopidogrel 7,8% gegenüber ASS [14]. Jedoch ergaben Subgruppenanalysen einen signifikanten Benefit von Clopidogrel gegenüber ASS nur für Patienten mit einer pAVK; hier betrug die RRR bis zu 23,3%. Auch Patienten mit einem zusätzlichen Diabetes mellitus oder mehreren zusätzlichen kardiovaskulären Risikofaktoren profitierten mehr von Clopidogrel.
In den Nebenwirkungen unterschieden sich die beiden Thrombozytenfunktionshemmer nicht (0,1% schwere Neutropenien, Fälle mit thrombotisch-thrombopenischer Purpura) [8]. Die Rate gastrointestinaler Blutungen war in der Clopidogrel-Gruppe signifikant geringer als in der ASS-Gruppe (1,99% vs. 2,66%).
Clopidogrel plus ASS
Die MATCH-Studie belegte in der Sekundärprävention der zerebralen Ischämie im Vergleich von ASS 75 mg plus Clopidogrel 75 mg gegenüber Clopidogrel 75 mg allein eine RRR von 6,4% zugunsten der Kombination. Bezüglich des Endpunkts „erneutes vaskuläres Ereignis oder vaskulärer Tod“ war der Unterschied nicht signifikant, denn mit der Kombination waren signifikant häufiger schwere Blutungskomplikationen (2,6% bei Kombination versus 1,3% bei Clopidogrel allein) zu verzeichnen [23].
Aus diesem Grund ist die Kombination von Clopidogrel und ASS bis auf wenige Ausnahmen nicht zu empfehlen. Zu den Ausnahmen gehören, entsprechend den Daten der CURE-Studie, die KHK mit instabiler Angina pectoris und der akute Myokardinfarkt [63]. Eine weitere Ausnahme stellt die Karotis-Stent-Implantation dar. Die kombinierte Gabe von ASS und Clopidogrel über 4 Wochen nach Karotis-Stent ist an die kardiologische Studie CLASSICS 2000 angelehnt, die einen vorteilhaften Effekt für Clopidogrel zusammen mit ASS nach Koronar-Stent in der Re-Epithelialisierungsphase belegte [10].
Dipyridamol plus ASS
Dipyridamol bewirkt über die Hemmung der Phosphodiesterase einen Anstieg von cAMP in den Thrombozyten, was die Hemmung der Plättchenaggregation zur Folge hat. Es hat eine geringere thrombozytenfunktionshemmende Wirkung als ASS oder Clopidogrel, weist aber daneben noch andere positive Effekte auf, wie zum Beispiel eine Stimulation der Endothelfunktion [65].
In der Studie ESPS-1 wurden Patienten nach zerebraler Ischämie mit ASS 990 mg + Dipyridamol 225 mg behandelt. Es wurde eine RRR von 33,5% für die Ereignisse ischämischer Schlaganfall und Tod gegenüber Plazebo ermittelt [84]. In ESPS-2 wurde die Kombination von ASS 25 mg plus Dipyridamol 200 mg (Aggrenox®; zweimal täglich) gegen die Monotherapie mit ASS 25 mg (zweimal täglich) oder Dipyridamol 200 mg (zweimal täglich) und gegen Plazebo verglichen. Die kombinierte Gabe von ASS plus Dipyridamol erbrachte gegenüber Plazebo eine RRR von 37% für die Ereignisse ischämischer Schlaganfall und/oder Tod, und gegenüber ASS-Monotherapie eine RRR von 23%. Für Dipyridamol allein ergab sich eine RRR von 16% gegenüber Plazebo, für ASS allein eine RRR von 18% [22]. Dieses Ergebnis wurde in der ESPRIT-Studie bestätigt [27]. Dort wurde für ASS plus Dipyridamol über einen Zeitraum von sechs Jahren eine RRR von ungefähr 25% gegenüber ASS nachgewiesen
Die Kombination von ASS und Dipyridamol führte nicht zu einer gesteigerten Rate von Blutungskomplikationen (8,7% bei Kombination versus 8,2% unter ASS allein). Jedoch litten Patienten unter Dipyridamol häufig unter Kopfschmerzen (ca. 8% der Fälle). Diese Rate konnte durch langsames Einschleichen vermindert werden [22]. Ein nach intravenöser Gabe von Dipyridamol beobachtetes koronares Steal-Phänomen war nach oraler Applikation nicht nachzuweisen.
Die Kombination aus ASS plus Dipyridamol versus Clopidogrel-Monotherapie wird derzeit in der PRoFESS-Studie geprüft.
GP-IIb/IIIa-Antagonisten
Aufgrund der guten Ergebnisse beim Einsatz der Glykoprotein-(GP-)IIb/IIIa-Antagonisten beim akuten Koronarsyndrom war ihr Einsatz in der Sekundärprophylaxe der zerebralen Ischämie zunächst vielversprechend angenommen worden. In der BRAVO-Studie kam es jedoch unter Anwendung von Lotrafiban plus ASS zu einer höheren Letalität als unter ASS allein, weswegen die Studie abgebrochen wurde [73]. Das Blutungsrisiko war unter der zusätzlichen Gabe von Lotrafiban signifikant erhöht, weswegen der Einsatz der GP-IIb/IIIa-Antagonisten zur Sekundärprävention des ischämischen Schlaganfalls nicht empfohlen wird.
Wahl des Thrombozytenfunktionshemmers
Die Wahl des Thrombozytenfunktionshemmers erfolgt entsprechend der aktuellen Studienlage nach einer Risikostratifizierung.
Basierend auf den Ergebnissen der CAPRIE-Studie [68] wurden die Risikofaktoren und Begleiterkrankungen identifiziert und ein Punkte-Modell entwickelt (Tab. 1). Die maximal erreichbare Punktzahl ist 10. Bis zu einer Punktzahl von 7 kommt es zu einem linearen Anstieg der Häufigkeit von Rezidivinsulten. In der Patientengruppe mit niedrigem Rezidivrisiko (0–2 Punkte, Rezidivrisiko <4% pro Jahr) besteht kein Wirksamkeitsunterschied zwischen ASS und Clopidogrel. Bei Patienten mit hohem Risiko (3–6 Punkte) und Patienten mit begleitender pAVK ist Clopidogrel signifikant wirksamer als ASS [24]. ASS plus Dipyridamol ist in der Risikogruppe mit einem Rezidivrisiko >4% pro Jahr (≥3 Punkte) der ASS-Monotherapie ebenfalls überlegen [21].
Tab. 1. Punkte-Modell zur Abschätzung des Risikos für Rezidivinsulte nach einem Schlaganfall [nach 68]
|
Risikofaktor |
Punkte |
|
<65 Jahre |
0 |
|
65–75 Jahre |
1 |
|
>75 Jahre |
2 |
|
Arterielle Hypertonie |
1 |
|
Diabetes mellitus |
1 |
|
Myokardinfarkt |
1 |
|
Andere kardiovaskuläre Ereignisse (außer Myokardinfarkt und Vorhofflimmern) |
1 |
|
pAVK |
1 |
|
Raucher |
1 |
|
Zusätzliche transitorische ischämische Attacke oder Insult zum qualifizierenden Ereignis |
1 |
Zusammenfassend soll bei einem Rezidivrisiko >4% pro Jahr die Sekundärprophylaxe mit einer Kombination aus ASS 25 mg und retardiertem Dipyridamol 200 mg zweimal täglich erfolgen. Die Gabe von Clopidogrel 75 mg wird bei einem Schlaganfallrezidiv unter ASS, bei begleitender pAVK, bei Unverträglichkeit oder Kontraindikationen gegenüber ASS empfohlen. Die Entwicklung eines Magen- oder Duodenalulkus gilt hierbei nicht als strenge Kontraindikation. Vor der dauerhaften Umsetzung von ASS auf Clopidogrel sollte stattdessen die Fortführung von ASS unter zusätzlichem Magenschutz mit einem Protonenpumpenhemmer versucht werden.
Antikoagulanzien
Antikoagulanzien hemmen die plasmatische Gerinnung. Ziel ist die Verhinderung der Bildung oder Zunahme venöser, kardialer oder arterieller Thromben.
Grundsätzlich wird die Antikoagulation mit Heparinen und Heparinoiden von der oralen Antikoagulation mit Cumarinderivaten unterschieden. Heparine können intravenös oder subkutan angewandt werden und wirken innerhalb von Stunden.
Heparine/Heparinoide
Unfraktioniertes Heparin wirkt als Kofaktor des körpereigenen Antikoagulans Antithrombin III, während niedermolekulare Heparine und die Heparinoide den pro-koagulatorischen Effekt von Faktor Xa hemmen.
Die Wirkung des unfraktionierten Heparins lässt sich durch die partielle Thrombinzeit (PTT) messen. Diese ist bei niedermolekularen Heparinen nicht verändert, hier ist die Bestimmung des Faktors Xa notwendig.
Cumarinderivate
Von den oralen Antikoagulanzien sind zurzeit nur die Cumarinderivate (Phenprocoumon [z.B. Marcumar®], Warfarin [Coumadin®]) zugelassen. Beide bewirken über die Inhibition der Vitamin-K-Epoxid-Reductase eine Hemmung der Synthese der Vitamin-K-abhängigen Faktoren II, VII, IX, X, Protein C und S.
Die volle Wirkung der Vitamin-K-Antagonisten wird erst nach etwa 48 bis 72 Stunden erreicht und klingt ohne gezielte Antagonisierung entsprechend langsam ab. Daraus resultiert die zum Teil schwierige Steuerbarkeit der oralen Antikoagulanzien.
Thrombinantagonisten
Ximelagatran und Melagatran sind direkte Thrombinantagonisten. Wegen hepatischer Komplikationen in der SPORTIF III-Studie wurde die Weiterentwicklung dieser Substanzen für die Sekundärprävention des Schlaganfalls bei Vorhofflimmern abgebrochen. Es konnte jedoch gezeigt werden, dass eine feste Dosis von 36 mg 2x täglich genauso wirksam ist wie Warfarin [26]. Die Wirkung tritt bereits nach 12 Sunden ein. Bei breiterem therapeutischem Fenster und stabilerer Pharmakokinetik sind Gerinnungskontrollen in größeren Zeitabständen ausreichend. Die Blutungsrate unter Ximelagatran war etwas geringer als unter Warfarin (29,8% vs. 25,8% pro Jahr).
Unter Ximelagatran traten im ersten halben Jahr nach Beginn der Therapie häufiger (bei 6,3% der Patienten) Leberenzymerhöhungen auf das Dreifache der Norm auf, diese waren jedoch meist spontan reversibel und damit klinisch nicht relevant. Andere orale Faktor-Xa-Antagonisten befinden sich gegenwärtig in der klinischen Prüfung.
Indikationen für eine Antikoagulation
In Anlehnung an die DGN-Leitlinien gibt es folgende Indikationen für die Antikoagulation (s. auch Abb. 1):
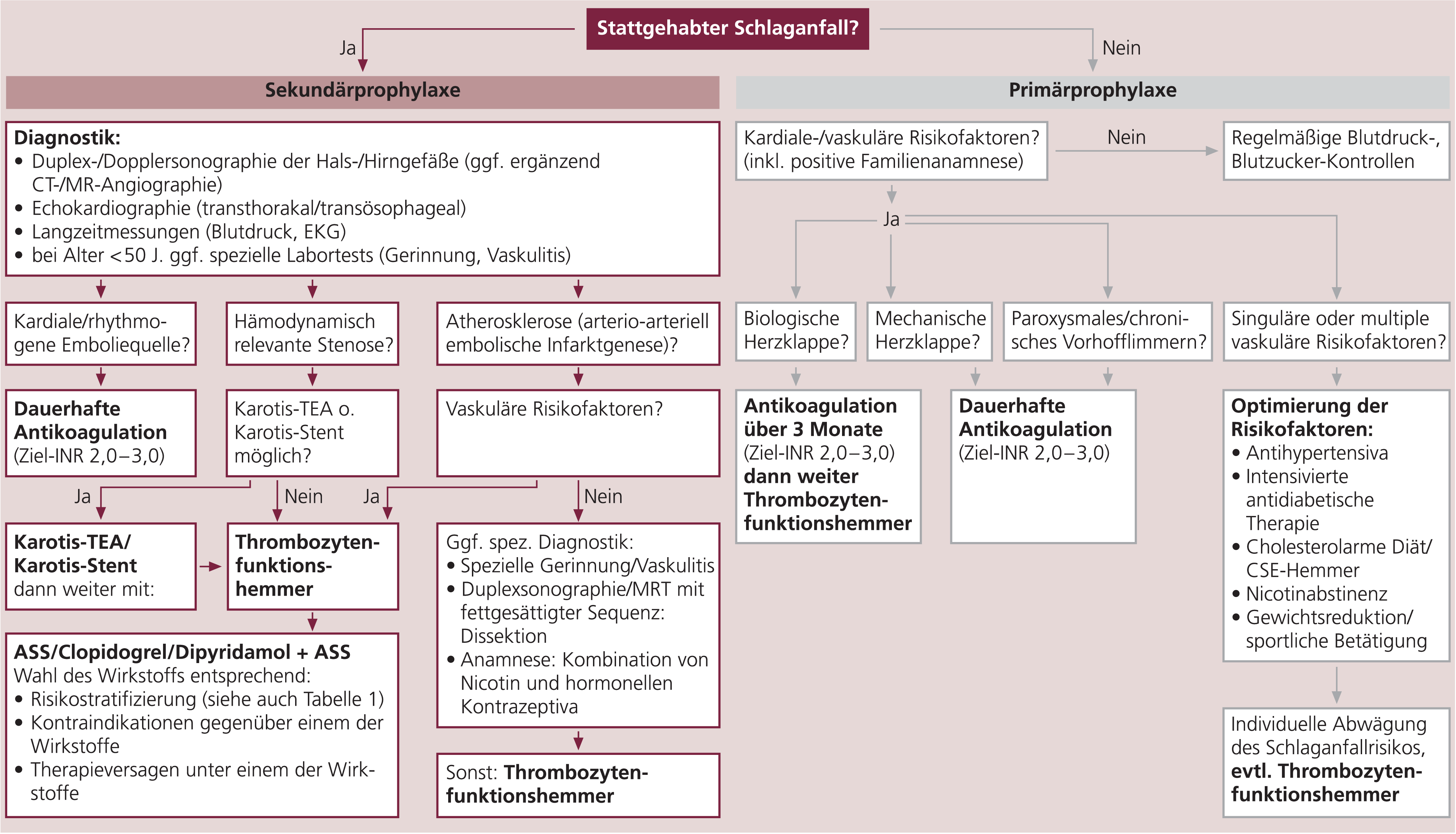
Abb. 1. Flussdiagramm zur Primär- und Sekundärprophylaxe zerebraler Ischämien
Kardiale Emboliequellen
Das Risiko für kardiale Embolien ist bei Zustand nach ausgedehntem Vorderwandinfarkt, bei mechanischem Klappenersatz, Vorhofflimmern und zusätzlicher Mitralstenose sowie bei Vorhofflimmern und Thromben im linken Vorhof oder im Aortenbogen erhöht. Für diese Patienten wird die Antikoagulation (Ziel-INR von 2,0−3,5) empfohlen [7, 42].
Für die Akutphase eines kardioembolisch bedingten Hirninfarkts konnte eine skandinavische Studie zeigen, dass ASS der Gabe von gewichtsadaptiertem niedermolekularem Heparin ebenbürtig ist [9]. Die PTT-gesteuerte Vollheparinisierung oder subkutane Heparine/Heparinoide hatten innerhalb der ersten 48 Stunden nach einem kardioembolischen Schlaganfall keine Vorteile gegenüber Plazebo oder ASS [45]. Zwar sank die Zahl der Rezidiv-Ischämien, gleichzeitig kam es aber insbesondere zu einer signifikanten Zunahme hämorrhagischer Schlaganfälle (von 0,4 auf 1,2%) und anderer Blutungskomplikationen (1,93% unter Heparin vs. 0,44% bei Kontrollen) [15, 45, 86].
Ist aufgrund eines sehr hohen Risikos für eine erneute zerebrale Ischämie dennoch die möglichst zeitnahe Antikoagulation indiziert, kann aufgrund des Wirkungseintritts nach nur wenigen Stunden mit einer Vollheparinisierung (unfraktioniertes oder niedermolekulares Heparin) begonnen werden. Überlappend kann dann die Umstellung auf orale Antikoagulanzien erfolgen. Hierbei ist zu berücksichtigen, dass in Studien zur Prävention tiefer Beinvenenthrombosen bei immobilisierten Schlaganfallpatienten bei gleicher Effektivität Blutungskomplikationen unter fraktionierten Heparinen seltener auftraten als unter unfraktionierten [25].
Nach stattgehabtem Schlaganfall sollte für die Festlegung des Beginns der Antikoagulation das Rezidivrisiko für eine zerebrale Ischämie gegenüber dem Einblutungsrisiko abgewogen werden. In den ersten Wochen nach einem Schlaganfall ist dieses Risiko, insbesondere bei größeren Ischämien, deutlich erhöht, deshalb sollte die Antikoagulation erst nach etwa vier Wochen begonnen werden. Nach einer TIA oder einem leichten ischämischen Insult kann die orale Antikoagulation innerhalb von drei bis fünf Tagen begonnen werden. Kontraindikationen für die Antikoagulation sind akute Blutungen, hämorrhagische Diathese, schwere therapieresistente Hypertonie, floride Endokarditis, Heparin-induzierte Thrombozytopenie (HIT) Typ II, Magen- und Darmulzera.
Bei Patienten ohne kardioembolische Schlaganfallursache ist die orale Antikoagulation zur Prävention von Sekundärereignissen wirkungslos [60, 88].
Eine Antikoagulationsschulung und -überwachung kann eine deutliche Reduktion der Blutungskomplikationen bewirken [4]. Durchschnittlich ist mit etwa 2% ernsten Blutungen (einschließlich intrazerebraler Blutungen) und 0,5% antikoagulationsbedingten Todesfällen pro Jahr zu rechnen.
Zustand nach Herzinfarkt. Eine dauerhafte Antikoagulation sollte bei Herzinfarktpatienten mit schlechter Ventrikelfunktion und begleitendem Vorhofflimmern durchgeführt werden [38].
Vorhofflimmern. Das Rezidivrisiko für einen Schlaganfall bei Vorhofflimmern beträgt etwa 12% pro Jahr. ASS in einer Dosierung von 75 oder 325 mg/d besitzt einen insultprotektiven Effekt, die Risikoreduktion beträgt jedoch nur etwa 20% [41]. Die RRR durch eine effektive Antikoagulation (Ziel-INR 2–3) beträgt etwa 67% [52], mit einer NNT (Number needed to treat) von 33. Im European Atrial Fibrillation Trial (1993) konnte bei Schlaganfall-Patienten mit Vorhofflimmern durch orale Antikoagulation (Ziel INR 3,0–4,5) eine 70%ige Risikoreduktion gegenüber einer 15%igen Risikoreduktion unter ASS (300 mg/d) erzielt werden.
Eine geringe Antikoagulation mit Ziel-INR von 1,5–1,9 besitzt nahezu keinen Nutzen. Die stärkere Antikoagulation mit Ziel-INR von 3,0–3,9 führte aufgrund vermehrter Hirnblutungen nur zu einer etwa 40%igen Reduktion aller zerebralen Ereignisse [39]. Der Nutzen der Antikoagulation gegenüber ASS ist, insbesondere ohne bisheriges ischämisches Ereignis (Primärprävention), nicht unumstritten [41]. Dem stehen die Ergebnisse der ACTIVE-Studie (Vergleich von ASS und Clopidogrel gegen Warfarin mit Ziel-INR 2,0–3,0 bei Vorhofflimmern mit zusätzlichen vaskulären Risikofaktoren) gegenüber [1]. Die Studie wurde vorzeitig abgebrochen, nachdem in der Behandlungsgruppe unter ASS plus Clopidogrel signifikant häufiger kardio- und neurovaskuläre Ereignisse auftraten.
Patienten mit persistierendem oder paroxysmalem Vorhofflimmern und begleitenden vaskulären Risikofaktoren (Hypertonie, koronare Herzerkrankung, Herzinsuffizienz, Alter >75 Jahre) sollten oral antikoaguliert werden mit einem Ziel-INR von 2,0–3,5 [34].
In Abhängigkeit von der Höhe des Rezidivrisikos für eine zerebrale Ischämie und unter Berücksichtigung eines erhöhten Blutungsrisikos sollte bei Patienten im Alter >75 Jahren ein INR um 2,0 angestrebt werden.
Ohne zusätzliche vaskuläre Risikofaktoren wird bislang im Alter über 65 Jahren aufgrund der besseren Steuerbarkeit und folglich aufgrund der besseren Compliance die Sekundärprophylaxe mit Acetylsalicylsäure (100–300 mg) empfohlen. ASS sollte auch eingesetzt werden bei Patienten mit Kontraindikationen für orale Antikoagulanzien, zum Beispiel nach früheren Blutungskomplikationen, bei zerebraler Mikroangiopathie, Demenz oder erhöhter Sturzgefahr [40].
Klappenersatz. Die orale Antikoagulation hat bei Patienten mit angeborenem oder erworbenem Klappenfehler oder mit mechanischen Kunstklappen einen präventiven Effekt [13]. Nach stattgehabter zerebraler Ischämie wird ein Ziel-INR zwischen 2,0 und 3,5 empfohlen. Dabei haben Prothesen in Mitralposition und Prothesen älterer Generation ein höheres Risiko für thrombembolische Ereignisse [79]. Bei Patienten mit mechanischen Klappenprothesen der jüngeren Generation in Aortenposition wird ein INR zwischen 2,0 und 3,0 als ausreichend erachtet, wenn ein Sinusrhythmus besteht und eine Erweiterung des linken Vorhofs ausgeschlossen ist [13, 79]. Bei Scheiben- und Flügelprothesen in Mitralposition wird von der European Society of Cardiology (ESC) ein Ziel-INR zwischen 3,0 und 3,5 empfohlen.
Bei biologischen Klappen besteht ein jährliches Schlaganfallrisiko von 0,2-2,9% (gegenüber 1–4% bei mechanischem Klappenersatz). Nach zerebraler Ischämie wird eine temporäre Antikoagulation für 3 Monate empfohlen. Anschließend soll eine Thrombozytenfunktionshemmung mit ASS fortgeführt werden.
Offenes Foramen ovale. Das offene/persistierende Foramen ovale (PFO) kommt bei 20 bis 25% der Bevölkerung vor. Es stellt nur dann eine signifikante kardiale Emboliequelle dar, wenn es in Verbindung mit einem spontanen Rechts-Links-Shunt und/oder einem Vorhofseptumaneurysma vorliegt [58]. Die Indikation zur Antikoagulation oder zum Verschluss durch ein Schirmchen ohne zuvor stattgehabtes zerebrovaskuläres Ereignis (Primärprävention) ist nur bei schweren kardialen hämodynamischen Auswirkungen des PFO zu stellen.
Den Untersuchungsergebnissen einer großen europäischen Multizenterstudie zufolge besteht bei alleinigem PFO unter ASS (325 mg) ein sehr geringes Rezidivrisiko (0,6% pro Jahr), so dass der Verschluss nicht indiziert ist [57]. Vitamin-K-Antagonisten waren entsprechend der PICSS-Studie der Gabe von ASS 325 mg nicht überlegen [44].
Besteht ein PFO mit zusätzlichem Vorhofseptumaneurysma (Risiko für Schlaganfall 6%, für Rezidivschlaganfall 15,2%) [57] oder kam es bereits zu einem Rezidivschlaganfall unter ASS, sollte die orale Antikoagulation mit einem Ziel-INR von 2,0 bis 3,0 für mindestens 2 Jahre erfolgen. Treten weitere Ereignisse auf oder bestehen Kontraindikationen für die Antikoagulation, sollte ein interventioneller PFO-Verschluss (Schirmverschluss) erfolgen.
Zerebrovaskuläre Risikofaktoren
Arterielle Hypertonie
Die arterielle Hypertonie ist der wichtigste Risikofaktor für zerebrovaskuläre Erkrankungen. Der Anstieg des mittleren Blutdrucks um 10 mmHg führt etwa zur Verdopplung des Schlaganfallrisikos, sowohl für ischämische wie auch für hämorrhagische Schlaganfälle [12]. Auch morgendliche Blutdruckspitzen bei sonst normalen Werten im Tagesverlauf sind mit einem erhöhten Risiko für eine zerebrale Ischämie oder eine intrazerebrale Blutung assoziiert [46].
In der Primärprävention des Schlaganfalls müssen 200 Patienten mit Hypertonie behandelt werden, um einen Schlaganfall zu verhindern. Dies gilt für sämtliche Altersklassen und Hypertonieformen [78]. In der Sekundärprävention bewirkt eine Senkung des systolischen Blutdrucks um 5 bis 10 mmHg beziehungsweise des diastolischen Blutdrucks um 2 bis 3 mmHg eine Reduktion des Rezidivrisikos um 30 bis 40% [36, 85]. Der präventive Effekt betrifft sowohl ischämische als auch hämorrhagische Insulte, ist umso ausgeprägter, je stärker der Blutdruck reduziert wird, und gilt nicht nur für hypertensive, sondern auch für normotensive Patienten [66]. Daher sollte im Allgemeinen der niedrigste tolerierbare Blutdruck angestrebt werden (systolisch <140 mmHg, diastolisch <90 mmHg, für Diabetiker: systolisch <130 mmHg, diastolisch <85 mmHg).
Ob unterschiedliche Antihypertensiva unterschiedlich effektiv in der Schlaganfallprävention sind, war bisher umstritten. Es werden folgende fünf Substanzklassen unterschieden: Angiotensin-Konversionsenzym-(ACE-)Hemmer, Angiotensin-II-Rezeptorblocker, Betablocker, Calciumantagonisten, Diuretika.
Die MOSES-Studie zeigte, dass der Angiotensin-II-Rezeptorblocker Eprosartan (z.B. Teveten®) dem Calciumantagonisten Nitrendipin (z.B. Bayotensin®) hinsichtlich Reduktion kardio- und zerebrovaskulärer Ereignisse in der Sekundärprophylaxe überlegen war [76]. Da beide Substanzen eine identische Blutdrucksenkung erzielten, kann postuliert werden, dass Angiotensin-II-Rezeptorblocker („Sartane“) möglicherweise zusätzliche pleiotrope Eigenschaften besitzen. Ähnliche Tendenzen fanden sich auch in den ACCESS-, LIFE- und SCOPE-Studien [17, 75].
Andere Studien zeigten einer Überlegenheit des Angiotensin-II-Rezeptorantagonisten Losartan (Lorzaar®) gegenüber dem Betablocker Atenolol (z.B. Tenormin®) [19]. Alphablocker waren weniger wirksam als andere Antihypertensiva [82]. Insgesamt unterscheiden sich die einzelnen Antihypertensiva jedoch nur geringfügig in ihrer schlaganfallpräventiven Wirkung.
Die konsequente Blutdrucksenkung nach einer frischen zerebralen Ischämie sollte ab dem 4. bis 5. Tag nach dem Ereignis begonnen werden. In den ersten Tagen ist ein erhöhter zerebraler Perfusionsdruck notwendig, um die sogenannte Penumbra, also das funktions- und perfusionsgestörte Hirnareal, welches noch nicht definitiv infarziert ist, zu schützen [59].
Bei hämodynamisch relevanten Stenosen ist die Dauer, in der hochnormale Blutdruckwerte anzustreben sind, möglicherweise länger zu wählen. Jedoch muss hier eine Nutzen-Risiko-Abwägung erfolgen, da die arterielle Hypertonie längerfristig den Progress der meist atherosklerotisch bedingten Stenose und damit das Schlaganfallrisiko unterstützt.
Neben der medikamentösen antihypertensiven Therapie wirken Diät (Diät mit viel Obst, Gemüse, fettarmer Milch, Geflügel, Fisch und Getreide, kochsalzarme Kost) und Ausdauersport unterstützend [72]. Mit diesen Maßnahmen kann eine mittlere Blutdrucksenkung von 11 mmHg erreicht werden.
Hypercholesterolämie
Während das Herzinfarktrisiko linear mit dem Serumcholesterolwert korreliert, ist ein solcher Zusammenhang für den Schlaganfall nicht nachgewiesen. Insgesamt konnte durch den Einsatz von CSE-Hemmern („Statinen“) eine Reduktion von Letalität und Myokardinfarktraten um 30 bis 40% erreicht werden.
Die Primärpräventionsstudien beziffern die durchschnittliche Risikoreduktion für Schlaganfälle durch CSE-Hemmer auf 11% (ALLHAT-Studie: Vergleich Pravastatin [z.B. Pravasin®] versus Plazebo) und 25% (Heart Protection Study: Vergleich Simvastatin [z.B. Zocor®] versus Plazebo) [43, 83]. In der CARDS-Studie, welche die Behandlung von Diabetikern mit Atorvastatin 10 mg versus Plazebo untersuchte, betrug die Risikoreduktion sogar 48% [18]. Dabei war die Risikoreduktion für einen Schlaganfall in den Studien unabhängig von den Serumcholesterolwerten. Die Sekundärpräventionsstudie SPARCL (Atorvastatin 80 mg versus Plazebo) zeigte eine signifikante Risikoreduktion für einen Schlaganfall, jedoch fand sich eine geringe Zunahme an Blutungsereignissen in der Atorvastatin-Gruppe [3].
Derzeit scheint eine routinemäßige Sekundärprophylaxe mit CSE-Hemmern bei Patienten mit zerebrovaskulären Erkrankungen und vaskulären Risikofaktoren auch bei normalem Serumcholesterol gerechtfertigt [20].
Die Wirkung der CSE-Hemmer beruht dabei zusätzlich zu der fettsenkenden Wirkung auf antiinflammatorischen, plaquestabilisierenden, vasodilatatorischen und blutdrucksenkenden Effekten. Die kardiologische Studie REVERSAL [62] verglich verschiedene CSE-Hemmer bei Patienten mit stabiler KHK, es wurde ein Vorteil von Atorvastatin gegenüber Pravastatin bezüglich der Plaqueprogression an den Koronargefäßen gezeigt. Unter Atorvastatin kam es zum Stillstand, zum Teil sogar zur Rückbildung des Plaquevolumens.
Eine sekundärpräventive Studie mit dem Fibrat Gemfibrozil (z.B. Gevilon®) zeigte nur eine Reduktion der Herzinfarktrate, nicht aber der Schlaganfallhäufigkeit [70].
Nicotinabusus
Rauchen steht in Assoziation mit der Entstehung der Atherosklerose und zählt somit zu den kardiovaskulären Risikofaktoren. Rauchen erhöht das Schlaganfallrisiko gegenüber Nichtrauchern um den Faktor 1,8 [33].
Es konnte nachgewiesen werden, dass durch Beenden des Nicotinabusus das Herzinfarktrisiko um rund 50% gesenkt wird. Randomisierte Studien zum Effekt des Einstellens des Rauchens auf das Schlaganfallrisiko fehlen. Ein ähnlicher Effekt wie für den Herzinfarkt scheint jedoch plausibel [47].
Diabetes mellitus
Auch der Diabetes mellitus unterstützt die Atherosklerosebildung (mit Makro- und Mikroangiopathie) und führt damit zu einem erhöhten Schlaganfallrisiko [35]. Dies betrifft beide Diabetes-mellitus-Typen. Wie in den Studien HOPE, UKPDS und Steno-2 gezeigt wurde, verlangsamt eine optimale Blutzuckereinstellung das Fortschreiten der Atherosklerose und vermindert so das Risiko aller kardiovaskulären Komplikationen im Rahmen der Primärprävention um 25 bis 50% [30, 32, 80]. Diese Ergebnisse erreichten allerdings kein Signifikanzniveau.
Zur Sekundärprävention gibt es bisher keine Studien. Ähnliche Ergebnisse wie in der Primärprävention sind jedoch zu erwarten.
Andere Risikofaktoren
Gewichtsreduktion und sportliche Aktivität besitzen indirekte Effekte auf das Schlaganfallrisiko (RRR 40–60%) durch positive Beeinflussung anderer Risikofaktoren wie arterieller Hypertonie, Hypercholesterolämie und Diabetes mellitus. Zusätzliche günstige Wirkungen auf Blutrheologie und Thrombozytenreaktivität wurden beschrieben [50, 51]. Die Effekte waren laut Framingham und Physicians’ Health Studien unabhängig vom Ausmaß der sportlichen Aktivität.
Karotisstenose
Einer Karotisstenose liegen in der Mehrzahl der Fälle atherosklerotische Veränderungen der Gefäßwand zugrunde. Der Grad der Verengung wird in der Regel im Ultraschall (Doppler/Duplex) beurteilt. Weitere bildgebende Verfahren wie Magnetresonanztomographie (MRT) und Computertomographie (CT) werden herangezogen, um die sonographischen Befunde zu verifizieren. Die Gefäßdarstellung in der MRT oder CT dient zudem der Klärung der Frage, ob in der Hirnregion, die von dem stenotischen Gefäß versorgt wird, Infarkte stattgefunden haben. Dies bietet Hinweise darauf, ob die Stenose hämodynamisch relevant ist (findet sich in der entsprechenden Hirnregion eine Verminderung/Verzögerung der Blutperfusion?). Nicht zuletzt kann anhand der MRT- oder CT-Bilder abgeschätzt werden, ob die Stenose einer interventionellen Therapie zugänglich ist. An interventionellen Methoden stehen die offene Operation und die perkutane transluminale Angioplastie (PTA) mit Ballondilatation mit oder ohne Stent-Implantation zur Verfügung.
Asymptomatische Karotisstenose. Die beiden bislang größten Studien zu dieser Thematik, ACAS aus Nordamerika mit 1600 Patienten [28] und ACST aus Europa mit 3100 Patienten [37], konnten zeigen, dass die Operation (Thrombendarteriektomie/TEA) bei Patienten mit einer asymptomatischen Karotisstenose und einem Stenosegrad >60% das Schlaganfallrisiko reduziert.
Seit 2005 wird die Operation asymptomatischer Karotisstenosen explizit in den Leitlinien der Deutschen Gesellschaft für Neurologie befürwortet. Dabei ist der Nutzen für folgende Patientengruppen besonders groß: Männer, jüngere Patienten <65 Jahre, Patienten mit nur mäßiger Stenose (60–80%) und Patienten mit stark erhöhtem Serum-Cholesterol (>250mg/dl) [37]. In den übrigen Fällen wird ein konservatives Prozedere mit sonographischen Kontrollen und Thrombozytenfunktionshemmung empfohlen.
Symptomatische Karotisstenose. Prädiktoren für ein erneutes ischämisches Ereignis (Rezidiv) sind, neben dem Stenosegrad, Stenosen im vertebrobasilären Bereich und weibliches Geschlecht. Der Nutzen der Operation bei symptomatischen >70%igen Karotisstenosen ist belegt [29, 69]. Patienten mit <50%igen Karotisstenosen profitieren nicht von einer Operation. Bei 50- bis 69%igen Stenosen ist der Vorteil der Operation sehr klein und betrifft nur Männer.
Bei einer symptomatischen Karotisstenose, also nach einer bereits abgelaufenen Hirnischämie, sollte die Intervention innerhalb der ersten 14 Tage nach dem Ereignis durchgeführt werden. Anschließend fand sich in den Studien gegenüber unbehandelten Stenosen kein präventiver Effekt mehr [69], was unter anderem mit dem stark erhöhten Risiko für ein Schlaganfallrezidiv in den ersten Tagen bis Wochen zusammenhängt.
Die Operation ersetzt nicht die Notwendigkeit einer Sekundärprophylaxe mit einem Thrombozytenfunktionshemmer. Sie sollte noch vor der Operation oder Angioplastie/Stent-Implantation begonnen und anschließend fortgeführt werden, vorzugsweise in Form einer niedrig dosierten ASS-Gabe (100–300 mg/d) [81].
Stent versus TEA. Die Daten zur Stent-Implantation (mit/ohne Ballondilatation) sind derzeit noch nicht abgesichert. Erste Ergebnisse weisen darauf hin, dass ähnliche Ergebnisse wie durch die Operation zu erzielen sind [93]. Die kürzlich veröffentlichten Ergebnisse der SPACE-Studie zum Verlauf innerhalb der ersten 30 Tage nach Stent versus Operation zeigten eine Überlegenheit der operativen Methode [77]. Daten der Langzeitverläufe liegen noch nicht vor.
Ein Stenting kommt vor allem in Betracht bei Patienten mit Rezidivstenosen nach TEA, bei hochgradigen Stenosen nach Strahlentherapie oder bei hoch sitzenden und einer chirurgischen Intervention schwer zugänglichen Stenosen. Eine Angioplastie ohne Stenting sollte bei extrakraniellen Stenosen angesichts der hohen Re-Stenoserate nicht mehr durchgeführt werden. Nach Einlage eines Stents wird die Gabe von Clopidogrel (75 mg/d) plus ASS (100 mg/d) für 1 bis 3 Monate empfohlen, anschließend die ASS-Monotherapie.
Die interventionelle Behandlung durch PTA mit oder ohne Stent-Implantation steht prinzipiell auch für die hinteren Halsschlagadern (Vertebralarterien) sowie für die intrakraniellen Gefäße zur Verfügung. Bei Stenosen der kleineren intrakraniellen Gefäße erfolgt bislang in der Regel nur eine Ballondilatation ohne Stent-Implantation in spezialisierten Zentren (größere Studien fehlen hierzu). In den übrigen Fällen ist die Thrombozytenfunktionshemmung indiziert.
Komplikationen. Wohl aufgrund einer sehr starken Selektion der Operateure waren in den großen Studien ACAS und ACST nur sehr geringe perioperativen Komplikationsraten von 2,7% (ACAS) und 3,1% (ACST) nachzuweisen [61]. Die Komplikationsraten bei unselektierten Operateuren hätten vermutlich um den Faktor 2 bis 3 höher gelegen. Ab einer Komplikationsrate >4% profitieren Patienten nicht mehr von der Operation [61].
Für die stentgestützte Ballonangioplastie liegen bislang keine prospektiven randomisierten Studien vor. Fallserien deuten jedoch darauf hin, dass deren periprozedurale Komplikationsrate ähnlich hoch liegt wie bei der Operation.
Komplikationen beruhen in erster Linie auf Embolien, Reperfusionstrauma und Re-Stenosen. Kleine Embolien können sowohl während der Operation als auch während der Angioplastie ausgelöst werden, sind jedoch klinisch meist nicht symptomatisch/nicht relevant. Die Angioplastie bietet gegenüber der TEA die Möglichkeit, einen größeren Embolus unmittelbar lokal zu lysieren. In der CARESS-Studie (Clopidogrel and aspirin for reduction of emboli in symptomatic carotid stenosis) wurde eine signifikante Reduktion asymptomatischer Mikroembolien bei Operation symptomatischer Karotisstenosen durch die Gabe von Clopidogrel plus ASS erreicht [56].
Ein Reperfusionstrauma kann sowohl nach TEA als auch nach PTA auftreten. Es entsteht dadurch, dass die poststenotischen Gefäße längerfristig maximal dilatiert waren [71] und sich nach erfolgter Intervention nicht rasch genug an die verbesserte Durchblutung anpassen/verengen können. Die Hyperperfusion äußert sich in Form von Kopfschmerzen, intrazerebralen Blutungen und Ödem. Eine strikte Blutdruckeinstellung im normotensiven Bereich kann diese Komplikationen weitestgehend vermeiden.
Re-Stenosen entstehen hauptsächlich durch Intima-/Media-Hyperplasie oder Narbenbildung. Sie sollten nur operiert werden, wenn sie symptomatisch sind.
Neben den interventionellen Maßnahmen können Gewichtsreduktion, Behandlung mit einem CSE-Hemmer und ACE-Hemmer das Voranschreiten einer Stenose verlangsamen [3, 89].
Dissektion der A. carotis interna oder A. vertebralis
Etwa 2,5% aller Schlaganfälle werden durch Dissektionen, also einen Einriss der inneren Gefäßwand der hirnversorgenden Arterien verursacht. Bei Patienten zwischen 30 und 45 Jahren macht dieser Anteil sogar 5 bis 25% aus [11]. Dissektionen treten hauptsächlich an den Karotiden im extrakraniellen Abschnitt auf, Rezidive sind sehr selten [74]. Als Pathomechanismus für einen Schlaganfall infolge einer Dissektion ist vornehmlich ein thrombembolisches Ereignis zu diskutieren. Seltener liegt ein hämodynamischer Mechanismus durch Stenosierung oder Okklusion des dissezierten Gefäßes zugrunde [74].
Entsprechend dieser Annahme wird nach einer Dissektion die zeitnahe Antikoagulation (initial mit niedermoluklarem oder unfraktioniertem Heparin, gefolgt von Vitamin-K-Antagonisten mit Ziel INR 2,0–3,0) empfohlen. Die Antikoagulation sollte über 3 Monate durchgeführt werden. Bei den meisten Patienten kommt es in dieser Zeit zur Rekanalisation. Sollte eine hämodynamisch relevante Stenose/Okklusion über diese Zeit hinaus fortbestehen (laut duplexsonographischer/CT- oder MR-angiographischer Befundkontrolle), sollte die Antikoagulation für weitere 3 Monate fortgesetzt werden. Danach sind Symptome nur noch äußerst selten zu erwarten [74]. Die Datenlage über Thrombozytenfunktionshemmer bei Dissektion ist unzureichend, randomisierte Studien existieren nicht. Eine Analyse von Studien und Fallserien über Karotisdissektionen und antithrombotische Therapie konnte aber keine signifikanten Unterschiede zur Antikoagulation bezüglich Schlaganfallrate, Outcome und Mortalität nachweisen [55].
Interventionelle Therapien, wie zum Beispiel die perkutane transluminale Angioplastie mit Stent-Implantation, sollten nur in Einzelfällen erwogen werden [53], da trotz sehr zufriedenstellender Kurzzeitergebnisse Komplikationen nicht selten auftreten.
Literatur
Das Literaturverzeichnis finden Sie im Internet:
www.ppt-online.de >Inhalt > 2007 > Heft 6
Dr. med. Hjördis Hentschel, Priv.-Doz. Dr. med. Georg Gahn, Klinik und Poliklinik für Neurologie, Universitätsklinikum Carl Gustav Carus der TU Dresden, Fetscherstraße 74, 01307 Dresden, E-Mail: Hjoerdis.Hentschel@neuro.med.tu-dresden.de
Die Leitlinie im Volltext:
Primär- und Sekundärprävention der zerebralen Ischämie. In: Kommission „Leitlinien der Deutschen Gesellschaft für Neurologie“, Diener HC et al. (Hrsg.). Leitlinien für Diagnostik und Therapie in der Neurologie. 3. Aufl. Stuttgart: Georg Thieme Verlag, 2005:192–214.
Aktualisierung 2007 in Akt Neurol 2007;34:8–12. Online unter www.dgn.org
Secondary prevention after ischemic stroke
One out of ten patients, who recently experienced an ischemic stroke, is likely to suffer from another event within the first year. Therefore, prevention of secondary events is essential.
About 10% of all ischemic strokes is caused by a stenosis of extra- or intracranial arteries, 30% can be explained by microvascular diseases. Another 30% of all events are due to cardiac embolism. In 30% of all cases, the reason for a stroke cannot be found.
Concomitant cardiovascular diseases, e.g. arterial hypertension, diabetes mellitus, hypercholesterinemia or smoking, are related to an increased risk for a stroke. Besides optimisation of these risk factors, the most important part of secondary prevention remains the treatment with platelet aggregation inhibitors. If a stenosis of extracranial or intracranial vessels is the cause of a stroke, interventional methods such as thrombendarterectomy or percutaneous transluminal angioplasty may be applied. Anticoagulation is usually recommended for prevention of cardiac embolism. Hemorrhagic stroke will not be discussed in this article.
Keywords: Stroke, ischemic, secondary prevention
Psychopharmakotherapie 2007; 14(06)
