Petra A. Thürmann, Wuppertal
Zulassung von Arzneimitteln – geschlechtsspezifische Aspekte
Voraussetzung für die Zulassung eines Arzneimittels ist der Nachweis seiner Wirksamkeit und Unbedenklichkeit in der beanspruchten Indikation [7]. Hierbei würde man selbstverständlich annehmen, dass mit der beanspruchten Indikation auch verknüpft wird, dass die Zielpopulation mit der betreffenden Erkrankung in möglichst vielen Ausprägungen (Alter, Geschlecht, Komorbidität, Nieren- und Leberfunktion) untersucht wurde. Angesichts der Tatsache jedoch, dass vor der Zulassung in der Regel etwa 3000 bis 5000 Patienten dem neuen Medikament exponiert werden, die üblicherweise sehr strenge Ein- und Ausschlusskriterien erfüllen mussten, ist es nicht verwunderlich, dass seltenere unerwünschte Wirkungen und manche Interaktionen erst später entdeckt werden [12].
In der Phase I werden in der Regel (außer bei zu toxischen Substanzen) gesunde, männliche Versuchspersonen dem neuen Arzneistoff ausgesetzt und es wird insbesondere die Pharmakokinetik überprüft [12]. Die gesunden Versuchspersonen genießen keinerlei therapeutischen Nutzen von dieser Exposition, daher ist hier eine besonders strenge Nutzen-Risiko-Abwägung zu treffen. Aufgrund der Erfahrungen mit Thalidomid (Contergan®) werden Frauen regelhaft ausgeschlossen, da sie potenziell schwanger werden könnten und das Risiko für das Ungeborene nicht abschätzbar ist [46]. Dies führt allerdings auch zu einem Verlust an Informationen, wenn beispielsweise die Pharmakokinetik bei Männern und Frauen unterschiedlich ist. In der Phase I wird außerdem versucht, eine erste Abschätzung der pharmakodynamischen Effekte vorzunehmen; sollten diese geschlechtsspezifisch unterschiedlich sein, wird man dies dementsprechend auch nicht erkennen.
In den Phasen II und III bei Patienten sollten selbstverständlich Frauen in der Häufigkeit repräsentiert sein, wie es auch bei der Erkrankung an sich der Fall ist. Wie Abbildung 1 (linke Hälfte) verdeutlicht, sind in zulassungsrelevanten Studien, die der amerikanischen Zulassungsbehörde FDA in den Jahren 1995 bis 1999 vorgelegt wurden, Frauen in Phase-I-Studien zu etwa 25% vertreten, in den weiteren Phasen offenbar zu einem adäquaten Anteil [5]. Allerdings ist diese Darstellung nur bezogen auf die Studien, in denen das Geschlecht der Teilnehmer bekannt war. Wie die rechte Hälfte der Abbildung verdeutlicht, wurde in einem nicht unerheblichen Teil der Studien das Geschlecht der Patienten gar nicht angegeben, und das trotz der Tatsache, dass die FDA im Jahre 1994 eine Guideline zur Beteiligung von Frauen in klinischen Studien herausgegeben hatte und neuere Dokumente sich mit geschlechtsspezifischen Subgruppenanalysen befassen [25].
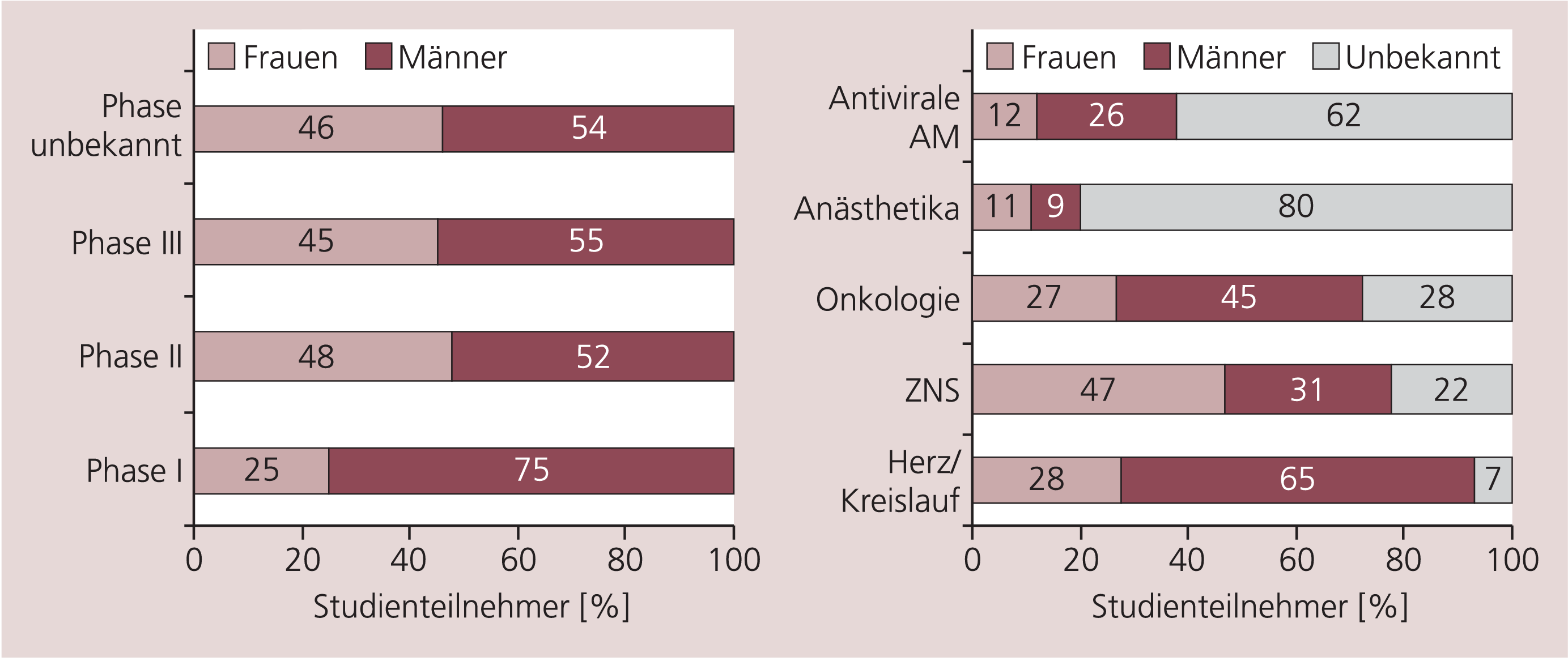
Abb. 1. Geschlechtsverteilung in 2581 Studien mit 334551 PatientInnen (außer Studien mit geschlechtsspezifischen Arzneimitteln) [nach 5]
Eine Analyse klinisch-pharmakologischer Fachzeitschriften aus dem Jahr 2001 mit insgesamt 239 Studien mit 15880 Versuchspersonen ergab, dass bei etwa der Hälfte der Studien mit gesunden Probanden Frauen ausgeschlossen waren, während bei den Patientenstudien zumindest Männer und Frauen (etwa 38%) beteiligt waren [6]. Bei öffentlich geförderten Studien lag der Frauenanteil im Mittel um 20,4% höher als bei Studien, die von der pharmazeutischen Industrie unterstützt wurden. Geschlechtsspezifische Subgruppenanalysen wurden nur selten durchgeführt, auch wenn die Studien mit Arzneimitteln erfolgten, für die geschlechtsspezifische Unterschiede bekannt sind [6].
Im Folgenden sollen basierend auf der Pharmakokinetik, der Pharmakodynamik und insbesondere im Hinblick auf die Verträglichkeit Beispiele für geschlechtsspezifische Unterschiede bei Arzneimitteln aufgezeigt und damit der Frage nach dem Off-Label-Gebrauch nachgegangen werden.
Geschlechtsspezifische Unterschiede bei der Pharmakokinetik
Aufgrund der Unterschiede zwischen Männern und Frauen bei Körpergröße, Muskelmasse, sowie Fett- und Wassergehalt sind Unterschiede bei der Verteilung von Arzneistoffen vorstellbar. Diese, sowie die antizipierte Variabilität infolge von hormonellen Schwankungen, führen dazu, dass Frauen in der Regel sogar von Bioäquivalenzstudien mit wohlbekannten Arzneistoffen ausgeschlossen werden. Eine aktuelle Analyse belegte allerdings, dass diese Vorkehrung nicht erforderlich ist [41].
Relevante Unterschiede sind im Wesentlichen für den Arzneistoff-Metabolismus bekannt. Etwa die Hälfte aller eingenommenen Arzneistoffe wird über das Cytochrom-P450-Enzymsystem metabolisiert, davon wiederum etwa die Hälfte über das Cytochrom P450-3A4 (CYP3A4). Dieses Enzym ist bei Frauen im Mittel etwas stärker exprimiert als bei Männern, wobei die Variabilität der Enzymexpression für CYP3A etwa um den Faktor 30 schwankt [45]. Substrate von CYP3A4 wie Methylprednisolon, Midazolam, Nifedipin und Verapamil werden bei Frauen meist schneller abgebaut als bei Männern [41].
Geschlechtsspezifische Unterschiede sind jedoch auch für andere Cytochrom-P450-Enzyme nachgewiesen. Der Betablocker Metoprolol wird überwiegend über CYP2D6 abgebaut; nach einer standardisierten Tagesdosis von 100 mg weisen Frauen etwa 40% höhere maximale Plasmakonzentrationen und eine etwa doppelt so hohe Fläche unter der Plasmakonzentrations-Zeit-Kurve wie Männer auf [20]. Dementsprechend sind blutdruck- und herzfrequenzsenkende Effekte auch bei Frauen deutlich ausgeprägter. Unter Einnahme von oralen Kontrazeptiva kommt es zu einem weiteren Anstieg der Metoprolol-Plasmaspiegel um etwa 50% [14]. Für den Betablocker Propranolol wurde bereits im Rahmen der Betablocker-Heart-Attack-Studie (BHAT) beobachtet, dass Frauen etwa 80% höhere Plasmaspiegel aufwiesen, wobei diese Substanz über CYP2D6 und CYP2C19 metabolisiert wird [44].
Da Betablocker über eine recht große therapeutische Breite verfügen und man in der Regel mit einer niedrigen Dosis die Therapie beginnt und nach Wirkung und Verträglichkeit steigert, werden eventuelle geschlechtsspezifische Unterschiede klinisch nicht erkannt. Die möglicherweise aus diesem Unterschied resultierenden Konsequenzen werden im Abschnitt Verträglichkeit näher dargestellt.
Venlafaxin ist ein CYP2D6-Substrat und durch enantioselektiven Metabolismus charakterisiert. Die Enantiomere von Venlafaxin haben unterschiedliche pharmakologische Wirkungen, wobei das (+)-Enantiomer überwiegend die Serotonin-Wiederaufnahme inhibiert, während das (–)-Enantiomer noradrenerge und serotonerge Aktivität aufweist. Interessanterweise wurde bei Frauen eine niedrigere Metabolisierungsrate für das (–)-Enantiomer bestimmt als bei Männern, was durch eine etwas schlechtere Funktion des CYP2D6 erklärt werden könnte [9]. Die daraus resultierenden etwas höheren Plasmaspiegel des (–)-Enantiomers korrelieren wiederum mit der Geschwindigkeit des Ansprechens auf eine Therapie [8].
Es liegen nur wenige systematische Untersuchungen zu geschlechtsspezifischen Unterschieden bei den Geno- und Phänotypen der Cytochrome vor. Nach derzeitigem Kenntnisstand gibt es möglicherweise jedoch bei der Verteilung der Genotypen geschlechtsspezifische Unterschiede [27], eventuell zusätzlich Unterschiede bei der phänotypischen Ausprägung. In Phänotypisierungsversuchen, beispielsweise mit Dextromethorphan zur Charakterisierung der CYP2D6-Aktivität, zeigte sich, dass Frauen – unabhängig von der Einnahme oraler Kontrazeptiva – etwas schlechtere Metabolisierer sind als Männer [11]. Einen etwas geringeren Unterschied sieht man für das Enzym CYP2C19, phänotypisiert mittels S-Mephenytoin und Omeprazol [17]. Dieses Enzym unterliegt einem starken Einfluss von oralen Kontrazeptiva, und zwar insbesondere bei Einnahme Estrogen- und Gestagen-haltiger Präparate.
Das Enzym CYP1A2, über welches beispielsweise Theophyllin und Coffein metabolisiert werden, weist ebenfalls eine geringere Aktivität bei Frauen als bei Männern auf. Dies führt zu etwa 35% höheren Plasmakonzentrationen von Clozapin und Norclozapin bei Frauen im Vergleich zu Männern [18]. Die Plasmakonzentrationen der Serotonin-Wiederaufnahmehemmer Fluvoxamin und Sertralin sind bei Frauen 70 bis 100% bzw. 50 bis 70% höher als bei Männern, dies wird auf unterschiedliche Aktivitäten von CYP1A2 und im Fall von Fluvoxamin auch auf CYP2C19 zurückgeführt [23]. Eine geschlechtsspezifische Analyse von drei vergleichenden Studien mit Clomipramin, Citalopram, Paroxetin und Moclobemid ergab keine signifikanten geschlechtsspezifischen Unterschiede in der Ansprechrate zwischen Männern und Frauen, lediglich die Clomipramin-Plasmaspiegel waren bei Frauen signifikant höher als bei Männern [13].
Cytochrome der P450-Familie gehören zu den Enzymen des so genannten Phase-I-Metabolismus. Aber auch der Phase-II-Metabolismus unterliegt offensichtlich hormonellen Einflüssen. So ist für Acetylsalicylsäure bekannt, dass sie bei Frauen etwa 30 bis 40% langsamer metabolisiert wird als bei Männern [24]. Die Clearance ist bei Frauen, die keine oralen Kontrazeptiva einnehmen, um etwa 30% reduziert, der Unterschied beruht auf dem Schritt der Glycinkonjugation [26]. Frauen, die orale Kontrazeptiva nehmen, haben dagegen fast die Eliminationskapazität von Männern. Ähnliche Befunde wurden auch für Paracetamol, Clofibrat und Phenprocoumon erhoben, die alle dem Stoffwechselschritt der Glukuronidierung unterliegen [41]. Ebenfalls im Phase-II-Metabolismus scheint die Ursache für die diskreten geschlechtsspezifischen Unterschiede in der Clearance von Fluorouracil zu liegen. Studien bei Patienten mit kolorektalen Karzinomen zeigten, dass der etwa 20%ige Unterschied in der Clearance [10] sich in einer signifikant höheren Rate an konzentrationsabhängiger Toxizität (Leukopenie, Mukositis, Diarrhö) manifestiert [36].
Geschlechtsspezifische Aspekte in der Pharmakodynamik und Wirksamkeit von Arzneimitteln
In Untersuchungen zur Patienten-kontrollierten postoperativen Analgesie mit Morphin-bestückten Schmerzpumpen benötigten Männer im Mittel 40% mehr Morphin, um Schmerzfreiheit zu erzielen, im Vergleich zu weiblichen Patienten [40]. Bei Frauen ist eine etwa 50% niedrigere Morphin-Konzentration am Rezeptor erforderlich als bei Männern, um ein vergleichbares Ausmaß der Analgesie zu erzielen [40]. Diese Rezeptorsensitivität wird durch den Befund unterstützt, dass Frauen besser auf Kappa-Opioide, zum Beispiel Pentazocin, ansprechen als Männer [40]. Im Hinblick auf unerwünschte Arzneimittelwirkungen wurde mehrfach dokumentiert, dass Frauen signifikant häufiger als Männer Übelkeit und Erbrechen nach Opioid-Gabe erleiden, sowohl postoperativ als auch in Notfallsituationen [40]. Frauen wachen nach einer körpergewichtsadaptierten standardisierten Narkose schneller auf als Männer, was möglicherweise an unterschiedlichen Empfindlichkeiten der Gamma-Aminobuttersäure-(GABA-)Rezeptoren liegt. Darüber hinaus können orale Progesteron-haltige Kontrazeptiva die Rezeptorbindung von Benzodiazepinen modifizieren; Frauen unter Progesteron-Einnahme reagieren signifikant stärker auf Triazolam i.v. als Frauen, die keine orale Kontrazeption anwenden [40].
Im Hinblick auf die Pharmakodynamik und Wirksamkeit von Antidepressiva ist zunächst zu beachten, dass Depressionen bei Frauen häufiger als bei Männern diagnostiziert und behandelt werden. Während Frauen im Mittel vermehrt unter Schlafstörungen, Schuldgefühlen und Somatisierungsstörungen sowie gleichzeitiger Angststörung leiden, so trifft man bei Männern vermehrt Alkohol- oder Drogen-Abusus [16].
So konnte in einer randomisierten Doppelblindstudie mit 105 Patienten mit Depression, charakterisiert mit >18 Punkten auf der Hamilton-Depressionsskala, gezeigt werden, dass Männer in allen Altersstufen auf Fluoxetin oder Maprotilin gleichermaßen gut ansprachen, während prämenopausale Frauen auf Fluoxetin besser anzusprechen schienen als auf Maprotilin. Nach der Menopause gab es hier keine Unterschiede mehr [21]. Mehrere Studien weisen mittlerweile darauf hin, dass prämenopausale Frauen besser auf einen selektiven Serotonin-Wiederaufnahmehemmer (SSRI) ansprechen, wohingegen postmenopausale Frauen eine vergleichbare Therapieresponse wie Männer auf trizyklische Antidepressiva oder Noradrenalin-Wiederaufnahmehemmer zeigen [15, 16, 21]. Allerdings gibt es bislang keine prospektiven, kontrollierten Studien zu diesen retrospektiven Beobachtungen.
Aus der Schizophreniebehandlung gibt es verschiedene Beobachtungen, dass Frauen niedrigere Dosen von Antipsychotika benötigen als Männer [35]. Möglicherweise sind unter anderem die bereits genannten pharmakokinetischen Unterschiede ein Grund hierfür. Es existiert allerdings auch die Hypothese, dass der vermehrte Nicotin-Konsum der männlichen Patienten (Rauchen induziert CYP1A2 sowie schwach CYP2D6) zu einem schnelleren Abbau der Substrate dieser Enzyme wie Haloperidol (CYP2D6) und Clozapin oder Olanzapin (CYP1A2) beiträgt [35]. Ferner könnte die häufigere Komedikation mit SSRI (Fluoxetin, Citalopram, Paroxetin und Fluvoxamin), die den Abbau einiger Neuroleptika hemmen, höhere Antipsychotika-Spiegel (z.B. Risperidon) und damit niedrigere erforderliche Dosen erklären [35].
Auch aus dem Herz-Kreislauf-System sind zahlreiche geschlechtsspezifische Unterschiede bekannt. Der ex vivo untersuchte Effekt von Acetylsalicylsäure (ASS) auf die Thrombozytenfunktion fällt bei Frauen schwächer aus als bei Männern [37]. Dies ist jedoch bestimmt nicht die Erklärung für die Befunde, dass niedrig dosierte ASS in der Primärprävention bei Frauen das Risiko für einen Herzinfarkt nicht reduziert, das Schlaganfallrisiko jedoch signifikant um 17% mindert [2, 30]. Frauen über 65 Jahre hingegen profitieren von einer Primärprävention mit ASS 100 mg jeden zweiten Tag im Hinblick auch auf Herzinfarkte und Gesamtsterblichkeit.
Ebenfalls deutliche Unterschiede zeigen sich bei den herzwirksamen Glykosiden (Digitalisglykosiden), die in Deutschland immer noch sehr oft verordnet werden. Eine retrospektive geschlechtsspezifische Analyse der DIG-Studie mit Patienten mit Herzinsuffizienz ergab, dass bei Frauen unter Digoxin-Therapie die Sterblichkeit höher ist als bei Frauen unter Plazebo, während bei Männern unter Digoxin die Sterblichkeit leicht abnimmt [29]. Wie in zahlreichen Studien zur Herzinsuffizienz gezeigt wurde, haben Frauen (selbst mit Digoxin) insgesamt eine bessere Überlebenswahrscheinlichkeit als Männer mit Herzinsuffizienz. Die Digoxin-Plasmakonzentrationen der Frauen in dieser Studie waren nicht häufiger im toxischen Bereich als bei Männern, ihre Spiegel lagen im Mittel um 0,1 µg/ml höher. Letztendlich ist dieser Unterschied ungeklärt. Es lässt sich daraus schlussfolgern, dass herzwirksame Glykoside bei Frauen vorsichtiger eingesetzt werden sollten als bei Männern, wobei keine Daten für das in Deutschland bevorzugte Digitoxin vorliegen.
Die bisher genannten Unterschiede zwischen Männern und Frauen in der Pharmakokinetik, der Pharmakodynamik und der Wirkung beziehungsweise Wirksamkeit im Hinblick auf Endpunkte wie Sterblichkeit spiegeln sich auch wider in den Befunden zur Verträglichkeit von Arzneimitteln, die teilweise bereits angesprochen wurden und im Folgenden noch näher beleuchtet werden sollen.
Geschlechtsspezifische Unterschiede in der Verträglichkeit von Arzneimitteln
Die höhere Rate von berichteten unerwünschten Arzneimittelwirkungen bei Frauen könnte zum einen auf der höheren Bereitschaft von Frauen beruhen, dem Arzt die Beschwerden zu kommunizieren, zum anderen jedoch auf dem deutlich höheren Arzneimittelgebrauch [33]. Martin et al. zeigten jedoch, dass die beobachtete Inzidenz unerwünschter Arzneimittelwirkungen pro 10000 Patientenmonate bei Frauen signifikant höher ist als bei Männern, das heißt, dass eine höhere Arzneistoffexposition bei Frauen nicht die erhöhte Rate unerwünschter Arzneimittelwirkungen erklärt [22].
Es ist hinreichend dokumentiert, dass QT-Verlängerung und Arzneistoff-induzierte Torsade-de-Pointes-Arrhythmien bei Frauen häufiger auftreten als bei Männern [3]. Für die QT-Verlängerung sind sogar zyklusabhängige Schwankungen beschrieben [31]. Dieser geschlechtsspezifische Unterschied lässt sich sogar beim isolierten Kaninchenherzen nachweisen [4]. Dementsprechend sind Neuroleptika-assoziierte QT-Verlängerungen ebenfalls häufiger bei Frauen anzutreffen [35].
Nicht nur die Herzreizleitung, sondern auch das zentrale Nervensystem ist bei Frauen für bestimmte Nebenwirkungen empfindlicher. So treten zentralnervöse Nebenwirkungen unter Mefloquin bei Frauen häufiger auf [34], obwohl unklar ist, ob höhere Mefloquin-Plasmakonzentrationen nicht doch eine Rolle spielen [42].
Für Neuroleptika zeigen sich hier neben den bereits erwähnten Effekten auf die Herzreizleitung zwei weitere auffällige geschlechtsspezifische Unterschiede. Bei Frauen scheint es in einem stärkeren Ausmaß als bei Männern zu Hyperprolaktinämien zu kommen, was möglicherweise das Osteoporoserisiko erhöht [1, 35]. Auch Adipositas und die metabolischen Störungen, die durch die atypischen Neuroleptika induziert werden, sind bei Frauen ausgeprägter als bei Männern [1, 35].
Aus der Datenbank der Arzneimittelkommission der Deutschen Ärzteschaft wurde eine Analyse schwerwiegender unerwünschter Arzneimittelwirkungen von Metoprolol durchgeführt mit dem Ziel, Einflüsse des bekannten genetischen Polymorphismus von CYP2D6 auf die Häufigkeit unerwünschter Arzneimittelwirkungen zu untersuchen. Unter den 24 ausgewählten Patienten mit unerwünschten Arzneimittelwirkungen befanden sich interessanterweise 18 Frauen; insgesamt waren so genannte „poor metaboliser“, also Menschen, die Metoprolol nur sehr langsam abbauen können, ebenfalls überproportional im Vergleich zur Normalbevölkerung vertreten [47]. Aus den Daten der nationalen Pharmakovigilanzzentren lässt sich ableiten, dass Frauen im Vergleich zu Männern statistisch signifikant häufiger schwerwiegende unerwünschte Arzneimittelwirkungen unter den Betablockern (Metoprolol, Propranolol, Carvedilol, Nebivolol) erleiden, die über CYP2D6 abgebaut werden. Bei den Betablockern, für die CYP2D6 keine Rolle spielt (Atenolol, Sotalol, Bisoprolol), gab es auch keine geschlechtsspezifischen Unterschiede bei den unerwünschten Arzneimittelwirkungen [39]. Unterschiedliche Quellen zu Verordnungsdaten in Deutschland weisen darauf hin, dass Betarezeptorenblocker bevorzugt an Männer verordnet werden, eine bevorzugte Verordnung von Betablockern an Frauen als Grund für die erhöhte Rate unerwünschter Arzneimittelwirkungen kann also weitgehend ausgeschlossen werden [39].
Während bei der QT-Verlängerung beispielsweise die geschlechtsbezogene unterschiedliche Pharmakodynamik eine Rolle spielt, liegen dem Beispiel mit den Betablockern Unterschiede in der Pharmakokinetik zugrunde. Im Gegensatz dazu ist die in Deutschland beobachtete Überdosierung mit herzwirksamen Glykosiden eher ein Dosierungsproblem: Knapp 80% der schwerwiegenden unerwünschten Arzneimittelwirkungen mit diesem Arzneistoff betreffen Frauen, in der Mehrzahl der Fälle ist die Missachtung des Körpergewichts bei der Dosierung ursächlich für eine unerwünschte Arzneimittelwirkung [32]. Die Missachtung von geschlechtsspezifischen Unterschieden beziehungsweise das Nichtwissen darüber führen jedoch nachweislich zu einem erhöhten Risiko für Frauen, eine unerwünschte Arzneimittelwirkung zu erleiden.
Zusammenfassung und Ausblick
Es gibt zahlreiche Hinweise für geschlechtsspezifische Unterschiede in der Pharmakokinetik, -dynamik, Wirksamkeit und Verträglichkeit von Arzneimitteln. Gerade die Häufung unerwünschter Arzneimittelwirkungen bei Frauen sollte Anlass zu einer differenzierteren Betrachtung, sowohl in der Forschung als auch bei der Verordnung, geben. In randomisierten Studien zur Wirksamkeit und Verträglichkeit von Pharmaka sind Frauen teilweise immer noch unterrepräsentiert [19, 43] beziehungsweise werden die Ergebnisse nicht geschlechtsspezifisch publiziert [6, 28].
Betrachtet man die in Deutschland vorhandenen Fachinformationen für Ärzte, so zeigt sich, dass potenzielle geschlechtsspezifische Unterschiede zunehmend beachtet werden: Hinweise auf geschlechtsspezifische Analysen oder Untersuchungen fanden sich nur in 10,2% der Fachinformationen zu neuen Wirkstoffen aus den Jahren 1989 bis 1994, hingegen bereits bei knapp der Hälfte aller Fachinformationen aus den Jahren 1999 bis 2004 (Abb. 2) [38]. Immerhin erfolgte in dem Zeitraum 1999 bis 2004 bei 18 Wirkstoffen ein Hinweis auf signifikante geschlechtsspezifische Unterschiede, überwiegend im Hinblick auf die Pharmakokinetik. Die eingangs erwähnten Kriterien für die Zulassung von Arzneistoffen in bestimmten Indikationen bei bestimmten Populationen werden somit auch zunehmend für die „Subgruppe“ der Frauen erfüllt, allerdings nicht immer adäquat kommuniziert und möglicherweise auch nicht ausreichend berücksichtigt.
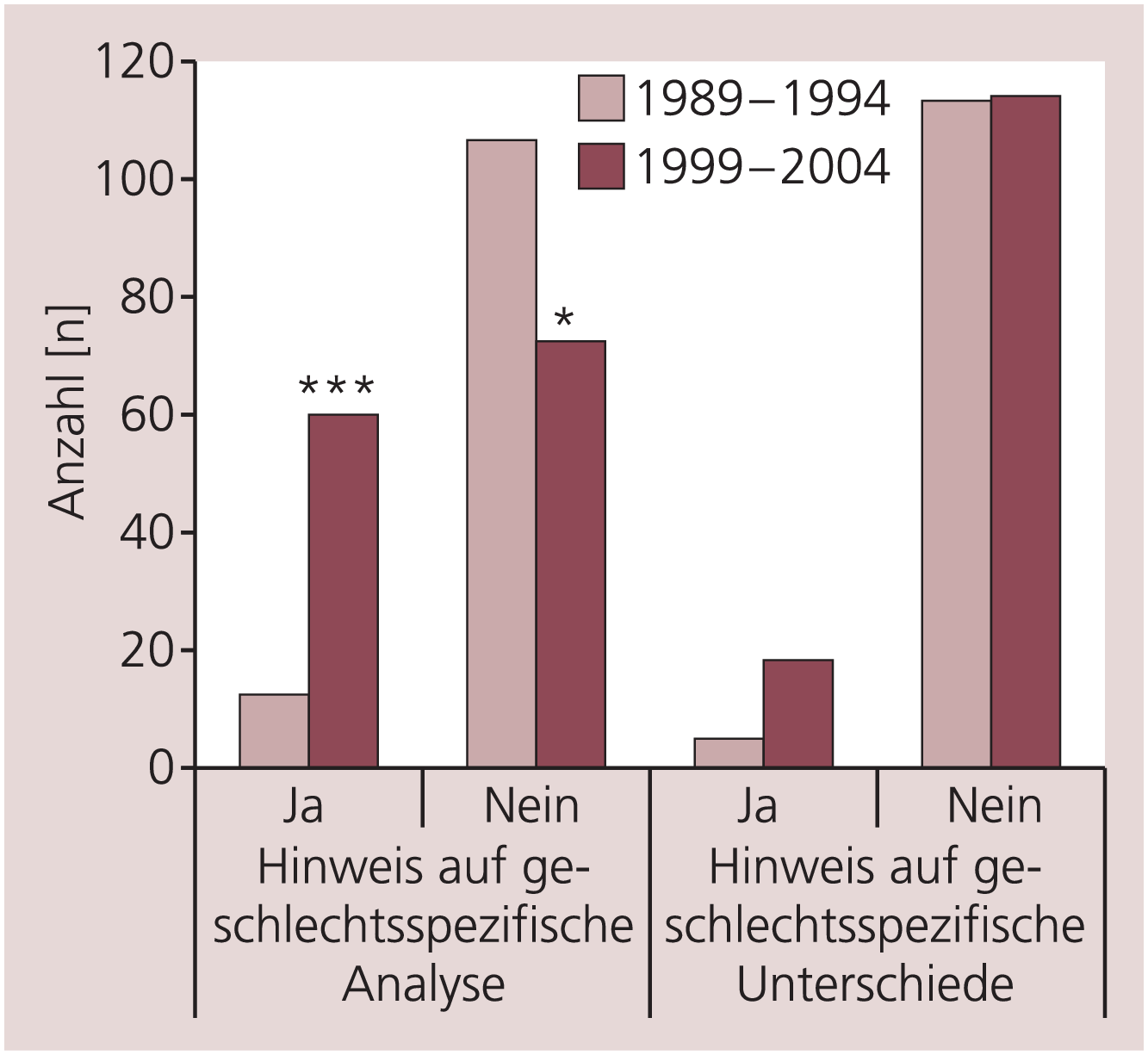
Abb. 2. Hinweise auf geschlechtsspezifische Analysen in Fachinformationen der Jahre 1989–1994 und 1999–2004 sowie tatsächlich gefundene geschlechtsspezifische Unterschiede (bezogen auf jeweils 118 und 132 Wirkstoffe, die für beiderlei Geschlecht zugelassen sind); *** p<0,0001; * p<0,05 [nach 47]
Literatur
1. Aichhorn W, Whitworth A, Weiss EM, Marksteiner J. Second-generation antipsychotics. Is there evidence for sex differences in pharmacokinetic and adverse effect profiles? Drug Saf 2006;29:578–98.
2. Berger J, Roncaglioni MC, Avanzini F, Pangrazzi I, et al. Aspirin for the primary prevention of cardiovascular events in women and men. JAMA 2006;295:306–13.
3. Drici MD, Clement N. Is gender a risk factor for adverse drug reactions? The example of drug-induced long QT syndrome. Drug Saf 2001;24:575–85.
4. Ebert SN, Liu XK, Woosley RL. Female gender as a risk factor for drug-induced cardiac arrhythmias: evaluation of clinical and experimental evidence. J Women’s Health 1998;7:547–57.
5. Evelyn B, Toigo T, Banks D, Pohl D, et al. Women’s participation in clinical trials and gender-related labeling. A review of new molecular entities approved 1995–1999. FDA, August 24, 2001. www.fda.gov/cder/reports/womens_health/women_clin_trials.htmwww.fda.gov/cder/reports/womens_health/women_clin_trials.htm (letzter Zugriff: 23.07.2007)
6. Fleisch J, Fleisch MC, Thürmann PA. Women in early-phase clinical drug trials: have things changed over the past 20 years? Clin Pharmacol Ther 2005;78:445–52.
7. Gesetz über den Verkehr mit Arzneimitteln. (Arzneimittelgesetz – AMG) 14.8.2006 www.bmg.bund.de/cln_040/nn_603266/SharedDocs/Gesetzestexte/Arzneimittel/AMG,templateId=raw,property=publicationFile.pdf/AMG.pdfZulassungskriterien
8. Gex-Fabry M, Balant-Gorgia AE, Balant LP, Rudaz S, et al. Time course of clinical response to venlafaxine: relevance of plasma level and chirality. Eur J Clin Pharmacol 2004;59:883–91.
9. Gex-Fabry M, Rudaz S, Balant-Gorgia AE, Brachet A, et al. Steady-state concentration of venlafaxine enantiomers: model-based analysis of between-patient variability. Eur J Clin Pharmacol 2002;58:323–31.
10. Gusella M, Toso S, Ferrazzi E, Ferrari M, et al. Relationship between body composition parameters and fluorouracil pharmacokinetics. Br J Clin Pharmacol 2002;54: 131–9.
11. Hägg S, Spigset O, Dahlqvist R. Influence of gender and oral contraceptives on CYP2D6 and CYP2C19 activity in healthy volunteers. Br J Clin Pharmacol 2001;51:169–73.
12. Hasford J, Staib AH (Hrsg.). Arzneimittelprüfungen und Good Clinical Practice. Planung, Durchführung und Qualitätssicherung. München: MMV Medizin Verlag, 1994.
13. Hildebrandt MG, Steyerberg EW, Stage KB, Passchier J, et al. Are gender differences important for the clinical effects of antidepressants? Am J Psychiatry 2003;160:1643–50.
14. Kendall MJ, Quarterman CP, Jack DB, Beeley L. Metoprolol pharmacokinetics and the oral contraceptive pill. Br J Clin Pharmacol 1982;14:120–2.
15. Kornstein SG, Schatzberg AF, Thase ME, Yonkers KA, et al. Gender differences in treatment response to sertraline versus imipramine in chronic depression. Am J Psychiatry 2000;157:1445–52.
16. Kornstein SG, Sloan DM, Thase ME. Gender-differences in depression and treatment response. Psychopharmacol Bull 2002;36:99–112.
17. Laine K, Tybring G, Bertilsson L. No sex-related differences but significant inhibition by oral contraceptives of CYP2C19 activity as measured by the probe drugs mephenytoin and omeprazole in healthy Swedish white subjects. Clin Pharm Ther 2000;68:151–9.
18. Lane H-Y, Chang Y-C, Chang W-H, Link SK, et al. Effects of gender and age in plasma levels of clozapine and its metabolites: analyzed by critical statistics. J Clin Psych 1999;60: 36–40.
19. Lee PY, Alexander KP, Hammill BG, Pasquali SK, et al. Representation of elderly persons and women in published randomized trials of acute coronary syndromes. JAMA 2001;286:708–13.
20. Luzier AB, Killian A, Wilton JH, Wilson MF, et al. Gender-related effects on metoprolol pharmacokinetics and pharmacodynamics in healthy volunteers. Clin Pharm Ther 1999;66:594–601.
21. Martenyi F, Dossenbach M, Mraz K, Metcalfe S. Gender differences in the efficacy of fluoxetine and maprotiline in depressed patients: a double-blind trial of antidepressants with serotonergic or norepinephrinergic reuptake inhibition profile. Eur Neuropsychopharmacol 2001;11:227–32.
22. Martin R, Biswas PN, Freemantle SN, Pearce GL, et al. Age and sex distribution of suspected adverse drug reactions to newly marketed drugs in general practice in England: analysis of 48 cohort studies. Br J Clin Pharmacol 1998;46:505–11.
23. Meibohm B, Beierle I, Derendorf H. How important are gender differences in pharmacokinetics? Clin Pharmacokinet 2002;41:329–42.
24. Menguy R, Desbaillets L, Masters YF, Okabe S. Evidence for a sex-linked difference in aspirin metabolism. Nature 1972;239:102–3.
25. Merkatz RB. Women in clinical trials of new drugs. A change in the Food and Drug Administration policy. N Engl J Med 1993;329: 292–6.
26. Miners JO, Grgurinovich N, Whitehead AG, Robson RA, et al. Influence of gender and oral contraceptive steroids on the metabolism of salicylic acid and acetylsalicylic acid. Br J Clin Pharmacol 1986;22:135–42.
27. Payami H, Zhu M, Montimurro J, Keefe R, et al. One step closer to fixing association studies: evidence for age- and gender-specific allele frequency variations and deviations from Hardy-Weinberg expectations in controls. Hum Genet 2005;118:322–30.
28. Pinn VW. Sex and gender factors in medical studies. Implications for health and clinical practice. JAMA 2003;289:397–400.
29. Rathore SS, Wang Y, Krumholz HM. Sex-based differences in the effect of digoxin for the treatment of heart failure. N Engl J Med 2002;347:1403–11.
30. Ridker PM, Cook NR, Lee I-M, Gordon D, et al. A randomized trial of low-dose aspirin in the primary prevention of cardiovascular disease in women. N Engl J Med 2005;352:1293–304.
31. Rodriguez I, Kilborn MJ, Liu XK, Pezzullo JC, et al. Drug-induced QT prolongation in women during the menstrual cycle. JAMA 2001;285:1322–6.
32. Schmiedl S, Szymanski J, Rottenkolber M, Drewelow B, et al. Drug-related hospital admissions with digitalis glycosides. Drug Saf 2006;29:945 (abstr. 63).
33. Schröder H, Selke W. Arzneimittelverordnungen nach Alter und Geschlecht. In: Schwabe U, Paffrath D (Hrsg.). Arzneiverordnungsreport 2000. Berlin: Springer Verlag, 2000:770–83.
34. Schwartz E, Potasman I, Rotenberg M, Almog S, et al. Serious adverse events of mefloquine in relation to blood level and gender. Am J Trop Med Hyg 2001;65:189–92.
35. Seeman MV. Gender differences in prescribing of antipsychotic drugs. Am J Psychiatry 2004;161:1324–33.
36. Sloan JA, Goldberg RM, Sargent DJ, Vargas-Chanes D, et al. Women experience greater toxicity with fluorouracil-based chemotherapy for colorectal cancer. J Clin Oncol 2002;20:1491–8.
37. Spranger M, Aspey BS, Harrison MJG. Sex difference in antithrombotic effect of aspirin. Stroke 1989;20:34–7.
38. Tenter U, Thürmann PA. References to sex-specific differences of drug effects in german SPCs for new entities from 1999–2004 [Abstract]. Int J Clin Pharmacol Ther 2006;44:531.
39. Thürmann PA, Haack S, Werner U, Szymanski J, et al. Tolerability of beta-blockers metabolized via cytochrome P450-2D6 is sex-dependent. Clin Pharmacol Ther 2006;80:551–3.
40. Thürmann PA. Geschlechtsspezifische Aspekte in der Pharmakotherapie: was ist gesichert? Z Allg Med 2006;82:380–4.
41. Thürmann PA. Geschlechtsspezifische Unterschiede bei der Pharmakokinetik und -dynamik von Arzneimitteln. Bundesgesundheitsbl Gesundheitsforsch Gesundheitsschutz 2005;48:536–40.
42. van Riemsdijk MM, Sturkenboom MCJM, Ditters JM, Tulen JH, et al. Low body mass index is associated with an increased risk of neuropsychiatric adverse events and concentration impairment in women on mefloquine. Br J Clin Pharmacol 2004;57:506–12.
43. Vidaver RM, Lafleur B, Tong C, Bradshaw R, et al. Women subjects in NIH-funded clinical research literature: lack of progress in both representation and analysis by sex. J Womens Health Gend Based Med 2000;9:495–504.
44. Walle T, Byington RP, Furberg CD, McIntyre KM, et al. Biologic determinants of propranolol disposition: results from 1,308 patients in the beta-blocker heart attack trial. Clin Pharmacol Ther 1985;38:509–18.
45. Wolbold R, Klein K, Burk O, Nüssler AK, et al. Sex is a major determinant of CYP3A4 expression in human liver. Hepatology 2003; 38:978–88.
46. Wright DT, Chew NJ. Women as subjects in clinical research. Appl Clin Trials 1996;5:44–54.
47. Wuttke H, Rau T, Heide R, Bergmann K, et al. Increased frequency of cytochrome P450-2D6 poor metabolizers among patients with metoprolol-associated adverse effects. Clin Pharmacol Ther 2002;72:429–37.
Prof. Dr. med. Petra A. Thürmann, Philipp Klee-Institut für Klinische Pharmakologie, HELIOS Klinikum Wuppertal, Lehrstuhl für Klinische Pharmakologie, Universität Witten/Herdecke, Heusnerstr. 40, 42283 Wuppertal, E-Mail: petra.thuermann@helios-kliniken.de
Drug therapy in women: “Off-label use”?
For many drugs, and this applies also for psychotropic drugs, sex-specific differences have been observed with regards to metabolism, adverse drug reactions and treatment response. Sex-specific differences have been demonstrated for clozapine, venlafaxine and fluvoxamine, where women exhibit higher plasma concentrations when compared to men. Hormone-dependent differences have also been shown for benzodiazepines, opioids and other sedatives/hypnotics. Men and women differ with regard to symptoms of depression and psychosis. This may – at least in part – explain differences in treatment response to different drug classes. The complex interaction between sex – or gender – and pharmacokinetics, pharmacodynamics and symptomatology is difficult to incorporate into the frame of randomized, controlled clinical trials. Sub-group analyses are often not adequately powered to confirm in a statistically correct way sex-specific differences.
Off-label use means use of a drug outside its labelled indication. Psychotropic drugs on the German market are licensed for men and women, i.e., there is no off-label use when prescribing these drugs to women. However, many sex-differences with respect to psychopharmacotherapy are not yet well described, are not included in the design of most clinical trials and will therefore remain field for future research.
Keywords: Sex-specific, pharmacokinetics, clinical trials, drug treatment, psychotropic drugs
Psychopharmakotherapie 2007; 14(06)
