Wiebke Schrempf und Tjalf Ziemssen, Dresden
Multiple Sklerose
Die multiple Sklerose (MS) ist eine autoimmun-vermittelte Erkrankung mit einer Prävalenz von etwa 50/100000 in der europäischen Bevölkerung und ist damit in Nordeuropa die häufigste chronisch-entzündliche Erkrankung des zentralen Nervensystems. In Deutschland sind etwa 100000 Menschen erkrankt; die jährliche Inzidenz liegt bei etwa 5/100000 Einwohner. Die multiple Sklerose betrifft vorwiegend Frauen (F:M 1,7:1) in einem Alter zwischen 20 und 40 Jahren. Die Erkrankung ist durch eine Demyelinisierung der weißen Substanz – insbesondere der Markscheiden – mit Infiltration von Entzündungszellen und durch eine axonale Degeneration gekennzeichnet [27]. Verschiedene histopathologische Muster der Entmarkung können für Subgruppen von Patienten beschrieben werden [19]. Klinisch lassen sich schubförmig-remittierende Verläufe von primär und sekundär chronisch-progredienten Verläufen mit und ohne aufgelagerte Schübe unterscheiden. Bei über 80% der Patienten beginnt die Erkrankung zunächst mit einem schubförmigen Verlauf (RRMS). Eine hohe Anzahl an Schüben in den ersten Jahren ist mit einer schlechteren Prognose und einer rascheren Progredienz der Erkrankung vergesellschaftet [35]. Im Verlauf der Erkrankung gehen 50 bis 60% der initial schubförmig verlaufenden Formen in einen sekundär chronisch-progredienten Verlauf (SPMS) über.
Die Pathogenese der MS ist bisher nicht abschließend geklärt, sowohl genetischen als auch Umweltfaktoren sowie noch nicht endgültig erfassten Auslösefaktoren wird eine Rolle zugeschrieben. Die Entzündung des zentralen Nervensystems (ZNS) wird durch Myelin-spezifische, autoreaktive T-Lymphozyten verursacht, insbesondere durch CD4- T-Zellen, die nach Aktivierung durch die Erkennung ihres spezifischen Antigens über die Blut-Hirn-Schranke ins Gehirn einwandern können. Diese sezernieren proinflammatorische Zytokine wie Interferon gamma (IFN-γ) und Tumornekrosefaktor alpha (TNF-α) sowie Chemokine und initiieren so eine Entzündungskaskade, die zur Rekrutierung von Monozyten und Makrophagen führt und die konsekutive Zerstörung des Myelins zur Folge hat. Insbesondere führen die Zytokine auch zur Expression von Adhäsionsmolekülen auf Makrophagen und Endothelzellen sowie Gliazellen des ZNS. Die experimentelle autoimmune Enzephalomyelitis (EAE), das Tiermodell der MS, konnte durch die Immunisierung mit Myelinbestandteilen sowie den Transfer von Myelin-spezifischen T-Zellen ausgelöst werden.
Leukozytenmigration
Die Einwanderung von Leukozyten über die Blut-Hirn-Schranke ins ZNS wird als einer der entscheidenden Faktoren in der Pathogenese der MS angesehen. Diese Einwanderung wird durch ein komplexes Zusammenspiel von Adhäsionsmolekülen, Zytokinen und Chemokinen auf Immun- und Endothelzellen geregelt. Die Auswanderung der Leukozyten ins Gewebe beginnt mit der initialen Anheftung an die Endotheloberfläche durch die Interaktion mit Selectinen (E- und P-Selectinen). Selectine werden konstitutiv auf der Oberfläche von Endothelzellen, Leukozyten und Thrombozyten exprimiert [18]. Die Leukozyten rollen durch die Selectin-Bindung auf der Endotheloberfäche, bis sie dort endgültig abstoppen, fest an die endotheliale Oberfläche binden und die Gefäßwand durchwandern können.
Die auf den Leukozyten für den Adhäsionsprozess verantwortlichen Integrine bestehen aus einer Alpha- (a1–4) und einer Beta-Untereinheit (b1, b2 und b7). Integrine müssen zunächst aktiviert werden, dies geschieht durch Chemokine, die an G-Protein-gekoppelte Rezeptoren auf den Lymphozyten binden. Für die Migration über die Blut-Hirn-Schranke ist vor allem das Alpha-4-Integrin (α4β1, very late antigen 4 [VLA-4]) und dessen Interaktion mit VCAM-1 (vascular cell adhesion molecule 1) verantwortlich [31, 36], während die Interaktion von α4β7 mit MadCAM-1 (mucosal addressin cell adhesion molecule 1) vornehmlich bei den chronisch entzündlichen Darmerkrankungen eine Rolle zu spielen scheint. Die Expression von Adhäsionsmolekülen in entzündetem Gewebe wird durch proinflammatorische Zytokine wie TNF-α und Interleukin 1 (IL-1) gefördert.
Die Aktivierung der T-Zellen erfolgt in der Peripherie nach Interaktion mit den Antigen-präsentierenden Zellen (APC) über den T-Zell-Rezeptor, Korezeptoren sowie kostimulatorische Signale. Diese aktivierten T-Zellen sind in der Lage, die Blut-Hirn-Schranke durch Wechselwirkung mit Adhäsionsmolekülen des Endothels zu durchwandern [17]. Im Gehirn treffen diese T-Zellen auf ihre spezifischen Zielantigene, die ihnen von lokalen APC, vor allem Mikroglia, präsentiert werden. Dies führt zur weiteren Freisetzung proinflammatorischer Zytokine mit direkten gewebsdestruierenden Folgen sowie Rekrutierung von weiteren Entzündungszellen an den Läsionsort. Auch die zusätzlich sezernierten freien Radikale können zur direkten zytotoxischen Schädigung der weißen Substanz führen.
Wirkungsmechanismen von Natalizumab
Natalizumab ist ein IgG4-Antikörper, bei dem zur Reduktion der Immunogenität und um die Halbwertszeit zu verlängern, die Antigen-bindenden Domänen in ein humanes Immunglobulingerüst kloniert wurden. Dadurch wurde der Antikörper zu 99% humanisiert. Die IgG4-Subklasse wurde aufgrund der fehlenden Komplementaktivierung und der relativ längeren Verweildauer in der Zirkulation gewählt. Dieser monoklonale Antikörper inhibiert sowohl die Interaktion von VCAM-1 als auch von MadCAM-1 mit den Integrinen α4β1 beziehungsweise α4β7 [11]. Zudem ließ sich nachweisen, dass die durch Bindung des Alpha-4-Integrins an Fibronectin induzierte Migration von mononukleären Zellen zusätzlich inhibiert werden konnte [22]. Natalizumab blockiert somit die Einwanderung von Leukozyten sowohl über die Blut-Hirn-Schranke (Abb. 1) als auch in andere Gewebe. So wurden bereits mehrere Studien an Patienten mit entzündlichen Darmerkrankungen durchgeführt, die einen positiven Effekt auf die Erkrankungen nachweisen konnten.
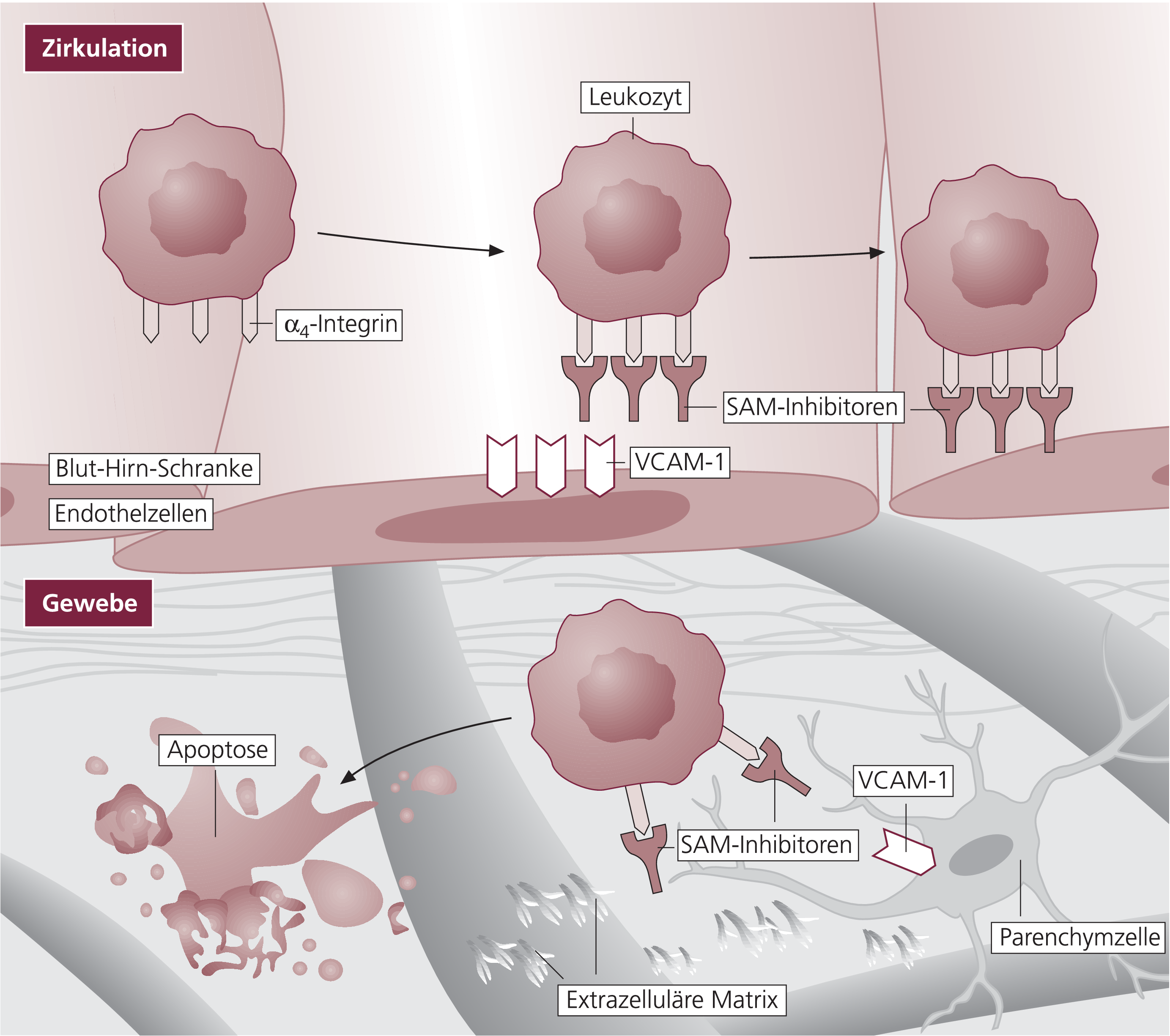
Abb. 1. Wirkungsmechanismus von Natalizumab: Inhibition der Leukozytenmigration an der Blut-Hirn-Schranke (SAM-Inhibitoren = selektive Adhäsionsmolekül-Inhibitoren)
Sowohl bei MS-Patienten als auch im Tiermodell konnte nachgewiesen werden, dass die VCAM-1-Expression auf Endothelzellen, die normalerweise gering ist, durch Entzündung erhöht und auch in MS-Plaques hochreguliert ist [17]. Die Injektion eines monoklonalen α4β1-Antikörpers im Tiermodell der EAE konnte die Schwere der Erkrankung abschwächen oder die Induktion der Erkrankung verhindern, wobei dieser protektive Effekt des Antikörpers dosisabhängig war [2]. Möglicherweise spielt α4β7-Integrin eine Rolle in der chronischen Phase der EAE, es scheint jedoch nicht die Entwicklung der Erkrankung selbst am Anfang der Erkrankung verhindern zu können [10].
Stüve und Kollegen wiesen nach, dass die Behandlung mit Natalizumab zu einer dramatischen Abnahme der mononukleären Zellen im Liquor führt. Hierbei ließ sich nicht nur eine Reduktion der CD4- und der CD8-Lymphozyten, sondern auch der B-Zellen und Plasmazellen nachweisen [29]. Zudem konnte nachgewiesen werden, dass die Expression von Alpha-4-Integrinen auf B-Zellen und Monozyten sogar höher ist als auf T-Zellen, zudem zeigten CD8-T-Zellen höhere Level als CD4-T-Zellen [22]. Insgesamt scheinen sowohl Effekte auf das zelluläre als auch das humorale Immunsystem zu bestehen.
Klinische Studien zu Natalizumab
Phase-II-Studien
In einer randomisierten, doppelblinden Phase-II-Studie mit 72 Patienten mit schubförmiger oder sekundär chronisch-progredienter MS wurde der Effekt von vierwöchentlichen Infusionen von Natalizumab in einer Dosis von 3 mg/kg Körpergewicht (KG) gegen Plazebo über einen Zeitraum von drei Monaten und weitere drei Monate nach Beendigung der Natalizumab-Applikation untersucht. Während der ersten 12 Wochen ließ sich eine signifikante Reduktion der Kontrastmittel-aufnehmenden oder aktiven T1-Läsionen (p<0,042 bzw. 0,017) nachweisen, in den 12 Wochen nach Ende der Therapie gab es jedoch keine signifikanten Unterschiede [30].
In einer randomisierten, doppelblinden, multizentrischen, Plazebo-kontrollierten Studie, die bei 180 Patienten mit schubförmiger MS oder sekundär chronischprogredienter MS mit aufgelagerten Schüben durchgeführt wurde, wurde insbesondere die Wirkung auf Schübe untersucht. Patienten mit Schubsymptomen wurden innerhalb von 24 bis 96 Stunden nach Symptombeginn eingeschlossen und mit einer Infusion von Natalizumab in einer Dosis von 1 oder 3 mg/kg KG oder Plazebo behandelt und über 14 Wochen nachbeobachtet. In dieser Studie ließ sich auch aufgrund der kurzen Studiendauer insgesamt keine Verbesserung auf der Kurtzke Expanded Disability Status Scale (EDSS) nachweisen, lediglich zwei beziehungsweise vier Wochen nach Applikation zeigte sich eine vorübergehende Abnahme des EDSS-Scores [23].
In einer weiteren randomisierten, multizentrischen, Plazebo-kontrollierten Studie bei 213 Patienten mit sekundär chronisch-progredienter oder schubförmiger MS sollte insbesondere die Sicherheit und Wirksamkeit von Natalizumab untersucht werden. Die Patienten erhielten über sechs Monate entweder Infusionen mit Plazebo oder 3 bzw. 6 mg/kg KG Natalizumab in monatlichen Abständen. Der primäre Zielparameter waren neu aufgetretene, Kontrastmittel-anreichernde (Gd+) T1-Läsionen im MRT [21], zusätzlich wurden auch T2-Läsionen und klinische Parameter wie beispielsweise Schubanzahl und EDSS berücksichtigt. In dieser Studie konnte bei allen Patienten zusammen eine Reduktion der neuen Gd+-Läsionen sowohl in der 3-mg/kg- als auch in der 6-mg/kg-Gruppe nachgewiesen werden (9,6 vs. 0,7 [p<0,001] bzw. 1,1 [p<0,001] Läsionen). Zudem zeigten sich weniger Läsionen mit persistierender Kontrastmittel-Aufnahme und eine Abnahme des Gesamtvolumens der Gd+-Herde. In der Plazebo-Gruppe erlitten 83% der Patienten einen Schub während der sechsmonatigen Studiendauer, hingegen nur 19% der Patienten sowohl in der 3-mg/kg- (p=0,02) als auch in der 6-mg/kg-Gruppe (p=0,02).
Phase-III-Studien
AFFIRM. In der AFFIRM-Studie wurden 942 Patienten eingeschlossen und erhielten entweder Plazebo (315 Patienten) oder Natalizumab (627 Patienten) als Monotherapie [24]. Die Infusionen des Medikaments erfolgte über 116 Wochen in einer Dosis von 300 mg i.v. alle vier Wochen. Der primäre Endpunkt nach einem Jahr war die Anzahl der Schübe, sekundäre Endpunkte waren die Anzahl neuer oder sich vergrößernder T2-hyperintenser Läsionen im MRT, die Anzahl der Gd+-Läsionen im MRT und die Anzahl der schubfreien Patienten. Als primärer Endpunkt nach zwei Jahren wurde die kumulative Wahrscheinlichkeit einer anhaltenden Behinderungsprogression gemessen am EDSS-Score gewählt. Sekundäre Endpunkte waren die Anzahl der Schübe, das Volumen T2-hyperintenser Läsionen, die Anzahl neuer hypointenser T1-Läsionen und die Behinderungsprogression gemessen am Multiple Sclerosis Functional Composite (MSFC).
Die relative Schubrate als primärer Endpunkt der Studie reduzierte sich im ersten Jahr in der Natalizumab-Gruppe um 68% (0,26 Schübe/Jahr vs. 0,81 Schübe/Jahr, p<0,001). Dieser Effekt bestätigte sich auch nach zwei Jahren (Abb. 2). Der Anteil der schubfreien Patienten war in der Natalizumab-Gruppe signifikant höher als in der Plazebo-Gruppe (77 vs. 56%, p<0,001 im 1. Jahr; 67 vs. 41%, p<0,001 im 2. Jahr). Natalizumab reduzierte das Risiko eines erneuten Schubs um 59% (p<0,001). Die Analyse der Patienten, die die Studie nicht beendeten, zeigte keinen Anhalt für eine Zunahme der Schübe nach Absetzen des Medikaments (so genannter Rebound), sondern eine vergleichbare Krankheitsaktivität wie vor Beginn der Therapie. Die Wahrscheinlichkeit einer anhaltenden Behinderungsprogression nach zwei Jahren war unter der Therapie mit Natalizumab signifikant geringer als unter Plazebo (17% vs. 29%, p<0,001). Dies entspricht einer Reduktion um 12 Prozentpunkte beziehungsweise einer 42%igen Reduktion des relativen Risikos einer Behinderungsprogression. Die Anzahl neuer und an Größe zunehmender T2-hyperintenser Läsionen war im Vergleich zu Plazebo nach zwei Jahren um 83% reduziert (p<0,001), bei 57% der mit Natalizumab behandelten Patienten fanden sich keine neuen oder an Größe zunehmenden T2-hyperintensen Läsionen im Vergleich zu 15% in der Plazebo-Gruppe. Hingegen hatten 68% der Patienten der Plazebo-Gruppe mindestens drei neue oder vergrößerte hyperintense Läsionen, in der Verum-Gruppe jedoch nur 18%. Die Anzahl der Gd+-Läsionen im MRT wurde durch Natalizumab sowohl nach einem als auch nach zwei Jahren um 92% reduziert (p<0,001), zudem waren bei 97% der mit Natalizumab behandelten Patienten keine Gd+-Läsionen im MRT nachweisbar, bei den Plazebo-Patienten hingegen lediglich bei 72%. 9% der Patienten der Verum-Gruppe entwickelten während des Studienverlaufs neutralisierende Antikörper. Bei 6% persistierten die Antikörper, bei diesen trat zusätzlich eine erhöhte Komplikationsrate bei den Infusionen und eine Reduktion der Natalizumab-Wirkung auf [24].
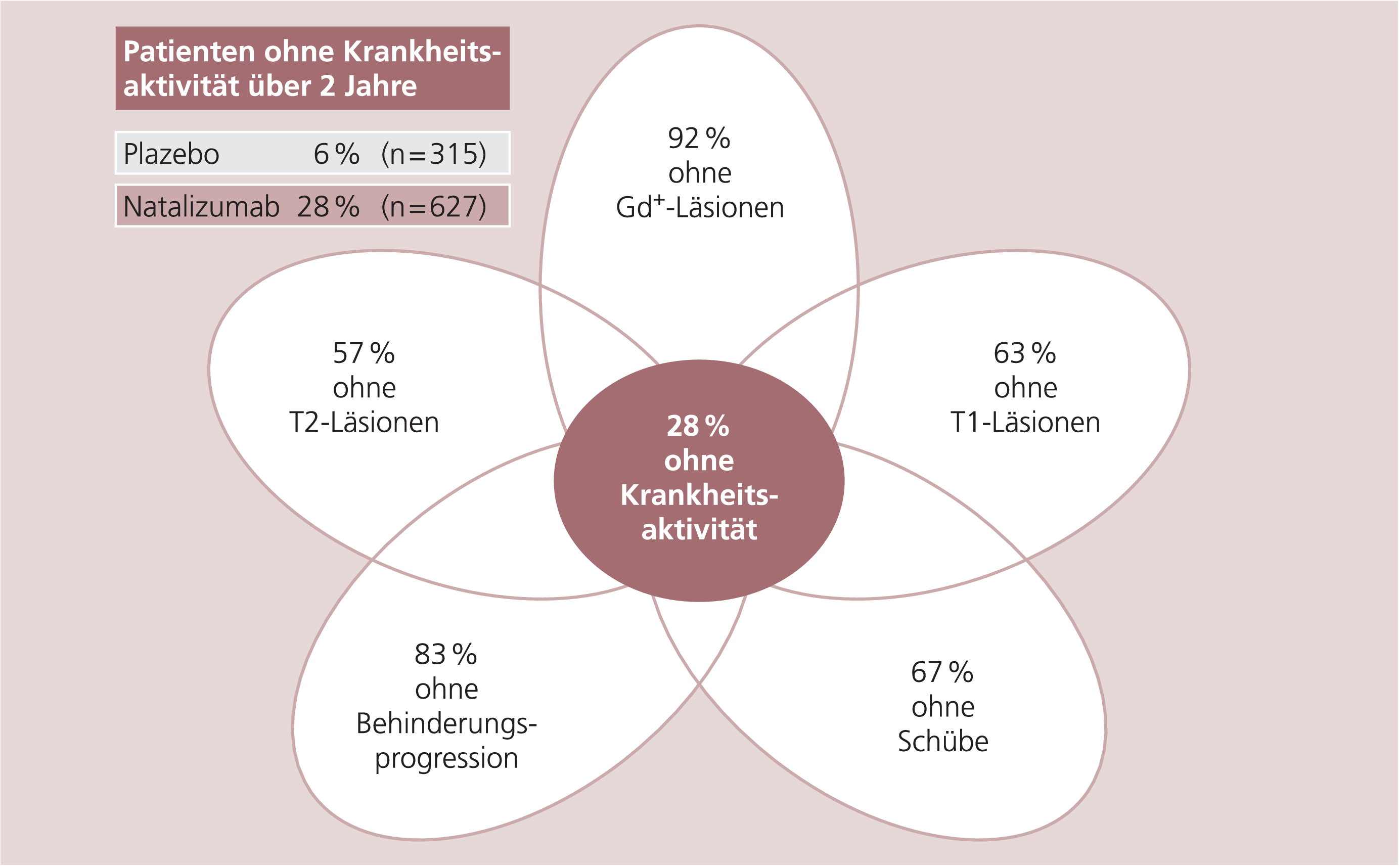
Abb. 2. Einfluss von Natalizumab auf die Krankheitsaktivität in der AFFIRM-Studie [nach Miller D, AAN 2005]
SENTINEL. In der SENTINEL-Studie [26] wurden Patienten eingeschlossen, die mindestens einen Schub unter der Therapie mit Interferon beta-1a (Avonex®) erlitten hatten. 589 Patienten erhielten Natalizumab 300 mg i.v. in vierwöchentlichen Abständen, die übrigen 582 erhielten Plazebo zusätzlich zur Fortsetzung ihrer Therapie mit Avonex® (30 µg i.m., einmal wöchentlich) über insgesamt 116 Wochen. Diese Studie wurde aufgrund von zwei Fällen von PML eine Woche vor dem regulären Ende im Februar 2005 gestoppt.
Auch in dieser Studie zeigte sich im ersten Jahr eine signifikante Reduktion der Schubrate unter der Therapie mit Natalizumab, im Vergleich zur Plazebo-Gruppe ließ sich eine 54%ige Reduktion der relativen Schubrate nach einem Jahr Kombinationstherapie im Vergleich zur Monotherapie mit Interferon beta-1a (0,38 vs. 0,82 Schübe/Jahr, p<0,001) und eine 55%ige Reduktion der Schubrate im zweiten Jahr (0,34 vs. 0,75 Schübe/Jahr, p<0,001) nachweisen. 54% der Patienten in der Kombinationsgruppe waren nach zwei Jahren schubfrei, in der Interferon-beta-1a-Monotherapie-Gruppe lediglich 32% (p<0,001). Die Kombinationstherapie führte zu einer 24%igen Reduktion des relativen Risikos einer Behinderungsprogression (p=0,02). Die kumulative Wahrscheinlichkeit einer Behinderungsprogression nach zwei Jahren betrug 23% bei der Kombinations- im Vergleich zu 29% bei der Interferon-beta-1a-Monotherapie. Die Anzahl neuer oder an Größe zunehmender T2-hyperintenser Läsionen war in der Kombinationsgruppe nach zwei Jahren um 83% reduziert (0,9 vs. 5,4, p<0,001), auch die Anzahl Gd+-Läsionen nahm um 89% ab (p<0,001) [26].
Insgesamt standen vor der Zulassung Daten von 1617 Patienten, die in verschiedenen Studien mit Natalizumab behandelt wurden zur Verfügung, die mittlere Dauer der Exposition betrug 20 Monate. Die FDA schloss aus den vorliegenden Daten, dass das Medikament den Standardmedikamenten (Interferon beta sowie Glatirameracetat) in der Wirksamkeit der Therapie der schubförmigen MS überlegen sei. Eine Zulassung erfolgte im November 2004 für die Behandlung der schubförmigen multiplen Sklerose.
Risiken/Nebenwirkungen
In den klinischen Studien war Natalizumab insgesamt gut verträglich, die häufigsten Nebenwirkungen waren Hypersensitivitätsreaktionen sowie Infekte. Schwerwiegende anaphylaktische Reaktionen waren selten (<1%) und traten vor allem bei Patienten mit nachgewiesenen Natalizumab-Antikörpern auf. In der ersten Phase-II-Studie wurde das Medikament gut vertragen, es zeigten sich lediglich etwas erhöhte Lymphozytenwerte im Blut, die jedoch noch im oberen Normbereich lagen und sich nach Ende der Therapie wieder normalisierten. Etwa 11% der Patienten, die mit Verum behandelt wurden, entwickelten Antikörper gegen dieses Medikament [30]. In der randomisierten, multizentrischen, Plazebo-kontrollierten Studie bei 213 Patienten mit sekundär chronisch-progredienter oder schubförmiger MS [21] erlitt in beiden Behandlungsgruppen (6 mg/kg KG vs. 3 mg/kg KG) jeweils ein Patient eine systemische Hypersensitivitätsreaktion und ein Patient in der 3-mg/kg-Gruppe entwickelte einen Bronchospasmus sowie Urtikaria. Dieser sprach jedoch direkt auf die Therapie mit Glucocorticoiden und Antihistaminika an. Es zeigte sich eine Erhöhung der Lymphozyten, Monozyten und Eosinophilen, jedoch nicht der Neutrophilen während der Behandlung, die Mittelwerte lagen jedoch nicht außerhalb der Normwerte.
In der AFFIRM-Studie gaben 95% der Patienten, die mit Natalizumab behandelt wurden, sowie 96% der Plazebo-Gruppe Nebenwirkungen der Therapie an. In der Natalizumab-Gruppe wurden signifikant häufiger Fatigue und allergische Reaktionen angegeben, ernsthafte Nebenwirkungen (serious adverse events) wurden bei 19% der Verum-Gruppe und 24% der Plazebo-Gruppe beobachtet (p=0,06), am häufigsten zeigten sich neue Schübe (6% unter Verum vs. 13% unter Plazebo, p<0,001). Während der Studie starben zwei mit Verum behandelte Patienten, einer an einer Alkoholintoxikation, einer an einem malignen Melanom. Die Infektionswahrscheinlichkeit war in der Verum-Gruppe genauso hoch wie in der Plazebo-Gruppe (p=0,32). In der Natalizumab-Gruppe traten fünf Fälle einer Tumorerkrankung auf, in der Plazebo-Gruppe lediglich ein Fall eines neu diagnostizierten Basalzell-Karzinoms. Infusionsreaktionen traten ebenfalls in der Natalizumab-Gruppe nicht signifikant häufiger auf (24% vs. 18%, p=0,04). Hypersensitivitätsreaktionen mit allergischen Reaktionen sowie Urtikaria, anaphylaktische Reaktionen oder allergische Dermatitis traten bei 4% der Patienten in der Verum-Gruppe auf, davon wurden 1,3% als ernsthafte Nebenwirkung (serious adverse event) gewertet. Bei allen Patienten mit einer Hypersensitivitätsreaktion wurde die Studienmedikation nicht fortgesetzt [24].
In der SENTINEL-Studie gaben >99% aller Patienten der Kombinations- und der Interferon-beta-1a-Monotherapie-Gruppe mindestens einmal Nebenwirkungen an, mit der Kombinationstherapie waren Angst, Pharyngitis und periphere Ödeme assoziiert. Die Inzidenz von Infektionen unterschied sich mit 83 bzw. 81% nicht signifikant zwischen beiden Gruppen, die Inzidenz von Krebserkrankungen betrug 1% in der Kombinations- und 2% in der Interferon-Monotherapie-Gruppe. In der Kombinationsgruppe waren Hypersensitivitätsreaktionen nach Infusion mit 1,9% häufiger als in der Monotherapie-Gruppe (0,3%). Zudem zeigte sich ein leichter Anstieg der Lymphozyten, Monozyten, Eosinophilen und Basophilen in der Kombinationsgruppe, die jedoch 16 Wochen nach Ende der Behandlung wieder abfielen. 12% der Patienten in der Kombinationsgruppe entwickelten Antikörper gegen Natalizumab. Zwei Patientinnen in der Interferon-Monotherapie-Gruppe verstarben, eine 23-Jährige mit bekannter Teilnahme an einem Methadon-Programm sowie einer Angststörung und eine 46-jährige Patientin mit einem Herzgeräusch sowie einer Sinusarrhythmie [26].
PML-Diskussion
Im Februar 2005 wurden zwei Fälle von progressiver multifokaler Leukenzephalopathie (PML) bei Patienten, die mit der Kombinationstherapie aus Natalizumab und Interferon-beta-1a (Avonex®) behandelt wurden, an die FDA gemeldet. Zwischen der Behandlung und der Entwicklung der Erkrankung bestand ein klarer Zusammenhang. Daraufhin nahm der Hersteller das Medikament zunächst vom Markt. Ein weiterer Erkrankungsfall mit Todesfolge trat bei einem ebenfalls mit Natalizumab behandelten 60-jährigen Patienten mit M. Crohn auf, dieser erhielt zusätzlich zur Behandlung mit Natalizumab eine Therapie mit Infliximab und litt unter einer chronischen Lymphozytopenie [32]. Beide MS-Patienten, die eine PML entwickelten, wurden mit Natalizumab über zwei Jahre lang behandelt, der Patient mit M. Crohn war bereits vier Jahre vor Beginn der Kombinationstherapie mit Natalizumab und Azathioprin immunsuppressiv behandelt worden, insgesamt erhielt dieser Patient jedoch lediglich acht Infusionen des Medikaments.
PML ist eine rasch progrediente, neurodegenerative, demyelinisierende Erkrankung, die durch das JC-Virus, ein doppelsträngiges Polyoma-Virus, verursacht wird. Die Erkrankung ist durch eine lytische Infektion der Oligodendrozyten verursacht. Der Name ist von neuropathologischen Beschreibungen der multifokalen Auffälligkeiten insbesondere der weißen Substanz abgeleitet. Nach einer Primärinfektion im Kindesalter persistiert das Virus in den Nieren, dem Knochenmark und der Milz [20], bis zu 64% der Erwachsenen scheiden das JC-Virus mit dem Urin aus, ohne klinische Symptome der Erkrankung zu zeigen [3]. Bei 50 bis 70% der erwachsenen Bevölkerung sind Antikörper gegen das JC-Virus nachweisbar [13, 28]. Ob die Erkrankung durch eine systemische Re-Aktivierung entsteht oder das Virus bereits nach der Primärinfektion latent in den Oligodendrozyten des Gehirns vorliegt und lokal reaktiviert wird, ist bisher nicht geklärt [1]. Es wird spekuliert, dass B-Zellen das Virus ins Gehirn einschleusen, da bei immunsupprimierten Patienten JC-Viren in B-Zellen im Knochenmark und Serum nachgewiesen wurden [8, 33], eine aktive Replikation im Blut wurde bisher jedoch nicht nachgewiesen [15, 34]. Auch konnten bisher keine JC-Virus-infizierten B-Zellen in PML-Läsionen im Gehirn nachgewiesen werden. Für die Theorie einer im Gehirn vorliegenden latenten Infektion spricht, dass nicht bei allen PML-Fällen der mit Natalizumab behandelten Patienten eine Virämie nachgewiesen werden konnte [12, 16].
In der Regel sind immunsupprimierte Patienten betroffen, bisher wurden vor allem Fälle bei HIV-Patienten, aber auch bei Patienten mit malignen hämatologischen Erkrankungen beschrieben. Zudem traten PML-Erkrankungen bei immunsuppressiv behandelten Patienten (z.B. mit Methotrexat, Azathioprin oder Cyclophosphamid) wie beispielsweise bei Erkrankungen des rheumatischen Formenkreises, bei der Behandlung der rheumatoiden Arthritis mit einem Antagonisten des TNF-α [9] sowie nach Organtransplantationen auf. Ein Fall wurde nach der Behandlung eines Patienten mit Stammzelltransplantation sowie Rituximab, einem spezifischen Antikörper gegen CD20, das auf B-Zellen exprimiert wird, beschrieben [4].
Die Erkrankung führt zu subakut über Tage und Wochen progredienten, sehr variablen fokalneurologischen Defiziten und insbesondere neuropsychologischen Auffälligkeiten. Sowohl die Großhirnhemisphären als auch der Hirnstamm können einbezogen sein, wobei die Hemisphären-Symptome insbesondere bei nicht HIV-assoziierten Erkrankungen überwiegen. Oft ist insbesondere die subkortikale, weiße Substanz betroffen. Die Letalität der PML ist sehr hoch, die Verbreitung des HI-Virus hat zu einer sprunghaften Zunahme der PML-Fälle geführt [7]. Ein Zusammenhang mit der multiplen Sklerose war bisher nicht bekannt [14]. Die Kontrolle der Erkrankung scheint durch JC-Virus-spezifische CD4- und möglicherweise auch zytotoxische CD8-T-Zellen zu erfolgen [3].
Detaillierte Nachuntersuchungen mit Bildgebung der in Studien mit Natalizumab behandelten über 3000 Patienten zeigten, dass eine PML ausschließlich bei den zwei Patienten unter der Kombinationstherapie von Natalizumab mit Interferon beta-1a (Avonex®) sowie bei dem einen M.-Crohn-Patienten nach vorangegangener und zum Teil überlappender immunsuppressiver Vorbehandlung unter der Monotherapie vorlag. Das errechnete Risiko, an einer PML zu erkranken, wird demnach mit etwa 1:1000 nach einer mittleren Behandlungszeit von knapp 18 Monaten angegeben. Mit einem sensitiven Polymerase-Kettenreaktionsverfahren (PCR) konnte kein JC-Virusgenom im Liquor von MS-Patienten gefunden werden, die nicht mit Natalizumab behandelt wurden. Es besteht durch die MS per se also kein erhöhtes Risiko einer JC-Virus-Replikation und Ausbreitung im ZNS.
Ob ein Einfluss der zusätzlich zu Natalizumab verabreichten Medikation auf den Ausbruch sowie den Verlauf der PML besteht, ist noch nicht endgültig geklärt. Möglicherweise erhöht die gleichzeitige Gabe mehrerer Immunsuppressiva oder/und Immunmodulatoren das Risiko einer PML durch Natalizumab, möglicherweise gibt es auch einen Zusammenhang mit der Dauer der Applikation sowie dem immunologischen Status des Patienten.
Konsequenzen für die Praxis
Nach Vorlage der Sicherheitsdaten erfolgte nun auch durch die EMEA eine Zulassung von Natalizumab zur Behandlung der schubförmigen MS unter Auflagen (www.emea.eu.int/humandocs/Humans/EPAR/tysabri/tysabri.htm). Seit Juli 2006 steht das Präparat in der EU zur Verfügung. Gemäß der aktuellen Fachinformation besteht eine Indikation für Natalizumab (Tysabri®) zur „krankheitsmodifizierenden Monotherapie von hochaktiver schubförmiger MS“, also bei Patienten mit hoher Krankheitsaktivität trotz immunmodulatorischer Behandlung oder unbehandelten Patienten mit rasch fortschreitender schubförmig-remittierend verlaufender MS (mindestens zwei schwere Schübe pro Jahr).
Der Zulassungstext stellt derzeit einen Kompromiss zwischen dem zu erwartenden Nutzen und den möglichen Risiken dieser Therapie unter Beachtung einer größtmöglichen Sicherheit für die Patienten dar. Es ist zu beachten, dass die hier genannten Zulassungsindikationen in wesentlichen Teilen nicht die Einschlusskriterien der beiden Phase-III-Studien (AFFIRM und SENTINEL) widerspiegeln. Unter den jetzt vorliegenden Zulassungsbedingungen kann Natalizumab daher als Präparat der Eskalationstherapie bei schubförmig verlaufender MS ohne Zeichen der sekundären Progression, aber nicht ausreichendem Effekt einer Basistherapie mit Interferon beta oder Glatirameracetat angesehen werden. Bisher war hierfür nach den Empfehlungen der Multiple-Sklerose-Therapie-Konsensusgruppe (MSTKG) allein Mitoxantron vorgesehen [25]. Diese Therapie ist aber ebenso mit einem Risiko schwerwiegender Nebenwirkungen (Kardiomyopathie und Medikamenten-assoziierte Leukämie – auch vor Erreichen der kumulativen Grenzdosis) behaftet. Natalizumab stellt daher als Monotherapie nach der aktuellen Datenlage eine Alternative in der Eskalationstherapie der schubförmigen MS dar. Konkret empfiehlt die MSTKG im Hinblick auf die derzeitige Datenlage und die Zulassungsbestimmungen der EMEA zunächst folgende Vorgehensweise beim Einsatz von Natalizumab:
l Indikationsstellung und Anwendung von Natalizumab soll vorzugsweise in MS-Zentren erfolgen.
l In Abhängigkeit von nationalen Gegebenheiten erscheint die Verabreichung von Natalizumab auch außerhalb von klinischen MS-Zentren möglich, wenn entsprechend etablierte Notfallmaßnahmen zur Behandlung allergischer und anaphylaktischer Reaktionen vorhanden sind und eine standardisierte MRT-Verlaufsdiagnostik möglich ist [5].
l Dokumentierte Aufklärung der Patienten über die besonderen Risiken der Therapie
l Einsatz nur als Monotherapie in zugelassener Dosierung und Applikationsintervallen bei immunkompetenten Patienten (normales Differenzialblutbild und Infektausschluss) nach Versagen einer Therapie mit rekombinantem Interferon beta oder Glatirameracetat (nach aktueller Einschätzung mindestens 14 Tage therapiefreies Intervall vor der ersten Natalizumab-Gabe) [6]
l Einsatz von Natalizumab bei Patienten mit vorangegangener Immunsuppression nur unter genauer individueller Abwägung des Nutzen/Risiko-Verhältnisses (nach aktueller Einschätzung/Expertenmeinung mindestens drei Monate therapiefreies Intervall vor der ersten Natalizumab-Gabe; es liegen aber noch keinerlei Erfahrungen zum zeitlichen Abstand vor!)
l Vor Beginn der Therapie kranielles MRT als Basisuntersuchung und zur differenzialdiagnostischen Abgrenzung „atypischer MS-Läsionen“
l Vierteljährliche neurologische Kontrolluntersuchungen durch MS-Zentren unter besonderer Berücksichtigung kognitiver und neuropsychologischer Funktionen (z.B. Aphasie, Apraxie, kortikale Blindheit als möglicher Hinweis für eine PML)
l Bei Verdacht auf das Vorliegen einer PML (klinisch oder MRT nach den Leitlinien der DGN) sollte die Therapie mit Natalizumab zunächst unterbrochen und ein MRT sowie eine Liquorpunktion mit PCR zum Nachweis/Ausschluss von JCV-DNS durchgeführt werden. Bei hochgradigem PML-Verdacht, aber negativer PCR, kann eine Hirnbiopsie in Erwägung gezogen werden.
Zur Indikationsstellung für eine Natalizumab-Therapie sollten also auf jeden Fall die klinische Krankheitsaktivität (Schübe und Progression) sowie die im MRT darstellbare Aktivität (Gd+-Läsionen, T2-Läsionen) evaluiert werden und erst nach deren Beurteilung die Indikation zur Therapie gestellt werden. Auch die Durchführung der Therapie mit den verbundenen Kontrolluntersuchungen sollte möglichst innerhalb von spezialisierten Zentren erfolgen.
Literatur
1. Aksamit AJ Jr. Progressive multifocal leukoencephalopathy: a review of the pathology and pathogenesis. Microsc Res Tech 1995;32: 302–11.
2. Brocke S, Piercy C, Steinman L, Weissman IL, et al. Antibodies to CD44 and integrin a4, but not L-selectin, prevent central nervous system inflammation and experimental encephalomyelitis by blocking secondary leukocyte recruitment. Proc Natl Acad Sci U S A 1999;96:6896–901.
3. Gasnault J, Kahraman M, de Goer de Herve MG, Durali D, et al. Critical role of JC virus-specific CD4 T-cell responses in preventing progressive multifocal leukoencephalopathy. Aids 2003;17:1443–9.
4. Goldberg SL, Pecora AL, Alter RS, Kroll MS, et al. Unusual viral infections (progressive multifocal leukoencephalopathy and cytomegalovirus disease) after high-dose chemotherapy with autologous blood stem cell rescue and peritransplantation rituximab. Blood 2002;99:1486–8.
5. Henze T. Symptomatische Therapie der multiplen Sklerose. Nervenarzt 2004;75(Suppl 1):2–39.
6. Henze T, Rieckmann P, Toyka KV. Symptomatic treatment of multiple sclerosis. Multiple Sclerosis Therapy Consensus Group (MSTCG) of the German Multiple Sclerosis Society. Eur Neurol 2006;56:78–105.
7. Holman RC, Janssen RS, Buehler JW, et al. Epidemiology of progressive multifocal leukoencephalopathy in the United States: analysis of national mortality and AIDS surveillance data. Neurology 1991;41:1733–6.
8. Houff SA, Major EO, Katz DA, et al. Involvement of JC virus-infected mononuclear cells from the bone marrow and spleen in the pathogenesis of progressive multifocal leukoencephalopathy. N Engl J Med 1988;318:301–5.
9. Imperato AK, Bingham CO 3rd, Abramson SB. Overview of benefit/risk of biological agents. Clin Exp Rheumatol 2004;22:S108–14.
10. Kanwar JR, Kanwar RK, Wang D, Krissansen GW. Prevention of a chronic progressive form of experimental autoimmune encephalomyelitis by an antibody against mucosal addressin cell adhesion molecule-1, given early in the course of disease progression. Immunol Cell Biol 2000;78:641–5.
11. Kent SJ, Karlik SJ, Cannon C, Hines DK, et al. A monoclonal antibody to alpha 4 integrin suppresses and reverses active experimental allergic encephalomyelitis. J Neuroimmunol 1995;58:1–10.
12. Kleinschmidt-DeMasters BK, Tyler KL. Progressive multifocal leukoencephalopathy complicating treatment with natalizumab and interferon beta-1a for multiple sclerosis. N Engl J Med 2005;353:369–74.
13. Knowles WA, Pipkin P, Andrews N, Vyse A, et al. Population-based study of antibody to the human polyomaviruses BKV and JCV and the simian polyomavirus SV40. J Med Virol 2003;71:115–23.
14. Koralnik IJ. New insights into progressive multifocal leukoencephalopathy. Curr Opin Neurol 2004;17:365–70.
15. Koralnik IJ, Boden D, Mai VX, Lord CI, et al. JC virus DNA load in patients with and without progressive multifocal leukoencephalopathy. Neurology 1999;52:253–60.
16. Langer-Gould A, Atlas SW, Green AJ, Bollen AW, et al. Progressive multifocal leukoencephalopathy in a patient treated with natalizumab. N Engl J Med 2005;353:375–81.
17. Lee SJ, Benveniste EN. Adhesion molecule expression and regulation on cells of the central nervous system. J Neuroimmunol 1999;98: 77–88.
18. Ley K. The role of selectins in inflammation and disease. Trends Mol Med 2003;9:263–8.
19. Lucchinetti CF, Bruck W, Rodriguez M, Lassmann H. Distinct patterns of multiple sclerosis pathology indicates heterogeneity on pathogenesis. Brain Pathol 1996;6:259–74.
20. Major EO, Amemiya K, Tornatore CS, Houff SA, et al. Pathogenesis and molecular biology of progressive multifocal leukoencephalopathy, the JC virus-induced demyelinating disease of the human brain. Clin Microbiol Rev 1992;5:49–73.
21. Miller DH, Khan OA, Sheremata WA, Blumhardt LD, et al. A controlled trial of natalizumab for relapsing multiple sclerosis. N Engl J Med 2003;348:15–23.
22. Niino M, Bodner C, Simard ML, Alatab S, et al. Natalizumab effects on immune cell responses in multiple sclerosis. Ann Neurol 2006;59:748–54.
23. O’Connor PW, Goodman A, Willmer-Hulme AJ, Libonati MA, et al. Randomized multicenter trial of natalizumab in acute MS relapses: clinical and MRI effects. Neurology 2004;62:2038–43.
24. Polman CH, O’Connor PW, Havrdova E, Hutchinson M, et al. A randomized, placebo-controlled trial of natalizumab for relapsing multiple sclerosis. N Engl J Med 2006;354:899–910.
25. Rieckmann P, Toyka KV. Immunmodulatorische Stufentherapie der Multiplen Sklerose. Neue Aspekte und praktische Umsetzung. Nervenarzt 2002;73:556–63.
26. Rudick RA, Stuart WH, Calabresi PA, Confavreux C, et al. Natalizumab plus interferon beta-1a for relapsing multiple sclerosis. N Engl J Med 2006;354:911–23.
27. Steinman L. Multiple sclerosis: a two-stage disease. Nat Immunol 2001;2:762–4.
28. Stolt A, Sasnauskas K, Koskela P, Lehtinen M, et al. Seroepidemiology of the human polyomaviruses. J Gen Virol 2003;84:1499–504.
29. Stuve O, Marra CM, Bar-Or A, Niino M, et al. Altered CD4+/CD8+ T-cell ratios in cerebrospinal fluid of natalizumab-treated patients with multiple sclerosis. Arch Neurol 2006;63:1383–7.
30. Tubridy N, Behan PO, Capildeo R, Chaudhuri A, et al. The effect of anti-alpha4 integrin antibody on brain lesion activity in MS. The UK Antegren Study Group. Neurology 1999;53:466–72.
31. Vajkoczy P, Laschinger M, Engelhardt B. Alpha4-integrin-VCAM-1 binding mediates G protein-independent capture of encephalitogenic T cell blasts to CNS white matter microvessels. J Clin Invest 2001;108:557–65.
32. Van Assche G, Van Ranst M, Sciot R, Dubois B, et al. Progressive multifocal leukoencephalopathy after natalizumab therapy for Crohn’s disease. N Engl J Med 2005;353:362–8.
33. Weber T, Major EO. Progressive multifocal leukoencephalopathy: molecular biology, pathogenesis and clinical impact. Intervirology 1997;40:98–111.
34. Wei G, Liu CK, Atwood WJ. JC virus binds to primary human glial cells, tonsillar stromal cells, and B-lymphocytes, but not to T-lymphocytes. J Neurovirol 2000;6:127–36.
35. Weinshenker BG, Bass B, Rice GP, et al. The natural history of multiple sclerosis: a geographically based study. I. Clinical course and disability. Brain 1989;112:133–46.
36. Yednock TA, Cannon C, Fritz LC, et al. Prevention of experimental autoimmune encephalomyelitis by antibodies against alpha 4 beta 1 integrin. Nature 1992;356:63–6.
Dr. Tjalf Ziemssen, Wiebke Schrempf, Multiple Sklerose Zentrum, Neurologische Universitätsklinik Dresden, Fetscherstr. 74, 01307 Dresden, E-Mail: Ziemssen@web.de
Natalizumab – a new option for multiple sclerosis
Monoclonal antibodies were designed to extend therapeutic options in the treatment of chronic inflammatory and neoplastic diseases by the specific blockade of pathophysiologically relevant molecules. Natalizumab (Tysabri®, Biogen/Elan), a humanized, monoclonal antibody against alpha-4-integrin, is the first promising example for the treatment of relapsing-remitting multiple sclerosis. In initial phase II studies, treatment with natalizumab to a significant decline of Gadolinium-enhancing (Gd+) T1-lesions and reduction of the volume of Gd+ lesions on MRI-scans. In the AFFIRM phase-III-trial, the relapse and progression rate in natalizumab-treated patients suffering from relapsing-remitting MS (RRMS) was significantly reduced compared with placebo. Three patients treated with natalizumab developed progressive multifocal leukencephalopathy (PML), an infection of the CNS caused by the Polyomavirus JC. The drug was temporarily phased out of the market, but under strict obligations it was re-authorized for the single treatment regimen of active relapsing-remitting multiple sclerosis. For the assessment of benefits and risks and also adverse effects of new drugs developed for the treatment of chronic diseases like multiple sclerosis longterm-trials need to be conducted. Until these data are available the use of natalizumab should be restricted to centres with wide experience in the treatment of multiple sclerosis.
Keywords: Multiple sclerosis, very late antigen (VLA-4), a4-integrin, natalizumab (Tysabri®), progressive multifocal leukencephalopathy (PML)
Psychopharmakotherapie 2007; 14(03)
