Hans-Jürgen Möller, München, Matthias C. Angermeyer, Leipzig, Borwin Bandelow, Göttingen, Michael Deuschle, Mannheim, Werner Kissling, München, Michael Linden, Berlin, Dieter Naber, Hamburg, Max Schmauß, Augsburg, und Ulrich Voderholzer, Freiburg
Die Compliance des Patienten ist wesentliche Voraussetzung für den Erfolg einer Therapie. Compliance-Probleme treten in vielen Bereichen der Medizin auf, vor allem aber bei chronischen Erkrankungen, weil hier besondere Anforderungen an die langfristige Motivation des Patienten gestellt werden.
Welche Faktoren die Compliance positiv und negativ beeinflussen und mit welchen Maßnahmen die Compliance verbessert werden kann, soll hier am Beispiel der Schizophrenie ausgeführt werden. Dabei sind die Überlegungen auch auf bipolare Störungen übertragbar, denn es gibt eine Reihe von Gemeinsamkeiten. Beide Erkrankungen erfordern nach der Akutbehandlung in der Regel eine langfristige rezidivprophylaktische Therapie. Bei beiden gibt es ähnliche Probleme in Bezug auf die Compliance, zum Beispiel einen Mangel an Krankheitseinsicht, fehlendes Verständnis für den Zusammenhang zwischen Non-Compliance und Rückfallrisiko, Vorbehalte der Patienten und ihres Umfelds gegenüber Psychopharmaka sowie das Nebenwirkungsspektrum der eingesetzten Medikamente. Da es die meiste Literatur zur Compliance bei Schizophrenie gibt, wird im Folgenden vorwiegend darauf fokussiert.
Begriffsklärung
Compliance wird in deutschsprachigen Publikationen auch mit Verordnungs-, Therapie- oder Medikamententreue umschrieben. In der englischsprachigen Literatur werden auch die Begriffe „adherence“ (Festhalten, Einhalten) oder „concordance“ (Übereinstimmung) benutzt, anstelle von Non-Compliance gelegentlich auch „attrition“ (Abnutzung [der Bereitschaft zur Therapiemitwirkung], also Abbruch der Therapie, „drop-out“). Diese Begriffe implizieren, dass der Patient der empfohlenen Therapie zustimmt, und weisen ihm damit eine aktive Rolle zu [36, 43]. „Compliance“ bezeichnet in der Physiologie ein passives Verhalten (z.B. pulmonale Compliance) und wird im übertragenen Sinn daher auch als passives Befolgen der ärztlichen Anordnung gedeutet. „Compliance“ kann aber auch übersetzt werden mit „sich anlehnen oder annähern an einen Standard“ [29].
Im Folgenden soll Compliance dementsprechend als Vergleich des Tatsächlichen mit einem Soll der Therapie verstanden werden. Dieses „Soll“ ist das Therapieziel, das Arzt und Patient auf der Basis eines gemeinsamen Wissens festlegen. Der Patient hat also ein Mitspracherecht, nachdem er ausreichend über die möglichen Therapieoptionen informiert worden ist, und hat somit einen aktiven Part. Dieses Konzept wird auch als „shared decision making“ (gemeinsame Entscheidungsfindung) bezeichnet [19]. Es setzt voraus, dass der Arzt sich als Partner des Patienten versteht, bedeutet also eine Abkehr von dem früher verbreiteten paternalistischen Selbst- und Fremdverständnis der Ärzte.
Ob die Therapie konsequent durchgeführt wird, das Soll also erfüllt wird, hängt von verschiedenen Voraussetzungen ab, die im Stufenmodell der Compliance (Abb. 1) zusammengefasst sind [30]. Danach gilt, dass zunächst einmal ein klarer Therapiestandard vorliegen muss und dass mit negativen Folgen zu rechnen ist, wenn er nicht eingehalten wird. Da es in der Medizin aber viele Fälle gibt, in denen mehrere Behandlungsalternativen denkbar sind, sollten nach dem Konzept des „shared decision making“ Arzt und Patient zunächst gemeinsam das Behandlungsziel und die geplante Therapie festlegen. Dabei sollte man sich selbstverständlich an Therapieleitlinien orientieren, aber auch Erfahrungen, Wünsche und individuelle Lebensentwürfe des Patienten berücksichtigen. In Bezug auf die bipolare Depression bedeutet das zum Beispiel, dass es dem Patienten überlassen bleibt zu entscheiden, ob er das Risiko eines Rezidivs oder Probleme einer Langzeitbehandlung mehr fürchtet. Dies ist nicht durch den Arzt medizinisch zu entscheiden. Die Therapieziele können sich im Verlauf der Therapie durchaus ändern.
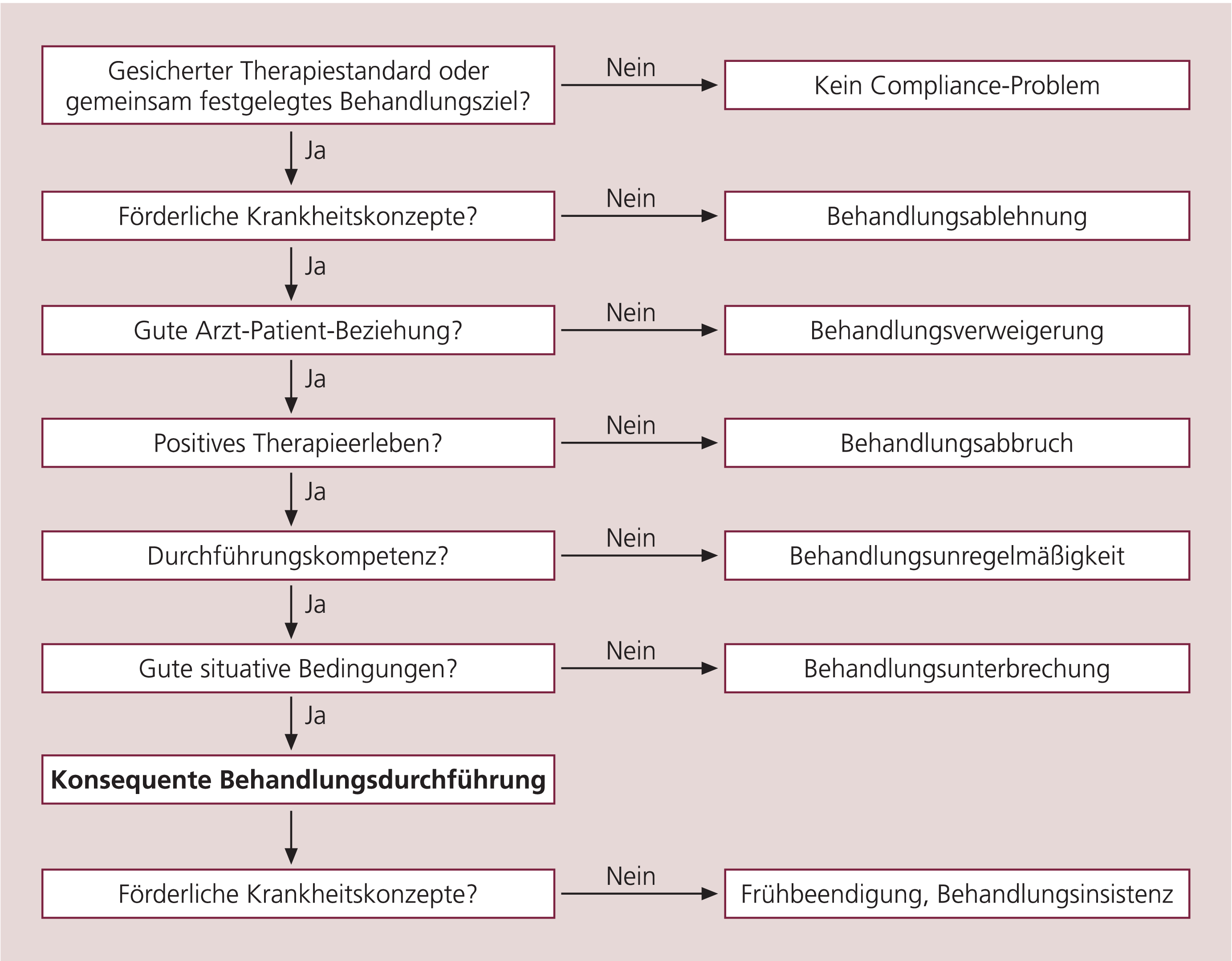
Abb. 1. Stufenmodell der Compliance [mod. nach 30]
Eine gute Compliance (= konsequente Behandlungsdurchführung) setzt voraus, dass die in der linken Spalte genannten Bedingungen in chronologischer Reihenfolge gegeben sind. Andernfalls sind verschiedengradige Compliance-Probleme zu erwarten.
Messung der Compliance
Zur Messung der Compliance gibt es verschiedene direkte und indirekte Verfahren (Tab. 1). Bei der Quantifizierung ist zu berücksichtigen, dass Compliance kein dichotomes, sondern ein graduelles Konstrukt ist: Patienten nehmen mehr oder weniger Tabletten mehr oder weniger regelmäßig ein, wie auch in dem Begriff der partiellen Compliance zum Ausdruck kommt. Man sollte daher auf Entweder-oder-Klassifizierungen verzichten, da dies nur abqualifizierend ist. Hilfreicher sind graduelle Feststellungen. Ab wann eine Medikationsunregelmäßigkeit zum Problem wird, hängt dann von der Art der Therapie ab. So können bei einer Behandlung mit Lithiumsalzen schon vergleichsweise kleine Abweichungen zur Intoxikation führen, während bei einer Behandlung mit Neuroleptika kurzfristig auch größere Dosisschwankungen in der Regel belanglos sind.
Tab. 1. Verfahren zur Compliance-Messung [nach 36]
|
Verfahren |
Probleme |
|
Direkte Verfahren |
|
|
Einnahme unter Aufsicht |
Patient spuckt Tablette hinterher wieder aus. Für Routinebetrieb ungeeignet |
|
Therapeutisches Drug-Monitoring |
Teuer. Fehlinterpretation durch Unterschiede im Metabolismus oder „Weißkittel-Compliance“ |
|
Indirekte Verfahren |
|
|
Patientenfragebogen oder -bericht |
Hohe Irrtumswahrscheinlichkeit, vor allem bei größerem Zeitintervall zwischen den Visiten. Leichte Verfälschung durch den Patienten |
|
Tablettenzählen |
Leicht vom Patienten zu verfälschen |
|
Ermittlung der eingelösten Wiederholungsverordnungen |
Setzt ein geschlossenes Apothekensystem voraus. Einlösen der Verordnung ist nicht gleichbedeutend mit Einnahme des Medikaments |
|
Beurteilung des klinischen Ansprechens |
Kann durch andere Faktoren als die regelmäßige Medikamenteneinnahme beeinflusst werden |
|
Elektronisches Kontrollsystem, das die Entnahme der Einzeldosen registriert |
Teuer. Entnahme der Dosis ist nicht gleichbedeutend mit Einnahme des Medikaments |
|
Patiententagebuch |
Leicht vom Patienten zu verfälschen |
|
Befragung der betreuenden Person |
Anfällig für verzerrte Darstellung |
Da die Feststellung des Ausmaßes der Compliance wesentlich vom Messverfahren abhängt, sind mit verschiedenen Verfahren erhobene Daten nicht ohne weiteres miteinander vergleichbar. Das muss bei der vergleichenden Interpretation von Compliance-Studien berücksichtigt werden.
Für die Praxis ist relevant, dass die Beurteilung der Compliance durch die Einschätzung des Arztes sich häufig als nicht valide erwies; zum Beispiel neigt der Arzt oft zur Überschätzung der Compliance. So war in der Studie von Byerly et al. [7] mit ambulanten Schizophrenie-Patienten gemäß Einnahmeerfassung mit einem elektronischen Kontrollsystem die Hälfte der Patienten nicht compliant (Einnahme von < 70% der Dosen), ohne dass dies von den Behandlern erkannt wurde.
Compliance bei Schizophrenie und bipolaren Störungen
Cramer und Rosenheck [11] fanden in ihrer Metaanalyse von 24 Neuroleptika-Studien, weit überwiegend mit Schizophrenie-Patienten, dass lediglich 58% der verordneten Antipsychotika eingenommen worden waren; die Spanne lag zwischen 24 und 90%, wobei verschiedene Erhebungsinstrumente (Patientenbefragung, Arzteinschätzung, Laborkontrollen der Urinspiegel) zugrunde lagen.
Compliance-Raten von 50 bis 60% bei Schizophrenie-Patienten wurden auch in etwas jüngeren Übersichtsarbeiten berichtet [24, 37]. Dabei waren die Compliance-Raten, gemessen an Wiederholungsverordnungen, bei atypischen Antipsychotika langfristig nur wenig besser als bei „typischen“ Antipsychotika (z.B. [14]: 54,9% vs. 50,1%). Hier sei daran erinnert, dass das Einlösen der Wiederholungsverordnung nicht notwendigerweise bedeutet, dass das Medikament auch eingenommen wird. Wurden dagegen Studienabbruchraten – also ein eindeutigeres Compliance-Maß – herangezogen, so ergaben sich in der Regel deutliche Unterschiede zugunsten der Atypika [Übersicht bei 45].
Für Patienten mit bipolarer Störung sind die Compliance-Raten eher noch schlechter, zum Beispiel 35% bei Colom und Vieta [10].
Zwar werden auch für chronische internistische Erkrankungen, zum Beispiel Hypertonie, ähnlich geringe Compliance-Raten angegeben [43]. Dieser Vergleich lässt aber außer Acht, dass bei psychischen Erkrankungen das subjektive Leiden höher ist und bei Nichtbehandlung Lebensbedrohung durch das erhöhte Suizidrisiko besteht, so dass eine zuverlässige Einhaltung der Therapie besonders wichtig ist.
Die hier zitierten Untersuchungen zur Compliance beziehen sich hauptsächlich auf die Arzneimitteltherapie. Die folgenden Betrachtungen sind allerdings auch auf andere Bereiche übertragbar, in denen die Compliance des Patienten gefordert ist, zum Beispiel die Teilnahme an psychosozialen Behandlungsprogrammen, Drogenenthaltsamkeit und Selbstpflege.
Einfluss der psychischen Erkrankung
Wie eingangs erwähnt, ist mangelnde Krankheitseinsicht bei Schizophrenie-Patienten wie bei Patienten mit bipolaren Störungen zu beobachten. Sie erschwert es, den Patienten von der Notwendigkeit der Therapie zu überzeugen. Auch psychopathologische Merkmale wie Wahnvorstellungen oder kognitive Störungen (z.B. beeinträchtigtes Gedächtnis) wirken sich nachteilig auf die Compliance aus. In verschiedenen Studien fanden sich bei nicht-complianten Patienten mehr Halluzinationen, Denkstörungen, aggressives Verhalten und produktiv-psychotische Symptome [Zusammenfassung bei 31]. Dies unterstreicht die Notwendigkeit einer suffizienten antipsychotischen Therapie.
Stellenwert der physischen Gesundheit
Patienten mit Schizophrenie oder bipolaren Störungen müssen meist über Jahrzehnte behandelt werden. Deswegen muss unter anderem auf ihre physische Gesundheit besondere Rücksicht genommen werden, schon bei der Planung (z.B. Kontraindikationen), aber auch bei der Kontrolle der Therapie. Körperliche Nebenwirkungen der Arzneimitteltherapie sind oft unvermeidlich, sollten aber möglichst gering gehalten werden – im Interesse der Gesundheit des Patienten und weil somatische Nebenwirkungen die Compliance maßgeblich beeinträchtigen können. Schon früh wurde der negative Einfluss von extrapyramidal-motorischen Störungen auf die Compliance von Schizophrenie-Patienten beschrieben [47]. Auch Gewichtszunahme und sexuelle Funktionsstörungen werden unter Umständen als so störend oder/und stigmatisierend empfunden, dass der Patient die Therapie eigenmächtig ändert oder abbricht. (Andererseits kann auch das Fehlen somatischer Nebenwirkungen Non-Compliance provozieren, wenn es als Unwirksamkeit der Therapie interpretiert wird.) Abgesehen von den medizinisch relevanten körperlichen Nebenwirkungen sind unter Compliance-Aspekten insbesondere auch die subjektiv störenden Nebenwirkungen zu berücksichtigen.
Der Arzt sollte ein Gesprächsklima schaffen, das es dem Patienten erlaubt, störende Nebenwirkungen aller Art anzusprechen. Überdies darf die Kontrolle relevanter somatischer Parameter (z.B. Gewicht, Lipidprofil, Blutdruck) nicht vernachlässigt werden, zumal diese durch die antipsychotische Therapie nachteilig beeinflusst werden können.
Langfristige physische Gesundheit liegt aber auch in der Verantwortung des Patienten und erfordert seine Compliance, zum Beispiel in Bezug auf die Selbstpflege, Rauchen oder Drogenabhängigkeit.
Compliance und Patientenzufriedenheit
Die Lebensqualität, Zufriedenheit und das Wohlbefinden des Patienten haben großen Einfluss auf seine Compliance. Diese in der Regel vom Patienten selbst beurteilten subjektiven Dimensionen gewinnen daher als Therapieziel immer größere Bedeutung [26, 34, 41]. Patientenzufriedenheit kann auf verschiedenen Stufen der Compliance (Abb. 1) entstehen oder gefährdet werden. Das beginnt bereits bei der Festlegung des Behandlungsziels und damit der Behandlungsakzeptanz. So kann Unzufriedenheit mit der Therapie aus dem Umstand resultieren, dass der Patient seine Erkrankung als wesentliches Element seiner Lebensführung ansieht und sie gar nicht in dem erreichten Maße zu unterdrücken wünscht. Ein Beispiel ist die Hypomanie, die von einigen Patienten eher positiv als negativ bewertet wird. Das Krankheits- und Therapiekonzept des Patienten hat wesentlichen Einfluss auf die Akzeptanz und langfristige Einhaltung der Therapie. Förderlich sind dabei externe Kontrollüberzeugungen, also Vertrauen in den Arzt und in die Wirksamkeit der Medikation, während idiosynkratische Annahmen (z.B. grundsätzliches Misstrauen gegenüber Psychopharmaka) und interne Kontrollüberzeugungen (z.B. das Gefühl, allein für den Gesundheitsstatus verantwortlich zu sein) eher kontraproduktiv sind [31].
Eine gute Arzt-Patienten-Beziehung und das Gefühl, die Krankheit „im Griff zu haben“, können zur Zufriedenheit des Patienten beitragen.
Ganz wesentlich hängt die Patientenzufriedenheit auch von der subjektiven Bewertung der Nebenwirkungen ab. Eng damit verknüpft ist die Frage, inwieweit der Patient sich durch seine Krankheit und deren Therapie stigmatisiert fühlt. Dass solche Stigmabefürchtungen sich auf die Compliance negativ auswirken, wurde zum Beispiel für die Therapie mit Antidepressiva gezeigt [44]. Dabei können für den Patienten Nebenwirkungen relevant sein, die nicht mit den üblichen Nebenwirkungsskalen erfasst werden oder unter einer Skalenschwelle liegen (z.B. Haarausfall). Generell besteht das Risiko für Stigmabefürchtungen eher bei sichtbaren Nebenwirkungen, zum Beispiel extrapyramidal-motorischen Störungen oder Gewichtszunahme.
Lambert et al. [25] befragten 213 Schizophrenie-Patienten, die mit konventionellen Antipsychotika behandelt wurden, und fanden, dass die Patienten sexuelle Funktionsstörungen, extrapyramidale und psychische Nebenwirkungen als belastender empfanden als Sedierung oder vegetative Nebenwirkungen. Nebenwirkungen beeinflussten die Einstellung zu Antipsychotika negativ, und eine solche negative Einstellung sowie die Erfahrung von Nebenwirkungen gingen mit schlechterer Compliance einher.
Unter Umständen werden einem Patienten allerdings die Gründe für seine Unzufriedenheit gar nicht bewusst; er empfindet lediglich ein undifferenziertes „Unwohlsein“, das langfristig seine Motivation zur konsequenten Therapiedurchführung untergräbt. Generell sollten Therapeuten die Patientenzufriedenheit systematischer erheben, um gegebenenfalls rechtzeitig reagieren zu können. In mehreren Untersuchungen zur Neuroleptika-Therapie wurde gezeigt, dass die Behandlung mit atypischen Neuroleptika in den Dimensionen Lebensqualität und Wohlbefinden als besser im Vergleich zu typischen Neuroleptika eingestuft wurde [4, 34].
Pharmakotherapie in der Akutphase und im Langzeitverlauf
Der erste Tag der Akuttherapie ist der Beginn der Langzeittherapie, denn unangenehme Erfahrungen, die der Patient in dieser Zeit macht, werden seine Einstellung zur gesamten Therapie prägen. Compliance-Überlegungen im hier gemeinten Sinne spielen zwar in dieser Phase keine Rolle, weil ein Patient in der floriden Phase der Schizophrenie über das „Soll“ der Therapie nicht wirklich diskutieren kann. Allerdings wird in dieser Phase die Grundlage für die Compliance bei der Langzeittherapie gelegt. Iatrogene Traumatisierungen bei der Behandlung der akuten Episode sollten deshalb möglichst vermieden werden. Um dies zu gewährleisten, sollte von vornherein ein Antipsychotikum ausgewählt werden, das im individuellen Fall möglichst nebenwirkungsarm ist. Als Nebenwirkungen sind zu Beginn der Therapie besonders die motorischen Nebenwirkungen, insbesondere Akathisie, relevant. In der Langzeitbehandlung sind neben den extrapyramidal-motorischen Störungen, einschließlich Spätdyskinesien, affektive Nebenwirkungen wie Dysphorie und depressiogene Wirkungen sowie Sedierung, Gewichtszunahme und sexuelle Funktionsstörungen ausschlaggebend [37].
Es ist sinnvoll, gleich zu Beginn ein Antipsychotikum einzusetzen – in der hochakuten Phase unter Umständen kombiniert mit einem Benzodiazepin –, das auch langfristig zur Rezidivprophylaxe eingesetzt werden kann. Damit erspart man sich und dem Patienten die Schwierigkeiten und Unwägbarkeiten eines Präparatewechsels (z.B. neue Unverträglichkeiten) und die damit zusammenhängenden Compliance-Probleme.
Für die Langzeittherapie sollten bevorzugt atypische Antipsychotika eingesetzt werden. Ein wichtiger Grund dafür ist das geringere Risiko für Spätdyskinesien im Vergleich zu konventionellen Antipsychotika. Überdies kann man sich zunutze machen, dass diese Substanzgruppe – von der Wirkung auf die Positivsymptomatik abgesehen – heterogene Eigenschaften aufweist. So kann abhängig von den individuellen Erfordernissen ein Präparat mit einer antidepressiven Wirkungskomponente, mit günstigen Wirkungen auf die Kognition oder auf Negativsymptome eingesetzt werden. Die atypischen Antipsychotika eröffnen die Möglichkeit einer differenzierten Psychopharmakotherapie der Schizophrenie (Tab. 2) [5].
Tab. 2. Differenzierte Psychopharmakotherapie bei Schizophrenie. Die Empfehlungen basieren auf publizierten kontrollierten und offenen Studien sowie Fallberichten [aus 5, modifiziert nach 1]
|
Problem |
Empfohlen |
Nicht empfohlen |
|
Negativsymptomatik |
Amisulprid, Aripiprazol, Clozapin, Olanzapin, Quetiapin, Risperidon, Ziprasidon, Flupentixol |
Haloperidol, Fluphenazin u. a. |
|
Depressive Syndrome |
Amisulprid, Aripiprazol, Olanzapin, Quetiapin, Risperidon, Ziprasidon, Flupentixol; bei Suizidalität Clozapin, ggf. kombiniert mit Antidepressivum |
Haloperidol, Fluphenazin u. a. |
|
Aggressivität, Antriebssteigerung |
Zuclopentixol |
Pimozid |
|
Ältere Patienten |
Haloperidol (?), Melperon |
Niedrigpotente Neuroleptika |
|
Patienten mit hoher Empfindlichkeit für EPMS |
Atypische Antipsychotika |
Haloperidol, Fluphenazin u. a. |
|
Patienten mit unerwünschter Sedierung |
Ziprasidon; Aripiprazol, Olanzapin, Risperidon |
Clozapin, Quetiapin |
|
Patienten mit Spätdyskinesien |
Atypische Antipsychotika |
Haloperidol, Fluphenazin u. a. |
|
Patienten mit Hypotonie |
Haloperidol (niedrig dosiert), Amisulprid, Risperidon, Ziprasidon |
Niedrigpotente Neuroleptika, Clozapin |
|
Patienten mit kardialer Vorschädigung |
Haloperidol |
Niedrigpotente Neuroleptika, Clozapin, Pimozid, Thioridazin, Ziprasidon |
|
Patienten mit Gewichtszunahme |
Aripiprazol, Ziprasidon, Fluphenazin |
Clozapin, Olanzapin |
|
Patienten mit Epilepsie |
Fluphenazin, Melperon |
Clozapin, Zotepin |
|
Patienten mit M. Parkinson |
Quetiapin, Olanzapin |
Haloperidol u. a. |
|
Patienten mit Diabetes mellitus |
Amisulprid, Aripiprazol, Ziprasidon |
Clozapin, Olanzapin |
Jede Therapie kann dabei ihre Wirkung besonders dann entfalten, wenn sie in einem Compliance-fördernden therapeutischen Umfeld stattfindet. Der Einsatz atypischer Antipsychotika ist nämlich nicht automatisch mit einer Verbesserung der Compliance verbunden, was nicht überraschen muss, weil die gute Verträglichkeit der Medikation nicht der einzige Compliance-relevante Faktor ist. Zum Beispiel fanden Valenstein et al. [46] gemessen an eingelösten Wiederholungsverordnungen von über 60 000 Patienten mit Atypika sogar etwas öfter eine schlechte Compliance als mit konventionellen Neuroleptika in der Routinebehandlung. Diaz et al. [13] statteten Schizophrenie-Patienten für drei Monate mit einem elektronischen Kontrollsystem für die Medikamenteneinnahme aus und fanden als wichtigen Compliance-Prädiktor die Dosierungsfrequenz (möglichst nur einmal täglich), daneben auch das Geschlecht und das Auftreten einer Akathisie, aber bei der globalen Auswertung keinen Unterschied zwischen atypischen und konventionellen Neuroleptika. Eine tendenziell bessere Compliance mit Atypika fanden zum Beispiel Dolder et al. [14] unter Bezug auf eingelöste Wiederholungsverordnungen, ein signifikanter Unterschied bestand aber nur nach sechs Monaten, nicht mehr nach zwölf Monaten. Awad und Voruganti stellten nach Auswertung entsprechender Studien ebenfalls fest, dass es lediglich einen Trend zu besserer Compliance bei Verwendung von Atypika gibt [4]. In der Metaanalyse von Neuroleptika-Langzeitstudien zeigten sich signifikante, wenn auch nummerisch mäßiggradige Vorteile der Atypika in den Absetzraten [27]. Gerade die im September 2005 publizierte CATIE-Studie (Clinical antipsychotic trials of intervention effectiveness) zeigte sehr hohe Absetzraten in der Langzeitbehandlung schizophrener Patienten auch unter verschiedenen Atypika [28]. Wie Dolder et al. schlussfolgerten, sind Compliance-fördernde Maßnahmen auch bei Patienten mit atypischer antipsychotischer Medikation angebracht [14].
Compliance und Rezidivprophylaxe
Die konsequente Antipsychotika-Behandlung – und somit auch eine hohe Compliance – ist Voraussetzung für eine erfolgreiche Prophylaxe schizophrener Rezidive. Eine Intervallbehandlung mit Frühintervention bei drohendem Rückfall oder gar erst Behandlung bei erneutem Schub konnte bei Patienten mit wiederholten Episoden Rückfälle deutlich weniger gut verhindern als eine antipsychotische Dauermedikation [18]. Kane berichtete in einer Übersichtsarbeit über Rückfallraten von 76% in durchschnittlich 18 Monaten bei Patienten, die ihre Medikation abgesetzt hatten; bei Intervallbehandlung zeigten sich Rückfallraten von 30 bis 35% pro Jahr, bei kontinuierlicher Behandlung Rückfallraten von 10 bis 20% pro Jahr [21].
Da höhere Rückfallraten mit einem höheren Bedarf an – besonders kostenintensiver – stationärer Behandlung einhergehen, ist ein Zusammenhang zwischen niedriger Compliance bei der Schizophrenie-Therapie und hohen Kosten einleuchtend [45]. Ein Beispiel ist die Analyse von Knapp et al. [23] aus Großbritannien, derzufolge Non-Compliance jährliche Mehrkosten durch Inanspruchnahme des Gesundheitssystems in Höhe von 5 000 Pfund pro Patient verursacht, davon die Hälfte durch stationäre Behandlung. Gilmer et al. [17] werteten kalifornische Krankenversicherungsdaten aus den Jahren 1998 bis 2000 aus und fanden, dass bei den Schizophrenie-Patienten, die ihre Medikamente vollständig genommen hatten, die psychiatrische Hospitalisierungsrate deutlich niedriger war als bei den nicht-complianten Patienten, aber auch niedriger als bei Patienten, die teilweise compliant waren oder mehr als die rechnerisch benötigte Medikation in Anspruch nahmen (Tab. 3). Die vollständig complianten Patienten hatten zwar höhere Arzneimittelkosten als die nicht oder teilweise complianten Patienten, aber deutlich niedrigere Krankenhauskosten. Entsprechende pharmakoökonomische Analysen für deutsche Verhältnisse würden wahrscheinlich ebenfalls verdeutlichen, dass es sinnvoll wäre, Maßnahmen zur Sicherung der Compliance zu fördern.
Tab. 3. Compliance und psychiatrische Hospitalisierungsrate in der Studie von Gilmer et al. [17]
|
Compliance-Charakteristik |
Häufigkeit |
Hospitalisierungsrate |
|
Vollständig compliant |
41% |
14% |
|
Nicht compliant |
24% |
35% |
|
Teilweise compliant |
16% |
24% |
|
Übermäßige Einnahme („excess fillers“) |
19% |
25% |
Die Chance für eine erfolgreiche Rezidivprophylaxe ist mit modernen Antipsychotika offenbar größer als mit konventionellen. Eine Metaanalyse von Studien mit Risperidon (Risperdal®), Sertindol (Serdolect®), Amisulprid (z.B. Solian®), Clozapin (z.B. Leponex®) und Olanzapin (Zyprexa) ergab Ein-Jahres-Rückfallraten von 15% im Vergleich zu 23% mit konventionellen Antipsychotika [27, 33].
Die Compliance und die rezidivprophylaktische Wirksamkeit können durch die Gabe eines Depot-Antipsychotikums verbessert werden, wie bereits mit konventionellen Antipsychotika gezeigt wurde [16]. Diese Behandlung war lange Zeit eher den schwer behandelbaren chronisch schizophrenen Patienten mit ausgeprägten Compliance-Problemen vorbehalten. Inzwischen ist auch ein atypisches Depot-Antipsychotikum verfügbar, so dass eventuelle Vorbehalte gegen die Depottherapie in Bezug auf Nebenwirkungen nicht mehr gerechtfertigt sind und diese Therapieform auch für weitere Patientenkreise erwogen werden kann [33]. Eine kürzlich publizierte Studie zur Depotform von Risperidon (Risperdal® Consta®) gibt anhand von Daten aus Deutschland Hinweise dafür, dass sich das Depotprinzip verbunden mit dem Atypika-Prinzip auch pharmakoökonomisch rechnet [32].
Neben der Art der Pharmakotherapie spielen verschiedene psychosoziale Aspekte für die Sicherung oder Verbesserung der Compliance eine Rolle. Auf diese wird im weiteren Verlauf eingegangen.
Wenn eine Rezidivprophylaxe über lange Zeit erfolgreich ist, stellt sich früher oder später die Frage, ob sie fortgeführt oder abgesetzt werden soll. Auch diese Frage sollte mit dem Patienten im Sinne eines gemeinsam festgelegten Therapieziels besprochen werden. Die Studienlage dazu ist allerdings dünn, da randomisierte Studien selten länger als zwei Jahre dauerten [33]. Eine Ausnahme ist die Studie von Cheung [8], in der 30 Patienten nach drei- bis fünfjähriger erfolgreicher neuroleptischer rezidivprophylaktischer Behandlung doppelblind auf ein Neuroleptikum oder Benzodiazepin umgestellt wurden. Die Vergleichsgruppe hatte innerhalb von 18 Monaten deutlich mehr Rezidive (62%) als die weiterhin neuroleptisch behandelte Gruppe (13%). Die Leitlinienempfehlung lautet, nach bisher rezidivierendem Verlauf die neuroleptische Rezidivprophylaxe für zwei bis fünf Jahre, nach multiplen Rezidiven unter Umständen lebenslang durchzuführen [12]. Die American Psychiatric Association empfiehlt eine lebenslange Rezidivprophylaxe bei mehreren vorangegangenen Rezidiven oder bei zwei Rezidiven innerhalb von fünf Jahren [1].
Das therapeutische Team
Die Einstellung des Patienten zu seiner Krankheit und ihrer Therapie wird auch in der Begegnung mit anderen Angehörigen des therapeutischen Teams (z.B. Pflegekräften, Sozialpädagogen, Psychologen, Arbeits- und Beschäftigungstherapeuten, Bewegungstherapeuten) geprägt. Diese Personen haben also maßgeblichen Einfluss auf die Compliance. Es ist daher wichtig, dass das therapeutische Team ausreichend über das Therapiekonzept informiert und darauf eingeschworen ist. Teilweise gibt es hier gravierende Diskrepanzen [40]. So herrscht in manchen Berufsgruppen eher Skepsis in Bezug auf den Wert von Psychopharmaka oder es existieren unterschiedliche Konzepte zur Lebensqualität (z.B. mit der Folge des ungehinderten Zugangs stationärer Patienten zu Süßigkeiten). Das therapeutische Team sollte aber gegenüber dem Patienten „mit einer Zunge sprechen“. So lassen sich auch Erwartungen des Patienten zum Rollenverhalten der Therapeuten nutzen. Beispielsweise dürfte die Glaubwürdigkeit einer Arzneimittelempfehlung aus dem Mund eines Psychologen manchmal höher sein, als wenn sie von einem Arzt kommt. Am besten gelingt die gemeinsame Umsetzung des Therapiekonzepts, wenn Compliance-verbessernde Maßnahmen fest in den Therapieplan und die Stationsroutine eingebaut werden.
Angehörige und Freunde des Patienten
Angehörige und andere enge Bezugspersonen des Patienten können seine Compliance im positiven wie im negativen Sinne stark beeinflussen. Dabei spielen Beziehungsaspekte (z.B. Fürsorge, Schuldgefühle) eine Rolle, aber auch der gesamtgesellschaftliche Rahmen, denn die Angehörigen spiegeln die Stereotypen der Bevölkerung und damit deren Einstellung gegenüber psychischen Erkrankungen und Psychopharmaka wider.
Diese Einstellung hat sich erfreulicherweise in den letzten Jahren etwas verbessert, ist aber noch weit von einem wünschenswerten Zustand entfernt. Das zeigen zum Beispiel zwei repräsentative Umfragen, die in Deutschland in den Jahren 1990 und 2001 durchgeführt wurden [2]. Mit der Fallvignette einer Schizophrenie konfrontiert, empfahlen 1990 noch 65,5% der Befragten, einen Psychiater aufzusuchen, 2001 waren es bereits 82,1%. Ein Psychotherapeut wurde von 65,6% und 83,0% empfohlen, ein Allgemeinarzt von 71,4% vs. 61,0%. Die psychische Erkrankung wurde also offenbar als solche gewürdigt und eher einem spezifischen Therapeuten zugeordnet. Der Empfehlungsgrad für eine psychotrope Pharmakotherapie stieg von 30,7% auf 57,3%, für eine Psychotherapie von 67,9% auf 83,5%. In diesen Zahlen drückt sich immer noch eine beträchtliche Skepsis gegenüber einer Pharmakotherapie aus. Diese zeigte sich auch, wenn den Befragten Aussagen zu den Wirkungen psychotroper Pharmaka vorgelegt wurden. Zum Beispiel stimmten der Aussage „Arzneimittel sind die Therapieform, mit der am wahrscheinlichsten eine schnelle Besserung erreicht werden kann“ 2001 erst 31,9% der Befragten zu (1990: 22,7%), während 37,3% (1990: 26,5%) der Meinung waren, dass Psychopharmaka einen letztlich nur kränker machen [3].
Insgesamt lassen die Ergebnisse aber darauf schließen, dass das Wissen der Bevölkerung für psychische Erkrankungen, speziell deren Therapie, zugenommen hat. Vergleichbares fanden in einer aktuellen Studie Jorm et al. in Australien [20]. Dennoch bleibt noch viel Aufklärungs- und Informationsarbeit zu tun. Besonders wichtig ist diese natürlich bei den Angehörigen psychisch Kranker. Durch ihre Einbeziehung in die Psychoedukation kann die Compliance deutlich verbessert werden, wobei die besten Ergebnisse mit einem bifokalen Ansatz erzielt werden, also der Unterrichtung von Patienten und Angehörigen in getrennten Gruppen [39].
Psychoedukative Verfahren
Die Wirksamkeit der Psychoedukation als Compliance-fördernde Maßnahme mit entsprechend günstigen Wirkungen auf den Langzeitverlauf ist inzwischen gut belegt. Ein Beispiel für den Erfolg der Psychoedukation bietet das Münchner Psychosen-Informations-Projekt (PIP-Studie), bei dem stationäre Schizophrenie-Patienten und ihre Angehörigen nach dem bifokalen Ansatz an acht Psychoedukationssitzungen teilnahmen und auch nach der Entlassung des Patienten entsprechend weiterbetreut wurden [6, 38]. Die Rehospitalisierungsrate der Teilstichprobe der TU München (n = 48) betrug in der Kontrollgruppe nach einem Jahr 33%, nach sieben Jahren 88%, in der Interventionsgruppe dagegen nur 13% bzw. 54%. Noch deutlicher war der Einfluss bei Betrachtung der kumulativen Rehospitalisierungsdauer pro Patient: Diese betrug in der Kontrollgruppe 28 Tage (1 Jahr) bzw. 225 Tage (7 Jahre), in der Interventionsgruppe dagegen 18 Tage bzw. 75 Tage.
Dolder et al. [15] werteten entsprechende Veröffentlichungen seit 1980 aus und kamen zu dem Ergebnis, dass die stärkste Verbesserung der Compliance erreicht wird, wenn auf Information, Verhalten und Affekt zielende Strategien kombiniert werden. Für ein gutes Therapieergebnis war außerdem ausschlaggebend, dass die Interventionen längerfristig erfolgten und dass ein Bündnis („alliance“) zwischen dem Patienten und den Therapeuten entstand.
Einen fehlenden langfristigen Nutzen einer Compliance-Therapie fanden zum Beispiel O’Donnell et al. [35]. Allerdings wurden hier lediglich fünf Sitzungen à 30 bis 60 Minuten durchgeführt und es erfolgte keine entsprechende Nachbetreuung. Indirekt stützt die Studie also die Forderung nach einer langfristigen Intervention.
Auch bei bipolaren Störungen haben psychoedukative Maßnahmen mit dem Ziel, die Compliance zu verstärken und die Früherkennung von Prodromalzeichen zu fördern, das Therapieergebnis verbessert [9].
Psychoedukation wird in den US-amerikanischen Leitlinien zur Therapie bei Schizophrenie [1] ebenso empfohlen wie in der unlängst erschienenen S3-Leitlinie Schizophrenie der DGPPN [12].
Trotz ihres unzweifelhaften Erfolgs wird die Psychoedukation in Deutschland aber noch wenig umgesetzt. Laut einer Umfrage unter 622 Klinikleitungen psychiatrischer Einrichtungen (Rücklaufquote: 54%) führten zwar 85% der antwortenden Einrichtungen Psychoedukation durch – 72% bei Schizophrenie, weniger bei anderen Diagnosen –, aber im Mittel nahmen nur 21% aller stationären Patienten und nur etwa 2% ihrer Angehörigen an einer Psychoedukation teil [42]. Noch ungünstiger dürfte es im niedergelassenen Bereich aussehen, zumal hier die Abrechnungsmöglichkeiten nach wie vor sehr ungünstig sind. Zwar gibt es inzwischen prinzipiell bessere Abrechnungsmöglichkeiten für die Psychoedukation; da die Gesamtaufwendungen aber durch die Quartalspauschale gedeckelt sind, kann Psychoedukation de facto trotzdem nicht angemessen abgerechnet werden. Eine Verbesserung des Zustands könnte durch die integrierte Versorgung erreicht werden. Erste Projekte sind inzwischen auch in der Psychiatrie mit den Kassen vereinbart worden und erfolgreich angelaufen [22]. Im Rahmen der integrierten Versorgung wird die Psychoedukation frei von sektoralen Grenzen angemessen honoriert.
Strukturelle Compliance-fördernde Maßnahmen
Ein positiver Nebenaspekt der integrierten Versorgung könnte sein, dass die Koordination von verschiedenen beteiligten Therapeutengruppen und insbesondere des Übergangs zwischen stationärem und ambulantem Bereich verbessert wird. Dies kann auch zur Förderung der Compliance beitragen. Einiges lässt sich aber auch ohne Einbindung in ein integriertes Versorgungssystem erreichen. So sollte ein Patient nur entlassen werden können, wenn er einen ambulanten Anschlusstermin hat (zu dem dann auch der Arztbrief vorliegen muss). Zu einer guten Entlassungsplanung gehört weiterhin, dass der Patient rechtzeitig ausreichend über seine Therapie informiert worden ist und möglichst ein entsprechendes Medikamententraining absolviert hat. Das Informationsmaterial dazu sollte patientengerecht sein (Beispiel: Dosierungsangabe in Tabletten, nicht in mg).
Wünschenswert ist eine gute Abstimmung mit den nicht-psychiatrischen Mitbehandlern, allerdings nur mit Zustimmung des Patienten.
Ein noch unzureichend gelöstes Problem ist die langfristige Koordination bei Wechsel des Arztes und die Frage, wie der Langzeitverlauf so dargestellt werden kann, dass ein neuer Therapeut schnell einen Überblick erhält.
Eine Zusammenfassung über Maßnahmen, die die Compliance des Patienten unterstützen und fördern können, gibt Tabelle 4.
Tab. 4. Maßnahmen zur Sicherung oder Verbesserung der Compliance
|
Klare Therapieziele definieren |
|
Krankheits- und Therapiekonzept des Patienten (und seiner Angehörigen) berücksichtigen |
|
Auswahl des Antipsychotikums unter Berücksichtigung der physischen und psychischen Disposition des Patienten |
|
Einfaches Dosierungsschema |
|
Vertrauensvolles Gesprächsklima schaffen (Thematisierung von Nebenwirkungen) |
|
Subjektiv störende Nebenwirkungen berücksichtigen |
|
Patientenzufriedenheit erfragen |
|
Therapeutisches Team einbinden |
|
Psychoedukation (auch für Angehörige) und Medikamententraining |
|
Transparente Versorgungsstrukturen schaffen (integrierte Versorgung) |
Aufgaben für die Zukunft
Ein wichtiges Ziel ist die weitere Etablierung der Psychoedukation, um bei den Patienten und deren Angehörigen Verständnis für ihre Erkrankung und die Besonderheiten der Therapie zu wecken. Hilfreich könnten hier strukturierte Programme mit vorgegebenen standardisierten Schulungs- und Arbeitsmaterialien sein. Auch die bessere Koordination der beteiligten Therapeutengruppen, die Einschwörung des therapeutischen Teams auf ein Behandlungskonzept, die Wahl einer individuell angepassten und möglichst unkomplizierten Therapie sind Aufgaben, die Optimierungsspielraum bieten. Außerdem gilt es, möglichst viele Informationen zur Non-Compliance und ihren beteiligten Faktoren zu sammeln. Dafür wären einfache, zuverlässige Erfassungsinstrumente wünschenswert. Hier besteht zweifellos noch Forschungsbedarf.
Danksagung
Für redaktionelle Unterstützung bei der Erstellung des Manuskripts danken wir Dr. Heike Oberpichler-Schwenk, Stuttgart.
Literatur
1. American Psychiatric Association. Treatment guideline for the treatment of patients with schizophrenia. 2nd edition, 2004. www.psych.org/psych_pract/treatg/pg/SchizPG-Complete-Feb04.pdfhttp://www.psych.org/psych_pract/treatg/pg/SchizPG-Complete-Feb04.pdf
2. Angermeyer CM, Matschinger H. Have there been any changes in the public’s attitudes towards psychiatric treatment? Results from representative population surveys in Germany in the years 1990 and 2001. Acta Psychiatr Scand 2005;111:68–73.
3. Angermeyer CM, Matschinger H. Public attitudes towards psychotropic drugs: have there been any changes in recent years? Pharmacopsychiatry 2004;37:152–6.
4. Awad AG, Voruganti LN. New antipsychotics, compliance, quality of life, and subjective tolerability – are patients better off? Can J Psychiatry 2004;49:297–302.
5. Bandelow B. Handbuch Psychopharmaka. 2. Auflage. Göttingen: Hogrefe-Verlag, 2004.
6. Bäuml J, Pitschel-Walz G, Basan A, et al. Die Auswirkungen des protektiven Potenzials von Angehörigen auf den Langzeitverlauf schizophrener Psychosen: Ergebnisse der 7-Jahreskatamnese der Münchner PIP-Studie. In: Binder W, Bender W (eds.). Die dritte Dimension in der Psychiatrie – Angehörige, Betroffene und Professionelle auf einem gemeinsamen Weg. Köln: Claus Richter Verlag, 2003:129–59.
7. Byerly M, Fisher R, Whatley K, Holland R, et al. A comparison of electronic monitoring vs. clinician rating of antipsychotic adherence in outpatients with schizophrenia. Psychiatry Res 2005;133:129–33.
8. Cheung HK. Schizophrenics fully remitted on neuroleptics for 3–5 years – to stop or to continue drugs? Br J Psychiatry 1981;138:490–4.
9. Colom F, Lam D. Psychoeducation: improving outcomes in bipolar disorder. Eur Psychiatr 2005;20:359–64.
10. Colom F, Vieta E, Martinez-Aran A, Reinares M, et al. Clinical factors associated with treatment concompliance in euthymic bipolar patients. J Clin Psychiatry 2000;61:549–55.
11. Cramer JA, Rosenheck R. Compliance with medication regimens for mental and physical disorders. Psychiatr Serv 1998;49:196–201.
12. Deutsche Gesellschaft für Psychiatrie, Psychotherapie und Nervenheilkunde (Hrsg.). S3-Praxisleitlinien in Psychiatrie und Psychotherapie. Band 1: Behandlungsleitlinie Schizophrenie. Darmstadt: Steinkopff, 2006.
13. Diaz E, Neuse E, Sullivan MC, Pearsall HR, et al. Adherence to conventional and atypical antipsychotics after hospital discharge. J Clin Psychiatry 2004;65:354–60.
14. Dolder CR, Lacro JP, Dunn LB, Jeste DV. Antipsychotic medication adherence: Is there a difference between typical and atypical agents? Am J Psychiatry 2002;159:103–8.
15. Dolder CR, Lacro JP, Leckband S, Jeste DV. Interventions to improve antipsychotic medication adherence: review of recent literature. J Clin Psychopharmacol 2003;23:389–99.
16. Gerlach J. Depot neuroleptics in relapse prevention: advantages and disadvantages. Int Clin Psychopharmacol 1995;9(Suppl 5):17–20.
17. Gilmer TP, Dolder CR, Lacro J, Folsom DP, et al. Adherence to treatment with antipsychotic medication and health care costs among Medicaid beneficiaries with schizophrenia. Am J Psychiatry 2004;161:692–9.
18. Godemann F, Linden M, Gaebel W, Köpke W, et al. Is interval medication a successful treatment regimen for schizophrenic patients with critical attitudes towards treatment? Eur Psychiatry 2003;18:82–4.
19. Hamann J, Cohen R, Leucht S, Busch R, et al. Do patients with schizophrenia wish to be involved in decisions about their medical treatment? Am J Psychiatry 2005;162:2382–4.
20. Jorm AF, Christensen H, Griffiths KM. The public’s ability to recognize mental disorders and their beliefs about treatment: changes in Australia over 8 years. Aust N Z J Psychiatry 2006;40:42–6.
21. Kane JM. What can we achieve by implementing a compliance-improvement program? Int Clin Psychopharmacol 1997;12(Suppl):S43–6.
22. Kissling W, Seemann U, Fritze J. Integrierte Versorgung. NeuroTransmitter 2004;10:30–5.
23. Knapp M, King D, Pugner K, Lapuerta P. Non-adherence to antipsychotic medication regimens: association with resource use and costs. Br J Psychiatry 2004;184:509–16.
24. Lacro JP, Dunn LB, Dolder CR, Leckband SG, et al. Prevalence and risk factors for medication non-adherence in patients with schizophrenia: a comprehensive review of recent literature. J Clin Psychiatry 2002;63:892–909.
25. Lambert M, Conus P, Eide P, Mass R, et al. Impact of present and past antipsychotic side effects on attitude toward typical antipsychotic treatment and adherence. Eur Psychiatry 2005;19:415–22.
26. Lambert M, Schimmelmann BG, Haasen C, Naber D. Subjektive Befindlichkeit unter neuroleptischer Therapie. Relevant für die Psychopharmakotherapie psychotischer Patienten? Psychopharmakotherapie 2002;9:53–9.
27. Leucht S, Barnes T, Kissling W, Engel R, et al. Relapse prevention in schizophrenia with new antipsychotic: a meta-analysis of randomized controlled trials. Am J Psychiatry 2003;160:1209–22.
28. Lieberman J, Stroup TS, McEvoy JP, Swartz MS, et al., Clinical Antipsychotic Trials of Intervention Effectiveness (CATIE) Investigators. Effectiveness of antipsychotic drugs in patients with chronic schizophrenia. N Engl J Med 2005;353:1209–23.
29. Linden M. Definition of compliance. Int J Clin Pharmacol Ther Toxicol 1981;19:86–90.
30. Linden M. Förderung der Patientencompliance. In: Möller HJ (Hrsg.). Therapie psychiatrischer Erkrankungen. Stuttgart: Thieme, 2000:139–46.
31. Linden M, Godemann F, Gaebel W, Köpke W, et al. A prospective study of factors influencing adherence to a continuous neuroleptic treatment program in schizophrenia patients during 2 years. Schizophr Bull 2001;27:585–96.
32. Möller HJ, Laux G, Naber D, Gastpar MT, et al. Kosten und Effekte von Risperidon in Depotform. Vergleich mit oralen Atypika und konventionellen Depotformulierungen in der Therapie von Schizophrenie-Patienten in Deutschland. Psychopharmakotherapie 2005;12:183–92.
33. Möller HJ. Der Einsatz neuer Antipsychotika in der Langzeittherapie schizophrener Patienten. Psychopharmakotherapie 2004;11: 2–10.
34. Naber D, Karow A, Lambert M. Subjective well-being under neuroleptic treatment and its relevance for compliance. Acta Psychiatr Scand 2005;111(Suppl 427):29–34.
35. O’Donnell C, Donohue G, Sharkey L, Owens N, et al. Compliance therapy: a randomised controlled trial in schizophrenia. BMJ 2003;327:834 (doi:10.1136/bmj.327.7419.834).
36. Osterberg L, Blaschke T. Adherence to medication. N Engl J Med 2005;353: 487–97.
37. Perkins DO. Predictors of non-compliance in patients with schizophrenia. J Clin Psychiatry 2002;63:1121–8.
38. Pitschel-Walz G, Bäuml J, Bender W, Engel RR, et al. Psychoeducation and compliance in the treatment of schizophrenia: results of the Munich PIP-Study. J Clin Psychiatry 2006;67:443–52.
39. Pitschel-Walz G, Leucht S, Bäuml J, Kissling W, et al. The effect of family interventions on relapse and rehospitalization in schizophrenia – a meta-analysis. Schizophr Bull 2001;27:73–92.
40. Rettenbacher MA, Burns T, Kemmler G, Fleischhacker WW. Attitudes of patients and professional carers towards the illness and antipsychotic medication. Pharmacopsychiatry 2004;37:103–9.
41. Rettenbacher MA, Hofer A, Eder U, Hummer M, et al. Compliance in schizophrenia: psychopathology, side effects, and patients’ attitudes toward the illness and medication. J Clin Psychiatry 2004;65:1211–8.
42. Rummel C, Pitschel-Walz G, Bäuml J, Kissling W. Umfrage zur aktuellen Versorgungssituation im Bereich Psychoedukation in deutschsprachigen Ländern. Nervenarzt 2004;75(Suppl 2):S48.
43. Sabaté E (Hrsg.). Adherence to long-term therapies: evidence for action. World Health Organization, Genf, 2003.
44. Sirey JA, Bruce ML, Alexopoulos GS, Perlick DA, et al. Stigma as a barrier to recovery: perceived stigma and patient-rated severity of illness as predictors of antidepressant drug adherence. Psychiatr Serv 2002;52:1615–20.
45. Thieda P, Beard S, Richter A, Kane J. An economic review of compliance with medication therapy in the treatment of schizophrenia. Psychiatr Serv 2003;54:508–16.
46. Valenstein M, Blow FB, Copeland LA, McCarthy JF, et al. Poor antipsychotic adherence among patients with schizophrenia: medication and patient factors. Schizophr Bull 2004;30:255–64.
47. Van Putten T. Drug refusal in schizophrenia: causes and prescribing hints. Hosp Community Psychiatry 1978;29:110–2.
Prof. Dr. Hans-Jürgen Möller, Psychiatrische Klinik und Poliklinik der Universität, Nussbaumstraße 7, 80336 München, E-Mail: hans-juergen.moeller@med.uni-muenchen.de
Prof. Dr. Matthias C. Angermeyer, Klinik und Poliklinik für Psychiatrie, Johannisallee 20, 04317 Leipzig
Prof. Dr. med. Dipl.-Psych. Borwin Bandelow, Psychiatrische Poliklinik, von-Siebold-Straße 5, 37075 Göttingen
Prof. Dr. Michael Deuschle, Zentralinstitut für seelische Gesundheit, J5, 68159 Mannheim
Priv.-Doz. Dr. Werner Kissling, Psychiatrische Klinik, Krankenhaus rechts der Isar, Ismaninger Straße, 81675 München
Prof. Dr. Michael Linden, BfA-Klinik Seehof, Lichterfelder Allee 55, 14513 Teltow
Prof. Dr. Dieter Naber, Klinik für Psychiatrische und Psychotherapie, Martinistraße 52, 20246 Hamburg
Prof. Dr. Max Schmauß, Bezirkskrankenhaus Augsburg,Dr.-Mack-Str. 1, 86156 Augsburg
Prof. Dr. Ulrich Voderholzer, Abt. Psychiatrie und Psychotherapie, Universitätsklinikum, Hauptstraße 5, 79104 Freiburg
Der vorliegende Beitrag entstand auf der Basis eines Expertentreffens am 20. Juni 2005, das von der Firma Pfizer finanziell unterstützt wurde.
Compliance in schizophrenia and comparable psychotic disorders
The term “compliance” is a measure for the quality of treatment. It describes to what extent the actual therapy matches a therapeutic optimum (e.g. a medication prescription), i.e., if the patient takes his medication as prescribed or takes part in other therapeutic measures. According to the current understanding of the relation between physician and patient, the therapeutic aim and measures are to be determined conjointly by physician and patient. To what extent these measures are put into practice, i.e. the compliance rate, is influenced by many factors. These factors are considered with regard to schizophrenia and bipolar disorders.
Keywords: Compliance, schizophrenia, bipolar disorder, psychoeducation
Psychopharmakotherapie 2007; 14(01)
