Dr. Annemarie Musch, Stuttgart
Epilepsie ist eine häufige Erkrankung, von der bis zu 1% der Bevölkerung betroffen ist. Bei zwei Drittel der Betroffenen wird die Erkrankung bereits im Kindesalter manifest.
Da bislang eine Antiepileptogenese nicht möglich ist, ist es das Ziel der antiepileptischen Therapie, Anfälle zu unterdrücken, bei den Patienten nach Möglichkeit Anfallsfreiheit, zumindest aber eine Reduktion der Anfallsfrequenz zu erreichen. Bei Kindern soll durch die Therapie eine normale Entwicklung insbesondere auch der kognitiven Fähigkeiten im sich entwickelnden Gehirn ermöglicht werden.
Seit 1870 sind zu Bromid zahlreiche neue Arzneistoffe für die antiepileptische Therapie hinzugekommen. Allerdings kann etwa einem Drittel der Patienten dennoch bislang nicht geholfen werden. Weiterhin ist das Nebenwirkungspotenzial der verfügbaren Arzneistoffe teilweise erheblich (z.B. Neurotoxizität, kognitive Beeinträchtigung, Beeinflussung des Verhaltens, Anfallsaktivierung, Beeinflussung des Hormonhaushalts). Einen Fortschritt stellen hier möglicherweise neuere Antiepileptika wie beispielsweise Levetiracetam (Keppra®) dar.
Levetiracetam ist ein Pyrrolidin-Derivat, das bereits seit September 2000 zur Zusatzbehandlung bei Epilepsie-Patienten mit partiellen Anfällen mit oder ohne sekundäre Generalisierung zugelassen ist (Abb. 1). Der Wirkungsmechanismus ist noch nicht eindeutig geklärt, scheint sich aber von dem anderer Antiepileptika zu unterscheiden. So wurde beispielsweise eine Interaktion mit einem Membran-Protein synaptischer Vesikel, dem SV2A-Protein (synaptic vesicle protein SV2A), nachgewiesen. SV2A spielt bei der Freisetzung von Neurotransmittern in den synaptischen Spalt, genauer gesagt bei der Fusion der Vesikel- mit der präsynaptischen Membran, eine Rolle.
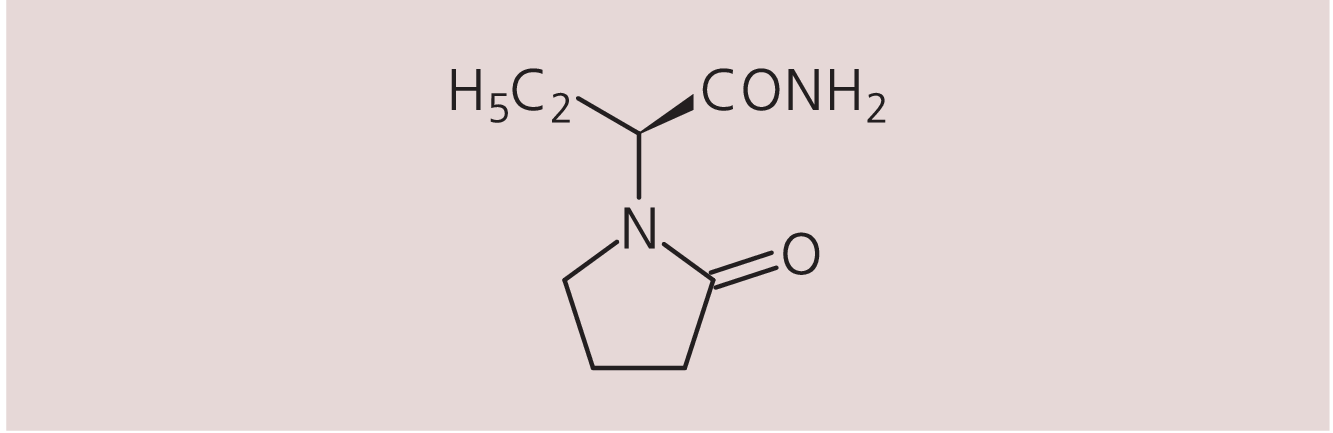
Abb. 1. Levetiracetam
Die Zulassung für Levetiracetam wurde von der europäischen Zulassungsbehörde im August 2005 erweitert, so dass der Arzneistoff auch zur Zusatztherapie bei Kindern ab 4 Jahren zur Verfügung steht.
In einer doppelblind und randomisiert durchgeführten Parallelgruppen-Studie wurden 216 Kinder (4–16 Jahre) mit fokalen Anfällen, die auf die Therapie mit ein oder zwei Antiepileptika bislang nicht angesprochen hatten, zusätzlich mit Levetiracetam oder Plazebo behandelt. Die Levetiracetam-Dosis wurde hierbei in einer 6-wöchigen Titrationsphase von 20 auf 60 mg/kg täglich gesteigert. Es folgte eine 8-wöchige Therapiephase, nach der die Patienten in einer offenen Langzeitstudie weiterbehandelt werden konnten oder die zusätzliche Medikation ausschleichend wieder abgesetzt wurde.
Die Daten von 198 Patienten konnten ausgewertet werden (Intention-to-treat-Gruppe, ITT-Gruppe), 193 Patienten schlossen die insgesamt 14-wöchige Studie ab.
Die zusätzliche Behandlung der Patienten mit Levetiracetam führte zu einer verglichen mit Plazebo signifikanten Reduktion der Anfallsfrequenz – dem primären Wirksamkeitskriterium der Studie – um 26,8% (p=0,0002). Signifikant mehr Patienten in der Levetiracetam- als in der Plazebo-Gruppe zeigten ein 50%ige Reduktion der Anfallsfrequenz (44,6 vs. 19,6%, p=0,0002). Gleiches galt für eine 75%ige Reduktion der Anfallsfrequenz (19,8 vs. 5,1%, p<0,0001). Weiterhin waren verglichen mit Plazebo mehr Patienten der Levetiracetam-Gruppe anfallsfrei (1 vs. 7%).
Bei der Untersuchung der Verträglichkeit wurden keine bislang unbekannten Nebenwirkungen der Therapie mit Levetiracetam festgestellt: Die Nebenwirkungen entsprachen denen, die bei der Therapie von Erwachsenen auftreten, beispielsweise wurden Somnolenz, zufällige Verletzungen und Asthenie berichtet.
In verschiedenen anderen Studien konnten die Wirksamkeit und Verträglichkeit der Therapie ebenfalls gezeigt werden. Meist wurden therapierefraktäre Kinder behandelt, denen nun eine weitere therapeutische Alternative angeboten werden kann. Dies ist ein wichtiger Fortschritt, nicht zuletzt, weil eine Epilepsie aufgrund der Akzeptanzprobleme in unserer Gesellschaft soziale Schwierigkeiten mit sich bringt, die die normale Entwicklung von Kindern mit Epilepsie beeinträchtigen können.
Weitere Studien laufen derzeit mit dem Ziel, in Zukunft beispielsweise auch noch jüngere Kinder behandeln zu können.
Quelle
Prof. Dr. med. Dietz Rating, Heidelberg, Prof. Dr. med. Gerhard Kurlemann, Münster, Prof. Dr. med. Florian Heinen, München, Dr. med. Jan-Peter Ernst, Kehl-Kork. „Turmgespräch Epilepsie: Keppra® – Jetzt ab 4!“, Köln, 25. November 2005, veranstaltet von UCB Pharma.
Glauser TA, et al. Multicenter, double-blind, placebo-controlled trial of adjunctive levetiracetam (Keppra®) therapy (up to 60mg/kg7day) in pediatric patients with refractory partial epilepsy. Epilepsia 2004;45(Suppl 7):186, ABS. B.03.
Lu Z, et al. Levetiracetam adjunctive therapy in children with refractory partial epilepsy, in comparison with other new antiepileptic drugs. Poster Presentation at the 6th European Paediatric Neurology Society Congress, Goteborg, September 2005.
Psychopharmakotherapie 2006; 13(03)
