Christina Lang und Albert C. Ludolph, Ulm
Narkolepsie
Die Narkolepsie ist eine seltene neurologische Erkrankung, der eine Störung der Schlaf-Wach-Regulation zugrunde liegt. Das wichtigste Symptom, und oft das erste, das auftritt, ist eine übermäßige Tagesschläfrigkeit (excessive daytime sleepiness, EDS), damit assoziiert können motorische, psychiatrische, emotionale, kognitive, metabolische und autonome Beeinträchtigungen auftreten. Die Symptome werden üblicherweise erstmals im Jugendalter oder im frühen Erwachsenenalter beobachtet, mit einer zweiten, kleineren Inzidenz-Spitze um das Alter von 35 Jahren [11]. Die weltweit geschätzte Verbreitung der Narkolepsie liegt bei 0,025 bis 0,05 % [25].
Im Jahr 1998 entdeckten zwei Forschergruppen unabhängig voneinander Orexin A und Orexin B (auch bekannt als Hypocretin 1 bzw. Hypocretin 2), kleine Neuropeptide, die ausschließlich von Neuronen im Hypothalamus produziert werden [14, 33]. Bald darauf zeigten Forschungsergebnisse, dass die Narkolepsie durch einen hochselektiven und ausgeprägten Verlust der Orexin-produzierenden Neuronen verursacht wird, der zu niedrigen Orexin-Konzentrationen im Gehirn und im Liquor führt [8, 42].
Die Narkolepsie geht mit einer Verschlechterung der Lebensqualität in zahlreichen Dimensionen einher [15]. Aufgrund ihrer Symptome sind Menschen mit Narkolepsie häufig nicht in der Lage, schulische oder berufliche Anforderungen zu erfüllen [16]. Das Risiko, mit einer Narkolepsie zusätzlich an einer Depression zu erkranken, ist erhöht [30, 39].
Leitsymptome und Diagnosekriterien
Zwei Typen der Narkolepsie werden in den aktuellen Diagnosekriterien der Internationalen Klassifikation der Schlafstörungen (International Classification of Sleep Disorders 3, ICSD-3) unterschieden [35] (Tab. 1). Bei der Narkolepsie Typ 1 liegen klinisch neben der EDS zusätzlich Kataplexien, und/oder ein verminderter Orexin-Spiegel im Liquor vor. Im Gegensatz dazu wird die Narkolepsie Typ 2 durch das Fehlen von Kataplexien definiert, die zugrunde liegende Neuropathologie ist weniger gut bekannt. Nach aktuellen Daten leiden etwa 65 bis 70 % der Patienten mit Narkolepsie auch an Kataplexien [16], wobei die Narkolepsie Typ 2 womöglich unterdiagnostiziert ist.
Tab. 1. Diagnosekriterien der Narkolepsie nach ICSD-3 [35]
|
Kriterium |
Narkolepsie Typ 1 |
Narkolepsie Typ 2 |
|
|
A |
Tagesschläfrigkeit |
Täglich unwiderstehliches Schlafbedürfnis/Einschlafen |
|
|
B |
Mindestdauer |
3 Monate (anamnestisch) |
|
|
Zusätzliche Bedingung |
C oder D + E |
C + D + E |
|
|
C |
Orexin-Wert im Liquor cerebrospinalis |
< 110 pg/ml |
> 110 pg/ml oder nicht gemessen |
|
D |
Kataplexie (anamnestisch) |
Vorhanden |
Keine |
|
E |
Multipler Schlaf-Latenz-Test (MSLT) |
Durchschnittliche Einschlaflatenz ≤ 8 min, mindestens 2-mal SOREM (1-mal SOREM in Polysomnographie möglich) |
|
|
Hinweise: Vor MSLT keine Einnahme von Substanzen, die Vigilanz oder REM-Schlaf beeinflussen, über mindestens 5 Halbwertszeiten; Kontrolle von 7 h Bettzeit (idealerweise polysomnographisch); Ausschluss anderer Erkrankungen, die Tagesschläfrigkeit erklären. |
|||
SOREM: sleep onset rapid eye movement sleep; REM: rapid eye movement; MSLT: multipler Schlaf-Latenz-Test
Die EDS stellt das Leitsymptom der Narkolepsie dar. EDS ist in monotonen Situationen besonders ausgeprägt (Monotonie-Intoleranz), doch im Unterschied zur physiologischen Schläfrigkeit kann diese bei Narkolepsie-Patienten meist nicht überwunden werden und kann auch in aktiven Phasen, beispielsweise während eines Gesprächs und während des Essens auftreten [6]. Gelegentlich kommt es bei Patienten in Phasen extremer Schläfrigkeit auch zu automatischen Handlungen, die dann meist fehlerbehaftet sind [6]. Die Tagesschläfrigkeit muss von einer Müdigkeit ohne Einschlafneigung oder von einer starken Erschöpfung abgegrenzt werden, da diese Beschwerden von Patienten häufig sehr ähnlich geschildert werden.
Zusätzlich zur EDS hat ein Teil der Patienten auch Symptome, die auf ein Auftreten von REM-Schlaf (Rapid-Eye-Movement-Schlaf) zu abnormalen Zeitpunkten hinweisen. Es wird grundsätzlich zwischen REM-Schlaf und Non-REM-Schlaf unterschieden. Der REM-Schlaf ist normalerweise durch Träume sowie durch eine Muskelatonie gekennzeichnet, die eine Person daran hindert, ihre Träume auszuagieren. Bei der Narkolepsie kann der REM-Schlaf durch die fehlende Suppression von Orexin zu jeder Tageszeit auftreten und Elemente des REM-Schlafs können sich in den Wachzustand oder in den Übergang zwischen Wach und Schlaf mischen [27]. Ein Ausdruck dieses Phänomens ist das Auftreten von Kataplexien. Bei Kataplexien handelt es sich um einen durch Emotionen ausgelösten, kurzzeitigen Tonusverlust der quergestreiften Muskulatur [13]. Plötzliche oder unerwartete Emotionen wie Lachen oder Erschrecken lösen Kataplexien aus und erklären ihr Auftreten in vielen alltäglichen Situationen, beispielsweise beim Sport. Der Tonusverlust kann partielle Körperbereiche wie die Nacken- oder Gesichtsmuskulatur (partielle Kataplexie) oder aber generalisiert die gesamte Haltemuskulatur betreffen und dauert meist nur wenige Sekunden an. Die emotionalen Trigger und das erhaltene Bewusstsein sind zuverlässige Kriterien für eine Kataplexie [31]. Durch diese Charakteristika können sie klinisch von Synkopen oder epileptischen Anfällen unterschieden werden.
Weitere Symptome
Bei der Narkolepsie können weitere Symptome vorhanden sein, die sich durch ein Auftreten von REM-Schlaf-Elementen erklären lassen und ebenfalls pathognomonisch für die Erkrankung sind: Es kann zu hypnopompen und hypnagogen Halluzinationen oder Schlaflähmungen kommen [36]. Diese Symptome kommen bei 40 bis 70 % der Narkolepsie-Patienten vor [40].
Traumartige und oft verstörende Halluzinationen sind bei Narkolepsie häufig. Wenn diese zu Beginn des Schlafs auftreten, werden sie als hypnagoge Halluzinationen bezeichnet; diejenigen, die beim Aufwachen auftreten, als hypnopompe Halluzinationen. Typische Halluzinationen sind beispielsweise das Gefühl, ein bedrohlicher Fremder sei im Schlafzimmer oder man werde von Tieren angegriffen [36].
Schlaflähmungen sind gekennzeichnet durch Aufwachen aus dem Schlaf mit einer kurzzeitigen Bewegungsunfähigkeit. Ein weiteres Symptom ist der fragmentierte Nachtschlaf mit zahlreichen kurzen nächtlichen Wachphasen.
Ätiologie und Pathophysiologie der Narkolepsie
Orexin-produzierende Nervenzellen, die ausschließlich im Hypothalamus vorkommen, sind unter anderem mit wachheitsfördernden neuronalen Netzwerken und dem limbischen System verbunden und spielen die Schlüsselrolle bei der Narkolepsie Typ 1 (Abb. 1). Der Verlust dieser Neuronen stellt die pathophysiologische Grundlage dieser Erkrankung dar [27]. Orexin fördert Wachepisoden und unterdrückt den REM-Schlaf. Ein Fehlen dieses Neuropeptids führt zu Schläfrigkeit und Schlafepisoden mit REM-Schlaf am Tag. Auch die weiteren REM-assoziierten Symptome wie Kataplexien oder Schlaflähmungen sind auf diesen Orexin-Mangel zurückzuführen [32].
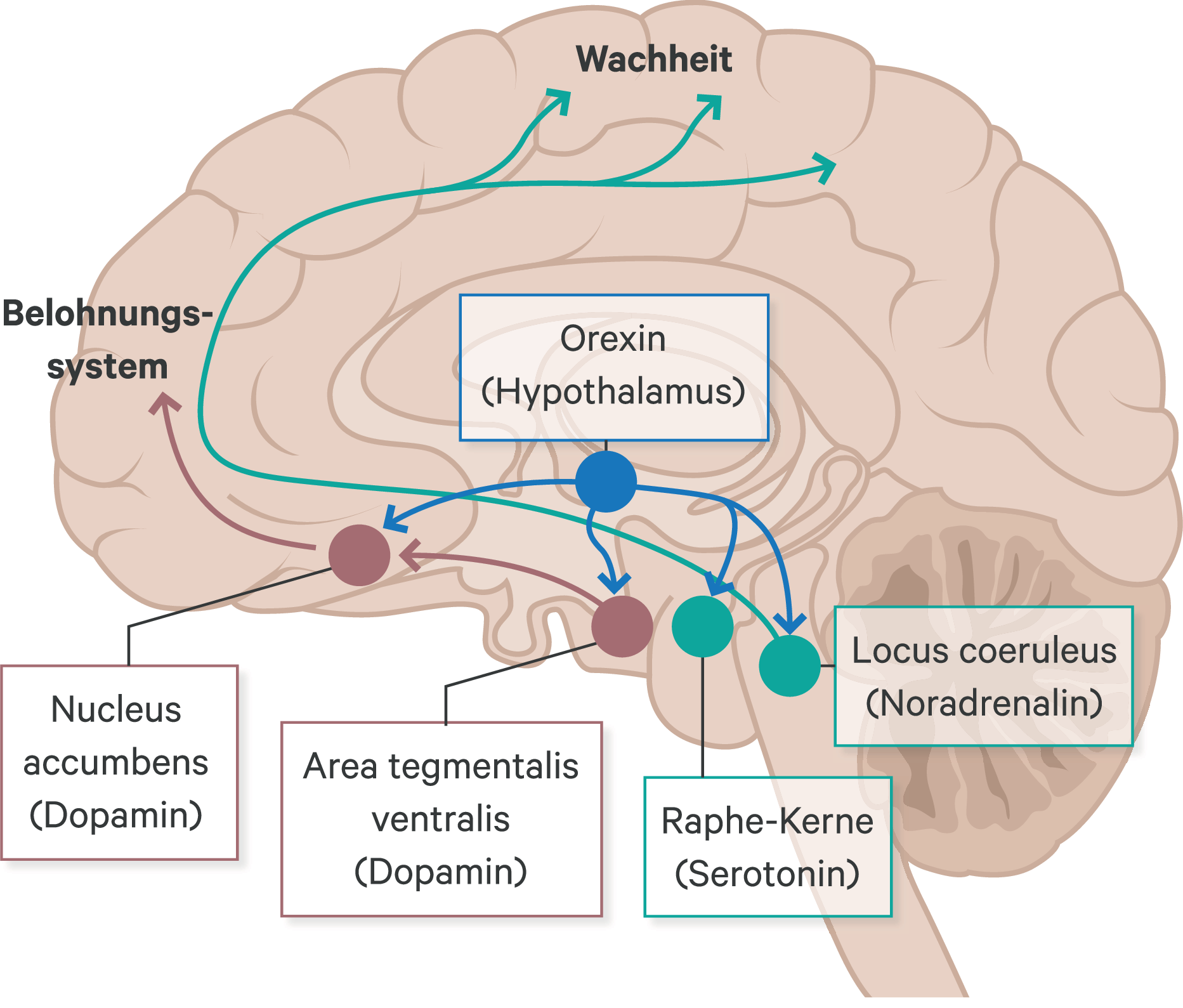
Abb. 1. Neuronale Vernetzung der Orexin-produzierenden Neuronen
Im Gegensatz dazu ist die Pathophysiologie der Narkolepsie Typ 2 (ohne Kataplexie und/oder ohne Orexin-Mangel) nach wie vor nur unzureichend verstanden. Die Existenz von unvollständigen Narkolepsie-Formen wird dadurch untermauert, dass ein Teil der Patienten mit dieser Diagnose im Verlauf – teilweise nach mehreren Jahren – Kataplexien entwickeln [6]. Zudem gibt es neuropathologische Hinweise für einen geringer ausgeprägten, aber vorhandenen Verlust von Orexin-produzierenden Neuronen [42].
Humangenetische Untersuchungen haben ergeben, dass Gene des Immunsystems an der Entstehung einer Narkolepsie beteiligt sind. Autoimmunkrankheiten werden häufig mit HLA-Genen in Verbindung gebracht. Eine HLA-Version, HLA-DQB1*06:02, ist bei mehr als 98 % der Menschen mit Narkolepsie vorhanden, während sie in der Allgemeinbevölkerung je nach ethnischer Zugehörigkeit nur bei 15 bis 30 % zu finden ist [26, 28]. Die in der Wissenschaft am weitesten akzeptierte Hypothese zur Ätiologie der Narkolepsie lautet daher, dass Orexin-produzierende Neuronen und eventuell auch Orexin-Rezeptoren durch aktivierte Zellen des Immunsystems zerstört werden [44].
Zusätzlich zur genetischen Prädisposition ist die Entstehung einer Narkolepsie getriggert durch verschiedene Umweltfaktoren, insbesondere durch Infektionen der oberen Atemwege [26]. Eine chinesische Studie mit 629 Patienten zeigte einen starken Zusammenhang zwischen der Entwicklung von Narkolepsie und Grippeinfektionen [18]. Dieser Studie zufolge steigt die Inzidenz der Krankheit jedes Jahr zwischen April und Juli. Zudem wird über einen dreifachen Anstieg der Narkolepsie-Inzidenz während der H1N1-Influenzapandemie 2009 berichtet, der jedoch nur vorübergehend war und zwei Jahre nach der Epidemie wieder auf das übliche Niveau zurückging [17]. Ebenso wurde ein Anstieg der Narkolepsie-Inzidenz nach Impfung mit dem H1N1-Impfstoff Pandemrix berichtet. Die Hypothese zur Erklärung des Zusammenhangs zwischen Narkolepsie und dem H1N1-Virus lautet, dass die Proteine dieses Virus eine gewisse Sequenzhomologie mit den Proteinen aufweisen, die von Orexin-produzierenden-Neuronen exprimiert werden [19].
Diagnostik
In der klinischen Praxis werden zur diagnostischen Sicherung einer Narkolepsie verschiedene Untersuchungen durchgeführt.
Der Epworth-Sleepiness-Scale-Test (ESS) ist ein Selbst-Fragebogen, der sich zur Einschätzung der EDS sowie zu deren Verlaufsbeurteilung anhand einfacher Fragen eignet. Es werden acht Alltagssituationen nach ihrer Wahrscheinlichkeit, einzuschlafen, abgefragt und mit 0 bis 3 Punkten bewertet. Dieser Test erleichtert die Differenzierung zwischen physiologischer und pathologischer Tagesschläfrigkeit [20, 43]. Weitere Fragebögen werden eingesetzt, um die Verdachtsdiagnose zu anderen Erkrankungen abzugrenzen und den Schweregrad der Narkolepsie-assoziierten Beschwerden einzuordnen [5, 34].
Zur diagnostischen Abklärung gehört weiterhin ein multipler Schlaf-Latenz-Test (MSLT): eine Untersuchung, bei der der Patient tagsüber in einem abgedunkelten Raum im Bett liegt und einschlafen darf, während EEG, EMG (Elektromyographie) am Kinn und EOG (Elektrookulographie) abgeleitet werden. Der Test besteht aus vier oder fünf Durchgängen mit einer Dauer von jeweils 20 Minuten. Eine pathologische Einschlafneigung liegt nach den Kriterien der ICSD-3 bei Narkolepsie bei einer Schlaflatenz von durchschnittlich weniger als acht Minuten vor. Als weiteres diagnostisches Kriterium gelten SOREM-Episoden (SOREM = sleep onset REM) – REM-Schlaf, der vorzeitig, also nicht nach der physiologischen Abfolge der Schlafstadien auftritt. Für die Validität des MSLTs ist die Einhaltung der Rahmenbedingungen wichtig: Alle Medikamente oder Substanzen, die die Wachheit beeinflussen oder REM-suppressiv wirken, müssen vorher pausiert werden (Abstand von fünf Halbwertszeiten bis zum Test); die Patienten dürfen zwischen den Durchgängen nicht schlafen, in der Nacht vor dem Test müssen mindestens sieben Stunden Bettzeit dokumentiert sein. Aus diesem Grund wird häufig zuvor eine nächtliche Polysomnographie durchgeführt. Diese hilft zudem, die Beschwerden von anderen Schlafstörungen abzugrenzen, aber auch die Identifikation von Narkolepsie-typischen Schlafmustern (SOREM und Schlaffragmentierung) zu unterstützen [16].
Die Orexin-Konzentrationsmessung im Liquor ist eine weitere Möglichkeit, die Diagnose einer Narkolepsie Typ 1 zu sichern. Das Vorliegen eines Orexin-Mangels ist definiert durch weniger als 110 pg/ml im Liquor [35] und hat eine Sensitivität von 87 % und Spezifität von 99 % für Narkolepsie Typ 1.
Therapie der Narkolepsie
Trotz Fortschritten im mechanistischen Verständnis der Narkolepsie gibt es derzeit keine Heilung, und die meisten Patienten benötigen eine Behandlung, die auf einer Reduktion der Symptome beruht [4, 12]. Da sich Symptome wie EDS und Kataplexien in ihrer Pathophysiologie unterscheiden, umfassen die Behandlungsmöglichkeiten sowohl einzelne Medikamente, die auf die Behandlung mehrerer Symptome abzielen, als auch den Einsatz mehrerer Medikamente, die jeweils auf einzelne Symptome abzielen. Zu den Optionen für die Behandlung von EDS bei Erwachsenen mit Narkolepsie gehören Modafinil und Natriumoxybat, die sowohl in der EU als auch in den USA zugelassen sind [3]. Die Zulassung von Modafinil wurde 2010 durch die Europäische Arzneimittelagentur EMA von initial mehreren Indikationen, unter anderem auch zur Behandlung der Tagesschläfrigkeit bei Patienten mit obstruktiver Schlafapnoe, auf die Anwendung bei Narkolepsie begrenzt. Grund waren Risiken für das Auftreten von psychiatrischen Reaktionen, schweren Hautreaktionen sowie von kardiovaskulären Nebenwirkungen. Auch Natriumoxybat hat eine Reihe von Einschränkungen, darunter das Missbrauchspotenzial und ein Dosierungsschema, das für manche Patienten schwer einzuhalten ist [7]. Andererseits wirkt Natriumoxybat als einzige Substanz gegen EDS und weitere Narkolepsie-Symptome. Auch andere Psychostimulanzien wie Methylphenidat und seltener Amphetamine (off Label) können als Zweit- und Drittlinientherapie zur EDS-Reduktion eingesetzt werden. Antidepressiva werden oft zusätzlich eingesetzt, um Kataplexien zu behandeln. Da Kataplexien, Schlaflähmungen und hypnagoge/hypnopompe Halluzinationen durch ein Auftreten von REM-Schlaf-Elementen zu nicht-physiologischen Zeitpunkten gekennzeichnet sind, macht man sich in der Therapie die REM-suppressive Wirkung zahlreicher Antidepressiva zunutze. Hier ist Clomipramin als einzige Substanz für die Reduktion der oben genannten REM-assoziierten Phänomene zugelassen [29]. Off Label werden hierfür häufig selektive Serotonin- und duale Serotonin- und Noradrenalin-Wiederaufnahmehemmer wie Fluoxetin, Paroxetin, Sertralin oder Venlafaxin verordnet. Als Zweitlinientherapie in diesem Kontext sind Therapieansätze mit weiteren trizyklischen Antidepressiva (z. B. Amitriptylin) oder Monoaminoxidase-Hemmern (z. B. Selegilin) möglich. Unter den trizyklischen Antidepressiva nimmt Trimipramin eine Sonderstellung ein: Es gilt als nicht REM-suppressiv, da es fast keine Serotonin- oder Noradrenalin-Wiederaufnahmehemmung zeigt. Aus diesem Grund wird Trimipramin nicht eingesetzt, um Symptome wie Kataplexien zu reduzieren. Neben Pitolisant als neue Substanz ist seit 2020 auch Solriamfetol zur Behandlung der EDS bei Narkolepsie in der EU zugelassen [2]. Solriamfetol reduziert die EDS durch eine Dopamin- und Noradrenalin-Wiederaufnahmehemmung.
Pitolisant
Wirkungsmechanismus
Histaminerge Neuronen, die vom hinteren Hypothalamus ausgehen, sind wichtig für die Schlafregulation und die Förderung des Wachseins [13]. Sie sind auch an höheren Hirnfunktionen wie Aufmerksamkeit und Lernen beteiligt [7]. Histaminerge Neuronen werden durch Orexin aktiviert. In Verbindung mit einem Orexin-Mangel wurde bei Patienten mit Narkolepsie eine verminderte Histamin-Ausschüttung nachgewiesen [5]. Der Histamin-3(H3)-Rezeptor hat sich daher als vielversprechendes pharmakologisches Ziel für die Behandlung der Narkolepsie erwiesen [5].
Pitolisant (Wakix® von Bioprojet Pharma) wirkt mittels eines dualen Wirkungsmechanismus als hochselektiver und potenter inverser Agonist und Antagonist des Histamin-H3-Rezeptors, was im Gehirn gezielt zu einer Aktivierung von histaminergen Neuronen und aminergen Neuronen führt, die wiederum mit den wachheitsfördernden Orexin-produzierenden Neuronen im Zusammenhang stehen [23, 37] (Abb. 2). Pitolisant passiert die Blut-Hirn-Schranke. Durch seine duale Wirkung auf präsynaptische H3-Rezeptoren hemmt es den negativen Rückkopplungsmechanismus dieses Autorezeptors und steigert damit die Histamin-Freisetzung im synaptischen Spalt. H3-Rezeptoren fungieren auch an nicht-histaminergen Neuronen als Autorezeptoren, sodass hier durch den H3-Antagonismus zusätzlich eine gesteigerte Freisetzung von Noradrenalin und Acetylcholin resultiert. Diese Mechanismen führen in Summe zu einer erhöhten Wachheit, einer Steigerung der Aufmerksamkeit, aber auch zur Reduktion von Häufigkeit und Ausprägung der Kataplexien und anderer REM-assoziierter Symptome [10, 41]. Allerdings wird die Dopaminfreisetzung im Nucleus accumbens, der eine zentrale Rolle im mesolimbischen System, dem „Belohnungssytem“ spielt, nicht beeinflusst, was Pitolisant neurochemisch von anderen wachheitsfördernden Mitteln, das heißt Amphetamin-ähnlichen Psychostimulanzien, unterscheidet [24].
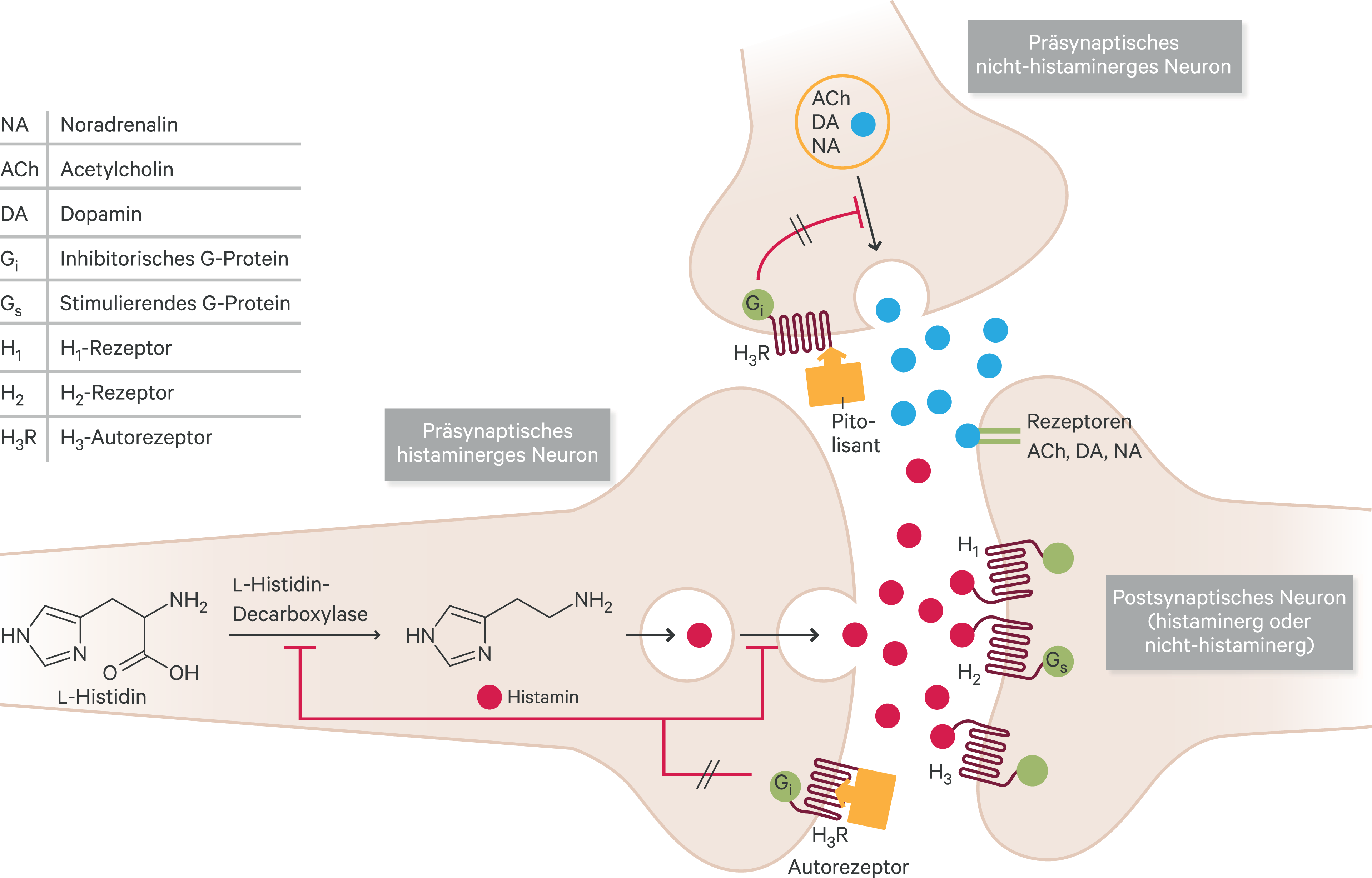
Abb. 2. Wirkungsmechanismus von Pitolisant (modifiziert nach J. S. Lin [23], mit Genehmigung von Bioprojet Pharma)
Die Wirksamkeit und Sicherheit von Pitolisant bei erwachsenen Patienten mit Narkolepsie wurden in fünf Phase-III-Studien untersucht. Zwei dieser Studien, HARMONY I [10] und HARMONY CTP [41], wurden als entscheidend für die Zulassung von Wakix® zur Therapie der Narkolepsie eingestuft [1]. Längerfristige unterstützende Wirksamkeitsdaten liegen aus der 12-monatigen, offenen, einarmigen, multizentrischen HARMONY-III-Studie vor, in der in erster Linie die Sicherheit von Pitolisant untersucht wurde [9].
Dosierung
Pitolisant wird oral verabreicht und sollte in der niedrigsten wirksamen Dosis unter Verwendung eines Aufdosierungsschemas angewendet werden (Tab. 2). Die Aufdosierung sollte an das Ansprechen und die Verträglichkeit des Patienten angepasst werden, ohne eine Dosis von 36 mg pro Tag zu überschreiten. Die tägliche Gesamtdosis wird morgens während des Frühstücks als Einzeldosis eingenommen, was, verglichen mit anderen Substanzen, die mehrfach am Tag eingenommen werden müssen, von Patienten als Vorteil gesehen wird.
Tab. 2. Empfohlene Dosistitration von Pitolisant bei der Narkolepsie-Behandlung
|
Dosierung |
Einnahmezeitpunkt |
|
|
Woche 1 |
Anfangsdosis von 9 mg Pitolisant pro Tag |
2 Filmtabletten à 4,5 mg 1-mal täglich morgens |
|
Woche 2 |
Dosiserhöhung auf 18 mg Pitolisant pro Tag (oder Dosisverringerung auf 4,5 mg Pitolisant pro Tag) |
1 Filmtablette à 18 mg 1-mal täglich morgens (oder 1 Filmtablette à 4,5 mg 1-mal täglich morgens) |
|
Woche 3 |
Dosiserhöhung auf 36 mg Pitolisant pro Tag |
2 Filmtabletten à 18 mg 1-mal täglich morgens |
Langzeitdaten aus Zulassungsstudien
Die Wirksamkeit und Sicherheit von Pitolisant bei der Behandlung von Narkolepsie-assoziierten Beschwerden über einen längeren Zeitraum wurde von Dauvilliers et al. in der HARMONY-III-Studie untersucht. 102 Patienten (davon 75 mit Narkolepsie Typ 1) erhielten Pitolisant in täglichen Dosen von bis zu 35,6 mg über einen Zeitraum von 12 Monaten. 68 Patienten (davon 51 mit Narkolepsie Typ 1) beendeten die 12-monatige Studie regulär [9]. Die Kohorte setzte sich zusammen aus Patienten ohne vorherige Pitolisant-Exposition und aus Teilnehmern vorheriger Studien mit Pitolisant, HARMONY I und HARMONY Ibis. In diesen ersten Phase-III-Studien konnte neben der Überlegenheit gegenüber Placebo bereits eine Nicht-Unterlegenheit zu Modafinil gezeigt werden [10, 21]. Erwähnenswert ist zudem, dass in der HARMONY-III-Studie Komedikationen mit anderen zentral wirksamen wachheitsfördernden Substanzen und mit anti-kataplektischen Substanzen erlaubt waren.
Tagesschläfrigkeit
Der mittlere ESS-Wert war zu Studienende nach 12 Monaten im Vergleich zum Ausgangswert sowohl in de novo mit Pitolisant behandelten Patienten als auch bei Patienten, die bereits zuvor Pitolisant erhalten hatten, signifikant verringert. Eine Verbesserung der ESS-Werte wurde bei der ersten Follow-up-Visite (Monat 1) beobachtet und über 12 Monate der Behandlung fortgesetzt, wie in Abbildung 3 dargestellt.
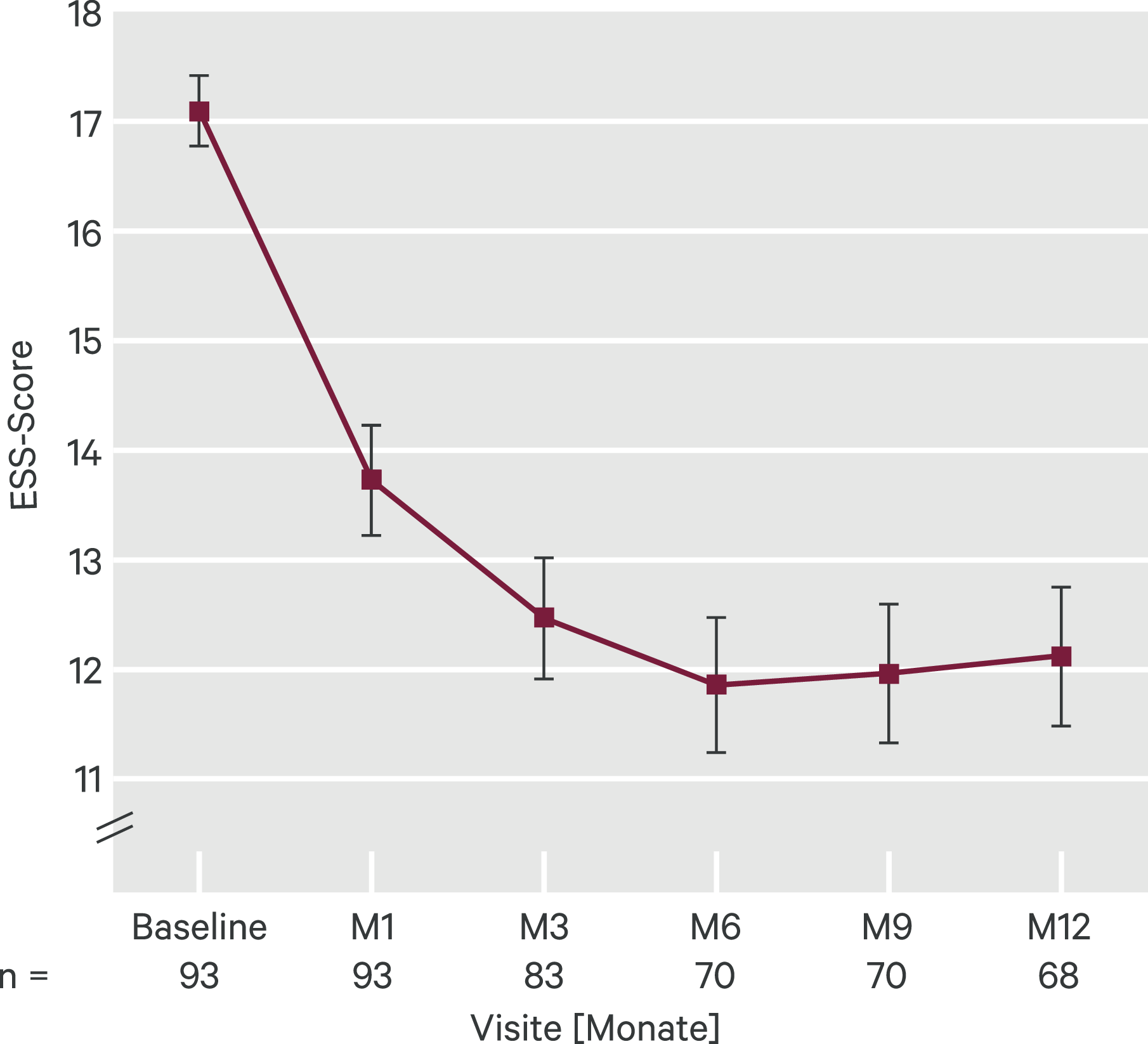
Abb. 3. Darstellung des Summenwerts des Epworth Sleepiness Scale im Verlauf der 12 Monate dauernden HARMONY-III-Studie in der Intention-to-treat-Population [9] ESS: Epworth Sleepiness Scale; M: Monat
Kataplexien und weitere Symptome
Die Behandlung mit Pitolisant reduzierte die Häufigkeit von Kataplexien und anderen REM-assoziierten Symptomen um jeweils mehr als 50 % nach 12 Monaten, wie in Tabelle 3 dargestellt. Bei Patienten, die bis zum 12. Monat Schlaftagebücher geführt hatten (n = 44), verringerte sich die durchschnittliche tägliche Anzahl unwillkürlicher Schlafattacken um 27 % (von 1,36 auf 0,99), die tägliche Anzahl nächtlicher Wachphasen reduzierte sich vom Ausgangswert bis zum 12. Monat signifikant (mittlere Veränderung –0,4; p < 0,001), während die mittlere Gesamtschlafdauer unverändert blieb.
Tab. 3. Veränderungen der Narkolepsie-Symptome nach einer 12-monatigen Behandlung mit Pitolisant. Ergebnisse aus der HARMONY-III-Studie zu Beginn der Studie und nach 12 Monaten Behandlung mit Pitolisant. Die Ergebnisse bezüglich der jeweiligen Symptome wurden anhand von Schlaftagebüchern erhoben [9].
|
Symptom (Anzahl der befragten Studienteilnehmer) |
Einschlafattacken (n = 44) |
Partielle Kataplexien (n = 44) |
Generalisierte Kataplexien (n = 43) |
Halluzinationen (n = 44) |
Schlaflähmungen (n = 44) |
|
Frequenz pro Tag zu Baseline |
1,36 |
0,77 |
0,33 |
0,13 |
0,16 |
|
Frequenz pro Tag nach 12 Monaten |
0,99 |
0,27 |
0,08 |
0,06 |
0,06 |
|
Veränderung der Frequenz pro Tag von Baseline zu Monat 12 |
–27 % |
–65 % |
–76 % |
–54 % |
–62 % |
Verträglichkeit von Pitolisant
Pitolisant wurde von Erwachsenen mit Narkolepsie, die an klinischen Studien teilnahmen, im Allgemeinen gut vertragen, wobei die meisten unerwünschten Ereignisse leicht bis mittelschwer waren [9, 10, 41]. Es liegen mehrere gepoolte Analysen von Verträglichkeitsdaten vor [21]. In den Phase-III-Studien betrug die mediane Dauer der Exposition 64 Tage; die Dosierung betrug 4,5 bis 36 mg einmal täglich. Behandlungsbedingte unerwünschte Ereignisse (TEAE) traten bei 52,3 %, 55,1 % bzw. 41,1 % der Pitolisant-, Modafinil- und Placebo-Patienten auf (0,276, 0,767 und 0,529 Ereignisse/Patientenmonat). Unerwünschte Arzneimittelwirkungen (UAW) traten bei 40,4 %, 38,8 % bzw. 20,3 % auf (0,161, 0,428 und 0,253 Ereignisse/Patientenmonat) [1]. Die am häufigsten berichteten Beschwerden bei mit Pitolisant behandelten Patienten waren Kopfschmerzen, Schlaflosigkeit, Übelkeit, Angstzustände und Reizbarkeit. Fälle von Kopfschmerzen und Schlaflosigkeit waren in der Regel leicht oder mittelschwer, und ihre Häufigkeit nahm mit der Dosis zu; nach Empfehlung sollte bei anhaltenden Kopfschmerzen oder Übelkeit eine Dosisreduktion oder ein Abbruch der Behandlung erwogen werden [9]. TEAE führten bei 5 % der Pitolisant-Patienten zum Abbruch der Behandlung (gegenüber 5,1 % und 3,2 % der Modafinil- und Placebo-Patienten) [12].
In der Langzeit-Studie wurde insbesondere die kardiale Verträglichkeit untersucht: bei der körperlichen Untersuchung, im Elektrokardiogramm oder im Labor wurden keine klinisch signifikanten Befunde beobachtet. Auch eine relevante Erhöhung des systolischen oder diastolischen Blutdrucks wurde nicht festgestellt. Die mittlere Änderung des korrigierten QT-Intervalls (QTc) von Beginn der Studie bis zum 12. Monat (n = 67) betrug 6,1 ms. Nach 12-monatiger Behandlung hatten alle Patienten QTc-Werte < 456 ms [9].
Verträglichkeit von Pitolisant
Häufige Nebenwirkungen unter einer Therapie mit Pitolisant sind Kopfschmerzen, Schlaflosigkeit, Übelkeit, Angst und Reizbarkeit. Im Verlauf der Behandlung zeigt sich oft eine Abnahme dieser Nebenwirkungen.
Bei gleichzeitiger Verabreichung von Pitolisant mit verschiedenen anderen Arzneimitteln sind pharmakokinetische und pharmakodynamische Wechselwirkungen möglich. In Bezug auf Kombinationen mit anderen bei Narkolepsie eingesetzten Medikamenten wurden bei der gleichzeitigen Verabreichung von Pitolisant mit Modafinil oder Natriumoxybat in therapeutischen Dosen bei gesunden Probanden keine klinisch relevanten pharmakokinetischen Arzneimittelwechselwirkungen beobachtet [1]. Es bestehen aber verschiedene Wechselwirkungen mit anderen Substanzen; hauptsächlich solchen, die das System der Cytochrom-P450-Metabolisierung verändern und deren gleichzeitige Verordnung unter gewissen Vorsichtsmaßnahmen geschehen sollte (Tab. 4). Insbesondere sollte bei Patientinnen vor der Menopause darauf hingewiesen werden, dass die Wirkung einer hormonellen Kontrazeption beeinträchtigt sein kann. Zudem sollten bei paralleler Gabe eines QT-Zeit-verlängernden Medikaments regelmäßige EKG-Kontrollen erfolgen.
Tab. 4. Wechselwirkungen von Pitolisant mit anderen Medikamenten und Empfehlungen zu Kombinationen
|
Substanzklasse |
Beispiele |
Kommentare |
|
Pharmakokinetische Interaktionen |
||
|
CYP2D6-Inhibitoren |
Paroxetin, Fluoxetin, Bupropion |
|
|
Starke CYP3A4-Induktoren |
Rifampicin, Carbamazepin, Phenytoin |
|
|
CYP3A4-Substrate |
Hormonelle Kontrazeptiva, Midazolam, Ciclosporin |
|
|
Pharmakodynamische Interaktionen |
||
|
Substanzen, die das QT-Intervall verlängern |
Klasse-1A- oder -3-Antiarrhythmika (z. B. Amiodaron), Antipsychotika und Antibiotika (z. B. Moxifloxacin) |
|
|
Zentral wirksame H1-Rezeptor-Antagonisten |
Antihistaminika, tri- oder tetrazyklische Antidepressiva |
|
CYP: Cytochrom P450; H1-Rezeptor: Histamin-H1-Rezeptor
Missbrauchspotenzial
Das Missbrauchspotenzial von Pitolisant wurde in der Studie um Setnik et al. untersucht [38]. Es wurden gesunde erwachsene Anwender von sogenannten Partydrogen im Alter von 18 bis 55 Jahren eingeschlossen (n = 38). Die Anwendung von Partydrogen wurde definiert als Nutzung von Stimulanzien für nichttherapeutische Zwecke (d. h. psychoaktive Wirkungen) für mindestens zehnmal im letzten Jahr und mindestens einmal in den letzten acht Wochen. Teilnehmer, die Phentermin (eine zentralnervös stimulierende Substanz) von Placebo unterscheiden konnten, wurden in einem doppelblinden Cross-over-Design randomisiert. Bei Phentermin handelt es sich um ein Appetit-reduzierendes und stimulierend wirkendes Amphetamin-Derivat. Es stimuliert die Katecholamin-Ausschüttung, und kann eine psychische Abhängigkeit hervorrufen.
Die Probanden erhielten Einzeldosen von Pitolisant 35,6 mg (optimale therapeutische Dosis), Pitolisant 213,6 mg (supratherapeutische Dosis), Phentermin-Hydrochlorid 60 mg und Placebo [38]. Der primäre Endpunkt war der maximale Effekt (Emax) für das „Drug Liking“ („in diesem Moment“), bewertet anhand einer visuellen Analogskala von 0 bis 100. Zu den wichtigsten sekundären Endpunkten gehörten die Gesamtbefürwortung der Substanz („Drug Liking“ generell) und die Bereitschaft, den Wirkstoff erneut einzunehmen („Take Drug Again“). Beides wurde ebenfalls auf einer visuellen Analogskala bewertet.
Der „Drug Liking“-Effekt war für Phentermin mit im Mittel 78,7 signifikant höher als für Pitolisant 35,6 mg (57,3) und Pitolisant 213,6 mg (59,0; beide p < 0,0001). Pitolisant wurde in beiden Dosierungen im Vergleich zu Placebo ähnlich bewertet (Tab. 5).
Tab. 5. Pharmakodynamische Messwerte im Zeitverlauf (n = 38) für (A) allgemeine Sympathie für die Substanz („Drug Liking“ in dem Moment), (B) für die generelle Sympathie für die Substanz und (C) für die erneute Einnahme der Substanz, für Placebo, Pitolisant und Phentermin [38]
|
Endpunkte (visuelle Analogskala von 0 bis 100) |
Placebo |
Pitolisant 35,6 mg |
Pitolisant 213,6 mg |
Phentermin HCl 60 mg |
|
|
A |
Emax „Drug Liking“ (in dem Moment) |
56,1 (2,1) |
57,3 (2,1)**** |
59,0 (2,1)**** |
78,7 (2,8) |
|
B |
Emax „Drug Liking“ (generell) |
54,4 (2,2) |
52,7 (2,1)**** |
49,2 (4,3)** |
77,4 (3,8) |
|
C |
Emax „Take Drug Again“ |
51,0 (2,9) |
49,4 (3,4)**** |
44,5 (4,9)**** |
78,7 (4,3) |
**p < 0,01 versus Phentermin; ****p < 0,0001 versus Phentermin Emax: maximaler Effekt auf visueller Analogskala
Zusammenfassend zeigte Pitolisant in dieser randomisierten, doppelblinden Cross-over-Studie im Vergleich zu Phentermin ein signifikant geringeres Missbrauchspotenzial und ein Placebo-ähnliches Gesamtprofil. Diese Ergebnisse legen nahe, dass bei Pitolisant kein relevantes Missbrauchsrisiko besteht.
Zulassung bei Kindern
Pitolisant ist noch nicht für Kinder zugelassen. Die Arbeitsgruppe um Lecendreux et al. konnte zeigen, dass sich Pitolisant bei Kindern und Jugendlichen in Dosen von bis zu 17,8 mg/Tag (bei einem Körpergewicht < 40 kg) bzw. von 35,6 mg/Tag (bei einem Körpergewicht ≥ 40 kg) zur Therapie der Narkolepsie eignet [22]. Dies wird aktuell in einer weiteren Studie (NCT02611687) geprüft.
Praxisbesonderheit/Orphan-Drug-Status von Pitolisant
Wakix® (Wirkstoff: Pitolisant) ist seit dem 1. Oktober 2017 als Praxisbesonderheit anerkannt.
Das Anwendungsgebiet lautet: „Wakix® wird angewendet bei Erwachsenen zur Behandlung der Narkolepsie mit oder ohne Kataplexie.“ Laut der Bewertung des Gemeinsamen Bundesausschusses (G-BA) ist Wakix® als Arzneimittel zur Behandlung eines seltenen Leidens zugelassen. Aus diesem Grund gilt der medizinische Zusatznutzen durch die Zulassung als belegt. Die Anerkennung als Praxisbesonderheit gilt nicht bei der Anwendung von Wakix® im Rahmen eines nicht bestimmungsgemäßen Gebrauchs („Off-Label-Use“).
Die kürzlich erfolgte Zulassungserweiterung für Pitolisant zur Behandlung bei obstruktiver Schlafapnoe als Ozawade® (s. a. S. 279 f.) wird nach derzeitigem Stand nicht zum Verlust des Orphan-Drug-Status führen.
Zusammenfassung
Die Narkolepsie ist eine seltene neurologische Erkrankung mit deutlicher Einschränkung von Funktion und Lebensqualität bei Betroffenen. Zentrales Symptom stellt die exzessive Tagesschläfrigkeit dar.
Pitolisant ist eine neue, wirksame und sichere Option in der Behandlung der Tagesschläfrigkeit und weiterer Narkolepsie-assoziierter Symptome. Durch seine Wirkung auf präsynaptische H3-Rezeptoren steigert Pitolisant die Histamin-Freisetzung im Gehirn und erhöht damit die Wachheit sowie die Aufmerksamkeit und vermindert Kataplexien und Halluzinationen. Pitolisant weist ein geringes Missbrauchspotenzial auf und unterscheidet sich damit signifikant von anderen wachheitsfördernden Mitteln, das heißt von Amphetamin-ähnlichen Psychostimulanzien. In der Langzeitanwendung konnten die Wirksamkeit und Sicherheit von Pitolisant als Monotherapie oder in Kombination mit anderen Narkolepsie-Medikamenten nachgewiesen werden. Damit stellt Pitolisant eine nebenwirkungsarme und wirksame Therapieoption, mit einem hohen Stellenwert in der Langzeitbehandlung der Narkolepsie, dar.
Interessenkonflikterklärung
Dr. med. Christina Lang hat von Bioprojet Pharma und von Jazz Pharmaceuticals Honorare für Vortrags- und Beratertätigkeiten erhalten.
Prof. Dr. Dr. med. Albert C. Ludolph: keine Interessenkonflikte.
Literatur
1. Pitolisant, Wakix, summary of product characteristics. London, United Kingdom. European Medicines Agency. 2016. EMEA/H/C/002616 – II/0023/G.
2. Sunosi (solriamfetol). An overview of Sunosi and why it is authorised in the EU. Amsterdam. European Medicines Agency. 2020. EMEA/H/C/004893. 3.
3. Barateau L, Lopez R, Dauvilliers Y. Management of narcolepsy. Curr Treat Options Neurol 2016;18:43.
4. Barateau L, Lopez R, Dauvilliers Y. Treatment options for narcolepsy. CNS Drugs 2016;30:369–79.
5. Bargiotas P, Dietmann A, Haynes AG, Kallweit U, et al. The Swiss Narcolepsy Scale (SNS) and its short form (sSNS) for the discrimination of narcolepsy in patients with hypersomnolence: a cohort study based on the Bern Sleep-Wake Database. J Neurol 2019;266:2137–43.
6. Bassetti CLA, Adamantidis A, Burdakov D, Han F, et al. Narcolepsy – clinical spectrum, aetiopathophysiology, diagnosis and treatment. Nat Rev Neurol 2019;15:519–39.
7. Busardo FP, Kyriakou C, Napoletano S, Marinelli E, et al. Clinical applications of sodium oxybate (GHB): from narcolepsy to alcohol withdrawal syndrome. Eur Rev Med Pharmacol Sci 2015;19:4654–63.
8. Crocker A, Espana RA, Papadopoulou M, Saper CB, et al. Concomitant loss of dynorphin, NARP, and orexin in narcolepsy. Neurology 2005;65:1184–8.
9. Dauvilliers Y, Arnulf I, Szakacs Z, Leu-Semenescu S, et al. Long-term use of pitolisant to treat patients with narcolepsy: Harmony III Study. Sleep 2019;42:zsz174.
10. Dauvilliers Y, Bassetti C, Lammers GJ, Arnulf I, et al. Pitolisant versus placebo or modafinil in patients with narcolepsy: a double-blind, randomised trial. Lancet Neurol 2013;12:1068–75.
11. Dauvilliers Y, Montplaisir J, Molinari N, Carlander B, et al. Age at onset of narcolepsy in two large populations of patients in France and Quebec. Neurology 2001;57:2029–33.
12. de Biase S, Nilo A, Gigli GL, Valente M. Investigational therapies for the treatment of narcolepsy. Expert Opin Investig Drugs 2017;26:953–63.
13. De la Herran-Arita AK, Garcia-Garcia F. Current and emerging options for the drug treatment of narcolepsy. Drugs 2013;73:1771–81.
14. de Lecea L, Kilduff TS, Peyron C, Gao X, et al. The hypocretins: hypothalamus-specific peptides with neuroexcitatory activity. Proc Natl Acad Sci U S A 1998;95:322–7.
15. Dodel R, Peter H, Spottke A, Noelker C, et al. Health-related quality of life in patients with narcolepsy. Sleep Med 2007;8:733–41.
16. Golden EC, Lipford MC. Narcolepsy: diagnosis and management. Cleve Clin J Med 2018;85:959–69.
17. Han F, Lin L, Li J, Dong XS, et al. Decreased incidence of childhood narcolepsy 2 years after the 2009 H1N1 winter flu pandemic. Ann Neurol 2013;73:560.
18. Han F, Lin L, Warby SC, Faraco J, et al. Narcolepsy onset is seasonal and increased following the 2009 H1N1 pandemic in China. Ann Neurol 2011;70:410–7.
19. Jacob L, Dauvilliers Y. [Narcolepsy with cataplexy: an autoimmune disease?]. Med Sci (Paris) 2014;30:1136–43.
20. Johns MW. A new method for measuring daytime sleepiness: The Epworth Sleepiness Scale. Sleep 1991;14:540–5.
21. Kollb-Sielecka M, Demolis P, Emmerich J, Markey G, et al. The European Medicines Agency review of pitolisant for treatment of narcolepsy: summary of the scientific assessment by the Committee for Medicinal Products for Human Use. Sleep Med 2017;33:125–9.
22. Lecendreux M, Plazzi G, Franco P, Jacqz-Aigrain E, et al. Pharmacokinetics of pitolisant in children and adolescents with narcolepsy. Sleep Med 2020;66:220–6.
23. Lin JS. Brain structures and mechanisms involved in the control of cortical activation and wakefulness, with emphasis on the posterior hypothalamus and histaminergic neurons. Sleep Med Rev 2000;4:471–503.
24. Lin JS, Dauvilliers Y, Arnulf I, Bastuji H, et al. An inverse agonist of the histamine H(3) receptor improves wakefulness in narcolepsy: studies in orexin–/– mice and patients. Neurobiol Dis 2008;30:74–83.
25. Longstreth WT, Jr., Koepsell TD, Ton TG, Hendrickson AF, et al. The epidemiology of narcolepsy. Sleep 2007;30:13–26.
26. Mahlios J, De la Herrán-Arita AK, Mignot E. The autoimmune basis of narcolepsy. Curr Opin Neurobiol 2013;23:767–73.
27. Mahoney CE, Cogswell A, Koralnik IJ, Scammell TE. The neurobiological basis of narcolepsy. Nat Rev Neurosci 2019;20:83–93.
28. Mignot E, Lin L, Rogers W, Honda Y, et al. Complex HLA-DR and -DQ interactions confer risk of narcolepsy-cataplexy in three ethnic groups. Am J Hum Genet 2001;68:686–99.
29. Deutsche Gesellschaft für Neurologie. Leitlinien für Diagnostik und Therapie in der Neurologie – Narkolepsie. Schlafstörungen. Prof. Dr. Christian Gerloff, Hamburg, 2012. AWMF-Registernummer: 030–056.
30. Raggi A, Plazzi G, Ferri R. Health-related quality of life in patients with narcolepsy: a review of the literature. J Nerv Ment Dis 2019;207:84–99.
31. Reading P. Cataplexy. Pract Neurol 2019;19:21–7.
32. Sakurai T. Orexin deficiency and narcolepsy. Curr Opin Neurobiol 2013;23:760–6.
33. Sakurai T, Amemiya A, Ishii M, Matsuzaki I, et al. Orexins and orexin receptors: a family of hypothalamic neuropeptides and G protein-coupled receptors that regulate feeding behavior. Cell 1998;92:573–85.
34. Sarkanen T, Alakuijala A, Partinen M. Ullanlinna Narcolepsy Scale in diagnosis of narcolepsy. Sleep 2019;42:zsy238.
35. Sateia MJ. International classification of sleep disorders – third edition: highlights and modifications. Chest 2014;146:1387–94.
36. Scammell TE. Narcolepsy. N Engl J Med 2015;373:2654–62.
37. Schwartz JC. The histamine H3 receptor: from discovery to clinical trials with pitolisant. Br J Pharmacol 2011;163:713–21.
38. Setnik B, McDonnell M, Mills C, Scart-Grès C, et al. Evaluation of the abuse potential of pitolisant, a selective H3-receptor antagonist/inverse agonist, for the treatment of adult patients with narcolepsy with or without cataplexy. Sleep 2020;43:zsz252.
39. Shneerson JM, Dauvilliers YA, Plazzi G, Myers AJ, et al. The impact of narcolepsy and its treatment – a European study. Eur Neurol Rev 2008;3:105–8.
40. Sturzenegger C, Bassetti CL. The clinical spectrum of narcolepsy with cataplexy: a reappraisal. J Sleep Res 2004;13:395–406.
41. Szakacs Z, Dauvilliers Y, Mikhaylov V, Poverennova I, et al. Safety and efficacy of pitolisant on cataplexy in patients with narcolepsy: a randomised, double-blind, placebo-controlled trial. Lancet Neurol 2017;16:200–7.
42. Thannickal TC, Nienhuis R, Siegel JM. Localized loss of hypocretin (orexin) cells in narcolepsy without cataplexy. Sleep 2009;32:993–8.
43. Walker NA, Sunderram J, Zhang P, Lu SE, et al. Clinical utility of the Epworth sleepiness scale. Sleep Breath 2020;24:1759–65.
44. Wurtman RJ. Narcolepsy and the hypocretins. Metabolism 2006;55:S36–9.
Dr. med. Christina Lang, Prof. Dr. Dr. med. Albert C. Ludolph, Abteilung Neurologie, Universitäts- und Rehabilitationskliniken Ulm (RKU), Oberer Eselsberg 45, 89081 Ulm, E-Mail: Christina.lang@uni-ulm.de
The role of pitolisant in the treatment of narcolepsy
Narcolepsy is a chronic neurological disorder with the key symptom of excessive daytime sleepiness. The impact on quality of life and daily living is severe. Narcolepsy type 1 is characterized by the additional presence of cataplexies and other sleep-wake symptoms such as hypnagogic hallucinations, sleep paralysis, and disturbed sleep. The peak of onset of initial symptoms is usually in young adulthood; lifelong symptomatic treatment is almost always necessary. The substance pitolisant, an inverse agonist and antagonist at the histamine H3 receptor, has been approved in Germany in 2016 for the treatment of narcolepsy with and without cataplexy. Histamine is a wakefulness-promoting neurotransmitter involved in stabilizing sleep-wake transitions. Pitolisant represents an important therapeutic option for patients with narcolepsy due to its new mechanism of action with reduction of daytime sleepiness and cataplexies as well as its safety profile.
Key words: narcolepsy, pitolisant, therapy, histamine H3 receptor, daytime sleepiness, cataplexy
Psychopharmakotherapie 2021; 28(06):251-259
