Thomas Messer und Eva Reil, Pfaffenhofen
Der Begriff „Psychonephrologie“ wurde von dem amerikanischen Psychiater Norman B. Levy Ende der 70er-Jahre eingeführt, um die vielfältigen psychologischen und psychiatrischen Problemfelder, die mit einer Niereninsuffizienz (NI) assoziiert sind, zu betonen [53].
Chronische Nierenerkrankungen stellen weltweit angesichts einer wachsenden Bevölkerung und regional unterschiedlichen Lebenserwartung ein zunehmendes Gesundheitsproblem dar [36]. Sie sind häufig assoziiert mit sogenannten „Wohlstandskrankheiten“ wie Diabetes mellitus, Adipositas oder kardiovaskulären Erkrankungen wie Hypertonie und Herzinsuffizienz [1, 54], die oft eine chronische Niereninsuffizienz zur Folge haben. Weltweit nahm zwar die Prävalenz chronischer Nierenerkrankungen, insbesondere der hypertensiven Nephropathie und der Glomerulonephritis, zwischen 1990 und 2013 um 3,6 % ab, allerdings war eine Zunahme der diabetischen Nephropathie um 12 % zu verzeichnen.
Insgesamt leiden in Deutschland nach Angaben der Deutschen Gesellschaft für Nephrologie etwa 11 % der Bevölkerung unter einer chronischen Nierenerkrankung, mit höherem Alter nimmt das Erkrankungsrisiko jedoch drastisch zu. Etwa die Hälfte der Personen über 75 Jahren haben ein chronisches Nierenleiden [2]. Angaben zur Jahresprävalenz dialysepflichtiger Patienten in Deutschland schwanken zwischen 50 800 [46] und knapp 92 000 [35].
Psychische Folgen von renalen Erkrankungen und deren Behandlung
Diabetes mellitus und Hypertonie stellen die häufigsten Ursachen einer renalen Erkrankung dar [71]. Neben zahlreichen Auswirkungen auf physiologische Parameter, etwa das Herz-Kreislauf-System sowie das zentrale Nervensystem, beeinträchtigen chronische Nierenerkrankungen in hohem Maße die allgemeine Lebensqualität und im Besonderen die psychische Gesundheit der Betroffenen [6, 20, 64, 71].
So verändern sich häufig soziale, familiäre und partnerschaftliche Beziehungen unter den Folgen einer Nierenerkrankung und deren Behandlung. Körperbild und Sexualität werden beeinträchtigt, Schmerzen, Schlafstörungen und Fatigue erschweren den Alltag und den Beruf signifikant [5].
Indem sich Erkrankte einer Dialysebehandlung unterziehen, kann zwar ihre Lebenserwartung verbessert werden, jedoch sollte diese Behandlungsform auch mit kritischem Blick betrachtet werden. Denn besonders dialysierte Patienten weisen deutlich häufiger psychiatrische Komorbiditäten auf als die Allgemeinbevölkerung.
Menschen mit chronischen Nierenerkrankungen und konsekutiver Dialysepflichtigkeit weisen mit einer geschätzten Prävalenz einer majoren Depression von 5 bis 22 % überproportional häufig depressive Störungen auf [17, 30, 42, 57]. Die Punktprävalenz für Angsterkrankungen wird zwischen 30 % und 45 % (zum Vergleich: in der Normalbevölkerung bei 18 %) geschätzt [20, 49].
Das medizinische Setting der Dialyse, die Wahrnehmung, von einer Maschine abhängig zu sein, sowie die Belastung durch somatische Komplikationen (z. B. Blutverlust, Elektrolytschwankungen, kardiologische Komplikationen) sind nur einige der dafür verantwortlichen Faktoren und wirken sich negativ auf die Behandlungsadhärenz aus [20]. In einer detaillierten Analyse von Cukor et al. zeigten sich hohe Prävalenzen für affektive Störungen (32,2 %) und Angststörungen (45,7 %), insbesondere Panikstörung und Blut-Spritzen-Phobie. Einige Patienten entwickeln darüber hinaus Symptome einer posttraumatischen Belastungsstörung und es finden sich hohe Komorbiditäten mit Medikamenten- und Alkoholmissbrauch (37,4 %) [14].
Eine Analyse zu geschlechtsspezifischen Risiken für eine Depression ergab bei 400 Hämodialysepatienten eine Prävalenz von fast 20 % und ein deutliches Überwiegen bei Frauen [29].
Als weitere häufige Folgen einer langfristigen Dialysebehandlung lassen sich kognitive Störungen von leichten kognitiven Beeinträchtigungen bis zu ausgeprägter Demenz feststellen, als deren Ursache unter anderem Blutdruckschwankungen und daraus resultierende ischämische Hirnläsionen diskutiert werden [18, 55].
Sexuelle Funktionsstörungen sind bei chronischen Nierenerkrankungen ebenfalls sehr häufig und werden von Männern in Form von Erektions- und Ejakulationsstörungen, von Frauen in Form von Lubrikationsstörungen und Dyspareunie berichtet. Libidoverlust und Orgasmusstörungen treten bei niereninsuffizienten Patienten mit einer geschätzten Prävalenz von 40 % bei Männern und 55 % bei Frauen auf [21]. Die Gründe sind multifaktoriell und lassen sich auf vaskuläre, neuropathische, endokrine, pharmakologische und psychologische Ursachen zurückführen.
Aufgrund der reduzierten körperlichen Funktionsfähigkeit und der ausgeprägten psychischen und psychosozialen Folgen unterliegen Personen, die sich einer Dialysebehandlung unterziehen müssen, im Vergleich zur Allgemeinbevölkerung einem erhöhten Risiko, Suizidgedanken zu entwickeln und Suizidhandlungen zu planen oder durchzuführen [47, 48, 61].
Darunter fällt im weitesten Sinne auch der Abbruch der Therapie durch aktives Beenden der Dialysebehandlung [11]. Männliches Geschlecht, höheres Alter, komorbider Substanzmissbrauch und der Verlust persönlicher Bindungen stellen auch vor allem in dieser Population Prädiktoren für Suizidalität dar.
Weibliches Geschlecht ist – neben Alter, niedriger Schulbildung, Diabetes, Arbeitslosigkeit und Hypalbuminämie – auch für die Depression bei dialysepflichtigen Personen ein Risikofaktor [4].
Nierentransplantation
2018 wurden in Deutschland rund 2000 Nierentransplantationen durchgeführt, etwa 8000 Patienten warten jährlich auf eine Transplantation. Die Wartezeit auf eine Spenderniere beträgt zwischen sechs und acht Jahren, was in vielen Fällen eine enorme psychische Belastung für die Betroffenen darstellen kann. Zu berücksichtigen ist eine Risiko-Nutzen-Abwägung zwischen den Belastungen, die mit einer Dialysebehandlung einhergehen, und den potenziellen negativen Folgen einer Transplantation. Dazu zählen Risiken primärer Funktionslosigkeit, Infektionen oder Abstoßung. Darüber hinaus hat die Transplantation eine lebenslange Behandlung mit Immunsuppressiva sowie häufige weitere medizinische Eingriffe zur Folge. Wegen dieser Belastungsfaktoren ist eine psychiatrische Einschätzung des Patienten vor einer Nierentransplantation unbedingt erforderlich. Nach einer Studie von Szeifert und Kollegen zur Depressionsprävalenz bei Transplantationspatienten und dialysierten Patienten, die auf eine Spenderniere warten, beträgt der Anteil derer mit depressiver Symptomatik unter Wartelisten-Patienten 33 %, unter transplantierten Studienteilnehmern 22 %. Komorbide Erkrankungen, sozioökonomischer Status und Nierenfunktion (post-treatment) konnten als Prädiktoren für depressives Outcome identifiziert werden [67]. Die Lebensqualität von Betroffenen verbessert sich nach einer Nierentransplantation im Allgemeinen deutlich [45, 63].
Veränderungen in Pharmakodynamik und Pharmakokinetik bei Nierenpatienten
Die genannten Faktoren begründen trotz einer begrenzten Datenlage die Notwendigkeit einer Psychopharmakotherapie bei renal erkrankten und dialysierten Patienten mit psychiatrischer Komorbidität. Jedoch muss in der Psychopharmakotherapie die Veränderung physiologischer Faktoren bei Nierenerkrankungen berücksichtigt werden. Aus pharmakodynamischer Sicht erhöht sich bei Nierenpatienten beispielsweise das Risiko kardialer Arrhythmien durch Elektrolytstörungen [43].
Als wichtiges Maß für die Funktionalität der Niere gilt die glomeruläre Filtrationsrate (GFR). Die GFR ist definiert als diejenige Menge an flüssigem Blutbestandteil, die pro Zeit in den Nephronen filtriert wird. Die GFR gilt für die Einschätzung der Nierenfunktion als wichtigste Größe und wird als synonym mit der Creatinin-Clearance (CrCl) angesehen. Gemäß den Empfehlungen der Kidney Disease Outcome Quality Initiative (KDOQI) bedeutet eine GFR von > 90 ml/min eine normale oder erhöhte GFR und eine GFR von 60 bis 89 ml/min eine leichtgradige Einschränkung der Nierenfunktion. Eine chronische Nierenerkrankung (Chronic kidney disease, CKD) wird bei einer GFR von < 60 ml/min angenommen, eine GFR von < 15 ml/min definiert die terminale Niereninsuffizienz [72].
Eine Stadieneinteilung der chronischen Nierenerkrankungen anhand der glomerulären Filtrationsrate (GFR) ist Tabelle 1 zu entnehmen.
Tab. 1. Stadieneinteilung der chronischen Nierenerkrankung anhand der glomerulären Filtrationsrate nach [72]
|
GFR-Stadium |
GFR |
Bezeichnung |
|
G1 |
≥ 90 |
Normal oder hoch |
|
G2 |
60–89 |
Leichtgradig eingeschränkt |
|
G3a |
45–59 |
Leicht- bis mäßiggradig eingeschränkt |
|
G3b |
30–44 |
Mäßig- bis hochgradig eingeschränkt |
|
G4 |
15–29 |
Hochgradig eingeschränkt |
|
G5 |
< 15 |
Terminale Niereninsuffizienz |
Im Stadium der terminalen Niereninsuffizienz dürfen vorwiegend renal eliminierte Pharmaka nicht mehr verordnet werden.
Während die meisten Psychopharmaka hepatisch metabolisiert werden und deshalb keine oder nur geringfügige renale Elimination der Muttersubstanz erforderlich ist, nimmt eine verringerte Nierenfunktion über verschiedene Mechanismen Einfluss auf die Pharmakokinetik. Die verringerte renale Elimination infolge reduzierter glomerulärer Filtration und reduzierter tubulärer Sekretion begünstigt die Akkumulation urämischer Toxine, was wiederum die hepatische Metabolisierung von Arzneistoffen sowohl über das Cytochrom-P450-System als auch P-Glykoprotein beeinträchtigt.
Nahezu alle für die Metabolisierung von Psychopharmaka verantwortlichen Cytochrom-P450-Enzyme (2C9, 2C19, 2D6 und 3A4) sind bei chronisch niereninsuffizienten Menschen vermutlich durch eine reduzierte CYP-Genexpression reduziert. Für die sogenannten Phase-II-Metabolisierung lassen sich ebenfalls eine verminderte Acetylierung, Glukuronidierung, Sulfation und Methylierung feststellen [60, 73].
Darüber hinaus ist aufgrund von Veränderungen im Körpergewicht und der Körperflüssigkeit das Verteilungsvolumen vermindert, die Bioverfügbarkeit und die Absorptionsrate sind reduziert und es lassen sich erhöhte Plasma- bzw. Serumspiegel von Psychopharmaka aufgrund verringerter Proteinbindung beobachten.
Abgesehen von den Veränderungen in der Pharmakokinetik erfordern die meisten Psychopharmaka keine Dosisanpassung. Ausgenommen davon sind solche Substanzen, deren Muttersubstanz oder aktiver Metabolit eine bedeutsame renale Elimination erfährt. Hierzu zählen insbesondere Lithium, Gabapentin, Pregabalin, Topiramat, Paliperidon, Risperidon, Paroxetin, Venlafaxin und Memantin.
Antidepressiva (AD)
Die empirische Datenlage zur Effektivität von Antidepressiva bei dialysierten Patienten ist gering. Zwar liefern einige wenige kleine Studien Hinweise auf positive Effekte, insgesamt kann aber von keiner robusten und nachhaltigen Wirksamkeit ausgegangen werden [58].
Prinzipiell sind keine Kontraindikationen für die Verschreibung von Antidepressiva bei Nierenerkrankungen bekannt, da Antidepressiva überwiegend hepatisch metabolisiert werden.
Die meisten klinischen Erfahrungen wurden aufgrund der jahrzehntelangen Verfügbarkeit mit den trizyklischen Antidepressiva (TZA) gesammelt. Für diese Substanzgruppe besteht eine erhöhte Sensitivität für Nebenwirkungen bei Dialyse-Patienten. Eine mögliche Ursache dafür ist die Erhöhung hydroxylierter Metaboliten, in deren Folge Sedierung, anticholinerge Toxizität, orthostatische Hypotension sowie QTc-Verlängerungen auftreten können. Sollen TZA zum Einsatz kommen, wird Nortriptylin empfohlen, weil es zu den TZA mit den geringsten anticholinergen Nebenwirkungen zählt (wie auch Desipramin, das allerdings in Deutschland nicht mehr auf dem Markt ist) [26].
Nachdem auch in den vergangenen Jahren keine signifikanten Wirksamkeitsvorteile von TZA gefunden wurden, ist ein Therapieversuch mit selektiven Serotonin-Wiederaufnahmehemmern (SSRI) wegen der besseren Verträglichkeit möglich und in einigen Fällen auch aussichtsreich [13].
Die Plasmakonzentration von Fluoxetin scheint durch eine Hämodialyse kaum verändert zu werden, da zwischen renaler Funktionseinschränkung und der Eliminationsgeschwindigkeit, dem Verteilungsvolumen oder der Plasmaproteinbindung bei Fluoxetin kein Zusammenhang gefunden wurde. Andererseits ist Fluoxetin zu einem sehr hohen Prozentsatz an Plasmaprotein gebunden und kann eine Reihe von anderen Arzneistoffen, beispielsweise Digoxin oder Phenprocoumon, aus dieser Proteinbindung verdrängen. Durch den erhöhten freien Anteil dieser Substanzen kann eine gesteigerte klinische Wirkung verursacht werden. Darüber hinaus ist mit Fluoxetin als einem potenten CYP2D6-Inhibitor ein klinisch relevantes Interaktionspotenzial zu beachten [38].
Frühere Studien zur Untersuchung der Wirksamkeit von Antidepressiva bei Patienten mit chronischer Niereninsuffizienz wurden in dialysepflichtigen Populationen durchgeführt und waren durch mangelnde Randomisierung und Kontrolle, kleine Stichproben, kurze Behandlungsdauer, geringe Adhärenz, hohe Abbrecherquoten und nicht standardisierte Kriterien für die Diagnose einer majoren Depression begrenzt.
Nur zwei Studien diagnostizierten majore Depression anhand eines psychiatrischen Interviews angemessen, von denen eine nur 14 Patienten umfasste, die über acht Wochen behandelt wurden [9], und die andere 30 Patienten über sechs Monate. In dieser multizentrischen, randomisierten, doppelblinden, Placebo-kontrollierten Studie mit Sertralin bei hämodialysierten Patienten mit Depression zeigten sich in beiden Gruppen klinische Verbesserungen, allerdings ohne statistischen Unterschied [25].
Es wird postuliert, dass eine hohe Placebo-Reaktion mit einem negativen Ausgang (Unwirksamkeit) von Antidepressiva-Studien verbunden ist [23]. Eine Metaanalyse von 169 randomisierten, Placebo-kontrollierten Studien zur Antidepressivum-Monotherapie ergab, dass eine Placebo-Ansprechrate von weniger als 30 % die beste Chance bietet, Wirksamkeit bei Arzneimittel-Placebo-Vergleichen zu finden [34]. Daher ist eine „hohe“ Placebo-Ansprechrate (im Sinne eines starken Placebo-Effekts) eine wahrscheinliche Erklärung dafür, dass in der Studie von Friedli et al. [25] kein signifikanter statistischer Unterschied in der Wirksamkeit von Placebo vs. Sertralin auf die Verbesserung depressiver Symptomatik gefunden wurde.
Ein weiterer Grund für die mangelnde Wirksamkeit könnte sein, dass eine mit chronischen Erkrankungen komorbide Depression eine andere klinische Einheit darstellt als die psychiatrische majore Depression bei Patienten ohne Komorbidität und die Depressionen, die nicht auf SSRI ansprechen. Die Studie von Friedli et al. umfasste Teilnehmer mit medizinischer Multimorbidität zusätzlich zu nicht dialysepflichtiger Niereninsuffizienz (58 % mit Diabetes, 27 % mit metabolischem Syndrom und 32 % mit Herzinsuffizienz), was es schwierig macht zu unterscheiden, ob die fehlende Reaktion auf Sertralin auf die chronische Niereninsuffizienz oder andere chronische Krankheiten zurückzuführen ist [25].
Diese Erwägungen gelten auch für Studien bei Patienten mit anderen chronischen Erkrankungen wie Asthma bronchiale, ischämischer Herzkrankheit und Herzinsuffizienz, in denen SSRI bei der Behandlung von Depressionen nicht oder nur wenig wirksamer erschienen als Placebo [3, 27].
In einer 12-wöchigen, randomisierten, Placebo-kontrollierten Studie (n = 201) bei chronisch niereninsuffizienten, allerdings nicht dialysepflichtigen Patienten war eine Behandlung mit Sertralin (Dosis 50 bis 200 mg/Tag) einer Placebo-Behandlung in Bezug auf die Reduktion depressiver Symptomatik ebenfalls nicht überlegen (Abb. 1) [31].
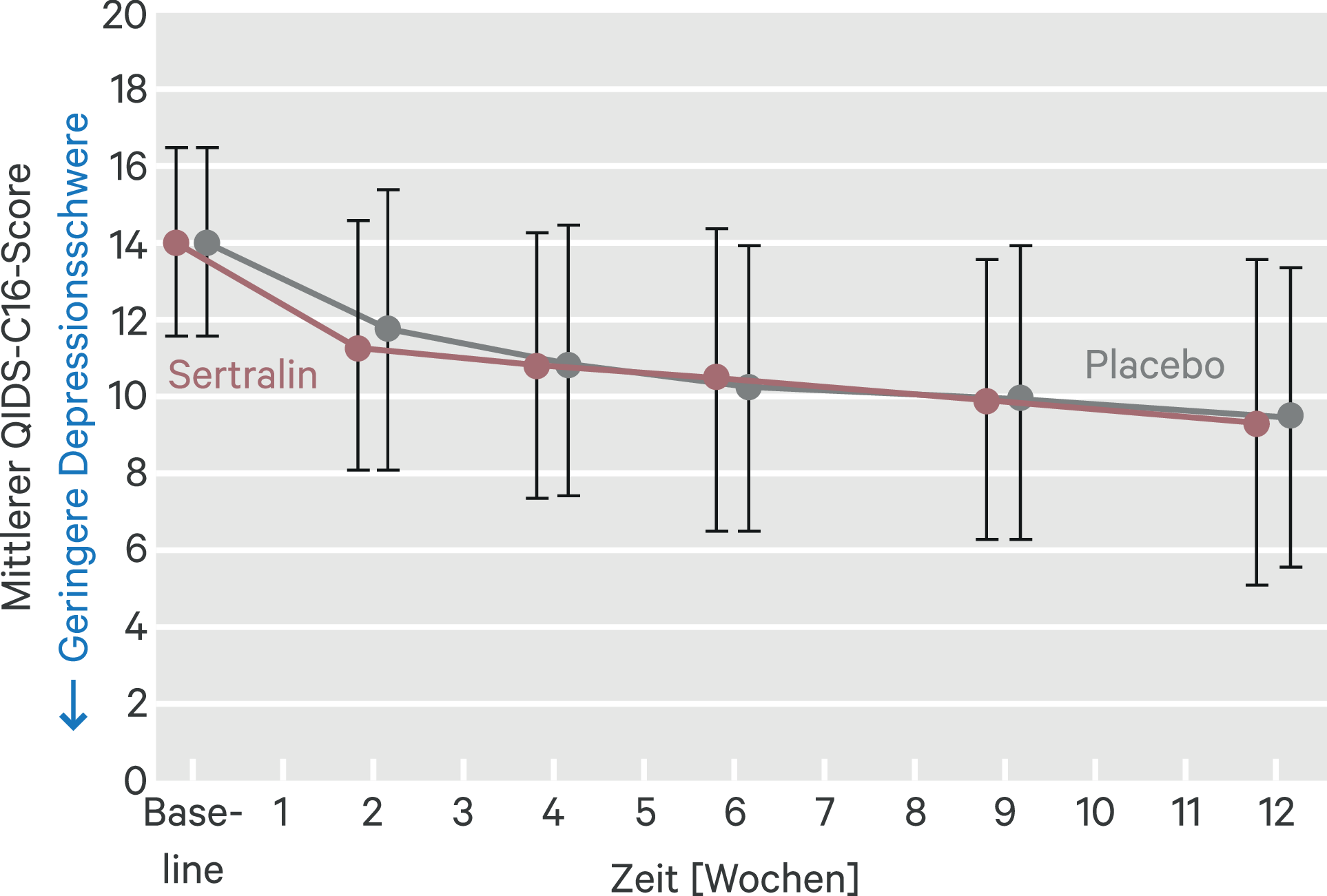
Abb. 1. Veränderung des mittleren (QIDS-C16) Scores (mod. nach [31]); QIDS-C16: 16-Item Quick Inventory of Depressive Symptomatology (Arztbewertung)
Für Citalopram bzw. Escitalopram wurde eine verlängerte Halbwertszeit und nur ein geringfügiger Anstieg der Plasmakonzentrationen bei Patienten mit eingeschränkter Nierenfunktion beobachtet (CrCl 10 bis 53 ml/min), weshalb auf eine Dosisanpassung verzichtet werden kann [65].
Mittels Paroxetin in geringer Dosis (10 mg/Tag) konnte in einer kleinen randomisierten Untersuchung in Kombination mit Psychotherapie ein geringfügiger Rückgang depressiver Symptome festgestellt werden [44]. Allerdings sollte die Verordnung von Paroxetin nicht nur wegen der potenten CYP2D6-Inhibition, sondern wegen einer bis zu 4-fach erhöhten Plasmakonzentration infolge reduzierter Clearance bei moderater bis schwerer Niereninsuffizienz generell nicht erwogen werden [16].
Beim Einsatz dual wirksamer Antidepressiva ist zu berücksichtigen, dass bei einer Niereninsuffizienz nicht die Clearance von Venlafaxin reduziert ist, sondern ausschließlich des Hauptmetaboliten Desvenlafaxin und somit dessen Eliminationshalbwertszeit verlängert ist, weshalb eine Dosisanpassung als prinzipiell notwendig angesehen wird [68]. Daher sollte bei moderater Niereninsuffizienz nur 50 bis 75 %, bei schwerer Niereninsuffizienz (GFR < 30 ml/min) etwa 25 bis 50 % der üblichen Dosis verordnet werden. Hämodialysierte Patienten sollten nur 50 % der üblichen Dosis nach jeder Behandlungseinheit erhalten. Duloxetin wird für Patienten mit schwerer Niereninsuffizienz (CrCl < 30 ml/min) nicht empfohlen.
Die Clearance von Mirtazapin kann bei moderater bis schwerer renaler Insuffizienz um 30 % bis 50 % reduziert sein, weshalb eine Dosisanpassung empfohlen wird. Für Trazodon ist keine Dosisanpassung notwendig, Vorsicht ist aber geboten, wenn das Arzneimittel Patienten mit schweren Nierenfunktionsstörungen verordnet wird. Allerdings hat eine große retrospektive Untersuchung keine nachteiligen Folgen einer höheren Dosis von Paroxetin, Mirtazapin oder Venlafaxin im Vergleich zu einer niedrigen Dosis nachgewiesen [15].
Bupropion sollte angesichts des Risikos für eine zerebrale Anfallsprovokation bei den hierfür prädisponierten Dialysepatienten nur in strenger Indikation und in Abhängigkeit vom Schweregrad nicht höher als 150 mg täglich eingesetzt werden [56, 69].
Für weitere Antidepressiva, beispielsweise Agomelatin oder Moclobemid, gibt es keine Empfehlungen für eine Dosisreduktion bei Niereninsuffizienz, die Dosis von Tianeptin sollte bei älteren Menschen mit Niereninsuffizienz auf 25 mg täglich begrenzt werden.
Antipsychotika
Agitationszustände und delirante Zustände gelten als häufige Komplikationen bei Niereninsuffizienz und Hämodialyse. Der Einsatz von älteren Neuroleptika, beispielsweise Haloperidol, wird im Bedarfsfall als unbedenklich angesehen [12]. Für die meisten neueren Antipsychotika, zum Beispiel Aripiprazol, Asenapin, Cariprazin, Clozapin, Olanzapin, Quetiapin oder Ziprasidon, besteht nach gegenwärtigem Kenntnisstand keine Erfordernis, die Verordnung einzuschränken oder die Dosis anzupassen.
Die Clearance für Risperidon und Paliperidon ist bei Niereninsuffizienz signifikant verringert, sodass bei leichter Niereninsuffizienz (CrCl > 60 ml/min) eine langsame Aufdosierung bis max. 6 mg/Tag, und bei moderater bis schwerer Niereninsuffizienz (CrCl 10 bis 50 ml/min) bis max. 3 mg/Tag über einen noch längeren Zeitraum erfolgen sollte [70]. Für Paliperidonpalmitat gilt gemäß Fachinformation die Empfehlung, bei Patienten mit leicht eingeschränkter Nierenfunktion (CrCl ≥ 50 ml/min) die Behandlung mit einer Dosis von 100 mg an Behandlungstag 1 und 75 mg eine Woche später zu beginnen. Die empfohlene monatliche Erhaltungsdosis beträgt 50 mg bzw. 25 bis 100 mg je nach individueller Verträglichkeit und/oder Wirksamkeit. Bei Patienten mit mittelschwerer oder schwerer Einschränkung der Nierenfunktion (CrCl < 50 ml/min) wird die Anwendung von Paliperidonpalmitat nicht empfohlen.
Bei dem ausschließlich renal eliminierten Amisulprid ist bei Niereninsuffizienz die Eliminationshalbwertszeit erhöht und die systemische Clearance um den Faktor 2,5 bis 3 vermindert, außerdem ist Amisulprid nur geringfügig dialysierbar. Deshalb fordert die Fachinformation, bei Patienten mit eingeschränkter Nierenfunktion die Tagesdosis bei einer Creatinin-Clearance zwischen 30 und 60 ml/min zu halbieren und bei einer Creatinin-Clearance zwischen 10 und 30 ml/min auf ein Drittel zu reduzieren; da bei Patienten mit schwerer Niereninsuffizienz (Creatinin-Clearance < 10 ml/min) keine Erfahrungen vorliegen, ist Amisulprid hier kontraindiziert.
Bei Dialysepatienten mit diabetisch bedingter Neuropathie besteht ein erhöhtes Risiko für Nebenwirkungen in Form von orthostatischer Hypotonie, Blasenfunktionsstörungen sowie gastrointestinalen und sexuellen Dysfunktionen. Bei Diabetes-Patienten empfiehlt sich daher eine Vermeidung der Gabe von Antipsychotika mit hyperglykämischem Risiko wie etwa Clozapin und Olanzapin. Unter Ziprasidon ist eine engmaschige EKG-Kontrolle wegen des dosisabhängig erhöhten Risikos für eine QTc-Zeit-Verlängerung erforderlich [52].
Eine retrospektive Kohortenanalyse an Antipsychotika-behandelten, schizophrenen und bipolaren Patienten ging der Frage nach, ob die Behandlung mit den Antipsychotika Aripiprazol, Fluphenazin, Haloperidol, Olanzapin, Quetiapin, Risperidon oder Ziprasidon zu einer akuten Nierenschädigung führen kann. Als Resultat dieser Untersuchung ergab sich eine Inzidenz einer akuten Nierenschädigung von 25 per 1000 Personenjahren. Unter Olanzapin, Quetiapin und Ziprasidon ergab sich im Verhältnis zu Haloperidol ein signifikant erhöhtes Risiko, Aripiprazol und Risperidon wiesen kein signifikant höheres Risiko auf. Fluphenazin hatte ein geringeres Risiko als Haloperidol. Im Klassenvergleich zeigte sich, dass die neueren Antipsychotika ein signifikant höheres Risiko für eine akute Nierenschädigung im Vergleich zu den älteren Antipsychotika bargen [37].
Anxiolytika und Sedativa/Hypnotika
Trotz der Häufigkeit von Angstzuständen liegen zur Behandlung von Angsterkrankungen mit Psychopharmaka bei dialysepflichtigen Patienten keine nennenswerten Studien vor. Es konnte zwar eine erhöhte Mortalität unter langfristiger Benzodiazepin-Einnahme festgestellt werden, eine Dosisanpassung wird jedoch als nicht zwingend notwendig angesehen. [52]. Auf Substanzen, die eine hohe Plasmaproteinbindung haben, beispielsweise Midazolam oder Chlordiazepoxid, sollte verzichtet werden. Für andere Benzodiazepine (BZD) wird keine Einschränkung gesehen, wobei solche BZD ohne aktive Metaboliten und mit kürzerer Halbwertszeit (Lorazepam, Oxazepam) anderen BZD (Diazepam, Lormetazepam) vorgezogen werden sollten. Die Halbwertszeit von Buspiron ist bei Patienten mit renaler Dysfunktion verlängert, weshalb diese Substanz nicht empfohlen wird. Für Zolpidem oder Zopiclon ist keine Dosisanpassung erforderlich.
Antikonvulsiva und Antimanika
Mehrere Studien haben gezeigt, dass eine Nierenfunktionsstörung nicht nur die renale Clearance verringert, sondern auch die hepatische Clearance von Arzneistoffen, die CYP3A4-Substrate sind. Die Ergebnisse einer retrospektiven Studie zum Einfluss der Nierenfunktion auf die Pharmakokinetik von Antiepileptika, die durch CYP3A4 metabolisiert werden, legen nahe, dass eine Dosisanpassung erforderlich ist, wenn bei Patienten mit mittelschwerer bis schwerer Nierenfunktionsstörung Topiramat, Clobazam oder Perampanel verschrieben wird. Für die Behandlung niereninsuffizienter Patienten mit Valproinsäure ist keine Dosisanpassung erforderlich. Gabapentin und Pregabalin werden häufig in der Behandlung neuropathischer Schmerzen, Pruritus oder auch Restless-Legs-Syndrom bei hämodialysierten Patienten eingesetzt. Für Gabapentin sollte bei einer CrCl von 30 bis 60 ml/min die Dosis von 600 mg/Tag, bei einer CrCl von 15 bis 30 ml/min 300 mg täglich und bei einer CrCl von < 15 ml/min 150 mg täglich nicht überschritten werden. Für Pregabalin wird bei einer CrCl von 30 bis 60 ml/min eine Dosisreduktion auf 50 %, bei einer CrCl von 15 bis 30 ml/min eine Dosisreduktion auf 25 % und bei einer CrCl von < 15 ml/min eine Dosisreduktion auf 12,5 % der üblichen Dosis empfohlen. Nachdem auch für Carbamazepin, Lamotrigin und Topiramat eine verringerte Clearance bei Niereninsuffizienz festgestellt wurde, sollte je nach Schwere der Niereninsuffizienz eine vergleichbare Dosisanpassung erfolgen.
Lithium
Besondere Vorsicht ist in der Behandlung mit Lithium geboten. Bereits bei einer GFR von 50 bis 60 ml/min kann eine signifikante Störung der Elimination von Lithium vorliegen, die eine moderate Dosisanpassung notwendig macht. Bei einer GFR von 30 bis 50 ml/min sollte die Dosis um 50 bis 75 % gesenkt werden. Eine GFR von < 30 ml/min gilt als schwere Niereninsuffizienz, die eine Behandlung mit Lithium ausschließt. Dialysepflichtige Patienten sollten 200 bis 600 mg nach einer Hämodialyse erhalten und die Serumspiegel sollten vor der nächsten Hämodialyse kontrolliert werden [12].
Um eine Niereninsuffizienz bei älteren Lithium-behandelten Patienten zu vermeiden, sollte der Lithium-Spiegel nicht höher als 0,8 mmol/l liegen, weshalb Laborkontrollen alle drei bis sechs Monate empfohlen werden. Darüber hinaus sollte eine Komedikation, insbesondere durch Diuretika und nichtsteroidale Antiinflammatorika, ebenso kritisch berücksichtigt werden wie die Entwicklung somatischer Komorbiditäten, beispielsweise ein nephrogener Diabetes insipidus, Rauchen, Diabetes mellitus, Hypertonie und koronare Herzerkrankung. In einer dänischen Kohorten-Studie, in der Patienten mit chronischer Niereninsuffizienz und einer Lithium-Behandlung (n = 754) mit Patienten unter einer Behandlung mit Antikonvulsiva (n = 5004) verglichen wurden, fand sich für die Lithium-behandelten Patienten kein erhöhtes Risiko dafür, das Endstadium einer Niereninsuffizienz, definiert als Dialysepflichtigkeit oder Transplantation, zu erreichen [40]. In Kombination mit Schleifendiuretika kann es zu einem Lithium-Anstieg kommen; ein Lithium-Abfall kann die Konsequenz einer gleichzeitigen Gabe von Carboanhydrase-Inhibitoren (z. B. Azetazolamid), Osmotika (z. B. Mannitol) oder Kalium-sparenden Diuretika (z. B. Amilorid, Triamteren, Spironolacton) sein.
Die Auswirkungen einer Pharmakotherapie mit Lithium auf die Nierenfunktion werden seit langem empirisch betrachtet und diskutiert [10]. In einer Untersuchung von Hestbech und Kollegen [32] zeigte sich, dass unter langjähriger Behandlung mit Lithium Nierenschädigungen in Form fokaler Atrophie und Fibrose auftraten. Bendz und Kollegen [7] konkludieren, dass schwerwiegende Nierenerkrankungen eine Folge der Langzeitbehandlung mit Lithium sein können, weshalb bei betroffenen Patienten regelmäßige Untersuchungen der Nierenfunktion durchgeführt werden sollten. Gleichwohl gibt es Hinweise darauf, dass eine Behandlung mit Lithium und Antikonvulsiva mit einem erhöhten Risiko für chronische Nierenerkrankungen, nicht aber für Nierenerkrankungen im Endstadium einhergeht [41]. Clos und Kollegen [10] hingegen fanden allgemein keine Hinweise auf die Abnahme der geschätzten glomerulären Filtrationsrate unter einer Erhaltungstherapie durch Lithium und schlussfolgern daher, dass weder Dauer der Therapie noch kumulative Dosis Bedingungsfaktoren für Nephrotoxizität darstellen.
In der Kombinationsbehandlung von Lithium und Risperidon, einer häufig angewandten Praxis in der Behandlung (schizo-)affektiver Psychosen, können neurotoxische und nephrotoxische Symptome beobachtet werden [33].
Antidementiva
Zu Donepezil gibt es keine Daten, die eine Dosisanpassung begründen würden, gleiches gilt für Rivastigmin. Für Galantamin wird bei moderater Niereninsuffizienz eine maximale Dosierung von 16 mg täglich empfohlen, bei schwerer Niereninsuffizienz sollte diese Substanz nicht eingesetzt werden. Memantin wird zwar extensiv renal eliminiert, eine Dosisreduktion auf 5 mg bis maximal 10 mg ist jedoch nur bei schwerer Niereninsuffizienz erforderlich [52].
Psychostimulanzien
Für Dexamfetamin, Atomoxetin, Methylphenidat und Modafinil ist keine Dosisanpassung erforderlich. Für Lisdexamfetamin wird als Maximaldosis bei moderater Niereninsuffizienz 50 mg/Tag, bei schwerer Niereninsuffizienz 30 mg/Tag empfohlen.
Unter einer Kombinationsbehandlung mit anticholinerg wirksamen Substanzen ergibt sich ein erhöhtes Risiko für typische unerwünschte Arzneimittelwirkungen. So kann die kombinierte Verabreichung von Thiaziden und Carbamazepin, Trizyklika, SSRI und Antipsychotika eine Hyponatriämie nach sich ziehen.
Unerwünschte renale Nebenwirkungen von Psychopharmaka
In der Behandlung mit serotonergen Pharmaka, insbesondere den serotonerg wirksamen trizyklischen Antidepressiva, SSRI, SNRI oder Carbamazepin kann es zu einem Syndrom der inadäquaten ADH-Sekretion (SIADH) kommen. Es handelt sich hierbei um eine vermehrte Sekretion von antidiuretischem Hormon (ADH) oder ADH-ähnlichen Peptiden mit der Folge einer hypotonen Hyperhydratation (gesteigerte Wasserretention) und Verdünnungshyponatriämie. Zu den Diagnosekriterien zählen neben einem Na-Wert von < 135 mmol/l eine Plasmahypoosmolalität von < 275 mOsm/kg, eine Urin-Osmolalität von > 100 mOsm/kg und ein Urin-Natrium von > 30 mmol/l.
Unter einer Kombination von Diuretika, insbesondere Thiaziden, mit SSRI ist das Risiko für das Auftreten einer Hyponatriämie nochmals erhöht [50]. Im klinischen Erscheinungsbild kann sich eine Hyponatriämie unter anderem in Form von ausgeprägter Müdigkeit und Lethargie, Stupor, Verwirrtheit, Delir, Psychose und Anfällen zeigen. Da diese Symptome, besonders wenn sie bei älteren Menschen beobachtet werden, denen eines demenziellen Syndroms ähneln, kann es zu Fehleinschätzungen mit möglicherweise irreversiblen Folgen kommen [66].
Im Gegensatz zur Diuretika-bedingten Hyponatriämie kann einzig unter Lithium im Rahmen eines nephrogenen Diabetes insipidus (NDI) auch eine Hypernatriämie auftreten. Wesentliches Merkmal des NDI ist die Unfähigkeit der Nieren, Urin zu konzentrieren. Durch den Mangel an ADH bzw. aufgrund des fehlenden Ansprechens an den entsprechenden Rezeptoren im distalen Tubulus und Sammelrohr ist die Fähigkeit der Niere zur Harnkonzentrierung vermindert (Asthenurie). ADH vermittelt den Einbau von Aquaporinen, wodurch freies Wasser rückresorbiert wird. Ist dieser Mechanismus, beispielsweise durch eine Downregulation von Aquaporin-2 durch Lithium, gestört, wird vermehrt hypotoner Harn ausgeschieden (Polyurie) und es kommt zu einem zwanghaften Durst (Polydipsie). Der ebenso nachts auftretende Harndrang (Nykturie) führt zu Schlafmangel und vermehrter Tagesmüdigkeit.
Neben der klinisch wegweisenden Polydipsie und Polyurie kann sich ein Delir-ähnliches Bild mit Verwirrtheit, kognitiver Dysfunktion, Anfällen, stuporösen Zuständen bis hin zu einem hyperosmolaren Koma manifestieren. Der NDI wird in der Regel erfolgreich mit nichtsteroidalen Antiinflammatorika, Thiaziden und insbesondere Amilorid behandelt [28]. Daher sind regelmäßige Laboruntersuchungen mit Kontrollen des Elektrolythaushalts dringend geboten.
Eine Langzeitbehandlung mit Lithium kann zu strukturellen Veränderungen der Nieren mit interstitieller Fibrose, tubulärer Atrophie und in 10 % bis 20 % der Patienten auch einer glomerulären Sklerosierung führen [8], ohne dass diese Veränderungen zwangsläufig mit einer klinisch bedeutsamen Funktionsbeeinträchtigung verbunden wären [59]. Eine Progression aus einer Beeinträchtigung der Nierenfunktion in ein dialysepflichtiges Endstadium wird – wenn überhaupt – mit sehr unterschiedlicher zeitlicher Latenz in etwa 0,2 % bis 0,7 % der Patienten beobachtet [41, 62].
Außerdem müssen physiologische Veränderungen infolge Alter, Komorbiditäten (z. B. Diabetes mellitus, Hypertonie) und eine Komedikation, beispielsweise mit nichtsteroidalen Antiinflammatorika, berücksichtigt werden. Obwohl die Lithium-Toxizität nicht obligat dosisabhängig ist, sollten im Hinblick auf die Behandlungssicherheit eine Überdosierung und Serumspiegel > 1,2 mmol/l vermieden werden, weshalb regelmäßige Kontrollen des Lithium-Spiegels erforderlich sind.
Entsprechend dem Stadium der Nierenerkrankung und der damit einhergehenden glomerulären Filtrationsrate müssen Dosisanpassungen bestimmter Medikamente, die zur Behandlung psychiatrischer Komorbiditäten eingesetzt werden, vorgenommen werden. Dies ist bei nierenabhängigen Psychopharmaka bei einer GFR unter 60 ml/min notwendig [39], wobei heuristisch eine „Zwei-Drittel-Regel“ gilt. Ab einer GFR von < 30 ml/min empfehlen die Autoren allgemein eine Halbierung der maximalen Dosis.
Unerwünschte psychische Nebenwirkungen von Substanzen zur Behandlung renaler Erkrankungen
Es gibt einige Medikamente zur Behandlung renaler Erkrankungen, die unerwünschte psychische Nebenwirkungen hervorrufen können (Tab. 2). Spasmolytika, die überwiegend anticholinerg wirken, können zu kognitiver Beeinträchtigung, Verwirrtheit, Erschöpfung und sogar psychotischen Zuständen führen. Thiazide und Thiazid-ähnliche Diuretika können eine Hyponatriämie-induzierte Lethargie, Stupor, Verwirrtheit, Psychosen, Reizbarkeit und zerebrale Anfälle verursachen. Unter der Einnahme von Alpha-1-Antagonisten leiden Patienten möglicherweise unter vermehrten Ängsten, Schlaflosigkeit und Impotenz, wobei Letztere auch unter der Einnahme von 5-Alpha-Reductase-Inhibitoren auftreten kann. Vasopressin-Antagonisten können Verwirrung und Schlaflosigkeit bei Betroffenen induzieren. Entsprechend ist eine engmaschige Überwachung der unerwünschten Arzneimittelwirkungen renal wirksamer Pharmaka unabdingbar.
Tab. 2. Psychiatrische Nebenwirkungen von Medikamenten zur Behandlung von renalen Erkrankungen [52, S. 211]
|
Medikation |
Psychiatrische unerwünschte Nebenwirkungen |
|
Spasmolytika |
|
|
Oxybutynin > Tolterodin, Solifenacin Darifenacin > Fesoterodin > Trospiumchlorid |
Kognitive Beeinträchtigung, Verwirrtheit, Erschöpfung, Psychose |
|
Thiazid und Thiazid-ähnliche Diuretika |
|
|
Bendroflumethiazid, Chlorothiazid, Chlortalidon, Hydrochlorothiazid, Indapamid |
Hyponatriämie-induzierte Lethargie, Stupor, Verwirrtheit, Psychose, Reizbarkeit, Krampfanfälle |
|
Alpha-1-Antagonisten |
|
|
Doxazosin, Tamsulosin |
Schlaflosigkeit, Impotenz (Doxazosin auch: Angst) |
|
5-Alpha-Reductase-Inhibitoren |
|
|
Dutasterid und Finasterid |
Impotenz, verringerte Libido |
|
Vasopressin-Antagonisten |
|
|
Tolvaptan |
Schlaflosigkeit |
Pharmakologische Wechselwirkungen von Psychopharmaka und Medikamenten zur Behandlung renaler Erkrankungen
Thiazide und Schleifendiuretika (Furosemid, Etacrynsäure) können schon in Monotherapie zu Elektrolytstörungen, beispielsweise einer Hyponatriämie, Hypokaliämie oder Hypomagnesiämie führen. In der Kombination mit trizyklischen Antidepressiva, Antipsychotika und Lithium kann es zu pharmakodynamischen Interaktionen kommen, die zu kardialen Arrhythmien und QTc-Verlängerung führen (Tab. 3). Eine Kombination von Antidepressiva oder Antipsychotika mit anticholinerg wirksamen Spasmolytika verstärkt die typischen Nebenwirkungen (Mundtrockenheit, Harnverhalt, Obstipation, trockene Haut und kognitive Störungen).
Tab. 3. Unerwünschte Nebenwirkungen (UAW) als Folge pharmakodynamischer und pharmakokinetischer Interaktionen nach [52, S. 215–222]
|
Medikation |
Interaktionsmechanismus |
UAW |
|
Diuretika |
||
|
Thiaziddiuretika |
Verringerte Absorption Additive Hyponatriämie Hypokaliämie/Hypomagnesiämie |
Risiko einer Lithiumintoxikation Folgen einer Hyponatriämie bei Kombination mit serotonergen Substanzen Risiko für Arrhythmien, QTc-Verlängerung, v. a. in Kombination mit trizyklischen Antidepressiva, typischen Antipsychotika, Risperidon, Paliperidon, Quetiapin, Ziprasidon, Lithium |
|
Schleifendiuretika |
Elektrolytveränderungen Hypokaliämie Hypomagnesiämie |
Folgen einer Hyponatriämie bei Kombination mit serotonergen Substanzen Risiko für Arrhythmien, QTc-Verlängerung, v. a. in Kombination mit trizyklischen Antidepressiva, typischen Antipsychotika, Risperidon, Paliperidon, Quetiapin, Ziprasidon, Lithium |
|
Carboanhydrase-Inhibitoren |
Alkalinisierung des Urins |
Reduzierte Exkretion von Amphetaminen, Amitriptylin, Imipramin, Memantin |
|
Osmotische Diuretika Spironolacton |
Erhöhte Lithium-Clearance |
Senkung des Lithiumspiegels |
|
Antidepressiva |
||
|
Fluoxetin |
Inhibition von CYP3A4 Inhibition von CYP2D6 |
Erhöhter Plasmaspiegel von Vasopressin-Antagonisten (Conivaptan, Tolvaptan) |
|
Johanniskraut (Hypericum perforatum) |
Induktion von CYP3A4 |
Senkung des Plasmaspiegels von Conivaptan und Tolvaptan |
|
Antipsychotika |
||
|
Typische und atypische Antipsychotika |
Additive, hypotensive Effekte |
Risiko von Hypotension in Kombination mit PDE5-Inhibitoren oder Alpha-1-Antagonisten |
|
Stimmungsstabilisatoren |
||
|
Carbamazepin |
Induktion von CYP3A4 |
Senkung des Plasmaspiegel von Conivaptan oder Tolvaptan |
|
Psychostimulanzien |
||
|
Modafinil |
Induktion von CYP3A4 |
Senkung des Plasmaspiegels von CYP3A4-Substraten |
|
Atomoxetin |
Inhibition von CYP2D6 |
Erhöhung des Plasmaspiegels von CYP2D6-Substraten |
Thiaziddiuretika reduzieren auch über pharmakokinetische Mechanismen die Lithium-Ausscheidung und tragen zu einem signifikanten Anstieg des Lithium-Serumspiegels bei. Schleifendiuretika hingegen erhöhen die Lithium-Ausscheidung, ebenso wie Carboanhydrase-Inhibitoren, beispielsweise Acetazolamid, oder osmotische Diuretika wie Mannitol. Sogenannte kaliumsparende Diuretika, zum Beispiel Amilorid oder Triamteren, und Aldosteron-Antagonisten, beispielsweise Spironolacton, können ebenfalls die Lithium-Ausscheidung erhöhen [19, 22].
Veränderungen im pH des Urins können ebenfalls die Elimination von Psychopharmaka beeinflussen. Thiazide und Schleifendiuretika verringern den pH des Urins und fördern darüber die Ausscheidung von Amphetaminen, Amitriptylin, Imipramin, Methadon und Memantin [24].
Fazit
Die hohe Prävalenz psychischer Störungen und kognitiver Einschränkungen bei Patienten mit Nierenerkrankungen stellt einen bedeutsamen Faktor in der Behandlungsplanung und für die Behandlungsadhärenz dar. Aufgrund der multifaktoriellen Ätiologie psychischer, psychosozialer und kognitiver Belastungen ist eine psychiatrische Mitversorgung betroffener Personen unumgänglich. Die Datenlage in Bezug auf Effektivität von Psychopharmaka bei Nieren- bzw. Dialysepatienten ist jedoch nach wie vor gering.
Bei psychopharmakologisch mitbehandelten Patienten liegen im Allgemeinen kaum Einschränkungen in der Verschreibung von Psychopharmaka vor, es empfiehlt sich die Anwendung der Zwei-Drittel-Regel bei der Dosisanpassung. Regelmäßig sollten Laborkontrollen und ein EKG durchgeführt werden, um Veränderungen im Elektrolythaushalt und QTc-Zeit-Verlängerungen zu identifizieren. Für das in der Behandlung affektiver Störungen unverzichtbare Lithium sollten zur Vermeidung bzw. Verringerung von renalen Langzeitschäden regelmäßig Spiegelkontrollen erfolgen. Gerade in der psychopharmakologischen Behandlung von Menschen mit einer psychischen Erkrankung und einer somatischen Komorbidität hat das therapeutische Drug-Monitoring (TDM) einen besonderen Stellenwert.
Interessenkonflikterklärung
TM: Honorare für die Beratung oder Teilnahme an einem Expertenbeirat von Janssen-Cilag und Otsuka/Lundbeck; Honorare für Vorträge, Stellungnahmen oder Artikel von Janssen-Cilag, Neuraxpharm und Otsuka/Lundbeck; Forschungsbeihilfe von Janssen-Cilag
ER: Keine Interessenkonflikte
Literatur
1. National Institute for Health and Care Excellence: Clinical Guidelines. Chronic kidney disease in adults: assessment and management. London: National Institute for Health and Care Excellence (UK). Copyright © NICE 2020, 2015.
2. Albers B. Weltnierentag 2019. Nierengesundheit geht uns alle an. Überall. https://www.dgfn.eu/pressemeldung/weltnierentag-2019-nierengesundheit-geht-alle-an-ueberall.html (Zugriff am 12.01.2021).
3. Angermann CE, Gelbrich G, Stork S, Gunold H, et al. Effect of escitalopram on all-cause mortality and hospitalization in patients with heart failure and depression: The MOOD-HF randomized clinical trial. JAMA 2016;315:2683–93.
4. Araujo SM, de Bruin VM, Daher Ede F, Almeida GH, et al. Risk factors for depressive symptoms in a large population on chronic hemodialysis. Int Urol Nephrol 2012;44:1229–35.
5. Artom M, Moss-Morris R, Caskey F, Chilcot J. Fatigue in advanced kidney disease. Kidney Int 2014;86:497–505.
6. Avramovic M, Stefanovic V. Health-related quality of life in different stages of renal failure. Artif Organs 2012;36:581–9.
7. Bendz H, Schon S, Attman PO, Aurell M. Renal failure occurs in chronic lithium treatment but is uncommon. Kidney Int 2010;77:219–24.
8. Bendz H, Sjodin I, Aurell M. Renal function on and off lithium in patients treated with lithium for 15 years or more. A controlled, prospective lithium-withdrawal study. Nephrol Dial Transplant 1996;11:457–60.
9. Blumenfield M, Levy NB, Spinowitz B, Charytan C, et al. Fluoxetine in depressed patients on dialysis. Int J Psychiatry Med 1997;27:71–80.
10. Clos S, Rauchhaus P, Severn A, Cochrane L, et al. Long-term effect of lithium maintenance therapy on estimated glomerular filtration rate in patients with affective disorders: a population-based cohort study. Lancet Psychiatry 2015;2:1075–83.
11. Cohen LM, Germain MJ. The psychiatric landscape of withdrawal. Semin Dial 2005;18:147–53.
12. Cohen LM, Tessier EG, Germain MJ, Levy NB. Update on psychotropic medication use in renal disease. Psychosomatics 2004;45:34–48.
13. Cohen SD, Cukor D, Kimmel PL. Anxiety in patients treated with hemodialysis. Clin J Am Soc Nephrol 2016;11:2250–5.
14. Cukor D, Coplan J, Brown C, Friedman S, et al. Anxiety disorders in adults treated by hemodialysis: a single-center study. Am J Kidney Dis 2008;52:128–36.
15. Dev V, Dixon SN, Fleet JL, Gandhi S, et al. Higher anti-depressant dose and major adverse outcomes in moderate chronic kidney disease: a retrospective population-based study. BMC Nephrol 2014;15:79.
16. Doyle GD, Laher M, Kelly JG, Byrne MM, et al. The pharmacokinetics of paroxetine in renal impairment. Acta Psychiatr Scand Suppl 1989;350:89–90.
17. Drayer RA, Piraino B, Reynolds CF, 3rd, Houck PR, et al. Characteristics of depression in hemodialysis patients: symptoms, quality of life and mortality risk. Gen Hosp Psychiatry 2006;28:306–12.
18. Elias MF, Elias PK, Seliger SL, Narsipur SS, et al. Chronic kidney disease, creatinine and cognitive functioning. Nephrol Dial Transplant 2009;24: 2446–52.
19. Eyer F, Pfab R, Felgenhauer N, Lutz J, et al. Lithium poisoning: pharmacokinetics and clearance during different therapeutic measures. J Clin Psychopharmacol 2006;26:325–30.
20. Feroze U, Martin D, Kalantar-Zadeh K, Kim JC, et al. Anxiety and depression in maintenance dialysis patients: preliminary data of a cross-sectional study and brief literature review. J Ren Nutr 2012;22:207–10.
21. Finkelstein FO, Shirani S, Wuerth D, Finkelstein SH. Therapy insight: sexual dysfunction in patients with chronic kidney disease. Nat Clin Pract Nephrol 2007;3:200–7.
22. Finley PR, Warner MD, Peabody CA. Clinical relevance of drug interactions with lithium. Clin Pharmacokinet 1995;29:172–91.
23. Finniss DG, Kaptchuk TJ, Miller F, Benedetti F. Biological, clinical, and ethical advances of placebo effects. Lancet 2010;375:686–95.
24. Freudenthaler S, Meineke I, Schreeb KH, Boakye E, et al. Influence of urine pH and urinary flow on the renal excretion of memantine. Br J Clin Pharmacol 1998;46:541–6.
25. Friedli K, Guirguis A, Almond M, Day C, et al. Sertraline versus placebo in patients with major depressive disorder undergoing hemodialysis: A randomized, controlled feasibility trial. Clin J Am Soc Nephrol 2017;12:280–6.
26. Gillman PK. Tricyclic antidepressant pharmacology and therapeutic drug interactions updated. Br J Pharmacol 2007;151:737–48.
27. Glassman AH, O’Connor CM, Califf RM, Swedberg K, et al. Sertraline treatment of major depression in patients with acute MI or unstable angina. JAMA 2002;288:701–9.
28. Grunfeld JP, Rossier BC. Lithium nephrotoxicity revisited. Nat Rev Nephrol 2009;5:270–6.
29. Hecking M, Bieber BA, Ethier J, Kautzky-Willer A, et al. Sex-specific differences in hemodialysis prevalence and practices and the male-to-female mortality rate: the Dialysis Outcomes and Practice Patterns Study (DOPPS). PLoS Med 2014;11:e1001750.
30. Hedayati SS, Finkelstein FO. Epidemiology, diagnosis, and management of depression in patients with CKD. Am J Kidney Dis 2009;54:741–52.
31. Hedayati SS, Gregg LP, Carmody T, Jain N, et al. Effect of sertraline on depressive symptoms in patients with chronic kidney disease without dialysis dependence: The CAST randomized clinical trial. JAMA 2017;318:1876–90.
32. Hestbech J, Hansen HE, Amdisen A, Olsen S. Chronic renal lesions following long-term treatment with lithium. Kidney Int 1977;12:205–13.
33. Hsu CW, Lee Y, Lee CY, Lin PY. Neurotoxicity and nephrotoxicity caused by combined use of lithium and risperidone: a case report and literature review. BMC Pharmacol Toxicol 2016;17:59.
34. Iovieno N, Papakostas GI. Correlation between different levels of placebo response rate and clinical trial outcome in major depressive disorder: a meta-analysis. J Clin Psychiatry 2012;73:1300–6.
35. IQTIG. Qualitätsreport 2019.
36. Jha V, Garcia-Garcia G, Iseki K, Li Z, et al. Chronic kidney disease: global dimension and perspectives. Lancet 2013;382:260–72.
37. Jiang Y, McCombs JS, Park SH. A retrospective cohort study of acute kidney injury risk associated with antipsychotics. CNS Drugs 2017;31:319–26.
38. Kapfhammer HP. Renale Erkrankungen. In: Möller HJ, Laux G, Kapfhammer HP (Hrsg.). Psychiatrie, Psychosomatik, Psychotherapie. 5. Auflage. Berlin, Heidelberg: Springer, 2018: 2763–7.
39. Keller F, Gahr M. Psychopharmaka und am Nervensystem wirkende Medikamente bei Patienten mit Niereninsuffizienz. Der Nephrologe 2014;9:447–51.
40. Kessing LV, Feldt-Rasmussen B, Andersen PK, Gerds TA, et al. Continuation of lithium after a diagnosis of chronic kidney disease. Acta Psychiatr Scand 2017;136:615–22.
41. Kessing LV, Gerds TA, Feldt-Rasmussen B, Andersen PK, et al. Use of lithium and anticonvulsants and the rate of chronic kidney disease: A nationwide population-based study. JAMA Psychiatry 2015;72:1182–91.
42. Kimmel PL, Peterson RA. Depression in end-stage renal disease patients treated with hemodialysis: tools, correlates, outcomes, and needs. Semin Dial 2005;18:91–7.
43. Kocheril AG. Arrhythmia issues in patients with renal disease. Semin Nephrol 2001;21:57–65.
44. Koo JR, Yoon JY, Joo MH, Lee HS, et al. Treatment of depression and effect of antidepression treatment on nutritional status in chronic hemodialysis patients. Am J Med Sci 2005;329:1–5.
45. Kostro JZ, Hellmann A, Kobiela J, Skora I, et al. Quality of life after kidney transplantation: A prospective study. Transplant Proc 2016;48:50–4.
46. Kraus D, Wanner C. [Epidemiology of chronic kidney disease – Ever more patients?]. Dtsch Med Wochenschr 2017;142:1276–81.
47. Kuhlmann SD. Der Dialyseabbruch: medizinische, ethische und juristische Aspekte. Halle-Wittenberg: Martin-Luther-Universität Halle-Wittenberg, Interdisziplinäres Zentrum, Medizin-Ethik-Recht, 2011.
48. Kurella M, Kimmel PL, Young BS, Chertow GM. Suicide in the United States end-stage renal disease program. J Am Soc Nephrol 2005;16:774–81.
49. Lee YJ, Kim MS, Cho S, Kim SR. Association of depression and anxiety with reduced quality of life in patients with predialysis chronic kidney disease. Int J Clin Pract 2013;67:363–8.
50. Letmaier M, Painold A, Holl AK, Vergin H, et al. Hyponatraemia during psychopharmacological treatment: results of a drug surveillance programme. Int J Neuropsychopharmacol 2012;15:739–48.
51. Levenson JL, Ferrando SJ. Clinical Manual of Psychopharmacology in the Medically Ill. Arlington: American Psychiatric Association, 2017.
52. Levenson JL, Owen JA. Renal and Urological Disorders. In: Levenson JL, Ferrando SJ (Hrsg.). Clinical Manual of Psychopharmacology in the Medically Ill. 2. Auflage. Arlington, Virginia: American Psychiatric Association Publishing, 2017:195–231.
53. Levy NB. Psychological problems of the patient on hemodialysis and their treatment. Psychother Psychosom 1979;31:260–6.
54. MacLaughlin HL, Hall WL, Sanders TA, Macdougall IC. Risk for chronic kidney disease increases with obesity: Health survey for England 2010. Public Health Nutr 2015;18:3349–54.
55. McIntyre CW, Goldsmith DJ. Ischemic brain injury in hemodialysis patients: which is more dangerous, hypertension or intradialytic hypotension? Kidney Int 2015;87:1109–15.
56. Nagler EV, Webster AC, Vanholder R, Zoccali C. Antidepressants for depression in stage 3–5 chronic kidney disease: a systematic review of pharmacokinetics, efficacy and safety with recommendations by European Renal Best Practice (ERBP). Nephrol Dial Transplant 2012;27:3736–45.
57. Palmer S, Vecchio M, Craig JC, Tonelli M, et al. Prevalence of depression in chronic kidney disease: systematic review and meta-analysis of observational studies. Kidney Int 2013;84:179–91.
58. Palmer SC, Natale P, Ruospo M, Saglimbene VM, et al. Antidepressants for treating depression in adults with end-stage kidney disease treated with dialysis. Cochrane Database Syst Rev 2016:CD004541.
59. Paul R, Minay J, Cardwell C, Fogarty D, et al. Meta-analysis of the effects of lithium usage on serum creatinine levels. J Psychopharmacol 2010;24:1425–31.
60. Pichette V, Leblond FA. Drug metabolism in chronic renal failure. Curr Drug Metab 2003;4:91–103.
61. Pompili M, Venturini P, Montebovi F, Forte A, et al. Suicide risk in dialysis: review of current literature. Int J Psychiatry Med 2013;46:85–108.
62. Presne C, Fakhouri F, Noel LH, Stengel B, et al. Lithium-induced nephropathy: Rate of progression and prognostic factors. Kidney Int 2003;64:585–92.
63. Reimer J, Franke GH, Lutkes P, Kohnle M, et al. [Quality of life in patients before and after kidney transplantation]. Psychother Psychosom Med Psychol 2002;52:16–23.
64. Soni RK, Weisbord SD, Unruh ML. Health-related quality of life outcomes in chronic kidney disease. Curr Opin Nephrol Hypertens 2010;19:153–9.
65. Spigset O, Hagg S, Stegmayr B, Dahlqvist R. Citalopram pharmacokinetics in patients with chronic renal failure and the effect of haemodialysis. Eur J Clin Pharmacol 2000;56:699–703.
66. Stiefelhagen P. Hyponatriämie: Diagnostik und Therapie sind komplex. InFo Neurologie & Psychiatrie 2018;50:20; https://doi.org/10.1007/s15005-018-2521-1.
67. Szeifert L, Molnar MZ, Ambrus C, Koczy AB, et al. Symptoms of depression in kidney transplant recipients: a cross-sectional study. Am J Kidney Dis 2010;55:132–40.
68. Troy SM, Schultz RW, Parker VD, Chiang ST, et al. The effect of renal disease on the disposition of venlafaxine. Clin Pharmacol Ther 1994;56:14–21.
69. Turpeinen M, Koivuviita N, Tolonen A, Reponen P, et al. Effect of renal impairment on the pharmacokinetics of bupropion and its metabolites. Br J Clin Pharmacol 2007;64:165–73.
70. Vermeir M, Naessens I, Remmerie B, Mannens G, et al. Absorption, metabolism, and excretion of paliperidone, a new monoaminergic antagonist, in humans. Drug Metab Dispos 2008;36:769–79.
71. Webster AC, Nagler EV, Morton RL, Masson P. Chronic kidney disease. Lancet 2017;389:1238–52.
72. Weckmann G, Chenot J, Stracke S. Versorgung von Patienten mit chronischer nichtdialysepflichtiger Nierenerkrankung in der Hausarztpraxis. Dtsch Ärztebl 2020;177:745–51.
73. Yamamoto Y, Usui N, Nishida T, Mori M, et al. Influence of renal function on pharmacokinetics of antiepileptic drugs metabolized by CYP3A4 in a patient with renal impairment. Ther Drug Monit 2018;40:144–7.
Prof. Dr. Thomas Messer, Eva Reil, Danuviusklinik Pfaffenhofen, Krankenhausstraße 68, 85276 Pfaffenhofen an der Ilm, E-Mail: thomas.messer@danuviusklinik.de
Psychopharmacotherapy in patients with renal disease
Chronic renal insufficiency affects around 11 % of the German population, the risk of the disease is increasing dramatically with age. Kidney disease and the need for dialysis can have a significant impact on psychological well-being, with depression and anxiety disorders in particular affecting the individual's quality of life. If psychopharmacotherapy is considered as indicated due to the severity of the psychiatric symptoms, a dose adjustment is necessary when prescribing substances that are mainly eliminated by the kidneys. On the other hand, undesirable side effects of individual psychotropic drugs on kidney function should also be known in order to prevent damage. After all, safe and tolerable pharmacotherapy requires knowledge of drug-drug-interaction risks when psychotropic drugs are combined with drugs for the treatment of renal diseases.
Key words: Psychopharmacotherapy, renal insufficiency, drug-drug interactions
Psychopharmakotherapie 2021; 28(01):21-30
