Heinz Grunze, Weinsberg/Schwäbisch Hall/PMU Nürnberg, Emanuel Severus, Dresden, Gerd Laux, Soyen/Waldkraiburg/München, und Walter E. Müller, Worms/Frankfurt a. M.
Teil 12-I dieses Weiterbildungs-Curriculums behandelte Stimmungsstabilisierer aus der Gruppe der Antiepileptika und atypischen Antipsychotika. Dieses Kapitel nun ist Lithium gewidmet. Lithium nimmt unter den Stimmungsstabilisierern eine gewisse Sonderstellung ein, da es über viele Jahrzehnte etabliert ist und bezüglich seiner Wirksamkeit bei bipolaren Erkrankungen als Goldstandard angesehen werden kann.
Lithium zählt zu den Alkalimetallen wie Natrium und Kalium, in Form seiner Salze kommt es überall in der Natur vor und ist auch Bestandteil des menschlichen Körpers in sehr niedrigen Konzentrationen. Im hier diskutierten therapeutischen Zusammenhang sind mit „Lithium“ stets Lithiumsalze oder -ionen gemeint.
Die Geschichte der Lithium-Behandlung speziell von affektiven Störungen geht in das 19. Jahrhundert zurück: Die dänischen Neurologen und Psychiater Frederick und Carl Lange beschrieben 1886 die Wirksamkeit von Lithium als Vorbeugung bei rezidivierenden Depressionen. Quasi wiederentdeckt wurde es 1949 in Australien durch John Cade, der die antimanische Wirksamkeit von Lithium zunächst im Tierversuch an Nagern und anschließend an Patienten beschrieb. Die systematische Forschung zu Lithium ist hauptsächlich ein Verdienst zweier dänischer Psychiater, Mogens Schou und Poul Baastrup, die die prophylaktische Wirksamkeit sowohl bei bipolaren Störungen als auch rezidivierenden Depressionen beschrieben. Etabliert hat sich die International Group for The Study of Lithium Treated Patients (IGSLI, https://www.igsli.org/).
Wirkungsmechanismus
Der Wirkungsmechanismus von Lithium ist bis heute noch nicht final geklärt und auf alle Fälle komplex, beginnend mit Wirkungen auf die neuronale Erregbarkeit bis zu Effekten auf die gestörte Neuroplastizität als möglicher gemeinsamer Nenner aller Stimmungsstabilisierer.
Lithium kann die Empfindlichkeit verschiedener Rezeptoren bidirektional beeinflussen, von besonderer Bedeutung sind die Effekte auf die interzelluläre Signalweiterleitung. Lithium hemmt die Aktivität der Adenylatcyclase und der Guanylatcyclase als Schlüsselenzyme der intrazellulären Signaltransduktion. Die intrazelluläre Erregungsweiterleitung wird durch eine Hemmung der Inositol-1-Phosphatase nachhaltig reduziert. Eine heute favorisierte Hypothese der prophylaktischen Wirksamkeit geht auf die Hemmwirkung der Glykogen-Synthase-Kinase 3 (GSK-3) zurück, wodurch die Bildung neurotropher Faktoren wie des Transkriptionsfaktors CREB oder des Neurotrophins BDNF, aber auch des antiapoptotischen Faktors Bcl-2 erhöht wird (Abb. 1). Als wichtigste Zielorganelle hat man die Mitochondrien identifiziert, sodass eine Mitochondrien-schützende bzw. die mitochondriale Funktion verbessernde Wirkung anzunehmen ist. Mitochondriale Funktionsstörungen werden auch als für bipolare Erkrankungen bedeutsam angesehen.
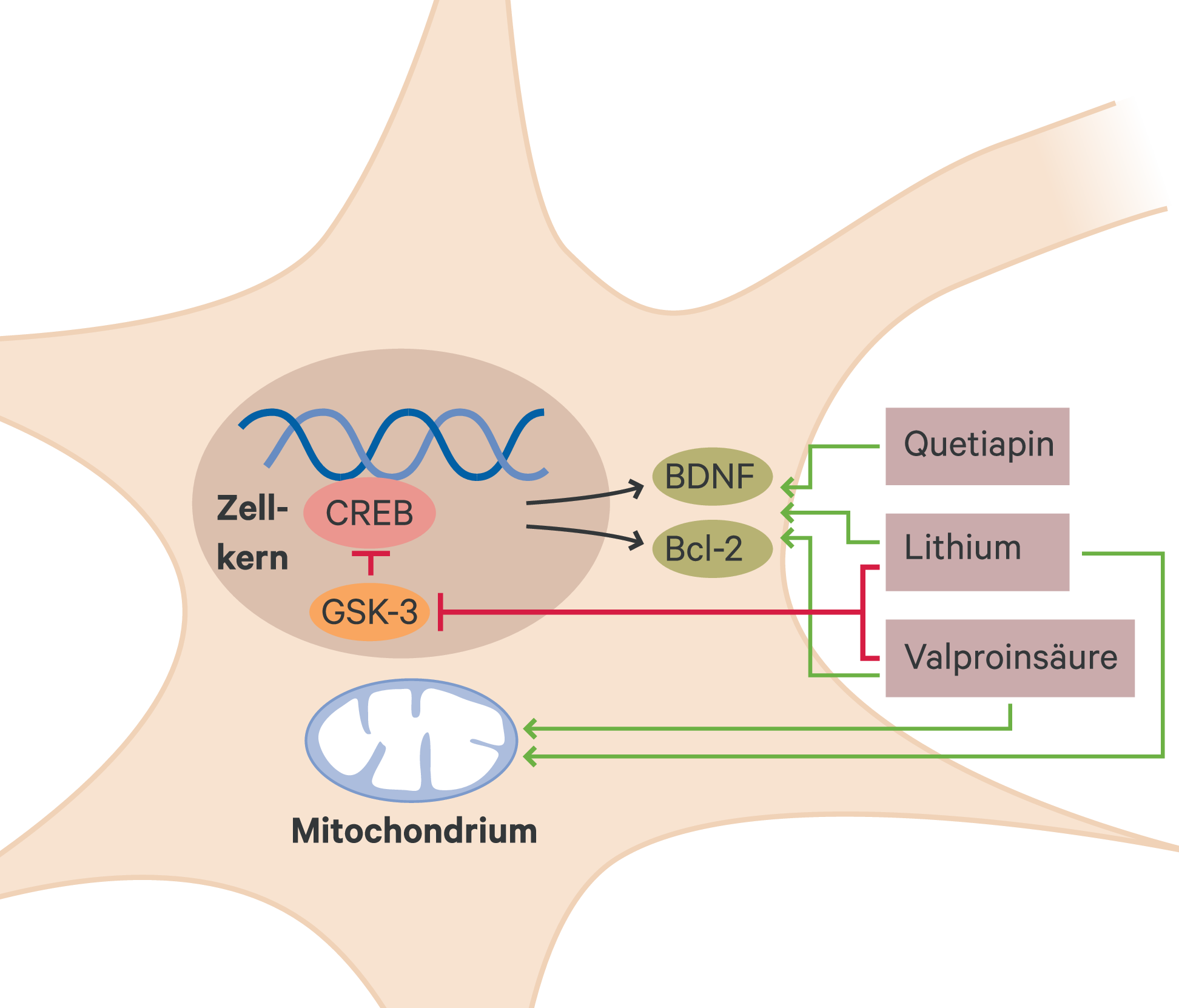
Abb. 1. Schematische Darstellung über die pharmakologische Beeinflussung von Neuroplastizität und mitochondrialer Dysfunktion als eine mögliche gemeinsame Endstrecke im biochemischen Wirkungsprofil von Stimmungsstabilisatoren [nach Müller WE und Müller JK, Med Monatsschr Pharm 2016;39:371–6]; Bcl-2: „B-cell lymphoma“, ein antiapoptotischer Faktor; BDNF: brain-derived neurotrophic factor; CREB: cAMP response element-binding protein, ein Transkriptionsfaktor; GSK-3: Glykogen-Synthase-Kinase 3
Der neuroprotektive Effekt von Lithium ist mittlerweile in vitro, in vivo und auch am Patienten beschrieben. MRI-Untersuchungen zeigen signifikant weniger Verlust grauer Hirnsubstanz, insbesondere im limbisch-kortikalen Bereich, bei bipolaren Patienten unter Lithium-Therapie im Vergleich zu nicht- oder anderweitig behandelten Patienten [10, 21].
Pharmakokinetik
Lithium wird nach oraler Einnahme relativ langsam (tmax 4 bis 5 Stunden), aber trotzdem vollständig resorbiert. Durch eine Einnahme der heute üblichen retardierten Tabletten wird die Zeit bis tmax noch einmal verlängert, um die Spitzen-Serumspiegel zu reduzieren. Die Eliminationshalbwertzeit t1/2 liegt bei 14 bis 30 Stunden. Aufgrund der hohen konzentrationsabhängigen Toxizität von Lithium spielt eine exakte Einhaltung des relativ engen therapeutischen Serumspiegelfensters eine große Rolle. Erhöhte Lithium-Serumspiegel können aus Störungen des Elektrolyt- und Wasserhaushalts resultieren, die Lithium-Ausscheidung ist bei Hyponatriämie (Dehydratation, Ödeme, Behandlung mit Thiazid-Diuretika) verringert. Angiotensin-converting-Enzym(ACE)-Inhibitoren sowie nichtsteroidale antiinflammatorische Arzneistoffe (NSAR) können den Lithium-Spiegel deutlich erhöhen. Wird eine Gabe dieser Medikamente erforderlich, ist die Lithium-Dosis entsprechend anzupassen, daher ist es wichtig, dass der Patient alle behandelnden Ärzte über die Lithium-Einnahme informiert (Lithium-Pass, zu beziehen beispielsweise über https://dgbs.de/fileadmin/cust/dgbs-materialien/DGBS-Lithiumpass-web02.pdf).
Klinische Anwendung (Tab. 1)
Tab. 1. Indikationsstellung einer Lithium-Prophylaxe (ergänzt und modifiziert nach Angst J, Bibl Psychiatr 1981:32–44)
|
Bipolare Störung |
Rezidivierende unipolare manische Episoden |
Unipolare Depression |
Schizoaffektive Störung |
|
≥ 2 Episoden in 4 Jahren oder ab der ersten manischen Episode bei entsprechender Schwere |
Ab der ersten manischen Episode bei entsprechender Schwere, sonst ab der zweiten Episode |
≥ 2 Episoden in 5 Jahren |
≥ 2 Episoden in 3 Jahren |
|
Für alle: |
|||
Bipolare Störung
Manische Episode
Die antimanische Wirksamkeit von Lithium ist seit Langem gut etabliert und wurde jüngst durch ein Cochrane-Metaanalyse noch einmal bestätigt [13].
Bipolare Depression
Die bisher größte und aussagekräftigste Studie mit einem doppelblinden Studiendesign konnte für Lithium in keinem depressionsbezogenen Zielparameter Überlegenheit gegenüber Placebo zeigen, ganz im Unterschied zu dem Atypikum Quetiapin, das Placebo in allen Zielparametern signifikant überlegen war [25]. Wenn jedoch unter einer bestehenden Lithium-Prophylaxe eine depressive Episode auftritt, insbesondere nach Dosisreduktion/Spiegelerniedrigung, sollte man den Lithium-Serumspiegel zunächst wieder auf 0,6 bis 0,8 mmol/l anheben. Diese Maßnahme kann für sich allein bereits zu einer Remission der depressiven Symptomatik führen [9].
Erhaltungstherapie und Prophylaxe
Die prophylaktische Wirksamkeit von Lithium ist schon seit über fünf Jahrzehnten bekannt. Insgesamt sind die Studienergebnisse bei Lithium-Langzeittherapie bezüglich der Manieprophylaxe relativ einheitlich und positiv, hinsichtlich der Verhütung neuer Depressionen kommen sie aber zu zum Teil unterschiedlichen Ergebnissen. Miura und Mitarbeiter fanden in einer Netzwerk-Metaanalyse, dass Lithium besser als Placebo in der Prävention manischer wie auch depressiver Episoden war [15]. Eine weitere Metaanalyse zeigte ebenfalls den rezidivprophylaktischen Effekt von Lithium für Manie und Episoden jeglicher Polarität, verfehlte Signifikanz für depressive Rezidive aber knapp [19]. Auch ein Review neuerer Studien von 2014 bis 2018 bestätigte die Ergebnisse der beiden Metaanalysen [18]. Die Studienlage für randomisierte, kontrollierte Vergleichsstudien ist deutlich dünner. Die < BALANCE> -Studie zeigte die Überlegenheit von Lithium gegenüber Valproinsäure in der Rezidivprophylaxe über einen Zeitraum von bis zu zwei Jahren. Im Vergleich zur Prophylaxe mit verschiedenen stimmungsstabilisierenden Antiepileptika schnitt Lithium in der Metaanalyse von Severus et al. (2014) hinsichtlich der Verhütung neuer Manie besser ab, keine signifikanten Unterschiede fanden sich jedoch hinsichtlich Depressionsverhütung, Prophylaxe gegenüber Episoden jeglicher Polarität und Abbruchraten [19].
Zur Frage, ob Unterschiede im Ansprechen auf Lithium zwischen Bipolar-I- und -II-Patienten bestehen, gibt es gegensätzliche Meinungen. Naturalistische Studienergebnisse sehen durchaus einen Nutzen der Lithium-Therapie bei Bipolar-II-Störungen.
Inwieweit bei einem Wiederansetzen von Lithium nach zwischenzeitlichem Pausieren ein Wirkverlust auftritt, wird weiter kontrovers beurteilt [6]. Da das Risiko eines Rückfalls unmittelbar nach einer Index-Episode am größten ist, ist es wichtig, dass ein prophylaktisch gegebenes Medikament eine relativ schnelle Wirksamkeit zeigt. Drei Studien, die in einer Metaanalyse zusammengefasst wurden [22], konnten zeigen, dass sich bereits innerhalb der ersten zwei Wochen der Behandlung eine rückfallprophylaktische Wirksamkeit zeigen kann. Dies scheint jedoch primär für manische Rückfälle zu gelten, Wirksamkeit gegen depressive Episoden scheint erst im weiteren Verlauf der Behandlung einzutreten.
Mindestens 15 bis 20 % aller Patienten mit bipolaren Störungen erleiden mindestens vier Krankheitsepisoden in einem Jahr (Rapid-Cycling, RC). Hier scheint Lithium weniger wirksam zu sein. Eine relativ schlechtere Wirksamkeit bei Patienten mit häufigen Episoden ist aber kein Lithium-spezifisches Phänomen, sondern tritt, wenn vielleicht auch in unterschiedlicher Ausprägung, ebenso mit anderen Medikamenten auf. In Ermangelung wirklich überzeugender Alternativen ist also ein RC-Verlauf kein Ausschlusskriterium einer Lithium-Therapie.
Schizoaffektive Störung
Insgesamt ist die Evidenz für eine leitliniengerechte Behandlung schizoaffektiver Störungen für alle Medikamente gering; in Deutschland haben nur Ziprasidon und Paliperidon eine explizite arzneimittelrechtliche Zulassung.
Unipolare Depression
Lithium-Monotherapie
Die Evidenzlage für Lithium als Monotherapie der akuten unipolaren Depression ist eher gering. Aktuelle Guidelines empfehlen daher Lithium nicht als Monotherapie der unipolaren Depression, sondern primär als Augmentationstherapie [3].
Augmentation bei Therapieresistenz
Zahlreiche offene, kontrollierte, randomisierte Studien und Metaanalysen kommen zu dem Schluss, dass Lithium-Augmentation sowohl bei Therapieresistenz gegenüber klassischen Trizyklika als auch gegenüber selektiven Serotonin-Wiederaufnahmehemmern (SSRI) wirksam ist. Empfohlen wird, einen Lithium-Spiegel im Bereich zwischen 0,6 und 0,9 mmol/l anzustreben. Zeigt sich innerhalb von zwei Wochen kein Hinweis auf Besserung bei suffizienter Lithium-Konzentration, so sollte Lithium wieder abgesetzt werden und es sollten Alternativen wie atypische Antipsychotika oder Schilddrüsenhormone ausprobiert werden [2]. Bei einer Besserung sollte jedoch die Zwei-Zügel-Therapie in jedem Fall für 6 bis 12 Monate fortgesetzt werden. Eine große Metaanalyse von Zhou und Mitarbeitern [26], die die Effektivität von insgesamt elf Substanzen als Augmentationstherapie zu Antidepressiva verglich, zeigte keinen signifikanten Wirksamkeitsunterschied der unterschiedlichen Strategien, einschließlich der Lithium-Augmentation. Sowohl Quetiapin, Aripiprazol, Schilddrüsenhormon als auch Lithium waren signifikant wirksamer als Placebo.
Erhaltungstherapie und Prophylaxe
Hinsichtlich der Prophylaxe bestätigen mehrere Metaanalysen den Nutzen einer Lithium-Langzeittherapie. Zum einen ist Lithium vergleichbar effektiv wie Antidepressiva in der Prophylaxe unipolarer Depressionen, des Weiteren hat es einen deutlichen antisuizidalen Effekt [5] und führt zu einer Verringerung der Gesamtmortalität, unabhängig von der Ursache.
Die Empfehlung lautet, eine Lithium-Prophylaxe spätestens nach zwei Episoden einer wiederkehrenden Depression innerhalb von fünf Jahren zu beginnen. Als therapeutisch wirksame Lithium-Spiegel in der Langzeittherapie werden 0,6 bis 0,8 mmol/l empfohlen. Die Chance eines Ansprechens auf Lithium-Prophylaxe scheint bei bestimmten Gruppen unipolar depressiver Patienten höher als bei anderen zu sein, nämlich bei Patienten mit dem endogenen Subtyp einer unipolaren Depression, psychotischen Merkmalen sowie Patienten, die Symptome einer bipolaren Spektrumstörung oder eine entsprechende Familienanamnese vorweisen.
Spezielle Patientengruppen
Indikatoren für eine Lithium-Response
Erfahrungswerte der letzten Jahrzehnte zeigen, dass bei bipolaren Patienten etwa zwei Drittel auf eine Lithium-Prophylaxe ansprechen und davon etwa die Hälfte völlige Symptomfreiheit erlangt. Genom-weite Assoziationsstudien (GWAS) haben verschiedene Gene mit einer Lithium-Response in Verbindung gebracht, von einer Art „Lithium-Response-Chip“ als genetischem Schnelltest sind wir aber noch weit entfernt. Vor allem der bisherige Krankheitsverlauf kann wertvolle Hinweise auf eine mögliche Lithium-Response liefern: Indexepisode Manie und nachfolgende manische Polarität bzw. ein Episodenmuster Manie – Depression – Euthymie, keine psychotischen Symptome, späterer Erkrankungsbeginn und kürzere Erkrankungsdauer vor Beginn der Lithium-Prophylaxe, positive Familienanamnese für bipolare Störungen. Zusätzlich werden als positive Prädiktoren das Fehlen psychiatrischer Komorbiditäten, klar abgrenzbare Episoden mit vollständiger Remission, kein Rapid-Cycling-Verlauf sowie eine Familienanamnese einer guten Lithium-Response genannt. Ob dies nun alles Lithium-spezifische Charakteristika sind oder generell Indikatoren für ein besseres Ansprechen auf medikamentöse Prophylaxe, sei dahingestellt. Komorbide Suchterkrankung und gehäufte Mischzustände sollen ungünstig für das Ansprechen auf eine Lithium-Prophylaxe sein [23].
Kinder-und Jugendliche
Eine Lithium-Therapie der akuten Manie scheint auch bei Kindern und Jugendlichen eine vergleichbare Wirksamkeit wie bei Erwachsenen zu haben, wobei mit dem Alter der Patienten auch die Ansprechrate stieg. Bei gleichzeitiger Aufmerksamkeitsdefizit-/Hyperaktivitätsstörung (ADHS) hingegen war die Wirksamkeit von Lithium schlechter [1]. In dieser Altersgruppe mutet die Symptomatik oft diffuser an, Fehldiagnosen wie ADHS sind häufiger und generell erschweren Mischzustände und psychotische Symptome die Behandlung.
Alterspatienten
Bipolare Störungen mit Beginn im Alter (Old age bipolar disorder, OABD) machen bereits 25 % aller bipolaren Störungen aus und werden bis 2030 auf 50 % steigen. In der OABD-Gruppe sind vollständige Remissionen seltener, residuale kognitive Defizite häufiger als bei früherem Erkrankungsbeginn. OABD stellt einen Risikofaktor einer späteren Demenzentwicklung dar. In diesem Zusammenhang sei das mögliche Potenzial von Lithium bei neurodegenerativen Erkrankungen einschließlich Demenz erwähnt [11]. Erste Studien berichten eine Reduktion des Demenzrisikos bei Lithium-behandelten vs. Nicht-Lithium-behandelten OABD-Patienten.
Die Expertenempfehlung der ISBD lautet, Lithium als Mittel der ersten Wahl in der Prophylaxe älterer bipolarer Patienten einzusetzen, vorausgesetzt Nieren- und Schilddrüsenfunktion lassen es zu. Für die Altersgruppe 60 bis 79 Jahre werden Serumspiegel von 0,4 bis 0,8 mmol/l empfohlen, ab dem 80. Lebensjahr dann 0,4 bis 0,7 mmol/l [20].
Schwangerschaft und Stillzeit
Schwangerschaft per se stellt kein erhöhtes Risiko eines Rückfalls bei einer bipolaren Erkrankung dar, wohingegen das Absetzen von Lithium in der Schwangerschaft natürlich zu einem erhöhten Rückfallrisiko führt. Im Einzelfall ist eine sorgfältige Nutzen-Risiko-Abwägung zu treffen. Hinsichtlich des Risikos der Lithium-Behandlung in der Schwangerschaft gibt es unterschiedliche Einschätzungen; eine jüngst publizierte Metaanalyse [8] schloss 29 Studien ein: Im Vergleich zu Schwangerschaften ohne Lithium-Exposition zeigten Schwangerschaften mit Lithium-Exposition eine signifikant erhöhte Rate an Missbildungen, insbesondere bei Expositionen im ersten Trimester, und insbesondere für Herzmissbildungen. Nach dem ersten Trimester war die Rate an Spontanaborten und Herzmissbildungen jedoch nicht erhöht, ebenso wenig das Risiko für Frühgeburten oder zu geringes Geburtsgewicht. Bezüglich kardialer Fehlbildung bleibt zudem festzustellen, dass eine signifikant höhere Rate zwar im Vergleich zur Gesamtbevölkerung bestand, jedoch nicht im Vergleich zu anderen Schwangerschaften von Patientinnen mit affektiven Störungen ohne Lithium-Einnahme, die Erkrankung also offenbar per se einen Beitrag leistet. Zudem ist das absolute Risiko als eher gering einzustufen, insbesondere bei Betrachtung prospektiver Studien. Weiterhin konnte die Metaanalyse zeigen, dass eine Fortführung der Lithium-Behandlung bezüglich des Auftretens von postpartalen affektiven Psychosen einen deutlichen Vorteil (Number needed to treat, NNT = 3) gegenüber dem Aussetzen einer Lithium-Behandlung zeigte. Basierend auf dieser Metaanalyse wird eine Fortführung der Lithium-Behandlung mit einem optimalen Lithium-Spiegel von 0,64 mmol/l beziehungsweise eine Tagesdosis von 600 mg empfohlen. Dadurch lässt sich offensichtlich das Risiko kardialer Malformationen minimieren sowie das sogenannte Floppy-Infant-Syndrom (apathische Babys mit geringem Muskeltonus, Hypothermie, insuffizienter Atmung, Zyanose, Arrhythmie und vermindertem Saugreflex) vermeiden.
Hinsichtlich des Stillens unter Lithium-Therapie gibt es wenig zuverlässige Daten, aus diesem Grunde raten Guidelines primär vom Stillen ab. Dennoch ist die Lithium-Einnahme keine absolute Kontraindikation für das Stillen und kann in manchen Fällen auch nützlich sein.
Suizidalität
Von allen psychischen Erkrankungen sind bipolare Störungen mit dem höchsten Suizidrisiko ausgestattet, etwa ein Drittel bis die Hälfte der bipolaren Patienten begeht mindestens einen Suizidversuch während ihres Lebens und ungefähr 15 bis 20 % versterben am Suizid [14].
Die antisuizidale Wirksamkeit von Lithium ist deutlich belegt, sowohl in epidemiologischen Untersuchungen als auch kontrollierten Studien. Es wird eine fünf- bis sechsfache Verringerung der Anzahl suizidaler Akte berichtet. Abruptes Absetzen einer Lithium-Prophylaxe kann allerdings zu einer ausgeprägten „Rebound“-Suizidalität mit bis zu 13-fach erhöhter Mortalität führen, weswegen die Therapiezuverlässigkeit ganz entscheidend ist.
Unerwünschte Wirkungen und Gegenanzeigen
Kontraindikationen für eine Lithium-Therapie sind akutes Nierenversagen, ausgeprägte Hyponatriämie und akuter Herzinfarkt. Relative Kontraindikationen stellen eine leichte bis mäßige Niereninsuffizienz, eine Psoriasis, Morbus Addison sowie bestehende Schwangerschaft dar. Ein vorbestehender Hypothyreoidismus ist nicht eine primäre Kontraindikation, sollte aber durch Levothyroxin-Therapie ausgeglichen werden.
Subjektiv belastende, aber nicht schwerwiegende Nebenwirkungen einer Lithium-Therapie sind nicht selten [4]. Häufige dosisabhängige, und auch bei Lithium-Spiegeln im therapeutischen Bereich auftretende Nebenwirkungen sind Tremor, Polyurie bei gesteigerter Trinkmenge (Polydipsie), Diarrhö, Gewichtszunahme, und, häufiger bei Frauen, Hypothyreoidismus und Ausbildung eines Kropfes. Der Tremor ist typischerweise hochfrequent und feinschlägig, normalerweise nur von leichter Ausprägung, kann jedoch in Einzelfällen Verrichtungen des täglichen Lebens erheblich beeinträchtigen. Eine Gewichtszunahme tritt typischerweise zu Beginn der Lithium-Therapie auf und ist zumindest teilweise auch auf anfängliche Flüssigkeitsretention zurückzuführen. Eine Metaanalyse ergab, dass die Lithium-Patienten ein etwa 1,9-fach erhöhtes Risiko einer klinisch bedeutsamen (> 7 % des Ausganggewichts) Gewichtszunahme im Vergleich zur Placebo-Behandlung aufweisen [12]. Im Regelfall hat die Gewichtszunahme aber nicht das Ausmaß, wie es beispielsweise bei einigen atypischen Antipsychotika oder bei Valproinsäure beobachtet wird. Bis auf Hypothyreoidismus und Kropfbildung sind die genannten Nebenwirkungen zumeist nur passager und unter Reduktion der Lithium-Dosis, sofern therapeutisch verantwortbar, reversibel. Lithium-induzierter Tremor spricht gut auf Betablocker an, Polydipsie und Gewichtszunahme bedürfen hingegen der Verhaltensmodifikation (Kontrolle der Trinkmenge, kalorienreduzierte Kost, sportliche Betätigung).
Eine funktionelle Einschränkung oder Organschädigung unter langfristiger Lithium-Therapie kann die Schilddrüse, die Nebenschilddrüsen, seltener das Herz, aber insbesondere die Nieren betreffen.
Die thyreostatische Wirkung von Lithium ist gut bekannt. Lithium blockiert die Iodid-Aufnahme in die Schilddrüse, die Kopplung von Mono- und Diiodtyrosin zu T3 (Triiodthyronin) und T4 (Thyroxin) und die Freisetzung (Proteolyse) von T3 und T4 aus Thyreoglobulin. Die Schilddrüsensuppression stellt im klinischen Alltag in aller Regel keinen Grund für die Beendigung einer Lithium-Therapie dar. Eine Lithium-induzierte Hypothyreose tritt in etwa 20 bis 30 % der Lithium-behandelten Patienten, häufiger bei Frauen, auf und ist nach Absetzen von Lithium in fast allen Fällen reversibel. Durch die frühzeitige Gabe von Levothyroxin kann die Ausbildung eines Kropfes verhindert werden. Eine Lithium-induzierte Hyperthyreose und Thyreotoxikose wird als gelegentliche Nebenwirkung (etwa 1 %) beobachtet.
Die Prävalenz einer Hyperparathyreoidose mit konsekutiver Hyperkalzämie ist bei Patienten nach über 15 Jahren Lithium-Therapie etwa 7,5 % höher als in der Gesamtbevölkerung. Hyperparathyreoidismus führt in bis zu 50 % der Fälle zu einer generellen Hyperplasie mit Bildung einzelner Adenome, die zumeist chirurgisch angegangen werden müssen.
Der mit Abstand häufigste Grund, eine Lithium-Therapie nicht zu beginnen bzw. eine bestehende Therapie infrage zu stellen, ist die Auswirkung von Lithium auf die Nierenfunktion. Renale Nebenwirkungen einer Lithium-Therapie kommen häufig vor [4]. Unklar bleibt der Zusammenhang von Lithium und der Entwicklung einer chronischen Nephropathie (Chronic kidney disease, CKD) mit strukturellen Veränderungen, die schließlich in einigen Fällen zu einem Nierenversagen führen können. Hier wird das Risiko eines Nierenversagens auf etwa 0,5 % (zum Vergleich: 0,2 % in der Normalbevölkerung) bei Patienten mit Lithium-Therapie eingeschätzt [12]. Geschätzt wird weiter, dass etwa die Hälfte der Lithium-Patienten im Verlauf von 20 Jahren Lithium-Einnahme eine moderate Nierenfunktionseinschränkung mit einer geschätzten glomerulären Filtrationsrate (eGFR) < 60 ml/min/1,73 m² entwickeln. Überwiegender Konsens der Studien und Reviews der letzten Jahre ist jedoch, dass insgesamt der therapeutische Nutzen einer Lithium-Therapie gegenüber dem Risiko einer CKD im Endstadium deutlich überwiegt.
Für eine ausführlichere Anleitung, wie bei eingeschränkter Nierenfunktion eine Lithium-Therapie möglich ist, sei daher auf einschlägige Übersichtsarbeiten (z. B. [17]) verwiesen.
Lithium ist im Regelfall kardial gut verträglich (Ausschlussindikation akuter Myokardinfarkt), kann aber in Einzelfällen zu einer kritischen Verlängerung des QTc-Intervalls führen.
Eine Lithium-Intoxikation kann akut auftreten, beispielsweise bei Überdosierung in suizidaler Absicht, oder sich chronisch-schleichend entwickeln. Zeichen einer Lithium-Intoxikation, die zu einem sofortigen Pausieren der Lithium-Einnahme und gegebenenfalls zu weiteren Maßnahmen (z. B. Magenspülung, Hämodialyse und gleichzeitiger Ausgleich der Dehydration und Hyponatriämie) führen müssen, sind: Apathie und psychomotorische Verlangsamung bis zur Somnolenz, verschiedenste Kleinhirnzeichen (verwaschene Sprache, Ataxie, Nystagmus, Dysdiadochokinese, verstärkter Tremor) und gastrointestinale und vegetative Symptome wie Übelkeit, Erbrechen, Inappetenz und Durchfall (Abb. 2). Diese Symptome sind zumeist erst ab einem Lithium-Spiegel von > 1,5 mmol/l zu beobachten und entstehen bei Überdosierung oder Natrium-Mangelzuständen, beispielsweise durch vermehrtes Schwitzen, Infektionserkrankungen (insbesondere mit Erbrechen oder Diarrhö) oder Gabe von Schleifendiuretika oder Thiaziden, sowie bei Nierenfunktionsstörungen. Bei weiter ansteigenden Lithium-Konzentrationen können zusätzlich Krampfanfälle, Herzrhythmusstörungen wie bereits beschrieben, sowie zunehmende Bewusstseinseintrübungen bis hin zum Koma und schließlich Tod eintreten. Eine intensivmedizinische Überwachung ist daher bei entsprechender klinischer Symptomatik, sowie in jedem Fall bei Lithium-Spiegeln über 2 mmol/l erforderlich. Hämodialyse sollte ab Spiegeln > 2,5 mmol/l bei entsprechenden Intoxikationssymptomen erwogen und bei Spiegeln > 4 mmol/l in jedem Fall durchgeführt werden.
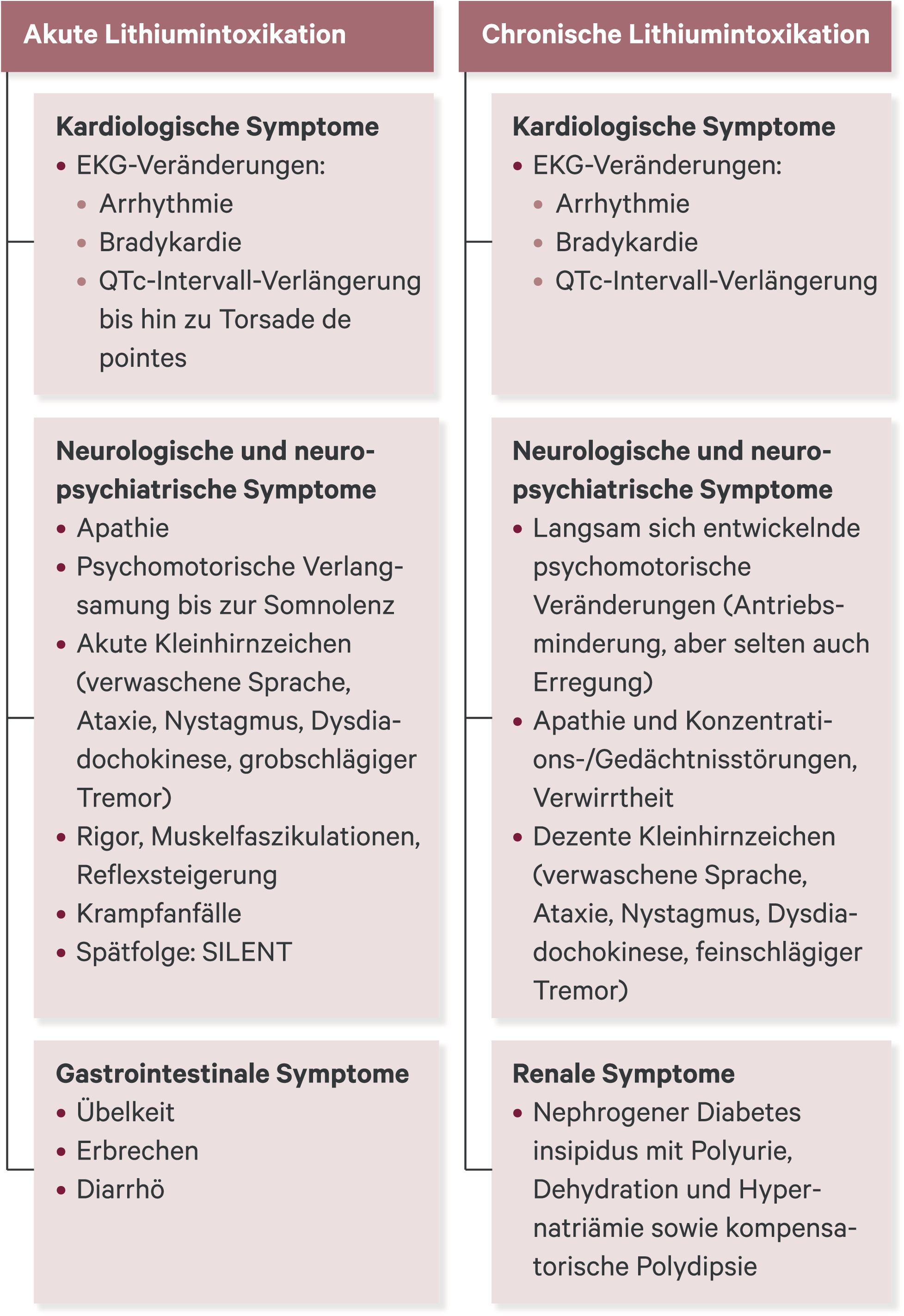
Abb. 2. Symptomatik der akuten und chronischen Lithium-Intoxikation; SILENT: Syndrome of lithium-effectuated neurotoxicity
Kontrolluntersuchungen
Grundsätzlich gilt, dass vor Beginn jeglicher Psychopharmakotherapie eine umfangreiche Labordiagnostik und körperliche Untersuchung zu erfolgen hat, wie in S3-Leitlinien angegeben [7]. Psychiatrische Patienten nehmen in der Regel weniger Kontakte mit dem Hausarzt sowie Gesundheitsvorsorge wahr, sind aber mit einem wesentlich höheren Risiko für endokrinologische, Herz-Kreislauf- sowie Tumorerkrankungen behaftet [24]. So bieten die vorbereitenden Untersuchungen vor einer Pharmakotherapie gleichzeitig die Chance eines umfassenden Gesundheits-Checks.
Speziell zur Lithium-Therapie werden folgende Empfehlungen gegeben [4, 7]: Vor Beginn einer Lithium-Therapie wird der Ausgangswert der Nierenfunktion ermittelt. Zur genauen Messung der Creatinin-Clearance ist eine 24-Stunden-Urinsammlung erforderlich, was im klinischen Alltag selten korrekt gelingt. Daher wird die Creatinin-Clearance zumeist mithilfe von Formeln wie der MDRD(Modification of diet in renal disease)-Formel oder der Methode von Cockcroft und Gault aus dem Serumcreatinin abgeschätzt, wobei mit wichtigen Einflussgrößen wie Alter, Geschlecht und Körpergewicht korrigiert wird.
Berechnung der Creatinin-Clearance nach Cockcroft-Gault:
Creatinin-Clearance [ml/min] = {(140 – Alter) x Körpergewicht [kg]}/{Creatinin im Serum [mg/dl] x 72}
(Bei Frauen ist das Ergebnis noch mit 0,85 zu multiplizieren.)
Für die Erfassung der Schilddrüsenfunktion ist es im klinischen Alltag meist ausreichend, das Thyreoidea-stimulierende Hormon (TSH) im Serum zu bestimmen und bei der körperlichen Untersuchung Halsumfang und eventuelles Vorhandensein einer Kropf- oder Knotenbildung zu erfassen. Bei veränderten TSH-Werten bzw. körperlichem Untersuchungsbefund sollten aber weitere laborchemische (freies Triiodthyronin [fT3], freies Tetraiodthyronin [fT4], Thyreotropin-Releasing-Hormone [TRH], gegebenenfalls TRH-Stimulationstest) und technische (Schilddrüsensonographie) Untersuchungen erfolgen. Da Lithium über eine Stimulierung der B-Lymphozyten Autoimmunerkrankungen der Schilddrüse fördern kann, sollten bei entsprechendem klinischem Verdacht (oder Familienanamnese) auch die Titer von Schilddrüsenantikörpern bestimmt werden.
Serumelektrolyte, insbesondere Calcium im Serum sollten vor Therapiebeginn und in regelmäßigen Abstanden kontrolliert werden, um einen Hyperparathyreoidismus rechtzeitig zu erkennen.
Bei stabil eingestellter Lithium-Dosis sind Kontrollen des Lithium-Spiegels im vierteljährlichen Abstand in der Regel ausreichend, sofern nicht besondere Umstände (interkurrente Erkrankungen, starke Flüssigkeitsverlust z. B. durch Diarrhö oder Erbrechen) hinzukommen.
Mindestens einmal jährlich sollte eine gründliche körperliche Untersuchung mit Messung des Halsumfangs und Gewichts erfolgen, selbstverständlich ist dabei besonders auf Zeichen eingeschränkter Nierenfunktion (Ödeme) bzw. Schilddrüsenfehlfunktion (Kropfbildung, Exophthalmus) zu achten. Eine EKG-Kontrolle ist bei den zwar seltenen, aber möglichen Reizleitungsstörungen durch Lithium ebenfalls indiziert [24], vor allem bei Polypharmazie.
Weitere laborchemische Kontrollen bei stabil eingestellten Lithium-Patienten werden in halbjährlichen bis jährlichen Abstand empfohlen.
Dosierung
Die übliche tägliche Anfangsdosis von Lithium beträgt bei Erwachsenen 450 bis 600 mg als Retardtablette, selten 900 mg, wobei der höhere Dosisbereich eher bei der akuten Manie zur Anwendung kommt (meist in Kombination mit einem weiteren antimanischen Medikament oder Sedativum). Nach 3 bis 7 Tagen erfolgt dann zumeist eine erste Serumspiegelkontrolle 12 Stunden nach der letzten Einnahme, und in Abhängigkeit vom Ergebnis und klinischen Eindruck (Wirkung, Nebenwirkungen) wird die Dosis angepasst (üblicher therapeutischer Bereich 0,6 bis 1,0 mmol/l).
Die Frage, welcher Serumspiegelbereich optimal für die Prophylaxe bipolarer Störungen ist, lässt sich rein evidenzbasiert nur sehr eingeschränkt beantworten. Ein systematisches Review einschließlich eines Delphi-Survey internationaler Experten ergab als Konsensus-Empfehlung für Erwachsene einen Serumspiegel von 0,6 bis 0,8 mmol/l [16].
Es besteht eine gewisse Unsicherheit, wie mit der Lithium-Einnahme bei nachlassender Nierenfunktion zu verfahren ist, hier ist im Einzelfall ein Nephrologe zu konsultieren. Zur Reduktion der nierentoxischen Wirkung von Lithium werden vor der letzten Option, dem vollständigen Ausschleichen der Substanz, verschiedene Therapiemodifikationen beschrieben. Eine Möglichkeit ist die generelle Reduktion der Dosis und damit der Lithium-Spiegel mit der Gefahr eines Wirkverlusts. Die andere beschriebene Option ist die Einmalgabe zur Nacht mit Dosisreduktion bei gleichbleibenden Serumspiegeln. Angesichts reduzierter nächtlicher Lithium-Clearance über die Nieren gibt es die Empfehlung, bei einer nächtlichen Einmalgabe die Dosis um 25 % zu reduzieren.
Beendigung der Lithiumtherapie
Bei sehr guten Lithium-Respondern und keinen oder nur geringen Nebenwirkungen sollte Lithium insbesondere bei bipolaren Patienten in der Regel eine lebenslange Therapie darstellen. Was ist jedoch zu beachten, wenn Wirkverlust oder Nebenwirkungen einen Therapiewechsel erforderlich machen?
Das Absetzen von Lithium nach längerfristiger Therapie kann problematisch sein und sollte unter regelmäßigen ärztlichen Kontrollen über einen längeren Zeitraum erfolgen. Sofern keine notfallmäßige Indikation besteht, sollte Lithium über mindestens ein Jahr ausgeschlichen werden. Lithium erzeugt keine körperliche Abhängigkeit, aber als psychische Absetzphänomene werden vermehrte Angst, Schlafstörungen und Nervosität beschrieben und können eine symptomatische Behandlung erforderlich machen. Darüber hinaus kann ein abruptes Abbrechen der Lithium-Behandlung oder eine starke Dosisreduktion ein erhebliches Rückfallrisiko, insbesondere manische Episoden, nach sich ziehen. So erleiden etwa 50 % der Patienten nach abruptem Absetzen von Lithium einen Rückfall innerhalb von drei Monaten. Erst wenn Lithium länger als zwei Jahre zuverlässig genommen wird, überwiegt nach der Modellrechnung von Goodwin der Nutzen den potenziellen Schaden durch ein Absetzen. Dies unterstreicht die Wichtigkeit einer guten Psychoedukation und eines vertrauensvollen Verhältnisses zwischen Therapeut und Lithium-Patient.
Auch wenn sich keine zufriedenstellende Affektstabilisierung mit Lithium erreichen lässt, kann manchmal die Fortführung, auch mit geringeren Serumspiegeln, zusätzlich zu einer anderen Therapie sinnvoll sein; synergistische Effekte in der Phasenprophylaxe sind beispielsweise für Lithium und Lamotrigin beschrieben. Auch ist unklar, ob für die antisuizidale Wirkung von Lithium unter Umständen auch subtherapeutische Spiegel ausreichend sind. Schließlich scheint es eine Subgruppe von Patienten zu geben, bei denen der therapeutische Erfolg der Lithium-Therapie erst über einen längeren Zeitraum und bei Veränderung der Krankheitsdynamik (z. B. zunehmendes Alter, kein Rapid-Cycling-Muster mehr) evident wird.
Interessenkonflikterklärung
HG: Forschungsunterstützung oder Honorare für Beratung oder Vorträge von folgenden Firmen oder Institutionen: Gedeon-Richter, Janssen-Cilag, Recordati, Sage und Servier.
ES: Mitglied in IGSLI und Co-Chair der “ISBD/IGSLI Task Force on treatment with lithium”
WEM: Keine Interessenkonflikte
GL: Honorare für Vorträge und Beratungen oder unbeschränkte Subventionen für Schulungen von Bayer, Janssen-Cilag, Lundbeck, Pfizer und Servier.
Literatur
1. Amerio A, Ossola P, Scagnelli F, Odone A, et al. Safety and efficacy of lithium in children and adolescents: A systematic review in bipolar illness. Eur Psychiatry 2018;54:85–97.
2. Bauer M, Adli M, Bschor T, Pilhatsch M, et al. Lithium’s emerging role in the treatment of refractory major depressive episodes: augmentation of antidepressants. Neuropsychobiology 2010;62:36–42.
3. Bauer M, Pfennig A, Severus E, Whybrow PC, et al. World Federation of Societies of Biological Psychiatry (WFSBP) guidelines for biological treatment of unipolar depressive disorders, part 1: update 2013 on the acute and continuation treatment of unipolar depressive disorders. World J Biol Psychiatry 2013;14:334–85.
4. Bschor T, Bauer M. Nebenwirkungs- und Risikoprofil von Lithium: Kritische Bewertung einer systematischen Übersicht und Metaanalyse. Nervenarzt 2013;84:860–3.
5. Cipriani A, Hawton K, Stockton S, Geddes JR. Lithium in the prevention of suicide in mood disorders: updated systematic review and meta-analysis. BMJ 2013;346:3646.
6. de Vries C, van Bergen A, Regeer EJ, Benthem E, et al. The effectiveness of restarted lithium treatment after discontinuation: reviewing the evidence for discontinuation-induced refractoriness. Bipolar Disord 2013;15:645–9.
7. DGBS e. V. und DGPPN e. V. S3-Leitlinie zur Diagnostik und Therapie Bipolarer Störungen. Langversion 2.0. http://www.leitlinie-bipolar.de/wp-content/uploads/2019/11/S3_Leitlinie-Bipolar_V2_Update_20191018.pdf (Zugriff am 08.02.2020).
8. Fornaro M, Maritan E, Ferranti R, Zaninotto L, et al. Lithium exposure during pregnancy and the postpartum period: A systematic review and meta-analysis of safety and efficacy outcomes. Am J Psychiatry 2020;177:76–92.
9. Grunze H, Vieta E, Goodwin GM, Bowden C, et al. The World Federation of Societies of Biological Psychiatry (WFSBP) Guidelines for the biological treatment of bipolar disorders: Update 2010 on the treatment of acute bipolar depression. World J Biol Psychiatry 2010;11:81–109.
10. Hozer F, Sarrazin S, Laidi C, Favre P, et al. Lithium prevents grey matter atrophy in patients with bipolar disorder: an international multicenter study. Psychol Med 2020:1–10. doi: 10.1017/S0033291719004112. [Epub ahead of print].
11. Matsunaga S, Kishi T, Annas P, Basun H, et al. Lithium as a treatment for Alzheimer‘s disease: A systematic review and meta-analysis. J Alzheimers Dis 2015;48:403–10.
12. McKnight RF, Adida M, Budge K, Stockton S, et al. Lithium toxicity profile: a systematic review and meta-analysis. Lancet 2012;379:721–8.
13. McKnight RF, de La Motte de Broons de Vauvert S, Chesney E, Amit BH, et al. Lithium for acute mania. Cochrane Database Syst Rev 2019;6:Cd004048.
14. Miller JN, Black DW. Bipolar disorder and suicide: a review. Curr Psychiatry Rep 2020;22:6.
15. Miura T, Noma H, Furukawa TA, Mitsuyasu H, et al. Comparative efficacy and tolerability of pharmacological treatments in the maintenance treatment of bipolar disorder: a systematic review and network meta-analysis. Lancet Psychiatry 2014;1:351–9.
16. Nolen WA, Licht RW, Young AH, Malhi GS, et al. What is the optimal serum level for lithium in the maintenance treatment of bipolar disorder? A systematic review and recommendations from the ISBD/IGSLI Task Force on treatment with lithium. Bipolar Disord 2019;21:394–409.
17. Severus E, Bauer M. Managing the risk of lithium-induced nephropathy in the long-term treatment of patients with recurrent affective disorders. BMC Med 2013;11:34.
18. Severus E, Bauer M, Geddes J. Efficacy and effectiveness of lithium in the long-term treatment of bipolar disorders: An update 2018. Pharmacopsychiatry 2018;51:173–6.
19. Severus E, Taylor MJ, Sauer C, Pfennig A, et al. Lithium for prevention of mood episodes in bipolar disorders: systematic review and meta-analysis. Int J Bipolar Disord 2014;2:15.
20. Shulman KI, Almeida OP, Herrmann N, Schaffer A, et al. Delphi survey of maintenance lithium treatment in older adults with bipolar disorder: An ISBD task force report. Bipolar Disord 2019;21:117–23.
21. Sun YR, Herrmann N, Scott CJM, Black SE, et al. Global grey matter volume in adult bipolar patients with and without lithium treatment: A meta-analysis. J Affect Disord 2018;225:599–606.
22. Taylor MJ. Timing of onset of lithium relapse prevention in bipolar disorder: evidence from randomised trials. Br J Psychiatry 2018;213:664–6.
23. Woo YS, Yoon BH, Song JH, Seo JS, et al. Clinical correlates associated with the long-term response of bipolar disorder patients to lithium, valproate or lamotrigine: A retrospective study. PLoS One 2020;15:e0227217.
24. Young AH, Grunze H. Physical health of patients with bipolar disorder. Acta Psychiatr Scand Suppl 2013;(442):3–10. doi: 10.1111/acps.12117.
25. Young AH, McElroy SL, Bauer M, Philips N, et al. A double-blind, placebo-controlled study of quetiapine and lithium monotherapy in adults in the acute phase of bipolar depression (EMBOLDEN I). J Clin Psychiatry 2010;71:150–62.
26. Zhou X, Ravindran AV, Qin B, Del Giovane C, et al. Comparative efficacy, acceptability, and tolerability of augmentation agents in treatment-resistant depression: systematic review and network meta-analysis. J Clin Psychiatry 2015;76:e487–98.
Priv.-Doz. Dr. med. Heinz Grunze, Zentrum für Psychiatrie, Klinikum am Weissenhof, Klinik für Allgemeine Psychiatrie und Psychotherapie Ost, 74189 Weinsberg, E-Mail: h.grunze@klinikum-weissenhof.de
Priv.-Doz. Dr. med. Emanuel Severus, Klinik und Poliklinik für Psychiatrie und Psychotherapie, Universitätsklinikum Carl Gustav Carus Dresden, TU Dresden, Fetscherstraße 74, 01307 Dresden
Prof. Dr. med. Dipl.-Psych. Gerd Laux, Institut für Psychologische Medizin (IPM), Nussbaumstraße 9, 83564 Soyen
Univ.-Prof. Dr. Walter E. Müller, Höhenstraße 49a, 67550 Worms
Psychopharmakotherapie 2020; 27(03)
