Tim Patrick Jürgens, Rostock, Kerstin Engel und Susanne Kraemer, Bad Homburg
Viele Migränepatienten brechen eine medikamentöse Prophylaxe aufgrund von Nebenwirkungen oder mangelnder Wirkung ab, bevor der volle Wirkeffekt eintritt. Mit monoklonalen Antikörpern gegen das Neuropeptid CGRP (Calcitonin gene-related peptide) bzw. dessen Rezeptor, die bei der Migräneentstehung eine Schlüsselrolle spielen, gibt es eine neue, gut verträgliche Gruppe von Prophylaktika. Hier werden die klinischen Studien für den monoklonalen Antikörper Galcanezumab (GMB) dargestellt. Galcanezumab hat die klinische Phase 3 erfolgreich durchlaufen und erhielt im November 2018 die Zulassung der europäischen Zulassungsbehörde EMA. Es ist laut Fachinformation angezeigt zur Migräne-Prophylaxe bei erwachsenen Patienten mit mindestens vier Migränetagen pro Monat.
Weltweit wird die Migräneprävalenz aktuell mit 11 bis 13 % (europaweit 11,4 %, Deutschland 13,4 %) angegeben [40, 42]. Bei mehreren Migräneattacken pro Monat mit besonderem Leidensdruck oder Risiken, Einschränkung der Lebensqualität und drohendem Medikamentenübergebrauch empfiehlt die aktuelle S1-Leitlinie eine medikamentöse Migräneprophylaxe, um Häufigkeit, Schwere und Dauer der Migräneattacken und die Entwicklung eines Medikamentenübergebrauchs zu reduzieren [21]. Zugelassen sind dafür bisher die Betablocker Propranolol, Metoprolol, der Calciumantagonist Flunarizin und das Antikonvulsivum Topiramat, das Antidepressivum Amitriptylin [21] sowie Botulinumtoxin A nur für die chronische Migräne [1]. Valproinsäure kann im Off-Label-Gebrauch zulasten der Krankenkassen gegeben werden [14].
Obwohl bei knapp 40 % aller Migränepatienten sinnvoll, führen nur 3 bis 13 % aller Betroffenen eine solche Prophylaxe durch [23]. Außerdem ist die Persistenz gering, denn mehr als 50 % der Patienten setzen die Medikation innerhalb der ersten sechs Monate ab, sei es wegen mangelnder Wirksamkeit, mangelnder Verträglichkeit oder weil sie nicht täglich Medikamente einnehmen wollen [6, 30]. Für diese Patienten könnte die neue Stoffgruppe der zielgerichteten Biologika die Behandlungsoptionen für die Migräneprophylaxe erweitern. Mehrere monoklonale Antikörper gegen das Neuropeptid CGRP bzw. seinen Rezeptor zeigten in klinischen Studien eine gute Wirksamkeit bei geringen Nebenwirkungen. Erstmals steht mit diesen Substanzen eine an den neuen Erkenntnissen zur Migräne-Pathophysiologie orientierte Wirkstoffgruppe zur Verfügung. Mehrere Antikörper gegen den Liganden CGRP sind weit fortgeschritten in der klinischen Entwicklung [10, 30]; als erster wurde der Antikörper Erenumab, der gegen den CGRP-Rezeptor gerichtet ist, danach die CGRP-Antikörper Galcanezumab (Tab. 1) im November 2018 und Fremanezumab Anfang 2019 europaweit zugelassen.
Tab. 1. Eigenschaften von Galcanezumab
|
Pharmakologie |
|
|
Pharmakokinetik |
|
|
Verteilung im Organismus |
|
|
Biotransformation und Elimination |
|
|
Dosierung |
|
CGRP: Calcitonin gene-related peptide; Cmax: maximale Serumkonzentration; IgG: Immunglobulin G; KD: Affinitätskonstante; tmax: Zeit bis zum Erreichen von Cmax
CGRP und seine Rolle in der Pathophysiologie der Migräne
Das aus 37 Aminosäuren bestehende Neuropeptid CGRP wird sowohl im peripheren als auch im zentralen Nervensystem sowie in nicht nervalen Geweben exprimiert [15, 31]. CGRP ist ein afferent-sensorischer, in C- und Aδ-Fasern lokalisierter, aber auch efferenter Neurotransmitter. Neben Relevanz in der Schmerzmodulation hat CGRP eine vasodilatorische Wirkung mit Beteiligung an physiologischen und pathologischen Prozessen in unterschiedlichen Organsystemen, so auch im kardiovaskulären System, dem Magen-Darm-Trakt oder bei der Wundheilung [31]. CGRP bindet an einen Rezeptor-Komplex aus CLR (Calcitonin receptor-like receptor) und RAMP1 (Receptor activity-modifying protein). Es bindet zudem an den Calcitonin-Rezeptor und den Amylin-1- bis Amylin-3-Rezeptor, der aus dem Calcitonin-Rezeptor und RAMP1 (bzw. RAMP2 oder RAMP3) besteht. Eine Blockade des freien CGRP könnte somit nicht nur durch den CGRP-Rezeptor vermittelte Vorgänge beeinflussen, sondern auch über den obengenannten Rezeptor vermittelte.
CGRP ist ein zentraler Mediator in der komplexen Migränepathophysiologie. So lässt sich CGRP in schmerzsensiblen perivaskulären Trigeminusfasern nachweisen, die die Blutgefäße der Dura mater und des Arachnoidalraums innervieren (Abb. 1). Die physiologischen Funktionen von CGRP im Bereich des Nervensystems umfassen unter anderem die Übertragung aufsteigender sensorischer Signale auf die nachgeschalteten Neurone, aber es fungiert auch als Neurotransmitter für absteigende Schmerzsignale über das trigeminovaskuläre System: An den perivaskulären Nervenendigungen setzen die Trigeminusneurone CGRP und weitere Neuropeptide frei. In der Dura induziert das freigesetzte CGRP neben einer Vasodilatation – die entgegen früheren Theorien (die „vaskuläre These“ von Wolff) [16] nicht die Ursache der Schmerzentstehung ist, sondern eher ein Epiphänomen – möglicherweise eine Degranulation duraler Mastzellen (Abb. 1) [31]. Gemäß dem Konzept der „neurogenen Inflammation“ kommt es zu gesteigertem Blutfluss, Ödembildung, Rekrutierung von Entzündungszellen und Freisetzung weiterer proinflammatorischer Neuropeptide und Mediatoren wie Histamin und Stickoxid. Es gibt allerdings auch Zweifel an dieser Hypothese, da auf humanen Mastzellen keine CGRP-Rezeptoren gefunden werden konnten und medikamentöse Blocker der neurogenen Inflammation in Studien bei Migräne keinen therapeutischen Nutzen hatten [16]. Durch eine vermehrte Aktivierung der Nozizeptoren kommt es zunächst zu einer Sensitisierung des peripheren trigeminovaskulären Systems, dann auch zentraler schmerzverarbeitender Strukturen [15, 31] (Abb. 1). Das trigeminovaskuläre System ist mit Strukturen der deszendierenden Hemmung, wie dem periaquäduktalen Grau, dem Nucleus salivatorius superior, dem Hypothalamus, dem Thalamus und zahlreichen kortikalen Strukturen über meist bilaterale Faserbahnen verbunden. Jüngere bildgebende Studien weisen auf eine relevante Rolle des Hypothalamus in der Attackengenerierung und der Chronifizierung der Migräne hin [32].
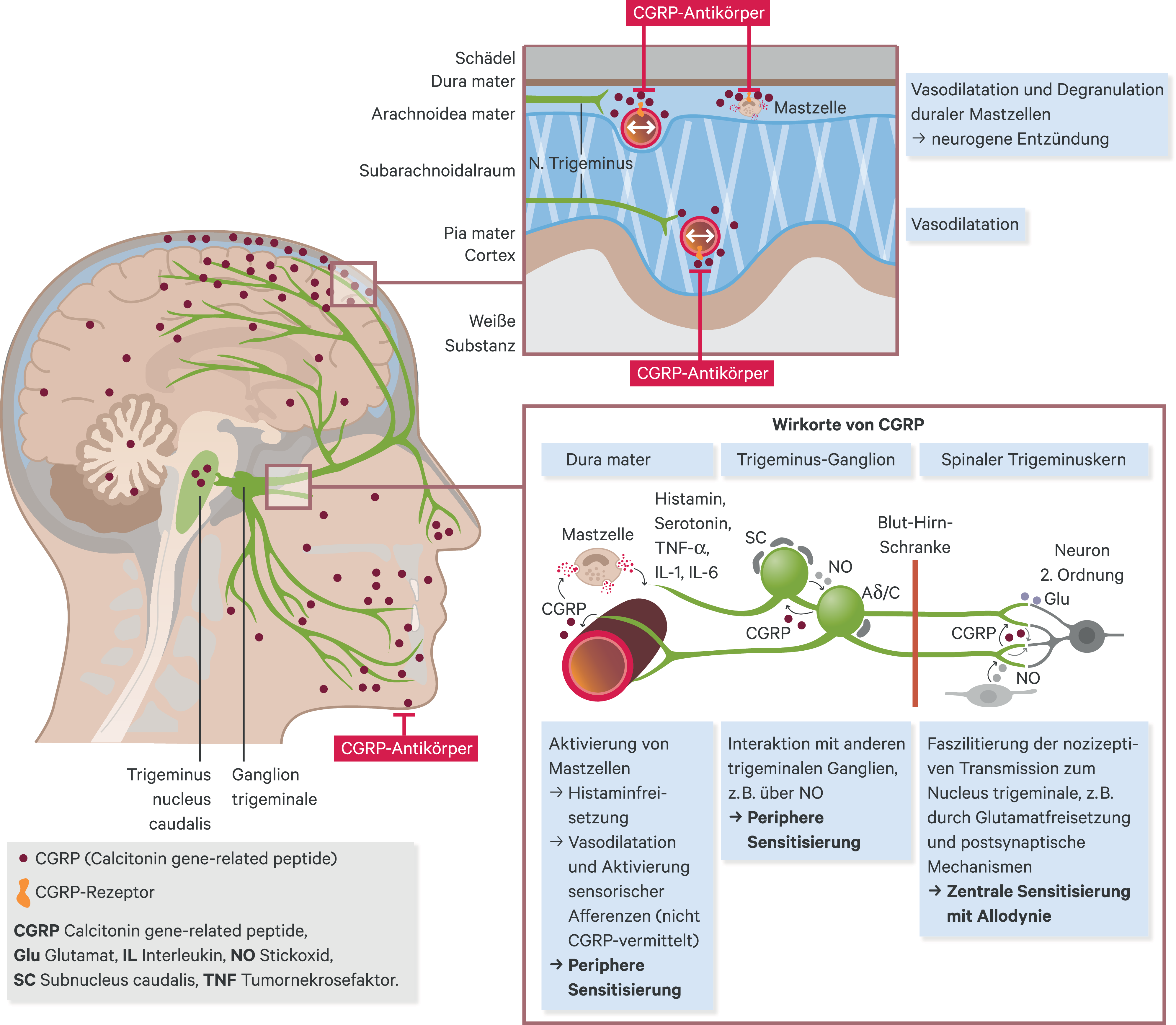
Abb. 1. Die multiplen Effekte von CGRP und seine Schlüsselrolle in der Pathophysiologie der Migräne (mod. nach Russell et al. 2014 [31] und Messlinger et al. 2012 [26]) CGRP wird in weiten Teilen des zentralen und peripheren Nervensystems exprimiert. Die Abbildung veranschaulicht das Wirkprinzip des Anti-CGRP-Antikörpers Galcanezumab bei der Migräneprophylaxe durch Hemmung der CGRP-induzierten Vasodilatation und Hemmung der neurogenen Entzündung durch Hemmung der CGRP-induzierten Degranulation von Mastzellen in der Dura Mater.
Klinische Studien bei Migränepatienten konnten zeigen, dass während einer spontanen Migräneattacke die CGRP-Spiegel in der Vena jugularis externa erhöht sind, dass sich die CGRP-Spiegel mit Triptanen senken lassen, und dass die Infusion von CGRP bei Patienten mit bekannter Migräne – im Gegensatz zu Probanden ohne Migräne – eine typische Migräneattacke auslösen kann. Diese Befunde sind ein Indiz dafür, dass CGRP eine fundamentale Rolle in der Pathophysiologie der Migräne spielt [15]. Vor diesem Hintergrund stellt die Hemmung von CGRP bzw. des CGRP-Rezeptors einen interessanten und pathophysiologisch fundierten spezifischen Ansatzpunkt für die Migränebehandlung dar. Klinische Studien mit niedermolekularen CGRP-Rezeptorantagonisten (den sogenannten Gepanten) lieferten klare Hinweise, dass mit CGRP-Antagonisten eine Besserung von Migräneattacken sowie eine Migräneprophylaxe möglich ist [10, 25, 30]. Aufgrund von Nebenwirkungen (v. a. Hepatotoxizität) der ersten Gepante in den Zulassungsstudien wurde die Entwicklung dieser Substanzen unterbrochen. Neuere Substanzen dieser Gruppe befinden sich in der klinischen Prüfung.
Wirkmechanismus und Pharmakologie von Galcanezumab
Galcanezumab ist ein humanisierter IgG4-Antikörper (Tab. 1), bei dem nur noch die CGRP-Bindungsstellen der variablen Antikörperregion von der Maus stammen. Das gesamte übrige Molekül besteht aus humanem Immunglobulin, wodurch Autoimmunreaktionen minimiert werden. Galcanezumab kann aufgrund seiner Molekülgröße die Blut-Hirn-Schranke kaum überwinden (nur 0,1 bis 0,5 %), sodass der Wirkort primär peripher anzunehmen ist [15], vorrangig im Bereich der meningealen Gefäße und der peripher gelegenen Anteile des N. trigeminus, insbesondere des Ganglion trigeminale. Galcanezumab bindet an CGRP und hemmt so CGRP-vermittelte Prozesse (wie die Vasodilatation kleiner Gefäße, möglicherweise neurogene Entzündungsprozesse und die nozizeptive Transmission an zentrale schmerzverarbeitende Strukturen) [15]. Präklinisch wurde die CGRP-neutralisierende Aktivität in vitro sowie durch verschiedene Tiermodelle belegt. Bei Ratten inhibiert subkutan (s. c.) verabreichtes Galcanezumab die Capsaicin-induzierte Vasodilatation in der Haut und reduziert schmerzassoziiertes Verhalten in einem intraartikulären Schmerzmodell [5].
Galcanezumab hat eine lange Halbwertszeit von etwa 27 Tagen, sodass es nur einmal monatlich injiziert werden muss. Wie Immunglobuline wird auch Galcanezumab weder in der Leber metabolisiert noch über die Niere ausgeschieden, sondern durch Proteolyse in kleinere Peptide bzw. einzelne Aminosäuren gespalten. Damit sind pharmakokinetische Wechselwirkungen mit anderen Arzneimitteln weitgehend ausgeschlossen. Alter, Geschlecht, Gewicht oder auch Ort der Injektionsstelle haben keinen Einfluss auf die Pharmakokinetik von Galcanezumab [20].
Das klinische Studienprogramm
In der ersten klinischen Studie mit 63 gesunden Probanden (Phase I, Dosiseskalation, Placebo-kontrolliert) zeigte Galcanezumab (1 bis 600 mg s. c.) eine lineare Pharmakokinetik im gesamten untersuchten Dosisbereich (Tab. 1) sowie eine anhaltende Hemmung des Capsaicin-induzierten Anstiegs der Hautdurchblutung [27]. Erste Daten zur klinischen Wirksamkeit als Migräneprophylaxe (Senkung der monatlichen Migränekopfschmerztage [MKT]) und Verträglichkeit lieferten dann zwei Placebo-kontrollierte Phase-II-Studien mit insgesamt ungefähr 600 Patienten mit episodischer Migräne; dabei wurden unterschiedliche Dosierungen und Dosierintervalle geprüft. Auf Basis dieser Daten wurde die s. c. Gabe von 120 mg oder 240 mga einmal monatlich als geeignetste Dosierungen für die Phase-III-Zulassungsstudien identifiziert [11, 29, 36].
Phase-III-Zulassungsstudien
Bisher liegen drei voll publizierte multinationale, randomisierte, Placebo-kontrollierte Phase-III-Doppelblindstudien zur Migräneprophylaxe mit Galcanezumab vor, davon zwei Studien mit einer Doppelblindperiode über sechs Monate bei episodischer Migräne (EVOLVE-1 [38], EVOLVE-2 [37]) sowie eine Studie doppelblind über drei Monate bei chronischer Migräne (REGAIN [8] (Abb. 2). Hinzu kommen 12-Monats-Daten aus einer offenen Langzeitstudie zur Verträglichkeit von Galcanezumab [39]. In allen Studien wurde Galcanezumab s. c. einmal monatlich verabreicht, und zwar einmal in der zugelassenen Dosierung von 120 mg s. c. (einmalige Anfangsdosis von 240 mg bei Behandlungsbeginn) und zusätzlich in einer höheren, nicht zugelassenen Dosierung von 240 mg. Alle Patienten konnten Akutmedikation zur Attackenbehandlung der Migräne verwenden (Opiate und Barbiturate an maximal drei Tagen/Monat).

Abb. 2. Design der Placebo-kontrollierten Phase-III-Studien bei Patienten mit episodischer (EVOLVE-1, EVOLVE-2) bzw. chronischer Migräne (REGAIN)
In die beiden identischen EVOLVE-Studien wurden jeweils Erwachsene (18 bis 65 Jahre) mit episodischer Migräne mit oder ohne Aura (gemäß internationaler Kopfschmerzklassifikation [18, 19]) und mit monatlich mindestens vier bis maximal 14 MKT (Definition MKT in Tab. 2) und mindestens zwei Migräneattacken während der prospektiven Baseline-Periode aufgenommen. Die Patienten wurden 1 : 1 : 2 auf Galcanezumab 120 mg bzw. 240 mga s. c./Monat bzw. auf Placebo s. c./Monat randomisiert. Hier berichtet werden die Daten bis zum Ende der 6-monatigen Doppelblindperiode (Abb. 2). EVOLVE-1 wurde ausschließlich in Nordamerika durchgeführt, EVOLVE-2 dagegen weltweit: hier stammten etwa 50 % der Patienten aus Nordamerika, 25 % aus Europa und 25 % aus anderen Regionen.
Tab. 2. In den Studien EVOLVE-1/-2 und REGAIN verwendete Endpunkte und Bewertungssysteme
|
Migränekopfschmerztage (MKT) |
Dokumentation der Kopfschmerzen in elektronischem Patiententagebuch Gezählt wurden Tage, an denen der Patient einen Kopfschmerz von ≥ 30 Minuten Dauer dokumentiert hat, der die Kriterien für „Migränekopfschmerz“ oder „wahrscheinlichen Migränekopfschmerz“ gemäß der Internationalen Kopfschmerzklassifikation [18] erfüllt. (Migränetage ohne Kopfschmerz oder Kopfschmerz anderer Ursache wurden beim primären Endpunkt nicht berücksichtigt) Bei der REGAIN-Studie zum chronischen Kopfschmerz wurde als „Migränekopfschmerz“ zusätzlich ein vom Patienten als Kopfschmerz mit Migränecharakter definiert, der nach Einnahme eines Triptans oder Ergotamins nachließ. |
|
Primärer Endpunkt |
Mittlere Änderung der MKT/Monat (modellbasiert) während der Doppelblindperiode (6 Monate EVOLVE-1 und -2, 3 Monate REGAIN) im Vergleich zum Ausgangswert (Baseline-Periode) |
|
Wichtige sekundäre Endpunkte |
|
|
Prozentuales Ansprechen |
Prozentsatz der Patienten, bei denen sich die MKT im Vergleich zum Ausgangswert in mindestens einer 30-Tage-Periode während der Doppelblindperiode um ≥ 30 (REGAIN)/≥ 50 %/≥ 75 %/100 % verringerte |
|
MKT mit Akutmedikation |
MKT/Monat, an denen der Patient während der Doppelblindperiode die Einnahme von Akutmedikation zur |
|
Lebensqualität (MSQ RF-R, MSQ EF) |
Patientenbewertung, Migräne-spezifischer Fragebogen: Migraine-Specific Quality of Life Questionnaire (MSQ, Version 2.1). Beim Role Function Restrictive (RF-R) Domain Score bewertet der Patient den Grad der Einschränkung sozialer und arbeitsbezogener Aktivitäten durch die Migräne in insgesamt 7 Items; beim Emotional Function (EF) Domain Score das emotionale Befinden in insgesamt 3 Items. Die Scores sind von 0–100 normalisiert, höhere Werte bedeuten bessere Lebensqualität. |
|
Alltagsfunktionsfähigkeit (MIDAS) |
Patientenbewertung, Migräne-spezifischer Fragebogen: Migraine Disability Assessment (Gesamtscore). Der Patient bewertet den Einfluss der Kopfschmerzen auf seine Funktionsfähigkeit im Alltag in den letzten 3 Monaten, indem er für 5 Items jeweils die Anzahl der Tage mit Beeinträchtigung durch Migräne angibt; die Summe der Items ergibt den Gesamtscore (0–5: wenig oder keine Beeinträchtigung; > 20: schwere Beeinträchtigung). |
In die REGAIN-Studie aufgenommen wurden Erwachsene (18 bis 65 Jahre) mit mindestens 15 Kopfschmerztagen monatlich während der prospektiven Baseline-Periode. Davon mussten mindestens acht Tage die Charakteristika einer Migräne erfüllen (Internationale Kopfschmerzklassifikation [ICHD-3β]) [18], und wenigstens ein Tag pro Monat musste frei von Kopfschmerzen sein. Die Patienten wurden 1 : 1 : 2 auf Galcanezumab 120 mg bzw. 240 mga bzw. auf Placebo randomisiert. Berichtet werden Ergebnisse für die 3-monatige doppelblinde und die 9-monatige offene Behandlungsperiode (Abb. 2) [8, 9].
In den EVOLVE- und REGAIN-Studien wurden alle Injektionen am Studienzentrum vorgenommen. Die Patienten dokumentierten täglich Kopfschmerzzeiten und -charakteristika sowie den Bedarf an Akutmedikation in einem elektronischen Tagebuch. Angaben zur Lebensqualität wurden bei den Studienvisiten am Zentrum erhoben. In der offenen 12-Monats-Studie, bei der die Patienten 1 : 1 entweder 120 mg bzw. 240 mga Galcanezumab erhielten, injizierten die Patienten Galcanezumab ab der 2. Injektion selbst. Die Kopfschmerzdokumentation nahmen die Patienten in ihrer gewohnten Weise vor; sie wurde bei den monatlichen Studienvisiten am Zentrum erfasst. Der primäre Endpunkt dieser Studie war die Verträglichkeit.
Ergebnisse der Phase-III-Studien
Abbruchraten
In EVOLVE-1 (n = 862), EVOLVE-2 (n = 922) und REGAIN (n = 1117) beendeten 83,1 %, 87,9 % bzw. 94,6 % der mit Galcanezumab 120 mg behandelten Patienten die 6- bzw. 3-monatige doppelblinde Behandlungsperiode wie geplant; die Abbruchraten lagen für beide Dosierungen unter denen der Placebo-Arme (Abb. 3). Die Abbruchrate wegen mangelnder Wirksamkeit oder unerwünschter Ereignisse betrug in allen Galcanezumab-Behandlungsarmen weniger als 5 % und liegt damit unter den Abbruchraten für konventionelle Migräneprophylaxen wie Topiramat [7].

Abb. 3. Patientenverteilung in den Phase-III-Studien EVOLVE-1, EVOLVE-2 und REGAIN
Patientenpopulation
Tabelle 3 zeigt die untersuchten Patientenpopulationen; die Galcanezumab- und Placebo-Arme waren jeweils vergleichbar. In allen Studien lag das Durchschnittsalter bei 39 bis 42 Jahren, über 80 % der Patienten waren Frauen. Es handelte sich um Patienten mit langjähriger Migräne (um 19 Jahre), mehrheitlich mit Migräneprophylaktika vorbehandelt. Während der EVOLVE-Studien durften keine Prophylaktika eingenommen werden, bei REGAIN (chronische Migräne) war die Fortführung bei stabiler Einnahme von Propranolol oder Topiramat erlaubt. Medikamentenübergebrauch (mehr als 60 % der eingeschlossenen Patienten) war in REGAIN kein Ausschlussgrund. Bei den REGAIN-Patienten war die Zahl der monatlichen Tage mit Migränekopfschmerz und anderem Kopfschmerz etwa doppelt so hoch wie bei EVOLVE (episodische Migräne); dementsprechend hatten diese Patienten besonders deutliche Einschränkungen bei Lebensqualität (MSQ RF-R) und Funktionsfähigkeit im Alltag (MIDAS) (Tab. 3).
Tab. 3. Patientenpopulation in den Studien EVOLVE-1/-2 (episodische Migräne) und REGAIN (chronische Migräne) an Baseline
|
EVOLVE-1 |
EVOLVE-2 |
REGAIN |
|||||||
|
GMB 120 mg (n = 213) |
GMB 240 mga (n = 212) |
Placebo (n = 433) |
GMB 120 mg (n = 231) |
GMB 240 mga (n = 223) |
Placebo (n = 461) |
GMB 120 mg (n = 278) |
GMB 240 mga (n = 277) |
Placebo (n = 558) |
|
|
Demographie |
|||||||||
|
Alter [Jahre] |
40,9 (11,9) |
39,1 (11,5) |
41,3 (11,4) |
40,9 (11,2) |
41,9 (10,8) |
42,3 (11,3) |
39,7 (11,9) |
41,1 (12,4) |
41,6 (12,1) |
|
Anteil Frauen [%] |
85,0 |
82,6 |
83,6 |
85,3 |
85,7 |
85,3 |
85,3 |
81,6 |
86,6 |
|
Migränestatus |
|||||||||
|
Migränedauer [Jahre] |
21,1 (13,0) |
19,3 (11,9) |
19,9 (12,3) |
19,9 (11,7) |
20,0 (12,1) |
21,2 (12,8) |
20,4 (12,7) |
20,1 (12,7) |
21,9 (12,9) |
|
MKT/Monat |
9,2 (3,1) |
9,1 (2,9) |
9,1 (3,0) |
9,1 (2,9) |
9,1 (2,9) |
9,2 (3,0) |
19,4 (4,3) |
19,2 (4,6) |
19,6 (4,6) |
|
MKT pro Monat mit Akutmedikation |
7,4 (3,7) |
7,3 (3,3) |
7,4 (3,5) |
7,5 (3,3) |
7,5 (3,3) |
7,6 (3,4) |
15,1 (6,3) |
14,5 (6,3) |
15,5 (6,6) |
|
Kopfschmerztage pro Monat |
10,6 (3,6) |
10,9 (3,9) |
10,6 (3,4) |
10,6 (3,4) |
10,7 (3,7) |
10,7 (3,5) |
21,2 (4,0) |
21,4 (4,1) |
21,5 (4,1) |
|
Migräneattacken pro Monat |
5,6 (1,7) |
5,7 (1,8) |
5,8 (1,7) |
5,5 (1,8) |
5,7 (1,8) |
5,7 (1,8) |
– b |
– b |
– b |
|
Mit Migräneprophylaktika vorbehandelt [%] |
62,4 |
59,0 |
59,4 |
68,0 |
64,6 |
64,6 |
75,9 |
79,4 |
78,0 |
|
≥ 1x/≥ 2x erfolglos vorbehandelt [%] |
18,8 |
18,9 |
18,2 |
14,7 |
15,3 |
13,7 |
24,5 |
35,0 |
29,2 |
|
Medikamentenübergebrauch [%] |
– c |
– c |
– c |
– c |
– c |
– c |
64,0 |
63,9 |
63,3 |
|
MSQ RF-R |
51,4 (16,2) |
48,8 (16,8) |
52,9 (15,4) |
52,5 (14,8) |
51,7 (16,3) |
51,4 (15,7) |
39,3 (17,3) |
38,9 (17,3) |
38,4 (17,2) |
|
MIDAS-Gesamtscore |
32,9 (28,2) |
36,1 (27,8) |
31,8 (27,3) |
30,9 (27,9) |
32,8 (28,8) |
34,3 (31,0) |
62,5 (49,5) |
69,2 (64,1) |
68,7 (57,4) |
Angegeben sind Mittelwert (Standardabweichung), sofern nicht anders angegeben.
a 240 mg als Erhaltungsdosis nicht zugelassen.
b Nicht zutreffend (chronische Migräne).
c In den EVOLVE-1/-2-Studien waren Patienten mit Medikamentenübergebrauch ausgeschlossen.
GMB: Galcanezumab; MKT: Migränekopfschmerztage; MIDAS: Migraine Disability Assessment; MSQ RF-R: Migraine-Specific Quality of Life Questionnaire, Role Function-restrictive Domain Score
Wirksamkeitsdaten
Bei episodischer und chronischer Migräne reduzierte Galcanezumab 120 mg die monatlichen Migränekopfschmerztage (primärer Endpunkt für EVOLVE-1/-2 und REGAIN) signifikant, und zwar um durchschnittlich 4,7/4,3 Tage über den 6-Monats-Zeitraum bei episodischer Migräne (EVOLVE-1/-2; Placebo 2,8/2,3 Tage) bzw. um 4,8 Tage über den 3-Monats-Zeitraum bei chronischer Migräne (REGAIN; Placebo 2,7 Tage). Mit der höheren Dosierung war die Reduzierung der Migränekopfschmerztage ähnlich. Die Abnahme der Migränekopfschmerztage war im Vergleich zu Placebo in beiden Studien ab dem 1. Monat signifikant, und dies blieb bis Studienende erhalten (p < 0,001 [Abb. 4 und Tab. 4]; alle p-Werte ohne Berücksichtigung multipler Testung).
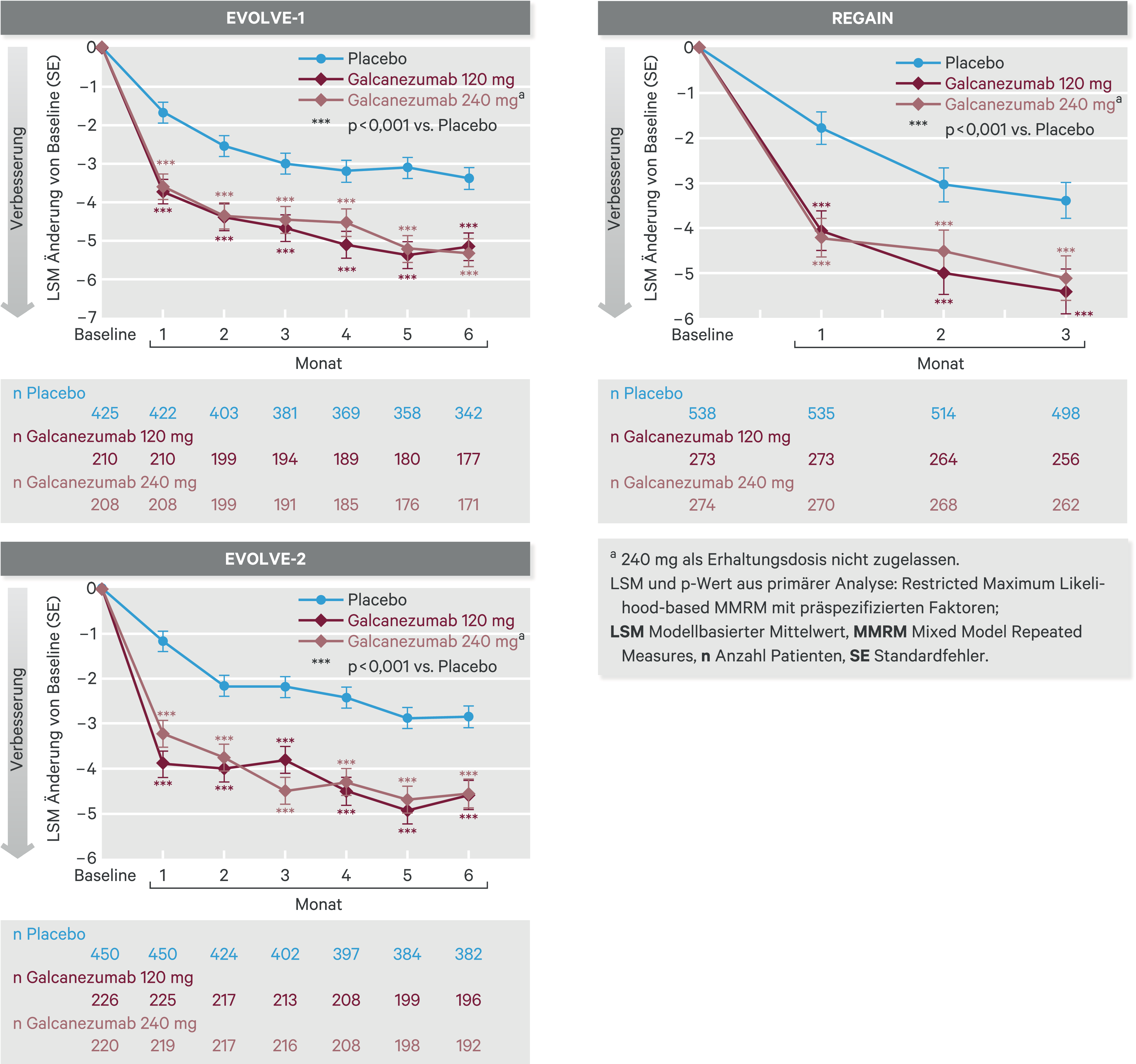
Abb. 4. Reduktion der Migränekopfschmerztage (MKT) bei monatlicher Gabe von Galcanezumab in den Phase-III-Studien EVOLVE und REGAIN
Tab. 4. Ergebnisse aus den Studien EVOLVE-1/-2 (episodische Migräne, Doppelblindperiode 6 Monate) und REGAIN (chronische Migräne, Doppelblindperiode 3 Monate)
|
Studie |
GMB 120 mg |
GBM 240 mga |
Placebo |
|||||
|
N |
LSMb |
LSMc [95%-KI]c |
N |
LSMb |
LSMc [95%-KI] |
N |
LSMb |
|
|
Primärer Endpunkt: MKT pro Monat Mittlere Änderung (über gesamte Behandlung) und Differenz vs. Placebo |
||||||||
|
EVOLVE-1 |
210 |
–4,7 |
–1,9 [–2,5; –1,4]*** |
208 |
–4,6 |
–1,8 [–2,3; –1,2]*** |
425 |
–2,8 |
|
EVOLVE-2 |
226 |
–4,3 |
–2,0 [–2,6; –1,5]*** |
220 |
–4,2 |
–1,9 [–2,4; –1,4]*** |
450 |
–2,3 |
|
REGAIN |
273 |
–4,8 |
–2,1 [–2,9; –1,3]*** |
274 |
–4,6 |
–1,9 [–2,7; –1,1]*** |
538 |
–2,7 |
|
Prozentuales Ansprechen (s. Tabelle 2), % und Odds-Ratio |
||||||||
|
≥ 50 % |
||||||||
|
EVOLVE-1 |
210 |
62,3 |
2,6 [2,1; 3,4]*** |
208 |
60,9 |
2,5 [1,9; 3,2]*** |
425 |
38,6 |
|
EVOLVE-2 |
226 |
59,3 |
2,6 [2,0; 3,3]*** |
220 |
56,5 |
2,3 [1,8; 3,0]*** |
450 |
36,0 |
|
REGAIN |
273 |
27,6 |
2,1 [1,6; 2,8]*** |
274 |
27,5 |
2,1 [1,6; 2,8]*** |
538 |
15,4 |
|
≥ 75 % |
||||||||
|
EVOLVE-1 |
210 |
38,8 |
2,7 [2,0; 3,5]*** |
208 |
38,5 |
2,6 [2,0; 3,4]*** |
425 |
19,3 |
|
EVOLVE-2 |
226 |
33,5 |
2,3 [1,8; 3,1]*** |
220 |
34,3 |
2,4 [1,8; 3,2]*** |
450 |
17,8 |
|
REGAIN |
273 |
7,0 |
1,6 [1,0; 2,5]* |
274 |
8,8 |
2,0 [1,4; 3,1]*** |
538 |
4,5 |
|
100 % |
||||||||
|
EVOLVE-1 |
210 |
15,6 |
2,8 [2,0; 4,0]*** |
208 |
14,6 |
2,6 [2,8; 3,8]*** |
425 |
6,2 |
|
EVOLVE-2 |
226 |
11,5 |
2,2 [1,5; 3,1]*** |
220 |
13,8 |
2,7 [1,9; 3,8]*** |
450 |
5,7 |
|
REGAIN |
273 |
0,7 |
1,4 [0,4; 4,4] ns |
274 |
1,3 |
2,6 [1,0; 7,0] ns |
538 |
0,5 |
|
MKT mit Akutmedikation pro Monat Mittlere Änderung (über gesamte Behandlung) und Differenz vs. Placebo |
||||||||
|
EVOLVE-1 |
210 |
–4,0 |
–1,8 [–2,3; –1,3]*** |
208 |
–3,8 |
–1,6 [–2,6; –1,1]*** |
425 |
–2,2 |
|
EVOLVE-2 |
226 |
–3,7 |
–1,8 [–2,3; –1,4]*** |
220 |
–3,6 |
–1,8 [–2,3; –1,3]*** |
450 |
–1,9 |
|
REGAIN |
273 |
–4,7 |
–2,5 [–3,3; –1,8]*** |
274 |
–4,3 |
–2,0 [–2,8; –1,3]*** |
538 |
–2,2 |
|
MIDAS Gesamtscore Mittlere Änderung (bis Monat 6 bzw. bis Monat 3) und Differenz vs. Placebo |
||||||||
|
EVOLVE-1 |
177 |
–21,2 |
–6,3 [–9,5; –3,1]*** |
170 |
20,1 |
–5,2 [–8,4; –2,0]** |
345 |
–14,9 |
|
EVOLVE-2 |
202 |
–21,2 |
–9,2 [–12,6; –5,7]*** |
194 |
-20,2 |
–8,2 [–11,7; –4,7]*** |
374 |
–12,0 |
|
REGAIN |
254 |
–20,3 |
–8,7 [–16,4; –1,1]** |
258 |
-17,0 |
–5,5 [–13,1; –2,1] ns |
504 |
–11,5 |
*** p < 0,001; * p < 0,05 (p-Werte vs. Placebo; ohne Berücksichtigung multipler Testung).
LSM, KI, Odds-Ratio und p-Werte aus der primären Analyse bzw. präspezifizierten sekundären Analysen (MKT: Restricted Maximum Likelihood-based MMRM; MIDAS: Kovarianzanalyse; prozentuales Ansprechen: kategorielles Pseudo-Likelihood-based MMRM); statistische Methodik: s. [38]für EVOLVE-1, [37] für EVOLVE-2, [8] für REGAIN.
a 240 mg als Erhaltungsdosis nicht zugelassen.
b Modellbasierter Mittelwert; beim prozentualen Ansprechen ist der modellbasierte Prozentsatz dargestellt (statistische Methodik: s. [34] für EVOLVE-1, [33] für EVOLVE-2, [8] für REGAIN).
c Differenz vs. Placebo als modellbasierter Mittelwert; beim prozentualen Ansprechen ist das modellbasierte Odds-Ratio dargestellt.
GMB: Galcanezumab; KI: Konfidenzintervall; LSM: modellbasierter Mittelwert; MKT: Migränekopfschmerztage; MIDAS: Migraine Disability Assessment; MMRM: Mixed Model Repeated Measures; N: Anzahl der Patienten (Baseline); ns: nicht signifikant (p > 0,05)
Aus klinischer Sicht und seitens der Behörden gilt eine Reduktion der Migränekopfschmerztage von ≥ 50 % bei episodischer und von ≥ 30 % bei chronischer Migräne als relevante Verbesserung (in den GMB-Studien verwendete Definitionen: siehe Tab. 2) [35]. Eine ≥ 50%ige Reduktion der Migränekopfschmerztage erreichten mit 120 mg Galcanezumab/Monat in allen Studien signifikant mehr Patienten als mit Placebo (p < 0,001 vs. Placebo; Tab. 4). Eine sogar ≥ 75%ige Reduktion erreichten in EVOLVE-1 38,8 %, in EVOLVE-2 33,5 % (Placebo: 19,3 % bzw. 17,8 %; p < 0,001 vs. Placebo) und in REGAIN 7,0 % der mit 120 mg Galcanezumab/Monat behandelten Patienten (Placebo 4,5 %; p < 0,05 vs. Placebo). Eine Auswertung der gepoolten Daten von EVOLVE-1 und -2 zum Anteil der Patienten mit 100%iger Response während der 6-monatigen Doppelblindperiode ergab, dass mit 120 mg Galcanezumab/Monat 38,8 % der Patienten mindestens einen Monat lang, 21,8 % mindestens zwei Monate lang und 10,6 % der Patienten mindestens drei Monate lang gar keinen Migränekopfschmerztag hatten [28]. Auch die monatliche Zahl der Migränekopfschmerztage, an denen die Patienten eine Akutmedikation zur Kupierung von Migränen benötigten, ging in beiden Studien signifikant zurück (Tab. 4; p < 0,001 vs. Placebo); gleichzeitig besserten sich alle weiteren präspezifizierten sekundären Endpunkte, wie Lebensqualität (MSQ RF-R [Abb. 5], MSQ-Gesamtscore [13]) und Funktionsfähigkeit im Alltag (MIDAS) unter Galcanezumab signifikant mehr als unter Placebo (Tab. 4). Insbesondere besserte sich auch die Domäne des MSQ, die die emotionale Belastung bei Migräne abbildet (MSQ EF), sowohl für die episodische als auch die chronische Migräne signifikant (p < 0,001 vs. Placebo) [8, 13].
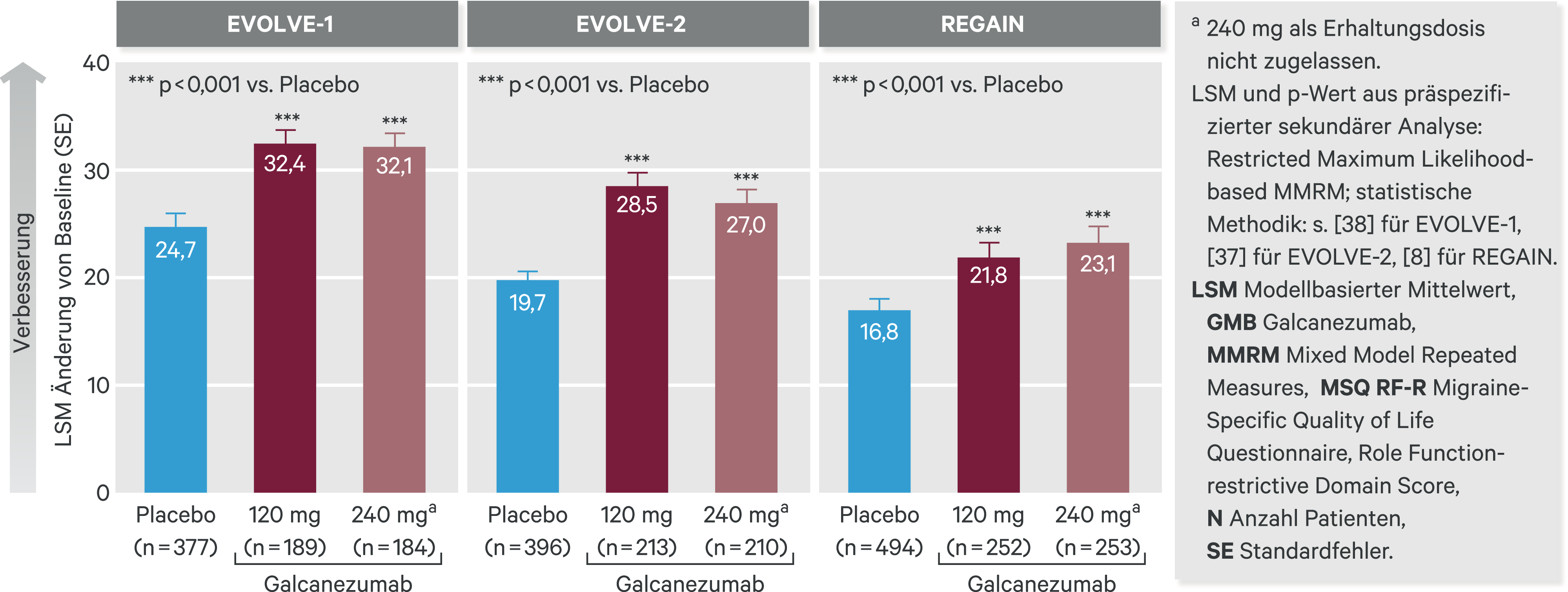
Abb. 5. Verbesserung der Lebensqualität (MSQ RF-R) bei monatlicher Gabe von Galcanezumab in den Phase-III-Studien EVOLVE und REGAIN
In der 9-monatigen offenen Periode von REGAIN erreichten Patienten, die in der Doppelblindperiode auf Placebo randomisiert gewesen waren, mit der ersten Gabe von Galcanezumab eine Verbesserung der Migränekopfschmerztage und Funktionsfähigkeit, die der der Patienten entsprach, die bereits in der Doppelblindperiode Galcanezumab erhalten hatten. In allen GMB-Gruppen nahm die mittlere Anzahl an Migränekopfschmerztagen über den gesamten Beobachtungszeitraum weiter ab, sodass sie nach der insgesamt 12-monatigen Behandlungsperiode um etwa 8 Tage reduziert war [9]. Dementsprechend verbesserte sich der MSQ RF-R-Score ebenfalls signifikant.
Praxisrelevante Zusatzanalysen
In Post-hoc-Analysen der EVOLVE- und REGAIN-Daten wurden einige besonders für den Praxisalltag relevante Fragestellungen untersucht. So zeigte eine Analyse der gepoolten EVOLVE-Daten, dass die Wirkung von Galcanezumab im Durchschnitt bereits wenige Tage nach Therapiebeginn eintritt [2]. Bei einem relevanten Anteil der Patienten mit episodischer oder chronischer Migräne, die nach einem Monat noch nicht oder nur minimal angesprochen haben, kann es bei Fortsetzen der Therapie noch zu einer relevanten Verbesserung kommen (Abb. 6) [33].
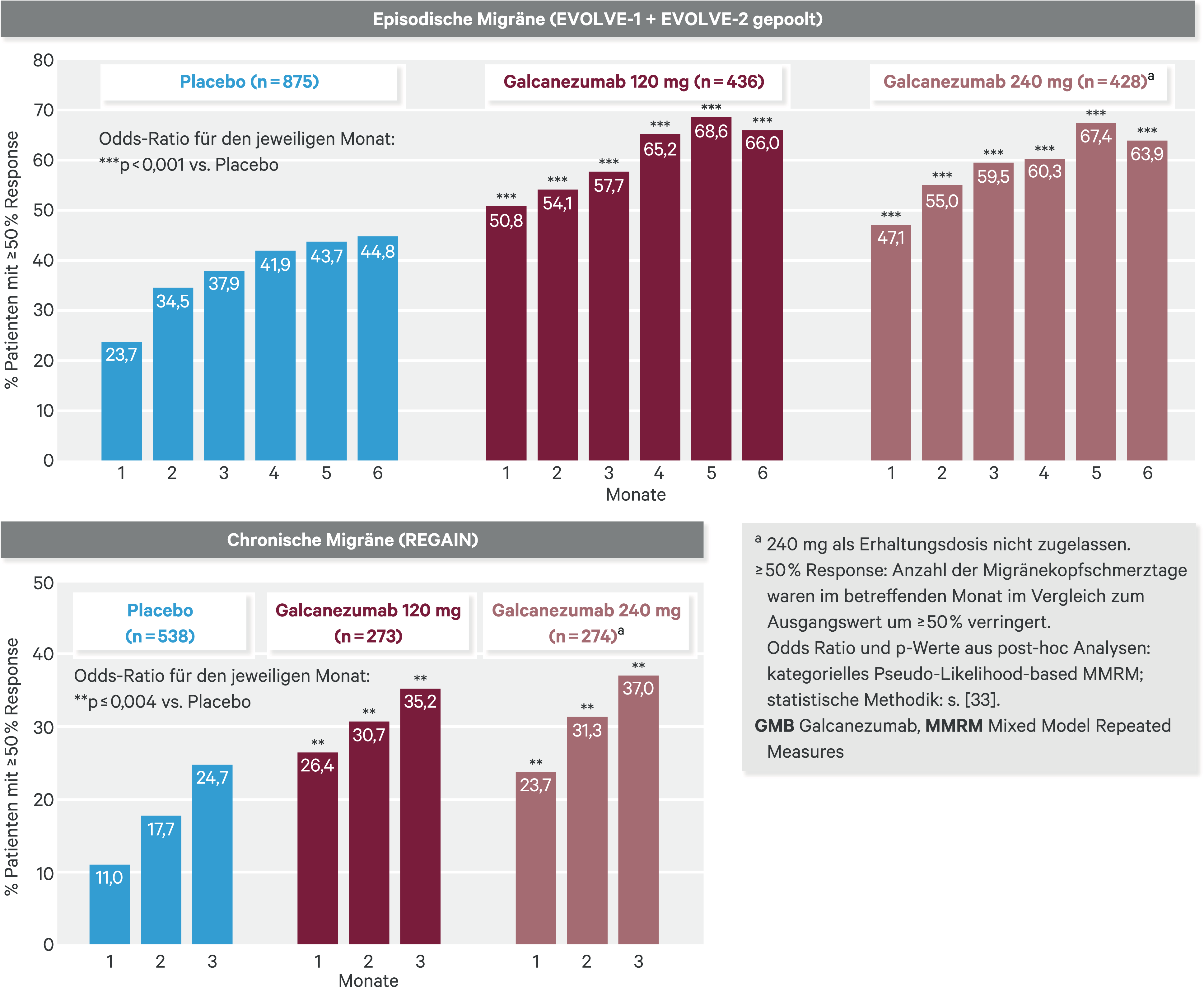
Abb. 6. Migräneprophylaxe mit Galcanezumab: Anteil der Patienten mit ≥ 50 %iger Reduktion der monatlichen Kopfschmerztage im Zeitverlauf, bei Patienten mit episodischer Migräne (EVOLVE) oder mit chronischer Migräne (REGAIN) [33]
Der Prozentsatz der Patienten, bei denen die Abnahme der Migränekopfschmerztage von ≥ 50 % über den gesamten Studienzeitraum erhalten blieb, war mit beiden Galcanezumab-Dosierungen höher als mit Placebo [4]. Außerdem war der Unterschied des Effekts von Galcanezumab im Vergleich zu Placebo deutlich größer, wenn die Patienten bereits andere Migräneprophylaktika angewendet hatten [3], was auf eine verringerte Erwartungshaltung hindeutet.
Etwa 5 % bzw. 14 % der Patienten aus EVOLVE-1 bzw. -2 und > 25 % der Patienten aus REGAIN waren in der Vergangenheit ohne Erfolg mit mindestens zwei Migräne-Prophylaktika vorbehandelt gewesen. Eine Post-hoc-Analyse mit gepoolten Daten genau dieser Patientengruppe aus den drei Studien zeigte, dass Galcanezumab auch bei diesen Patienten wirksam war: Mit 120 mg Galcanezumab sank die Zahl der monatlichen Migränekopfschmerztage in dieser Subpopulation bei episodischer Migräne um 3,5 Tage (Placebo 0,8 Tage) bzw. bei chronischer Migräne um 5,9 Tage (Placebo 1,4 Tage) (alle p < 0,001 vs. Placebo) [43].
Verträglichkeitsdaten
Die Daten zu unerwünschten Ereignissen aus den EVOLVE- und REGAIN-Studien sprechen insgesamt für eine gute Verträglichkeit der Migräneprophylaxe mit 120 mg Galcanezumab einmal monatlich nach einer Anfangsdosis von 240 mg (Tab. 5). Schmerzen an der Injektionsstelle waren das häufigste unerwünschte Ereignis (bis zu 16 % der Patienten), sie traten allerdings nicht häufiger auf als mit Placebo. Rötung, Juckreiz sowie nicht weiter spezifizierte Reaktionen an der Injektionsstelle waren in den Galcanezumab-Gruppen häufiger als mit Placebo. Die einzigen anderen unerwünschten Ereignisse mit einer Häufigkeit > 5 % pro Behandlungsgruppe waren Nasopharyngitis, Harnwegsinfekte und obere Atemwegsinfektionen, jeweils mit leicht erhöhter Häufigkeit in den Galcanezumab-Gruppen. Schwerwiegende unerwünschte Ereignisse traten mit Galcanezumab nur vereinzelt und nicht häufiger als unter Placebo auf (Tab. 5), außerdem betrafen sie verschiedene Organsysteme ohne ein erkennbares Muster. Zwei Cholelithiasis-Fälle in der EVOLVE-1-Placebo-Gruppe waren die einzigen, die in EVOLVE-1/-2 und REGAIN bei mehr als einem Patienten auftraten [8, 37, 38]. Laborwerte, Blutdruck und EKG-Parameter zeigten in keiner der Studien klinisch relevante Veränderungen.
Tab. 5. Verträglichkeitsdaten während der doppelblinden Behandlungsperiode in den Studien EVOLVE-1/-2 (6 Monate) und REGAIN (3 Monate)
|
EVOLVE-1 (6 Monate) |
EVOLVE-2 (6 Monate) |
REGAIN (3 Monate) |
|||||||
|
GMB 120 mg (n = 206) |
GMB 240 mga (n = 220) |
Placebo (n = 432) |
GMB 120 mg (n = 226) |
GMB 240 mga (n = 228) |
Placebo (n = 461) |
GMB 120 mg (n = 273) |
GMB 240 mga (n = 282) |
Placebo (n = 558) |
|
|
Übersicht |
|||||||||
|
≥ 1 UE |
135 (65,5) |
149 (67,7) |
261 (60,4) |
147 (65,0) |
163 (71,5) |
287 (62,3) |
159 (58,2) |
160 (56,7) |
279 (50,0) |
|
≥ 1 UE schwerwiegend |
6 (2,9) |
0 |
5 (1,2) |
5 (2,2) |
7 (3,1) |
5 (1,1) |
1 (0,4) |
4 (1,4) |
4 (0,7) |
|
≥ 1 UE mit Therapieabbruch |
7 (3,4) |
9 (4,1) |
10 (2,3) |
5 (2,2) |
9 (4,0) |
8 (1,7) |
1 (0,4) |
4 (1,4) |
6 (1,1) |
|
Reaktionen an der Einstichstelle (Häufigkeit ≥ 2,0 % pro Studie für GMB gesamt) |
|||||||||
|
Schmerz |
33 (16,0) |
45 (20,5) |
75 (17,4) |
21 (9,3) |
20 (8,8) |
39 (8,5) |
17 (6,2) |
20 (7,1) |
24 (4,3) |
|
Rötung |
10 (4,9) |
9 (4,1) |
11 (2,6) |
6 (2,7) |
7 (3,1) |
4 (0,9) |
4 (1,5) |
13 (4,6) |
5 (0,9) |
|
Juckreiz |
9 (4,4) |
10 (4,6) |
1 (0,2) |
6 (2,7) |
7 (3,1) |
0 |
0 |
7 (2.5) |
1 (0,2) |
|
Reaktion [nicht spezifiziert] |
7 (3,4) |
12 (5,5) |
4 (0,9) |
7 (3,1) |
18 (7. 9) |
0 |
8 (2,9) |
15 (5,3) |
10 (1,8) |
|
Häufigste sonstige UE (Häufigkeit ≥ 2,5 % pro Studie für GMB gesamt) |
|||||||||
|
Nasopharyngitis |
16 (7,8) |
6 (2,7) |
27 (6,3) |
19 (8,4) |
16 (7,0) |
41 (8,9) |
17 (6,2) |
9 (3,2) |
26 (4,7) |
|
Infektion der oberen Atemwege |
9 (4,4) |
15 (6,8) |
31 (7,2) |
13 (5,8) |
12 (5,3) |
16 (3,5) |
9 (3,3) |
9 (3,2) |
13 (2,3) |
|
Harnwegsinfekte |
8 (3,9) |
13 (5,9) |
15 (3,5) |
25 (5,5) |
16 (3,5) |
6 (2,2) |
4 (1,4) |
7 (1,3) |
|
|
Benommenheit |
6 (2,9) |
5 (2,3) |
11 (2,6) |
8 (3,5) |
7 (3,1) |
10 (2,2) |
6 (2,2) |
8 (2,8) |
20 (3,6) |
|
Sinusitis |
10 (4,9) |
8 (3,6) |
13 (3,0) |
9 (2,0) |
13 (2,8) |
4 (1,5) |
8 (2,8) |
5 (0,9) |
|
|
Übelkeit |
5 (2,4) |
8 (3,6) |
15 (3,5) |
7 (1,5) |
15 (3,3) |
9 (3,3) |
8 (2,8) |
23 (4,1) |
|
|
Müdigkeit |
5 (2,4) |
5 (2.3) |
12 (2,8) |
6 (2,7) |
5 (2,2) |
12 (2,6) |
6 (2,2) |
6 (2,1) |
10 (1,8) |
|
Rückenschmerz |
5 (2,4) |
7 (3,2) |
6 (1,4) |
7 (1,5) |
20 (4,3) |
9 (3,3) |
2 (0,7) |
14 (2,5) |
|
|
Influenza/Influenza-ähnlich |
5 (2,4) |
4 (1,8) |
5 (1,2) |
3 (1,3) |
10 (4,4) |
14 (3,0) |
5 (1,8)b |
4 (1,4)b |
3 (0,5)b |
Dargestellt sind Anzahl (%) der Patienten mit UE unter der Therapie.
a 240 mg als Erhaltungsdosis nicht zugelassen
b Influenza-ähnliche Erkrankungen
GMB: Galcanezumab; UE: unerwünschtes Ereignis
Antikörper gegen Galcanezumab wurden in den verschiedenen Studien bei 5,9 % bis 11,2 % der teilnehmenden Patienten bereits vor der ersten GMB-Injektion nachgewiesen. Unter Therapie neu auftretende Antikörper gegen Galcanezumab – mehrheitlich auch neutralisierend – wurden zwar bei 3,5 % bzw. 8,6 % der in EVOLVE-1 bzw. -2 über sechs Monate und bei 2,7 % der in REGAIN über drei Monate mit 120 mg GMB/Monat behandelten Patienten nachgewiesen, sie hatten jedoch keine Auswirkung auf die Wirksamkeit oder Verträglichkeit von Galcanezumab [8, 37, 38]. Dabei ist zu berücksichtigen, dass der verwendete Antikörpertest eine deutlich höhere Sensitivität als üblich hatte [24].
In der offenen Studie zur Sicherheit von Galcanezumab über 12 Monate schlossen über beide Dosierungen 77,8 % der Patienten die Studie vollständig ab. Es zeigten sich hier keine neuen Aspekte bezüglich der Verträglichkeit. Die mittlere Anzahl der Migränekopfschmerztage nahm in der 120-mg-Gruppe von 9,72 (Standardabweichung 5,82) um 5,61 Tage ab (modellbasierter Mittelwert) [39].
Insgesamt zeigte die 120-mg-Dosis einmal monatlich eine ähnliche Wirksamkeit, aber eine etwas geringere Rate unerwünschter Ereignisse als die 240-mg-Dosis. Die Zulassung der EMA erfolgte daher für die Erhaltungsdosis von 120 mg (mit einer Anfangsdosierung von 240 mg bei der ersten Gabe) [22].
Diskussion
Drei Placebo-kontrollierte Phase-III-Studien sowie eine offene 12-Monatsstudie mit insgesamt mehr als 3100 Patienten (davon ca. 1700 mit 120 mg oder 240 mga GMB behandelt) bestätigten die Wirksamkeit von Galcanezumab in der Migräneprophylaxe sowohl bei episodischer als auch bei chronischer Migräne. Auch bei Patienten mit Medikamentenübergebrauch und bei Patienten, die in der Vergangenheit ohne Erfolg mit mindestens zwei Migräne-Prophylaktika behandelt worden waren, war Galcanezumab Placebo signifikant überlegen [43]. Sowohl die monatlichen Migränekopfschmerztage insgesamt als auch die Migränekopfschmerztage mit Migräne-Akuttherapie waren im Vergleich zu Placebo signifikant verringert (p < 0,001). Die Verbesserung war klinisch relevant: Für beide Gruppen waren die präspezifizierten 50%- und 75%-Responderraten für Galcanezumab signifikant höher als für Placebo. Bei der episodischen Migräne traf dies auch auf die 100%-Responderraten in den jeweiligen Monaten zu. Durchschnittlich hatten Galcanezumab-behandelte Patienten monatlich zwei Migränekopfschmerztage weniger als die Placebo-Gruppe sowie absolut vier bis fünf Migränekopfschmerztage weniger, einhergehend mit einer Verbesserung des emotionalen Befindens (MSQ EF) und der Funktionsfähigkeit im Alltag (MSQ R-FR, MIDAS). Der mittlere Gewinn von 24 Tagen ohne Migränekopfschmerz pro Jahr ist auch aus gesundheitsökonomischer Sicht relevant, denn oft sind die Patienten während der Migräneattacke arbeitsunfähig oder in ihrer Leistungsfähigkeit deutlich gemindert und nicht in der Lage, sich um ihre privaten Belange zu kümmern [12, 17].
Galcanezumab wirkt innerhalb weniger Tage nach Therapiebeginn [2] und damit deutlich schneller als konventionelle Prophylaktika [10]. Arzt und Patient erhalten daher früh im Therapieverlauf einen ersten Eindruck, ob die Prophylaxe mit Galcanezumab Erfolg verspricht. Ein relevanter Anteil der Patienten, die nach einem Monat noch nicht auf die Therapie ansprechen, kann von einer Fortführung der Therapie noch profitieren [33]. Die therapeutischen Effekte halten auch über 12 Monate an, wie eine offene, primär zur Untersuchung der Verträglichkeit angelegte Langzeitstudie zeigen konnte [39].
Die Abbruchraten waren in allen Studien niedrig und lagen für Galcanezumab unterhalb der für Placebo; weniger als 5 % der Patienten brachen die Prophylaxe mit Galcanezumab nebenwirkungsbedingt ab. Diese Daten lassen für die Praxis auf eine gute Persistenz hoffen, denn hier setzen bisher etwa 50 % der Patienten mit chronischer Migräne die derzeit vorhandenen Prophylaktika innerhalb von sechs Monaten wieder ab [6, 10, 30], oft noch bevor sie den vollen Behandlungseffekt mit diesen Wirkstoffen erreichen konnten.
Galcanezumab zeigte eine gute Verträglichkeit, die in allen Phase-II- und -III-Studien bestätigt wurde. Reaktionen an der Einstichstelle (≥ 10 % der Patienten) waren die häufigsten unerwünschten Ereignisse im Zusammenhang mit der Therapie. Bei den wenigen schwerwiegenden unerwünschten Ereignissen wurde kein konsistentes Muster identifiziert.
Da CGRP auch ein potenter Vasodilatator kleiner Gefäße ist, könnte theoretisch bei einer Behandlung mit einem Antikörper gegen CGRP bei Patienten mit kardiovaskulären Erkrankungen im Falle einer Minderperfusion, beispielsweise durch eine Gefäßstenose, ein CGRP-vermittelter Kompensationsmechanismus beeinträchtigt und damit die Folgen kardiovaskulärer Ereignisse verstärkt werden. Allerdings wurde ein solcher Effekt weder in vitro noch in vivo weder mit Galcanezumab noch mit anderen CGRP-Antikörpern [41] beobachtet. Auch bleibt unklar, ob aufgrund der Expression von CGRP im Darm ein erhöhtes Risiko für Patienten mit entzündlichen Darmerkrankungen besteht, wenn sie CGRP-Antikörper anwenden. Hier müssen die Effekte in der klinischen Anwendung engmaschig beobachtet werden. Die Bildung von Autoantikörpern gegen Galcanezumab war in keiner der Phase-II- und -III-Studien mit Nebenwirkungen oder einer Minderung der Wirksamkeit verbunden.
Zusammenfassend sind die Daten der Placebo-kontrollierten Studien mit Galcanezumab vielversprechend. Neben weiteren Studien werden vor allem die kommenden Erfahrungen aus der Praxis zeigen, wie sich Galcanezumab als ein Repräsentant der neuen CGRP-Antikörper-Klasse in der Migräneprophylaxe bei einer breiteren Patientenpopulation außerhalb von klinischen Studien bewährt.
Fazit für die Praxis
- Der CGRP-Antikörper Galcanezumab greift über die Inaktivierung des Neurotransmitters CGRP gezielt in die Migränepathophysiologie ein.
- Drei Placebo-kontrollierte Zulassungsstudien und eine offene Langzeitstudie mit insgesamt über 3100 Patienten belegen, dass Galcanezumab einmal monatlich s. c. (Anfangsdosis 240 mg, danach 120 mg/Monat) eine wirksame Prophylaxe bei episodischer und chronischer Migräne ermöglicht.
- Erste Effekte treten binnen einer Woche ein; die monatlichen Migränekopfschmerztage gingen in den Studien signifikant zurück, Lebensqualität und Funktionsfähigkeit im Alltag verbesserten sich, unter anderem auch bei Patienten mit Medikamentenübergebrauch oder Vorbehandlung mit konventionellen Prophylaktika.
- Die Verträglichkeit war in allen Studien gut; Reaktionen an der Einstichstelle waren die häufigsten Nebenwirkungen (≥ 10 %); das Fehlen beispielsweise kardiovaskulärer Effekte in den Studienpopulationen muss durch Erfahrungen in der Praxis bestätigt werden.
- Die Abbruchraten waren numerisch niedriger als mit Placebo (nebenwirkungsbedingt < 5 %), was in der Praxis auf eine verbesserte Persistenz hoffen lässt.
- Galcanezumab ist von der EMA zur Migräne-Prophylaxe bei erwachsenen Patienten mit mindestens vier Migränetagen pro Monat zugelassen und erstattungs- und verordnungsfähig.
- Für die Verordnung gilt das Wirtschaftlichkeitsgebot nach § 12 SGB V. Preislich liegen die CGRP-Antikörper als neu und spezifisch entwickelte Wirkstoffe über denen der herkömmlichen Prophylaktika. Galcanezumab (Stand Juli 2019) bewegt sich derzeit in dem für monoklonale CGRP-Antikörper bekannten Rahmen.
Danksagung
Für die Unterstützung bei der Erstellung des Manuskripts danken wir K. Helsberg, Trilogy Writing and Consulting GmbH, Frankfurt am Main.
Die Studien und die Manuskripterstellung wurden unterstützt von der Lilly Deutschland GmbH, Bad Homburg.
Abkürzungen
|
CGRP |
Calcitonin gene-related peptide |
|
CLR |
Calcitonin Receptor-like Receptor |
|
CTR |
Calcitonin-Rezeptor |
|
EMA |
European Medicines Agency |
|
GMB |
Galcanezumab |
|
ICHD-3β |
International Classification of Headache Disorders 3 Beta-Version |
|
IgG4 |
Immunglobulin G4 |
|
ITT |
Intention-to-treat |
|
LSM |
Modellbasierter Mittelwert (least square mean) |
|
MHD |
Migraine headache day |
|
MIDAS |
Migraine Disability Assessment Test |
|
MKT |
Migränekopfschmerztage |
|
MSQ EF |
Migraine Specific Quality-of-Life Questionnaire, Domäne “role function-restrictive” |
|
MSQ RF-R |
Migraine Specific Quality-of-Life Questionnaire, Domäne “emotional function” |
|
N |
Anzahl der Patienten |
|
PK |
Pharmakokinetik |
|
RAMP |
Receptor activity-modifying protein |
|
s. c. |
subkutan |
|
SE |
Standard Error (Standardfehler) |
|
SUE |
Schwerwiegendes unerwünschtes Ereignis |
|
UE |
Unerwünschtes Ereignis |
a 240 mg als Erhaltungsdosis nicht zugelassen
Interessenkonflikterklärung
S. Kraemer und K. Engel sind Angestellte der Lilly Deutschland GmbH, Bad Homburg, Deutschland. S. Kraemer besitzt Aktien von Eli Lilly and Company.
T. Jürgens berichtet Vortragstätigkeiten und/oder Teilnahme an Advisory Boards für die folgenden Firmen: Autonomic Technologies, Inc., Desitin, Lilly Deutschland, Novartis, Pharmallergan und TEVA.
Literatur
1. Allergan Pharmaceuticals. Fachinformation BOTOX® https://www.fachinfo.de/pdf/020408 (Zugriff am 14.02.2019).
2. Aurora S, Detke HC, Millen BA. Rapid onset of effect of galcanezumab for the prevention of episodic migraine: Post-hoc analyses of two phase 3 studies. Abstract. Präsentiert: 60th Annual Scientific Meeting of the American Headache Society, San Francisco, USA, 28. Juni – 1. Juli 2018; Abstract IOR05.
3. Aurora S, Ruff D, Zhang Q, Pearlman E. Factors associated with significant reduction in migraine headache days: A post hoc analysis of phase 3 placebo-controlled trials of patients with episodic and chronic migraine treated with galcanezumab. Präsentiert: 60th Annual Scientific Meeting of the American Headache Society, San Francisco, USA, 28. Juni – 1. Juli 2018; Abstract PS26.
4. Aurora S, Zhang Q. Persistence of effect of galcanezumab in patients with episodic or chronic migraine: Phase 3, randomized, double-blind, placebo-controlled EVOLVE-1, 22 and REGAIN studies. Abstract. Präsentiert: 60th Annual Scientific Meeting of the American Headache Society, San Francisco, USA, 28. June - 1. July 2018; Abstract PS46.
5. Benschop RJ, Collins EC, Darling RJ, Allan BW, et al. Development of a novel antibody to calcitonin gene-related peptide for the treatment of osteoarthritis-related pain. Osteoarthritis Cartilage 2014;22:578–85.
6. Berger A, Bloudek LM, Varon SF, Oster G. Adherence with migraine prophylaxis in clinical practice. Pain Pract 2012;12:541–9.
7. Brandes JL, Saper JR, Diamond M, Couch JR, et al. Topiramate for migraine prevention: A randomized controlled trial. JAMA 2004;291:965–73.
8. Detke HC, Goadsby PJ, Wang S, Aurora SK. Galcanezumab in chronic migraine: the randomized, double-blind, placebo-controlled REGAIN study. Neurology 2018;91:e2211–21.
9. Detke HC, Li LQ, Wang S, Friedman DI, et al. One-year treatment with galcanezumab in Patients with chronic migraine: Results from the open-label phase of the REGAIN study. Abstract. 17th Biennial Migraine Trust International Symposium, London, 6.–9. September 2018; Abstract MTIS 2018–178.
10. Diener HC, Gaul C, Holle-Lee D, Lazaridis L, et al. Neues bei Kopfschmerzen. Fortschr Neurol Psychiatr 2017;85:352–65.
11. Dodick DW, Goadsby PJ, Spierings EL, Scherer JC, et al. Safety and efficacy of LY2951742, a monoclonal antibody to calcitonin gene-related peptide, for the prevention of migraine: a phase 2, randomized, double-blind, placebo-controlled study. Lancet Neurol 2014;13:885–92.
12. Eli Lilly and Company (2018) Migraine Impact Report. https://www.multivu.com/players/English/8259051-lilly-migraine-impact-report/ (Zugriff am 14.02.2019).
13. Ford J, Ayer D, Zhang Q, Carter J, et al. Changes in patient functioning and disability: Results from two phase 3 double-blind placebo-controlled clinical trials evaluating galcanezumab for episodic migraine prevention (EVOLVE-1 and EVOLVE-2). Abstract. Präsentiert: 60th Annual Scientific Meeting of the American Headache Society, San Francisco, USA, 28. Juni – 1. Juli 2018; Abstract PS37.
14. Gemeinsamer Bundesausschuss (2018) Arzneimittelrichtlinie. Anlage VI: Verordnungsfähigkeit von zugelassenen Arzneimitteln in nicht zugelassenen Anwendungsgebieten. https://www.g-ba.de/informationen/richtlinien/anlage/15/ (Zugriff am 14.02.2019).
15. Giamberardino MA, Affaitati G, Curto M, Negro A, et al. Anti-CGRP monoclonal antibodies in migraine. Current Perspectives Intern Emerg Med 2016;11:1045–57.
16. Goadsby PJ, Holland PR, Martins-Oliveira M, Hoffmann J, et al. Pathophysiology of migraine: A disorder of sensory processing. Physiol Rev 2017;97:553–622.
17. Göbel H. Migräne. Diagnostik – Therapie – Prävention. Kapitel 2.8: Repräsentative Daten zur Migräne in Deutschland. Heidelberg: Springer Verlag, 2012.
18. International Headache Society. The International Classification of Headache Disorders, 3rd edition (beta version). Cephalalgia 2013;33:629–808. http://beta.ichd-3.org/ (Zugriff am 14.02.2019).
19. International Headache Society. The International Classification of Headache Disorders, 3rd edition. Cephalalgia 2018;38:1–211. https://www.ichd-3.org/ (Zugriff am 14.02.2019).
20. Kielbasa W, O’Brien L, Moser B, Quinlan T. Assessment of pharmacokinetics, target engagement and immunogenicity in patients with migraine administered galcanezumab, an anti-CGRP antibody. Abstract. 60th Annual Scientific Meeting of the American Headache Society, San Francisco, USA, 28. Juni – 1. Juli 2018; Abstract IOR09.
21. Kommission Leitlinien der Deutschen Gesellschaft für Neurologie (DGN) in Zusammenarbeit mit der Deutschen Migräne- und Kopfschmerzgesellschaft (DMKG) (Hrsg). Leitlinien für Diagnostik und Therapie in der Neurologie: Therapie der Migräneattacke und Prophylaxe der Migräne. http://www.awmf.org/uploads/tx_szleitlinien/030-057l_S1_Migraene-Therapie_2018-04_1.pdf (Zugriff am 14.02.2019).
22. Lilly Deutschland GmbH. Emgality (Galcanezumab) Fachinformation, Stand November 2018.
23. Lipton RB, Bigal ME, Diamond M, Freitag F, et al. Migraine prevalence, disease burden, and the need for preventive therapy. Neurology 2007;68:343–9.
24. Martinez JM, Garces S, Anglin G, Hodsdon M, et al. Immunogenicity findings from phase 3 galcanezumab trials in patients with episodic or chronic migraine. Abstract. 12th European Headache Federation Congress, Florence, 28.–30. September 2018; Poster P25.
25. Messlinger K, Holle-Lee D, Diener HC. Bedeutung des Neuropeptids CGRP bei primären Kopfschmerzen. Arzneimitteltherapie 2017;35:272–81.
26. Messlinger K, Lennerz JK, Eberhardt J, Fischer MJ, et al. CGRP and NO in the trigeminal system: Mechanisms and role in headache generation. Headache 2012;52:1411–27.
27. Monteith D, Collins EC, Vandermeulen C, Van Hecken A, et al. Safety, tolerability, pharmacokinetics, and pharmacodynamics of the CGRP binding monoclonal antibody LY2951742 (Galcanezumab) in healthy volunteers. Front Pharmacol 2017;8:740.
28. Nagy AJ, Pearlman EP, Ruff RD, Day K, et al. 100 % response rate to galcanezumab in patients with episodic migraine: Randomized, double-blind, placebo-controlled studies. Abstract. 17th Biennial Migraine Trust International Symposium, London, 6.-9. September 2018; Abstract MTIS 2018–081.
29. Oakes TMM, Skljarevski V, Zhang Q, Kielbasa W, et al. Safety of galcanezumab in patients with episodic migraine: A randomized placebo-controlled dose-ranging phase 2b study. Cephalalgia 2018;38:1015–25.
30. Reuter U. A review of monoclonal antibody therapies and other preventative treatments in migraine. Headache 2018;58(Suppl 1):48–59.
31. Russell FA, King R, Smillie SJ, Kodji X, et al. Calcitonin gene-related peptide: Physiology and pathophysiology. Physiol Rev 2014;94:1099–142.
32. Schulte LH, May A. Of generators, networks and migraine attacks. Curr Opin Neurol 2017;30:241–5.
33. Sheena K, Aurora MD, Zhang Q, Stauffer VL. Persistence of effect of galcanezumab in patients with episodic or chronic migraine: Phase 3, randomized, double-blind, placebo-controlled EVOLVE-1, EVOLVE-2, and REGAIN studies. Abstract. 12th European Headache Federation Congress, Florenz, 28.–30. September 2018; Vortrag 018.
34. Silberstein S, Lenz R, Xu C. Therapeutic monoclonal antibodies: What headache specialists need to know. Headache 2015;55:1171–82.
35. Silberstein S, Tfelt-Hansen P, Dodick DW, Limmroth V, et al. Guidelines for controlled trials of prophylactic treatment of chronic migraine in adults. Cephalalgia 2008;28:484–95.
36. Skljarevksi V, Oakes TM, Zhang Q, Ferguson MB, et al. Effect of different doses of galcanezumab vs placebo for episodic migraine prevention: A randomized clinical trial. JAMA Neurol 2018;75:187–93.
37. Skljarevksi V, Matharu M, Millen BA, Ossipov MH, et al. Efficacy and safety of galcanezumab for the prevention of episodic migraine: Results of the EVOLVE-2 phase 3 randomized controlled clinical trial. Cephalalgia 2018;38:1442–54.
38. Stauffer VL, Dodick DW, Zhang Q, Carter JN, et al. Evaluation of galcanezumab for the prevention of episodic migraine. Results from the EVOLVE-1 study, a randomized phase 3 placebo-controlled clinical trial. JAMA Neurol 2018;75:1080–8.
39. Stauffer VL, Sides R, Camporeale A, Skljarevksi V, et al. A phase 3, long-term, open-label safety study of self-administered galcanezumab injections in patients with migraine. Abstract. Cephalalgia 37 (IS), pp330. Präsentiert: IHC 2017 (PO-01–184).
40. Woldeamanuel YW, Cowan RP. Migraine affects 1 in 10 people worldwide featuring recent rise: A systematic review and meta-analysis of community-based studies involving 6 million participants. J Neurol Sci 2017;372:307–15.
41. Yeh JF, Akinci A, Al Shaker M, Chang MH, et al. Monoclonal antibodies for chronic pain: A practical review of mechanisms and clinical applications. Mol Pain 2017;13:1–14.
42. Yoon MS, Katsarava Z, Obermann M, Fritsche G, et al. Prevalence of primary headaches in Germany: Results of the German headache consortium study. J Headache Pain 2012;13:215–23.
43. Zhang Q, Ruff DD, Pearlman EM, Govindan S, et al. Efficacy of galcanezumab in patients who failed to respond to preventives previously: Results from EVOLVE-1, EVOLVE-2 and REGAIN studies. Abstract. Neurology 2018;90(Suppl 15):S20.004. Präsentiert: AAN 2018.
Priv.-Doz. Dr. med. T. P. Jürgens, Universitätsmedizin Rostock, Zentrum für Nervenheilkunde, Klinik und Poliklinik für Neurologie, Gehlsheimer Straße 20, 18147 Rostock, E-Mail: TimPatrick.Juergens@med.uni-rostock.de
Dr. phil. nat. Kerstin Engel, Dr. med. Susanne Kraemer, Lilly Deutschland GmbH, Bad Homburg
Galcanezumab for migraine prevention: Mode of action and overview of clinical study data
Background: Galcanezumab (GMB) is a humanized monoclonal antibody that was specifically developed for migraine prophylaxis and binds selectively to the neuropeptide CGRP (calcitonin gene-related peptide).
Objectives: Presentation of mode of action and key data from clinical studies.
Methods: In 3 registration trials, patients with episodic migraine (EVOLVE-1 and -2, n = 862 and n = 922) were treated for 6 months, and patients with chronic migraine (REGAIN, n = 1117) were treated in the double-blind period for 3 months with GMB or placebo 1x/month subcutaneously (sc). Primary endpoint was the mean reduction of monthly migraine headache days (MHDs) from baseline. Key secondary endpoints included response rates, reduction of monthly MHDs requiring acute medication, migraine disability assessment and quality of life. Additionally, 12-month data from an open-label long-term study (n = 270) and post hoc analyses on relevant clinical questions are presented.
Results: In patients with episodic (EVOLVE-1/-2) or chronic (REGAIN) migraine, GMB 120 mg reduced monthly MHDs by a mean of 4.7/4.3 or 4.8 days, respectively (placebo 2.8/2.6 or 2.7 days; all p < 0.001 vs. placebo). All prespecified secondary endpoints also improved in both populations. GMB was also effective in patients with prior use of ≥ 2 other prophylactic agents (post-hoc analysis). Discontinuation rates of GMB were numerically lower than for placebo. Tolerability was good in all studies with injection site reactions as the most common adverse events.
Conclusion: GMB injected sc once monthly significantly reduced monthly MHDs and improved quality of life in patients with both episodic and chronic migraine, and was associated with low discontinuation rates and good tolerability.
Key words: migraine, headache, CGRP, antibody, galcanezumab
Psychopharmakotherapie 2019; 26(05)
