Christoph U. Correll, Berlin
Warum Partialagonisten?
Patienten, die an Schizophrenie erkrankt sind, müssen ihre Medikation meist ihr Leben lang einnehmen, um Rückfälle zu vermeiden [10, 17]. Die Ziele von neu diagnostizierten Patienten sind dabei vor allem weniger Krankheitssymptome, klares Denken, weniger Krankenhausaufenthalte, und ein verbessertes Funktionsniveau [3]. Unter den Zielen der Patienten finden sich neben der Vermeidung von Rückfällen und akuten Symptomen der Schizophrenie auch die Vermeidung von Nebenwirkungen wie Schlaflosigkeit und Ruhelosigkeit, aber auch Abgeschlagenheit [25]. Da die Freiheit von Rückfällen nur durch eine hohe Adhärenz gewährleistet ist [17], sind die Verträglichkeit und vorteilhaftes Nebenwirkungsprofil für die Psychopharmakotherapie besonders wichtig. Nebenwirkungen stellen nämlich mitunter einen wichtigen Grund für Nichtadhärenz dar [14].
Historisch standen ab Mitte der 50er-Jahre zunächst Antipsychotika der ersten Generation, heute auch als „Typika“ bezeichnet, zur Verfügung. Diese entfalten ihre Wirkung hauptsächlich über eine Blockade der dopaminergen D2-Rezeptoren [45]. Dies führt zwar zu einer Reduktion der Positivsymptome der Schizophrenie, aber auch zu starken Nebenwirkungen, vor allem extrapyramidalmotorischer Natur [28]. Es wurden in der Folge Antipsychotika der zweiten Generation entwickelt, auch als „Atypika“ bezeichnet, vor allem gekennzeichnet durch weniger extrapyramidalmotorische Nebenwirkungen. Dennoch treten auch unter den heute verfügbaren Antipsychotika zahlreiche unerwünschte Wirkungen auf. Zu den typischen Problemen gehören Akathisie und Parkinsonismus, aber vor allem auch Gewichtszunahme und metabolische Nebenwirkungen sowie Nebenwirkungen im Zusammenhang mit Prolactinerhöhung [6, 7, 28]. Außerdem beeinträchtigen sowohl sedierende Nebenwirkungen, wie Schläfrigkeit, als auch aktivierende Nebenwirkungen, wie Unruhe und Schlaflosigkeit, die Patienten [14]. Auch kardiale Nebenwirkungen, wie QTc-Verlängerungen, wurden beobachtet [21].
Antipsychotika der ersten und zweiten Generation haben jeweils die Eigenschaft, D2-Rezeptoren zu blockieren [45]. Die Dopaminhypothese der Schizophrenie besagt, dass bei Schizophrenie eine hyperdopaminerge Funktionsstörung in der mesolimbischen Bahn vorliegt. Die übermäßige Stimulation der D2-Rezeptoren führt zur für Schizophrenie charakteristischen Positivsymptomatik mit Wahnvorstellungen und Halluzinationen sowie formalen Denkstörungen. Deshalb bringt eine Blockade der D2-Rezeptoren eine Besserung dieser Symptome mit sich. Doch von dieser Blockade sind auch weitere dopaminerge Bahnen betroffen: Unter anderem kann das Belohnungssystem betroffen sein, was zu mehr negativen Symptomen, wie Alogie, Anhedonie, Amotivation und Affektverflachung, führen kann. Die nigrostriatale Bahn, verantwortlich für Bewegung, kann ebenfalls beeinträchtigt sein. Die möglichen Folgen der Blockade von D2-Rezeptoren im nigrostriatalen Bereich sind Parkinsonismus und tardive Dyskinesie. Außerdem kann eine Blockade der tuberoinfundibulären Bahn zu Hyperprolaktinämie führen. Ein Ansatz zur Lösung des Problems, dass die erwünschte Dopaminblockade in einem Hirnbereich auch andere Funktionsbereiche in Mitleidenschaft zieht, was wiederum zu unerwünschten Wirkungen führt, war die Entwicklung von Dopamin-D2-Partialagonisten mit geringer intrinsischer Aktivität am D2-Rezeptor.
Brexpiprazol
Derzeit sind insgesamt drei Dopamin-D2-Partialagonisten zur Behandlung von Schizophrenie verfügbar: Aripiprazol, Brexpiprazol und Cariprazin. Aripiprazol ist bereits seit 2002 zugelassen [39], zu dieser Substanz ist daher viel Literatur verfügbar. Neu hinzugekommen sind Cariprazin und Brexpiprazol. Cariprazin wurde in diesem Periodikum bereits vorgestellt [47].
Brexpiprazol wurde zunächst 2015 in den USA zugelassen, und zwar für die Behandlung der Schizophrenie und als adjuvante Therapie zusammen mit einem Antidepressivum bei behandlungsresistenter Depression [40]. Die Indikation als Adjuvans für behandlungsresistente Depression wird besprochen in [2, 15, 48]. Seit 2018 ist Brexpiprazol auch in der EU und der Schweiz zugelassen (https://www.ema.europa.eu/en/medicines/human/EPAR/rxulti; http://www.swissmedicinfo.ch/, Fachinformation Rexulti). Es verbindet eine Wirksamkeit, die vergleichbar ist mit etablierten Antipsychotika der zweiten Generation, mit einem vorteilhaften Nebenwirkungsprofil. In diesem Artikel soll Brexpiprazol anhand seiner Zulassungsstudien vorgestellt werden, dabei wird allerdings nur auf die in Europa zugelassene Indikation Schizophrenie eingegangen.
Brexpiprazol wirkt als partieller Agonist am dopaminergen D2-Rezeptor und am serotonergen 5-HT1A-Rezeptor sowie als Antagonist an den 5-HT2A- und noradrenergen Alpha1B- und Alpha2C-Rezeptoren [30, 31]. Anders als bei allen anderen derzeit verfügbaren Antipsychotika ist die Affinität für alle diese Rezeptoren ähnlich, was bedeutet, dass alle ihre Wirkung entfalten können [13]. Die Wirksamkeit, Sicherheit und Verträglichkeit von Brexpiprazol zur Behandlung von Schizophrenie wurde durch ein Studienprogramm belegt, das Akut- und Langzeitstudien umfasste.
Die Akutstudien: BEACON und VECTOR
In Kurzzeitstudien wurde die Wirksamkeit, Sicherheit und Verträglichkeit von Brexpiprazol bei akuter Exazerbation der Schizophrenie untersucht. Die Studien BEACON [24] und VECTOR [12] waren multizentrische, doppelverblindete, randomisierte, kontrollierte Studien über sechs Wochen mit festgelegten Dosen an Brexpiprazol. In diese Studien wurden insgesamt 1310 erwachsene Patienten (18–65 Jahre) mit Schizophrenie eingeschlossen, die unter einer akuten psychotischen Exazerbation litten. In der VECTOR-Studie wurden die Patienten auf Brexpiprazol 0,25 mg/Tag, 2 mg/Tag, 4 mg/Tag oder Placebo (1 : 2 : 2 : 2) randomisiert. In der BEACON-Studie wurden die Patienten auf Brexpiprazol 1 mg/Tag, 2 mg/Tag, 4 mg/Tag oder Placebo (2 : 3 : 3 : 3) randomisiert. Die Dosierungen von 0,25 und 1 mg sollten dazu dienen, die Untergrenzen einer wirksamen Dosis zu evaluieren – Phase-II-Studien hatten Hinweise erbracht, dass 1 mg die niedrigste wirksame Tagesdosis sein dürfte, von der 0,25-mg-Dosis wurde keine Wirksamkeit erwartet. In allen Studien wurde Brexpiprazol in den 2-mg- und 4-mg-Gruppen zunächst mit 1 mg begonnen und am 4. Tag auf 2 mg erhöht, mit einer weiteren Dosiserhöhung auf 4 mg am Tag 8 in der 4-mg-Gruppe.
Wirksamkeit
In beiden Akutstudien war der primäre Endpunkt die Veränderung im Gesamtscore der Positive and Negative Syndrome Scale (PANSS) von Baseline bis Woche 6. Er wurde mithilfe eines gemischten Modells für Messwiederholungen (Mixed model for repeated measures, MMRM) analysiert. Weitere Maße für die Wirksamkeit waren verschiedene PANSS-Subskalen, Clinical Global Impression – Severity of Illness (CGI-S), Clinical Global Impression – Improvement (CGI-I), und die Personal and Social Performance (PSP)-Skala [35]. Auch sie wurden mithilfe des MMRM analysiert.
Die Wirksamkeitspopulation umfasste jeweils alle Patienten, die mindestens eine Dosis der Studienmedikation erhalten hatten und für die ein Baseline-Wert sowie mindestens ein Wert nach Baseline auf den Wirksamkeitsskalen festgestellt worden war. In einer nachfolgenden Analyse wurden die Daten der 2-mg/Tag- und 4-mg/Tag-Gruppen sowie der Placebo-Gruppen aus beiden Studien jeweils kombiniert [11].
Die Patienten, die in die Metaanalyse [11] eingeschlossen wurden, waren auf Brexpiprazol 2 mg/Tag (n = 368), 4 mg/Tag (n = 364) oder Placebo (n = 368) randomisiert (Tab. 1). Aus den kombinierten Brexpiprazol-Gruppen schlossen mehr Patienten die Studien ab als aus den Placebo-Gruppen (2 mg/Tag: 68,8 %; 4 mg/Tag: 69,0 %; Placebo: 61,7 %). Die Wirksamkeitspopulationen umfassten je 359 Patienten für beide kombinierte Brexpiprazol-Gruppen und 358 Patienten für die kombinierte Placebo-Gruppe.
Tab. 1. Patientendisposition der Akutstudien VECTOR und BEACON (nach [11])
|
Placebo (n = 358) |
Brexpiprazol |
||
|
2 mg/Tag (n = 359) |
4 mg/Tag (n = 359) |
||
|
Demographische Charakteristika |
|||
|
Alter [Jahre] |
39,7 (10,8) |
38,2 (10,6) |
39,6 (11,1) |
|
BMI [kg/m2] |
26,5 (5,5) |
26,7 (5,8) |
27,1 (6,2) |
|
Geschlecht, weiblich [n (%)] |
135 (37,7) |
132 (36,8) |
138 (38,4) |
|
Klinische Charakteristika |
|||
|
PANSS-Gesamtscore |
95,2 (12,2) |
96,1 (13,3) |
94,8 (12,2) |
|
PANSS Positive Subskala |
25,1 (4,4) |
25,2 (4,3) |
24,9 (4,4) |
|
PANSS Negative Subskala |
23,7 (4,9) |
23,7 (5,0) |
23,6 (4,8) |
|
CGI-S-Wert |
4,8 (0,6) |
4,9 (0,6) |
4,8 (0,6) |
Tabelle ist ein Auszug aus [11]. Placebo-, 2-mg- und 4-mg-Gruppen wurden kombiniert aus BEACON [24] und VECTOR [12]. Werte sind Mittelwerte (Standardabweichung), außer bei anderen Angaben. BMI: Body-Mass-Index; PANSS: Positive and Negative Syndrome Scale; CGI-S: Clinical Global Impression – Severity of illness
In der BEACON-Studie war hinsichtlich des primären Endpunkts (Veränderung des PANSS-Gesamtscores zu Woche 6 gegenüber Baseline) der 2-mg/Tag-Arm nicht signifikant verschieden vom Placebo-Arm gewesen [24]. In der gepoolten Analyse hingegen zeigten sowohl der 2-mg/Tag- als auch der 4-mg/Tag-Arm signifikant größere Verbesserungen als Placebo hinsichtlich des primären Endpunkts (p = 0,0004 und p < 0,0001 mit Cohen’s d Effektstärken von 0,27 und 0,33; Tab. 2). In beiden Gruppen war eine signifikante Wirkung ab der ersten Behandlungswoche sichtbar und blieb während der gesamten Studie erhalten (Abb. 1) [11]. In der Gruppe mit 0,25 mg/Tag Brexpiprazol wurden nur minimale Veränderungen gegenüber Baseline festgestellt, und in der 1-mg/Tag-Gruppe war die Veränderung suboptimal und geringer als in den Gruppen mit 2 oder 4 mg/Tag [11].
Tab. 2. Wirksamkeitsendpunkte der Akutstudien VECTOR und BEACON (nach [11])
|
Placebo (n = 358) |
Brexpiprazol 2 mg/Tag (n = 359) |
p-Wert |
Cohen’s d-Effektstärke (95%-KI) |
Brexpiprazol 4 mg/Tag (n = 359) |
p-Wert |
Cohen’s d-Effektstärke (95%-KI) |
|
|
Primärer Endpunkt |
|||||||
|
PANSS-Gesamtscore, |
–13,33 |
–18,79 |
–20,01 |
||||
|
Behandlungsunterschied |
–5,46 |
0,0004 |
0,27 |
–6,69 |
< 0,0001 |
0,33 |
|
|
Sekundäre Endpunkte |
|||||||
|
CGI-S-Score, |
–0,82 |
–1,07 |
–1,20 |
||||
|
Behandlungsunterschied |
–0,25 |
0,0035 |
0,21 |
–0,38 |
< 0,0001 |
0,34 |
|
|
PSP-Skala, |
9,51 |
11,99 |
13,01 |
||||
|
Behandlungsunterschied |
2,48 |
0,0086 |
0,20 |
3,50 |
0,0002 |
0,29 |
|
|
PANSS Positive Subskala, mittlere Änderung (SE)a |
–4,74 |
–6,06 |
–6,76 |
||||
|
Behandlungsunterschied |
–1,31 |
0,0107 |
0,19 |
–2,02 |
< 0,0001 |
0,30 |
|
|
PANSS Negative Subskala, mittlere Änderung (SE)a |
–2,31 |
–3,51 |
–3,59 |
||||
|
Behandlungsunterschied |
–1,20 |
0,0015 |
0,24 |
–1,28 |
0,0007 |
0,25 |
|
|
CGI-I-Score, |
3,48 |
3,06 |
2,94 |
||||
|
Behandlungsunterschied |
–0,42 |
< 0,0001 |
0,30 |
–0,50 |
< 0,0001 |
0,36 |
|
|
PANSS-Marder-Faktoren [32] |
|||||||
|
Positive Symptome, |
–5,95 |
–7,17 |
–7,55 |
||||
|
Behandlungsunterschied |
–1,22 |
0,0070 |
0,20 |
–1,61 |
0,0004 |
0,27 |
|
|
Negative Symptome, |
–2,82 |
–4,06 |
–4,06 |
||||
|
Behandlungsunterschied |
–1,24 |
0,0013 |
0,24 |
–1,24 |
0,0012 |
0,24 |
|
|
Desorganisierte Gedanken, |
–2,36 |
–3,48 |
–3,89 |
||||
|
Behandlungsunterschied |
–1,12 |
0,0018 |
0,23 |
–1,54 |
< 0,0001 |
0,32 |
|
|
Unkontrollierte Feindseligkeit/Erregung, mittlere Änderung (SE)a |
–0,79 |
–1,41 |
–1,97 |
||||
|
Behandlungsunterschied |
–0,62 |
0,0311 |
0,16 |
–1,18 |
< 0,0001 |
0,31 |
|
|
Angst/Depression, |
–3,04 |
–3,72 |
–3,65 |
||||
|
Behandlungsunterschied |
–0,69 |
0,0053 |
0,21 |
–0,61 |
0,0126 |
0,19 |
|
Die Tabelle stellt einen Auszug aus [11] dar. PANSS: Positive and Negative Syndrome Scale; CGI-S: Clinical Global Impression – Severity of illness; CGI-I: Clinical Global Impression – Improvement; PSP: Personal and Social Performance; SE: Standardfehler; 95%-KI: 95%-Konfidenzintervall.
a Mittlere Änderung der kleinsten Quadrate (Standardfehler) von Baseline bis Woche 6; p-Werte wurden durch eine Analyse mit gemischtem Modell für Messwiederholungen erhalten.
b p-Werte wurden durch Cochrane-Mantel-Haenszel-Test erhalten.
c Placebo, n = 362; Brexpiprazol 2 mg/Tag, n = 361; Brexpiprazol 4 mg/Tag, n = 361
d Placebo, n = 333; Brexpiprazol 2 mg/Tag, n = 343; Brexpiprazol 4 mg/Tag, n = 342
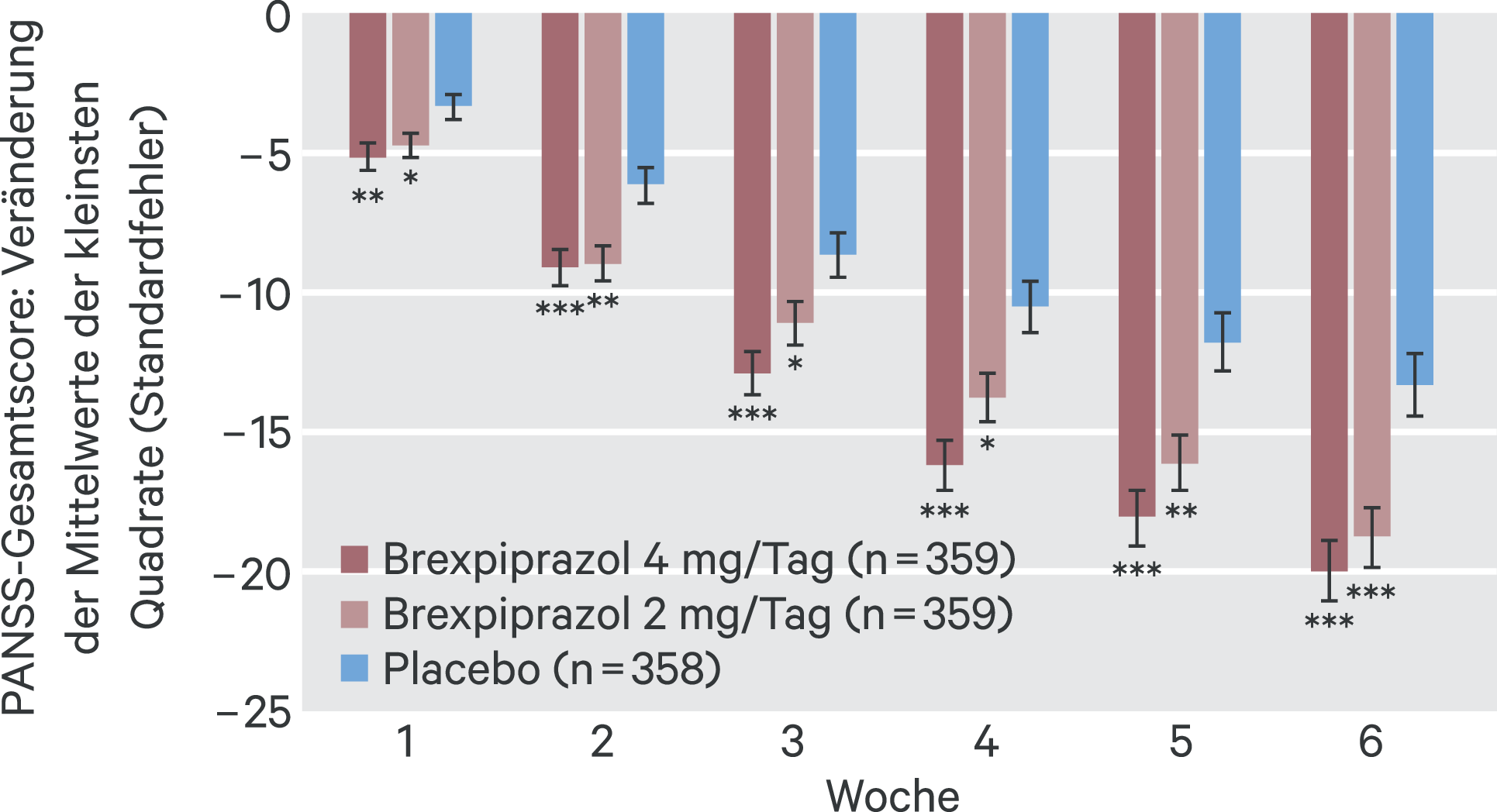
Abb. 1. Mittlere Veränderung versus Baseline im PANSS-Gesamtscore, gepoolte Daten aus den Studien BEACON und VECTOR (nach [11]) PANSS-Gesamtscore bei Baseline: Placebo, 95,2; 2 mg, 96,1; 4 mg, 94,8 *p < 0,05, **p < 0,01, ***p < 0,001 versus Placebo; gemischtes Modell für Messwiederholungen. PANSS: Positive and Negative Syndrome Scale
Die kombinierten 2-mg/Tag- und 4-mg/Tag-Gruppen waren auch hinsichtlich der Veränderung der CGI-S-Werte zu Woche 6 signifikant verschieden von Placebo (Abb. 2, Tab. 2). Des Weiteren zeigten diese Gruppen auch in allen anderen Endpunkten eine stärkere Verbesserung als unter Placebo bei p < 0,05 (Tab. 2) außer bei der Abbruchrate wegen Mangel an Wirksamkeit in der kombinierten 2-mg/Tag-Gruppe [11].
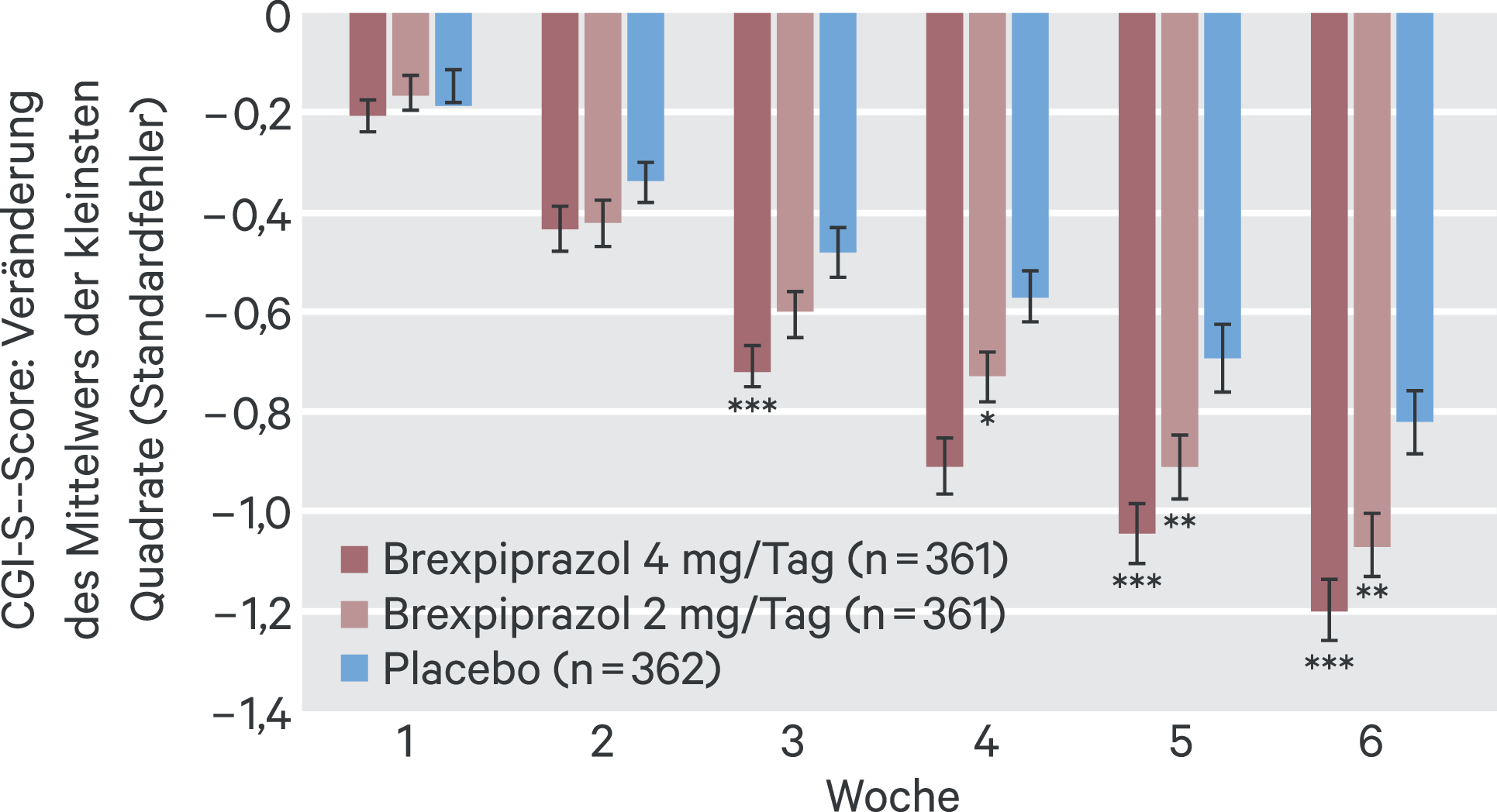
Abb. 2. Mittlere Veränderung versus Baseline des CGI-S-Scores, gepoolte Daten aus den Studien BEACON und VECTOR (nach [11]) CGI-S-Scores bei Baseline: Placebo, 4,8; 2 mg, 4,9; 4 mg, 4,8. *p < 0,05, **p < 0,01, ***p < 0,001 versus Placebo; gemischtes Modell für Messwiederholungen CGI-S: Clinical Global Impression – Severity of illness
Die Verbesserungen auf der PANSS-Skala wurden nach den PANSS-Marder-Faktoren aufgeschlüsselt analysiert (Tab. 2). Die PANSS-Marder-Faktoren wurden durch eine Faktorenanalyse aus den Daten von Studien zu Risperidon abgeleitet und bilden fünf Dimensionen der Schizophrenie ab [32]. Bei allen Faktoren war für die Brexpiprazol-Gruppen ein signifikanter Unterschied zu Placebo festzustellen (Tab. 2). Dieser signifikante Effekt über die verschiedenen Dimensionen der Schizophrenie hinweg ist klinisch relevant.
Ein therapeutisches Ansprechen war definiert als eine Verbesserung von mindestens 30 % im PANSS-Gesamtscore oder ein CGI-I von 1 („sehr viel gebessert“) oder 2 („viel gebessert“) zu Woche 6. Die Ansprechrate unter Brexpiprazol 2 mg/Tag lag bei 43,2 % und unter 4 mg/Tag bei 47,9 %, gegenüber einer Rate unter Placebo von 31,0 %. Daraus leitet sich eine Number needed to treat (NNT) ab von 9 für 2 mg/Tag und 6 für 4 mg/Tag (je niedriger die NNT, desto besser die Ansprechrate).
Die Wirksamkeitsvorteile gegenüber Placebo beinhalteten auch funktionelle Aspekte, gemessen mit der PSP-Skala [35] (Abb. 3). In einer Post-hoc-Analyse wurden unter Brexpiprazol 4 mg/Tag in allen vier Outcome-Domänen signifikant größere Verbesserungen als Placebo unter Placebo erreicht, unter Brexpiprazol 2 mg/Tag jedoch nur in den Domänen „Sozial nützliche Aktivitäten“ und „Selbstpflege“. Offenbar bietet die höhere Dosis zusätzliche Vorteile für die Funktionalität, was bei guter Verträglichkeit den Verordner anregen sollte, bei residualen Symptomen oder Funktionseinbußen über eine Erhöhung von Brexpiprazol auf 4 mg nachzudenken.
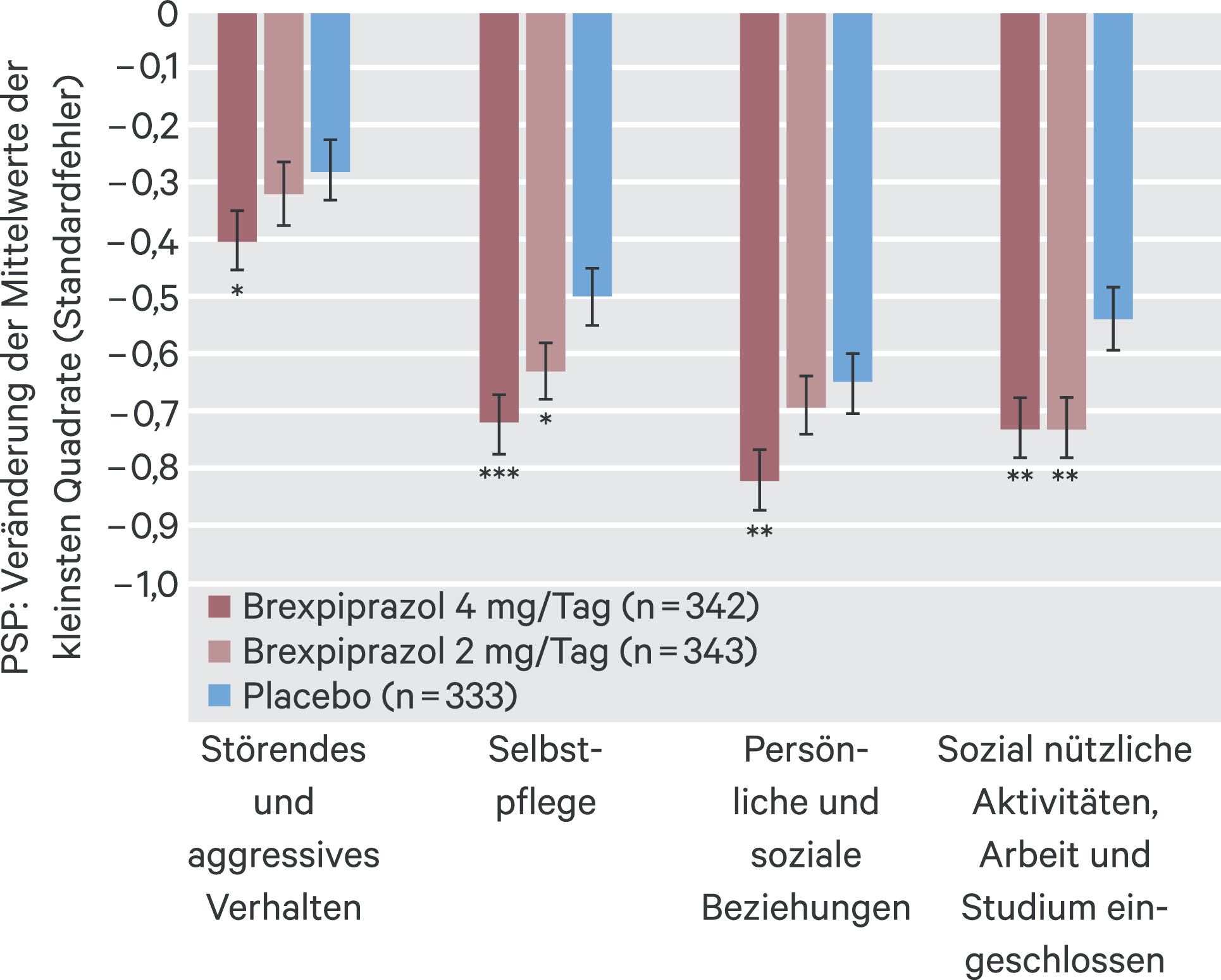
Abb. 3. Mittlere Änderung versus Baseline bei einzelnen Domänen der Personal and Social Performance Scale zu Woche 6 (nach [11]) *p < 0,05, **p < 0,01, ***p < 0,001 versus Placebo; gemischtes Modell für Messwiederholungen; PSP: Personal and Social Performance
Sicherheit
Die gepoolten Sicherheitsdaten aus BEACON und VECTOR, sowie die Sicherheitsdaten aus der Phase-II-Studie STEP 203, wurden in einer Metaanalyse zusammengefasst besprochen [23]. Insgesamt wurden in diesen drei Studien 1256 Patienten auf verschiedene Dosierungen von Brexpiprazol und 463 Patienten auf Placebo randomisiert (Tab. 3).
Tab. 3. Patientendisposition der gepoolten Sicherheitsdaten aus VECTOR, BEACON und STEP 203 (nach [23])
|
Brexpiprazol < 2 mg/Tag (n = 341) |
Brexpiprazol 2–4 mg/Tag (n = 822) |
Brexpiprazol > 4 mg/Tag (n = 93) |
Brexpiprazol gepoolt (n = 1256) |
Placebo (n = 463) |
|
|
Alter [Jahre] |
39,7 (11.0) |
38,8 (10,8) |
39,5 (11,1) |
39,1 (10,9) |
39,4 (10,9) |
|
Geschlecht weiblich [n (%)] |
123 (36,1) |
305 (37,1) |
38 (40,9) |
466 (37,1) |
176 (38,0) |
|
Kaukasier [n (%)] |
215 (63,0) |
517 (62,9) |
60 (64,5) |
792 (63,1) |
291 (62,9) |
|
Gewicht [kg] |
77,8 (20,3) |
78,5 (19,5) |
72,1 (18,4) |
77,8 (19,7) |
77,4 (18,4) |
|
BMI [kg/m2] |
26,7 (6,4) |
26,8 (6,0) |
25,3 (6,3) |
26,7 (6,2) |
26,5 (5,5) |
|
Alter bei Diagnosestellung [Jahre] |
26,7 (8,9) |
26,3 (8,4) |
26,9 (9,6) |
26,5 (8,6) |
26,3 (8,9) |
|
Dauer der aktuellen Episode, geschätzt [Wochen] |
2,5 (2,2) |
2,6 (2,4) |
2,3 (1,6) |
2,5 (2,3) |
2,7 (2,8) |
Daten sind Mittelwerte (Standardabweichung), wenn nicht anders angegeben. BMI: Body-Mass-Index
Bei dieser Population wurde die Behandlung von 65,4 % der Patienten unter Brexpiprazol und 60,5 % der Patienten unter Placebo abgeschlossen [23]. Die häufigsten Gründe für einen Studienabbruch waren „Widerruf der Einwilligung“ für Brexpiprazol (13,9 % vs. 11,9 % unter Placebo) und „unerwünschte Ereignisse“ unter Placebo (12,7 % vs. 8,1 % unter Brexpiprazol).
Nebenwirkungen, die bei 5 % oder mehr der Patienten einer Gruppe auftraten, sind in Tabelle 4 dargestellt. Die meisten Nebenwirkungen waren nach Einschätzung der Studienärzte geringfügig bis moderat ausgeprägt.
Tab. 4. Nebenwirkungen [n (%)], gepoolte Sicherheitsdaten aus VECTOR, BEACON und STEP 203 (nach [23])
|
Brexpiprazol < 2 mg/Tag (n = 341) |
Brexpiprazol 2–4 mg/Tag (n = 822) |
Brexpiprazol > 4 mg/Tag (n = 93) |
Brexpiprazol gepoolt (n = 1256) |
Placebo (n = 463) |
|
|
Mindestens eine Nebenwirkung |
204 (59,8) |
487 (59,2) |
70 (75,3) |
761 (60,6) |
283 (61,1) |
|
Schwerwiegende Nebenwirkung |
10 (2,9) |
19 (2,3) |
4 (4,3) |
33 (2,6) |
20 (4,3) |
|
Nebenwirkung, die zum Abbruch der Studie führte |
30 (8,8) |
61 (7,4) |
11 (11,8) |
102 (8,1) |
59 (12,7) |
|
Nebenwirkungen, die bei mindestens 5 % der Patienten einer Gruppe auftraten |
|||||
|
39 (11,4) |
93 (11,3) |
9 (9,7) |
141 (11,2) |
61 (13,2) |
|
32 (9,4) |
91 (11,1) |
7 (7,5) |
130 (10,4) |
52 (11,2) |
|
22 (6,5) |
57 (6,9) |
7 (7,5) |
86 (6,8) |
36 (7,8) |
|
12 (3,5) |
47 (5,7) |
14 (15,1) |
73 (5,8) |
21 (4,5) |
|
16 (4,7) |
41 (5,0) |
3 (3,2) |
60 (4,8) |
43 (9,3) |
|
15 (4,4) |
38 (4,6) |
6 (6,5) |
59 (4,7) |
9 (1,9) |
|
12 (3,5) |
33 (4,0) |
6 (6,5) |
51 (4,1) |
24 (5,2) |
|
8 (2,3) |
30 (3,6) |
6 (6,5) |
44 (3,5) |
16 (3,5) |
|
13 (3,8) |
15 (1,8) |
10 (10,8) |
38 (3,0) |
14 (3,0) |
|
5 (1,5) |
21 (2,6) |
5 (5,4) |
31 (2,5) |
12 (2,6) |
|
8 (2,3) |
16 (1,9) |
5 (5,4) |
29 (2,3) |
8 (1,7) |
|
6 (1,8) |
17 (2,1) |
5 (5,4) |
28 (2,2) |
5 (1,1) |
|
4 (1,2) |
15 (1,8) |
6 (6,5) |
25 (2,0) |
10 (2,2) |
Bei Dosierungen von Brexpiprazol bis 4 mg/Tag wurden keine Nebenwirkungen beobachtet, die bei mindestens 5 % der Patienten und doppelt so häufig wie unter Placebo auftraten. Dieses Ergebnis ist von klinischer Relevanz, da Nebenwirkungen einen häufigen Grund darstellen, dass Patienten das Medikament selbstständig absetzen, und da Nebenwirkungen ebenfalls zu eingeschränktem Wohlbefinden und zu reduzierter Funktionalität führen können. Akathisie wurde selten beobachtet, bei 5,8 % der Patienten unter Brexpiprazol und 4,5 % unter Placebo. Sedierung trat bei 2,3 % der Patienten unter Brexpiprazol und 0,6 % unter Placebo auf. Schläfrigkeit wurde bei 2,5 % unter Brexpiprazol und 2,6 % unter Placebo beobachtet. Die häufigsten schwerwiegenden Nebenwirkungen waren unter Brexpiprazol und Placebo mit der zugrunde liegenden Erkrankung assoziiert: Schizophrenie (1,2 % bzw. 2,4 %) und Psychose (0,6 % bzw. 0,9 %). Ein Patient unter Brexpiprazol verstarb, die Todesursache wurde nicht angegeben.
EPS-assoziierte Nebenwirkungen waren zumeist nach Einschätzung der Studienärzte geringfügig bis moderat ausgeprägt. Lediglich vier Patienten brachen wegen EPS die Behandlung ab, davon drei aus den Brexpiprazol-Armen und einer aus einem Placebo-Arm.
Die Gewichtszunahme betrug im Mittel 1,1 kg unter Brexpiprazol bzw. 0,2 kg unter Placebo. Insgesamt zeigten 9,9 % der Patienten unter Brexpiprazol und 4,8 % unter Placebo eine klinisch relevante Gewichtszunahme ≥ 7 %. Ein metabolisches Syndrom wurde bei 1,2 % bzw. 0,8 % der Patienten während der Studien neu diagnostiziert.
Nebenwirkungen, die möglicherweise in Zusammenhang mit erhöhtem Prolactin standen, wurden für 0,5 % der Patienten unter Brexpiprazol und 0,4 % unter Placebo berichtet. Sie waren nach Einschätzung der Studienärzte geringfügig bis moderat ausgeprägt. Unter Brexpiprazol zeigten 5,5 % der Frauen und 2,7 % der Männer Prolactinerhöhungen über das Doppelte des Normalwerts, und je 0,9 % der Frauen und Männer erreichten sogar mehr als das Dreifache des Normalwerts. Diese Patienten zeigten aber alle keine Symptome.
Je 0,2 % der Patienten in beiden Gruppen gaben eine Nebenwirkung im Zusammenhang mit Suizidalität an. Suizidales Verhalten nach C-SSRS wurde bei zwei Patienten festgestellt, davon erhielt einer 2 mg/Tag Brexpiprazol und einer Placebo.
Die Langzeitstudie EQUATOR
In EQUATOR wurde die Wirksamkeit und Sicherheit einer Erhaltungsbehandlung mit Brexpiprazol über 52 Wochen untersucht [18]. Schizophrenie-Patienten mit akuter Exazerbation ihrer psychotischen Symptome wurden innerhalb von ein bis vier Wochen auf Brexpiprazol 1 bis 4 mg/Tag eingestellt (mittlere Dosis: 3,6 mg/Tag) und kamen dann in eine einfach verblindete Stabilisierungsphase. Diejenigen Patienten, die in zwölf aufeinander folgenden Wochen bei einer konstanten Dosis an Brexpiprazol die Stabilitätskriterien erfüllten, wurden 1 : 1 auf eine doppelblinde Behandlung bis zu 52 Wochen mit Brexpiprazol (Stabilisierungsdosis) oder Placebo randomisiert.
Wirksamkeit
Der primäre Endpunkt war die Zeit ab Randomisierung bis zum bevorstehenden Rückfall. Weitere Endpunkte waren das Verhältnis an Patienten, die während der doppelblinden Erhaltungsphase die Kriterien eines bevorstehenden Rückfalls erfüllten, sowie unter anderem die Änderungen des PANSS-Gesamtscores und verschiedener PANSS-Subskalen, CGI-S, CGI-I und der PSP-Skala [35].
Insgesamt wurden 524 Patienten eingeschlossen, von denen 202 sich unter Brexpiprazol stabilisierten und auf Brexpiprazol (n = 97) oder Placebo (n = 105) randomisiert wurden (Tab. 5). Die Wirksamkeit von Brexpiprazol wurde bei einer vorab geplanten Interimsanalyse nach 45 Ereignissen eines bevorstehenden Rückfalls nachgewiesen. Deshalb wurde die Studie vorzeitig beendet.
Tab. 5. Patientendisposition der Langzeitstudie EQUATOR [18]
|
Auswasch-/ (n = 406) |
Einfachblinde Stabilisierungsphase (n = 464) |
Doppelblinde Erhaltungsphase |
||
|
Placebo (n = 105) |
Brexpiprazol (n = 97) |
|||
|
Demographische Charakteristika |
||||
|
Alter [Jahre] |
39,8 (11,3) |
39,2 (11,2) |
41,6 (10,6) |
38,8 (10,7) |
|
BMI [kg/m2] |
27,5 (6,1) |
27,8 (6,4) |
29,1 (6,9) |
28,2 (6,7) |
|
Männlich [n (%)] |
244 (60,1) |
278 (59,9) |
65 (61,9) |
58 (59,8) |
|
Kaukasier [n (%)] |
267 (65,8) |
277 (59,7) |
65 (61,9) |
62 (63,9) |
|
Klinische Charakteristika |
||||
|
Alter bei Diagnosestellung [Jahre] |
26,6 (8,7) |
25,0 (8,5) |
27,9 (8,3) |
26,5 (8,2) |
|
PANSS-Gesamtscore |
91,1 (8,7) |
84,4 (12,3) |
58,1 (8,1) |
56,5 (8,7) |
|
CGI-S-Score |
4,6 (0,6) |
4,3 (0,8) |
3,1 (0,6) |
3,0 (0,6) |
|
PSP-Gesamtscore |
48,3 (11,3) |
48,0 (11,6) |
48,7 (11,7) |
50,1 (12,4) |
Daten sind Mittelwerte (Standardabweichungen), außer bei anderen Angaben. BMI: Body-Mass-Index; PANSS: Positive and Negative Syndrome Scale; CGI-S: Clinical Global Impression – Severity; PSP: Personal and Social Performance
Die abschließende Auswertung nach 53 Ereignissen eines bevorstehenden Rückfalls umfasste 200 Patienten und ergab, dass die Zeit bis zum bevorstehenden Rückfall unter Brexpiprazol signifikant länger war als unter Placebo (p < 0,0001, Log-Rank-Test; Abb. 4). Das Hazard-Ratio betrug 0,292 (95%-Konfidenzintervall [KI] 0,156–0,548; Abb. 4), damit senkte Brexpiprazol das Risiko eines bevorstehenden Rückfalls um 71 %. Eine solch robuste Reduktion der Rückfälle ist eher selten, da die meisten anderen Antipsychotika, inklusive die anderen beiden D2-Partialagonisten, Aripiprazol [41] und Cariprazin [16], die Rückfallrate um etwa 50 bis 55 % reduziert haben. Der Anteil der Patienten, die die Kriterien für einen bevorstehenden Rückfall erfüllten, betrug 13,5 % unter Brexpiprazol und 38,5 % unter Placebo (p < 0,0001, Chi-Quadrat-Test, NNT = 4). Für Patienten, die die Studie abbrachen, betrug die mittlere Dauer bis zum Abbruch während der Erhaltungsphase 169 Tage unter Brexpiprazol und 111 Tage unter Placebo. Die Abbruchraten lagen bei 34,4 % bzw. 54,8 % (p = 0,0014, Log-Rank-Test). Hierbei wurden diejenigen Patienten, die die Studien nicht beendeten, weil sie nach der Interimsanalyse abgebrochen wurde, nicht berücksichtigt. Der Anteil der Patienten, der bei der letzten Visite in der Erhaltungsphase noch die Stabilitätskriterien erfüllte, lag bei 79,2 % der Brexpiprazol-Gruppe und 56,7 % der Placebo-Gruppe (p = 0,0007, Chi-Quadrat-Test, NNT = 4). Weitere Endpunkte zur Wirksamkeit sind in Tabelle 6 dargestellt. Wegen des Studienabbruchs zur Interimsanalyse erreichte nur eine geringe Zahl an Patienten Woche 52 (23 Patienten, 4,4 % der eingeschlossenen Population), weshalb neben der MMRM auch eine Last-observation-carried-forward-(LOCF-)Analyse durchgeführt wurde.
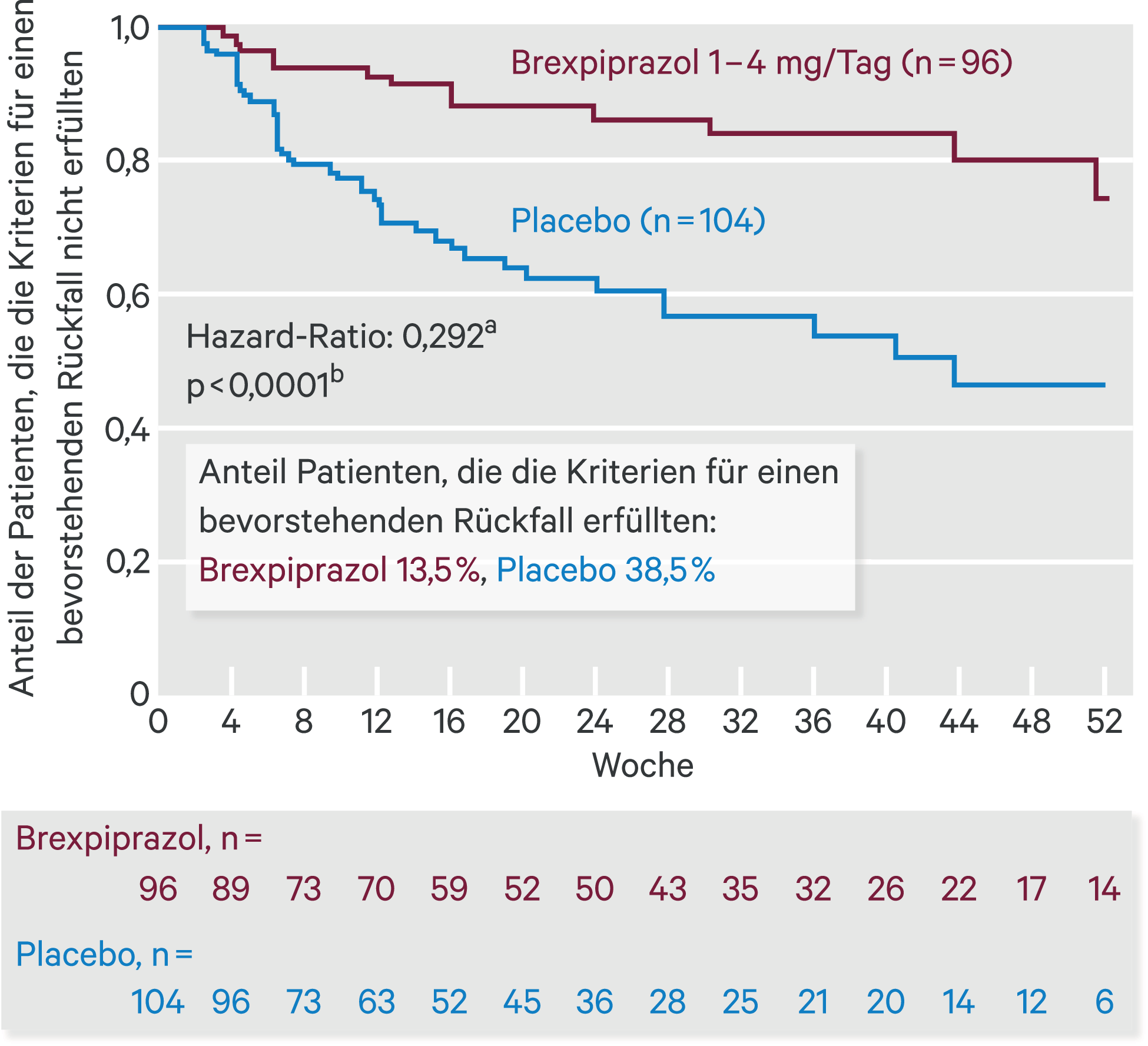
Abb. 4. Zeit bis zum bevorstehenden Rückfall aus der Langzeitstudie EQUATOR (nach [18]) aCox-Proportional-Hazards-Model mit Behandlung als Einflussvektor; blLog-Rank-Test. Da die Wirksamkeit bei der vordefinierten Interimsanalyse gezeigt werden konnte, wurde die Studie vorzeitig abgebrochen.
Tab. 6. Sekundäre Wirksamkeitsendpunkte aus der Langzeitstudie EQUATOR [18]
|
Stabilisierungsphase |
Erhaltungsphase |
|||||||||||
|
Analyse nach gemischtem Modell für Messwiederholungen |
Last observation carried forward, Kovarianzanalyse |
|||||||||||
|
Mittelwert bei Baseline (SD) |
Mittlere Änderung bei letzter Visite (SD) |
Mittelwert bei Baseline (SD) |
Änderung des Mittelwerts der kleinsten Quadrate zu Woche 52 (SE) |
Behandlungsunterschied (95%-KI) |
p-Wert |
Änderung des Mittelwerts der kleinsten Quadrate zu Woche 52 (SE) |
Behandlungsunterschied (95%-KI) |
p-Wert |
||||
|
Brexpiprazol (n = 449) |
Brexpiprazol (n = 447) |
Brexpiprazol (n = 96) |
Placebo (n = 104) |
Brexpiprazol (n = 15) |
Placebo (n = 9) |
Brexpiprazol (n = 96) |
Placebo (n = 104) |
|||||
|
PANSS-Gesamtscore |
84,26 (12,33) |
–15,13 (15,99) |
56,66 (8,51) |
58,07 (8,13) |
0,61 (3,34) |
6,92 (4,53) |
–6,31 (–18,1; 5,46) |
0,2800 |
3,25 (1,94) |
11,20 (1,77) |
–7,95 (–12,5; –3,41) |
0,0007 |
|
PANSS Positive Subskala |
21,35 (4,75) |
–4,99 (5,45) |
12,48 (3,66) |
12,63 (3,13) |
–1,21 (0,73) |
1,50 (0,99) |
–2,71 (–5,20; –0,22) |
0,0399 |
0,99 (0,64) |
4,17 (0,59) |
–3,18 (–4,70; –1,66) |
< 0,0001 |
|
PANSS Negative Subskala |
22,14 (4,64) |
–3,16 (4,61) |
16,30 (3,46) |
17,00 (3,64) |
1,30 (1,37) |
0,87 (1,71 |
0,43 (–4,14; 5,00) |
0,8470 |
0,39 (0,54) |
1,63 (0,49) |
–1,24 (–2,50; 0,01) |
0,0516 |
|
CGI-S-Score |
4,31 (0,78) |
–0,73 (0,96) |
3,00 (0,60) |
3,08 (0,60) |
–0,23 (0,17) |
0,28 (0,22) |
–0,51 (–1,09; 0,06) |
0,780 |
0,02 (0,11) |
0,55 (0,11) |
–0,53 (–0,79; –0,26) |
0,0002 |
|
CGI-I-Score |
2,84 (1,24)a [n = 454] |
3,77 (1,26)b |
4,40 (1,32)b |
–0,61 (–0,96; –0,25) |
0,0009 |
|||||||
|
PSP Gesamtscore |
49,82 (12,20) |
48,22 (11,64) |
18,63 (2,76) |
12,55 (3,48) |
6,08 (–2,71; 14,87) |
0,1677 |
15,06 (1,43) |
10,31 (1,34) |
4,75 (1,31; 8,18) |
0,0071 |
||
|
PEC-Score |
11,03 (3,44) |
–1,89 (3,97) |
6,98 (1,92) |
7,37 (2,50) |
–0,04 (0,46) |
1,00 (0,59) |
–1,03 (–2,58; 0,51) |
0,1803 |
0,82 (0,41) |
2,35 (0,38) |
–1,54 (–2,52; –0,56) |
0,0023 |
|
PANSS-Marder-Faktoren [32] |
||||||||||||
|
Positive Symptome |
25,46 (5,13) |
–5,48 (5,66) |
15,89 (3,99) |
15,80 (3,21) |
–1,62 (0,83) |
1,78 (1,05) |
–3,40 (–6,05; –0,75) |
0,0136 |
0,58 (0,66) |
4,02 (0,60) |
–3,44 (–4,99; –1,89) |
< 0,0001 |
|
Negative Symptome |
21,05 (4,92) |
–3,23 (4,81) |
15,07 (3,53) |
16,06 (3,68) |
1,37 (1,39) |
1,06 (1,77) |
0,31 (–4,40; 5,02) |
0,8927 |
0,34 (0,56) |
1,57 (0,50) |
–1,23 (–2,52; 0,07) |
0,0630 |
|
Desorganisierte Gedanken |
19,98 (3,86) |
–3,42 (3,95) |
14,54 (2,89) |
14,31 (3,06) |
–0,37 (0,99) |
–0,30 (1,24) |
–0,07 (–3,32; 3,17) |
0,9632 |
0,29 (0,48) |
1,97 (0,45) |
–1,69 (–2,81; –0,56) |
0,0035 |
|
Unkontrollierte Feindseligkeit/Erregung |
8,58 (3,14) |
–1,42 (3,35) |
5,56 (1,76) |
5,72 (2,17) |
–0,20 (0,40) |
0,94 (0,50) |
–1,14 (–2,46; 0,18) |
0,0875 |
0,49 (0,37) |
1,75 (0,34) |
–1,26 (–2,12; –0,39) |
0,0046 |
|
Angst/Depression |
9,18 (3,21) |
–1,57 (3,42) |
5,59 (1,76) |
6,18 (2,47) |
0,04 (0,43) |
0,28 (0,56) |
–0,23 (–1,68; 1,21) |
0,7437 |
1,17 (0,31) |
1,88 (0,29) |
–0,72 (–1,47; 0,03) |
0,0608 |
a Mittelwert (Standardabweichung) bei letzter Visite; b Mittelwert (Standardabweichung) zu Woche 52
SD: Standardabweichung; SE: Standardfehler; KI: Konfidenzintervall; PANSS: Positive and Negative Syndrome Scale; CGI-S: Clinical Global Impression – Severity; CGI-I: Clinical Global Impression – Improvement; PSP: Personal and Social Performance; PEC: PANSS Excited Component
Während der Stabilisierungsphase verbesserten sich die Symptome der Schizophrenie, wie auf verschiedenen Skalen erfasst (Abb. 5, Tab. 6). Während der doppelblinden Erhaltungsphase blieben die Verbesserungen unter Brexpiprazol erhalten, wohingegen unter Placebo Verschlechterungen eintraten (Abb. 5, Tab. 6, LOCF-Analyse). Der PSP-Score, der Funktionalität abbildet, verbesserte sich ebenfalls unter Brexpiprazol in einem klinisch relevanten Maß (definiert als Zunahme um 4 bis 7 Punkte [37]). Diese Ergebnisse sind von klinischer Bedeutung, da die Verbesserung der Funktionalität ein vordringliches Ziel bei der Behandlung von Patienten mit einer Schizophrenie darstellt.

Abb. 5. Mittlere Änderung des PANSS-Gesamtscores versus Baseline in der Stabilisierungs- und Erhaltungsphase von EQUATOR (nach [18]) *p < 0,05, **p < 0,01, ***p < 0,001 versus Placebo; Stabilisierungsphase: gemischtes Modell für Messwiederholungen (mixed model for repeated measures, MMRM); Erhaltungsphase: Last observation carried forward (LOCF), Kovarianzanalyse. PANSS-Gesamtscore bei Baseline: Stabilisierungsphase (n = 449), 84,3; Erhaltungsphase: Placebo (n = 104), 58,1; Brexpiprazol (n = 96), 56,7. PANSS: Positive and Negative Syndrome Scale
Sicherheit
Während der Stabilisierungsphase brachen 8,8 % der Patienten die Studie wegen Nebenwirkungen ab. Während der Erhaltungsphase waren es 5,2 % der Patienten in der Brexpiprazol-Gruppe und 11,5 % der Placebo-Gruppe. Die häufigsten Nebenwirkungen während der Studie sind in Tabelle 7 aufgeführt. Es gab keine Nebenwirkungen, die sowohl häufiger unter Brexpiprazol als unter Placebo auftraten als auch eine Inzidenz von über 5 % hatten. Der Großteil der Nebenwirkungen war gering bis moderat ausgeprägt. Zusammengenommen zeigen diese Resultate, dass Brexpiprazol sehr gut verträglich ist.
Tab. 7. Nebenwirkungen [n (%)] aus der Langzeitstudie EQUATOR [18]
|
Stabilisierungsphase |
Erhaltungsphase |
||
|
Brexpiprazol (n = 464) |
Placebo (n = 104) |
Brexpiprazol (n = 97) |
|
|
Mindestens eine Nebenwirkung |
267 (57,5) |
58 (55,8) |
42 (43,3) |
|
Nebenwirkungen, die bei ≥ 5 % der Patienten auftraten |
|||
|
23 (5,0) |
10 (9,6) |
6 (6,2) |
|
56 (12,1) |
8 (7,7) |
5 (5,2) |
|
16 (3,4) |
7 (6,7) |
3 (3,1) |
|
28 (6,0) |
7 (6,7) |
3 (3,1) |
|
5 (1,1) |
6 (5,8) |
1 (1,0) |
|
30 (6,5) |
3 (2,9) |
1 (1,0) |
|
42 (9,1) |
1 (1,0) |
1 (1,0) |
|
24 (5,2) |
0 (0,0) |
1 (1,0) |
Während der Stabilisierungsphase wurde eine mittlere Gewichtszunahme von 0,8 kg beobachtet. 11,3 % der Patienten nahmen ≥ 7 % an Gewicht zu. Während der Erhaltungsphase nahmen die Patienten im Mittel ab, nämlich um 0,3 kg unter Brexpiprazol und 2,2 kg unter Placebo. Hier lag die Inzidenz einer ≥ 7%igen Gewichtszunahme bei 5,2 % bzw. 1,0 %.
Die Langzeitstudie ZENITH
Zusätzliche Langzeit-Sicherheitsdaten wurden in der Open-Label-Studie ZENITH erhoben [20]. Patienten, die die Studien VECTOR, BEACON oder EQUATOR abgeschlossen hatten, konnten an ZENITH teilnehmen. Außerdem wurden auch neue Patienten aufgenommen. Insgesamt wurden 1072 Patienten eingeschlossen (Tab. 8), von denen 952 für 52 Wochen und 120 für 26 Wochen offen mit Brexpiprazol behandelt wurden. Primärer Endpunkt war hier das Auftreten von Nebenwirkungen, die Wirksamkeit wurde nur in sekundären Endpunkten festgestellt.
Tab. 8. Patientendisposition der Langzeitstudie ZENITH [20]
|
Demographie |
Eingeschlossene Population (n = 1072) |
|
Alter [Jahre] |
40,0 (11,1) |
|
BMI [kg/m2] |
27,9 (6,6) |
|
Weiblich [n (%)] |
409 (38,2) |
|
Ethnie [n (%)] |
|
|
665 (62,0) |
|
267 (24,9) |
|
63 (5,9) |
|
77 (7,2) |
|
Klinische Charakteristika |
Sicherheitspopulation (n = 1031) |
|
PANSS-Gesamtscore |
69,5 (17,2) |
|
CGI-S-Score |
3,5 (0,9) |
|
PSP-Gesamtscore |
58,5 (12,8) (n = 1015) |
47,4 % der Patienten schlossen die Studie ab. Von den Patienten unter Brexpiprazol brachen 14,6 % wegen Nebenwirkungen ab, davon die meisten wegen Schizophrenie (8,8 %) oder psychotischer Störung (1,5 %). Die häufigsten Nebenwirkungen sind in Tabelle 9 aufgeführt. Die meisten davon waren gering bis moderat ausgeprägt.
Tab. 9. Nebenwirkungen [n (%)] aus der Langzeitstudie ZENITH [20]
|
Sicherheitspopulation (n = 1031) |
|
|
Mindestens eine Nebenwirkung |
623 (60,4) |
|
Studienabbruch wegen Nebenwirkung |
151 (14,6) |
|
Nebenwirkungen, die bei ≥ 5 % der Patienten auftraten |
|
|
120 (11,6) |
|
89 (8,6) |
|
80 (7,8) |
|
66 (6,4) |
|
56 (5,4) |
|
Andere wichtige Nebenwirkungen |
|
|
49 (4,8) |
|
23 (2,2) |
|
22 (2,1) |
|
9 (0,9) |
|
9 (0,9) |
|
7 (0,7) |
|
1 (0,1) |
Die mittlere Gewichtszunahme betrug 1,3 kg nach 26 Wochen und 2,1 kg nach 52 Wochen. Eine Gewichtszunahme von ≥ 7 % wurde bei 18,6 % der Patienten beobachtet und eine Gewichtsabnahme von ≥ 7 % bei 9,2 % der Patienten. Es gab keine klinisch relevanten Ereignisse im Zusammenhang mit Prolactin, Lipidwerten, Glucosewerten oder dem QT-Intervall.
Im Mittel nahmen die Symptome der Schizophrenie während der Studie ab und die Funktionalität der Patienten verbesserte sich.
In der Studie ZENITH gab es keine Vergleichsgruppe. Jedoch ist diese Studie durch das offene Design näher an der Behandlungsrealität und die Daten dürften damit gut auf das alltägliche klinische Geschehen übertragbar sein.
Diskussion
Bei akuter Exazerbation der Schizophrenie ist Brexpiprazol 2 mg/Tag und 4 mg/Tag wirksam bei Erwachsenen, wie die Metaanalyse der Akutstudien BEACON (in dieser Studie war nur 4 mg der Placebo-Gruppe überlegen) und VECTOR ergab [11, 12, 24]. In BEACON war der Brexpiprazol-Arm 2 mg/Tag nicht erfolgreich, unter anderem weil in dieser Studie ein großer Placebo-Effekt von –13,5 im PANSS-Gesamtscore zur verzeichnen war. In der Metaanalyse mit den gepoolten Ergebnissen ergaben sich aber trotzdem signifikante Vorteile auch für die 2-mg/Tag-Dosierung. Hinsichtlich Funktionalität war die 4-mg-Tagesdosis hinsichtlich aller vier Outcome-Domänen, gemessen mit der PSP, signifikant Placebo überlegen, die 2-mg/Tag-Dosis hingegen lediglich in zwei der vier Domänen. Auch die Verträglichkeit und Sicherheit einer Akutbehandlung der Schizophrenie mit Brexpiprazol ist gezeigt worden [12, 23, 24].
Ebenso ist Brexpiprazol 1 bis 4 mg/Tag bei der langfristigen Erhaltung der Stabilität bei Schizophrenie wirksam und sicher und schützt vor Rückfällen [18]. Die mittlere Dosis von 3,6 mg/Tag unterstreicht, dass für die meisten chronisch kranken schizophrenen Patienten 4 mg/Tag die Zieldosis sein sollte, es sei denn es treten Nebenwirkungsprobleme bei der Dosiserhöhung von 2 mg/Tag auf 4 mg/Tag auf. Zusätzlich wurde die langfristige Sicherheit und Verträglichkeit in einer Open-Label-Studie gezeigt [20].
Die gefundenen Effektstärken (Cohen’s d, Tab. 2) beziehungsweise Behandlungsunterschiede (Tab. 6) erscheinen nicht besonders groß, außerdem war in der BEACON-Studie der 2-mg/Tag-Arm nicht erfolgreich [24]. Ebenso scheint Brexpiprazol in einer aktuellen Metaanalyse im Vergleich mit anderen Antipsychotika vergleichsweise schlecht abzuschneiden (Abb. 3 in [29]). Der Grund hierfür ist aber nicht etwa eine geringe Wirksamkeit: Vielmehr werden abnehmende Effektstärken für Antipsychotika allgemein um 0,08 Einheiten pro Jahrzehnt beobachtet, sodass Studien im Jahr 1970 eine durchschnittliche Effektstärke von 0,74 fanden, Studien im Jahr 2015 jedoch nur noch 0,38 [29]. Dieser Effekt wird besonders deutlich, wenn der Wirkstoff Haloperidol über längere Zeit betrachtet wird [29]. Eine etwaige geringere Wirksamkeit neuerer Antipsychotika ist also nicht die Ursache. Tatsächlich bleibt die Wirksamkeit von Antipsychotika über die Zeit gleich, wenn die absolute Veränderung durch die Behandlung auf der PANSS-Skala betrachtet wird [29]. Ursache für die abnehmende Effektstärke ist vielmehr eine wachsende Placebo-Response, die 1970 noch durchschnittlich 3 Punkte auf der PANSS-Skala betrug, 2015 jedoch bereits 10 Punkte [27]. Daher kann angenommen werden, dass die antipsychotische Wirksamkeit von Brexpiprazol relativ vergleichbar mit anderen verfügbaren Substanzen ist.
Brexpiprazol bietet zusätzlich Vorteile beim Nebenwirkungsprofil. Es hat nur geringe Auswirkungen auf Prolactinspiegel [22], wie Daten aus BEACON, VECTOR und einer weiteren sechswöchigen Kurzzeitstudie [33] (n = 882 Patienten unter Brexpiprazol 2 bis 4 mg/Tag) sowie der Langzeitstudie ZENITH und einer weiteren Langzeitstudie über 52 Wochen (n = 1240 Patienten unter Brexpiprazol 1 bis 4 mg/Tag) belegen. Hier wurde nur ein geringer Anteil an Patienten mit erhöhten Prolactinwerten gefunden, und Nebenwirkungen im Zusammenhang mit Prolactin waren selten. Darüber hinaus wurde sogar beobachtet, dass hohe Prolactinspiegel zu Beginn der Studie tendenziell sanken [22], was durch den partiellen Agonismus am D2-Rezeptor plausibel erscheint. Da erhöhte Prolactinspiegel mit sexueller Dysfunktion einhergehen können, stellt die Normalisierung des Prolactinspiegels ein weiteres Element der guten Tolerabilität von Brexpiprazol dar.
Bisher sind keine verblindeten, direkten Vergleichsstudien mit Brexpiprazol und anderen Antipsychotika in ausreichend großen Patientengruppen verfügbar, daher sind derzeit nur indirekte Vergleiche in Placebo-kontrollierten Studien möglich. Indirekte Wirksamkeitsvergleiche werden allerdings dadurch erschwert, dass aufgrund steigender Placebo-Effekte über die Jahre [27] der Unterschied zwischen Verum und Placebo abnimmt [29], wobei offenbar eine große Zahl an Studienteilnehmern zu einem größeren Placebo-Effekt beiträgt [27]. Hier soll Brexpiprazol im Vergleich mit den anderen beiden Dopamin-D2-Partialagonisten, Aripiprazol und Cariprazin, betrachtet werden.
Cariprazin wurde in einer Studie an Patienten mit vorrangig negativer Symptomatik mit Erfolg getestet [38]. Für Brexpiprazol gibt es keine Studie, in der diese spezielle Gruppe genauer untersucht wurde, jedoch wurde in sekundären Analysen die Wirksamkeit von Brexpiprazol auch in diesen Bereichen gezeigt.
Bezogen auf die Lebensqualität wurde am Beispiel von Aripiprazol-Depot gezeigt, dass Partialagonisten Dopaminantagonisten wie Paliperidonpalmitat überlegen sein können [36, 42]. Ähnliches ließ sich für den Bereich Negativsymptome feststellen, in dem Cariprazin signifikant überlegen gegenüber Risperidon war [38]. Schließlich war in einer 12-Wochen-Studie bei Ersterkrankten mit einer Schizophrenie Aripiprazol einerseits gleich wirksam wie Risperidon für Positivsymptome, Allgemeinsymtome und Schweregrad der schizophrenen Erkrankung, aber andererseits war Aripiprazol Risperidon signifikant überlegen bezüglich Anhedonie und Depression [43]. Durch solche Ergebnisse deutet sich an, dass die Partialagonisten bei relevanten Outcomes wie Lebensqualität, Negativsymptomatik und Depression, eine eigene Gruppe darstellen, die sich möglicherweise hinsichtlich bestimmter, relevanter Outcome-Domänen von den „herkömmlichen“ antidopaminergen Atypika abgrenzen lassen.
Aripiprazol ist mit Nebenwirkungen assoziiert, die durch D2-Partialagonismus ausgelöst sein könnten, wie Akathisie, Schlaflosigkeit, Ruhelosigkeit und Übelkeit/Erbrechen [19, 39]. Die intrinsische D2-Rezeptoraktivität von Brexpiprazol ist allerdings geringer als die von Aripiprazol und könnte daher in dieser Hinsicht Verbesserungen mit sich bringen. Außerdem hat Brexpiprazol im Vergleich mit Aripiprazol eine etwa zehnfach höhere Affinität für die Serotoninrezeptoren 5-HT1A und 5-HT2A [5, 31, 44]. In einer wegen der Patientenzahl und dem offenen Studiendesign nur explorativen Studie wurden 64 Patienten auf Brexpiprazol und 33 Patienten auf Aripiprazol als aktive Vergleichssubstanz randomisiert [4]. Tatsächlich war hier ein Signal im Bereich der Nebenwirkungen sichtbar, mit einer etwa halb so hohen Rate an Akathisie-Ereignissen unter Brexpiprazol wie unter Aripiprazol. Dabei waren die Maße der Wirksamkeit nach sechs Wochen Behandlungszeit vergleichbar, mit einer Abnahme des PANSS-Gesamtscores von 22,9 (SD: 1,7) unter Brexpiprazol und 19,4 (SD: 2,4) unter Aripiprazol und einer Reduktion des CGI-S von 1,6 (SD: 0,1; Brexpiprazol) beziehungsweise 1,3 (SD: 0,2; Aripiprazol) [4]. Der verstärkte Antagonismus an den 5-HT2A-Rezeptoren könnte dazu beitragen, dass Brexpiprazol weniger EPS und Akathisie verursacht [23, 26], beides Nebenwirkungen, die Patienten zum Teil erheblich beeinträchtigen können.
Citrome hat eine Übersicht über die Unterschiede der drei derzeit verfügbaren Partialagonisten verfasst [8]. Anhand der jeweiligen Zulassungsstudien wurde die NNT (niedrigere Zahl = bessere Wirksamkeit) für alle drei Substanzen abgeschätzt, die nötig ist, um ein klinisches Ansprechen zu erzielen. Das klinische Ansprechen war definiert als mindestens 30%ige Reduktion der PANSS oder ein CGI-I-Score von 1 (sehr stark verbessert) oder 2 (stark verbessert) für Aripiprazol und Brexpiprazol. Damit gelangt Citrome zu einer NNT = 7 (95%-KI 5–12) für Brexpiprazol; diese liegt etwas niedriger liegt als die von Aripiprazol (NNT = 8; 95%-KI 6–13) und Cariprazin (NNT = 10; 95%-KI 7–18), wobei für Cariprazin nur eine 30%ige PANSS-Reduktion als Kriterium für klinisches Ansprechen diente. Weiterhin fasst Citrome auch die wichtigsten Nebenwirkungen zusammen, wobei unter Aripiprazol und Cariprazin in den Zulassungsstudien Akathisie bzw. Akathisie und EPS häufiger als 5 % und mindestens doppelt so häufig wie unter Placebo auftraten, unter Brexpiprazol hingegen war Gewichtszunahme am prominentesten mit einer Inzidenz von über 4 % und doppelt so häufig wie unter Placebo. Daraus ergeben sich Numbers needed to harm (NNH, hohe Zahl = weniger Nebenwirkungsbelastung): für Aripiprazol eine NNH = 25 für Akathisie, für Brexpiprazol eine NNH = 50 für Gewichtszunahme und für Cariprazin eine NNH = 12 für EPS. Für einen definitiven Vergleich der drei Substanzen wären allerdings direkte und verblindete Vergleichsstudien nötig.
Insgesamt unterscheiden sich Antipsychotika der zweiten Generation nur geringfügig, was ihre Wirksamkeit angeht [28], sehr wohl aber bei den Nebenwirkungsprofilen [6, 7, 28]. Weiterhin sind eventuelle individuelle Wirksamkeitsunterschiede nicht leicht vorherzusagen, wohingegen Nebenwirkungsunterschiede leichter und zuverlässiger prädizierbar sind.
Eine Analyse der aktivierenden und sedierenden Nebenwirkungen von Antipsychotika der zweiten Generation anhand der Fachinformationen ist verfügbar [9]. Als aktivierende Nebenwirkungen wurde hier Akathisie, Ruhelosigkeit, Agitiertheit, Angst und Schlaflosigkeit eingestuft; als sedierende Nebenwirkungen wurden Schläfrigkeit, Sedierung und Abgeschlagenheit berücksichtigt. Hier stachen Paliperidon und Brexpiprazol als einzige Substanzen hervor, die als weder aktivierend noch sedierend eingestuft wurden [9]. Da sowohl sedierende als auch aktivierende Nebenwirkungen subjektiv beeinträchtigend sein können, ist dieses ausbalancierte Nebenwirkungsprofil klinisch relevant. Allerdings wurden für diese Einschätzung nur die jeweiligen Zulassungsstudien berücksichtigt, die für Nebenwirkungen in Fachinformation herangezogen worden waren; für Brexpiprazol waren dies VECTOR und BEACON [12, 24].
Für eine erfolgreiche Behandlung der Schizophrenie ist es wichtig, die Sicht des Patienten zu beachten: Je nach den persönlichen Präferenzen und Werten sind bestimmte Nebenwirkungen auf jeden Fall zu vermeiden, während andere tolerierbar sind. Es gibt individuelle Unterschiede, welche Nebenwirkungen überhaupt auftreten und wie sie bewertet werden [25]. Beim sogenannten patientenzentrierten Ansatz wird die Behandlung auf die persönlichen Ziele des Patienten abgestimmt; dies erhöht die Patientenzufriedenheit und Adhärenz [46]. Akathisie war in einer Studie stark mit Nicht-Adhärenz assoziiert [14], in solchen Fällen dürfte Brexpiprazol vorteilhaft sein. Auch sind Sedierung und die kognitive Leistung beeinträchtigende Effekte mit einer Einschränkung der Lebensqualität bei Patienten mit einer Schizophrenie vergesellschaftet [1, 34], was ebenfalls zu einer Abnahme der Adhärenz führen kann. In diesem Zusammenhang erweitert die neue, zusätzliche Option Brexpiprazol das Spektrum der Behandlungsmöglichkeiten.
Fazit
Brexpiprazol als neue Behandlungsoption bei der Schizophrenie ist akut und langfristig wirksam, verträglich und sicher. Bisher stehen vor allem Daten aus den Placebo-kontrollierten Zulassungsstudien zur Verfügung. In Zukunft ist zu erwarten, dass diese um direkte Vergleiche mit anderen Antipsychotika und naturalistische Daten ergänzt werden. Aus den bisher verfügbaren Daten zeichnen sich als Vorteile einer Behandlung mit Brexpiprazol vor allem die geringe Inzidenz von Akathisie und extrapyramidaler Symptomatik sowie unerwünschter Aktivierung oder Sedierung ab.
Interessenkonflikterklärung
Christoph Correll hat Vortragshonorare von der Janssen GmbH, Lundbeck GmbH und Otsuka Pharma GmbH erhalten.
Literatur
1. Angermeyer MC, Matschinger H. [Attitude of family to neuroleptics]. Psychiatr Prax 1999;26:171–4.
2. Beyer JL, Weisler RH. Adjunctive brexpiprazole for the treatment of major depressive disorder. Expert Opin Pharmacother 2016;17:2331–9.
3. Bridges JF, Beusterien K, Heres S, Such P, et al. Quantifying the treatment goals of people recently diagnosed with schizophrenia using best-worst scaling. Patient Prefer Adherence 2018;12:63–70.
4. Citrome L, Ota A, Nagamizu K, Perry P, et al. The effect of brexpiprazole (OPC-34712) and aripiprazole in adult patients with acute schizophrenia: results from a randomized, exploratory study. Int Clin Psychopharmacol 2016;31:192–201.
5. Citrome L, Stensbøl TB, Maeda K. The preclinical profile of brexpiprazole: what is its clinical relevance for the treatment of psychiatric disorders? Expert Rev Neurother 2015;15:1219–29.
6. Citrome L, Volavka J. Review: 15 antipsychotic drugs are more effective than placebo for the treatment of schizophrenia, but vary in their tolerability. Evid Based Ment Health 2014;17:9.
7. Citrome L. A review of the pharmacology, efficacy and tolerability of recently approved and upcoming oral antipsychotics: an evidence-based medicine approach. CNS Drugs 2013;27:879–911.
8. Citrome L. The ABC’s of dopamine receptor partial agonists – aripiprazole, brexpiprazole and cariprazine: the 15-min challenge to sort these agents out. Int J Clin Pract 2015;69:1211–20.
9. Citrome L. Activating and sedating adverse effects of second-generation antipsychotics in the treatment of schizophrenia and major depressive disorder: Absolute risk increase and number needed to harm. J Clin Psychopharmacol 2017;37:138–47.
10. Correll CU, Rubio JM, Kane JM. What is the risk-benefit ratio of long-term antipsychotic treatment in people with schizophrenia? World Psychiatry 2018;17:149–60.
11. Correll CU, Skuban A, Hobart M, Ouyang J, et al. Efficacy of brexpiprazole in patients with acute schizophrenia: Review of three randomized, double-blind, placebo-controlled studies. Schizophr Res 2016;174:82–92.
12. Correll CU, Skuban A, Ouyang J, Hobart M, et al. Efficacy and safety of brexpiprazole for the treatment of acute schizophrenia: A 6-week randomized, double-blind, placebo-controlled trial. Am J Psychiatry 2015;172:870–80.
13. Correll CU. From receptor pharmacology to improved outcomes: individualising the selection, dosing, and switching of antipsychotics. Eur Psychiatry 2010;25(Suppl 2):S12–21.
14. Dibonaventura M, Gabriel S, Dupclay L, Gupta S, et al. A patient perspective of the impact of medication side effects on adherence: results of a cross-sectional nationwide survey of patients with schizophrenia. BMC Psychiatry 2012;12:20.
15. Diefenderfer LA, Iuppa C. Brexpiprazole: A review of a new treatment option for schizophrenia and major depressive disorder. Ment Health Clin 2017;7:207–12.
16. Durgam S, Earley W, Li R, Li D, et al. Long-term cariprazine treatment for the prevention of relapse in patients with schizophrenia: A randomized, double-blind, placebo-controlled trial. Schizophr Res 2016;176:264–71.
17. Emsley R, Chiliza B, Asmal L, Harvey BH. The nature of relapse in schizophrenia. BMC Psychiatry 2013;13:50.
18. Fleischhacker WW, Hobart M, Ouyang J, Forbes A, et al. Efficacy and safety of brexpiprazole (OPC-34712) as maintenance treatment in adults with wchizophrenia: a randomized, double-blind, placebo-controlled study. Int J Neuropsychopharmacol 2017;20:11–21.
19. Fleischhacker WW. Aripiprazole. Expert Opin Pharmacother 2005;6:2091–101.
20. Forbes A, Hobart M, Ouyang J, Shi L, et al. A long-term, open-label study to evaluate the safety and tolerability of brexpiprazole as maintenance treatment in adults with schizophrenia. Int J Neuropsychopharmacol 2018;21:433–41.
21. De Hert M, Detraux J, van Winkel R, Yu W, et al. Metabolic and cardiovascular adverse effects associated with antipsychotic drugs. Nat Rev Endocrinol 2011;8:114–26.
22. Ivkovic J, Lindsten A, George V, Eriksson H, et al. Effect of brexpiprazole on prolactin: An analysis of short- and long-term studies in schizophrenia. J Clin Psychopharmacol 2019;39:13–9.
23. Kane JM, Skuban A, Hobart M, Ouyang J, et al. Overview of short- and long-term tolerability and safety of brexpiprazole in patients with schizophrenia. Schizophr Res 2016;174:93–8.
24. Kane JM, Skuban A, Ouyang J, Hobart M, et al. A multicenter, randomized, double-blind, controlled phase 3 trial of fixed-dose brexpiprazole for the treatment of adults with acute schizophrenia. Schizophr Res 2015;164:127–35.
25. Kinter ET, Schmeding A, Rudolph I, dosReis S, et al. Identifying patient-relevant endpoints among individuals with schizophrenia: an application of patient-centered health technology assessment. Int J Technol Assess Health Care 2009;25:35–41.
26. Laoutidis ZG, Luckhaus C. 5-HT2A receptor antagonists for the treatment of neuroleptic-induced akathisia: a systematic review and meta-analysis. Int J Neuropsychopharmacol 2014;17:823–32.
27. Leucht S, Chaimani A, Leucht C, Huhn M, et al. 60 years of placebo-controlled antipsychotic drug trials in acute schizophrenia: Meta-regression of predictors of placebo response. Schizophr Res 2018;201:315–23.
28. Leucht S, Cipriani A, Spineli L, Mavridis D, et al. Comparative efficacy and tolerability of 15 antipsychotic drugs in schizophrenia: a multiple-treatments meta-analysis. Lancet 2013;382:951–62.
29. Leucht S, Leucht C, Huhn M, Chaimani A, et al. Sixty years of placebo-controlled antipsychotic drug trials in acute schizophrenia: Systematic review, Bayesian meta-analysis, and meta-regression of efficacy predictors. Am J Psychiatry 2017;174:927–42.
30. Maeda K, Lerdrup L, Sugino H, Akazawa H, et al. Brexpiprazole II: antipsychotic-like and procognitive effects of a novel serotonin-dopamine activity modulator. J Pharmacol Exp Ther 2014;350:605–14.
31. Maeda K, Sugino H, Akazawa H, Amada N, et al. Brexpiprazole I: in vitro and in vivo characterization of a novel serotonin-dopamine activity modulator. J Pharmacol Exp Ther 2014;350:589–604.
32. Marder SR, Davis JM, Chouinard G. The effects of risperidone on the five dimensions of schizophrenia derived by factor analysis: combined results of the North American trials. J Clin Psychiatry 1997;58:538–46.
33. Marder SR, Hakala MJ, Josiassen MK, Zhang P, et al. Brexpiprazole in patients with schizophrenia: overview of short- and long-term phase 3 controlled studies. Acta Neuropsychiatr 2017;29:278–90.
34. McIntyre RS. Understanding needs, interactions, treatment, and expectations among individuals affected by bipolar disorder or schizophrenia: the UNITE global survey. J Clin Psychiatry 2009;70(Suppl 3):5–11.
35. Morosini PL, Magliano L, Brambilla L, Ugolini S, et al. Development, reliability and acceptability of a new version of the DSM-IV social and occupational functioning assessment scale (SOFAS) to assess routine social functioning. Acta Psychiatr Scand 2000;101:323–9.
36. Naber D, Hansen K, Forray C, Baker RA, et al. Qualify: a randomized head-to-head study of aripiprazole once-monthly and paliperidone palmitate in the treatment of schizophrenia. Schizophr Res 2015;168:498–504.
37. Nasrallah H, Morosini P, Gagnon DD. Reliability, validity and ability to detect change of the personal and social performance scale in patients with stable schizophrenia. Psychiatry Res 2008;161:213–24.
38. Németh G, Laszlovszky I, Czobor P, Szalai E, et al. Cariprazine versus risperidone monotherapy for treatment of predominant negative symptoms in patients with schizophrenia: a randomised, double-blind, controlled trial. Lancet 2017;389:1103–13.
39. Otsuka. ABILIFY prescribing information. 2016 [cited 2019 Feb 7]; available from: https://www.otsuka-us.com/media/static/Abilify-PI.pdf.
40. Otsuka. REXULTI (Brexpiprazole) tablets, for oral use. Prescribing information. 2015 [cited 2019 Feb 6];Available from: http://www.otsuka-us.com/Products/Documents/Rexulti.PI.pdf.
41. Pigott TA, Carson WH, Saha AR, Torbeyns AF, et al. Aripiprazole for the prevention of relapse in stabilized patients with chronic schizophrenia: a placebo-controlled 26-week study. J Clin Psychiatry 2003;64:1048–56.
42. Potkin SG, Loze J-Y, Forray C, Baker RA, et al. Reduced sexual dysfunction with aripiprazole once-monthly versus paliperidone palmitate: results from QUALIFY. Int Clin Psychopharmacol 2017;32:147–54.
43. Robinson DG, Gallego JA, John M, Petrides G, et al. A randomized comparison of aripiprazole and risperidone for the acute treatment of first-episode schizophrenia and related disorders: 3-month outcomes. Schizophr Bull 2015;41:1227–36.
44. Shapiro DA, Renock S, Arrington E, Chiodo LA, et al. Aripiprazole, a novel atypical antipsychotic drug with a unique and robust pharmacology. Neuropsychopharmacology 2003;28:1400–11.
45. Stahl SM. Stahl’s essential psychopharmacology: Neuroscientific basis and practical application. 4th edition. Cambridge: Cambridge University Press, 2013.
46. Stanghellini G, Bolton D, Fulford WKM. Person-centered psychopathology of schizophrenia: building on Karl Jaspers’ understanding of patient‘s attitude toward his illness. Schizophr Bull 2013;39:287–94.
47. Wagner E, Hasan A. Cariprazin – eine neue medikamentöse Therapieoption in der Schizophreniebehandlung. Psychopharmakotherapie 2018;25:278–85.
48. Yoon S, Jeon SW, Ko Y-H, Patkar AA, et al. Adjunctive brexpiprazole as a novel effective strategy for treating major depressive disorder: A systematic review and meta-analysis. J Clin Psychopharmacol 2017;37:46–53.
Prof. Dr. med. Christoph U. Correll, Charité – Universitätsmedizin Berlin, Campus Virchow Klinikum, Klinik für Psychiatrie, Psychosomatik und Psychotherapie des Kindes- und Jugendalters, Augustenburger Platz 1, 13353 Berlin, E-Mail: christoph.correll@charite.de und The Donald and Barbara Zucker School of Medicine at Hofstra/Northwell, 500 Hofstra Blvd, Hempstead, NY 11549, USA.
Brexpiprazole: a new D2 partial agonist as a treatment option for patients with schizophrenia
The treatment of schizophrenia most often necessitates continued antipsychotic pharmacotherapy. In order to facilitate optimized adherence, it is important that the chosen medication exhibits good tolerability and a favorable adverse event profile. A new partial agonist at the dopaminergic D2 receptor, brexpiprazole, is now available. The efficacy, safety and tolerability of brexpiprazole has been shown in short- and long-term trials. The advantages of brexpiprazole treatment comprise primarily the low incidence of akathisia und extrapyramidal symptoms as well as unwanted activation or sedation, while at the same time having a good cardiometabolic profile.
Key words: Partial agonist, dopamine schizophrenia, antipsychotic, brexpiprazole
Psychopharmakotherapie 2019; 26(04):206-218
