Dieter Naber, Hamburg, Jens Kuhn, Oberhausen/Köln, Karolina Leopold, Berlin, Wolfgang Janetzky, Hamburg, und Rita Wietfeld, Witten
Bei der Behandlung der Schizophrenie können phasenspezifisch unterschiedliche Behandlungsziele leitend sein: Bei einer akuten psychotischen Episode soll durch den frühen Einsatz von Antipsychotika eine rasche Remission der klinischen Symptomatik erreicht werden. Insbesondere bei ersterkrankten Patienten ist eine frühe symptomatische Remission ein starker Prädiktor für einen guten Funktionsstatus und eine Verbesserung der Lebensqualität [1, 2, 11]. Nach erfolgreicher Akuttherapie verringert eine kontinuierliche antipsychotische Therapie das Risiko von Rückfällen und die damit assoziierten Folgen, insbesondere den Verlust des Funktionsniveaus [28]. Bereits in frühen Krankheitsstadien und in der Langzeittherapie sind Depot-Formulierungen eine wertvolle Behandlungsalternative zu oralen Antipsychotika. Die Patienten profitieren von einer effektiven Rückfallprophylaxe und einer Reduktion von Hospitalisierungen [13, 14]. Ein weiterer Vorteil ist auch die bessere Lenkung und Begleitung des Patienten, da die ständige Diskussion um die Dosierung und Einnahme der Medikation entfällt und so mehr Zeit zum Aufbau einer vertrauensvollen Arzt-Patienten-Beziehung bleibt. Dazu trägt auch die regelmäßige Applikation des Depots in der Praxis bei [13]. Auch von den Angehörigen wird eine Depotmedikation oft als entlastend empfunden, weil damit die tägliche Medikamenteneinnahme des Betroffenen entfällt und so auch die damit verbundene Konfrontation mit der Erkrankung.
Die Möglichkeit der individualisierten Therapie als Kombination aus pharmakologischen und psychotherapeutischen Elementen führte zu einer Erweiterung der Behandlungsziele um ehrgeizigere Parameter wie die Verbesserung des Funktionsniveaus und der Lebensqualität [3, 9]. Das Erreichen einer klinischen Remission (Symptomfreiheit) ist nur begrenzt mit einer Verbesserung der Lebensqualität und des Funktionsniveaus assoziiert [11, 33]. Insgesamt unterscheiden sich die Lebensqualitätsziele junger schizophrener Patienten nicht von denen gesunder Individuen: soziale Integration, Ausbildung und Beruf, Aufbau von sozialen Beziehungen und Gründung einer Familie. Die Verbesserung der Lebensqualität ist daher heute neben der bestmöglichen Normalisierung des Funktionsniveaus ein wichtiges Behandlungsziel, damit die Patienten „ein Leben so normal wie möglich“ leben können. Die Lebensqualität kann heute mithilfe krankheitsspezifischer, validierter Beurteilungsinstrumente wie der Heinrichs-Carpenter Quality-of-Life Scale (QLS) gemessen werden [6]. Die QLS erfasst die gesundheitsbezogene Lebensqualität und Funktionsfähigkeit von Patienten mit Schizophrenie anhand von 21 Items aus vier Domänen (zwischenmenschliche Beziehungen, instrumentelle Rolle, intrapsychische Grundbefindlichkeit sowie alltägliche Dinge und Aktivitäten; Gesamtscore 0 bis 126). Ein Anstieg der Werte zeigt eine Verbesserung der Lebensqualität und Funktionsfähigkeit an; eine Veränderung um mehr als fünf Punkte ist als klinisch relevant anzusehen [4].
Die QUALIFY-Studie
Die QUALIFY-Studie (Quality of life with Abilify Maintena®, Registernr. NCT01795547) war die erste Studie, die zwei atypische Depot-Antipsychotika in einem naturalistischen Setting bei Patienten mit Schizophrenie im Hinblick auf die Beeinflussung der Lebensqualität und des Funktionsniveaus als primärem Studienendpunkt direkt miteinander verglich [20]. Dabei wurde ein randomisiertes Open-Label-Design gewählt. Auch wenn offene Studien Limitationen aufweisen, sind sie eine wesentliche wissenschaftliche Ergänzung zu Zulassungsstudien mit ausgewählten Patientengruppen, da deren Ergebnisse in die tägliche Praxis übertragen und ergänzt werden können.
Die Beurteilung der Lebensqualität (primärer Endpunkt), gemessen mit dem QLS-Score, sowie die Wirksamkeit, Sicherheit und Verträglichkeit der antipsychotischen Medikation (sekundärer Endpunkt), gemessen mit dem Investigator‘s Assessment Questionnaire (IAQ), erfolgte Auswerter-verblindet. Die weiteren sekundären Endpunkte (u. a. Arbeitsfähigkeit gemäß Readiness for Work Questionnaire [WoRQ]) waren nicht verblindet.
Ziel der Studie war, Aripiprazol-Depot auf Nichtunterlegenheit gegenüber der Vergleichssubstanz zu prüfen. Nach Nachweis der Nichtunterlegenheit von Aripiprazol-Depot gegenüber dem Komparator wurde auf Überlegenheit geprüft. Bei der statistischen Auswertung wurden bei sekundären Analysen die p-Werte nominal betrachtet und nicht für multiples Testen und Vergleichen korrigiert. Die Studie bestand aus einer Screening- und drei Behandlungsphasen, gefolgt von einem Sicherheits-Follow-up:
- Umstellungsphase auf orales Aripiprazol oder orales Paliperidon (3 Wochen)
- Einleitung der monatlichen Depotbehandlung gemäß Fachinformation (Aripiprazol-Depot oder Paliperidonpalmitat) (5 Wochen)
- Fortsetzung der monatlichen Depotbehandlung (20 Wochen)
Aripiprazol ist ein partieller Agonist am Dopamin-D2- und am -D3-Rezeptor und an Serotonin-5-HT1A-Rezeptoren und wirkt antagonistisch an 5-HT2A-Rezeptoren. Paliperidon wirkt antagonistisch an Dopamin-D2- und 5-HT2A-Rezeptoren.
Aripiprazol-Depot wurde als Erhaltungsdosis von 400 mg einmal monatlich verabreicht. In Abhängigkeit von der individuellen Verträglichkeit war eine Reduktion auf 300 mg einmal monatlich möglich. Das Depot Paliperidonpalmitat wurde in einer flexiblen Dosis von 50 bis 150 mg einmal monatlich verabreicht. Als Teilnehmer wurden 295 Patienten von 18 bis 60 Jahren mit einer DSM-IV-TR-Diagnose einer Schizophrenie und stabilem Krankheitsverlauf rekrutiert, die eine Umstellung des Präparats wegen ungenügender Wirksamkeit, Verträglichkeitsproblemen oder mangelnder Adhärenz benötigten und nach Ansicht des behandelnden Arztes von einer Umstellung auf ein Depot-Antipsychotikum profitieren könnten. Gefordert wurde ein CGI-S-Score (Clinical global impression of severity) > 3 bis < 5 (leicht bis deutlich krank) beim Screening und zu Studienbeginn (Baseline) und eine Einstellung mit oralen Antipsychotika innerhalb der letzten drei Monate vor dem Screening.
Primärer (Auswerter-verblindeter) Studienendpunkt war die Veränderung der Lebensqualität, gemessen mit der QLS, von Baseline bis Woche 28. Sekundäre, nicht verblindete Endpunkte waren unter anderem die Veränderung der globalen Beurteilung der Symptomschwere (CGI-S) und der Arbeitsfähigkeit, abgefragt mithilfe des WoRQ, sowie Sicherheits- und Verträglichkeitsparameter [24].
Den Patienten, die bis zum Ende der QUALIFY-Studie Aripiprazol-Depot erhielten, wurde eine Fortführung der Therapie mit Aripiprazol-Depot über weitere 24 Wochen unter den kontrollierten Bedingungen einer klinischen Prüfung (Open-Label-Extension-Study) angeboten. 88 % dieser 100 Patienten stimmten der Weiterbehandlung zu. Baseline für die Extensionsstudie entspricht dem Besuch in Woche 28 der QUALIFY-Studie. Primärer Endpunkt waren Sicherheit und Verträglichkeit. Sekundäre nicht verblindete Endpunkte waren die Veränderungen der Lebensqualität (QLS) und des klinischen Gesamteindrucks (CGI) [19].
Ergebnisse
Die mittlere Dosierung der monatlichen Antipsychotika-Gabe betrug in Woche 24 für Aripiprazol-Depot 387 mg und Paliperidonpalmitat 110 mg. Der QLS-Gesamtscore veränderte sich unter Aripiprazol-Depot um 7,5 Punkte und unter Paliperidonpalmitat um 2,8 Punkte (Differenz 4,7; 95%-Konfidenzintervall [KI] 0,32–9,02; p = 0,036). Der Unterschied zwischen den beiden Behandlungsgruppen war in der achten Woche und nach 28 Wochen statistisch signifikant (p < 0,05). Die Verbesserung des QLS-Gesamtscores unter Aripiprazol-Depot ab Studienbeginn über die 28-wöchige Behandlungsdauer kann als klinisch relevant eingestuft werden [4]. Bei Betrachtung der QLS-Domänen zeigte sich in drei der vier Domänen (zwischenmenschliche Beziehungen, instrumentelle Rolle, Alltagsgegenstände und -aktivitäten) eine numerisch stärkere Besserung unter Aripiprazol-Depot im Vergleich zu Paliperidonpalmitat, der Unterschied im Hinblick auf die Verbesserung der intrapsychischen Grundlagen erreichte Signifikanz (p = 0,039). Bei den Items „soziale Initiative“, „Zielstrebigkeit“ und „planlose Beschäftigung/Untätigkeit“ zeigten sich unter Aripiprazol-Depot statistisch signifikante Vorteile [20, 26]. In einer vordefinierten, explorativen, altersstratifizierten Subgruppenanalyse der QUALIFY-Basisstudie profitierte die Gruppe der Patienten ≤ 35 Jahre stärker von Aripiprazol-Depot als die älteren Teilnehmer. In Woche 28 lag der mittlere QLS-Gesamtscore in dieser jüngeren Altersgruppe statistisch um 10,7 Punkte signifikant höher als unter Paliperidonpalmitat (p = 0,037) (Abb. 1). Auch im Hinblick auf den klinischen Gesamteindruck (CGI-S) war die Verbesserung bei den Jüngeren stärker ausgeprägt. In der Aripiprazol-Depot-Gruppe war die mittlere Veränderung des CGI-S-Scores signifikant stärker ausgeprägt und wies eine Differenz von 0,44 Punkten zu Paliperidonpalmitat auf [20].
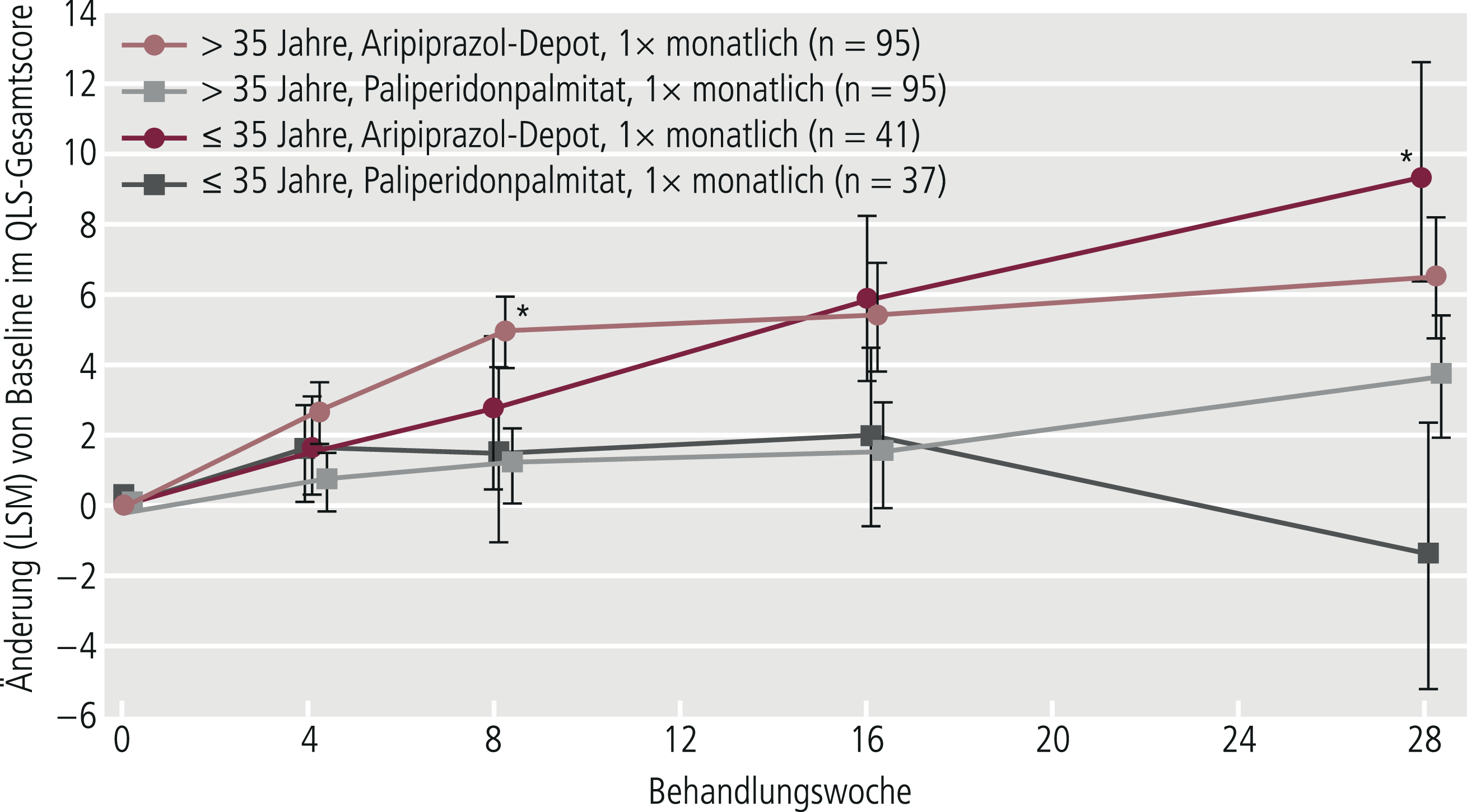
Abb. 1. Veränderung des mittleren QLS-Gesamtscores bei Patienten ≤ 35 Jahre und > 35 Jahre unter Aripiprazol-Depot und Paliperidonpalmitat (mod. nach [20]); LSM: Least-Squares Means; * p < 0,05 vs. Paliperidonpalmitat in der gleichen Altersgruppe
Die Verbesserung der Arbeitsfähigkeit, beurteilt anhand des WoRQ-Fragebogens, verbesserte sich im Therapieverlauf unter Aripiprazol-Depot signifikant stärker als unter Paliperidonpalmitat (angepasstes Odds-Ratio [OR] 2,67; 95%-KI 1,39–5,14; p = 0,003). Bis Woche 28 stieg der Anteil als arbeitsfähig eingeschätzter Patienten unter Aripiprazol-Depot um 60 % (von 32,8 % auf 52,8 %, nichtverblindete Gesamtbeurteilung). Demgegenüber stieg der Anteil unter Paliperidonpalmitat um 10 % (von 29,6 % auf 32,6 %) [21, 24, 26].
Unter beiden Depot-Formulierungen berichteten Patienten nach 28 Wochen von einer Verbesserung ihres subjektiven Wohlbefindens (SWN-S, Subjective wellbeing under neuroleptics) (p = 0,56). Die Unterschiede zwischen beiden Behandlungsarmen erreichten keine statistische Signifikanz, wobei eine numerisch stärkere Verbesserung unter Aripiprazol-Depot im Vergleich zu Paliperidonpalmitat in den Items mentale sowie physische Funktionen und Selbstkontrolle dokumentiert wurde. Dies spiegelt sich ebenfalls im TooL (Tolerability and quality of life questionnaire) wider. Der Effekt der unerwünschten Wirkung auf die Lebensqualität verringerte sich in Woche 28 in beiden Gruppen, wobei es auch hier eine numerisch stärkere Verbesserung unter Aripiprazol-Depot gab (p = 0,10) [26].
In der klinisch relevanten Subgruppe von Patienten mit Drogenmissbrauch (Aripiprazol-Depot 19 %; Paliperidonpalmitat 22 %) ergab sich in einer Post-hoc-Analyse ein deutlicher, aber nicht signifikanter Unterschied hinsichtlich der Veränderung der Lebensqualität zugunsten von Aripiprazol-Depot (p = 0,17) [18a]. Insgesamt wurde mit Aripiprazol-Depot unabhängig von der Symptomschwere in allen Subgruppen eine deutlichere Verbesserung der Lebensqualität erreicht als mit Paliperidonpalmitat [29].
In einer weiteren Post-hoc-Analyse der QUALIFY-Daten wurde das Auftreten sexueller Dysfunktion untersucht, die mittels der ASEX-Skala (Arizona sexual experience scale) durch den Patienten bewertet wurde. Zusätzlich wurden die Prolactin-Konzentrationen im Serum vor und nach der Behandlung erfasst. Unter Aripiprazol-Depot sank das Risiko einer sexuellen Dysfunktion um 30 %. Ebenso sank der Prolactin-Spiegel sowohl bei Männern als auch bei Frauen (–150,6 [274,4] mIU/l) [21, 25, 27] (Abb. 2).
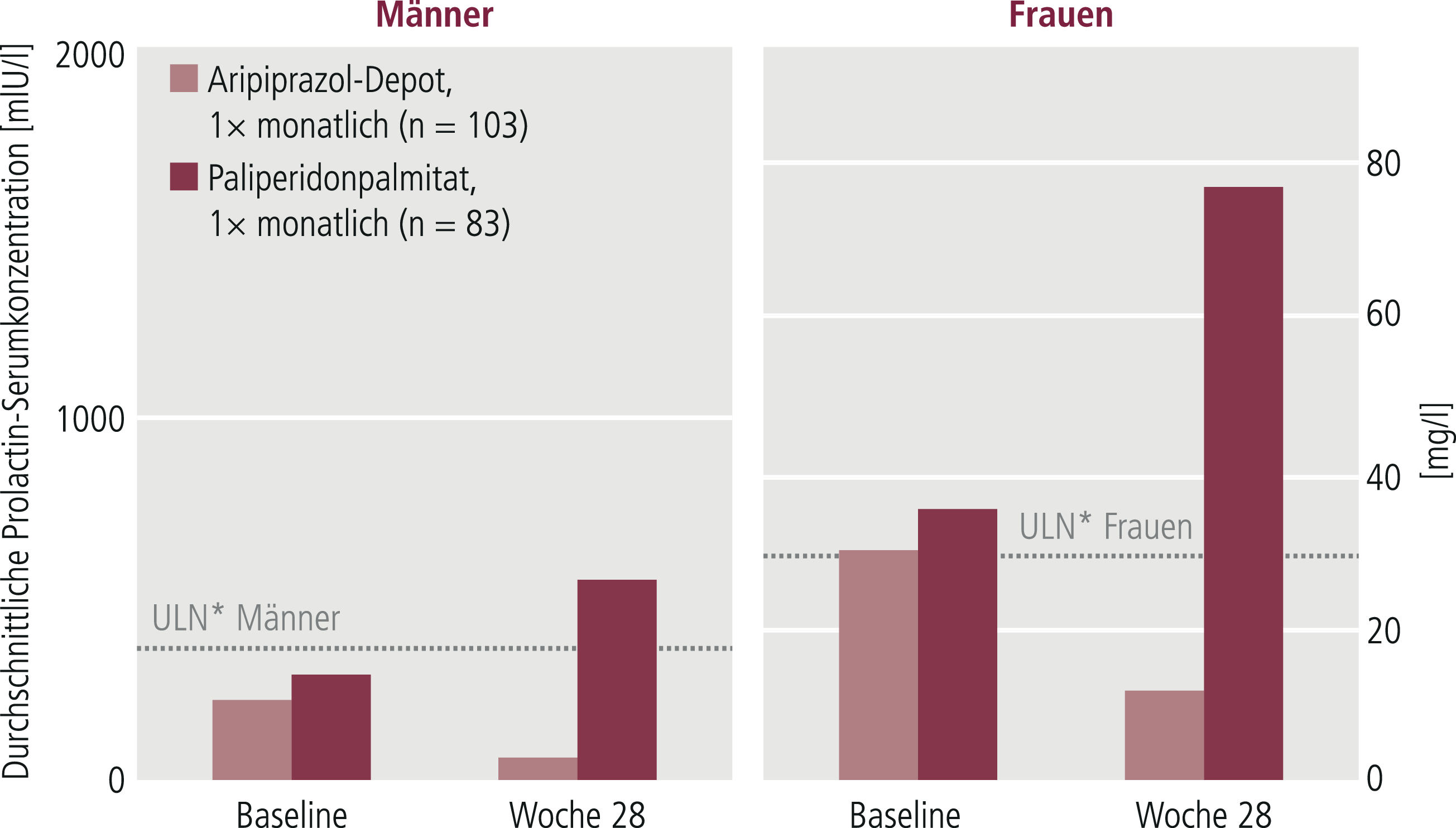
Abb. 2. Prolactin-Spiegel – vor und nach der Behandlung mit Depot-Antipsychotika (mod. nach [25]); ULN: Höchstgrenze (upper limit of normal)
Studienabbrüche aufgrund von unerwünschten Ereignissen (TEAEs [treatment emergent adverse events]) traten in 11 % (Aripiprazol-Depot: 16/144) bzw. 20 % (Paliperidonpalmitat: 27/137) der Fälle auf [20]. Die TEAEs während der 20-wöchigen Hauptbehandlungsphase (ohne zusätzliche orale Gabe) waren Gewichtszunahmen (10,1 % bzw. 15,6 %), psychotische Störungen (2,5 % bzw. 5,5 %) und Insomnie (2,5 % bzw. 5,5 %) [19]. Prolactin-Erhöhungen über den oberen Grenzwert und damit das Risiko für sexuelle Dysfunktion traten bei beiden Geschlechtern nur unter Paliperidonpalmitat auf [21, 25, 27].
In der QUALIFY-Extensionsstudie verbesserte sich bei den Patienten nach 52 Wochen die Lebensqualität gemäß QLS-Gesamtscore kontinuierlich weiter [19]. Damit einher ging eine Stabilisierung des in der Hauptstudie erreichten und unabhängig vom vorherigen Schweregrad gezeigten klinischen Gesamteindrucks (CGI-S).
Diskussion
Neurobiologische Grundlage der heutigen antipsychotischen Therapien ist eine Dysbalance der zerebralen dopaminergen Neurotransmission (Dopaminhypothese). Neben einer breiteren Wirksamkeit wurde mit der Entwicklung neuer Zweitgenerations-Antipsychotika auch eine bessere Verträglichkeit zugunsten einer besseren Lebensqualität angestrebt. Ein wesentlicher Grund für die bessere Nutzen-Verträglichkeits-Relation der Zweitgenerations-Antipsychotika ist ihr niedrigeres Risiko extrapyramidal-motorischer Störungen (EPMS) sowie die Reduktion sexueller Dysfunktion [7, 11, 30]. Das Auftreten von EPMS ist nach gängiger Auffassung mit einer Bindung an über 80 % der striatalen D2-Rezeptoren assoziiert. Eine niedrige Blockade der D2-Rezeptoren erscheint daher besonders bei einer langfristigen Behandlung wünschenswert, um das subjektive Befinden und die Lebensqualität der Patienten nicht zu verschlechtern [17]. Die Mechanismen, über die Zweitgenerations-Antipsychotika das EPMS-Risiko verringern, sind unterschiedlich und reichen von einer raschen molekularen Dissoziation der Substanz vom D2-Rezeptor („loose binding“) bis hin zu einer starken Blockade serotonerger 5-HT2A-Rezeptoren [10].
Aripiprazol unterscheidet sich von allen anderen Antipsychotika durch seine partiell agonistische Wirkung am D2- und D3-Rezeptor. Es besitzt daher bei einer guten Wirksamkeit auf Positiv- und Negativsymptomatik nur ein sehr geringes Risiko für EPMS und Prolactin-Erhöhungen als Risikofaktor für eine sexuelle Dysfunktion. Die Bindung an 5-HT1A-Rezeptoren könnte möglicherweise aktivierende Effekte der Neuroplastizität auslösen [18]. Eine Reihe von offenen und Placebo-kontrollierten Studien belegt hierzu eine gute Wirksamkeit von Aripiprazol als Add-on-Medikation bei therapieresistenten Depressionen oder Angsterkrankungen. Allerdings ist Aripiprazol für keine der beiden Erkrankungen zugelassen. In diesem Zusammenhang werden auch Unterschiede in der Beeinflussung des Belohnungssystems als Grund für die differenzielle Entwicklung der QLS-Scores diskutiert [8].
Die Leitlinien definieren als Behandlungsziel das Erreichen einer symptomatischen und funktionellen Remission und bestmöglichen Lebensqualität (Recovery) [5]. Mittel- und langfristig gilt es, die Funktionalität und damit die Lebensqualität als Voraussetzung für eine möglichst normale Lebensführung zu verbessern. Die meisten Patienten unterschätzen die Risiken eines Rückfalls und die Konsequenzen beim Absetzen der antipsychotischen Medikation. Leucht et al. zeigten in einer Metaanalyse, dass eine stabile Einstellung remittierter Patienten auf eine antipsychotische Erhaltungstherapie über eine Dauer von drei bis sechs Jahren zu einer signifikanten Reduktion von Rückfallhäufigkeit, Re-Hospitalisierungen, Suiziden und gewalttätigen Verhaltens insgesamt führt. Die Ergebnisse weisen darauf hin, dass eine Behandlung mit Antipsychotika im Vergleich zu Placebo zu einer Verbesserung der Lebensqualität führt. In den explorativen Subgruppenanalysen war das relative Risiko eines Rückfalls durch Depot-Antipsychotika signifikant geringer als mit oralen Antipsychotika [15].
Die subjektive Bewertung der Lebensqualität unterscheidet sich erheblich von der psychiatrischen Perspektive. So zeigen mehrere Studien, dass die Veränderung der subjektiven Lebensqualität und die Psychopathologie nur wenig miteinander korrelieren [22, 23]. Arzt und Patient haben konkrete Erwartungen an das Behandlungsergebnis, gewichten jedoch die Faktoren zur Bewertung des Behandlungserfolgs und der Lebensqualität teilweise unterschiedlich. Während die Patientenkommunikation auf allgemeinen emotionalen und praktischen Aspekten ihres täglichen Lebens beruht, orientieren sich Denkweise und Kommunikation von Ärzten eher an objektivierbaren, symptombezogenen Parametern. Für die Behandlung wünscht sich der Patient von seinem Arzt eine gute Erreichbarkeit, Vertrauen und Empathie sowie eine gute Kommunikation [16, 31, 32].
Die industriegesponsorte QUALIFY-Studie wurde in einem offenen Design angelegt, wenn auch die QLS-Veränderungen verblindet beurteilt wurden. Grundsätzlich unterliegen offene Studien bestimmten Einschränkungen hinsichtlich ihrer Aussagekraft. Daher sind weitere Vergleichsstudien notwendig, um eine endgültige Beurteilung abgeben zu können. So ist es prinzipiell nicht auszuschließen, dass das Wissen um die Behandlung die Antworten der Patienten beeinflusst haben könnte. Dieses Caveat gilt aber aufgrund der Randomisierung für beide Studienarme. Die Validität und Aussagekraft der in der QUALIFY-Studie zusätzlich zur Arzt-Beurteilung erhobenen Patienten-Beurteilungen wird unterstrichen durch ihre hohe Konsistenz, gleichgültig, ob die Beurteilung verblindet oder unverblindet erfolgte.
In der QUALIFY-Studie verbesserten sich die QLS-Scores bei Patienten ≤ 35 Jahre unter Aripiprazol-Depot signifikant stärker als bei älteren Patienten. Auch wenn diese vordefinierten Analysen als explorativ einzustufen sind, unterstreichen die deutlichen, statistisch signifikanten Unterschiede zwischen den Altersgruppen die Notwendigkeit einer frühen Behandlung mit Depot-Antipsychotika. Auch zeigten jüngere Patienten ein geringeres Risiko für eine sexuelle Dysfunktion und einen geringeren Anstieg des Prolactin-Spiegels als unter Paliperidonpalmitat [25]. Diese unterschiedlichen Effekte der beiden Antipsychotika sind möglicherweise auch auf das unterschiedliche Verhalten am Dopamin-D2-Rezeptor zu erklären. Auch scheinen junge Patienten sensibler auf Medikamenten-induzierte Nebenwirkungen zu reagieren. Weiter können Veränderungen der Therapiezufriedenheit und Lebensqualität zu dem gezeigten deutlichen Unterschied bei den jüngeren gegenüber den älteren Patienten mit Schizophrenie beigetragen haben. Das entspricht Therapieerfahrungen, nach denen bei älteren, chronisch schizophrenen Patienten mit einer antipsychotischen Therapie nur noch vergleichsweise geringe Behandlungserfolge erzielt werden können [12].
Die Ergebnisse der randomisierten Vergleichsstudie QUALIFY unterstreichen, Zweitgenerations-Antipsychotika in Depotform nicht als homogene Wirkstoffgruppe anzusehen, vergleichbar mit oralen Zweitgenerations-Antipsychotika. Die gezeigten Unterschiede in wichtigen patientenrelevanten Parametern (PROs) wie der Lebensqualität können nicht nur zu einer besseren langfristigen klinischen Prognose beitragen, sondern auch zu einem sinnvolleren Einsatz von Antipsychotika unter medizinökonomischen Aspekten. Bereits junge Patienten mit einer Erstmanifestation können von einer Einstellung auf eine antipsychotische Depotmedikation profitieren und daher sollte diese häufiger eingesetzt und nicht nur Patienten mit schlechter Adhärenz vorbehalten werden.
Interessenkonflikterklärung
Dieter Naber hat Vortragshonorare von Lundbeck und Otsuka Pharma erhalten.
Jens Kuhn hat von Janssen, Lilly, Lundbeck, Otsuka Pharma, Schwabe und Servier Vortragshonorare und Reisekostenunterstützung erhalten. Außerdem hat er Forschungszuwendungen von Medtronic GmbH erhalten.
Karolina Leopold hat Vortragshonorare von AstraZeneca, BMS, Janssen-Cilag, Lilly, Lundbeck, Otsuka und Pfizer sowie Forschungszuwendungen von AstraZeneca, Janssen-Cilag und Otsuka Pharma erhalten.
Wolfgang Janetzky ist Mitarbeiter von Lundbeck.
Rita Wietfeld hat Vortragshonorare von Lundbeck und Otsuka Pharma erhalten.
Literatur
1. Bodatsch M, Kuhn J. Differenzialindikation medikamentöser Erhaltungstherapie in der Schizophrenie-Behandlung. Psychopharmakotherapie 2016;23:50–7.
2. Bodén R, Sundström J, Lindström E, Lindström L. Association between symptomatic remission and functional outcome in first-episode schizophrenia. Schizophr Res 2009;107:232–7.
3. Deutschenbaur L, Lambert M, Walter M, Naber D. Pharmakologische Langzeitbehandlung schizophrener Erkrankungen. Nervenarzt 2014;85:363–77.
4. Falissard B, Sapin C, Loze JY, Landsberg W, et al. Defining the minimal clinically important difference (MCID) of the Heinrichs-carpenter quality of life scale (QLS). Int J Methods Psychiatr Res 2016;25:101–11.
5. Hasan A, Falkai P, Wobrock T, Lieberman J, et al. World Federation of Societies of Biological Psychiatry (WFSBP) guidelines for biological treatment of schizophrenia, part 2: update 2012 on the long-term treatment of schizophrenia and management of antipsychotic-induced side effects. World J Biol Psychiatry 2013;14:2–44.
6. Heinrichs DW, Hanlon TE, Carpenter WT Jr. The quality of life scale: an instrument for rating the schizophrenic deficit syndrome. Schizophr Bull 1984;10:388–98.
7. Hofer A, Rettenbacher MA, Widschwendter CG, Kemmler G, et al. Correlates of subjective and functional outcomes in outpatient clinic attendees with schizophrenia and schizoaffective disorder. Eur Arch Psychiatry Clin Neurosci 2006;256:246–55.
8. Juckel G. Inhibition of the reward system by antipsychotic treatment. Dialogues Clin Neurosci 2016;18:109–14.
9. Juckel G. Therapieziel soziale Funktionsfähigkeit. Der Neurologe und Psychiater 2014;15:46–54.
10. Kapur S, Seeman P. Does fast dissociation from the dopamine D2-receptor explain the action of atypical antipsychotics? A new hypothesis. Am J Psychiatry 2001;158:360–9.
11. Karow A, Wittmann L, Schöttle D, Schäfer I. The assessment of quality of life in clinical practice in patients with schizophrenia. Dialogues Clin Neurosci 2014;16:185–95.
12. Konstantakopoulos G, Ploumpidis D, Oulis P, Patrikelis P, et al. Apathy, cognitive deficits and functional impairment in schizophrenia. Schizophr Res 2011;133:193–8.
13. Kühn KU, Wiedemann K, Hellweg K, Möller HJ, et al. Stellenwert von Depotformulierungen in der Langzeittherapie der Schizophrenie. Fortschr Neurol Psychiat 2014;82:557–65.
14. Leucht C, Heres S, Kane JM, Kissling W, et al. Oral versus depot antipsychotic drugs for schizophrenia – a critical systematic review and meta-analysis of randomised long-term trials. Schizophr Res 2011;127:83–92.
15. Leucht S, Tardy M, Komossa K, Heres S, et al. Antipsychotic drugs versus placebo for relapse prevention in schizophrenia: a systematic review and meta-analysis. Lancet 2012;379:2063–71.
16. Loughland C, Kelly B, Ditton-Phare P, Sandhu H, et al. Improving clinician competency in communication about schizophrenia: a pilot educational program for psychiatry trainees. Acad Psychiatry 2015;39:160–4.
17. Mizrahi R, Rusjan P, Agid O, Graff A, et al. Adverse subjective experience with antipsychotics and its relationship to striatal and extrastriatal D2 receptors: a PET study in schizophrenia. Am J Psychiatry 2007;164:630–7.
18. Müller W. Therapeutische Anwendung von Aripiprazol-Depot. Psychopharmakotherapie 2014;21:97–105.
18a. Naber D, Baker RA, Eramo A, Forray C, et al. Effects of aripiprazole once-monthly and paliperidone palmitate in patients with schizophrenia and concomitant substance use: A post-hoc analysis of QUALIFY, a head-to-head study. Poster präsentiert beim ACNP Congress; 6.10.12.2015, Hollywood (Florida), USA.
19. Naber D, Baker RA, Eramo A, Forray C, et al. Long-term effectiveness of aripiprazole once-monthly for schizophrenia is maintained in the QUALIFY extension study. Schizophr Res 2018;192:205–10.
20. Naber D, Hansen K, Forray C, Baker RA. Qualify: a randomized head-to-head study of aripiprazole once-monthly and paliperidone palmitate in the treatment of schizophrenia. Schizophr Res 2015;168:498–504.
21. Naber D, Hansen K, Forray C, Baker RA, et al. Secondary effectiveness outcomes in QUALIFY, a head-to-head clinical study of aripiprazole once-monthly and paliperidone palmitate in schizophrenia. Poster präsentiert beim Annual Meeting der American Society of Clinical Psychopharmacology (ASCP); 22.-25.6.2015, Miami, USA.
22. Naber D, Moritz S, Lambert M, Pajonk FG, et al. Improvement of schizophrenic patients’ subjective well-being under atypical antipsychotic drugs. Schizophr Res 2001;50:79–88. Erratum in: Schizophr Res 2002;57:125.
23. Naber D, Riedel M, Klimke A, Vorbach EU, et al. Randomized double blind comparison of olanzapine vs. clozapine on subjective well-being and clinical outcome in patients with schizophrenia. Acta Psychiatr Scand 2005;111:106–15.
24. Potkin SG, Bugarski-Kirola D, Edgar CJ, Soliman S, et al. Psychometric evaluation of the work readiness questionnaire in schizophrenia. CNS Spectr 2016;21:199–206.
25. Potkin SG, Loze J-Y, Forray C, Baker RA, et al. Effects of aripiprazole once-monthly and paliperidone palmitate on QLS domain scores: results from QUALIFY, a randomized, head-to-head clinical study. Poster präsentiert beim Annual NEI Psychopharmacology Congress; 12.-15.11.2015, Orlando, USA.
26. Potkin SG, Loze J-Y, Forray C, Baker RA, et al. Multidimensional assessment of functional outcomes in schizophrenia: Results from QUALIFY, a head-to-head trial of aripiprazole once-monthly and paliperidone palmitate. Int J Neuropsychopharmacol 2017;20:40–9.
27. Potkin SG, Loze JY, Forray C, Baker RA, et al. Reduced sexual dysfunction with aripiprazole once-monthly versus paliperidone palmitate: results from QUALIFY. Int Clin Psychopharmacol 2017;32:147–54.
28. Roll SC, Knecht G, Kuhn J, Spittler S. Antipsychotika-Depotbehandlung im Wandel der Zeit. Nervenheilkunde 2016;35:41–9.
29. Salzmann P, et al. Poster at the ECNP Congress, Vienna, Austria, 17–20 Sept 2016.
30. Schimmelmann BG, Paulus S, Schacht M, Tilgner C, et al. Subjective distress related to side effects and subjective well-being in first admitted adolescents with early-onset psychosis treated with atypical antipsychotics. J Child Adolesc Psychopharmacol 2005;15:249–58.
31. Schneider B, Scissons H, Arney L, Benson G, et al. Communication between people with schizophrenia and their medical professionals: a participatory research project. Qual Health Res 2004;14:562–77.
32. Theisel S, Schielein T, Spießl H. Der „ideale“Arzt aus Sicht psychiatrischer Patienten. Psychiatr Prax 2010;37:279–84.
33. World Health Organization (WHO). The World Health Organization Quality of Life assessment (WHOQOL): position paper from the World Health Organization. Soc Sci Med 1995;41:1403–9.
Prof. Dr. med. Dieter Naber, Klinik und Poliklinik für Psychiatrie, Universitätsklinikum Hamburg-Eppendorf, Martinistraße 52, 20246 Hamburg, E-Mail: naber@uke.de
Prof. Dr. med. Jens Kuhn, Klinik für Psychiatrie, Psychotherapie und Psychosomatik, Johanniter Krankenhaus Oberhausen, Evangelischer Klinikverbund Niederrhein gGmbH & Klinik für Psychiatrie und Psychotherapie, Uniklinik Köln, Steinbrinkstraße 96a, 46145 Oberhausen
Dr. med. Karolina Leopold, Kliniken für Psychiatrie, Psychotherapie und Psychosomatik mit Frühinterventions- und Therapiezentrum, Vivantes Netzwerk für Gesundheit GmbH, Vivantes Klinikum Am Urban und Klinikum im Friedrichshain, Akademische Lehrkrankenhäuser Charité-Universitätsmedizin, Dieffenbachstraße 1, 10967 Berlin
Dr. rer. nat. Wolfgang Janetzky, Lundbeck GmbH, Ericusspitze 2, 20457 Hamburg
Dr. med. Rita Wietfeld, Fachärztin für Neurologie, Psychiatrie und Psychotherapie, Annenstraße 172, 58453 Witten
Effectiveness of atypical long-acting injectable antipsychotics on quality of life of patients with schizophrenia
While new treatment options such as second-generations antipsychotics as oral or long-acting injectable formulations are available as well as including patients in therapeutic decision processes, increasing attention is being focused on approach, which includes more ambitious treatment goals such as patient quality of life and functioning. The QUALIFY study was the first head-to-head, open-label, randomised study that compared the effects of two atypical long-acting injectable antipsychotics – aripiprazole once-monthly and paliperidone palmitate (once-monthly) – in patients with schizophrenia in a naturalistic setting. Results of the primary outcome, health-related quality of life and functioning, showed that aripiprazole once-monthly (400 mg) provided superior improvement in rater-blinded QLS score (Heinrichs-Carpenter quality of life scale) compared with paliperidone palmitate (once-monthly). Consistently greater improvements were observed with aripiprazole once-monthly vs. paliperidone palmitate (once-monthly) across secondary endpoints, including patient psychopathology and readiness for work. The exploratory analyses of pre-defined, age-stratified subgroups showed significantly greater improvements of the QLS with aripiprazole once-monthly in patients ≤ 35 years than in older patients (p = 0.036). In both treatment groups, there were no unexpected adverse events vs. oral formulations. The findings of the QUALIFY study were previously published. We discuss possible reasons and examine therapeutic consequences of the results.
Key words: aripiprazole once-monthly, maintenance therapy, schizophrenia, treatment goals, quality of life, psychopathology, readiness for work
Psychopharmakotherapie 2018; 25(06):286-291
